一种肠道保护剂及其应用的制作方法
本发明涉及一种添加剂,具体涉及一种肠道保护剂及其应用。
背景技术
人体胃肠道系统非常容易受到外来抗原、微生物和有害分子物质的侵害,造成肠道炎症的发生。炎症性肠病(ibd)在中国、欧洲和美洲等国家都比较常见,并且会反复发作。其发病原因涉及到外界刺激和内在遗传或免疫系统病的缺陷等问题,过量活性氧(ros)诱导的氧化应激导致的损伤是ibd重要的病理之一。疾病的发展恶化与氧化应激和炎症有关的相关细胞因子和信号通路有密切关系。针对氧化应激和炎症造成的肠道损伤,有效的应对方法包括通过抗氧化防御系统抑制氧化应激,或通过抗炎症防御系统减轻炎症,或两者兼而有之。但是目前针对ibd的治疗还比较保守,即服用一些免疫抑制剂、皮质类固醇和抗-tnf-α抗体。虽然这些治疗方案有助于缓解病情症状,但是不可避免的存在一些副作用。为了降低和避免药物带来的副作用,研发新型安全的具有维持或改善肠道健康的食源性生物活性物质是当前的研究热点。
蛋壳膜是位于蛋清和蛋壳内表面之间的一层薄而高度交联的纤维蛋白膜,主要由蛋白质,唾液、糖醛酸和少量的糖类组成,目前已知其具有抗菌性和抗微生物活性,能够保护发育中的胚胎不受外界微生物的感染,同时还具有促进皮肤再生的作用,因此,其对于生物体的有效性得到关注。然而在工业生产中,特别是在食品工业,蛋膜大都作为蛋壳附带物被处理掉,壳膜上残留的蛋清极易被微生物污染而发生腐败,这对生产过程中的环境安全是不利的,也因此给工业化处理鸡蛋膜构成了重大挑战。据统计,全世界鸡蛋年产量大于6000万吨,其中,中国生产的鸡蛋大约2876万吨。因此,蛋壳作为一种常见的产业废料,可以随时随地大量收集。如能保护好蛋壳膜中的活性成分,将其作为添加剂加入到食品或医药保健品中将产生非常好的经济效益和社会效益。
有报告称蛋壳膜具有改善胰岛素抵抗、保护肝脏损伤以及抗氧化抗炎等生物活性,但是关于鸡蛋膜蛋白及其多肽的研究大多是通过不同的蛋白酶将其水解后的水解物进行相关活性的评价,虽具有一定的自由基清除能力和化学抗氧化活性,但是对这些产物的生物活性没有进行研究确认,没有为蛋膜的实际应用提供足够的理论依据,因此,目前暂时没有关于蛋壳膜对肠道菌群和肠道健康的报导,对其在肠道中的生物学抗氧化应激能力和抗炎活性以及对肠道微生态的影响尚属未知。
技术实现要素:
为了克服现有技术的不足,针对现有技术中病原生物或抗营养因子对肠道造成伤害,发生肠道炎症,从而影响机体健康的现状,本发明提供了一种肠道保护剂,该保护剂以蛋壳膜为主要成分,安全性高,可以保护肠道免疫系统,改善肠道微环境,从而促进人体健康,来源广泛,制备简单,同时降低废弃蛋壳对环境的污染,且该保护剂可用于制备将生物体维持和/或改善为良好状态的药物和/或食品组合物、食品(补充剂)或食品添加剂等。
为实现上述目的,本发明采取的技术方案为:
一种肠道保护剂,所述肠道保护剂含有蛋壳膜成分,所述蛋壳膜成分为可溶性蛋壳膜成分、含蛋壳膜的粉末或者蛋壳膜的酶解产物。
所述蛋壳膜来源于鸡蛋壳/鸭蛋壳/鹌鹑蛋壳等家禽或鸟类蛋壳内侧形成的膜;其中,从获取容易度、成本等方面来看,优选使用鸡蛋的蛋壳膜。
本发明所述肠道健康保护剂的实施方式中,所述肠道保护剂通过促进肠道内乳酸杆菌、双歧杆菌等益生菌的增殖,抑制肠球菌和肠杆菌等有害菌的生长来调节肠道微生态平衡,保护肠屏障功能。
本发明所述肠道健康保护剂的实施方式中,所述肠道保护剂为tnf-α、il-1β、il-6、il-8、il-12中的一种或多种促炎细胞因子分泌的抑制剂。
本发明所述肠道健康保护剂的实施方式中,所述肠道保护剂为gpx、gr和gst、γ-gcs中的一种或多种抗氧化酶活性的增强剂。
本发明所述肠道健康保护剂可用于制备口服组合物、食品(补充剂)、食品添加剂等。
所述口服组合物含有本发明的肠道健康保护剂和至少一种赋形剂。在制成口服组合物时,可以制成口服用栓剂、软膏剂、灌肠剂,也可以通过混合常用的公知成分,并根据其使用目的而调制成液剂、固体剂、半固体剂等各种剂型。在口服或者经口摄取的用途中,优选制成片剂、散剂、颗粒剂、胶囊剂、液剂等的口服用组合物。本发明的口服组合物的实施方式中,优选含有5%~40%比例的蛋壳膜成分。
所述食品添加剂由本发明所述的肠道健康保护剂构成、或者含有该肠道健康保护剂。所述食品添加有上述的食品添加剂;所述的食品或食品添加剂中的“食品”并不限定于人用食品,还包括作为宠物或家畜饲养的狗或猫等哺乳动物用的饲料。
本发明具有以下有益效果:
(1)以可溶性蛋壳膜成分或者含蛋壳膜粉末等的蛋壳膜成分为主要成分,可以充分利用食品加工过程中被废弃的蛋壳膜,变废为宝,可以减少资源的浪费,消除对环境的污染;
(2)本发明的肠道保护剂来源于具有天然、安全的食源性生物活性物质,能够直接改善目标细胞/肠道的疾病,降低和避免药物带来的副作用;
(3)本发明的肠道保护剂无刺激性,并且能够以各种形态与各种成分同时使用,因此,能够与其他营养(食品)、保健成分同时使用以进一步获得协同效果、或者应用于专门制成为具有特定效果的组合物中在普通食品、营养补助食品、健康食品、药品中将具有广泛的应用,产品市场前景广阔。
附图说明
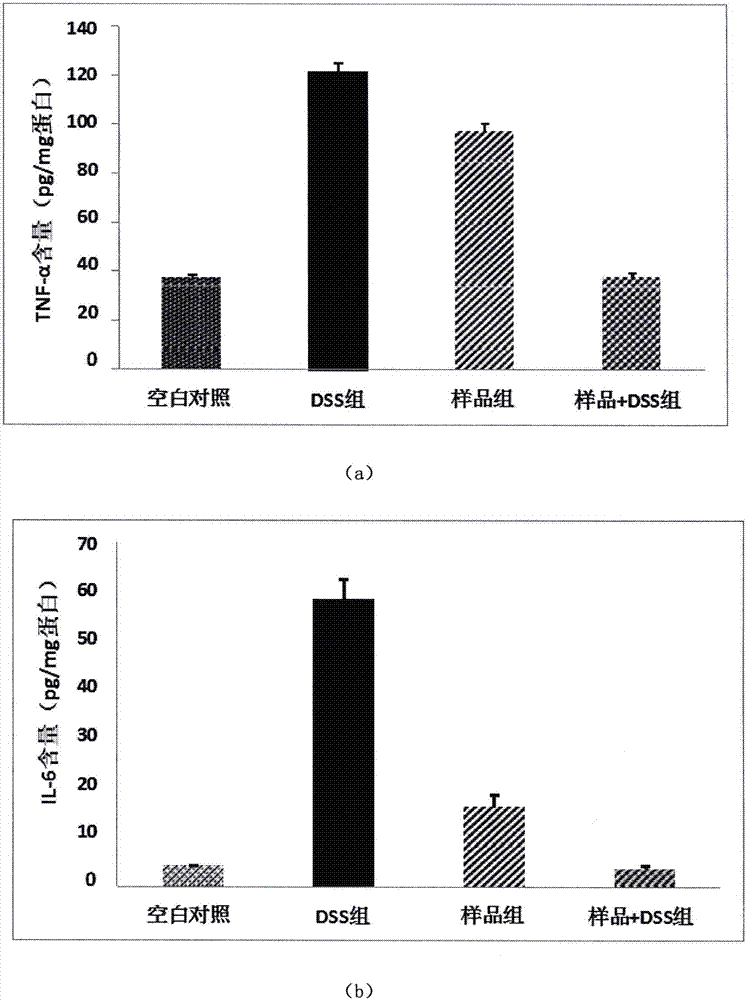
图1为口服样品c对dss诱导小鼠结肠炎发病部位tnf-α和il-6的影响。
图2为口服样品c对dss诱导小鼠结肠炎中的促炎细胞因子基因表达的影响。
图3为口服样品c对dss诱导结肠炎小鼠肠道内乳杆菌的影响。
图4为口服样品c对dss诱导结肠炎小鼠肠道内双歧杆菌的影响。图5为口服样品c对dss诱导结肠炎小鼠肠道内肠杆菌的影响。图6为口服样品c对dss诱导结肠炎小鼠肠道内肠球菌的影响。
具体实施方式
为了使本发明的目的及优点更加清楚明白,以下结合实施例对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例1
含有可溶性蛋壳膜水解物的片剂a的制备将用清水洗净的蛋膜进行热风干燥后,用粉碎机研磨制至粒度小于100目,得干燥的壳膜粉;取5g干燥的壳膜粉,加入500ml乙酸中,向悬浊液中加入3-巯基丙酸,使其浓度为2%,置于37℃的恒温震荡器中连续反应8h,取出,8000r/min离心10min,上清液浓缩后进行冷冻干燥,得粉末;
取上述粉末20g,加入蛋壳粉10g、乳糖25.2g、β-胡萝卜素5.0g、维生素b20.05g、维生素e0.05g、烟酸2.0g,混合均匀后加入15g乙醇,置于湿式造粒装置内进行造粒,接着以50℃的温度干燥约12h,得颗粒;
将颗粒与维生素c及蔗糖脂肪酸酯按质量比10∶1∶1的比例混合,并使用压片装置制成一粒200mg的未包衣片剂。
实施例2
含蛋壳膜粉的组合物片剂b制备
将用清水洗净的蛋膜进行热风干燥后,用粉碎机研磨制至粒度小于100目,得干燥的壳膜粉;取上述干燥的壳膜粉20g,加入蛋壳粉10g、乳糖25.2g、、β-胡萝卜素5.0g、维生素b20.05g、维生素e0.05g、烟酸2.0g,混合均匀后加入15g乙醇,置于湿式造粒装置内进行造粒,接着以50℃的温度干燥约12h,得颗粒;将颗粒与维生素c及蔗糖脂肪酸酯按质量比10∶1∶1的比例混合,并使用压片装置制成一粒200mg的未包衣片剂。
实施例3
含蛋壳膜酶解物的口服液c的制备
将用清水洗净的蛋膜进行热风干燥后,用粉碎机研磨制至粒度小于100目,得干燥的壳膜粉;取5g干燥的壳膜粉,加入100ml的0.4mol/l的食用naoh溶液中震荡3h,调整ph=10后加入碱性蛋白酶,55℃反应4h,再加入中性蛋白酶反应12h,100℃加热10min终止反应,产物6000g离心10min后冷冻干燥得到含蛋壳膜酶解物的粉末;
将上述粉末20g加蒸馏水100ml,65℃搅拌溶解,滤布滤去杂质等不溶物,得混合液a,在混合液a中加入8g蔗糖,用磁力搅拌器充分搅拌5min后得到混合液b,称量0.05g蛋白糖、0.2g柠檬酸,0.2gpga加少量b液溶解后过滤,加入剩余b液混合搅匀,食用氢氧化钠调ph至4.8,灌装后在63℃灭菌30min得成品样品;
蛋壳膜酶解物的口服液c对炎症性肠损伤模型小鼠的改善效果;
balb/c小鼠40只,每组10只,包括不做任何处理的空白对照组、经dss诱导结肠炎的阳性对照组、只给样品c的实验组和既给样品c又用dss诱导结肠炎的实验组。对实验组的具体操作:每天用灌胃法给予小鼠样品c(换算成有效成分含量为200mg/kgbw),共14天。第7天时,开始将5%(w/v)dss(36-50kda)加入饮用水,以诱导急性结肠炎。实验期间,每周采用逼迫法无菌收集各组小鼠粪便约0.1g,并将其置于无菌ep管中,然后进行十倍梯度稀释至适当的梯度,每个稀释度取三个平行,采用倾注平板法进行平板计数,分析各组小鼠粪便中双歧杆菌、肠球菌、乳酸杆菌和肠杆菌的变化。14天后,对小鼠实施安乐死,将结肠切除和测量,并分段切片以备进一步分析。按照现有技术公知的方法测定gsh含量、γ-gcs活性及其mrna表达、tnf-α和il-6浓度以及gapdh、tnf-α、il-1β、il-6和il-17等相关基因的表达。
对所得小鼠结肠组织细胞中促炎细胞因子tnf-α和il-6的浓度进行检测。发现与阳性对照组相比,使用口服样品c的实验组小鼠其体内结肠组织细胞中tnf-α和il-6浓度有所降低(图1)。同时考察了样品c对发病部位细胞因子mrna表达的影响,以讨论其抗炎活性。结果发现与阳性对照组小鼠比较,口服200mg/kg样品c可使所检测炎症细胞因子的mrna表达减少。尤其是样品c可使dss诱导的结肠炎小鼠发病部位的il-6表达显著减少(图2)。说明样品c通过抑制促炎细胞因子的表达对dss诱导的结肠炎小鼠模型中具有抗炎活性。
对dss诱导结肠炎小鼠肠道内乳酸杆菌、双歧杆菌、肠球菌和肠杆菌进行定量分析,实验开始时(即第0天),各组小鼠肠道内菌群构成和数量接近,不存在明显的差异。在实验第3天除正常对照组外,各组小鼠肠道内乳酸杆菌和双歧杆菌的数量均明显降低,其中dss模型组乳酸杆菌数量下降最为明显,与样品c组之间均产生显著性差异(p<0.01)。肠道内肠杆菌的数量增加,其中以模型组升高幅度最为明显。在实验的第7天样品c组内乳酸杆菌和双歧杆菌数量均明显上升,明显高于模型组,肠杆菌数量均达到最低水平,与正常对照组相比差异极显著(p<0.01);与正常对照组和模型组相比较发现,两种菌群的p值均小于0.05,说明对dss小鼠摄入样品c可以促进小鼠肠道内乳酸杆菌和双歧杆菌的增殖,降低小鼠肠道内肠球菌的数量。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!