导管的制作方法
本发明涉及为了切除附着于血管内壁的栓塞而插入于血管的导管。
背景技术:
一直以来,进行着将导管插入血管而切除在血管内产生的栓塞的治疗。在血管内是否产生了栓塞的检查是通过将具有超声波探头的导管插入向血管,获得超声波图像而进行的。另外,对于在血管内是否存在有栓塞,可通过例如光学相干层析成像法(optical coherence tomography,以下也称为“OCT”)进行图像检查(参照专利文献4)。
为了切除在血管内发现了的栓塞,可使用通过侧壁的开口利用切削部将栓塞切除的栓塞切除导管。将该栓塞切除导管插入血管直到开口处于与栓塞相对的位置,设置于开口附近的球囊(balloon)扩张时,开口靠近栓塞,栓塞通过开口而进入栓塞切除导管的内腔内。在栓塞切除导管的内腔中,切削部被设置成可在轴方向移动。该切削部由马达驱动传输,在内腔内旋转。通过使切削部一边旋转一边在内腔内移动,切除进入了内腔的栓塞。切除了的栓塞容纳于栓塞切除导管的内腔(专利文献1、2)。
在前面叙述了的栓塞切除中,为了将栓塞与栓塞切除导管的开口的位置对准,在即将切除之前取得超声波图像。其后,利用栓塞切除导管而切除栓塞。进一步,在切除栓塞后,为了确认血管的状态再次取得超声波图像。假如,判断为没有充分地切除栓塞时,再次利用栓塞切除导管切除残存的栓塞,其后,再次确认血管的状态。在这样的施术中,将具有超声波探头的导管和栓塞切除导管交替插入血管,施术容易变繁杂。鉴于这样的情形,考虑在栓塞切除导管中设置可围绕轴线旋转的超声波探头的导管(专利文献3)。
现有技术文献
专利文献
专利文献1:日本特开平6-30943号公报
专利文献2:日本特开平5-56984号公报
专利文献3:日本特表平9-182754号公报
专利文献4:日本特表2008-523954号公报
技术实现要素:
发明要解决的课题
上述那样的设置了超声波探头的栓塞切除导管存在有如下的问题:切削部与超声波探头的组装结构、用于使其各自旋转的结构复杂,导管大型化,或者因故障等而导致的运作不稳定增大。
在前面叙述了的栓塞的切除中,为了使栓塞与栓塞切除导管的开口的位置对准,在切除之前进行基于OCT的图像检查。其后,利用栓塞切除导管切除栓塞。进一步,在栓塞的切除后,为了确认血管的状态,再次进行基于OCT的图像检查。假如,在判断为没有充分地切除栓塞时,再次利用栓塞切除导管而切除残存的栓塞,其后,再次确认血管的状态。在这样的施术中,将OCT中使用的导管与栓塞切除导管交替插入血管,施术容易变繁杂。
本发明是鉴于这样的情形而做成的,其目的在于提供一种简易结构的导管,其可切除血管的栓塞,且可取得血管的超声波图像。
另外,本发明的另一目的在于提供一种简易结构的导管,其可切除血管的栓塞,且可取得基于OCT的血管的图像。
解决课题的手段
(1)本发明涉及的导管具备:在前端侧的侧壁的一部分具有开口的管体,和在上述管体的内部空间中,位于上述开口附近,可在上述管体的轴线方向移动的切削部,和配置在相对于上述管体的轴线与上述开口相反的一侧,从上述管体的侧壁向外侧凸起的球囊,和至少在相对于上述管体的轴线的与上述开口相同的一侧,沿着上述开口附近的上述侧壁的外周面的圆周方向而配置的相控阵型的超声波探头。
导管从前端侧插入血管。通过在管体的开口对准血管的栓塞的状态下使球囊凸起,管体相对于血管固定,栓塞从开口进入向管体的内部空间。利用向管体的轴线方向移动了的切削部,将进入了管体的内部空间的栓塞切除。利用配置在管体的开口附近的超声波探头,取得切除了的栓塞的超声波图像。
(2)上述导管也可以进一步具备设置于上述管体的外侧且可相对于上述管体在轴线方向上相对移动的外管体,上述超声波探头也可以设置在上述外管体上。
超声波探头可伴随着外管体的相对移动而在血管内移动,因而使超声波探头相对于栓塞而移动,可取得血管的长度方向的位置不同的剖面或者一部分剖面的超声波图像。
(3)上述外管体也可以具有:与上述球囊对应的一部分被切开后的切口部,和配置在相对于上述外管体的轴线与上述切口部相反的一侧,可通过上述相对移动而覆盖上述开口的第1位置以及开放上述开口的第2位置的可移动的支撑部;上述超声波探头也可以设置于上述支撑部,上述切口部也可以在上述第1位置上不与向外侧凸起的状态的上述球囊抵接。
在球囊凸起了的状态下,即使外管体相对移动至与开口重合的第1位置,因为有缺口部,外管体与球囊不发生干涉。另外,在第1位置的支撑部上,使处于与开口对应的位置的栓塞与超声波探头相对,可取得栓塞的超声波图像。
(4)上述超声波探头也可以固定于上述管体中的上述开口的前端侧。
(5)上述超声波探头也可以固定于上述管体中的上述开口的基端侧。
(6)本发明涉及的导管具备:在前端侧的侧壁的一部分上具有开口的管体,和在上述管体的内部空间中,位于上述开口附近,可在上述管体的轴线方向移动的切削部,和贯穿上述管体的内部空间,与上述切削部连接、可将转矩传导至上述切削部的扭矩轴,和沿着上述扭矩轴而设置的导光材料,将从上述导光材料出射的光向与上述导光材料延展的第1方向交叉的第2方向反射的反射材料,和配置在相对于上述管体的轴线与上述开口相反的一侧,从上述管体的侧壁向外侧凸起的球囊。
导管从前端侧插入血管。通过在管体的开口对准血管的栓塞的状态下使球囊凸起,管体相对于血管固定,栓塞从开口进入至管体的内部空间。利用在管体的轴线方向移动的切削部,将进入管体的内部空间的栓塞切除。从沿着扭矩轴设置的导光材料出射的光,通过反射材料反射而照向血管。源自血管的反射光穿过反射材料以及导光材料,利用OCT系统作为干涉信号进行处理,从而取得栓塞附近的血管的图像。
(7)优选的是,上述导光材料以及上述反射材料配置于上述扭矩轴的内部空间,上述反射材料,通过形成于上述扭矩轴的侧壁的开口,将向上述第2方向反射了的光,向上述扭矩轴的外部出射。
由此,可在扭矩轴内将光进行导光而反射。
(8)优选的是,上述导光材料以及上述反射材料可与上述扭矩轴一体地旋转。
由此,通过控制与扭矩轴连接的马达等旋转装置的转速,可实现栓塞的切除与OCT。
(9)优选的是,上述导光材料以及上述反射材料可与上述扭矩轴一体地沿着上述第1方向移动。
由此,可沿着第1方向而取得血管的图像。
(10)优选的是,上述导光材料以及上述反射材料配置于上述扭矩轴的内部空间。
由此,由于导光材料以及反射材料被扭矩轴覆盖保护,导光材料以及反射材料不易破损。
(11)优选的是,上述导光材料以及上述反射材料配置于上述扭矩轴的外周面侧。
由此,即使在扭矩轴的内部空间贯通引导线,也不会因引导线而阻断从反射材料反射的光。
(12)优选的是,沿着上述管体而设置了引导线内腔。
由此,可沿着引导线将导管插入血管。
发明的效果
根据本发明涉及的导管,利用简易的结构,可切除血管的栓塞,且可取得血管的超声波图像。
另外,根据本发明涉及的导管,利用简易的结构,可切除血管的栓塞,且可取得基于OCT的血管的图像。
附图说明
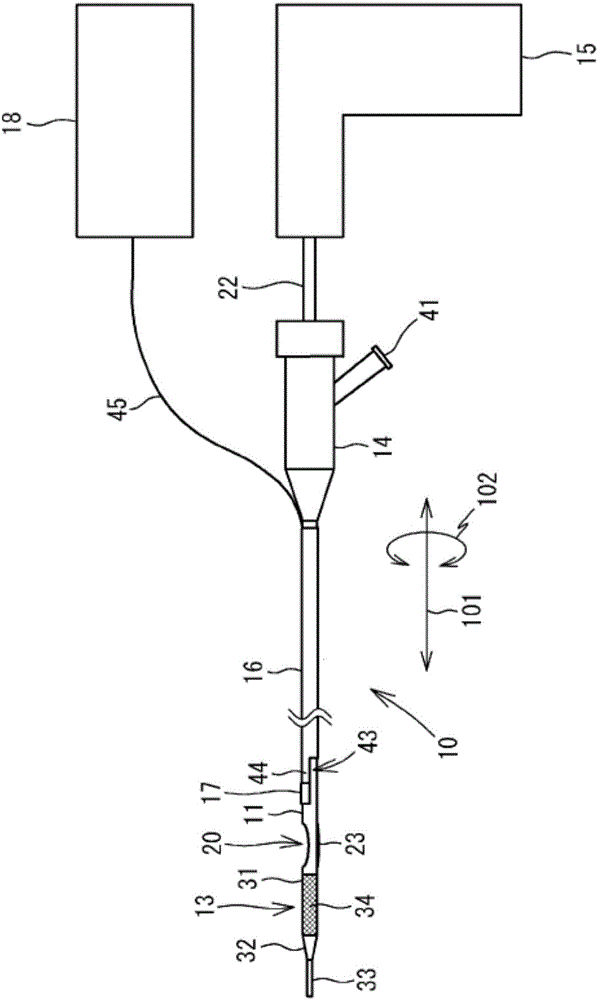
图1为展示球囊23的收缩状态下的导管10的外观结构的图。
图2为展示导管10的前端部13附近的内部结构的放大剖视图。
图3是展示在血管50中球囊23的扩张状态的模式图。
图4为展示在血管50中切除了栓塞51后,支撑部44位于第1位置的状态的模式图。
图5为展示导管10的变形例的图。
图6为展示导管10的变形例的图。
图7为展示球囊223的收缩状态下的导管210的外观结构的图。
图8为展示导管210的前端部213附近的内部结构的放大剖视图。
图9为展示在血管50中球囊223的扩张状态的模式图。
图10为展示在血管50中切除了栓塞51的状态的模式图。
图11为展示导管210的变形例的放大剖视图。
附图标记
10 导管
11 轴(管体)
12 切削部
16 IVUS用轴(外管体)
17 超声波探头
20 开口
23 球囊
43 切口部
44 支撑部
210 导管
211 轴(管体)
212 切削部
216 扭矩轴
217 OCT图像导线(导光材料)
218 反射材料
219 引导线用细管(引导线内腔)
220、221 开口
223 球囊
具体实施方式
以下,说明本发明的优选实施方式。此外,本实施方式不过是本发明的一个实施方式而已,自不用言可在不变更本发明的要旨的范围变更实施方式。
[第1实施方式]
如图1、2所示,导管10具备:轴11,和设置于轴11内的切削部12,和构成轴11的前端的前端部13,和连接于轴11的基端的基端部14,和驱动切削部12进行旋转的驱动部15,和IVUS用轴16,和设置于IVUS用轴16的超声波探头17。导管10被用作插入血管而切除栓塞、拍摄血管的超声波图像的医疗器具。
轴11是可在内部内包切削部12的细管。轴11由例如医疗用不锈钢制的圆管和/或合成树脂制的圆管构成,具有根据血管的弯曲形状而弹性弯曲的柔软性。轴11的前端以及基端分别开口。轴11的外径是根据应当插入的血管,例如冠状动脉的内径而设定的。轴11的内径是根据切削部12的外径而设定的。轴11的外径以及内径沿轴11的轴线方向101大致均等。轴11在轴线方向101的长度是考虑从人的四肢等的导管插入部到患部的长度而设定的。
如图2所示,在轴11中,在前端部13的近旁形成开口20。开口20通过将轴11的侧壁的一部分切掉而形成。开口20的形状和/或大小是考虑在患部形成的栓塞的形状和/或大小而设定的。轴11相当于管体。
如图2所示,在轴11的内部空间在开口20的近旁,设置有切削部12。切削部12具有刃部21与轴22。刃部21是大致圆筒形状,其外径相比于轴11的内径稍小。在刃部21的前端侧,从中心放射状延伸而形成多个刃。在该图中没有显现,但是在刃部21的中心,沿着轴线方向101而形成有贯通孔。轴22从刃部21的基端延展到基端部14的外侧。轴22是细长的管,其内部空间与刃部21的贯通孔连通。轴22的内部空间以及刃部21的贯通孔用于贯通引导线。
如图1所示,轴22连接于驱动部15。通过从驱动部15进行驱动传输、轴22旋转,刃部21旋转。另外,通过轴22在轴线方向101移动,刃部21在轴11的内部空间在轴线方向101移动。
如图1、2所示,在相对于轴11的轴线与开口20相反的一侧的位置,设置有球囊23。球囊23可从轴11的侧壁向外侧凸起,直到导管10插入血管为止,折叠并紧贴于轴11的侧壁。作为球囊23的原材料,优选为具有生物体适应性的材料,具体列举出聚氨酯、聚乙烯、聚酯、聚丙烯、聚酰胺、聚酰胺弹性体、聚四氟乙烯、聚偏氟乙烯等。
如图2所示,球囊23的基端侧连接于沿着轴11的侧壁而设置的球囊用管体24。球囊用管体24的内部空间与球囊23的内部空间连通。球囊用管体24延展到基端部14,球囊用管体24的内部空间与基端部14的端口41连接。通过使从基端部14的端口41注入了的生理盐水等液体流入于球囊23内,球囊23在血管内凸起。球囊用管体24是聚酰胺、聚酰胺弹性体、聚醚酰胺等的可弹性变形的软质塑料的成型体。
如图1、2所示,在轴11的前端连接着前端部13。如图2所示,前端部13具有编织管31、和缩径部32、和前端尖头33。
如图1、2所示,编织管31是两侧开口的圆管。编织管31连接于轴11的前端,其内部空间与轴11的内部空间连通。编织管31是将聚酰胺、聚酰胺弹性体、聚醚酰胺等的可弹性变形的软质塑料通过芯材34增强。芯材34埋入于编织管31的侧壁内。芯材34是将医疗用不锈钢等的线材网状编织为筒状。编织管31的内径与轴11的外径为同等程度,在轴11的前端从外侧嵌入编织管31。编织管31的外径以及内径沿轴线方向101大致均等。此外在除了图1以外的各图中,省略着芯材34的图示。
如图1、2所示,缩径部32是两侧开口而将外径缩小成为锥形形状而得到的圆管。缩径部32连接于编织管31的前端,其内部空间与编织管31的内部空间连通。缩径部32由聚酰胺和/或聚醚酰胺等可弹性变形的软质塑料形成。缩径部32的基端侧的内径与编织管31的前端的外径为同程度,在编织管31的前端,从外侧嵌入、热焊接有缩径部32。缩径部32的前端侧的内径与前端尖头33的中央部分的外径为同程度。在缩径部32的前端侧,壁厚朝向前端侧而变薄。
如图1、2所示,前端尖头33是两侧开口、基端36侧的外径以锥形形状地扩大的圆管。前端尖头33连接于缩径部32的前端,其内部空间与缩径部32的内部空间连通。前端尖头33的前端35从缩径部32的前端向轴线方向101的外侧突出。前端尖头33的基端36侧,是在缩径部32的内部空间中在轴线方向101延展,基端36到达编织管31的内部空间。即,形成如下的二重管结构:从编织管31的前端侧部分到缩径部32,将编织管31以及缩径部32设为外侧,将前端尖头33设为内侧。
前端尖头33的直径在基端36侧扩大,但是其它的部分的外径以及内径大致均等。均等的部分的外径小于编织管31的内径,与缩径部32的前端的内径为同程度。另外,基端36侧直径扩大,但是其最大直径小于编织管31的内径。
前端尖头33由聚酰胺和/或聚醚酰胺等可弹性变形的软质塑料形成。前端尖头33插入并热焊接于缩径部32的前端。此外,在前端尖头33的前端,也可设置可通过X线等来确认的标记。
在轴11的基端设置有基端部14。基端部14是具有与轴11的内部空间连续的内部空间的筒状构件。基端部14是聚丙烯和/或ABS等树脂的成型体。基端部14在将轴11向血管插拔时等的操作中可成为手柄。
在基端部14,设置有向与轴线方向101交叉的方向延展的端口41。通过在端口41连接注射器等其它的设备,从其它的设备流出流入的生理盐水等流体从基端部14向球囊用管体24流出流入。予以说明,在基端部14,也可设置与轴11的内部空间相连的其它的端口。这样的端口被应用于例如回收进入轴11的内部的切除完的栓塞的目的等。
切削部12的轴22从基端部14的基端侧的开口起延展,在该轴22上连接着驱动部15。驱动部15内置马达以及电池等。将驱动部15的马达的旋转传输于轴22。
如图1、2所示,在轴11的外侧,设置有IVUS用轴16。IVUS用轴16是:在内部,可在轴线方向101上可相对移动地插入轴11的细管。IVUS用轴16由例如医疗用不锈钢制的圆管和/或合成树脂制的圆管构成,具有根据血管的弯曲形状而弹性弯曲的柔软性。IVUS用轴16的前端以及基端分别开口。IVUS用轴16的外径根据应当插入的血管例如冠状动脉的内径而设定。IVUS用轴16的内径根据轴11的外径而设定。IVUS用轴16的外径以及内径沿轴线方向101大致均等。IVUS用轴16在轴线方向101的长度相比于轴11在轴线方向101的长度稍短。因此,如图1所示,在IVUS用轴16相对于轴11向基端侧移动、直到抵接于基端部14为止的状态下,轴11的开口20的前端侧从IVUS用轴16的前端突出来而向外部露出。IVUS用轴16相当于外管体。
如图2所示,在IVUS用轴16的前端部,在对应于轴11的球囊23侧的位置,沿着轴线方向101形成向基端侧延伸的切口部43。关于切口部43的圆周方向102的长度,长于球囊23的圆周方向102的长度,切入IVUS用轴16的圆周方向102的约近二分之一。切口部43在轴线方向101的长度是,IVUS用轴16的前端部相对于轴11向前端侧相对移动直到覆盖开口20的位置为止的状态(参照图4)下,不与球囊23抵接的长度;大概与开口20的轴线方向101的长度同等。
在IVUS用轴16的前端部之中,利用切口部43而成为大概一半的管形状的部分是超声波探头17的支撑部44。支撑部44位于在圆周方向102中的与轴11的开口20相同的一侧。IVUS用轴16向轴11的前端侧移动时,会到达支撑部44覆盖开口20的第1位置(参照图4)。IVUS用轴16向轴11的基端侧移动时,会到达支撑部44使开口20开放的第2位置(参照图3)。
在支撑部44的外侧,设置有超声波探头17。超声波探头17是所谓的相控阵型的超声波探头,并且在支撑部44的外周面沿着圆周方向102而排列了多个元件。元件数没有特别限制,例如如果是IVUS用轴16的半周份,那么32个元件排列在圆周方向。通过使各元件按通电顺序点亮,收集超声波探头17的周围的血管的断层图像。在超声波探头17的各元件上连接着电缆45,电缆45插通IVUS用轴16的内部空间,从基端向外部延展,连接于控制装置18。控制装置18向超声波探头17供给电力,同时根据由超声波探头17获得的电信号形成断层图像,是在血管内超声波法(IVUS)中使用的公知的控制装置。
此外,在各图中没有显现,但是也可按照IVUS用轴16相对于轴11在圆周方向(轴线方向101周围)上不相对旋转、仅可相对于轴线方向101进行相对移动的方式,设置限制在圆周方向的移动的嵌合结构等。通过设置嵌合结构等,IVUS用轴16的切口部43以及超声波探头17的位置相对于轴11的圆周方向102不发生变位。
[导管10的使用方法]
以下,一边参照图3、4一边说明导管10的使用方法。
导管10在切除形成在血管50的内壁的栓塞51时使用。栓塞51的位置预先由IVUS等确认。导管10在球囊23的收缩状态(参照图1)下从前端部13插入血管50。在各图中没有示出,但是在将导管10插入血管50时,预先将引导线插入于血管50。关于引导线向血管50的插入,利用公知的技术进行。一边将插入血管50的引导线依次从前端部13的前端尖头33的内部空间向轴11的内部空间、进一步向切削部12的刃部21的贯通孔、轴22的内部空间插入,一边将导管10从前端部13插入血管50。
如冠状动脉那样,在血管50弯曲的部位中,前端部13一边沿着引导线弹性弯曲,一边推进直到血管50的栓塞51为止。前端部13到达栓塞51,轴11的开口20与栓塞51相对时,结束轴11向血管50的插入。通过使IVUS用轴16的支撑部44移动至覆盖开口20的第1位置,使超声波探头17通电点亮,收集包含开口20的血管50的断层图像。通过利用控制装置18确认所形成的血管50的断层图像,可确认开口20到达对应栓塞51的位置、栓塞51的状况。其后,将引导线从导管10的基端部14侧拔出。另外,将驱动部15连接于切削部12的轴22。
如图3所示,是轴11的开口20与栓塞51相对的状态,在IVUS用轴16的支撑部44处于使开口20开放的第2位置的状态下,利用从端口41向球囊用管体24流入的流体,使得收缩状态的球囊23扩张。通过使扩张了的球囊23抵接于与栓塞51侧为相反侧的血管50的内壁,开口20紧贴于栓塞51,在栓塞51的一部分从开口20进入了轴11的内部空间的状态下,导管10相对于血管50固定。
然后,将驱动部15的马达驱动,通过切削部12的轴22使刃部21旋转。在基端部14侧,通过使轴22相对于轴11朝向轴线方向101的前端侧行进,旋转的刃部21抵接于栓塞51,利用刃部21切除栓塞51。切除了的栓塞51的残片52通过轴11的内部空间而进入编织管31的内部空间。
利用切削部12切除栓塞51,使IVUS用轴16的支撑部44位于覆盖开口20的第1位置。而后,通过使超声波探头17通电点亮,收集切除了栓塞51的状态的血管50的断层图像。由此,切除了栓塞51的状态可立即确认,即不必相对于血管50拔出导管10,因而例如,如果栓塞51的切除不充分,那么再次使IVUS用轴16的支撑部44位于第2位置,可利用切削部12切除残存的栓塞51。此外,关于血管50的断层图像的收集,也可一边使IVUS用轴16相对于轴11在轴线方向101移动,一边将超声波探头17通电点亮而进行。由此,在血管50的长度方向(与轴线方向101大致一致)连续地收集断层图像。而后,栓塞51的切除结束时,收缩球囊23,将导管10从血管50拔出回收。
[第1实施方式的作用效果]
根据1实施方式涉及的导管10,利用简易的结构,可切除血管50的栓塞51,且可取得血管50的超声波图像。
另外,IVUS用轴16相对于轴11在轴线方向101相对移动,与此同时,超声波探头17可在血管50内沿长度方向(轴线方向101)移动,因而超声波探头17相对于栓塞51移动,可取得血管50在长度方向的位置不同的断层图像。
另外,在IVUS用轴16上设置了切口部43,即使设置在与切口部43相反的一侧的支撑部44位于覆盖开口20的第1位置,也会因切口部43,向外侧凸起的球囊23与IVUS用轴16不抵接,因而在第1位置的支撑部44处,可取得包含处于与开口20相对的位置的栓塞51在内的断层图像。
[第1实施方式的变形例]
前面叙述了的第1实施方式中,在IVUS用轴16设置有超声波探头17,但是也可不设置IVUS用轴16,在轴11的外周面设置超声波探头17。
如图5所示,超声波探头17设置于轴11中的开口20附近,设置于开口20的前端侧。在该变形例中,是超声波探头17与球囊23不干涉的配置,因而超声波探头17,也可以与前面叙述了的第1实施方式同样地,具有在轴11的半周份上的32个元件,也可以具有在轴11的全周份上的64个元件。在该图中未显现,但是从超声波探头17延展的电缆45贯通轴11的内部空间而与控制装置18连接。另外,如图6所示,超声波探头17也可设置于轴11中的开口20附近,设置于比开口20的基端侧。
根据这样的变形例,由于没有设置IVUS用轴16,可谋求导管10的小型化、特别是细径化,另外结构变得更简易。另外,通过使球囊23缩瘪,使超声波探头17与导管10一同地在血管50的长度方向上移动,可收集包含栓塞51在内的血管50的断层图像和/或、在血管50的长度方向连续的断层图像。另外,通过围绕轴11的全周而设置超声波探头17,可收集血管50的全周的断层图像。
[第2实施方式]
如图7、8所示,导管210具备轴211(相当于管体)、和设置于轴211内的扭矩轴216以及切削部212、和构成轴211的前端的前端部213、和连接于轴211的基端的基端部214、和给予切削部212旋转驱动的驱动部215、和设置于扭矩轴216内的OCT图像导线217(相当于导光材料)以及反射材料218、和引导线用细管219。导管210被用作插入血管而切除栓塞、或者拍摄血管的剖面图像的医疗器具。
轴211是可在内部内包切削部212的细管。轴211由例如医疗用不锈钢制的圆管和/或合成树脂制的圆管构成,具有根据血管的弯曲形状而弹性弯曲的柔软性。轴211的前端以及基端分别开口。轴211的外径根据应当插入的血管例如冠状动脉的内径而设定。轴211的内径根据切削部212的外径而设定。轴211的外径以及内径沿轴211的轴线方向101大致均等。轴211在轴线方向101的长度,考虑从人的四肢等的导管插入部直到患部为止的长度而设定。
如图8所示,在轴211中,在前端部213的近旁形成开口220。开口220通过将轴211的侧壁的一部分切掉而形成。关于开口220的形状和/或大小,考虑在患部形成的栓塞的形状和/或大小而设定。
如图8所示,在轴211的内部空间在开口220的近旁,设置有切削部212。切削部212是大致圆筒形状,其外径相比于轴211的内径稍小。因此,切削部212可在轴211的内部空间沿着轴线方向101移动。在切削部212的前端侧,多个刃按照从中心放射状地延伸的方式形成。在该图中没有显现,但是在切削部212的中心,沿着轴线方向101而形成着贯通孔。
扭矩轴216贯通轴211的内部空间,前端侧与切削部212连接,基端侧延展到轴211的基端部214的外侧。扭矩轴216与轴211一同,具有根据血管的弯曲形状而弹性弯曲的柔软性,且具有传输围绕轴线方向101的旋转的扭转刚性。扭矩轴216,例如,通过将医疗用不锈钢螺旋形状地连接,作为整体形成管形状而构成。
如图7所示,扭矩轴216连接于驱动部215。通过由驱动部215驱动传输、扭矩轴216旋转,使切削部212旋转。另外,通过在轴线方向101移动扭矩轴216,切削部212在轴211的内部空间在轴线方向101移动。
如图8所示,在扭矩轴216上,在与切削部212连接的前端的近旁形成开口221。开口221是通过将扭矩轴216的侧壁的一部分切掉而形成的。开口221的形状和/或大小,考虑被反射材料218反射而朝向与轴线方向101正交的方向出射的近红外线的形状和/或大小而设定。
如图8所示,OCT图像导线217从基端部214贯通扭矩轴216的内部空间,延展到开口221。扭矩轴216的内部空间的内径与OCT图像导线217的外径同等。因此,OCT图像导线217的轴线与扭矩轴216的轴线大致吻合。在各图中没有详细地显现,但是OCT图像导线217在透明的外筒的内部内置有光纤,设置有对前端部照射近红外线的透镜。由该透镜照射的近红外线沿着OCT图像导线217的轴线方向而出射。OCT图像导线217将从内置于OCT本体显示器部222的光源供给的近红外线向前端侧传播。
反射材料218,在扭矩轴216的内部空间,在轴线方向101上与OCT图像导线217的前端相对配置。反射材料218中与OCT图像导线217的前端相对的反射面225是,相对于OCT图像导线217的轴线成为45度的角度而倾斜的平面。反射面225通过扭矩轴216的开口221向扭矩轴216的外部露出。反射材料218是由光纤和/或树脂等形成的圆柱体,其外径与扭矩轴216的内部空间的内径同等。因此,反射材料218的轴线与扭矩轴216的轴线大致吻合。在反射材料218中,包含反射面225的表面上层叠有金属层。金属层,例如,通过使镍、金、铝、铬等单独或混合而在反射材料218的表面上镀敷或溅射等形成。利用反射面225,将从OCT图像导线217沿着轴线方向101出射的近红外线朝向与轴线方向101正交的方向(第2方向)反射,通过开口221向扭矩轴216的外部出射。此外,反射面225的相对于OCT图像导线217的轴线的角度只是一例,也可以不一定是45度。即,将从OCT图像导线217沿着轴线方向101出射的近红外线朝向与轴线方向101交叉的方向反射即可。
OCT图像导线217以及反射材料218,在保持相互的位置关系、即、间隔距离以及反射面225的角度的状态下,可与扭矩轴216成为一体,围绕着轴线(轴线方向101)进行旋转,且可向轴线方向101滑动。OCT图像导线217以及反射材料218的旋转以及滑动,通过直接或间接地对从基端部214延展的扭矩轴216的基端侧进行操作而控制。具体而言,通过在扭矩轴216的基端侧赋予源自驱动部215的驱动力,使扭矩轴216旋转以及滑动。
如图7、8所示,在相对于轴211的轴线与开口220相反的一侧的位置,设置有球囊223。球囊223可从轴211的侧壁向外侧凸起,直到导管210插入于血管为止,折叠地紧贴于轴211的侧壁。作为球囊223的原材料,优选为具有生物体适应性的材料,具体列举出聚氨酯、聚乙烯、聚酯、聚丙烯、聚酰胺、聚酰胺弹性体、聚四氟乙烯、聚偏氟乙烯等。
如图8所示,球囊223的基端侧连接于沿着轴211的侧壁而设置的球囊用细管224。球囊用细管224的内部空间与球囊223的内部空间连通着。球囊用细管224延展到基端部214,球囊用细管224的内部空间与基端部214的端口241连接。通过使从基端部214的端口241注入的生理盐水等液体流入球囊223内,球囊223在血管内凸起。球囊用细管224是聚酰胺、聚酰胺弹性体、聚醚酰胺等可弹性变形的软质塑料的成型体。
如图7、8所示,在轴211的前端连接着前端部213。如图8所示,前端部213具有编织管231、和缩径部232、和前端尖头233。
如图7、8所示,编织管231是两侧开口的圆管。编织管231连接于轴211的前端,其内部空间与轴211的内部空间连通。编织管231是将聚酰胺、聚酰胺弹性体、聚醚酰胺等可弹性变形的软质塑料用芯材234增强的编织管。芯材234埋入于编织管31的侧壁内。芯材234,是将医疗用不锈钢等的线材网状编织成筒形状。编织管231的内径与轴211的外径为同等程度,编织管231从外侧嵌入于轴211的前端。编织管231的外径以及内径沿轴线方向101大致均等。此外,在除了图7以外的各图中,省略着芯材234的图示。
如图7、8所示,缩径部232是,在编织管231侧开口、将外径朝向前端缩径为锥形形状的圆管。缩径部232连接于编织管231的前端,其内部空间与编织管231的内部空间连通。缩径部232由聚酰胺和/或聚醚酰胺等可弹性变形的软质塑料形成。缩径部232的基端侧的内径与编织管231的前端的外径为同程度,缩径部232从外侧嵌入、热焊接至编织管231的前端。缩径部232的前端侧被密封。在缩径部232的前端侧,壁厚朝向前端侧而变薄。
如图7、8所示,前端尖头233连接于缩径部232的前端。前端尖头233的前端235从缩径部232的前端向轴线方向101的外侧突出。前端尖头233由聚酰胺和/或聚醚酰胺等可弹性变形的软质塑料形成。前端尖头233在缩径部232的前端侧进行了热焊接。此外,在前端尖头233的前端,也可设置可通过X线等来确认的标记。
如图7所示,在前端尖头233、编织管231以及轴211的前端侧的一部分,沿着各个的外周面设置有引导线用细管219。引导线用细管219是,聚酰胺、聚酰胺弹性体、聚醚酰胺等可弹性变形的软质塑料的成型体。引导线用细管219配置在不与轴211的开口220以及球囊223重合的位置,例如,轴211与球囊223的边界附近。引导线用细管219的内部空间是引导线内腔,贯通有未图示的引导线。
在轴211的基端设置有基端部214。基端部214是具有与轴211的内部空间连续的内部空间的筒状的构件。基端部214是聚丙烯和/或ABS等树脂的成型体。基端部214在将轴211从血管插拔时等的操作中可成为手柄。
在基端部214中,设置有朝向与轴线方向101交叉的方向延展的端口241。在端口241连接注射器等其它的设备,从其它的设备流出流入的生理盐水等流体从基端部214向球囊用细管224流出流入。此外,在基端部214中,也可设置与轴211的内部空间相连的其它的端口。这样的端口被应用于,例如,回收进入了轴211内部的切除完的栓塞的目的等。
扭矩轴216从基端部214的基端侧的开口延展,在该扭矩轴216上连接着驱动部215。驱动部215中内置马达以及电池等。将驱动部215的马达的旋转传输至扭矩轴216。
另外,配置在扭矩轴216的内部空间的OCT图像导线217,介由驱动部215而连接于OCT本体显示器部222。OCT本体显示器部222具备供给近红外线的光源、干涉计、移动式参照镜、监控器、运算装置等。从光源供给的近红外线,利用干涉计进行拆分而分别供给至OCT图像导线217与移动式参照镜,在血管中被反射的近红外线与反射至移动式参照镜的近红外线在干涉计内汇合。利用运算装置处理这些近红外线的干涉信号,用监控器作为血管的断层图像而表示。
[导管10的使用方法]
以下,一边参照图9、10一边说明导管210的使用方法。
导管210在切除形成在血管50的内壁的栓塞51时使用。栓塞51的位置利用基于OCT的血管断层图像而确认。导管210在球囊223的收缩状态(参照图7)下从前端部213插入血管50。在各图中没有示出,但是在将导管210插入血管50之时,预先将引导线插入血管50。引导线向血管50的插入利用公知的技术而进行。一边将插入血管50的引导线插入引导线用细管219,一边将导管210从前端部213插入血管50。
如冠状动脉那样,在血管50弯曲的部位中,前端部213一边沿着引导线而弹性弯曲一边推进直到血管50的栓塞51为止。前端部213到达栓塞51,轴211的开口220与栓塞51相对时,结束轴211向血管50的插入。通过利用驱动部215使扭矩轴216旋转,同时从OCT本体显示器部222将近红外线供给至OCT图像导线217,在OCT本体显示器部222中示出血管50的断层图像。通过确认血管50的断层图像,可确认开口220到达对应栓塞51的位置、栓塞51的状况。其后,将引导线从导管210的基端部214侧拔出。另外,在切削部212的扭矩轴216上连接驱动部215。此外,在图9、10中,省略引导线。
如图9所示,在轴11的开口220与栓塞51相对的状态下,利用从端口241向球囊用细管224流入的流体,使收缩状态的球囊223扩张。通过使扩张的球囊223抵接于与栓塞51相反的一侧的血管50的内壁,在开口220紧贴于栓塞51、栓塞51的一部分从开口220进入了轴211的内部空间的状态下,导管210被相对于血管50固定。
然后,将驱动部215的旋转通过扭矩轴216传输到切削部212,使切削部212旋转。在基端部214侧,通过使扭矩轴216相对于轴211向轴线方向101的前端侧行进,将旋转的切削部212抵接于栓塞51,利用切削部212切除栓塞51。切除的栓塞51的残片52通过轴211的内部空间进入编织管231的内部空间。
利用切削部212切除了栓塞51后,利用与前述同样的OCT,可获得切除了栓塞51的状态的血管50的断层图像。由此,切除了栓塞51的状态可立即确认,即在不必从血管50将导管210拔出,因而例如,如果栓塞51的切除不充分,那么可使切削部212旋转而切除残存的栓塞51。此外,血管50的断层图像的收集,也可一边使反射材料218与扭矩轴216一同相对于轴211在轴线方向101移动,一边进行。由此,在血管50的长度方向(与轴线方向101大致一致)获得连续的断层图像。然后,结束栓塞51的切除时,球囊223收缩,将导管210从血管50拔出而回收。
[第2实施方式的作用效果]
根据第2实施方式涉及的导管210,利用简易的结构,可切除血管50的栓塞51,且可取得血管50的OCT图像。
另外,由于将OCT图像导线217以及反射材料218配置于扭矩轴216的内部空间,可在扭矩轴216内将近红外线导光至血管50的栓塞51附近而反射。
另外,由于OCT图像导线217以及反射材料218可与扭矩轴216一体地旋转,通过在驱动部215中控制马达的转速,可实现栓塞51的切除与OCT。
另外,由于OCT图像导线217以及反射材料218可与扭矩轴216一体地沿着轴线方向101移动,可取得沿着轴线方向101的血管50的断层图像。
另外,由于OCT图像导线217以及反射材料218配置于扭矩轴216的内部空间,OCT图像导线217以及反射材料218被扭矩轴216覆盖保护。
另外,由于沿着轴211而设置有引导线用细管219,可沿着引导线将导管210插入血管50。
[变形例]
前面叙述了的实施方式中,引导线用细管219是配置在轴211的外侧的所谓快速交换型(rapid exchange type)的结构,但是如图11所示,也可将扭矩轴216的内部空间用作引导线内腔而采用所谓内置导丝型(over-the-wire type)的结构。
在采用内置导丝型的结构的情况下,OCT图像导线217以及反射材料218,如图11所示,两者沿着扭矩轴216的外周面在轴线方向101相对地配置。从OCT图像导线217沿着轴线方向101而出射的近红外线,利用反射材料218朝向扭矩轴216的外侧、向与轴线方向101交叉的方向(正交的方向)反射。由此,不需对贯通扭矩轴216的内部空间的引导线照射近红外线。另外,在内置导丝型的结构中,不需要在扭矩轴216上形成开口221。
另外,在采用内置导丝型的结构的情况下,如图11所示,作为前端尖头233,采用两侧开口、基端236侧为外径扩大为锥形形状的圆管。前端尖头233连接于缩径部232的前端,其内部空间与缩径部232的内部空间连通。前端尖头233的前端235从缩径部232的前端向轴线方向101的外侧突出着。在前端尖头233的基端236侧,缩径部232的内部空间在轴线方向101延展,基端236到达了编织管231的内部空间。即,从编织管231的前端侧部分到缩径部232,制成如下的二重管结构:将编织管231以及缩径部232设为外侧,将前端尖头233设为内侧。
前端尖头233的直径在基端236侧扩大,但是其它的部分的外径以及内径大致均等。均等的部分的外径小于编织管231的内径,与缩径部232的前端的内径为同程度。另外,基端236侧的直径扩大,但是其最大直径小于编织管231的内径。
另外,在切削部212中,形成沿着轴线方向101的贯通孔,利用扭矩轴216的内部空间、利用切削部212的贯通孔、编织管231的内部空间、以及前端尖头233的内部空间,沿着轴211的轴线方向101而形成引导线内腔。
此外,OCT图像导线217的前端面是按照相对于轴线方向101成为45度的角度的方式倾斜的平面,其前端面可具备反射材料218。在该情况下,不存在有在与OCT图像导线217间隔的距离处配置的反射材料218。
- 还没有人留言评论。精彩留言会获得点赞!