包含2,5‑二羟基苯磺酸的用于促进神经细胞中髓鞘再生的组合物及其用途的制作方法
本申请要求2015年8月21日向韩国专利局提交的韩国专利申请No.10-2015-0118267的权益,其通过提述完整并入本文。
发明背景
1.领域
本公开涉及用于预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病的组合物,用于促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的组合物,用于降低哺乳动物的神经细胞中PMP22表达的组合物,预防或治疗哺乳动物中神经细胞的脱髓鞘有关的疾病的方法,促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的方法,和降低哺乳动物的神经细胞中PMP22表达的方法。
2.相关领域说明
脱髓鞘疾病(demyelinating disease)是神经系统的疾病,其中神经元的髓鞘受损。该损伤损害受影响神经元中的信号转导,继而,根据受影响的是哪些神经,导致感觉、运动、认知或其他功能中的缺陷。脱髓鞘疾病可以包括影响中枢神经系统和周围神经系统的疾病。周围神经系统的脱髓鞘疾病包括格-巴二氏综合征(Guillain-Barre Syndrome)和夏-马-图三氏(Charcot Marie Tooth,CMT)病。中枢神经系统的脱髓鞘疾病包括多发性硬化。已显示抗坏血酸在动物模型中针对周围神经病是有效的;然而,该化合物在临床测试中失败。因此,需要用于脱髓鞘疾病的基础性治疗的药物。
发明概述
提供了用于预防或治疗与哺乳动物中神经细胞的脱髓鞘有关的疾病的组合物,该组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
提供了用于促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的组合物,所述组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
提供了用于降低哺乳动物的神经细胞中周围髓磷脂蛋白22(PMP22)表达的组合物,所述组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
提供了预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病的方法,所述方法包括对该哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,从而预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病。
提供了促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的方法,所述方法包括对该哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,从而促进哺乳动物的神经细胞中的髓鞘再生或抑制脱髓鞘。
提供了降低哺乳动物的神经细胞中PMP22表达的方法,该方法包括对哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,由此降低该哺乳动物的神经细胞中PMP22的表达。
另外的方面部分将在以下说明书中列出,部分从说明书将是明显的或可通过实践所呈现的例示性实施方案而知悉的。
附图简述
从对例示性实施方案的以下说明连同所附附图,这些和/或其它方面将变得明显和更容易领会的。
图1例示了通过大鼠施旺(Schwann)细胞的Western印迹的PMP22基因表达分析的结果,包括在存在以不同浓度(小图A)和暴露时间(小图B)的酚磺乙胺(ES)的情况下过表达的PMP22;
图2提供使用共聚焦激光显微镜获得的斑马鱼(Mbp:gal4;UAS:nfsB(NTR,毒素)::UAS:gfp)的显微镜图像,和用于髓鞘形成、脱髓鞘和髓鞘再生的实验规程的示意图(小图A-D);
图3例示了在不同条件下(小图A-D)孵育的斑马鱼(Mbp:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的后侧线神经(PLL)轴突周围的髓磷脂上使用共聚焦激光显微镜的绿色荧光蛋白(GFP)--荧光显微术的结果;
图4例示了在不同条件下(小图A-C)孵育的斑马鱼(Claudink:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的周围神经系统的髓磷脂上使用共聚焦激光显微镜的GFP-荧光(绿色)显微术和使用乙酰化-微管蛋白染色(红色荧光)的免疫荧光显微术的结果;
图5例示了从图4中荧光图像的荧光强度获得的有髓鞘轴突对总轴突的比率;
图6例示了在不同条件下(小图A-C)孵育的斑马鱼(Claudink:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的中枢神经系统中Mauthner轴突和髓磷脂的切片上使用共聚焦激光显微镜的源自GFP的荧光显微术和使用特异于轴突表达的乙酰化-微管蛋白的免疫染色的红色荧光显微术的结果;
图7是将g比率定义为轴突对神经纤维的直径比的示意图;和
图8是从图6的结果获得的g比率的图。
发明详述
现将对例示性的实施方案进行详细提述,其例子例示在附图中,其中相似的参照编号从头到尾指相似的要素。在此方面,目前的例示性实施方案可能具有不同形式且不应理解为受限于本文中陈述的说明。因此,下文仅通过参照附图描述了例示性实施方案以解释各方面。如本文中使用的,术语“和/或”包括一个/种或多个/种所列关联项的任意和所有组合。表述如“至少一个/种”在置于一组要素之前时修饰整组要素而不修饰该组的单个要素。
根据本公开的第一方面,提供用于预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病的组合物,所述组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
根据本公开的第二方面,提供用于促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的组合物,所述组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
根据本公开的第三方面,提供用于降低哺乳动物的神经细胞中周围髓磷脂蛋白22(PMP22)表达的组合物,所述组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。
在根据本公开的第一、第二和第三方面的组合物中,所述2,5-二羟基苯磺酸可以可以为其药学可接受的盐的形式。药学可接受的盐的例子可以包括通常用于制药领域的酸加成盐,例如源自无机酸如盐酸、溴酸、硫酸、氨基磺酸(sulfamic acid)、磷酸或硝酸的盐;和源自有机酸如乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、柠檬酸、马来酸、丙二酸、甲磺酸、酒石酸、苹果酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、2-乙酰氧基苯甲酸(2-acetoxybenzoic acid)、富马酸、甲苯磺酸、草酸、或三氟乙酸的盐。药学可接受的盐的例子可以包括碱加成盐,例如源自碱如铵、二甲胺、一甲胺、一乙胺或二乙胺的盐。药学可接受的盐的例子可以包括常见金属盐,例如源自金属如锂、钠、钾、镁或钙的盐。上述酸加成盐、碱加成盐和金属盐可以根据本领域中常见的方法制备。例如,碱加成盐或金属盐可以通过使2,5-二羟基苯磺酸的离子形式,即2,5-二羟基苯磺酸根/盐与适宜碱(例如二乙胺)或金属离子(例如钙、镁或钠离子)反应而获得。例如,所得碱加成盐可以是2,5-二羟基苯磺酸二乙铵盐(下文中的“酚磺乙胺(ethamsylate)”)。
2,5-二羟基苯磺酸的药学可接受的盐可以具有式1的结构。
在式1中,M可以是[NH4-xRx]+,其中x可以是0,1,2,3或4;且当x>1时,R(s)可以彼此相同或不同,例如,可以是分支或不分支的C1-4-烷基(alkyl-radical)。
2,5-二羟基苯磺酸可以为其溶剂合物的形式。术语“溶剂合物”指包含或组成为至少一种溶质分子(即由式1代表的化合物或该化合物的药学可接受盐);和至少一种溶剂分子的复合物或聚集物。溶剂合物可以是例如与水、甲醇、乙醇、异丙醇或乙酸形成的复合物或聚集物。
2,5-二羟基苯磺酸可以为化合物的立体异构体的形式。立体异构体的例子包括所有类型的立体异构体如对映异构体(enantiomer)和非对映异构体(diastereomer)。2,5-二羟基苯磺酸化合物可以为一种立体异构体的立体异构上纯的形式或至少两种立体异构体的混合物,例如外消旋混合物。可使用本领域中已知的方法之一来实施特定立体异构体的分离。
2,5-二羟基苯磺酸可以是化学合成或商业购买的。
在本公开的第一、第二和第三方面中,所述组合物可以是药物组合物。所述组合物可进一步包含药学可接受的载体。如本文使用的,术语“药学可接受的载体”指与活性成分组合使用的材料,其一般为惰性材料,以帮助活性成分的应用。药学可接受的载体的例子通常可包括,药学可接受的赋形剂、添加剂或稀释剂。药学可接受的载体的例子可包括选自下组的至少一种:填充剂、粘合剂、崩解剂、缓冲剂、防腐剂、抗氧化剂、滑润剂、调味剂、稠化剂、增色剂、乳化剂、悬浮剂、稳定剂和等渗剂。
所述组合物可以以“治疗有效的量”包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。在组合物中,术语“治疗有效的量”如用于本文指在对需要治疗的受试者施用时产生治疗效果的充足量。术语“治疗/处理”如用于本文指治疗受试者,如哺乳动物(包括人)的疾病或医学状况,例如与脱髓鞘有关的疾病,且治疗的含义如下:(a)改善疾病或医学状况,如通过消除患者的疾病或医学状况或导致其消退;(b)抑制疾病或医学状况,如通过延缓或阻止患者的疾病或医学状况的进展;或(c)以任意程度减轻患者的疾病或医学状况的症状。所述组合物还可以用于疾病或医学状况的预防性(防护性)治疗/处理。
所述组合物可包含“用于促进哺乳动物中神经细胞的髓鞘再生的有效量的2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物”或“用于降低哺乳动物神经细胞中PMP22表达的有效量的2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物”。“有效量”可以是由本领域普通技术人员适宜选择的。例如,“有效量”可以在约0.01mg至约10,000mg、约0.1mg至约1000mg、约1mg至约100mg、约0.01mg至约1000mg、约0.01mg至约100mg、约0.01mg至约10mg、或约0.01mg至约1mg的范围内。
所述组合物可包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物作为活性成分。术语“活性成分”指实现如上文描述的组合物的功能的成分,但排除其中活性成分量过少以致于表现如同杂质的情况。
所述组合物可以制备用于口服施用或胃肠外施用,包括静脉内、腹膜内、皮下、直肠和局部施用。如此,组合物可以配制为多种形式,如片剂、胶囊剂、水性溶液、或悬浮剂。在用于口服施用的片剂的情况中,一般可向其添加赋形剂如乳糖或玉米淀粉和滑润剂如硬脂酸镁。在用于口服施用的胶囊剂的情况中,乳糖和/或干玉米淀粉可以用作稀释剂。当需要用于口服施用的水性悬浮剂时,活性成分可以附着于乳化剂和/或悬浮剂。若需要,可将预确定的甜味剂和/或调味剂添加到组合物中。在神经内、肌内、腹膜内、皮下和静脉内施用的情况中,通常制备活性成分的无菌溶液,其中需要适宜地调整无菌溶液的pH和将溶液缓冲。对于静脉内施用,需要控制溶质的总浓度以使得配制的组合物等渗。组合物可配制成水性溶液的形式,其包含药学可接受的载体,如pH 7.4的盐水。水性溶液可以通过局部推注注射施用至患者的肌内或神经内血流中。
2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物可以抑制脱髓鞘或通过使神经元髓鞘再生来恢复脱髓鞘的神经元。
所述组合物可以与至少一种用于治疗与脱髓鞘有关的疾病的其他治疗剂组合使用。或者,组合物可以包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物,而没有用于治疗与脱髓鞘有关的疾病的任何其他活性成分。
所述组合物可以用于治疗与哺乳动物神经细胞中的脱髓鞘有关的疾病。与神经元脱髓鞘有关的疾病(下文亦称为“脱髓鞘疾病”)指神经系统疾病,其中神经元的髓鞘受损。神经元的髓鞘损伤可以包括降低神经元中信号转导的任何损伤,包括结合神经元的髓磷脂的分离,或髓磷脂的量减少或结构变形。该损伤损害受影响神经中的信号转导,继而根据涉及的神经是哪些神经,其导致感觉、运动、认知或其他功能中的缺陷。该疾病可以包括影响中枢神经系统(亦称为“中枢神经系统脱髓鞘疾病”)和周围神经系统(亦称为“周围神经系统脱髓鞘疾病”)的疾病。中枢神经系统脱髓鞘疾病可以包括:多发性硬化、德维克病(Devic’s disease)、炎性脱髓鞘疾病;中枢神经系统神经病如由维生素B12缺乏所引起的那些;脊髓病如脊髓痨(Tabes dorsalis),脑白质病(leukoencephalopathies)如进行性多灶性白质脑病(progressive multifocal leukoencephalopathy),脑白质营养不良(leukodystrophies);格-巴二氏综合征;和慢性炎性脱髓鞘多神经病,其为格-巴二氏综合征对应的慢性病;或其组合。周围神经系统脱髓鞘疾病可以包括抗MAG周围神经病、夏-马-图三氏(CMT)病、铜缺乏(copper deficiency)、进行性炎性神经病、或其组合。例如,与神经元脱髓鞘有关的疾病可以是多发性硬化、格-巴二氏综合征、CMT病、或其组合。CMT病可以是CMT1A亚型、CMT1E亚型或CMT3亚型。
在所述组合物的一些实施方案中,与神经元脱髓鞘有关的疾病可以由PMP22的过表达导致。PMP22是在人中由PMP22基因编码的蛋白质。该基因编码的整合膜蛋白是主要在施旺细胞中表达的疏水性四分子交联体(tetraspan)糖蛋白且是周围神经系统中紧凑的髓磷脂的主要组分。尽管PMP22是周围神经系统中紧凑的髓磷脂的主要组分,但根据如上文描述的实施方案的组合物可以不仅对于周围神经系统的神经细胞,而且对于中枢神经系统的神经细胞也有效。已知PMP22与髓磷脂蛋白zero相互作用。该基因的多种突变是CMT1A、代-索二氏病(Dejerine-Sottas)、和易感于压迫性麻痹的遗传性神经病(HNPP)的起因。CMT1A是该病的最常见形式,所有CMT患者的至少60%属于CMT1A。CMT1A由17号染色体上PMP22基因的重复导致。该CMT病不仅可以由具有基因的两个拷贝导致,而且可以由具有基因的三个拷贝(包括在一条染色体上的两个拷贝在另一条染色体上的一个拷贝)所导致。
在所述组合物的一些实施方案中,哺乳动物可以是人。哺乳动物可以具有脱髓鞘的神经元和/或与脱髓鞘有关的疾病。
在所述组合物的一些实施方案中,神经细胞中PMP22的过表达可以处于进展中或完成中。神经细胞可以处于由PMP22过表达导致的脱髓鞘的进展中或完成中。神经细胞可以在周围神经系统和/或中枢神经系统中。神经细胞可以体内或体外存在或存活。在一个实施方案中,神经细胞是体外细胞系,例如购自美国典型培养物中心(ATCC)的施旺细胞。
根据本公开的另一个方面,提供预防或治疗与哺乳动物神经细胞中PMP22过表达有关的疾病的组合物,该组合物包含2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物。如本文使用的,“PMP22的过表达”指相比于无髓鞘损伤的正常神经细胞(例如正常、健康受试者的神经细胞)增加的PMP22表达。PMP22的表达可以在mRNA水平或蛋白水平测量。mRNA水平可以通过使用RNA分离、核酸扩增方法如聚合酶链式反应(包括RT-PCR)等测量。蛋白水平可以通过使用层析如离子交换、大小排阻、亲和层析等、过滤、盐析等分离蛋白来测量。蛋白水平可以通过使用检测方法来测量。例如,可以使用特异于PMP22的抗体的检测方法如酶联免疫吸附测定法。“PMP22的过表达”指相比于正常神经细胞的,增加了例如5%或更多、10%或更多、50%或更多、100%或更多、5%至100%、10%至100%、20%至100%、5%至80%、5%至50%、10%至50%的PMP22表达。
根据本公开的另一个方面,提供了上文定义的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物在治疗与脱髓鞘有关的疾病中的用途。
根据本公开的另一个方面,提供了上文定义的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物在制备用于治疗与脱髓鞘有关的疾病的药物中的用途;上文定义的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物在制备用于促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的药物中的用途;和上文定义的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物在制备用于降低哺乳动物的神经细胞中PMP22的表达的药物中的用途。根据本公开的另一个方面,提供了能够降低PMP22表达的化合物用于治疗与脱髓鞘有关的疾病或促进髓鞘再生的用途;和另外,能够降低PMP22表达的化合物在制备用于治疗与脱髓鞘有关的疾病或促进髓鞘再生的药物中的用途。
根据本公开的第四方面,提供了预防或治疗与哺乳动物的神经细胞中脱髓鞘有关的疾病的方法,该方法包括对该哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,从而预防或治疗与哺乳动物神经细胞的脱髓鞘有关的疾病。
根据本公开的第五方面,提供了促进哺乳动物神经细胞的髓鞘再生或抑制脱髓鞘的方法,该方法包括对该哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,从而促进哺乳动物神经细胞的髓鞘再生或抑制脱髓鞘。
根据本公开的第六方面,提供了降低哺乳动物的神经细胞中PMP22表达的方法,该方法包括对该哺乳动物施用有效量的2,5-二羟基苯磺酸或其药学可接受的盐或溶剂合物,由此降低该哺乳动物的神经细胞中PMP22的表达。
在本公开的第四、第五和第六方面中,除非另外定义,与关于本公开第一、第二和第三方面使用的那些相同的术语理解为具有与在第一、第二和第三方面中描述的相同的含义。
在本公开的第四方面中,脱髓鞘可以发生在中枢神经系统或周围神经系统的神经细胞中。脱髓鞘可由PMP22过表达导致。与哺乳动物神经细胞中的脱髓鞘有关的疾病可以是CMT病、代-索二氏病、易感于压迫性麻痹的遗传性神经病(HNPP)、多发性硬化、或格-巴二氏综合征。
在本公开的第五方面中,可以通过促进哺乳动物神经细胞的髓鞘再生或抑制脱髓鞘来治疗与脱髓鞘有关的疾病。所述神经细胞可以处于由PMP22过表达所致的脱髓鞘的进展中或完成中。脱髓鞘可以发生在中枢神经系统或周围神经系统的神经细胞中。
在本公开的第六方面,可以通过降低哺乳动物的神经细胞中PMP22表达来治疗与脱髓鞘有关的疾病。所述神经细胞可以处于由PMP22过表达所致的脱髓鞘的进展中或完成中。脱髓鞘可以发生在中枢神经系统或周围神经系统的神经细胞中。
在根据本公开的第四、第五和第六方面的方法中,施用路径可以由本领域普通技术人员适宜地选择。例如,施用路径可以是口服、胃肠外、或局部(local)或局部(topical)施用。局部施用可施用至神经系统,例如脑。
施用量可根据患者的状况、施用路径和医师的决定而变化。可以基于经由体外或动物模型测试获得的剂量-应答曲线获得有效施用量。根据上文所述任一个实施方案的组合物中的化合物,即2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物的比率和/或浓度可根据化学属性、施用路径、和治疗有效量来确定。对受试者施用量可以是,例如约1μg/kg至约1g/kg每日,或约0.1mg/kg至约500mg/kg每日的有效量。量可以根据受试者的年龄、重量、敏感性或症状而改变。
在本公开的第四、第五和第六方面中,所述方法可进一步包括在施用前收集关于受试者中神经细胞脱髓鞘的相关信息。关于脱髓鞘的相关信息可包括脱髓鞘水平、脱髓鞘速率、脱髓鞘类型等。关于脱髓鞘的相关信息可通过用光学或荧光显微镜或通过使用髓鞘特异性标志物观察神经细胞获得。因此,在本公开的第四、第五和第六方面中,所述方法可进一步包括测量神经细胞的脱髓鞘。所述神经细胞可以源自怀疑患有与脱髓鞘有关的疾病或潜在患有该病的受试者。所述方法还可以进一步包括基于收集的关于脱髓鞘的相关信息,确定脱髓鞘是否处于比对照组中更快的进展或完成态中。对照组可以具有与源自没有脱髓鞘疾病的受试者的正常神经细胞或正常受试者的正常神经细胞的相似的髓鞘形成水平。所述方法可包括对受试者施用2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物,所述受试者即在确定步骤中确定的处于比对照组中更多的脱髓鞘进展或完成的哺乳动物。
在本公开的第四、第五和第六方面中,所述方法可进一步包括在施用前测量受试者中或受试者的神经细胞中PMP22的表达水平。PMP22的表达水平可以在mRNA水平或蛋白水平测量。PMP22的表达可以通过扩增(例如聚合酶链式反应(PCR))、Southern印迹、或使用mRNA特异性引物核苷酸的序列分析,或通过分离PMP22表达蛋白、Western印迹等来测量。神经细胞可以源自患有与脱髓鞘有关的疾病或潜在具有该病风险的受试者。所述方法可进一步包括确定在测量步骤中获得的PMP22的测量的表达水平是否高于对照组中的表达水平。对照组可以具有与源自没有脱髓鞘疾病的受试者的正常神经细胞或正常健康受试者的正常神经细胞的相似的髓鞘形成水平。所述方法可以包括对受试者施用2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物,所述受试者即在确定步骤中确定为具有比对照组中的高的PMP22表达水平的哺乳动物。PMP22的高出的表达水平可以是至少约1%、约5%、约10%、约20%、约50%、约100%、约200%、约500%、约1000%、约1至约1000%、约5至约1000%、约10至约1000%、约20至约1000%、约50至约1000%、约100至约1000%、约200至约1000%、或约500至约1000%。
根据本公开的另一个方面,提供了促进哺乳动物神经细胞的髓鞘再生或抑制脱髓鞘的方法,该方法包括使哺乳动物的神经细胞与有效量的2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物接触,从而促进哺乳动物神经细胞的髓鞘再生或抑制脱髓鞘。所述神经细胞可以是从受试者分离的神经细胞或体外存活的神经细胞。
根据本公开的另一个方面,提供了降低哺乳动物的神经细胞中PMP22表达的方法,该方法包括使哺乳动物的神经细胞与有效量的2,5-二羟基苯磺酸、或其药学可接受的盐或溶剂合物接触,由此降低该哺乳动物的神经细胞中PMP22的表达。神经细胞可以是从受试者分离的神经细胞或体外存活的神经细胞。神经细胞可以是体外培养的神经细胞株系且所述方法在体外系统中进行。
在根据本公开的上述方面的方法中,所述接触可以在液体培养基,例如神经细胞的培养基或缓冲液中实施。
现将参照以下实施例更详细地描述本公开的一个或多个实施方案。然而,这些实施例仅用于例示性目的且不意图限制本公开的一个或多个实施方案的范围。
实施例
实施例1:酚磺乙胺对神经细胞中髓鞘再生的影响
(1)酚磺乙胺对神经细胞中PMP22表达的影响
将大鼠施旺细胞以约105细胞/mL的浓度接种到12孔板的每个孔中,该孔中包含含有10%胎牛血清(FBS)、100单位/mL的青霉素、和100单位/mL的链霉素的2mL Dulbecco's Modified Eagle's培养基(DMEM),并在5%-CO2培养箱中在约37℃温育至细胞密度为约60%至约65%。然后,将酚磺乙胺(二乙基铵2,5-二羟基苯磺酸(“ES”),可从Selleckchem,TX获得)以不同浓度添加到孔中,接着在相同条件下温育约24小时。大鼠施旺细胞经常用在体外模型中用于神经元功能和分化。本文使用的大鼠施旺细胞是经过修饰以一致地过表达人PMP22基因的,其通过慢病毒介导将PMP22整合到染色体中,并选择性使用嘌呤霉素抗性标志物,从而构建新的大鼠施旺PMP22细胞模型。该大鼠施旺细胞(ATCC编号;CRL-2768)购自美国典型培养物保藏中心(ATCC)。
在除去2mL培养基后,将所得大鼠施旺细胞用磷酸盐缓冲盐水(PBS)洗涤,接着向其添加含有溶于PBS中的0.5%triton X-100的裂解溶液,使用刮刀收集细胞,将细胞留置冰上约30分钟,然后破坏细胞。使用二喹啉甲酸(BCA)蛋白测定法,将每份样品中的蛋白量标准化至1ug/uL,继之以十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE,Invitrogen)和使用兔抗PMP22(Novus biological)和兔抗肌动蛋白(Sigma)一抗以及缀合辣根过氧化物酶(HRP)的抗兔二抗的Western印迹。
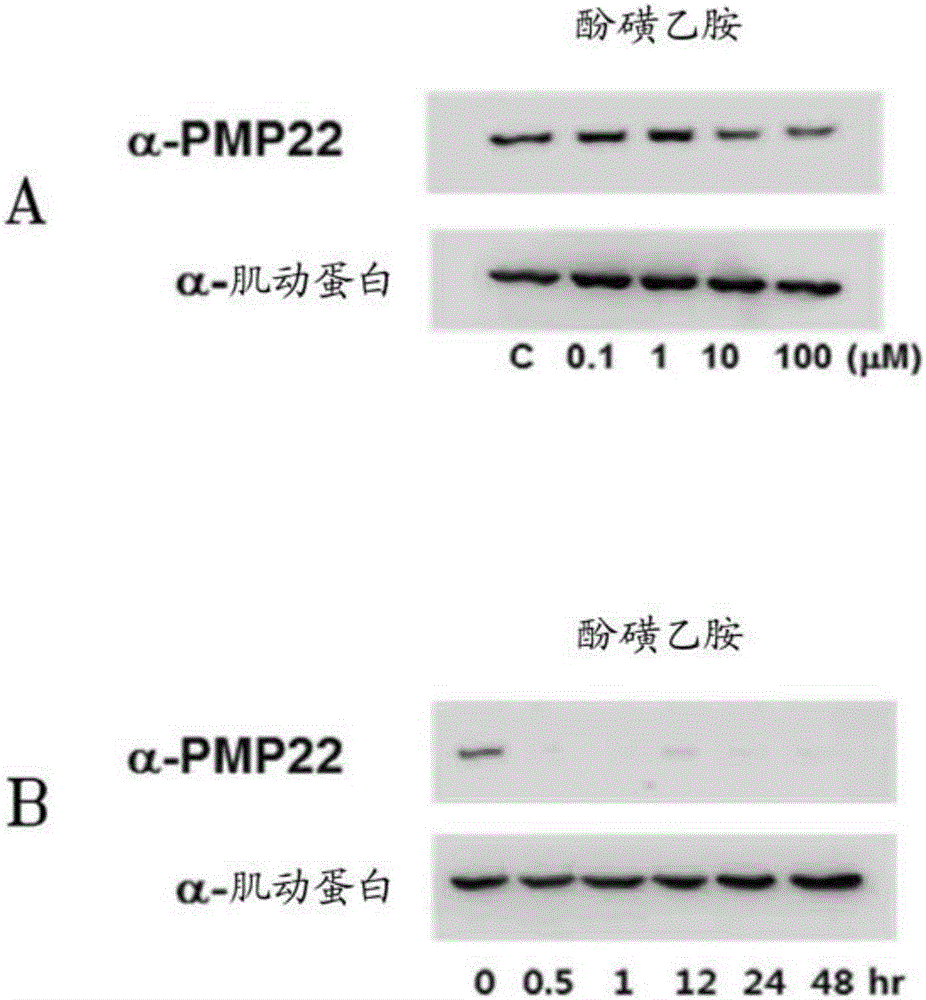
图1例示了通过Western印迹,对包含在存在酚磺乙胺情况下过表达的PMP22的大鼠施旺细胞的PMP22基因表达分析的结果。在图1中,A和B均为Western印迹图像,其中小图A显示在用溶于二甲亚砜(DMSO)中的0.1μM,1μM,10μM和100μM的酚磺乙胺处理约24小时的细胞中的PMP22蛋白表达。在图1的小图A中,“C”指对照组,包含作为溶剂的DMSO而不包含酚磺乙胺。实验重复4次(n=4)。图1的小图B显示在用10μM的酚磺乙胺处理0,0.5,1,12,24和48小时的细胞中的PMP22蛋白表达,其中“0小时”指不添加酚磺乙胺的对照组。
如图1的小图A中显示的,增加浓度的酚磺乙胺导致表达的PMP22蛋白的量降低。还发现在含有10μM酚磺乙胺的培养基中温育0.5,1,12,24和48小时后PMP22蛋白的表达水平相比于对照组降低(图1中的小图B)。
(2)酚磺乙胺对体内PMP22表达的影响
通过用分别编码Mbp:EGFP融合蛋白和Claudink:EGFP融合蛋白的基因转化斑马鱼细胞来准备经转化的斑马鱼(Danio rerio),其中通过使用髓磷脂碱性蛋白(MBP)基因和Claudink基因的启动子表达在髓磷脂中特异性表达并发射荧光的分别编码Mbp:EGFP融合蛋白和Claudink:EGFP融合蛋白的基因。具体地,NfsB毒性基因编码酶硝基还原酶(NTR)。NTR在典型的斑马鱼中不导致任何细胞毒性。然而,但向细胞添加甲硝哒唑(MTZ)时,细胞通过使用NTR将MTZ转化成细胞毒性材料,其诱导细胞凋亡。通过使用mbp和claudink基因的启动子(在分化的髓磷脂中特异性运行以表达结合髓磷脂的髓磷脂特异性基因和使用Gal4-UAS反式激活物系统,制备遗传工程化的斑马鱼,即在分化的少突胶质细胞和施旺细胞中特异性表达NfsB毒性基因的经转化的斑马鱼。接着,确认NfsB毒性基因在转化的斑马鱼中髓磷脂特异性表达。
当将MTZ底物添加到在少突胶质细胞和施旺细胞中特异性表达NfsB毒性基因的该转化的斑马鱼的培养基中时,发现在转化的斑马鱼的少突胶质细胞和施旺细胞中诱导细胞凋亡,在该斑马鱼中mbp和claudink基因的启动子特异性运行,且相应地诱导脱髓鞘。结果,建立了在存在MTZ的情况下诱导的脱髓鞘的动物模型。下文中,该动物模型也称为斑马鱼(Mbp(或claudink):gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)。在从培养基除去添加的MTZ底物后,接着在没有MTZ的培养基中培养转化的斑马鱼1天,之后是恢复期。该研究(在下文更详细描述)确认了脱髓鞘的中枢神经系统和周围神经系统中发生天然髓鞘再生,以及ES药物具有促进髓鞘再生的效果。
在含有1L水的约28.5°℃的水浴中,将100个斑马鱼温育于卵水(egg water)或胚胎培养基(EM)(包含15mM NaCl,0.5mM KCl,1mM CaCl2,1mM MgSO4,0.15mM KH2PO4,0.05mM NH2PO4和0.7mM NaHCO3)中达出生日起4.5dpf(受精后天数),然后向其添加溶解于包含0.2%DMSO的EM的10mM MTZ(Sigma)以脱髓鞘36小时。斑马鱼被转移到含有不同药物的96孔板的孔中并在约28.5℃温育(图2小图B)。一些斑马鱼通过在出生日起6dpf后用新EM将脱髓鞘的斑马鱼清洗3次以除去EM中的MTZ来允许髓鞘再生(图2小图C)。另一组斑马鱼在与小图C相同的条件下温育,只不过添加10μM ES(图2小图D,其中“化学处理”指ES处理)。在相同条件下温育对照组,只不过添加0.2%DMSO而非MTZ。
图2提供了使用共聚焦激光显微镜获得的斑马鱼(Mbp:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的显微镜图。在图2的显微镜图中,白色虚线框划定了监测中枢神经系统和周围神经系统的髓鞘再生的髓磷脂区域。中央最亮区域对应于中枢神经系统,而在中枢神经系统区域下面的相对暗的区域对应于周围神经系统。在图2中,在共聚焦激光显微镜图像下面的小图A-D提供了实验过程的示意图,即从出生日起3dpf的髓鞘形成(A),在4.5dpf添加MTZ(B),在6dpf洗掉或除去MTZ(下文中也称为“恢复第1天”)(C),和添加10μM的ES(D)。实施实验直至7dpf,以一式18份进行(The test was performed by a multiple of 18)(n=18)。在图2中,指示“Zebrafish(Mbp(claudink):gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)”中的“Mbp(claudink)”意指"Mbp"或"claudink"启动子可以等同地用于转化的斑马鱼中。
图3例示了在不同条件下孵育的斑马鱼(Mbp:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的后侧线神经(PLL)轴突周围的髓磷脂上使用共聚焦激光显微镜的绿色荧光蛋白(GFP)--荧光显微术的结果。图3,小图A,B,C和D例示了如上文关于图2中A,B,C和D和实验过程描述的实施的实验的结果。当如图3小图A中的在不存在MTZ和酚磺乙胺的情况下孵育斑马鱼时,在斑马鱼的周围神经系统中存在充足的髓磷脂(图3小图A)。当在存在MTZ的情况下从约4.5dpf至7dpf(达约2.5天)培养斑马鱼时,几乎没有观察到GFP荧光,表明大部分髓磷脂被除去(图3小图B)。当将在存在MTZ的情况下从4.5dpf至6dpf培养的斑马鱼进一步在通过洗涤从培养基除去MTZ后未添加ES的培养基中从6dpf温育至7dpf(达约1天)时,周围神经系统中的髓磷脂仍然部分未形成髓鞘(见图3小图C中的白色虚线区)。在另一方面,当在存在MTZ的情况下从4.5dpf至6dpf培养的斑马鱼进一步在通过洗涤从培养基除去MTZ后添加ES的培养基中从6dpf温育至7dpf(达约1天)时,周围神经系统中的髓磷脂完全髓鞘再生,从而在所有区域中均观察到GFP来源的绿色荧光(图3小图D)。在图3中,绿色荧光的强度与髓鞘形成的程度成比例。
图4例示了在不同条件下孵育的斑马鱼(Claudink:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的周围神经系统的髓磷脂上使用共聚焦激光显微镜的GFP-荧光(绿色)显微术和使用乙酰化-微管蛋白染色(红色荧光)的免疫荧光显微术的结果。比Mbp启动子更特异性地作用于髓磷脂的Claudink启动子可以用于更定量地观察神经细胞中的脱髓鞘和髓鞘再生。在图4中,“claudink”和“ac-微管蛋白”分别指示通过claudink启动子由在髓磷脂中特异性表达的GFP产生的绿色荧光图像和利用在轴突中特异性表达的乙酰化微管蛋白的免疫染色产生的红色荧光图像,且"merge"指示两个图像的融合图像。乙酰化微管蛋白的免疫染色使用抗小鼠乙酰化微管蛋白一抗和缀合Alexa647的抗小鼠二抗实施以测量蓝色荧光,接着是蓝色到红色转化以用于相对于绿色荧光的高对比度成像。下文中,乙酰化微管蛋白的免疫染色以与此处描述的相同方式实施。在图4中,"PLL髓磷脂"指示PLL的轴突周围的髓磷脂。如图4中显示的,发现ES促进髓鞘再生。图4小图A,B和C分别指示在相同条件下与图2的A,B和D相同的实验过程。
图5例示了从图4中荧光图像的荧光强度获得的有髓鞘轴突对总轴突的比率。在图5中,"Cont","MTZ"和"酚磺乙胺"分别指示来自图4的小图A,B和C的结果。有髓鞘轴突对总轴突的比率表示为图4中显示的通过claudink启动子由在髓磷脂中特异性表达的GFP产生的绿色荧光强度相对于通过在轴突中特异性表达的乙酰化微管蛋白的免疫染色产生的红色荧光强度的比率。
如图4和5中显示的,有髓鞘轴突对总轴突的比率在存在ES的情况下显著高于用MTZ处理的样品,表明ES促进脱髓鞘的神经细胞中的髓鞘形成。
图6例示了在不同条件下孵育的斑马鱼(Claudink:gal4::UAS:nfsB(NTR,毒素)::UAS:gfp)的中枢神经系统中Mauthner轴突和髓磷脂的切片上使用共聚焦激光显微镜的源自GFP的荧光显微术和使用特异于轴突表达的乙酰化-微管蛋白的免疫染色的红色荧光显微术的结果。图6,小图A,B和C分别指示来自在相同条件下,与图2和3中的小图A,B和D相同的实验过程的结果。在图6中,小图A指在既不包含MTZ也不包含ES的培养基中培养的对照组。通过用Image J程序从源自GFP的荧光和红色轴突荧光的强度计算直径而获得轴突和纤维直径。
图7是将g比率定义为轴突对神经纤维的直径比的示意图。
图8是从图6的结果获得的g比率的图。在图8中,“Cont”,“MTZ”和“酚磺乙胺"分别指示来自图6的A,B和C的结果。如图8中显示的,酚磺乙胺处理组相比于MTZ处理组具有显著降低的g比率,表明轴突的髓磷脂层在酚磺乙胺处理组中变得显著更厚。如图6和8中显示的,在存在MTZ的情况下温育的斑马鱼的中枢神经系统中损坏或脱髓鞘的神经细胞在酚磺乙胺的存在下温育时比其他情况以显著更高的效率再生或髓鞘再生。
如上文实施方案中描述的,根据所述一个或多个实施方案,用于预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病的组合物可以预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病。用于促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的组合物,如上文实施方案中描述的,可以促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘。用于降低哺乳动物的神经细胞中PMP22表达的组合物,如上文实施方案中描述的,可以降低哺乳动物的神经细胞中PMP22表达。预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病的方法,如上文实施方案中描述的,可以有效预防或治疗哺乳动物中与神经细胞的脱髓鞘有关的疾病。促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘的方法,如上文实施方案中描述的,可以有效促进哺乳动物中神经细胞的髓鞘再生或抑制脱髓鞘。降低哺乳动物的神经细胞中PMP22表达的方法,如上文实施方案中描述的,可以降低哺乳动物的神经细胞中PMP22表达。
应理解本文中描述的例示性实施方案应仅以描述性含义考虑,而不是用于限制目的。在每个例示实施方案中的特征或方面的描述通常应视为可用于其他例示实施方案中的其他类似特征或方面。
虽然已参照附图描述了一个或多个例示性实施方案,但本领域普通技术人员应理解可在其中进行形式和细节的多种变化而不背离由权利要求限定的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!