一种基于钆修饰的Fe3O4@PDA纳米材料的光热诊疗剂的制备的制作方法
本发明属于新型纳米复合材料的制备技术,具体涉及一种钆修饰的Fe3O4@PDA纳米材料的光热诊疗剂的制备。
背景技术:
目前,肿瘤的临床诊断和治疗面临两大问题。第一,当前临床上使用的三种癌症治疗方法包括外科手术、放疗和化疗,但治疗效果欠佳,更糟糕的是它们存在引发第二原发癌的风险,且癌症患者在治疗过程中常常遭受极大的痛苦和副作用;第二,肿瘤的诊断和治疗是分开的,因此,在肿瘤的治疗过程中无法监测肿瘤的动态变化过程,这将造成疗效评估不准确、时间滞后。针对以上问题,当前,开发成像指导的新型癌症治疗方式成为目前科学研究的一个热点。
光热治疗癌症是借助于光敏试剂吸收光能并将其转化为热能,所产生的热能促使癌细胞变性、坏死从而达到治疗癌症的目的。光热治疗方法具有以下优势:(1)高选择性:光热治疗只针对有光热治疗试剂富集的肿瘤部位给予局部激光照射,正常组织即便有光热治疗试剂存在,在不给于激光照射时不会对其造成损害;(2)技术操作简便,损伤小,恢复快,不会引发耐药性和严重的副作用,因此,光热治疗在癌症治疗方面具有非常大的潜力,引起了研究者们的广泛关注。制备基于光热治疗的诊疗剂是目前研究的一个热点。当前有大量的研究工作集中于制备不同种类的纳米粒子并用于癌症的光热治疗方面,这些材料主要有以下几类:基于Au的贵金属纳米粒子(如,金纳米壳、金纳米笼、金纳米星、金纳米棒等),半导体纳米粒子(如硫化铜,硫化钼等),碳材料(碳纳米管、石墨烯等)和有机聚合物纳米材料(叶绿素,聚吡咯等),尽管展现了良好的治疗效果。但这些纳米粒子作为光热治疗试剂仍然没有在临床肿瘤治疗中得到应用,最主要的原因可能是由于这些纳米材料存在潜在的体内毒性问题。例如,研究表明金属类纳米粒子在体内无法降解,且金属本身就存在着毒性问题。而碳材料会产生许多毒副反应,如氧化应激和肺部感染等。Zheng小组利用卟啉化合物与脂质形成的配体作为单体通过自组装方法制备了这样一类的光热治疗试剂,由于卟啉是一种天然化合物,所得到的porphysomes纳米粒子在体内可降解,同时不会引起严重的急性中毒现象,但是,这一类材料制备非常繁琐,需要预先合成有机配体。又如Lu等报道了一种简单有效的方法制备基于多巴胺黑色素胶束纳米球的新型光热治疗剂,该材料具有较高的光热转换效率以及较为理想的肿瘤治疗效果。更为重要的是,该材料由人体内广泛存在的多巴胺黑色素组成,且其表面易于修饰和体内生物降解。
磁共振成像(Nuclear Magnetic Resonance Imaging,简称NMRI)是当前分子影像技术中使用最普遍的分子成像技术之一,是目前癌症临床诊断的一种重要方式。四氧化三铁具有良好的生物兼容性,静脉注射入人体后不会对人体产生明显的毒副作用,且右糖旋酐保护的四氧化三铁纳米粒子已经临床化。
基于以上背景,本文通过在四氧化三铁外面包裹聚多巴胺(PDA)纳米材料,在其表面修饰氨基,,最后得到了需要的Fe3O4@PDA-NH2-DTPA-Gd纳米复合材料,实现了T1-T2双模式造影剂指导的光热诊疗剂的制备。
技术实现要素:
本发明利用人体内广泛存在的黑色素多巴胺作为原材料,在Fe3O4纳米小球外包裹多巴胺(PDA)纳米材料,得到Fe3O4@PDA纳米粒子,再将Gd-DTPA接在经1, 6-己二胺修饰后的Fe3O4@PDA纳米粒子上,得到Fe3O4@PDA-NH2-DTPA-Gd纳米材料(如图1所示)。
一种基于钆修饰的Fe3O4@PDA纳米材料的光热诊疗剂的制备,包括如下步骤:
(1)制备粒径为10 nm的四氧化三铁纳米粒子,具体方法如下:
①称取1.4mmol FeCl3·6H2O 0.4g,0.7mmol FeSO4·7H2O 0.2g,溶解到20mL去离子水中,超声15min除去空气;
②将步骤①的溶液置于50℃下水浴,在N2保护下磁力搅拌15min,然后向其中缓慢滴加氨水5 mL,调节pH至11,将温度升高到80℃;
③将0.16g柠檬酸溶解到1mL水中,加入到步骤②的反应溶液中,反应1h,制得Fe3O4纳米粒子;
④将步骤③制得的Fe3O4纳米粒子,用乙醇洗涤两次,最后分散到20mL超纯水中。
(2)在四氧化三铁小球表面原位包覆上一层聚多巴胺纳米材料,其中聚多巴胺壳厚度为30nm左右,四氧化三铁核的尺寸为10 nm,具体步骤如下:
①取步骤(1)最后制得的Fe3O4溶液5mL,分散在21mL水和0.4mL氨水混
合成的溶液中;
②称取0.1g多巴胺溶于2ml水中,逐滴加入到步骤①的反应溶液中,在常温下磁力搅拌24h;
③将步骤②的溶液在11000W下离心15min,吸出上清液,加去离子水、超声分散再离心,如此3遍,第三遍离心后吸出上清液后再加20ml去离子水超声分散后保存。
(3)制备Fe3O4@PDA-NH2-DTPA-Gd纳米材料,具体步骤如下:
①取20mg的Fe3O4@PDA分散到100mlPBS缓冲溶液(pH=8.5,10mM)中,向该溶液中加入40mg的1,6-己二胺,强烈搅拌下反应12小时;然后离心得到氨基化的Fe3O4@PDA-NH2,用水洗三次后,重新分散到去离子水中;最后向此溶液中加入过量的DTPAA,并滴加NaOH 调整溶液的pH值到7,反应24小时后,离心分离,弃掉上清液得到Fe3O4@PDA@-NH2-DTPA沉淀;
②将Fe3O4@PDA@-NH2-DTPA分散在0.01mol/L的NaOH中,再用HCl调节Fe3O4@PDA@-NH2-DTPA水溶液pH为7,缓慢加入1.8mlGdCl3水溶液(25mM),同时用NaOH溶液(0.1M)调节pH在6到7之间,将上述的混合液继续搅拌12小时,即可制得Fe3O4@PDA@-NH2-DTPA-Gd纳米材料。
本发明与以往报道的纳米诊疗剂相比较,该Fe3O4@PDA@-NH2-DTPA-Gd纳米材料同时具有以下优势:
(1)该Fe3O4@PDA@-NH2-DTPA-Gd纳米材料具有较好的生物相容性和体内可降解性:制备该材料的聚多巴胺由一种人体内广泛存在的多巴胺黑色素组成,另外Fe3O4和Gd-DTPA造影剂已经被临床使用,因此所制备材料具有良好的安全性和稳定性。
(2)Fe3O4@PDA@-NH2-DTPA-Gd纳米材料同时具有T1成像和T2成像功能,从而使成像信息更具准确性、精确性和可靠性,更有利于早期病变的诊断。
(3)将磁共振成像与光热治疗结合起来,将赋予该材料磁共振成像指导的癌症光热治疗效果。
附图说明
图1 为本发明制备Fe3O4@PDA@-NH2-DTPA-Gd纳米材料的流程图。
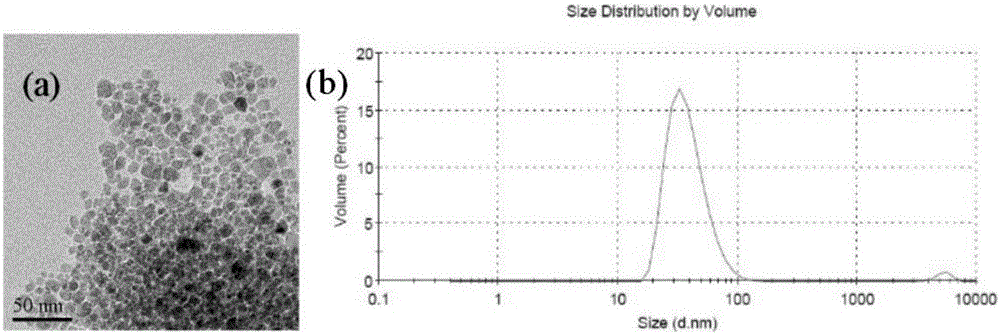
图2 (a)为Fe3O4的透射电镜示意图,(b)为Fe3O4的粒径分布图。
图3(a)为Fe3O4@PDA的透射电镜示意图,(b)为Fe3O4@PDA的粒径分布图。
图4 (a)为Fe3O4@PDA-NH2-DTPA-Gd的透射电镜示意,(b)为Fe3O4@PDA-NH2-
DTPA-Gd的粒径分布图。
图5 (a)为Fe3O4@PDA-NH2-DTPA-Gd的成像图;(b)为Gd-DTPA的纵向磁豫率值r1;(c)为Fe3O4@PDA的横向弛豫率值r2。
图6 不同浓度的Fe3O4@PDA@-NH2-DTPA-Gd的光热转换图。
具体实施方式
(1)采用了共沉淀方法制备了粒径为10nm的四氧化三铁纳米粒子,具体方法如下:
①称取1.4mmol FeCl3·6H2O 0.4g,0.7mmol FeSO4·7H2O 0.2g,溶解到20mL去离子水中,超声15min除去空气;
②将步骤①的溶液置于50℃下水浴,在N2保护下磁力搅拌15min,然后向其中缓慢滴加氨水5 mL,调节pH至11,将温度升高到80℃;
③将0.16g柠檬酸溶解到1mL水中,加入到步骤②的反应溶液中,反应1h,制得Fe3O4纳米粒子;
④将步骤③制得的Fe3O4纳米粒子,用乙醇洗涤两次,最后分散到20mL超纯水中。
(2)四氧化三铁小球表面原位包覆上一层聚多巴胺纳米材料,其中,聚多巴胺壳厚度为30nm左右,具体方法如下:
①取步骤(1)最后制得的Fe3O4溶液5mL,分散在21mL水和0.4mL氨水混
合成的溶液中;
②称取0.1g多巴胺溶于2ml水中,逐滴加入到步骤①的反应溶液中,在常温下磁力搅拌24h;
③将步骤②的溶液在11000W下离心15min,吸出上清液,加去离子水、超声分散再离心,如此3遍,第三遍离心后吸出上清液后再加20ml去离子水超声分散后保存。
(3)制备Fe3O4@PDA@-NH2-DTPA纳米材料,具体方法如下:
取20mg的Fe3O4@PDA分散到100mlPBS缓冲溶液(pH=8.5,10mM)中,向该溶液中加入40mg的1,6-己二胺,强烈搅拌下反应12小时;然后离心得到氨基化的Fe3O4@PDA-NH2,用水洗三次后,重新分散到去离子水中;最后向此溶液中加入过量的DTPAA,并滴加NaOH 调整溶液的pH值到7,反应24小时后,离心分离,弃掉上清液得到Fe3O4@PDA@-NH2-DTPA沉淀。
(4)制备Fe3O4@PDA@-NH2-DTPA-Gd纳米材料:
将Fe3O4@PDA@-NH2-DTPA分散在0.01mol/L的NaOH中,再用HCl调节Fe3O4@PDA@-NH2-DTPA水溶液pH为7,缓慢加入1.8mlGdCl3水溶液(25mM),同时用NaOH溶液(0.1M)调节pH在6到7之间,将上述的混合液继续搅拌12小时,即可制得Fe3O4@PDA@-NH2-DTPA-Gd纳米材料。
(5)材料的表征和性能测试:
动态光散射检测粒径:分别取2ml的Fe3O4、Fe3O4@PDA、Fe3O4@PDA@-NH2、Fe3O4@PDA@-NH2-DTPA和Fe3O4@PDA@-NH2-DTPA-Gd纳米材料,利用Nanosizer Nano-ZS马尔文公司纳米粒径分析仪粒径进行粒径检测。
透射电镜表征:分别取2ml的Fe3O4、Fe3O4@PDA、和Fe3O4@PDA@-NH2-DTPA-Gd纳米材料,在JEOL公司生产的2000-FX型场发射透射电子显微镜上进行TEM观察,加速电压:200 kV。TEM 样品的制备是将所测样品分散至环己烷或者水溶液中,然后滴一滴于涂碳的铜网上,过量的液体用滤纸吸干,后将铜网在室温下干燥,通过JEM-2100透射电子显微镜得到上述材料的微观结构图。
光热转换测试:取0.35mg/ml、0.175mg/ml的Fe3O4@PDA@-NH2-DTPA-Gd纳米材料,并取水做对照,置于1W/cm2的MDL-N-808-8W红外激光器1W cm-2的测量池光照500s,检测其光热转换。采用数字温度计,每隔30s记录一次升温数字。
弛豫率和体外成像性能测试:T1、T2时间在25℃,9.4T条件下,在Bruker Avance 400NMR分光仪上测定;T1、T2弛豫效率在德国Bruker公司生产的AVII-500型核磁共振仪上测量,MRI 成像通过 Magnetom Espree MIR 系统(西门子, 1.5T)测定。
为了考察Fe3O4纳米粒子的形貌及粒径大小,我们对其进行了TEM和DLS分析。其TEM图显示,该纳米粒子的形貌呈球形,具有单分散性,平均粒径为10nm,如图2 (a)。共沉淀法制备的Fe3O4纳米小球的水合粒径为32.8nm,如图2(b)图所示,其多分散性指数(PDI)为0.18,该值小于0.2,进一步说明所制备的纳米材料尺寸均一,单分散性较好。
接下来对Fe3O4@PDA纳米材料进行了电镜考察,结果如图3(a),其粒径在70nm左右,因此PDA壳厚度约为30nm。图3(b)显示Fe3O4@PDA纳米材料的水合粒径为162.2nm,其测试PDI为0.145,表明该纳米粒子具有较好的单分散性。
然后,我们通过在Fe3O4@PDA表面修饰氨基,最终得到了Fe3O4@PDA@-NH2-DTPA-Gd纳米材料。如图4(a),所得TEM图表明Fe3O4@PDA@-NH2-DTPA-Gd纳米粒子的外部形貌与Fe3O4@PDA(图 3a)类似,都呈现平均粒径为70nm的球形结构,并且具有良好的单分散性,说明表面氨基-NH2、Gd-DTPA配体的修饰对于Fe3O4@PDA结构没有明显的影响。该纳米粒子的粒径分布测试表明,其水合粒径为316.6nm,PDI为0.290,如图4(b)。水合粒径与TEM图显示的粒径相差较大的原因是,我们所制备的Fe3O4@PDA-NH2-DTPA-Gd外连有氨基-NH2、Gd-DTPA配体,在水溶液中检测粒径时,配体呈舒展状态,而TEM检测粒径时,是将样品滴在铜网上并干燥,因此水合粒径较大。
所制备纳米材料的T1、T2成像效果如图5(a)所示,随着Fe3O4@PDA@-NH2-DTPA-Gd浓度的减小,T1加权信号逐渐变弱,成像逐渐变暗;T2加权信号逐渐变弱,成像逐渐变暗。该图5(a)直观表明Fe3O4@PDA@-NH2-DTPA-Gd同时具有良好的T1和T2加权成像效果。图5(b)、(c)分别表示Fe3O4@PDA@-NH2-DTPA-Gd的纵向磁豫率值r1=12.6mM-1S-1、横向弛豫率值r2=104.0mM-1S-1,与商用Gd-DTPA(r1=3.7 mM -1s -1) 相比提升了3.4倍的弛豫系数,进一步说Fe3O4@PDA@-NH2-DTPA-Gd具有良好的磁共振成像效果。
为了探索Fe3O4@PDA@-NH2-DTPA-Gd在光热治疗方面的可行性,我们考察了它们的光热转换性能。我们分别将0.35mg/ml、0.175mg/ml的Fe3O4@PDA@-NH2-DTPA-Gd和水溶液用808nm激光器照射500秒,记录溶液的温度变化,结果显示在图6中。很明显,纯水溶液在激光照射下400秒仅升高2度。而当给予激光照射后,Fe3O4@PDA@-NH2-DTPA-Gd的温度快速升高,并且浓度越高,溶液温度增加越快。造成这种结果的原因是,随着浓度的增加,Fe3O4@PDA@-NH2-DTPA-Gd纳米材料在808nm处的光吸收值变强,从而导致其光热转换能力增强。通过光热转化实验,我们得出Fe3O4@PDA@-NH2-DTPA-Gd纳米材料具有良好的光热转换能力,并且浓度越高,光热转换能力越好。
综上,本发明采用已被临床应用的T1造影剂(Gd-DTPA)、T2造影剂(Fe3O4),和具有良好的生物相容性和近红外吸收能力的PDA,用共沉淀法合成了10nm左右的Fe3O4纳米粒子,在其表面包裹PDA,得到单分散性较好的Fe3O4@PDA纳米材料;接下来为了将Gd-DTPA与之接合,我们使Fe3O4@PDA氨基化,最后得到了Fe3O4@PDA-NH2-DTPA-Gd纳米复合材料。实验结果证实,该材料同时具有良好的T1、T2成像效果和光热转换能力,这为开发新的成像指导的光热诊疗剂提供了一个新的平台。
- 还没有人留言评论。精彩留言会获得点赞!