一种多肽纳米微球、制备方法及其在抗肿瘤药物中的应用与流程
本发明属于肿瘤分子生物学领域,特别是涉及一种多肽纳米微球、制备方法及其在抗肿瘤药物中的应用。
背景技术:
多肽在生命过程中具有关键作用,多肽药物是发展最快的领域之一,随着多肽合成技术及多肽重组表达技术的发展,越来越多的多肽药物应用于临床治疗。多肽药物具有制备方便、活性强、容易修饰、不易产生耐药性等优点,但也存在体内容易降解、半衰期短等问题。此外,许多大分子多肽具有良好的抑瘤作用,但由于其难于进入细胞发挥作用,无法作为抗肿瘤药物应用,限制了这类药物的应用。因此,迫切需要采用新的技术提高多肽穿透细胞膜/核膜的能力,提高这类药物的血浆半衰期,这一技术的突破对发展多肽/蛋白药物具有重要价值。
海鞘多肽CS5931是我们研究团队由海洋生物海鞘中获得的抗肿瘤多肽,前期研究表明,CS5931由58个氨基酸组成,分子量5931Da,可以通过线粒体途径诱导多种肿瘤细胞凋亡,对肝癌、结肠癌及肺癌等都具有很强的杀伤活性,对小鼠肝癌和人结肠癌裸鼠移植性肿瘤的抑瘤率分别达到59%和70%。CS5931具有发展成为新型抗肿瘤药物的潜力。但我们前期研究发现CS5931可以主要作用于肿瘤细胞膜表面的烯醇式酶1(Enolase1),能进入细胞内的量很少。但多肽作为药物应用,极易受到体内蛋白酶的攻击而降解,多数多肽的半衰期仅为十至几十分钟。我们测定了CS5931的半衰期,发现其在兔体内的血浆半衰期仅为22min。因此,增加多肽的半衰期对进一步提高其抗肿瘤效果具有重要意义。
纳米技术是近年来发展最快的领域之一,在生物科学的研究方面,纳米技术也获得了广泛应用,包括新型纳米药物的研发、纳米医用材料的应用都取得了突破性进展。本发明将多肽CS5931制备为纳米微球,可大大提高其抗肿瘤活性。
技术实现要素:
本发明的目的是提供了一种多肽CS5931纳米微球,并提供了该纳米微球的制备方法及其在抗肿瘤药物中的应用。
本发明是通过以下技术方案实现的:
一种多肽纳米微球,其特征在于:包括纳米载体和由载体包裹或吸附的多肽CS5931。
优选的,所述多肽CS5931由58个氨基酸组成,分子量5931Da,N末端序列为:MVVPCDGQSECPDGNT。
优选的,所述纳米载体为植物油或十二烷制备的纳米颗粒,所述植物油包括大豆油,橄榄油或其它可食用非调和油。
更优选的,所述纳米载体与多肽CS5931的体积重量比为10:1-3ml/g。
更进一步的,所述的多肽微球的制备方法,包括以下步骤:将多肽CS5931溶于5-15倍体积蒸馏水制备为水溶液,加入植物油或十二烷,将超声探头置于水油液面分界处,超声处理制备成纳米微球,采用超滤膜分离纳米微球,即得。
优选的,所述的多肽纳米微球的制备方法,其特征在于包括以下步骤:将多肽CS5931溶于10倍体积蒸馏水制备为多肽水溶液,多肽水溶液按体积比3:2加入植物油或十二烷,将超声探头置于水油液面分界处,反应温度为20℃,超声强度为150W/cm2,超声时间为3min,采用超滤膜分离纳米微球,收集微球体积小于200纳米的微球,即得。
本发明还提供了上述的多肽纳米微球在抗肿瘤治疗药物中的应用。
相对于现有技术,本发明具有以下有益效果:
1)多肽CS5931具有一定的抗肿瘤活性,但其稳定性差,同时不能直接进入细胞发挥抗肿瘤作用;本发明将多肽CS5931制备成稳定的纳米微球,其稳定性显著增强,在室温(25℃)条件下保存一周而不降解。这很好地解决了多肽的保存问题,为多肽药物的应用开辟了新的途径。
2)本发明将具有显著抗肿瘤活性的多肽CS5931制备为多肽纳米微球,经MTT法检测,该纳米微球具有更高的抗肿瘤活性,其半数抑制浓度(IC50)约为多肽CS5931的十分之一,抗肿瘤活性显著增强。
附图说明
下面结合附图对本发明进一步说明。
附图1为本发明的多肽CS5931纳米微球用戊二醛固定后的电镜扫描图。
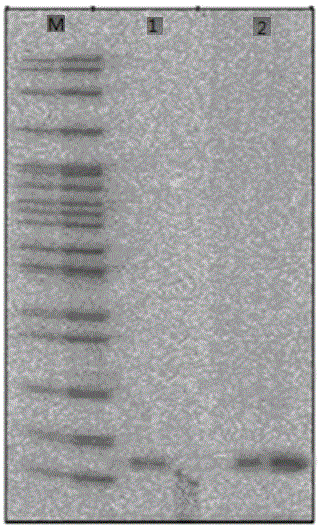
附图2为本发明的多肽CS5931纳米微球的甲醛变性PAGE凝胶电泳图,图中,M:蛋白Marker;1:Cs5931凝胶电泳;2:Cs5931纳米微球凝胶电泳。
附图3为本发明的多肽CS5931纳米微球对结肠癌HCT116和肝癌Bel7402细胞增殖作用图;
具体实施方式
下面结合实施例对本发明进一步说明。
实施例1.多肽CS5931纳米微球的制备方案
多肽CS5931参照以下文献方法进行制备:
MarDrugs.2016Mar21;14(3).pii:E47.doi:10.3390/md14030047.
将多肽CS5931溶于10倍体积蒸馏水制备为多肽水溶液,多肽水溶液按体积比3:2加入保护油层(大豆油),将超声探头置于水油液面分界处(≈150W/cm2),反应温度设定为20℃,超声时间为3Min。采用20kDa的超滤膜分离纳米微球,纳米微球分离出来后经DLS和SME方法分析其大小及粒径分布。多肽CS5931纳米颗粒用戊二醛固定后用扫描电镜分析,实施结果见附图1所示,标尺:100纳米。结果表明应用此方法可制备为200纳米直径大小的多肽CS5931纳米微球,且成均质分布在溶液中。
实施例2.多肽CS5931纳米微球体外稳定性检测
为检测多肽CS5931纳米微球的体外稳定性,将制备得到多肽CS5931样品和采用本发明制备的多肽纳米微球样品,分别在25℃条件下放置0-7天,期间用紫外分光广度计在280纳米处监测蛋白的紫外吸收值变化,结果表明,多肽CS5931放置7天后,吸收度显著降低,但其纳米微球,吸收度没有变化,说明多肽CS5931制备为纳米微球后稳定性显著升高。进一步我们采用甲醛变性PAGE凝胶电泳检测多肽CS5931的完整性,以评价多肽CS5931纳米微球在室温条件下的保存时间。实施结果见附图2,结果表明:多肽CS5931应用实施例1的方法制备为纳米颗粒后可以在室温25℃条件下存放7天而保持多肽的完整性,但未经处理的多肽CS5931在室温条件下存放7天完全降解。
实施例3.多肽CS5931纳米微球体外抗肿瘤活性检测
消化收集处于对数生长期的结肠癌HCT116和肝癌Bel7402细胞,每孔3000个细胞接种于96孔板,24h后,分别加入不同浓度的未处理的多肽及纳米微球(0.25、0.5、1、2、4µM)、阴性对照采用PBS缓冲液,分别于44h加入0.5mg/mLMTT,4h后每孔加入DMSO150µL,溶解后于490nm处测吸收。计算不同浓度的抑制率,并计算IC50。存活率计算公式如下:存活率(%)=OD实验/OD对照×100。
不同浓度的多肽及纳米微球对结肠癌HCT116和肝癌Bel7402细胞的抑制曲线如图3所示。可以看出,多肽能剂量依赖性抑制HCT116和肝癌Bel7402细胞生长,IC50分别为7.9和9.5µM,而多肽制备为纳米微球后抗肿瘤活性大大升高,且对这两种细胞的IC50分别为0.75,1.1µM。
- 还没有人留言评论。精彩留言会获得点赞!