水性外用制剂的制作方法
本发明涉及一种有效成分为酸性药物或其盐的水性外用制剂。
背景技术:
作为酸性药物的外用制剂,广为人知的是双氯芬酸等苯乙酸类非甾体消炎镇痛剂、洛索洛芬等丙酸类非甾体消炎镇痛剂等消炎镇痛剂的外用制剂,为提高药物经皮渗透性的多个技术已被提出(例如,专利文献1~6)。
现有技术文献
专利文献
专利文献1:jph07-173058a
专利文献2:jph10-182450a
专利文献3:jp2005-336063a
专利文献4:jp2014-208623a
专利文献5:jp2014-172857a
专利文献6:jp2014-101338a
技术实现要素:
发明要解决的技术问题:
本发明的目的是,提供一种具有优异的酸性药物经皮渗透性且使用舒适感优异的水性外用制剂。
解决问题的技术方案:
本发明人等努力研究的结果,发现含有异硬脂酸及链烷醇胺的水性外用制剂可以解决上述问题,完成了本发明。即,本发明提供含有酸性药物或其盐、异硬脂酸及链烷醇胺的水性外用制剂。
本发明的水性外用制剂,进而优选含有c2-6脂肪族羟基酸、ph值为4.5~7.8。上述c2-6脂肪族羟基酸,可从乳酸、乙醇酸、苹果酸、酒石酸、柠檬酸组成的群中选择一种或两种以上的组合而成。
上述酸性药物,优选为芳基乙酸类非甾体消炎镇痛剂。
本发明的水性外用制剂,进而优选含有甘油。
发明的有益效果:
本发明的水性外用制剂,具有优异的经皮渗透性,特别是当药物为芳基乙酸类非甾体消炎镇痛剂等消炎镇痛剂时,可期待短时间内有充分的消炎镇痛效果;
本发明的水性外用制剂,还具有优异的使用舒适感,适于用作前端带有发泡树脂或球形等涂布器的填充液体制剂。
附图说明
图1是采用实施例3、5及11所制备的本发明的水性外用制剂及市售的1%双氯芬酸钠液体制剂的大鼠皮肤渗透性试验结果示意图。
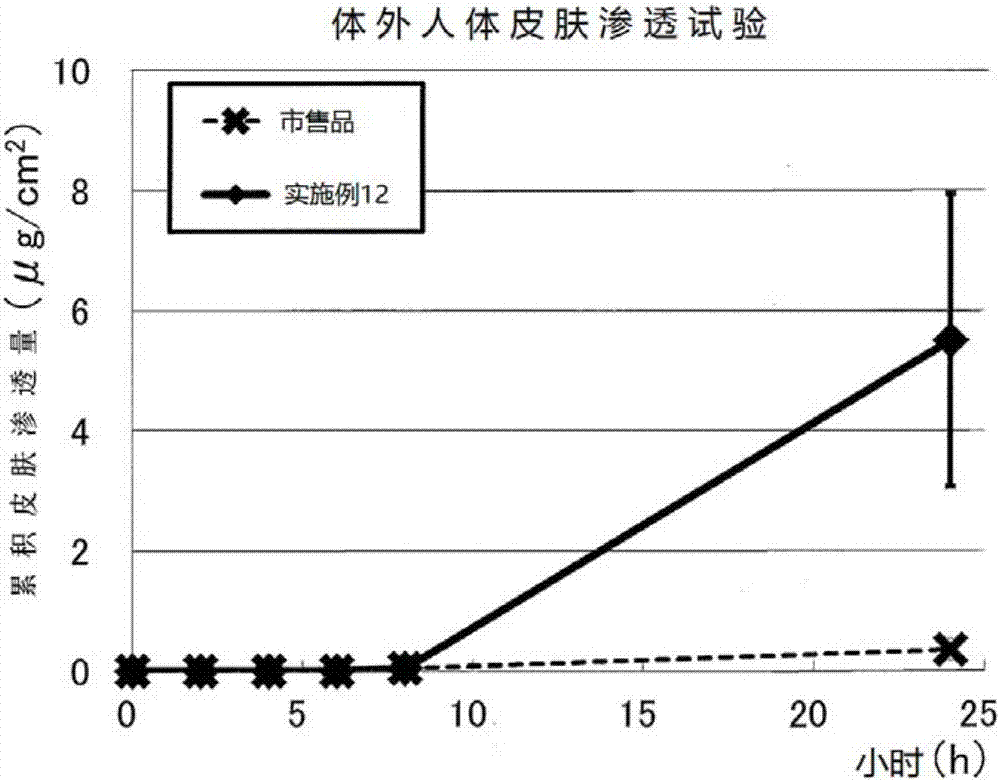
图2是采用实施例12所制备的本发明的水性外用制剂及市售的1%双氯芬酸钠凝胶剂的人体皮肤渗透性试验结果示意图。
具体实施方式
本发明的水性外用制剂,含有作为有效成分的酸性药物或其盐。酸性药物可例示如下:阿氯芬酸、双氯芬酸、联苯乙酸等苯乙酸类非甾体消炎镇痛剂;吲哚美辛、依托度酸、阿西美辛等吲哚乙酸类非甾体消炎镇痛剂;水杨酸、阿司匹林、邻乙氧基苯甲酰胺和双氟尼酸等水杨酸类非甾体消炎镇痛剂;布洛芬、酮洛芬、扎托布洛芬、舒洛芬、普拉洛芬、氟比洛芬和洛索洛芬等丙酸类非甾体消炎镇痛剂;甲灭酸等灭酸类非甾体消炎镇痛剂;头孢唑林、青霉胺、亚胺培南和西司他丁等抗生素;硫喷妥、戊巴比妥、异戊巴比妥、苯巴比妥等巴比妥酸药物;色甘酸等抗过敏剂;普伐他汀、瑞舒伐他汀、阿托伐他汀、辛伐他汀等hmg-coa还原酶抑制剂。其中,优选芳基乙酸类非甾体消炎镇痛剂,如苯乙酸类非甾体消炎镇痛剂、吲哚乙酸类非甾体消炎镇痛剂等,最优选苯乙酸类非甾体消炎镇痛剂。可用于本发明的酸性药物的盐,例示如下:钠、钾等碱金属盐;钙、镁等碱土金属盐;铵盐;二甲胺、二乙胺、三甲胺等烷基胺盐;吡咯乙醇(羟乙基吡咯脘盐)等环胺盐等。
酸性药物或其盐的含量,无特别限制,但可在以下范围选择,如:0.1~20wt%,优选为0.1~10wt%,特别优选为0.5~5wt%。酸性药物或其盐的含量小于上述范围时,可能得不到充分的药物功效,因此不优选。酸性药物或其盐的含量超过上述范围时,酸性药物或其盐不能充分溶解,经过一段时间后可能析出结晶,因此不优选。
本发明的水性外用制剂,构成成分必须含有水,代表性的是液体试剂,但也可应用于凝胶剂、霜剂、巴布剂等。例如,通过在水与低级醇的混合溶液中,溶解酸性药物或其盐、异硬脂酸、链烷醇胺,进而根据需要加入c2-6脂肪族羟基酸溶解而制备的溶液,是本发明的优选方式。
尽管已知使用脂肪酸作为经皮渗透促进剂,但是在含有酸性药物的水性外用制剂中,使用异硬脂酸与使用其它脂肪酸相比,药物的经皮渗透性有飞跃性的提高。特别是,当酸性药物为芳基乙酸类非甾体消炎镇痛剂时,通过添加异硬脂酸的经皮渗透促进效果是显著的。异硬脂酸的含量,例如可在以下范围选择:水性外用制剂的重量的0.5~20wt%,优选2~15wt%,特别优选3~10wt%。而对于酸性药物或其盐,可在以下范围选择:0.1~8倍摩尔,优选0.5~3倍摩尔,更优选1.0~2.5倍摩尔,特别优选1.5~2.4倍摩尔。
链烷醇胺,可以使用具有2至12个碳原子的伯、仲或叔链烷醇胺中的任意一种,但优选三乙醇胺、三异丙醇胺等叔链烷醇胺。
链烷醇胺的含量,可在异硬脂酸含量的0.4~8.0倍摩尔、优选为0.5~4.0倍摩尔的范围选择。当酸性药物为双氯芬酸等苯乙酸类非甾体消炎镇痛剂时,链烷醇胺的含量可以在异硬脂酸含量的0.4~1.5倍摩尔、特别优选为0.6~1.2倍摩尔的范围选择。当酸性药物是吲哚美辛等吲哚乙酸类非甾体消炎镇痛剂时,链烷醇胺的含量可在异硬脂酸含量的2.5~8.0倍摩尔、优选为3.0~4.0倍摩尔的范围选择。
当水性外用制剂还含有后述的c2-6脂肪族羟基酸时,链烷醇胺的含量,例如可在以下范围选择:相对于异硬脂酸和脂肪族羟基酸之总和,为
当酸性药物为双氯芬酸等苯乙酸类非甾体消炎镇痛剂时,链烷醇胺的含量优选为,异硬脂酸含量的
c2-6脂肪族羟基酸,可例示为乳酸、乙醇酸、苹果酸、酒石酸和柠檬酸。c2-6脂肪族羟基酸可以使用1种或组合使用2种以上。当通过含有c2-6脂肪族羟基酸,将水性外用制剂的液体性质调整到适当范围时,不仅酸性药物的溶解度提高,得到即使在长期保存后也不会析出结晶或分离等的稳定外用制剂,并且酸性药物的经皮渗透性也得到提高。含有异硬脂酸以及链烷醇胺的本发明的水性外用制剂,液体性质变为酸性时容易分离,但通过含有c2-6脂肪族羟基酸而变成稳定的液体制剂。c2-6脂肪族羟基酸的含量可适当调整,使水性外用制剂的酸碱性在后述的适当范围内,没有特别限制。例如,可以在如下范围选择:相对于酸性药物为
c2-6脂肪族羟基酸优选至少包含一种酒石酸或一种乳酸,特别优选包含酒石酸。酒石酸包含在内不仅改善了水性外用制剂的稳定性,而且特别提高了经皮渗透性。这可能是因为酒石酸易溶于水性溶媒和脂肪性溶媒,因此在水性外用制剂施用于皮肤后,即使在水和醇等水性溶媒蒸发后,也可以保持溶解状态,因此容易渗入皮肤。c2-6脂肪族羟基酸优选使用酒石酸与乳酸的组合。当酒石酸和乳酸组合使用时,两者的混合比可以在
本发明的水性外用制剂的酸碱度可选择范围为:ph
通过与水混合而用作溶媒的低级醇,可例示为乙醇、丙醇、异丙醇和丙二醇等
本发明的水性外用制剂至少含水10wt%、优选20wt%、特别优选25wt%以上。
本发明的水性外用制剂,进而优选含有甘油。在含有甘油的情况下,酸性药物或其盐的皮肤渗透速度可得到提高,且施用于皮肤后酸性药物或其盐能快速透过皮肤,可得到速效性优异的外用制剂。甘油的含有量可在如下范围内选择:
本发明的水性外用制剂,作为酸性药物或其盐的增溶剂、经皮吸收促进剂,进而也可含有亲油性成分。亲油性成分,按照小于水性外用制剂的20wt%,优选小于15wt%的比例混合。亲油性成分,可例示如下:肉豆蔻酸异丙酯,棕榈酸异丙酯、癸二酸二乙酯等脂肪酸酯;n-甲基吡咯烷酮;二甲基异山梨醇等。其中,优选n-甲基吡咯烷酮或二甲基异山梨醇。
本发明的水性外用制剂,可根据需要包含增稠剂、保湿剂、溶解辅助剂、稳定剂和香料等添加剂。上述增稠剂可例示如下:甲基纤维素、羟甲基纤维素、羟乙基纤维素、羧甲纤维素、羧甲纤维素钠、羧甲基纤维素钙等纤维素;聚乙烯吡咯烷酮;聚乙烯醇;羧基乙烯基聚合物;聚丙烯酸钠等聚丙烯酸酯;等。增稠剂的含量,例如可在
实施例
以下,通过实施例对本发明进行具体说明,但本发明并不受这些实施例的任何限制。
[水性外用制剂的制备]
制备具有表1和表2所示组成(wt%)的水性外用制剂。测量每种制剂的ph值。此外,用肉眼观察水性外用制剂充满玻璃容器时的外观。结果合并表示在表1和表2中。
外观按照以下标准进行评价:
○:澄清溶液
△:得到透明溶液,但随时间经过或因振动等刺激而分离成油相和水相。
[皮肤渗透性试验]
对制备的水性外用制剂以及市售的1%双氯芬酸钠液体制剂,按照常规方法使用弗兰茨扩散池(franzcell)法来进行皮肤渗透性试验。用作试验的是大鼠(5周龄,wistar大鼠,雄性)腹部切下的皮肤。在试验开始后2、4、6小时进行取样。6小时后的累积皮肤渗透量合并表示于表1和表2中。实施例3、5、11以及市售的液体制剂的累积皮肤渗透量的推移示意图,如图1所示。
表1
含有异硬脂酸及链烷醇胺的本发明的实施例1和实施例2的水性外用制剂,与不含有两者的比较例5的制剂相比,显示出更高的皮肤渗透性。含有癸酸和乙酰丙酸作为脂肪酸替代异硬脂酸而制备的比较例1~4的液体制剂,与比较例5的制剂相比,皮肤渗透性更差。实施例3的制剂因进而含有乳酸,相比实施例2的制剂,显示更优异的皮肤渗透性。实施例4的制剂因进而含有甘油,相比实施例3的制剂,显示更优异的皮肤渗透性。
表2
异硬脂酸含量为4~6wt%的实施例4~实施例11的水性外用制剂,均显示良好的皮肤渗透性。其中,异硬脂酸含量较高的制剂,存在皮肤渗透性更优异的倾向。有机胺含量低的实施例7~实施例9的水性外用制剂,存在皮肤渗透性略差的倾向。
如图1所示,本发明的水性外用制剂具有优异的皮肤渗透性,与市售的双氯芬酸钠液体制剂相比,可观察到最大约3倍的双氯芬酸的皮肤渗透。特别是含有甘油的实施例5的液体制剂,具有高渗透速度。
实施例12~21
制备表3所示组成(wt%)的水性外用制剂。测量每种制剂的ph值。此外,用肉眼观察水性外用制剂充满玻璃容器时的外观。结果合并表示于表3中。
外观按照以下标准进行评价。
○:澄清溶液
△:得到透明溶液,但随时间经过或因振动等刺激而分离成油相和水相。
实施例12~15的水性外用制剂,按照常规方法使用弗兰茨扩散池(franzcell)法来进行皮肤渗透性试验。用作试验的是猪皮(yucatan微型猪,雄性,5个月龄)。在试验开始后8及24小时进行取样。累积皮肤渗透量(μg/cm2)合并表示于表3中。
表3
ph值5.0~7.5范围内的所有外用制剂均为稳定的液体制剂,即使在保存后也不会发生分离等。
对实施例12的水性外用制剂和市售的1%双氯芬酸钠凝胶制剂,按照常规方法采用弗兰茨扩散池(franzcell)法来进行人体皮肤渗透性试验。双氯芬酸的累积皮肤渗透量的推移示意图,如图2所示。
实施例2-1~2-6
制备含有表4所示组成(wt%)的吲哚美辛为活性成分的水性外用制剂。测量每种制剂的ph。此外,用肉眼观察玻璃容器充满水性外用制剂时的外观。结果示于表4。
外观按照以下标准进行评价。
○:澄清溶液
对实施例2-1至2-5的水性外用制剂和市售的1%吲哚美辛液体制剂,按照常规方法采用弗兰茨扩散池(franzcell)法来进行皮肤渗透性试验。用作试验的是猪皮(yucatan微型猪,雄性,5个月龄)。从试验开始后到24小时之间的累积皮肤渗透量(μg/cm2)如表4所示。
表4
工业实用性
本发明的水性外用制剂,可用作快速表现出优异消炎镇痛效果的液体制剂,特别是可用作前端带有发泡树脂或球形等涂布器的填充用液体制剂。
- 还没有人留言评论。精彩留言会获得点赞!