预防或治疗癌症的药物组合物及使用该药物组合物的方法与流程
本公开涉及一种用于预防或治疗癌症的药物组合物和使用该药物组合物的治疗方法。
背景技术:
癌症免疫治疗是指使用身体免疫系统治疗癌症的治疗方法。癌细胞可以具有细胞表面分子,例如蛋白质或碳水化合物,其可以经常被免疫系统检测。癌症免疫治疗可以通过靶向这些抗原来诱导免疫系统侵袭癌细胞。激活抗肿瘤免疫的一种方法是阻断免疫检查点通路。免疫检查点通路是指维持自身耐受并保护组织免受导致损伤的过度免疫反应的细胞内信号通路。一些免疫检查点是肿瘤细胞的主要免疫逃避机制。因此,抑制或阻滞免疫检查点可以诱导t细胞的活化,从而可以改善抗肿瘤免疫。
转化生长因子(tgf)-β是调节细胞增殖和分化、伤口愈合、细胞外基质产生等的细胞因子。tgf-β家族属于tgf-β超家族,该tgf-β超家族包括激活素、抑制素、骨形态发生蛋白和抗缪勒氏激素。各种癌症晚期肿瘤内的肿瘤细胞和基质细胞通常过度表达tgf-β。tgf-β会引起刺激血管生成和细胞运动性、抑制免疫系统、并增加肿瘤细胞与细胞外基质的相互作用。tgf-β受体是丝氨酸/苏氨酸激酶受体,且分为tgf-β受体1、tgf-β受体2和tgf-β受体3。其中,tgf-β受体1也称为激活素a受体ii型样激酶(alk5)。
因此,为了有效预防或治疗癌症,需要能够有效抑制tgf-β信号通路以及提高抗肿瘤免疫力的药物组合物。
技术实现要素:
技术方案
提供了一种用于预防或治疗癌症的药物组合物,该药物组合物包括具有tgf-β信号通路抑制活性的化合物和t淋巴细胞激活因子。
提供了一种使用具有tgf-β信号通路抑制活性的化合物和t淋巴细胞激活因子来治疗或预防癌症的方法。
有益效果
可以使用根据一方面的用于预防或治疗癌症的药物组合物和使用该药物组合物预防或治疗癌症的方法来有效预防或治疗癌症。
附图说明
从以下结合附图对实施方式的说明中,这些和/或其他方面将变得显而易见并且更容易理解,其中:
图1a至图1c是示出根据tew-7197、抗ctla4抗体、抗-pd-l1抗体或抗pd1抗体的组合的肿瘤体积(mm3)的图。
具体实施方式
一方面提供了用于预防或治疗癌症的药物组合物,所述药物组合物包括由式i表示的化合物,其药学上可接受的盐、溶剂合物或立体异构体,或它们的组合;和t淋巴细胞激活因子:
[式i]
其中,在式i中,ra可以各自独立地为氢(h)、卤素、c1-6烷基、c1-6卤代烷基、c3-6环烷基、oh、-o-c1-6烷基,-o-c1-6卤代烷基、-o-c3-6环烷基、-nh2、-nh-c1-6烷基、-nh-c1-6卤代烷基、-nh-c3-6环烷基、-s-c1-6烷基、-s-c1-6卤代烷基、-s-c3-6环烷基、-cn或-no2-;
m可以为0、1、2、3或4;
a1和a2中的任一个可以是n,另一个是nr1,其中r1可以是h、oh、c1-6烷基、c1-6卤代烷基或c3-6环烷基;
x可以是键、-(ch2)p-、-nr2-、-o-或-s-,其中p可以是0或1,并且r2可以是h或c1-3烷基;
rb可以各自独立地为h、卤素、c1-6烷基、c1-6卤代烷基、c3-6环烷基、c2-6烯基、c2-6炔基、-(ch2)q-or3、-(ch2)q-nr3r4、-(ch2)q-sr3、-(ch2)q-no2、-(ch2)q-conhoh、-(ch2)q-cn、-(ch2)q-cor3、-(ch2)q-co2r3、-(ch2)q-conr3r4、-(ch2)q-四唑、-(ch2)q-ch=ch-cn、-(ch2)q-ch=ch-co2r3、-(ch2)q-ch=ch-conr3r4、-(ch2)q-ch=ch-四唑、-(ch2)q-nhcor3、-(ch2)q-nhco2r3、-(ch2)q-conhso2r3、-(ch2)q-nhso2r3、-(ch2)q-c=c-cn、-(ch2)q-c=c-co2r3、-(ch2)q-c=c-conr3r4、-(ch2)q-c=c-四唑、-(ch2)q-sor5、-(ch2)q-so2r5或-(ch2)r-(or3)2,其中r3和r4各自独立地为h、c1-6烷基、c1-6卤代烷基或c3-6环烷基,或和与其结合的氮原子一起形成单环,例如咪唑、吡咯烷、哌啶、吗啉、哌嗪和高哌嗪,r5可以是c1-6烷基、c1-6卤代烷基或c3-6环烷基,q可以是0、1、2、3或4,r可以是1、2、3或4;并且
n可以是0,1,2,3,4或5。
烷基可以是直链或支链的。烷基的示例可以包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、正戊基和正己基。烷基可以被选自烷氧基、环烷氧基、氨基、硝基、羧基、氰基、卤素、羟基、磺基、巯基或其组合中的至少一种取代。
环烷基可以是环丙基、环丁基、环戊基或环己基。
卤素可以是氟、氯、溴或碘。
烯基可以是直链或支链的。烯基可以是乙烯基、烯丙基、异戊二烯基、2-丁烯基或2-己烯基。烯基可以被烷氧基、环烷氧基、氨基、硝基、羧基、氰基、卤素、羟基、磺基、巯基或其组合取代。
炔基可以是直链或支链的。炔基可以是乙炔基、炔丙基或2-丁炔基。炔基可以被烷氧基、环烷氧基、氨基、硝基、羧基、氰基、卤素、羟基、磺基、巯基或其组合取代。
化合物可以是由式ii表示的化合物:
[式ii]
式ii的化合物可以是n-((4-([1,2,4]三唑并[1,5-a]吡啶-6-基)-5-(6-甲基吡啶-2-基)-1h-咪唑-2-基)甲基)-2-氟苯胺。
式i的化合物,例如式ii的化合物可以选择性地抑制tgf-β受体1(alk5)和/或1b型激活素受体(acvr1b或alk-4)。
药学上可接受的盐可以是不会对给药了化合物的生物体引起显著刺激并且不会消除化合物的生物活性和特性的盐。该盐可以是例如无机酸盐、有机酸盐或金属盐。无机酸盐可以是盐酸、溴酸、磷酸、硫酸或焦硫酸的盐。有机酸盐可以是甲酸、乙酸、丙酸、乳酸、草酸、酒石酸、苹果酸、马来酸、柠檬酸、富马酸、苯磺酸,樟脑磺酸、乙二磺酸、三氯乙酸、三氟乙酸、苯甲酸、葡萄糖酸、甲磺酸、乙醇酸、琥珀酸、4-甲苯磺酸、半乳糖醛酸、扑酸、谷氨酸,乙磺酸、苯磺酸、对甲苯磺酸或天冬氨酸的盐。金属盐可以是钙盐、钠盐、镁盐、锶盐或钾盐。
溶剂合物可以是由溶质分子和溶剂分子之间的吸引力形成的化合物。溶剂合物可以是水合物。
立体异构体是指其原子具有相同的分子式和连接性但原子的空间排列不同的分子。立体异构体可以是化学式i的化合物的非对映异构体或对映异构体。
t淋巴细胞激活因子是指诱导t细胞活化的分子。t淋巴细胞激活因子可以是免疫检查点抑制剂、免疫刺激分子、免疫抑制因子抑制剂或其组合。
免疫检查点是指免疫系统中增大t细胞信号(共刺激分子)或降低t细胞信号的分子。免疫检查点分子可以是免疫刺激分子或免疫抑制分子。免疫刺激分子可以是诱导t细胞活化的激动剂。免疫刺激分子可以是cd27、cd40、ox40、gitr、cd137、cd28、诱导型t细胞共刺激因子(icos)或其组合。
免疫检查点的抑制或阻滞可以指对免疫耐受性的抑制或对免疫系统的激活。免疫检查点阻滞可以包括激活t细胞以增加抗肿瘤免疫应答的任何信号通路。免疫检查点抑制剂可以指抑制或阻滞抑制性检测点分子以激活t细胞的分子。免疫检查点抑制剂可以是释放对t细胞的抑制的拮抗剂。
t淋巴细胞激活因子可以是可以抑制信号转导或减少t细胞受体的表达的激动剂,所述t细胞受体选自由以下所组成的组:程序性细胞死亡蛋白1(pd1)、细胞毒性t淋巴细胞相关抗原4(ctla4)、b和t淋巴细胞弱化子(btla)、杀伤细胞免疫球蛋白样受体(kir)、淋巴细胞激活基因3(lag3)、t细胞膜蛋白3(tim3)和腺苷a2a受体(a2ar)。pd1、ctla4、btla、kir、lag3、tim3和a2ar是传递t细胞抑制信号的t细胞受体。在这方面,t淋巴细胞激活因子可以抑制信号转导或降低pd1、ctla4、btla、kir、lag3、tim3、a2ar或其组合的表达以激活t细胞。
t淋巴细胞激活因子可以是可以抑制信号转导或降低抗原呈递细胞(apc)的表面蛋白的表达的拮抗剂,抗原呈递细胞(apc)的表面蛋白选自由以下所组成的组:程序性死亡配体1(pd-l1或pdl1)、程序性死亡配体2(pd-l2或pdl2)、分化簇(cd)80、cd86、b7-h3、b7-h4、疱疹病毒侵入介质(hvem)和半乳凝素9(gal9)。pd-l1、pd-l2、cd80、cd86、b7-h3、b7-h4、hvem、gal9或其组合是apc的表面蛋白,其可以与传递t细胞的抑制信号的t细胞受体结合。在这方面,t淋巴细胞激活因子可以抑制信号转导或降低pd-l1、pd-l2,、cd80、cd86、b7-h3、b7-h4、hvem、gal9或其组合的表达以活化t细胞。
t淋巴细胞激活因子可以是激活t淋巴细胞受体的激动剂。t淋巴细胞激活因子可以是可以诱导信号转导或提高t淋巴细胞受体的表达的激动剂,所述t淋巴细胞受体选自由cd28、icos、cd137、ox40和cd27所组成的组。cd28、icos、cd137、ox40和cd27是传递t细胞的活化信号的t细胞受体。可通过激活信号转导或提高t淋巴细胞受体的表达来激活t细胞。在这方面,刺激检查点分子可以激活信号转导或提高d28、icos、cd137、ox40、cd27或其组合的表达以激活t细胞。
免疫抑制因子是指抑制或阻滞抗肿瘤免疫反应性的分子。免疫抑制因子可以是转化生长因子-β(tgfβ)、白介素(il)-10、前列腺素e2(pge2)、ccl2(也称为巨噬细胞化学吸引蛋白1:mcp-1)、fas受体(fasr)/配体(fasl)、细胞毒性t淋巴细胞抗原-4(ctla-4)、b7同系物1(b7-h1)、程序性死亡配体-1(pd-l1)或其组合。免疫抑制因子的抑制剂可以诱导t细胞的活性。免疫抑制因子可以是选自由tgfβ、il-1、il-6、il-10、il-12和il18所组成的组中的一种,或可以是调节选自该组中所述一种的激动剂。该调节可能是对功能的抑制或激活,或对表达的减少或提高。tgfβ、il-1、il-6、il-10、il-12和il-18是细胞因子,并且对细胞因子的抑制可以激活t细胞。
免疫抑制因子的激动剂、拮抗剂或抑制剂可以是多肽、糖、核酸、低分子量化合物或其组合。多肽可以是抗体或其抗原结合片段。术语“抗体”可以与术语“免疫球蛋白(ig)”互换使用。整个抗体具有包括两条全长轻链和两条全长重链的结构,每条轻链通过二硫键(ss-键)与重链结合。抗体可以是iga、igd、ige、igg或igm。术语“抗原结合片段”是指ig的整个结构的片段,即包括抗原可以结合的部分的多肽的一部分。抗原结合片段可以是f(ab')2、fab'、fab、fv或scfv。抗体可以是单克隆抗体或多克隆抗体。核酸的示例可以包括微rna(mirna)和小干扰rna(sirna)。
t淋巴细胞激活因子可以是pd-l1抑制剂、pd1抑制剂、ctla4抑制剂或其组合。pd-l1抑制剂的示例可包括bms-936559(mdx1105,bristolmyerssquibb)、medi4736(medimmune,astrazeneca)、mpdl3280a(roche)和msb0010718c(merck)。pd1抑制剂的示例可以包括amp-224(amplimmune,glaxosmithklein)、amp-514(medi0680,amplimmune,glaxosmithklein)、nivolumab(opdivo,bristolmyerssquibb)、pembrolizumab(keytruda,merck)和pidilizumab(curetech)。ctla4抑制剂的示例可以包括ipilimumab(yervoy,bristolmyerssquibb)和tremelimumab(pfizer)。
癌症可能是实体癌或非实体癌。实体癌是指在器官中出现癌性肿瘤,所述器官例如肝、肺、乳房、皮肤等。非实体癌是指在血液中出现的癌症,也称为血癌。癌症可以是癌、肉瘤、源自造血细胞的癌症、生殖细胞肿瘤或胚细胞瘤。癌可以是源自上皮细胞的癌症。肉瘤可以是源自结缔组织(即骨、软骨、脂肪和神经)的癌症,该缔结组织可从源自骨髓外部的间充质细胞的细胞生长而来。源自造血细胞的癌症可以源自倾向于在淋巴结和离开骨髓的血液中成熟的造血细胞。生殖细胞肿瘤可以是源自多能细胞的癌症。多能细胞通常可存在于睾丸或卵巢中。胚细胞瘤可以源自未成熟的前体细胞或胚胎组织。癌症可以选自由以下所组成的组:黑素瘤、脑脊液脑肿瘤、头颈癌、肺癌、乳腺癌、胸腺瘤、间皮瘤、食道癌、胃癌、结肠癌、肝癌、胰腺癌、胆道癌、肾癌、膀胱癌、前列腺癌、睾丸癌、精原细胞瘤、甲状腺癌、卵巢癌、宫颈癌、子宫内膜癌、淋巴瘤、骨髓增生异常综合征(mds)、骨髓纤维化、急性白血病、慢性白血病、多发性骨髓瘤、肉瘤和皮肤癌。
术语“预防”是指通过给药药物组合物来延缓癌症的发生的所有作用,术语“治疗”是指通过给药药物组合物使癌症的症状得以好转或得以有利地减轻的所有作用。
药物组合物还可以包括药学上可接受的载体。载体可以意在包括赋形剂、稀释剂或补充剂。载体可以选自由以下所组成的组:乳糖、右旋糖、蔗糖、山梨醇、甘露糖醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、金合欢胶、藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、聚乙烯基吡咯烷酮、水、生理盐水、缓冲剂例如pbs、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁、矿物油等。组合物可以包括填充剂、抗凝剂、润滑剂、湿润剂、香料、乳化剂、防腐剂等。
该药物组合物可以基于传统方法被制备成任何制剂。该组合物可以被配制成口服剂型(例如粉剂、片剂、胶囊剂、糖浆、丸剂或颗粒剂)或肠胃外剂型(例如可注射制剂)。此外,该组合物可以被制备成全身剂型或局部剂型。
该药物组合物可以是单一组合物或分立组合物。例如,包括式i化合物,其药学上可接受的盐、溶剂合物、立体异构体,或它们的组合的药物组合物可以是口服剂型的组合物,而t淋巴细胞激活因子可以是腹部剂型的组合物。
药物组合物可以包括式i化合物,其药学上可接受的盐、溶剂合物、立体异构体,或它们的组合;和有效量的t淋巴细胞激活因子。术语“有效量”是指当向需要预防或治疗的受试者给药时显示出预防或治疗效果的足够量。本领域普通技术人员可以根据要选择的细胞或受试者而适当选择有效量。有效量可以根据包括以下的因素而定:疾病的严重程度,患者的年龄、体重、健康状况、性别和对药物的敏感性,给药时间,给药途径,排泄率,治疗期,与该组合物混合或组合使用的药物,还可以根据医疗领域众所周知的其它因素而定。基于该药物组合物,有效量可以在如下范围:约0.5μg至约2g、约1μg至约1g、约10μg至约500mg、约100μg至约100m或约1mg至约50mg。
药物组合物的给药剂量可以为,例如,对于成人,在约0.001mg/kg至约100mg/kg、约0.01mg/kg至约10mg/kg或约0.1mg/kg至约1mg/kg的范围内,每天一次、每天多次、每月一次至四次或每年一次至十二次。
另一方面提供了一种预防或治疗癌症的方法,所述方法包括向受试者给药根据本发明的一个方面的式i化合物,其药学上可接受的盐、溶剂合物或立体异构体,或它们的组合以及t淋巴细胞激活因子。
式i化合物,其药学上可接受的盐、溶剂合物或立体异构体;t淋巴细胞激活因子;癌症;预防和治疗与上述相同。
受试者可以是人、牛、马、猪、狗、绵羊、山羊或猫。受试者可能是患有癌症或高概率罹患癌症的受试者。
可以通过任何合适的方法,例如口服给药、静脉内给药、肌肉内给药、透皮给药、粘膜给药、鼻内给药、气管内给药或皮下给药而对化合物,其药学上可接受的盐、溶剂合物、立体异构体或它们的组合以及t淋巴细胞激活因子直接进行给药。化合物,其药学上可接受的盐、溶剂合物、立体异构体或它们的组合以及t淋巴细胞激活因子可以单独与另一种药学活性化合物被全身或局部给药。
化合物,其药学上可接受的盐、溶剂合物、立体异构体或它们的组合以及t淋巴细胞激活因子可以同时、单独或顺序地给药。
化合物,其药学上可接受的盐、溶剂合物、立体异构体或它们的组合以及t淋巴细胞激活因子的优选给药剂量可以根据患者的病情和体重、疾病严重程度、药物制剂、给药途径和给药期而不同,但是本领域普通技术人员可以适当地对其进行选择。给药剂量可以为,例如,对于成人,在约0.001mg/kg至约100mg/kg、约0.01mg/kg至约10mg/kg或约0.1mg/kg至约1mg/kg的范围内,每天一次、每天多次、每月一次至四次或每年一次至十二次。
现在将详细参考实施方式(其示例在附图中示出),其中相同的附图标记始终表示相同的元件。在这方面,当前实施方式可以具有不同的形式,并且不应被解释为限于本文中所阐述的说明。因此,下面仅通过参考附图来描述实施方式进而解释本说明书的多个方面。如本文所用,术语“和/或”包括一个或多个相关所列项的任何和所有组合。
在下文中,将参考示例对本发明进行更详细的说明。然而,这些示例仅用于说明的目的,本发明不受这些示例的限制。
示例1.在异种移植有黑素瘤细胞的小鼠模型中的抗肿瘤效果测试
1.制备小鼠模型和药物
为了验证体内抗肿瘤效果,从koatechco.(southkorea)购得5周龄的雌性spfc57bl6小鼠。将这些小鼠保持在温度控制在约22℃的房间内,同时给它们自由地供应食物和水。1周后,通过皮下注射将5×104个b16f10黑素瘤细胞系(atcc,crl-6475tm)细胞注射到这些6周龄的小鼠中。在实验中使用注射了黑素瘤细胞系2周后的8周龄小鼠。
作为载体,将7ml37%(v/v)胃酸、2.0gnacl、3.2g胃蛋白酶(sigma-aldrich)和蒸馏水混合在一起以制备1000ml人造胃液。作为给药药物,将n-((4-([1,2,4]三唑并[1,5-a]吡啶-6-基)-5-(6-甲基吡啶-2-基)-1h-咪唑-2-基)甲基)-2-氟苯胺(以下称为“tew-7197”)(syngene,india)溶解在载体中以制备2.5mg/ml的tew-7197溶液。
对于另一种给药药物,制备抗pd-l1单克隆抗体(通过请求anrtherapeuticsco.,ltd.而制备,宿主细胞:hek293f)、抗-pd1单克隆仓鼠抗体(bioxcell,目录号be0033-2)、抗ctla4单克隆仓鼠抗体(bioxcell,目录号be0131)、人免疫球蛋白g(igg)(thermoscientific,目录号31154)和单克隆仓鼠igg(bioxcell,目录号be0091)。
2.向小鼠模型给药药物并测量通过给药药物引起的体重
向在1中制备的小鼠模型口服给药2.5mg/ml的tew-7197溶液,剂量为25mg/kg,每日一次,在一周中连续进行5天。然后,在最后的两天期间,不向它们给药tew-7197溶液。通过腹腔注射向这些小鼠以每只小鼠约100μg的剂量给药抗体,每2天一次。对于tew-7197的对照组,使用赋载体给药组。对于抗体对照组,使用人igg给药组和仓鼠igg给药组。
给药至小鼠模型的药物示于表1中。
【表1】
从给药当天(开始日期)到第11天,每2天测量小鼠的体重。通过药物给药引起的小鼠变化(%)(平均(%)±标准偏差)示于表2。
【表2】
t-测试:**p<0.01(相对于人igg给药组)
如表2所示,通过抗pd-l1抗体、抗pd1抗体、抗ctla4抗体、tew-7197及其组合几乎没有引起的小鼠的显著体重变化。
3.测试药物在小鼠模型中的肿瘤抑制作用
如2.所述进行药物给药,然后在最后一剂给药后20分钟处死小鼠,从小鼠切除肿瘤。用卡尺测量肿瘤体积,并使用等式1计算:
[等式1]
肿瘤体积(mm3)=[长度(mm)×宽度(mm)×高度(mm)]/2
计算起始日期的初始肿瘤体积(v0)与给药药物后的肿瘤体积(vt)之差,以计算肿瘤体积的变化(δt=vt-v0)。从计算的肿瘤体积,计算通过药物给药的肿瘤抑制率(%)。其结果示于表3。
【表3】
t-测试:*p<0.05,**p<0.01,***p<0.001(相对于赋形剂给药组、人igg给药组或仓鼠igg给药组),
如表3所示,在第11天,抗pd-l1抗体和tew-7197给药组(组7)的肿瘤抑制率是抗pd-l1抗体给药组(组4)的肿瘤抑制率的约2.5倍,并且是tew-7197给药组(组10)的肿瘤抑制率的约1.9倍。在第11天,抗pd1抗体和tew-7197给药组(组8)的肿瘤抑制率是抗pd1抗体给药组(组5)的肿瘤抑制率的约3.5倍并且是tew-7197给药组(组10)的肿瘤抑制率的约1.3倍。在第11天,抗ctla4抗体和tew-7197给药组(组9)的抗肿瘤抑制率是抗ctla4抗体给药组(组6)的抗肿瘤抑制率的约3.2倍并且是tew-7197给药组(组10)的抗肿瘤抑制率的约1.3倍。
因此,与抗pd-l1抗体、抗pd1抗体、抗ctla4抗体和tew-7197中的各个相比,发现作为免疫检查点抑制剂的抗pd-l1抗体、抗-pd1抗体和抗ctla4抗体与作为tgf-β受体的抑制剂的tew-7197的组合具有显著的肿瘤抑制效果。
4.小鼠模型中的药物协同组合测试
进行通过免疫检查点抑制剂和tgf-β受体抑制剂的协同组合对肿瘤抑制效果的测试。
详细地,如1.中所述,制备c57bl/6小鼠,向每只小鼠注射1×104个b16f10黑素瘤细胞系(atcc,crl-6475tm)细胞。当每组平均肿瘤大小达到26.0mm3时,进行药物给药。
如1所述,制备tew-7197、抗ctla4抗体、抗-pd-l1抗体、抗pd1抗体、人igg和仓鼠igg作为药物。
向所制备的小鼠口服给药tew-7197溶液,剂量为10mg/kg,每天一次,在一周中连续进行5天。然后,在最后2天期间,不给药tew-7197溶液。通过腹腔注射向这些小鼠以每只小鼠约100μg的剂量给药抗体,每2天一次。在阴性对照组中,对于tew-7197,给药赋形剂;对于抗体,给药人igg或仓鼠igg。药物给药11天后,用卡尺测量肿瘤体积,并如3所述进行计算。
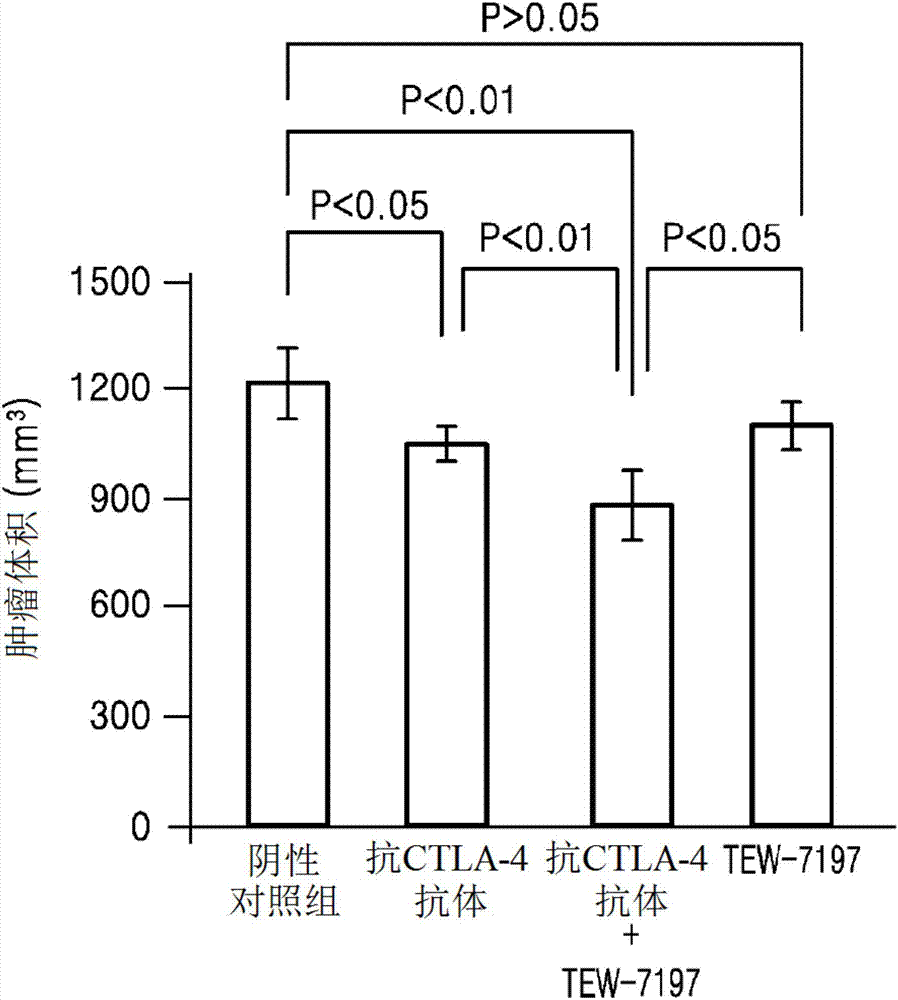
根据tew-7197和抗ctla4抗体、抗-pd-l1抗体或抗pd1抗体的组合的肿瘤体积示于图1a至图1c中。
如图1a所示,与阴性对照组的肿瘤体积相比,抗ctla4抗体给药组、tew-7197给药组和抗ctla4抗体与tew-7197给药组组合的肿瘤体积分别减少约14.5%、约10.1%和约27.1。
如图1b所示,与阴性对照组的肿瘤体积相比,抗pd-l1抗体给药组、tew-7197给药组和抗pd-l1抗体与tew-7197给药组组合的肿瘤体积分别减少约15.0%、约9.2%和28.8%。
如图1c所示,与阴性对照组的肿瘤体积相比,抗pd1抗体给药组、tew-7197给药组和抗pd1抗体与tew-7197给药组组合的肿瘤体积分别减少约9.6%、约8.1%和约23.3%。
因此,与抗-pd-l1抗体、抗pd1抗体、抗ctla4抗体和tew-7197中的每个相比,作为免疫检查点抑制剂的抗pd-l1抗体、抗-pd1抗体和抗ctla4抗体与作为tgf-β受体的抑制剂的tew-7197的组合具有协同的肿瘤抑制效果。
应当理解,本文描述的实施方式应仅在说明性意义上被考虑,而并非为了限制的目的。对每个实施方式内的特征或方面的描述应通常被认为可用于在其它实施方式中的其它类似特征或方面。
虽然已经参考附图描述了一个或多个实施方式,但是本领域普通技术人员将会理解,在不脱离如通过所附权利要求限定的本发明构思的精神和范围的情况下,可以对形式和细节进行各种改变。
- 还没有人留言评论。精彩留言会获得点赞!