用于自适应放射治疗的三维定位和追踪的制作方法
相关申请的交叉引用
本申请与于2015年1月28日提交的题目为“threedimensionallocalizationandtrackingofamovingtargetforadaptiveradiationtherapy(用于自适应放射治疗的移动靶的三维定位和追踪)”的12475.0058-00000相关,该申请的全部内容通过引用并入本文。
本公开总体上涉及放射治疗或放射疗法。更具体地,本公开涉及在制定在放射疗法期间要使用的放射疗法治疗计划时使用的用于对肿瘤进行三维追踪的系统和方法。
背景技术:
放射疗法用于治疗哺乳动物(例如人和动物)组织中的癌症或其它疾病。一种这样的放射疗法技术是“伽马刀”,通过“伽马刀”,患者被以较高强度和高精度汇聚到靶(例如肿瘤)处的大量低强度的γ射线照射。在另一个示例中,使用直线加速器提供放射疗法,由此靶区被高能粒子(例如电子、质子、离子等)照射。必须准确地控制放射束的放置和剂量以确保肿瘤接收处方的放射,并且射束的放置应当使得对周围健康组织(通常被称为“危及器官”(oar))的损害最小化。
例如,放射束可以通过使用多叶准直器而被成形为匹配肿瘤的形状(例如,多叶准直器包括可以彼此独立地移动以创建定制的放射束形状的多个钨叶)。(放射被称为“处方的”,因为医师为肿瘤和周围的器官开出了类似于药物处方的预定义的放射量)。
传统上,对于每个患者,可以使用基于临床和剂量测定目标和约束(例如,对肿瘤和关键器官的最大、最小和平均放射剂量)的优化技术来创建放射疗法治疗计划(“治疗计划”)。治疗计划过程可以包括使用患者的三维图像来识别靶区(例如,肿瘤),并且识别肿瘤附近的关键器官。治疗计划的创建可能是一个耗时的过程,其中,计划者试图遵守各种治疗目标或约束(例如,剂量体积直方图(dvh)目标),考虑它们各自的重要性(例如,权重),以产生临床上可接受的治疗计划。这个任务可能是由于各种危及器官(oar)复杂化的耗时的试错过程,因为随着oar的数量增大(例如,对于头颈部治疗高达十三处),该过程的复杂性也增大。远离肿瘤的oar可以更容易地免于放射,但靠近靶肿瘤或与靶肿瘤重叠的oar可能更难以免于放射。
传统上,计算机断层摄影(ct)成像用作用于放射治疗的治疗计划的图像数据的主要来源。ct图像提供患者几何形状的准确表示,并且ct值可以直接转换为用于放射剂量计算的电子密度(例如,亨斯菲尔德单位)。然而,使用ct使患者暴露于附加的放射剂量。除ct图像之外,磁共振成像(mri)扫描由于它们相比于ct图像的较好的软组织对比度而可以被用于放射治疗。mri没有电离放射,并且可以被用于捕捉诸如组织代谢和功能的人体的功能信息。
可以使用诸如计算机断层摄影(ct)、荧光透视、以及核磁共振成像(“mri”)的成像系统来确定靶的定位并追踪靶(例如,组织、肿瘤等)。由于mri可以在不使用如ct所使用的电离放射的情况下提供极好的软组织对比度,因而通常使用mri。与成像系统集成的放射治疗系统的示例可以包括mri-linac,其可以使用靶(例如肿瘤)的三维(3d)图像。mri-linac的mri装置可以提供对应于患者的组织中氢核的局部图的多个图像。该患者图像可以在二维(2d)平面或三维体积中获取。由于器官和肿瘤在患者体内移动,因此对靶进行快速和准确的3d定位是重要的。例如,靶器官或肿瘤可能由于多种类型的运动(例如,呼吸、心脏的、蠕动或其它类型的患者运动)而移动。然而,2dmr切片通常是在患者的身体的特定位置处获取的,并且由于靶器官或肿瘤的运动,2dmr切片可能不包括肿瘤/靶。因此,需要一种获取靶肿瘤并且追踪该肿瘤的结构和运动的系统和方法,使得所获取的2dmr切片在位置、取向和/或厚度方面包含靶肿瘤并且是在临床环境中在2dmr切片上是可见的。
本概述是本申请的一些教导的概述,并不旨在作为本主题的排他或穷尽的处理。关于本主题的进一步细节在具体实施方式和所附权利要求中找到。在阅读并理解以下具体实施方式并参见形成具体实施方式的一部分的附图之后,本发明的其它方案对于本领域技术人员将是显而易见的,每一个方案都不被视为限制性含义。本发明的范围由所附权利要求及它们法律上的等同物限定。
技术实现要素:
本公开的某些实施例涉及一种用于医疗图像处理的方法,所述方法可以由执行多个计算机可执行指令的处理器装置来实现。所述方法可以对经受图像引导放射治疗的患者中移动的三维(3d)靶进行定位及追踪,并且所述方法包括:(a)接收用于所述患者中的关注区域的自适应滤波器模型,其中所述自适应滤波器模型基于待追踪的所述靶;(b)由图像采集装置获得所述患者中的关注区域的二维(2d)切片;(c)由处理器将所述自适应滤波器模型应用于所述2d切片,其中所述自适应滤波器模型包括偏移值;(d)由所述处理器基于所述自适应滤波器模型确定在所述2d切片中所述靶的位置;(e)由所述处理器基于所述偏移值估计所述靶的可能位置;以及由所述处理器重复(b)到(e)以在对所述患者的图像引导放射治疗期间对所述移动的靶进行追踪。
本公开的某些实施例涉及一种医学图像处理系统。所述系统可以对根据放射疗法治疗计划使用图像引导放射治疗装置待照射的移动的三维(3d)靶进行定位和追踪,所述系统可以包括:处理器以及可操作地联接到所述处理器的存储器。所述存储器可以存储多个医学图像、多个自适应滤波器模型、采集方案、以及计算机可执行指令,当由所述处理器执行所述计算机可执行指令时,使所述处理器执行方法。所述方法可以包括:(a)根据所述采集方案从存储器取得二维(2d)切片;(b)由所述处理器将所述2d切片转换到特定处理域;(c)由所述处理器将所述自适应滤波器模型应用于所述2d切片,其中所述自适应滤波器模型包括偏移值;(d)由所述处理器为每个自适应滤波器模型生成响应图,其中,所述响应图包括所述2d切片的每个位置的置信度得分;(e)由所述处理器基于高置信度得分识别所述自适应滤波器模型与所述2d切片上的一个或更多位置之间的匹配;(f)由所述处理器基于所述高置信度得分确定所述2d切片中的所述靶的位置;(g)由所述处理器基于所述偏移值估计所述靶的可能位置;并且从存储器取得后续的2dmri切片,并且重复(b)至(g),以便在对所述患者进行图像引导放射治疗期间对移动的所述靶进行追踪。
本公开的附加目的和优点将在下面的具体实施方式中进行部分地阐述,并且将部分地从本说明书中显而易见,或者可以通过本公开的实践来习得。本公开的目的和优点可以通过所附权利要求中特别指出的元件和组合的方式来实现和获得。
应当理解的是,以上的大体说明以及下面的详细说明仅仅是示例性和说明性的,而不是对所要求保护的本发明的限制。
附图说明
在不一定按比例绘制的附图中,相同的附图标记可以在不同的视图中描述相似的部件。具有字母后缀或不同字母后缀的相同附图标记可以表示相似部件的不同实例。附图大体上通过举例而不是限制的方式示出各种实施例,并且与说明书以及权利要求书一起用于对所公开的实施例进行说明。在适当的时候,在所有附图中使用相同的附图标记指代同一或相似的部分。这样的实施例是例证性的,而并非旨在作为本装置、系统或方法的穷尽性的或排他性的实施例。
图1示出了对用于放射治疗的三维靶进行定位和追踪的示例性放射治疗系统;
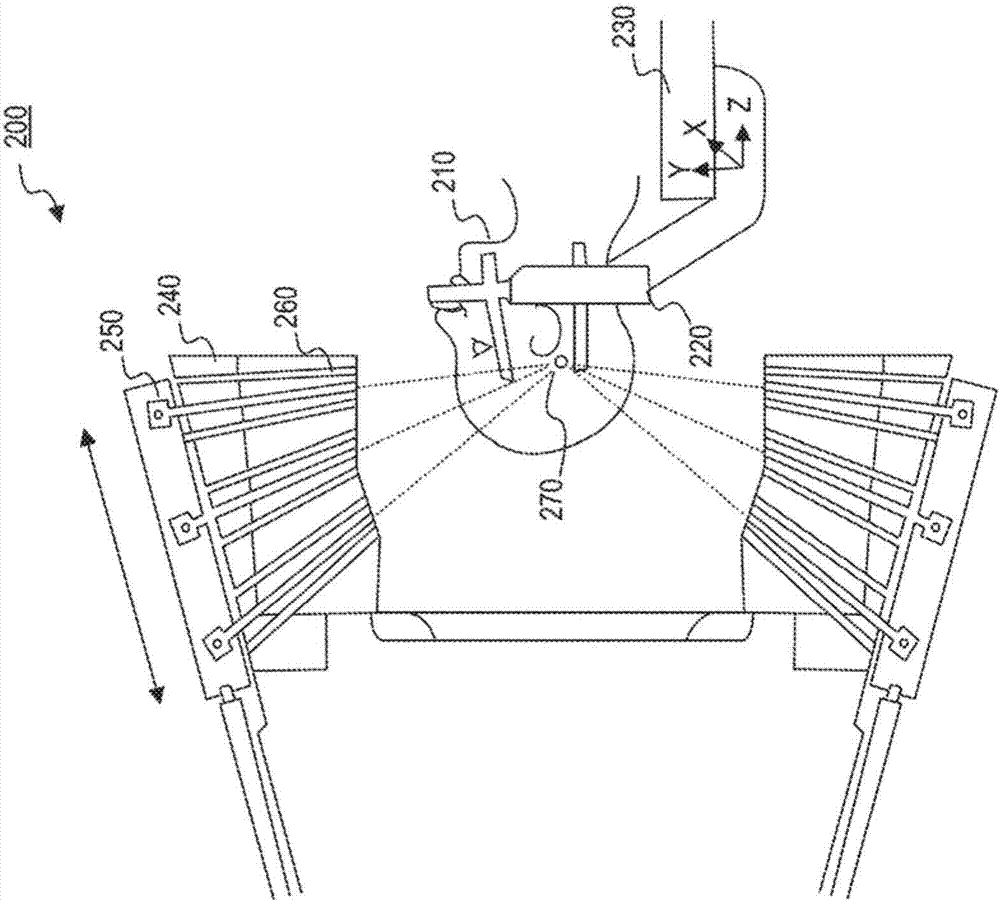
图2示出了图1的放射疗法系统中使用的放射治疗装置,伽玛刀;
图3示出了图1的放射疗法系统中使用的放射治疗装置,直线加速器;
图4示出了用于训练模块以生成自适应滤波器模型的示例性流程图;
图5示出了在患者的放射治疗期间使用一个或更多训练好的自适应滤波器模型来定位和追踪肿瘤的示例性流程图;
图6为自适应滤波器模型、响应图、以及追踪患者中的靶的图像的图示。
具体实施方式
在本公开中,介绍了用于对经受放射疗法治疗的患者的解剖结构中的肿瘤进行定位和追踪的放射治疗系统和相应的方法。具体地,在放射疗法治疗计划期间,捕获多个3d磁共振图像(mri)或4dmri图像。可以通过放射线治疗系统使用本领域中公知的分割技术来确定靶(例如患者的解剖结构中的肿瘤)的精确位置。肿瘤的位置被确定之后,系统可以生成多个图像块,并且可以确定从图像块的中心到肿瘤的偏移。放射治疗系统可以使用诸如相关性或使用外观模型技术的多种方法来增强多个图像块的选择特征,这导致了多个自适应滤波器模型。随后,在患者的实际“在线”治疗期间放射治疗系统可以使用这些自适应滤波器模型。
这种方法的一个优点是在放射疗法治疗期间可以对靶肿瘤进行定位和追踪。由于诸如呼吸、心脏运动、蠕动引起的运动、患者的不自主运动(例如,咳嗽、打喷嚏等)、或由放射治疗期间治疗台上的患者导致的自主运动的多种类型的运动,肿瘤通常在患者的解剖结构内移动。当使用mri引导的放射治疗时,只有患者的解剖结构的图像的2d切片是可用的。这种方法允许确定哪个(些)2d切片包括肿瘤,并且进一步有利地提供了通过估计可能的未来位置来追踪肿瘤的能力。
图1示出用于在放射疗法治疗期间执行靶定位和追踪的示例性放射治疗系统100。放射治疗系统100可以包括连接到网络120的放射治疗装置110,网络120连接到因特网130。网络120可以将放射治疗装置110与数据库140、医院数据库142、肿瘤信息系统(ois)150(例如,其可提供患者信息)、治疗计划系统(tps)160(例如,用于生成待由放射治疗装置110使用的放射疗法治疗计划)、图像采集装置170、显示装置180和用户接口190连接。
放射治疗装置110可以包括处理器112、存储装置116、以及通信接口114。存储装置116可以存储用于操作系统118、治疗计划软件120、生成自适应滤波器126的训练模块124、以及靶定位模块120的计算机可执行指令,以及待由处理器240执行的任何其他计算机可执行指令。
处理器112可以通信地联接到存储装置116,并且处理器112可以被配置为执行存储于其上的计算机可执行指令,例如,处理器112可以执行训练模块124以实现训练模块124的功能以及靶定位模块128的功能,以便在放射治疗的执行期间确定患者内的靶的位置。此外,处理器112可以执行治疗计划软件120(例如,诸如由elekta(医科达)公司制造的
处理器112可以是处理装置,包括例如微处理器、中央处理单元(cpu)、图形处理单元(gpu)、或加速处理单元(apu)等的一个或更多通用处理装置。更具体地,处理器112可以是复杂指令集计算(cisc)微处理器、精简指令集计算(risc)微处理器、超长指令字(vliw)微处理器、实现其它指令集的处理器、或实现指令集的组合的处理器。处理器112还可以是一个或更多专用处理装置,例如专用集成电路(asic)、现场可编程门阵列(fpga)、数字信号处理器(dsp)、片上系统(soc)等。如本领域技术人员将领会的,在一些实施例中,处理器112可以是专用处理器而不是通用处理器。处理器112可以包括一个或更多已知的处理装置,例如来自由inteltm制造的pentiumtm、coretm、xeontm、或
存储装置116可存储从图像采集装置179接收的图像数据122(例如,3dmri、4dmri、2d切片等)、或放射治疗装置110可以使用以执行与所公开的实施例一致的操作的任何格式的任何其它类型的数据/信息。存储装置210可包括只读存储器(rom)、闪存、随机存取存储器(ram)、诸如同步dram(sdram)或rambusdram的动态随机存取存储器(dram)、静态存储器(例如,闪存、静态随机存取存储器)等,在其上存储有任何格式的计算机可执行指令。该计算机程序指令可以由处理器112访问,从rom或任何其它合适的存储位置读取,并且加载到ram中以供处理器112执行。例如,存储器116可以存储一个或更多软件应用程序。例如,存储在存储器116中的软件应用程序可以包括用于常见计算机系统以及用于软件控制装置的操作系统118。此外,存储器116可以存储整个软件应用程序或由处理器112执行的仅一部分软件应用程序。例如,存储装置116可以存储一个或更多由治疗计划系统160生成的作为治疗计划软件120的放射疗法治疗计划。
在一些实施例中,存储装置116可以包括机器可读的存储介质。而在实施例中,机器可读存储介质可以是单一介质,但是术语“机器可读存储介质”应当被理解为包括存储一个或更多的计算机可执行指令或数据集的单一介质或多介质(例如,集中式或分布式数据库,和/或相关的缓存和服务器)。术语“机器可读存储介质”还应当被理解为包括能够对由机器执行并且使得机器执行本公开的方法中的任何一个或更多方法的指令集进行存储或编码的任何介质。因此,术语“机器可读存储介质”应当被理解为包括但不限于固态存储器、光介质和磁性介质。例如,存储器/存储装置210可以是一个或更多的易失性的、非暂时性的、或非易失性有形计算机可读介质。
放射治疗装置110可以经由通信地联接到处理器112和存储器116的通信接口114与网络130通信。例如,通信接口114可以包括网络适配器、电缆连接器、串行连接器、usb连接器、并行连接器、高速数据传输适配器(例如,如光线、usb3.0、雷电等)、无线网络适配器(例如,wifi适配器),电信适配器(例如,3g,4g/lte等)等。通信接口114可以包括一个或更多允许放射治疗装置110经由网络130与其他机器和装置(如远程部件)通信的数字和/或模拟通信装置。
网络130可以提供局域网(lan)、无线网络、云计算环境(例如,服务软件、服务平台、服务基础设施等)、客户端-服务器、广域网(wan)等的功能。因此,网络130可以允许放射治疗装置110与若干各种其它系统和装置之间的数据传输,若干各种其它系统和装置例如:治疗计划系统160、肿瘤信息系统150,和图像采集装置170。此外,由治疗计划系统160、ois150和图像采集装置170生成的数据可以被存储在存储器116、数据库140、或医院数据库142中。该数据可以根据需要通过通信接口114经由网络130被发送/接收,以便由处理器112进行访问。
另外,网络130可以连接到互联网132以与位于远程并连接到互联网的服务器或客户端进行通信。如所描述的,网络130可以包括其它系统s1(134)、s2(136)、s3(138)。系统s1、s2和/或s3可以与系统100相同,或者可以是不同的系统。在一些实施例中,连接到网络130的一个或更多系统可形成协作执行图像采集、靶定位和靶追踪、以及向患者提供放射治疗的其他方案的分布式计算/仿真环境。
另外,放射治疗系统100可以与数据库140或医院数据库142进行通信,以便执行一个或更多远程存储的程序。举例来说,数据库140、医院数据库142、或二者可以包括诸如oracletm数据库、sybasetm数据库、或其他的关系数据库,并且可以包括诸如hadoop序列文件、hbase、cassandra或其他的非关系数据库。例如,这样的远程程序可以包括肿瘤信息系统(ois)软件或治疗计划软件。例如,该ois软件可以被存储在医院数据库142、数据库140、或ois150中。例如,治疗计划软件可以被存储在数据库140、医院数据库142中、治疗计划系统160或ois150中。从而,例如,放射治疗装置110可以与医院数据库142进行通信以实现肿瘤信息系统150的功能
然而,公开的实施例的系统和方法并不限于分离的数据库。在一个方案中,放射治疗系统100可以包括数据库220或医院数据库230。可替代地,数据库220和/或医院数据库230可以位于距放射治疗系统100很远处。数据库140和医院数据库142可以包括计算部件(例如,数据库管理系统,数据库服务器等),计算部件配置为接收和处理对存储在数据库140或医院数据库142的存储装置中的数据的请求,并从数据库220或(一个或数个)医院数据库230提供数据。本领域技术人员将领会的是数据库140、142可以包括多个以集中式或分布式的方式定位的装置。
此外,放射治疗装置110可以通过网络130与数据库140进行通信以发送/接收存储在数据库140中的多个各种类型的数据。例如,在一些实施例中,数据库140可以被配置为存储来自图像采集装置140的多个图像(例如,3dmri、4dmri、2dmri切片图像、ct图像、2d荧光图像、x射线图像、来自mr扫描或ct扫描的原始数据、数字成像以及医学通信(dimcom)数据等)。数据库140可以存储靶定位模块128、训练模块124和治疗计划软件120所要使用的数据。如下所述,放射治疗装置110可以从数据库120接收图像数据(例如,3dmri图像、4dmri图像)以生成多个自适应滤波器模型。
进一步地,放射治疗系统100可以包括图像采集装置170,其可以采集患者的医学图像(例如,磁共振成像(mri)图像、3dmri、2d流mri、4d体积mri、计算机断层摄影(ct)图像、锥形束ct、正电子发射断层摄影(pet)图像、功能mri图像(例如,fmri、dce-mri和扩散mri)、x射线图像、荧光图像、超声图像、放射治疗射野图像、单光子发射计算机断层摄影(spect)图像等)。例如,图像采集装置170可以是mri成像装置、ct成像装置、pet成像装置、超声装置、荧光镜装置、spect成像装置、或用于获得患者的一个或更多医学图像的其他医学成像装置。通过图像采集装置170采集的图像可以作为成像数据和/或测试数据而被存储在数据库140内。作为示例,通过图像采集装置170采集的图像也可以由放射治疗装置110存储在存储器116中。
在一个实施例中,例如,图像采集装置140可以与放射治疗装置110集成为单个装置(例如,与直线加速器组合的mri装置也被称为“mri-linac”或作为与伽玛刀组合的集成的mri装置)。例如,可以使用这种mri-linac来确定患者中的靶器官或靶肿瘤的位置,从而根据对预定靶的放射疗法治疗计划来引导放射治疗。
图像采集装置170可以被配置为获取对关注区域(例如,靶器官,靶肿瘤或两者)的患者的解剖结构的一个或更多图像。每个2d切片可包括一个或更多参数(例如,2d切片厚度、取向和位置等等)。通过使用处理器112可以对该一个或更多参数进行调整以包含靶。例如,通过调整梯度或rf波形的特性可以操纵2d切片的选择的特征。例如,通过改变rf脉冲的基本频率并保持相同的梯度强度可以改变切片的位置。另外,例如,通过使用身体上不同的梯度轴(例如,所选择的切片可以是正交于施加的梯度)可以改变切片的取向。在一个实例中,图像采集装置170(例如,mri或mri-linac)可以获取任何取向上的2d切片。例如,2d切片的取向可以包括矢状取向、冠状取向或轴状取向。这些取向可以对应于与mri或mri-linac相关联的磁场梯度(例如,分别为gx、gy或gz)。处理器112可以调整诸如2d切片的厚度的参数以包含靶器官或靶肿瘤。在一个实施例中,例如可以通过使用等式1来计算和调节切片的厚度:
在等式1中,t可以表示2d切片厚度,如可以以距离的单位(例如,毫米)进行测定。δωs可以代表对应于以指定的频率(例如,赫兹、“hz”)施加的射频脉冲的激励带宽。字母γ可以代表称为旋磁比的常数(例如,对于质子,γ具有267.54mhz/特斯拉的值)。gslice可以表示磁场梯度(例如,以特斯拉/米测量)。在一个示例中,2d切片可从诸如3dmri体积的信息确定。例如,当使用放射治疗装置110时,在患者经受放射疗法治疗的同时,这种2d切片可以由图像采集装置170“实时”地采集。
治疗计划系统160可以生成并存储用于待治疗的特定患者的放射疗法治疗计划、对于其他患者的放射疗法治疗计划、以及其他放射治疗信息(例如,射束角度、剂量直方图体积信息、治疗过程中待使用的放射束的数量、射束角度、每束剂量等)。例如,治疗计划系统160可以提供关于要被施加到患者的特定的放射剂量的信息和其他放射治疗相关的信息(例如,诸如图像引导放射治疗(igrt)、调强放射疗法(imrt)、立体定向放射治疗等的治疗的类型)。
生成治疗计划可包括与图像采集装置170(例如,ct装置、mri装置、pet装置、x射线装置、超声装置等)进行通信,以便访问患者的图像并勾画诸如肿瘤的靶。在一些实施例中,可能需要对例如肿瘤周围或紧密接近肿瘤的健康组织的一种或更多危及器官进行勾画。因此,当oar靠近靶肿瘤时可以执行oar的分割。另外,如果靶肿瘤靠近oar(例如,前列腺靠近接近膀胱和直肠),oar的分割,治疗计划系统160可不仅允许研究靶中的剂量分布,还允许研究oar中的剂量分布。
为了相对于oar勾画出靶器官或靶肿瘤,可以通过图像采集装置170非侵入性地获得经受放射治疗的患者的诸如mri图像、ct图像、pet图像、fmri图像、x射线图像、超声图像、放射治疗射野图像、spect图像等医学图像,以揭露身体部分的内部结构。基于来自医学图像中的信息,可以获取3d结构。此外,在治疗计划过程中,可以考虑许多参数以实现对靶肿瘤的有效治疗(例如,使得靶肿瘤接收对于有效治疗足够的放射剂量)与对(一个或数个)oar的低照射(例如,(一个或数个)oar接收尽可能低的放射剂量)之间的平衡,靶器官和靶肿瘤的位置,oar的位置,以及与oar有关的靶的移动。例如,通过在mri或ct图像的每个2d层或切片内绘制靶或绘制oar的轮廓并对每个2d层或切片的轮廓进行组合可以获得3d结构。轮廓可以手动地生成(例如,由医师、剂量师、或医护人员)或自动地生成(例如,使用诸如由瑞典斯德哥尔摩医科达公司制造的基于图谱的自动分割软件,
在靶肿瘤和(一个或数个)oar已被定位并勾画之后,剂量师、医生或医护人员可以确定要被施加到靶肿瘤和邻近肿瘤的任何oar(例如,左和右腮腺、视神经、眼睛、晶状体、内耳、脊髓、脑干等)的放射剂量。在确定用于每个解剖结构(例如,靶肿瘤、oar)的放射剂量之后,可以执行称为逆向计划的过程以确定一个或更多治疗计划的参数,诸如体积勾画(例如,限定靶体积、绘制敏感结构轮廓)、靶肿瘤和oar周围的边距、剂量约束(例如,对肿瘤靶全剂量和对任何oar零剂量;对ptv95%的剂量,而脊髓≤45gy、脑干≤55gy、以及视神经结构<54gy分别接收所述的剂量)、射束角选择、准直器设置、以及射束开启时间。逆向计划的结果可以构成可以被存储在治疗计划系统160或数据库140中的放射疗法治疗计划。这些处理参数中的一些可以是相关的。例如,在改变治疗计划的尝试中调谐一个参数(例如,用于不同的目的的权重,如对靶肿瘤增大剂量)可能影响至少一个其它参数,这进而可能导致制定不同的治疗方案。从而,治疗计划系统160可以生成具有这些参数的定制的放射疗法治疗计划,以便使放射治疗装置110向患者提供放射治疗。
此外,该放射治疗系统100包括显示装置180和用户接口190。显示装置180可以将包括医学图像、接口信息、治疗计划参数(例如,轮廓、剂量、射束角度等)、治疗计划、靶,定位靶和/或追踪靶、或者任何相关的信息显示给用户的一个或更多显示屏幕。用户接口190可以是键盘、小型键盘、触摸屏或用户可以将信息输入到放射治疗系统100的任何类型的装置。
为了使放射治疗装置110对关注的解剖区域中的靶肿瘤进行定位和追踪,例如,处理器112可以执行靶定位模块128。如本公开中稍后描述的,靶获取模块120可利用由训练模块124生成的自适应滤波器模型126。此外,自适应滤波器模型可以包括特定的域信息(例如,空间域或频域),位置信息(例如,体积中的3d位置、3d偏移信息、或2d位移信息)。如下所述,靶定位模块128使用至少一个由训练模块124生成的自适应滤波器模型126。
此外,在一个实施例中,放射治疗系统100的任何和所有部件可以被实现为虚拟机(例如,vmware,hyper-v等)。例如,虚拟机可以是用作硬件的软件。因此,虚拟机可以包括共同起到硬件作用的至少一个或更多虚拟处理器、一个或更多虚拟存储器、以及一个或更多虚拟通信接口。例如,ois150、tps160、图像采集装置170可以被实现为虚拟机。考虑到可用的处理能力、存储器以及计算能力时,整个放射治疗系统可以被实现为虚拟机。
图2示出放射疗法治疗装置200的一种类型的示例,例如,由瑞典斯德哥尔摩医科达公司制造的leksell伽玛刀。伽玛刀可以被配置为利用靶定位模块128(在图l中示出),其可以远程访问mri图像(例如,从图像采集装置170)以定位脑中的靶肿瘤。在实施例中,作为图像采集装置170的mri装置可以与伽玛刀集成。如图2所示,放射疗法分次治疗期间,患者210可以戴有坐标架220,以使经受手术或放射疗法的患者的身体部分(例如,头部)保持稳定。坐标架220和患者定位系统230可以建立一个空间坐标系统,其可以在对患者进行成像时或在放射手术期间使用。放射治疗装置200可以包括保护壳体240以包围多个放射源250。放射源250可以通过射束通道260生成多个放射束(例如,子束)。多个放射束可以被配置为从不同的方向聚集于等中心270。虽然每个单独的放射束可以具有相对低的强度,但当来自不同放射束的多个剂量积聚在等中心270时,等中心270可以接收相对高水平的放射。在某些实施例中,等中心270可以对应于手术或治疗中的靶,例如肿瘤。
图3示出放射治疗装置300的类型的另一个示例(例如,直线加速器,被称为linac,由瑞典斯德哥尔摩医科达公司制造)。使用直线加速器300,患者302可以定位在患者台304上以接收由治疗计划系统160(图1中所示)生成的放射疗法治疗计划所确定的放射剂量。放射疗法治疗计划可被用于定位和追踪体积中的3d靶,例如位于患者302的解剖结构内的靶器官或靶肿瘤。
直线加速器300可以包括连接到围绕患者302旋转的台架308的放射头306。放射头306生成指向靶器官或靶肿瘤的放射束310。当台架308旋转时,放射头306可以围绕患者302旋转。在旋转的同时,放射头306可以根据由治疗计划系统160(图1中所示)生成的治疗计划取决于肿瘤的角度、形状和尺寸给患者302提供多种不同剂量的放射。由于器官和肿瘤在患者的身体内移动,靶的快速和准确的3d定位是重要的。例如,靶器官或肿瘤可能由于各种类型的运动(例如,呼吸,心脏,蠕动或其它类型的患者运动)而移动。因此,直线加速器300可以被配置为通过使用靶定位模块128在放射疗法治疗期间定位靶(例如,器官或肿瘤)并追踪靶。
此外,患者台304的下面,可以设置平板闪烁体检测器312,其可以围绕定位在患者32身体的靶器官或靶肿瘤上的等中心314与放射头306同步旋转。平板闪烁器可以获取具有最高可达信噪比的图像,并且可以用于验证在任何特定的放射疗法治疗分次(例如,放射疗法治疗可能需要多个分次的放射治疗,其中每个分次通常被称为“分份”)期间由患者302接收的放射量。此外,这样的图像被用于确定相对于放射头306的患者放置的几何精度。
轴线316与放射头306生成的射束310的中心的交点通常被称为“等中心”。患者台304可以被机动化,使得患者302可以被定位为使得肿瘤部位位于或接近等中心314。例如,患者台304可以相对于直线加速器300的一个或更多其他部件而改变位置,如相对于位于该放射头306中的治疗放射源升高、改变患者302的纵向位置、或横向位置。
在一个实施例中,直线加速器300可以与图像采集装置170(图1所示)诸如磁共振成像装置集成为单个装置(例如,mri-linac)。在这样的情况下,当由于放射疗法治疗期间患者台304插入通过的孔大小的有限尺寸导致患者台304被配置为不移动时,mri-linac可以包括“虚拟诊查台”,其可以关于所述放射源“虚拟地”调整患者302的对准。在这样的实施例中,mri-linac可以用于使用靶定位模块128确定靶的定位并且在患者302中追踪靶,以便将放射治疗引导到预定的靶。
图4示出了用于让训练模块124生成自适应滤波器模型126的过程400。靶定位模块128可以利用自适应滤波器模型126(图1中所示)来确定靶的定位,然后对靶进行追踪。
在402,训练模块124(示于图1)从图像采集装置170接收特定患者的关注区域的多个图像(例如,3dmri、4dmri等)。例如,该多个图像可以是包含靶(例如,靶器官、靶肿瘤等)的关注区域的3dmri图像或4dmri图像。
在404,训练模块110利用处理器112继续进行从该多个mri图像中提取包含关注区域中的靶(例如,靶器官、靶肿瘤等)的多个切片(例如,2d切片)。在开始放射疗法治疗之前,可以预先确定(例如,从基于所述3dmri体积或4dmri体积的信息来确定)2d切片的例如厚度。该信息可以包括2d切片应当是在频域还是空间域。可替换地,当正在用放射疗法(例如,实时地)对患者402进行治疗时,训练模块110可以接收2d切片信息。例如,可以使用mri-linac用放射疗法治疗患者402。在该放射治疗的过程期间,mri-linac可以在治疗过程中取得多个3dmri图像或4dmri图像。提取的切片代表包围靶的患者的解剖结构的2d切片。此外,所提取的2d切片可以平行或正交于靶的运动。
在406,处理器112为每个提取的2d切片确定一个或更多2d图像块。在一个示例中,2d图像块可对应于能够包含靶的2d切片图像的区域。2d图像块可以被构造为任何形状(例如,正方形、矩形、圆形、多边形形状等),并且可以在尺寸上不同(例如,32×32像素的图像块、64×64像素的图像块等)。为了说明,一个正方形图像块例如可以是对应于512×512像素的2d切片中的靶的32×32像素。在一个示例中,2d图像块可以包括关于靶的信息以及对应于不包括靶的区域的信息(例如,背景信息)。
在408,处理器112确定偏移值。例如,该偏移值是从2d图像块的中心到待追踪的靶的中心的距离。2d图像块可以包括域信息(例如,关于2d图像块的空间域或频域的信息)。此外,偏移信息可以包括例如从基准点(例如,对应于体积中的靶的基准点)起2d图像块的位移的信息、以及关于靶的形状变化(例如,变形)的信息。在一个示例中,基准点可以包含靶的计算中心(例如,肿瘤的质心)。对每个包含靶的2d图像块均确定偏移值。因此,每个2d图像块具有其自身关联的偏移值。多个偏移值及它们的关联图像块被存储在存储器116中。
例如假设2d图像块的中心的坐标为(例如,[xp,yp,zp])并且靶肿瘤的中心的坐标为(例如,[xt,yt,zt]),则与靶肿瘤的3d位置相关的2d图像块中心的偏移可以是向量(例如,[ox,oy,oz]=[xt-xp,yt-yp,zt-zp])。因此,处理器112可以追踪靶肿瘤。在追踪期间,处理器112可为新患者摆位而定位2d图像块的中心(例如,“在线/实时”诸如为[xpnew,ypnew,zpnew])。然后,处理器112可确定肿瘤的位置(例如,[xtnew,ytnew,ztnew]=[xpnew+ox,ypnew+oy,zpnew+oz])。
在410,处理器112可以使用一个或更多类型的自适应滤波器的设计技术将每个图像块转换到自适应滤波器模型126中。例如,可使用以下类型的自适应滤波器设计:匹配滤波器、最大间隔相关滤波器、综合判别函数过滤器、最小均方滤波器等。此外,自适应滤波器模型126可以包括域信息和从对应于体积中的靶的2d图像块确定的偏移信息。
一般地,例如,自适应滤波器模型126“建模”待定位的对象(例如,肿瘤)。可以生成多个自适应滤波器模型126。例如,可以有用于肿瘤的顶部的自适应滤波器模型126、用于肿瘤的中部的自适应滤波器模型126以及用于肿瘤的底部的自适应滤波器模型126。此外,可以为人体解剖结构的不同部分(例如,一个或更多关注的靶器官,诸如前列腺、乳腺、肺、心脏,脑等)创建自适应滤波器模型126。此外,可以为每个关注的靶生成自适应滤波器模型126(例如,在特定器官中的一个或更多肿瘤,例如在肺中的多发性肿瘤;或在癌症已经转移且一个或更多器官中存在一个或更多肿瘤的情况等)。
此外,自适应滤波器模型126既可以在空间域中也可以在频域中设计。在一个示例中,在频域中将自适应滤波器模型126应用到2d切片中可以使计算效率更高。自适应滤波器模型126可以存储在存储器116中(在图1中示出),并由处理器112调取以被应用到随后采集的2d切片(例如,“实时”/“在线”地采集的2d切片)来在患者的放射疗法治疗期间预测靶的位置。
图5示出了在患者的“实时”/“在线”放射疗法治疗期间使用一个或更多自适应滤波器模型126对靶进行追踪的工作流过程500的示例性流程图。
在502,过程500开始,放射治疗装置10(在图1中示出)使用处理器116访问靶定位模块128,该靶定位模块128调取针对包含特定患者的靶肿瘤的关注区域(例如,前列腺、乳腺、肺等)所设计的多个自适应滤波器模型126。
在504,处理器116接收采集方案以提供给图像采集装置170,以生成一组初始的2d切片。例如,该方案可以包括要取得的切片的位置(例如,肺、前列腺、脑、肾等)、切片的取向(例如,基于预定的可能的器官运动–诸如平行于或正交于要取得的切片)、以及切片厚度(例如,5mm切片、10mm切片、15mm切片等)。用户可以提供对靶的位置的初始估计,该初始估计可以通过用户接口190来提供。处理器116可以利用该初始估计作为何处开始取得2d切片的初始位置。可替换地,可以自动地由处理器116确定这样的位置信息。
在506,放射治疗装置根据来自图像采集装置170(例如,mri装置或mri-linac装置)的方案进一步接收多个2dmri切片。该2d图像可以对应于具有肿瘤的关注区域。该2d切片可以平行于或正交于肿瘤。2d切片可以围绕肿瘤。另外,2d切片可以是肿瘤周围的区域。典型地,mri装置提供频域中的2d切片。
如下所述,在508至514,处理器116确定肿瘤在2d切片上的位置及其在3d体积中的位置。
在508,处理器116可以将2d切片转换到频域或空间域。该2d切片被转换以匹配自适应滤波器模型126的域。例如,如果自适应滤波器模型126在空间域中被创建,则该2d切片,例如,处理器116可以将该2d切片转换到空间域。可选地,如果自适应滤波器模型126在频域中被创建,处理器116可以将该2d切片转换到频域。
在510,处理器116可以应用自适应滤波器模型126。如上文所讨论,自适应滤波器模型126是由多个2d图像块生成的已经由训练模块126训练过的多个模型。处理器112将多个自适应滤波器模型126应用于2d切片。例如,2d切片和自适应滤波器模型可以具有相同的取向(例如,正交于运动的方向、平行于运动方向或两者)。在一个示例中,在频域中将自适应滤波器模型126应用于2d切片计算效率可以更高。如下是自适应滤波器模型126可以如何应用于2d切片的一个示例:
在空间域中,自适应滤波器模型126可以由2d模板t(x,y)表示,并且2d切片(例如,2d图像)可由i(x,y)表示。将自适应滤波器模型126应用到2d切片的特定位置可提供与相关性有关的“置信度得分”。例如,该置信度得分提供该特定的自适应滤波器模型与2d切片的特定位置匹配得有多好的指示。
在一个示例中,自适应滤波器模型126相对于2d切片的特定位置具有越好的匹配,则置信度得分越高。置信度得分可以被用来预测靶肿瘤是否位于2d切片内以及位于何处。根据情况,可利用许多不同类型的相关性来确定置信度得分。例如,可以使用以下类型的相关性:互相关、归一化互相关、或相关系数,它们可以被定义如下:
互相关:r(x,y=∑i,j∈pt(i,j)·i(x-i,y-j);
归一化互相关:
或
相关系数:
在上述等式中:p表示模板的空间域;
也可以通过应用卷积定理在频域中进行这三个相关计算,例如:r=
在512,作为将自适应滤波器模型126应用到2d切片的结果,处理器112可确定响应图。对于单个2d切片可以创建多个响应图,因为每个响应图可以对应于一特定自适应滤波器模型。自适应滤波器模型126和2d切片二者可以具有相同的取向。该响应图可以在空间域或频域中生成。2d切片和自适应滤波器模型126二者必须都处于空间域中以生成在空间域中的响应图。类似地,2d切片和自适应滤波器模型126二者必须都处于频域中以生成频域中的响应图。可以为每个2d切片来创建响应图。所生成的响应图可以是指示一特定的自适应滤波器模型126与一给定的2d切片内的不同位置的匹配程度的图像。
例如,自适应滤波器模型a(未示出)可以由处理器112应用到2d切片的每个位置上。对于每个位置,例如,处理器112可以确定指示例如该自适应滤波器a与该2d切片的特定位置匹配得有多好的置信度得分。自适应滤波器模型a相对于2d切片上的特定位置匹配得越好,则对于该特定位置的置信度得分越高(例如,越接近+1)。响应图图像上更亮的区域可以指示更好的匹配,并且因此,与较暗区域比具有更高的置信度得分(例如,在自适应滤波器模型a与2d切片的特定位置之间)。在响应图中,较亮的区域可以具有与较暗的区域相比更高的置信度得分。之后,自适应滤波器模型a被应用到2d切片,可以生成响应图a。处理器112可以调取另一个自适应滤波器模型b(未示出),例如,并重复将自适应滤波器模型b应用到2d切片上的每一个位置以生成响应图b的过程。从而,使用靶定位模块的处理器可以将多个自适应滤波器模型应用于2d切片以生成多个响应图,响应图可以被存储在存储器116中。在2d切片的每个位置处,生成对应于所使用的自适应滤波器模型的置信度得分。高置信度得分可以对应于2d切片上靶肿瘤可能处于的位置。
在514,处理器112可以基于置信度得分预测2d切片上靶肿瘤的位置。例如,对于响应图上的一特定位置,可以有多个置信度得分值,其中每个置信度得分可以对应于一特定自适应滤波器模型。为了预测肿瘤的位置,处理器112可以选择对于2d切片上一特定位置的最大置信度得分值。可替换地,处理器112可以使用对于2d切片上一特定位置的所有置信度得分的加权平均值。在一个示例中,处理器112可以计算前n个置信度得分的加权平均值,其中n是预定数。利用通过使用多个自适应滤波器模型生成的置信度得分可以提高预测的准确度。因此,对于特定位置的高置信度得分可以指示2d切片上靶的位置,而低置信度得分可以指示肿瘤不在该位置。最接近+1的置信度得分可以指示一部分肿瘤或整个肿瘤位于该2d切片上。
如果处理器112确定该2d切片不包含肿瘤,过程500追随501返回到506以获得另一2d切片。过程500可以使处理器112调整采集方案以采集下一2d切片。可替代地,取决于切片厚度、肿瘤的尺寸、肿瘤的取向和其他因素,肿瘤可能被包含在一个或更多2d切片内。例如,如果肿瘤的底部被包含在当前2d切片中,处理器112可以使用偏移信息来确定随后应获取什么样的2d切片(例如,包含肿瘤的质心的2d切片、或者可以是包含肿瘤的顶部的2d切片)。
例如,使用来自一特定自适应滤波器模型及其相应的响应图的信息,处理器112可以确定先前2d切片上的肿瘤的位置。另外,使用与该自适应滤波器模型相关联的偏移信息,处理器112还可以估计3d体积中肿瘤的位置(例如,中心)。例如,处理器112可确定该肿瘤在例如第(5,10)像素位置与该2d切片相交,并且肿瘤的中心可能沿切片法线方向距2d切片的中心5mm。为了估计肿瘤的下一个位置(例如,随着肿瘤运动而对其进行追踪)或者为了获取关于肿瘤的形状的更完整的信息(例如,肿瘤的形状是否已经改变),处理器112可以调整各种参数(例如,接下来将获取2d切片的位置、获取平行于先前的切片但处于不同位置的接下来的2d切片、获得正交于先前的切片的2d切片、调整接下来的切片的厚度,等)。另外,使用来自先前的自适应滤波器模型的偏移信息,处理器112还可以估计肿瘤的下一位置。从而,当患者经受放射治疗时,处理器112可以实时地肿瘤的运动进行追踪。
在516,当患者“实时”经受放射疗法治疗时,处理器112可以对肿瘤进行追踪。此外,当利用多个2d切片时,处理器112可以估计肿瘤的形状。
图6图示地示出应用于2dmri切片以确定靶(例如,肝脏)的位置的示例性自适应滤波器模型。在602,用图表示在空间域中的自适应滤波器模型的一个示例。处理器112(示于图1)可以使用靶定位模块129以将602中示出的自适应滤波器模型应用于也处于空间域的特定的2d切片。通过将示例性自适应滤波器模型602应用于2d切片,处理器112可以确定对于2d切片的每个位置,示例性自适应滤波器模型602与2d切片的特定位置匹配得有多好。有利地,处理器112可以在约300毫秒内计算每个2d切片。靶定位模块129生成示例性响应图,其在604中图示地示出。示例性响应图604可以表示自适应滤波器模型602与2d切片的每个位置匹配得有多好。在示例性响应图604中示出的较亮的区域指示更好的匹配,并因此与较暗的区域相比在自适应滤波器模型602与2d切片的特定位置之间有更高的置信度得分。在响应图604中,较亮的区域可以具有比较暗的区域更高的置信度得分。如图所示,响应图604表示如处理器112所确定的可以对应于该2d切片的最高置信度得分的亮区域608。因此,响应图604上的亮区域608可以对应于这一特定2d切片上的靶的位置,因此,处理器112已经确定位于该特定的2d切片上的靶608的位置。此外,由于通过图像采集装置170对其生成2d切片的患者的解剖结构的位置,处理器112可以确定如在606中示出的患者的解剖结构上靶608的位置。例如,606中的红色区域对应于覆盖患者的解剖结构的自适应滤波器模型602。例如,在另一个实施方案中,靶可以表示肿瘤。
可替代地,例如,取决于2d切片和自适应滤波器模型是否处于频域中,可以在频域中表示响应图。为了在频域中生成响应图,处理器112可对2d切片进行快速傅立叶变换(fft)。处理器112通过在频域中执行逐点相乘而应用自适应滤波器模型。为了生成响应图,处理器112可以进行快速傅立叶逆变换。
其他注意事项
本文件中提及的所有出版物、专利和专利文献通过引用它们而整体并入本文,如同通过引用单独并入。如果本文件与通过引用并入的那些文件之间的用法不一致,则并入的参考文献中的用法应被视为对本文件的补充;对于不可调和的不一致,则以本文件中的用法为准。
示例性公开的实施例描述了当患者经受放射疗法治疗时用于对患者的解剖结构中的靶(例如,肿瘤)进行追踪的系统和方法。前面的描述已经出于说明的目的而示出。这并非穷尽的且不限于所公开的准确的形式或实施例。考虑到说明书及所公开的实施例的实践,变形例和适应例的修改将是显而易见的。
在本文件中,使用了术语“一个(a)”或“一个(an)”,如专利文件中常用的,其包括一个或多于一个,独立于“至少一个”或“一个或更多”的任何其它实例或用途。在本文件中,术语“或”用于指非排他性的或,除非另外指明,否则“a或b”包括“有a没有b”、“有b没有a”、以及“a和b”。在本文件中,术语“包括”和“其中(inwhich)”用作各个术语“包括”和“其中(wherein)”的通俗易懂的等效。此外,在下列权利要求中,术语“包括(including)”和“包括(comprising)”是开放式的,即,包括除了在权利要求中的这样的术语之后列出的那些元件之外的元件的设备、系统、装置、制品、构成、构想或过程仍被视为落入该权利要求的范围。此外,在下面的权利要求中,术语“第一”、“第二”和“第三”等仅用作标记,并不意图对其对象施加数值要求。
本文描述的方法示例至少部分地可以是机器或计算机实现的。一些示例可以包括编码有指令的计算机可读介质或机器可读介质,该指令可经操作以配置电子装置来执行如上述示例中所描述的方法。这些方法的实现可以包括例如微代码、汇编语言代码、更高级语言代码等的软件代码。可以使用各种软件编程技术来创建各种程序或程序模块。例如,可以用或通过java、python、c、c++、汇编语言、或任何已知的编程语言来设计程序段或程序模块。一个或更多这样的软件段或模块可以被集成到计算机系统和/或计算机可读介质中。这样的软件代码可以包括用于执行各种方法的计算机可读指令。该软件代码可以形成计算机程序产品的部分或计算机程序模块。此外,在一个示例中,例如在执行期间或在其它时间,代码可以有形地存储在一个或更多易失性、非暂时性或非易失性有形计算机可读介质上。这些有形的计算机可读介质的示例可以包括但不限于硬盘、可移动磁盘、可移动光盘(例如,压缩盘和数字视频盘)、磁带、存储卡或存储棒、随机存取存储器(ram)、只读存储器(rom)等。
此外,尽管已经在本文中描述了示例性实施例,其范围包括任何和所有基于本公开的具有等同元件、修改、省略、组合(例如,各种实施例的方案的组合)、改编或改变的实施例。权利要求书中的元件将被基于权利要求中采用的语言宽泛地解释,并不限于在本说明书中或本申请的进行期间所描述的示例,其示例将被解释为非排他性的。此外,可以以任何方式对所公开的方法的步骤进行修改,包括通过对步骤重新排序或插入或删除步骤。因此,本说明书和示例旨在仅被认为是示例,真正的范围和精神由以下权利要求以及其等同物的全部范围所指示。
以上描述旨在是说明性的而不是限制性的。例如,上述示例(或其一个或更多方案)可以彼此组合使用。例如本领域普通技术人员在阅读上述描述时可以使用其它实施例。提供符合37c.f.r.§1.72(b)的摘要以允许读者快速确定技术公开的本质。其以这样的理解而提交:它不会用于解释或限制权利要求的范围或含义。另外,在上述具体实施方式中,各种特征可以被分组在一起以简单化本公开。这不应解释为一种使不要求保护的公开的特征对于任一权利要求是必要的意图。相反,本发明的主题可以少于公开的特定实施例的全部特征。从而,以下权利要求书作为示例或实施例并入具体实施方式中,其中每个权利要求独立地作为单独的实施例,并且考虑这些实施例可以以各种组合或排列彼此组合。本发明的范围应参照所附权利要求以及这些权利要求赋权的等同形式的全部范围来确定。
- 还没有人留言评论。精彩留言会获得点赞!