BMP‑2/PLLA/nHA缓释微球及其制备方法与流程
本发明涉及骨修复材料的制备技术领域,尤其涉及一种BMP-2/PLLA/nHA缓释微球及其制备方法。
背景技术:
膝关节前交叉韧带(anterior cruciate ligament,ACL)是膝关节重要的静力和动力性稳定结构之一,可以防止胫骨前移、过伸和过度旋转,防止膝关节失稳后的相关并发症。ACL损伤是常见病、多发病,主要困扰广大青少年,是青少年人群中最常见的疾病之一。ACL损伤后出现膝关节不稳,增加关节其他结构损伤机率、加速半月板及关节软骨的退变,导致严重的慢性疼痛和关节功能障碍,严重影响患者的日常活动和生活质量,给青少年患者带来了巨大的痛苦和精神负担。ACL重建术是利用移植肌腱固定于骨道内,替代正常前交叉韧带的功能,是治疗ACL损伤最有效的方法。移植肌腱与骨隧道内壁的愈合是腱骨界面间纤维组织形成连接、新骨形成、骨向肌腱内长入、局部塑形改造的的过程。BMP-2是目前发现的唯一一种可以作为诱导骨形成的充分条件的蛋白因子,即在只有单独BMP-2存在的况下即可诱导软骨和骨组织的形成,并且在成骨的各个阶段都起着重要作用。另外,BMP-2能明显诱导从骨髓中分离得到的多潜能干细胞向软骨细胞、骨细胞分化,合成骨钙素等蛋白质,发生软骨内成骨,骨细胞形成,骨盐沉积形成新骨。但单纯的BMP-2在体内扩散太快,也易被蛋白酸分解,易发生流失、降解和吸收,因而不能在有效时间内作用于更多的靶细胞,因此基础和临床研究中主要用于与其它载体材料复合应用于组织的修复。微球(microsphere)是指药物溶解或者分散在高分子材料的基质中形成的微小球状实体,属于基质型骨架微粒。因其对特定器官和组织的靶向性及微粒中药物释放的缓释性,已经成为近年来缓控释剂型研究的热点。但现有的BMP-2缓释微球系统中,多数采用人工合成的亲脂性高分子多聚物材料作为BMP-2的缓释载体,其生物相容性差,细胞吸附力较弱、机械强度不足等缺点,从而导致现有的BMP-2缓释微球系统吸收率低,药物释放不平稳,最终导致高分子材料/BMP-2缓释系统在骨愈合过程中影响骨修复。
技术实现要素:
本发明要解决的技术问题是克服现有技术的不足,提供一种生物相容性好、吸收性好、力学强度高、可降解性好、稳定性好的BMP-2/PLLA/nHA缓释微球及其制备方法。
为解决上述技术问题,本发明采用以下技术方案:
一种BMP-2/PLLA/nHA缓释微球的制备方法,包括以下步骤:
(1)将BMP-2溶于聚乙烯醇水溶液中,并加入纳米羟基磷灰石,形成BMP-2/nHA的聚乙烯醇水溶液;
(2)将聚乙烯左旋丙交酯溶于二氯甲烷中,并加入油相乳化剂,得到PLLA-二氯甲烷乳液;
(3)将步骤(1)所得的BMP-2/nHA的聚乙烯醇水溶液和步骤(2)所得的PLLA-二氯甲烷乳液混合,超声乳化,得初乳液;再加入聚乙烯醇水溶液,磁力搅拌,得到复乳液;
(4)将步骤(3)所得的复乳液进行磁力搅拌,使有机溶剂蒸发,得到含水微球,将所得含水微球进行抽滤,得到BMP-2/PLLA/nHA缓释微球。
上述的BMP-2/PLLA/nHA缓释微球的制备方法,优选的,所述BMP-2、纳米羟基磷灰石与聚乙烯左旋丙交酯的质量比为=10~20∶10~20∶150~250。
上述的BMP-2/PLLA/nHA缓释微球的制备方法,优选的,所述步骤(2)中,所述油相乳化剂为油相乳化剂SPAN-80。
上述的BMP-2/PLLA/nHA缓释微球的制备方法,优选的,所述步骤(3)中,磁力搅拌的转速为750r/min~850r/min,时间为5min~10min。
上述的BMP-2/PLLA/nHA缓释微球的制备方法,优选的,所述步骤(4)中,磁力搅拌的转速为350r/min~450r/min,时间为3.5h~4h。
上述的BMP-2/PLLA/nHA缓释微球的制备方法,优选的,所述步骤(4)中,所述抽滤采用的滤膜为孔径为0.4μm~0.5μm的微孔滤膜。
作为一个总的发明构思,本发明还提供一种BMP-2/PLLA/nHA缓释微球,采用上述的方法制备。
与现有技术相比,本发明的优点在于:
1、本发明将BMP-2通过吸收法与纳米羟基磷灰石(nano-Hydroxyapatite,简称nHA)载体结合并使用复乳法复合聚乙烯左旋丙交酯(Poly-L-lactide,PLLA)制备成缓释微球,PLLA是植物来源,完全无毒害作用,逐渐降解的过程中缓慢释放BMP-2/羟基磷灰石微粒,并最终分解为水和二氧化碳;具有良好的可降解性、吸收性、力学强度以及生物安全性,PLLA与纳米羟基磷灰石复合的微球缓释系统,可大幅度提高药物及蛋白质的包封效果,延长药物的释放时间,可以通过控制成份含量来调节材料的降解速度,稳定性好。将nHA与PLLA进行复合,一方面能使大幅提高缓释微球的包封效果、延长药物的缓释时间,尽量减少爆发性释放和蛋白质的不稳定,极大限度的提高微球蛋白质的利用率,避免大量蛋白质突释产生的局部酸性浓度过高的现象,从而避免影响骨组织的生成。一方面能使聚乳酸的酸性降解产物可被HA缓冲,同时HA的骨传导性可提供良好的骨细胞粘附生长环境,复合物的多孔结构则为细胞生长、组织再生及粘附提供条件,符合骨组织工程的生物学要求。在缓慢降解的过程中缓释BMP-2/纳米羟基磷灰石微球,在腱骨界面维持一定的BMP-2浓度,缓释的BMP-2可以促进腱骨交界处间充质干细胞分化,并且可以促进新生的软骨组织向骨组织结构重塑,最终形成自然组织,从而重现原有腱骨界面生物学功能。通过特殊工艺可将缓释微球相互结合制成膨胀螺栓,所制备的BMP-2缓释可吸收膨胀螺栓在关节镜的辅助下就可以进行临床操作,方便简洁。
附图说明
图1为本发明实施例1制备的BMP-2/PLLA/nHA缓释微球的SEM图(放大1000倍)。
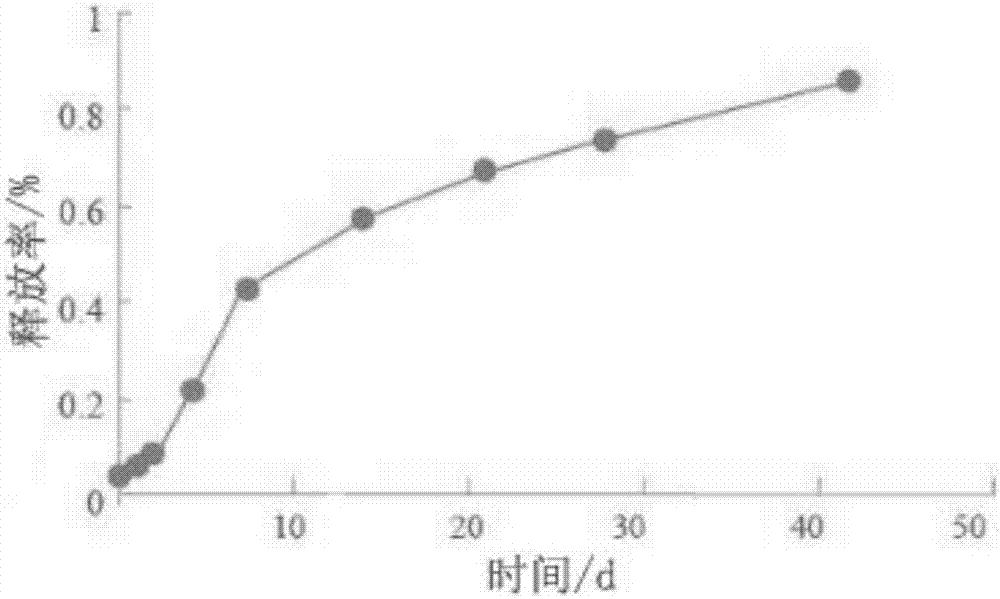
图2为本发明实施例1制备的BMP-2/PLLA/nHA缓释微球的体外药物释放曲线。
具体实施方式
以下结合说明书附图和具体优选的实施例对本发明作进一步描述,以下实施例描述了本发明的特殊实施例子,以便对本发明作进一步的说明,这些实施例只是说明而不表示本发明所有的可能性,本发明并不仅仅局限于这些实施例中的材料、反应条件或参数。任何在相关领域具备经验的人,都可以按照本专利的原理利用其他的材料或反应条件实现本发明所描述的生物素-亲和素标记技术结合免疫层析技术制备疾病标志物检测卡。这些并不脱离本发明描述的基本概念,因此这些修改的或者不同的应该都在本发明覆盖的范围内。
实施例1:
(1)将15mg的BMP-2溶于聚乙烯醇(PVA)水溶液中,并加入15mg纳米羟基磷灰石,形成BMP-2/nHA的聚乙烯醇水溶液;
(2)将200mg聚乙烯左旋丙交酯溶于二氯甲烷中,并加入油相乳化剂SPAN-80,得到PLLA-二氯甲烷乳液;
(3)将步骤(1)所得的BMP-2/nHA的聚乙烯醇水溶液和步骤(2)所得的PLLA-二氯甲烷乳液混合,超声乳化,得初乳液;再加入聚乙烯醇水溶液,磁力搅拌,转速为800r/min,时间为10min,得到复乳液;
(4)将步骤(3)所得的复乳液进行磁力搅拌,转速为400r/min,时间为4h,使有机溶剂蒸发,得到含水微球,将所得含水微球采用孔径为0.45μm的微孔滤膜进行抽滤,得到BMP-2/PLLA/nHA缓释微球。
图1为本实施例制备的BMP-2/PLLA/nHA缓释微球的SEM图,可见微球形态规整均匀,近似圆形,无粘连。
通过工艺把缓释微球相互结合制成膨胀螺栓,在体外制备与关节腔相似的环境,膨胀螺栓在该环境内固定后缓慢降解并缓释BMP-2/纳米羟基磷灰石微球。通过舒加法测定BMP-2缓释浓度。舒加法测定原理是利用分光光度计测定溶液在一定波长下的吸光度变化来测定这一反应。首先定义F.T.P.BMP-2单位,其相当于在规定条件下于450nm处每分钟使吸光度降低0.001时所需的BMP-2量。在实际操作中,以原始天然活性BMP-2的活性作为测定基准,每次在测量BMP-2活用天然活性BMP-2校正F.T.P.BMP-2单位,从而回归出吸光度的降低值。采用的缓冲体系为Na2HPO4-NaH2PO4磷酸盐缓冲溶液。底物溶液采用磷酸盐缓冲溶液溶解的BMP-2溶液,以磷酸盐缓冲溶液为参比,调节底物溶液吸光度值在1.30后使用。由于BMP-2自身能发生分解,该底物溶液应在配置后一个小时内使用。测试过程中,一般用磷酸盐缓冲溶液将BMP-2稀释到0.01mg/mL测量吸光度的变化,尽量保证每15s吸光度改变0.01~0.04。用取液器将2.5mL底物溶液滴入一只1cm比色皿,加0.5mL酶溶液,将这两种溶液充分混合,用分光光度计于450nm处以磷酸盐缓冲液为参比测定吸光度。在大约3min内每隔15s读取一次吸光度。BMP-2活性计算公式如下:
式中:
Ew——每0.5mL所用酶溶液中含有酶的重量;
0.001——一个单位在每分钟内使吸光度下降0.001;
ΔE450——在450nm处每分钟吸光度的变化;
每批BMP-2均采用一定浓度的BMP-2标准溶液作为测定基准,再测定样品中BMP-2的酶活性,对比求出样品中BMP-2浓度。最后计算BMP-2的释放率。
图2为本发明的BMP-2/PLLA/nHA缓释微球体制备膨胀螺栓后的体外药物释放曲线,由图可知,微球内BMP-2的释放率24h内超过15%,7d的释放率超过35%,这主要是由于微球表面的BMP-2溶出所致,突释后进入缓慢释放期,大约90%的BMP-2量于43d内释放完全,这段时期的释放行为是PLLA材料的缓慢降解和药物扩散引起的。这充分说明该BMP-2/PLLA/nHA缓释微球能较平稳地释放BMP-2,与骨重生和骨愈合周期较一致。
以上所述仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例。凡属于本发明思路下的技术方案均属于本发明的保护范围。应该指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下的改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!