GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用的制作方法
本发明涉及生物医药
技术领域:
,具体地说,涉及GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用。
背景技术:
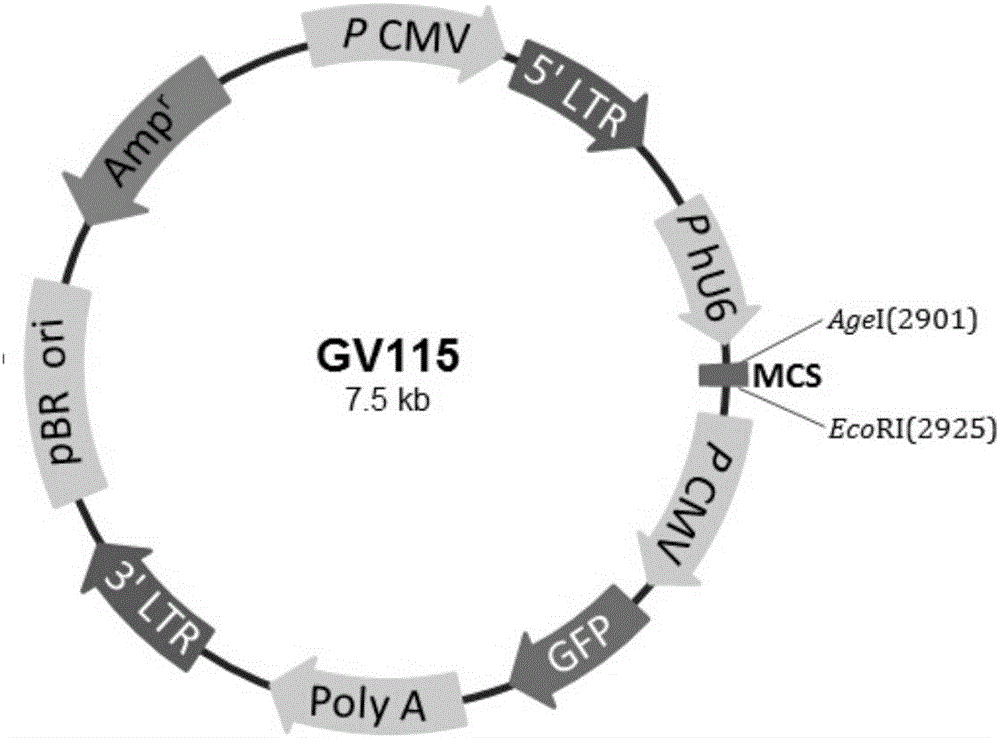
:随着人类生活习惯和行为模式的改变,以及农工业发展过程带来的环境污染和人口老龄化等原因,恶性肿瘤成为人类致死的主要疾病。世界卫生组织国际癌症研究中心(IARC/WHO)的最新数据显示恶性肿瘤在全球的发病率呈上升趋势,2008年760万人死于恶性肿瘤,其中64%发生在发展中国家。在我国,肿瘤防治面临的形势也极为严峻,最新报告显示,在过去30年间,我国恶性肿瘤的发病率和死亡率均呈明显上升趋势;据预测,在未来20-30年间,我国恶性肿瘤发病率和死亡率不断上升的趋势将继续维持。因此,对肿瘤的研究是生命科学和医学领域的持续研究热点之一。恶性肿瘤传统疗法如放疗、化疗和手术治疗的局限性促使人们寻找新的抗肿瘤方法。随着对肿瘤发生发展分子机制认识的深入,人们已意识到肿瘤是一种基因病,纠正发生缺陷的基因可为肿瘤的治疗提供新的希望。近年来发展了许多针对肿瘤的基因治疗方法的研究,但迄今为止进入临床应用的几种基因药物的临床疗效有限,且具有潜在的、长期的、延迟的副作用,因此,寻求治疗的新靶点和开发新的基因治疗方法已成为国内外肿瘤基因治疗的研究方向。RNA干扰(RNAinterference,RNAi)是一门基因阻断技术,为一种双链RNA(double-strandedRNA,dsRNA)分子在mRNA水平上阻断特异基因的表达或使其沉默的过程,即序列特异性的转录后基因沉默(Post-transcriptionalgenesilencing,PTGS)。近年来,RNAi已成为肿瘤基因治疗的有效策略。利用RNAi技术可以抑制原癌基因、突变的抑癌基因、细胞周期相关基因、抗凋亡相关基因等表达来抑制肿瘤的发生和发展。GINS2是DNA复制复合体GINS家族成员之一,位于人染色体16q24上,其mRNA长度为1196bp,编码相对分子质量为21000的蛋白质。GINS是一种复制解旋酶,在移动到复制叉前打开DNA双链。研究表明,GINS家族成员在癌症的发生中起一定作用,如GINS家族成员在侵袭性黑色素瘤中过表达,也有文献表明,DNA复制相关蛋白在不同细胞中有不同的作用,如在决定中心体复制数量和疾病发生的不同阶段方面,GINS均发挥了一定功能,特别是与染色体的分离密切相关。而目前关于GINS2在肿瘤相关领域的报道很少。技术实现要素:本发明的目的是针对现有技术中的不足,提供GINS2基因或蛋白的抑制剂的新用途。本发明提供了GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用。作为一种具体实施方式,所述的抑制剂选自以GINS2蛋白或其转录本为靶序列、且能够抑制GINS2蛋白表达或基因转录的siRNA、dsRNA、shRNA、miRNA、反义核酸;或能表达或形成所述siRNA、dsRNA、miRNA、反义核酸的构建物。作为一个优选例,所述的抑制剂选自下列中的一种:a)siRNA,所述siRNA的靶序列如SEQIDNO.1所示;b)shRNA,所述shRNA的编码序列正义链如SEQIDNO.5所示,反义链如SEQIDNO.6所示;c)能够表达a)所述siRNA或b)所述shRNA的载体;d)包含c)所述载体的病毒。作为本发明的一种具体实施方式,所述的肿瘤为人乳头状甲状腺癌。本发明还提供了一种siRNA分子,所述siRNA的靶序列如SEQIDNO.1所示。本发明还提供了一种shRNA分子,所述shRNA的编码序列正义链如SEQIDNO.5所示,反义链如SEQIDNO.6所示。本发明还提供了一种表达载体,所述表达载体能够表达所述siRNA分子或所述shRNA分子。本发明还提供了一种病毒,其包含所述表达载体。作为本发明的一种具体实施方式,所述病毒为慢病毒。本发明还提供了一种抗肿瘤药物,其包含所述siRNA分子、所述shRNA分子、所述表达载体和/或所述病毒,以及药学上可接受的载体。本发明还提供了检测人GINS2基因或蛋白表达水平的试剂在制备乳头状甲状腺癌诊断试剂或试剂盒中的应用。本发明优点在于:1、本发明设计了针对人GINS2基因的小分子干扰RNA(siRNA)序列,RNA干扰载体和RNA干扰慢病毒,进一步检测了GINS2基因的沉默效率、GINS2-siRNA慢病毒对肿瘤细胞增殖能力和凋亡水平的影响,结果表明:(1)采用RNAi方法下调人GINS2基因的表达后可有效抑制肿瘤细胞的增殖和生长并促进其凋亡,这一研究成果表明GINS2基因可促进肿瘤生长,是原癌基因,可作为肿瘤治疗的靶点,通过RNAi方式沉默GINS2基因的表达可作为抑制肿瘤发展的有效手段;(2)本发明的siRNA序列能够显著地特异性沉默人肿瘤细胞中内源GINS2基因的表达(沉默效率高达80.6%),显著优于常规方法所得的其他众多siRNA序列,表达该siRNA序列的慢病毒能够高效地抑制人肿瘤细胞的增殖和促进人肿瘤细胞的凋亡,因此本发明的siRNA序列、shRNA序列以及它们的构建体和病毒可用于制备高效的抗肿瘤药物。2、本发明证实人GINS2基因在乳头状甲状腺癌肿瘤组织和瘤旁组织表达差异显著,因此可作为乳头状甲状腺癌的诊断标志物。附图说明图1.GV115载体图谱。图2.载体线性化后目的片段的琼脂糖凝胶电泳图片。泳道1:1kbMarker:从上至下依次为10kb,8kb,6kb,5kb,4kb,3.5kb,3kb,2.5kb,2kb,1.5kb,1kb,750bp,500bp,250bp;泳道2:AgeI和EcoRI双酶切线性化后的载体质粒;泳道3:没有酶切的载体质粒。图3.RNA干扰载体构建及阳性克隆鉴定示意图。图4.RNA干扰载体阳性克隆鉴定的琼脂糖凝胶电泳图片。泳道1:阴性对照(ddH2O),排除系统中外源核酸污染导致假阳性结果;泳道2:自连对照(空载体自连对照组);泳道3:250bpMarker:从上至下依次为5kb,3kb,2kb,1.5kb,1kb,750bp,500bp,250bp,100bp;泳道4-8:单克隆psc45562-1,2,3,4,5。图5.GINS2-RNAi慢病毒侵染人乳头状甲状腺癌K1细胞3天后,GINS2mRNA表达水平显著降低。图6.GINS2-RNAi慢病毒侵染人乳头状甲状腺癌K1细胞5天后,引起细胞增殖抑制。经shRNA慢病毒感染,细胞铺于96孔板。Celigo连续检测5天,发现实验组K1细胞的增殖速率受到显著抑制。提示GINS2基因与K1细胞的增殖能力显著相关。图7和图8.FACS检测GINS2基因消减对人乳头状甲状腺癌细胞周期的影响。shRNA慢病毒感染后第3天传代,第5天检测,实验组处于G1期的细胞显著减增多,实验组处于S期的细胞显著减少,处于G2/M期的细胞减少,提示GINS2基因与K1细胞的凋亡显著相关。图9和图10.FACS检测GINS2基因消减对凋亡的影响。shRNA慢病毒感染第3天传代,第5天检测,实验组发生凋亡的K1细胞显著增加,提示GINS2基因与K1细胞的凋亡显著相关。图11.人GINS2基因在乳头状甲状腺癌患者肿瘤组织和瘤旁组织的差异表达。具体实施方式下面结合附图对本发明提供的具体实施方式作详细说明。应理解,实施例仅用于说明本发明,而非限制本发明的范围。实施例中未注明具体条件的实验方法及未说明配方的试剂均为按照常规条件。实施例1:针对人GINS2基因RNAi慢病毒的制备技术路线为:从Genbank中调取人GINS2基因序列;预测siRNA位点;合成针对GINS2基因的有效siRNA序列,两端含酶切位点粘端的双链DNAOligo;慢病毒载体双酶切后与双链DNAOligo连接,构建表达GINS2基因的siRNA序列的RNAi质粒;将RNAi质粒和慢病毒包装需要的辅助载体共转染人胚肾细胞293T细胞,产生种族慢病毒颗粒,即可制得高效沉默GINS2基因的慢病毒。1、RNA干扰靶点设计及双链DNAoligo制备(1)设计合成针对人GINS2基因的有效的siRNA靶点从Genbank调取GINS2(NM_016095)基因信息;设计针对GINS2基因的有效的siRNA靶点。表1为针对GINS2基因的有效siRNA靶点序列。表1靶向人GINS2基因的有效siRNA靶点序列(2)DNAoligo序列合成根据已选靶点序列设计shRNA干扰序列,并在两端添加合适的限制性内切酶酶切位点以完成载体构建。除此之外,在正链3’端添加TTTTT终止信号,而反链5’端添加终止信号互补序列。合成单链DNAoligo。表2两端含AgeI和EcoRI酶切位点粘端的单DNAOligo*CCGG:AgeI酶切位点;AATTC:EcoRI酶切位点;G:EcoRI酶切位点互补序列。(3)双链DNAoligo制备将合成的单链DNAoligo干粉溶解于退火缓冲液中(终浓度20μM),90℃水浴15min。自然冷却至室温后,形成带粘性末端的双链,其序列为:正链:5’-CCGGGCGATTAACCTGAAACAAAGACTCGAGTCTTTGTTTCAGGTTAATCGCTTTTTG-3’(SEQIDNO.5);反链:5’-AATTCAAAAATCTTTGTTTCAGGTTAATCGCCTCGAGGCGATTAACCTGAAACAAAGAAATTCAAAAA-3’(SEQIDNO.6)。(4)线性化载体制备按照NEB说明书配制50μl反应体系,使用AgeI和EcoRI双酶切GV115载体(购于上海吉凯基因化学技术有限公司,载体图谱见图1)使其线性化。反应体系如下:37℃(最适温度)反应1h,之后切胶回收目的片段。目的片段的琼脂糖凝胶电泳图片见图2。2、RNA干扰慢病毒载体构建(1)连接按照FermentasT4DNALigase说明书配制20μl反应体系,将双链DNAoligo与线性化的载体相连。反应体系如下:于16℃反应1-3h,连接产物命名为psc45562,之后进行转化实验。(2)转化将连接产物转化大肠杆菌感受态细胞,详细操作步骤如下:1)将10μl连接产物psc45562加入到100μl大肠杆菌感受态细胞中,冰浴30min。2)42℃热激90sec,冰浴2min。3)加入500μL无抗生素的LB液体培养基,200rpm于37℃摇床震荡培养1hr。4)取150μl菌液均匀涂抹在含有Amp的LB固体培养基上,于37℃培养箱中过夜培养。(3)阳性克隆的PCR鉴定①RNA干扰载体构建及阳性克隆鉴定示意图RNA干扰载体构建及阳性克隆鉴定示意图参见图3。②引物鉴定引物序列如下:③PCR扩增用无菌枪头挑取单个菌落为模板,进行PCR扩增,反应条件为:94℃3min;94℃30s,55℃30s,72℃30s,22次循环;72℃5min。PCR反应体系如下:④琼脂糖凝胶电泳检测PCR结束后,取5μl产物,1%琼脂糖凝胶电泳检测条带。琼脂糖凝胶电泳图片见图4。连接入shRNA片段的阳性克隆PCR片段大小为:342bp;没有连接入shRNA片段的空载体克隆PCR片段大小为:307bp。由此判断psc24135-1,2,4,5为阳性克隆,保存鉴定结果正确的克隆。(4)阳性克隆测序结果分析以鉴定引物-F进行阳性克隆测序,挑选测序结果与目标序列完全一致的克隆用于下一步实验。测序结果如SEQIDNO.9所示,其中第198-256bp为shRNA干扰序列插入片段,AgeI酶切位点被破坏。3、质粒抽提将测序正确的菌液转接于150ml含Amp抗生素的LB液体培养基中,37℃摇床震荡培养过夜。按照EndoFreeMaxiPlasmidKit说明书提取质粒,质检合格的质粒进入下游流程。质粒抽提的详细操作步骤如下:1)8000rpm离心4min收集菌体;2)加入7mlP1,震荡混匀;3)加入7mlP3,颠倒混匀6~8次,静置5min;4)加入7mlP4,颠倒混匀6~8次,冰浴10min;5)9000rpm离心10min,将上清转移到过滤器CS中,过滤后加入10ml异丙醇混匀;6)向吸附柱中加入2.5ml的平衡液BL,8000rpm离心2min,倒掉收集管中的废液,将柱子放回备用;7)将上清分两次倒入吸附柱中,8000rpm离心2min,弃废液;8)向吸附柱中加入10ml漂洗液PW(已加入无水乙醇),相同转速离心2min,弃废液,重复该步骤一次;10)向吸附柱中加入3ml无水乙醇,8000rpm离心2min,弃废液;11)9500rpm空甩5min,除去残留的漂洗液;将吸附柱转移至一新的白管中,在柱中心滴加800μl洗脱缓冲液TB(先预热),室温放置5min,然后9500rpm离心2min;12)将管中的洗脱液转移到一干净的1.5mlEP管中,-20℃保存;13)取样电泳,使用分光光度计(Thermo_Nanodrop2000)测定质粒浓度,质检;14)将质检合格的质粒进行病毒包装。4、慢病毒包装人胚肾细胞293T,慢病毒的包装细胞,为贴壁依赖型成上皮样细胞,生长培养基为DMEM(含10%FBS),贴壁细胞经培养生长增殖形成单层细胞。大肠杆菌菌株DH5α,用于扩增慢病毒载体和辅助包装载体质粒。以Qiagen公司的质粒抽提试剂盒提取RNAi质粒,慢病毒包装系统中三种质粒DNA(GV载体质粒、pHelper1.0载体质粒、pHelper2.0载体质粒),配制成100ng/μl储存液。转染前24h,用胰蛋白酶消化对数生长期的293T细胞,以含10%血清的培养基调整细胞密度约5×106细胞/15ml,重新接种于10cm细胞培养皿,37℃、5%CO2培养箱内培养。24h待细胞密度达70%~80%时即可用于转染。转染前2h更换为无血清培养基;向一灭菌离心管中加入所制备的各DNA溶液(GV载体质粒20μg、pHelper1.0载体质粒15μg、pHelper2.0载体质粒10μg),把相应体积的转染试剂混合均匀,调整总体积为1ml,在室温下温育15min;混合液缓慢滴加至293T细胞培养液中,混匀,于37℃、5%CO2细胞培养箱中培养;培养6h后弃去含有转染混和物的培养基,加入10ml的PBS液清洗一次,轻柔晃动培养皿以洗涤残余的转染混和物后倒弃;缓慢加入含10%血清的细胞培养基20ml,于37℃、5%CO2培养箱内继续培养48-72h。慢病毒浓缩与纯化:根据细胞状态,收集转染后48h(转染即可计为0h)的293T细胞上清液;于4℃、4000g离心10min,除去细胞碎片;以0.45μm滤器过滤上清液于40ml超速离心管中;分别配平样品,将带有病毒上清液的超速离心管逐一放入至Beckman超速离心机内,设置离心参数为25000rpm,离心时间为2h,离心温度控制在4℃;离心结束后,弃去上清,尽量去除残留在管壁上的液体,加入病毒保存液(可用PBS或细胞培养基替代),轻轻反复吹打重悬;经充分溶解后,高速离心10000rpm、5min后,取上清分装。实施例2:RT-PCR检测GINS2基因的沉默效率将处于对数生长期的人乳头状甲状腺癌K1细胞进行胰酶消化,制成细胞悬液(细胞数约为5×104/ml),接种于6孔板,培养至细胞融合度达到约30%。加入适量的实施例1制备的病毒,培养6小时后更换培养基,待侵染时间达到3天后,收集细胞。RNA抽提及cDNA合成:①收取样品,Trizol裂解:收集细胞,2000rpm离心5min,去上清,细胞沉淀中加入1mLTrizol,充分混匀后室温静置5min,然后转移至新的1.5mLEP管中。②每管加入200μL氯仿,用手上下颠倒EP管15s,室温静置10min。③4℃、12800rpm,离心15min。④吸取上层液体移至新的1.5mLEP管,加入等体积预冷的异丙醇,混匀后4℃静置10min。⑤4℃、12800rpm离心12min后,弃上清。⑥加入1mL、75%乙醇(用DEPC水新鲜配制),洗涤沉淀。⑦4℃、11800rpm离心5min,弃去大部分上清。⑧4℃、11800rpm再次离心5min,弃去上清,室温干燥。⑨待RNA沉淀基本透明时,加入RNase-free水(加入体积视RNA沉淀量而定)至完全溶解,Nanodrop2000/2000C分光光度计分析测定所抽提RNA的浓度及质量。⑩将RNA逆转录获得cDNA,逆转录体系在42℃水浴反应1h,然后在70℃水浴10min使RT酶失活,逆转录反应体系如下:试剂每管加入量5×RTbuffer5μl10mMdNTPs2μlRnasin(40U/μL)0.4μlM-MLV-RTase(200U/μl)1μlRNase-FreeH2O5.6μlRT-PCR:采用Agilent公司的MX3000p型的RealtimePCR进行实时定量检测。GINS2基因的引物如下:上游引物5’-CCCGAAGGCAGACGAAATCC-3’(SEQIDNO.10),下游引物5’-TGAGGAAAGTCCCGCTGGTG-3’(SEQIDNO.11)。以管家基因GAPDH为内参,引物序列如下:上游引物5’-TGACTTCAACAGCGACACCCA-3’(SEQIDNO.12),下游引物5’-CACCCTGTTGCTGTAGCCAAA-3’(SEQIDNO.13)。反应体系如下:试剂每管加入量SYBRpremixextaq10.0μL上游引物(2.5μM)0.5μL下游引物(2.5μM)0.5μLcDNA1.0μLRNase-FreeH2O8.0μL设定程序为两步法Real-timePCR:预变性95℃,30s,之后每一步变性95℃,5s;退火延伸60℃,30s;共进行45个循环。每次在延伸阶段读取吸光值。PCR结束后,95℃变性1min,然后冷却至55℃,使DNA双链充分结合。从55℃开始到95℃,每一步增加0.5℃,保持4s,同时读取吸光值,制作熔解曲线。采用2-ΔΔCt分析法计算侵染GINS2mRNA的表达丰度。实验结果表明,人乳头状甲状腺癌K1细胞中GINS2mRNA的表达水平显著下降,具体下调了80.6%(图5)。实施例3:检测侵染GINS2-siRNA慢病毒的肿瘤细胞的增殖能力将处于对数生长期的人乳头状甲状腺癌K1细胞进行胰酶消化,制成细胞悬液(细胞数约为5×104/ml),接种于6孔板,培养至细胞融合度达到约30%。加入适量的实施例1制备的病毒,培养6小时后更换培养基,待侵染时间达到5天后,收集细胞。完全培养基重悬成细胞悬液(2×104/ml),以细胞密度约为2000个/孔接种于96孔板。每组3个复孔,每孔100μl。铺好板后,置细胞培养箱培养。从铺板后第二天开始,每天用Celigo检测读板一次,连续检测读板3-5天;通过调整analysissettings的输入参数,准确地计算出每次扫描孔板中的带绿色荧光的细胞的数量;对数据进行统计绘图,绘出5天的细胞增殖曲线。根据细胞计数值和时间点,绘制基于细胞计数值的细胞生长曲线。实验结果表明,慢病毒侵染组肿瘤细胞在体外培养5天后,增殖速度显著减缓,远低于对照组肿瘤细胞的增殖速度,人乳头状甲状腺癌K1细胞的活力细胞数目相对对照组下调了77.5%(图6)。实施例4:检测侵染GINS2-siRNA慢病毒的肿瘤细胞凋亡水平待各实验组6孔板细胞生长至覆盖率约为70%时,干扰组用GINS2-siRNA诱导凋亡;胰酶消化,完全培养基重悬成细胞悬液,与上清细胞收集于同一5mL离心管中,每组设三个复孔(为保证上机细胞数足够,细胞数目≥5×105/处理);1300rmp离心5min,弃上清,4℃预冷的D-Hanks(pH=7.2~7.4)洗涤细胞沉淀;1×bindingbuffer洗涤细胞沉淀一次,1300rmp、3min离心,收集细胞;200μL1×bindingbuffer重悬细胞沉淀;加入10μLAnnexinV-APC染色,室温避光10-15min;根据细胞量,补加400-800μL1×bindingbuffer,上机检测。结果表明,GINS2-siRNA干扰组肿瘤细胞凋亡率显著高于对照组,如图所示,在人乳头状甲状腺癌K1细胞(图7、图8、图9、图10)中,图7和图8提示沉默GINS2表达,实验组处于G1期的细胞显著增多,实验组处于S期的细胞显著减少,处于G2/M期的细胞减少,提示GINS2基因与K1细胞的凋亡显著相关。图9和图10提示实验组细胞凋亡率显著高于对照组。表明下调GINS2表达水平可导致肿瘤细胞凋亡。实施例5:靶向人GINS2基因的有效siRNA序列的筛选针对人GINS2基因设计siRNA序列,除实施例1中SEQIDNO.1所示序列外,设计的其他siRNA靶序列选择示例如下:表3靶向人GINS2基因的siRNA靶序列按照实施例1-4所述的方法构建慢病毒载体,检测对GINS2基因的沉默效率以及对人乳头状甲状腺癌K1细胞增殖和凋亡的影响,结果见表4。表4siRNA序列的沉默效率、对细胞增殖和凋亡的影响实验结果表明,实施例1中siRNA序列对人GINS2基因的沉默效率和对人乳头状甲状腺癌K1细胞的增殖下调能力以及凋亡促进能力显著优于其他siRNA序列,其可用于制备高效的抗肿瘤药物。实施例6:检测人GINS2基因在肿瘤组织和瘤旁组织的差异表达取59例乳头状甲状腺癌患者肿瘤组织和瘤旁组织标本,其中男性17例,女性42例,年龄中位数为42岁(15~81岁)。分别检测肿瘤组织和瘤旁组织GINS2mRNA的相对表达量,以β-actin为内参基因进行标化,结果显示肿瘤组织GINS2mRNA的表达量显著高于瘤旁组织(P<0.05),如图11所示。肿瘤组织GNIS2mRNA相对表达量中位数为156.26(P25~P75为99.81~220.26),瘤旁组织GNIS2mRNA相对表达量中位数为66.80(P25~P75为48.45~100.76)。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。SEQUENCELISTING<110>上海市第七人民医院<120>GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用<130>/<160>15<170>PatentInversion3.3<210>1<211>19<212>DNA<213>人工序列<400>1gattaacctgaaacaaaga19<210>2<211>10<212>DNA<213>人工序列<400>2aattcaaaaa10<210>3<211>21<212>DNA<213>人工序列<400>3gcgattaacctgaaacaaaga21<210>4<211>21<212>DNA<213>人工序列<400>4tctttgtttcaggttaatcgc21<210>5<211>58<212>DNA<213>人工序列<400>5ccgggcgattaacctgaaacaaagactcgagtctttgtttcaggttaatcgctttttg58<210>6<211>68<212>DNA<213>人工序列<400>6aattcaaaaatctttgtttcaggttaatcgcctcgaggcgattaacctgaaacaaagaaa60ttcaaaaa68<210>7<211>24<212>DNA<213>人工序列<400>7cctatttcccatgattccttcata24<210>8<211>20<212>DNA<213>人工序列<400>8gtaatacggttatccacgcg20<210>9<211>853<212>DNA<213>人工序列<400>9tgttagagagataattggaattaatttgactgtaaacacaaagatattagtacaaaatac60gtgacgtagaaagtaataatttcttgggtagtttgcagttttaaaattatgttttaaaat120ggactatcatatgcttaccgtaacttgaaagtatttcgatttcttggctttatatatctt180gtggaaaggacgaaacaccgggcgattaacctgaaacaaagactcgagtctttgtttcag240gttaatcgcttttttgaattctcgacctcgagacaaatggcagtattcatccacgaattc300ggatccattaggcggccgcgtggataaccgtattaccgccatgcattagttattaatagt360aatcaattacggggtcattagttcatagcccatatatggagttccgcgttacataactta420cggtaaatggcccgcctggctgaccgcccaacgacccccgcccattgacgtcaataatga480cgtatgttcccatagtaacgccaatagggactttccattgacgtcaatgggtggagtatt540tacggtaaactgcccacttggcagtacatcaagtgtatcatatgccaagtacgcccccta600ttgacgtcaatgacggtaaatggcccgcctggcattatgcccagtacatgaccttatggg660actttcctacttggcagtacatctacgtattagtcatcgctattaccatggtgatgcggt720tttggcagtacatcaatgggcgtggatagcggtttgactcacggggatttccaagtctcc780accccattgacgtcaatgggagtttgttttggcaccaaaatcaacgggactttccaaaat840gtcgtaacaactc853<210>10<211>20<212>DNA<213>人工序列<400>10cccgaaggcagacgaaatcc20<210>11<211>20<212>DNA<213>人工序列<400>11tgaggaaagtcccgctggtg20<210>12<211>21<212>DNA<213>人工序列<400>12tgacttcaacagcgacaccca21<210>13<211>21<212>DNA<213>人工序列<400>13caccctgttgctgtagccaaa21<210>14<211>19<212>DNA<213>人工序列<400>14caccgctggcgattaacct19<210>15<211>18<212>DNA<213>人工序列<400>15caccggatcatgaacgaa18当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种制备自噬小体型瘤苗的培养基添加剂及其制备方法与制造工艺
- N-萘烷基取代的含氮杂环衍生物、制备方法及其抗肿瘤用途与制造工艺
- 作为BET蛋白抑制剂的1H‑吡咯并[2,3‑c]吡啶‑7(6H)‑酮和吡唑并[3,4‑c]吡啶‑7(6H)‑酮的制造方法与工艺
- 一种人肿瘤抑制蛋白变体及其应用的制造方法与工艺
- 一种人肿瘤抑制蛋白变体及其应用的制造方法与工艺
- G蛋白信号调节因子6及其抑制剂在治疗脂肪肝和Ⅱ型糖尿病中的功能和应用的制造方法与工艺
- 蛋白酶体抑制剂在制备降低动物脂含量或脂储积能力产品中的应用的制造方法与工艺
- GINS2基因或蛋白的抑制剂在制备抗肿瘤药物中的应用的制造方法与工艺
- ZNF383蛋白在制备抑制p53蛋白活性的产品中的应用的制造方法与工艺
- 蛋白酶体抑制剂MLN9708的合成方法与制造工艺