一种超声刺激响应性聚酰胺囊泡的制备方法与流程
本发明涉及聚合物材料领域,具体涉及一种超声刺激响应性聚酰胺囊泡的制备方法。
背景技术:
囊泡是广泛存在于生命系统中的结构,在基因药物运输等领域中有很广泛的应用,因而已经引起了科研工作者极大的研究兴趣。一般来说,囊泡可以由脂质体分子、表面活性剂、嵌段共聚物的自组装得到。其中,毫无疑问,聚合物囊泡位于纳米科技革命的最前沿,这是由于聚合物囊泡在药物封装、药物运输、纳米反应器和微米或纳米材料模板等领域拥有无限可能的应用潜力。超声是一种对人体无害的物理信号,因此超声刺激响应性聚合物囊泡在生物体内药物运输和缓释具有非常大的前景。然而,目前聚合物囊泡大多数都是由二嵌段共聚物,三嵌段共聚物、树枝状聚合物和超支化聚合物的自组装得到的,而关于利用多嵌段的缩聚物则很难制备出囊泡,并且目前聚合物囊泡很难具备超声响应性能。
技术实现要素:
为解决上述现有技术中存在的问题,本发明提供一种超声刺激响应性聚酰胺囊泡的制备方法。
本发明的超声刺激响应性聚酰胺囊泡的制备方法,包括以下步骤:
(1)向反应球瓶中加入干燥剂、溶剂,缓慢加热至40-70℃,搅拌使之完全溶解,随后再向溶液中加入含磺酸基的芳香族二元羧酸和稳定剂,待其完全溶解后,再加入稍过量的二元胺,随后关闭控温仪,待溶液冷却后,再抽排三次,用惰性气体置换出体系中的空气,在保持惰性气氛下,进行反应,得到亲水聚酰胺嵌段;以脂肪族二元羧酸代替含磺酸基的芳香族二元羧酸,以同样的方法得到疏水聚酰胺链段;
(2)迅速将质量比为1:4-3:5的亲水聚酰胺链段和疏水聚酰胺链段混合加入到反应球瓶中,同时补加干燥剂补偿整个反应体系的损失,在惰性气氛下,继续反应,得到共聚酰胺溶液,用甲醇使其沉淀,静置后,过滤、洗涤,收集到多嵌段共聚酰胺,进一步在90-105℃下真空干燥;所述真空干燥的时间为20-30小时,优选24小时。
(3)将多嵌段共聚酰胺溶于去离子水中制得多嵌段共聚酰胺溶液,在40-60℃下加热搅拌,得到超声刺激响应性聚酰胺囊泡;所述加热搅拌优选12小时。
根据如上所述的制备方法,在步骤(1)及步骤(2)中,所述干燥剂为氯化钙、硫酸钙、硫酸铜中的一种或几种。
根据如上所述的制备方法,在步骤(1)及步骤(2)中,所述反应的条件是加热升温至95℃-110℃、反应2-20小时。其中,反应温度更为优选95℃、100℃、105℃或110℃,反应时间更为优选2小时、3小时、4小时、5小时、6小时、7小时、10小时或20小时。
另外,在步骤(3)中,亲水聚酰胺链段与疏水聚酰胺链段的质量比为1:4-3:5,该质量比也可优选1:4、2:5或3:5。
根据如上所述的制备方法,在步骤(1)及步骤(2)中,所述溶剂为n-甲基吡咯烷酮和吡啶的混合溶液,其中n-甲基吡咯烷酮与吡啶的体积比为5-9:1-4,其中更为优选例如5:1、6:2、7:1、8:3或9:4。
根据如上所述的制备方法,在步骤(1)及步骤(2)中,所述稳定剂为磷酸三苯酯、磷酸三甲酯或亚磷酸酯中的一种或几种。
根据如上所述的制备方法,在步骤(1)及步骤(2)中,所述二元胺为乙二胺、丁二胺、己二胺或葵二胺中的一种或几种。
根据如上所述的制备方法,在步骤(1)中,所述含磺酸基的芳香族二元羧酸至少为间苯二甲酸-5-磺酸钠、对苯二甲酸-5-磺酸钠中的一种或几种
根据如上所述的制备方法,在步骤(1)中,所述的脂肪族二元酸为丁二酸、己二酸、壬二酸或癸二酸中的一种或几种。
所述的制备方法,步骤(1)中亲水聚酰胺链段制备中各成分用量的质量比为60-100份混合溶剂:20-30份含磺酸基的芳香族二元羧酸:6-18份二元胺:60-100份稳定剂:1-6份干燥剂;步骤(1)中疏水聚酰胺链段制备中各成分用量的质量比为60-100份混合溶剂:12-20份脂肪族二元酸:6-18份二元胺:60-100份稳定剂:1-6份干燥剂;
根据如上所述的制备方法,在步骤(3)中,所述反应的反应时间为24-96小时、反应温度为100-130℃,其中反应时间优选为24小时、48小时、72小时或96小时;反应温度优选100℃、105℃、120℃或130℃。
另外,在步骤(3)中,真空干燥温度为90-105℃,其中优选90℃、95℃、100℃或105℃。
根据如上所述的制备方法,在步骤(4)中,多嵌段共聚酰胺溶液的浓度为0.5mg/ml-10mg/ml。其中,优选0.5mg/ml、1mg/ml或2mg/ml。
另外,在步骤(4)中,搅拌温度为40-60℃,可优选为40℃、50℃或60℃。
由本发明所制备的聚酰胺囊泡具有超声响应性,在超声的作用下囊泡会发生破裂。本发明所涉及的制备方法简单,囊泡性能稳定。
选用不溶于水的尼罗红分子作为模型药物分子,对囊泡水溶液而言,如果包裹在囊泡疏水壁中的尼罗红分子被释放到水溶液中,由于尼罗红分子不溶于水,会聚集沉淀下来,从而导致囊泡水溶液中尼罗红染料荧光强度的降低,因此可以通过检测囊泡水溶液的荧光光谱,来确定mbcpa囊泡的药物释放能力,并且可以通过与hbpo-star-peo囊泡的释放进行比较来验证本发明超声响应的独特性。
通过对比室温下、50℃、50℃超声作用下囊泡的荧光发射光谱来验证本发明中囊泡的稳定性。
附图说明
图1是实施例1制得的mbcpa的核磁图谱。
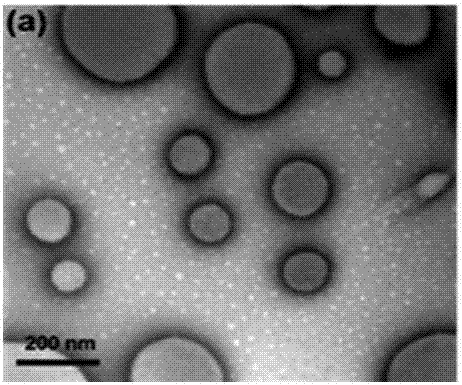
图2是实施例1制得的囊泡的透射电镜图。
图3是实施例1中的在不同超声作用时间后囊泡溶液中尼罗红紫外吸收强度的测试结果。
图4是超声作用后囊泡溶液图。
图5是在超声作用下包裹有尼罗红染料分子的实施例1制得的囊泡或hbpo-star-peo囊泡水溶液的荧光发射光谱归一化曲线。
图6是实施例1制得的囊泡在室温下、50℃、50℃超声作用下囊泡的荧光发射光谱归一化曲线。
具体实施方式
下面结合实施例对本发明进行详述,但本发明并不限定于这些实施例。
下述实施例中所使用的实验方法如无特殊说明,均为本领域技术人员所知的常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径常规获得。
一、超声刺激响应性聚酰胺囊泡的制备
实施例1
1)在50ml的反应球瓶中加入0.1g的无水氯化钙、5.0ml的n-甲基吡咯烷酮与1ml的吡啶的混合溶液,缓慢加热至70℃,搅拌使之完全溶解。随后再向溶液中加入2.68g间苯二甲酸-5-磺酸钠(5-ssipa)和5.2ml亚磷酸三苯酯,待其完全溶解后,再加入稍过量的1.2g己二胺。随后关闭控温仪,待溶液冷却后,再抽排三次,用氮气置换出体系中的空气。在保持体系惰性气氛下,开始加热升温至100℃,反应2小时即可得到亲水pa6sip嵌段。采用相同的方法以己二酸(1.2g)代替间苯二甲酸-5-磺酸钠合成疏水的pa66链段。
2)随后,按pa6sip:pa66质量比1:4迅速的把pa6sip嵌段溶液与pa66嵌段溶液混合转移到反应球瓶中。同时补加无水氯化钙补偿整个反应体系的损失。在惰性气氛下,反应在100℃继续反应24小时。最后得到的共聚酰胺溶液用250ml甲醇沉淀。静置过夜后,过滤可以得到纤维粉末状产物,并用甲醇洗涤产物三次。收集到的超声响应性多嵌段共聚酰胺在90℃下,真空干燥24小时。为了方便起见,将制备的多嵌段共聚酰胺记为mbcpa。图1是实施例1制得的mbcpa的核磁图谱,该图谱显示成功合成mbcpa聚酰胺。
3)将3mg多嵌段共聚酰胺溶于6ml的去离子水中,在60℃下,加热搅拌12小时,最后得到超声刺激响应性聚酰胺囊泡溶液。图2是实施例1制得的囊泡的透射电镜图。
实施例2
1)在50ml的反应球瓶中加入0.2g的无水硫酸铜,7.0ml的n-甲基吡咯烷酮与1ml的吡啶的混合物溶液,缓慢加热至60℃,搅拌使之完全溶解。随后再向溶液中加入2.0g对苯二甲酸-5-磺酸钠和8.2ml亚磷酸三苯酯,待其完全溶解后,再加入稍过量的1.4g丁二胺。随后关闭控温仪,待溶液冷却后,再抽排三次,用氮气置换出体系中的空气。在保持体系惰性气氛下,开始加热升温至95℃,反应10小时即可得到亲水pa6sip嵌段。采用相同的方法用己二酸(2.0g)代替对苯二甲酸-5-磺酸钠合成疏水链段。
2)随后,按亲水链段:疏水链段质量比2:5迅速的把亲水和疏水链段混合到反应球瓶中。同时补加0.05g无水硫酸铜补偿整个反应体系的损失。在惰性气氛下,反应在120℃继续反应48小时。最后得到的共聚酰胺溶液用250ml甲醇沉淀。静置过夜后,过滤可以得到纤维粉末状产物,并用甲醇洗涤产物三次。收集到的超声响应性多嵌段共聚酰胺在95℃下,真空干燥24小时。
3)将6mg多嵌段共聚酰胺溶于6ml的去离子水中,在40℃下,加热搅拌12小时,最后得到超声刺激响应性聚酰胺囊泡溶液。
实施例3
1)在50ml的反应球瓶中加入0.4g的无水硫酸钙,8.0ml的n-甲基吡咯烷酮与3ml的吡啶的混合溶液,缓慢加热至40℃,搅拌使之完全溶解。随后再向溶液中加入3.0g间苯二甲酸-5-磺酸钠(5-ssipa)和6.6ml磷酸三苯酯,待其完全溶解后,再加入稍过量的0.6g己二胺。随后关闭控温仪,待溶液冷却后,再抽排三次,用氮气置换出体系中的空气。在保持体系惰性气氛下,开始加热升温至95℃,反应20小时即可得到亲水聚酰胺嵌段。用相同的方法,用丁二酸(1.5g)代替间苯二甲酸-5-磺酸钠(5-ssipa)合成疏水聚酰胺链段。
2)随后,按亲水链段:疏水链段质量比3:5迅速的将亲水链段和疏水链段混合到反应球瓶中。同时补加0.05g无水硫酸钙补偿整个反应体系的损失。在惰性气氛下,反应在110℃继续反应72小时。最后得到的共聚酰胺溶液用250ml甲醇沉淀。静置过夜后,过滤可以得到纤维粉末状产物,并用甲醇洗涤产物三次。收集到的超声响应性多嵌段共聚酰胺在105℃下,真空干燥24小时。
3)将60mg多嵌段共聚酰胺溶于6ml的去离子水中,在50℃下,加热搅拌12小时,最后得到超声刺激响应性聚酰胺囊泡溶液。
实施例4
1)在50ml的反应球瓶中加入0.6g的无水氯化钙,9.0ml的n-甲基吡咯烷酮和4ml的吡啶,缓慢加热至50℃,搅拌使之完全溶解。随后再向溶液中加入2.42g对苯二甲酸-5-磺酸钠和6.5ml磷酸三甲酯,待其完全溶解后,再加入稍过量的1.8g葵二胺。随后关闭控温仪,待溶液冷却后,再抽排三次,用氮气置换出体系中的空气。在保持体系惰性气氛下,开始加热升温至105℃,反应20小时即可得到亲水链段段。用相同的方法,以壬二酸(1.3g)代替对苯二甲酸-5-磺酸钠合成疏水聚酰胺链段。
2)随后,按亲水链段:疏水链段质量比1:4迅速的将亲水链段和疏水链段混合到反应球瓶中。同时补加0.05g无水氯化钙补偿整个反应体系的损失。在惰性气氛下,反应在130℃继续反应96小时。最后得到的共聚酰胺溶液用250ml甲醇沉淀。静置过夜后,过滤可以得到纤维粉末状产物,并用甲醇洗涤产物三次。收集到的超声响应性多嵌段共聚酰胺在100℃下,真空干燥24小时。
3)将12mg多嵌段共聚酰胺溶于6ml的去离子水中,在60℃下,加热搅拌12小时,最后得到超声刺激响应性聚酰胺囊泡溶液。
二、实施例1-4所述的囊泡的药物释放能力测试
选用不溶于水的尼罗红分子作为模型药物分子测试所制备囊泡的超声响应特性,对囊泡水溶液而言,如果包裹在囊泡疏水壁中的尼罗红分子被释放到水溶液中,由于尼罗红分子不溶于水,会聚集沉淀下来,从而导致囊泡水溶液中尼罗红染料荧光强度的降低,因此可以通过检测囊泡水溶液的荧光光谱,来确定mbcpa囊泡的药物释放能力。
图3是实施例1中的在不同超声作用时间后囊泡溶液中尼罗红紫外吸收强度的测试结果。图4是超声作用后囊泡溶液图。由图3及图4可以明显看到囊泡在超声的刺激下会发生破裂。
表1是实施例1-4囊泡溶液在超声作用下尼罗红紫外吸收强度下降50%所用时间。
表1
图5是在超声作用下,包裹有尼罗红染料分子的实施例1制得的囊泡及hbpo-star-peo囊泡水溶液的荧光发射光谱;根据包裹有尼罗红染料的囊泡的荧光发射光谱得到的归一化曲线。从图中看出普通的hbpo-star-peo囊泡在超声作用下不释放尼罗红,即不具有超声响应性,而本发明中制得的囊泡具有超声响应独特性。
图6是实施例1制得的囊泡在室温下、50℃、50℃超声作用下囊泡的荧光发射光谱归一化曲线。由图6可发现本发明所述囊泡在远高于体温的50℃温度下也不破裂,说明本发明所述囊泡性能稳定。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!