HIV疫苗及其制备方法与流程
本发明属于疫苗领域,具体涉及一种基于构象诱导加特异性表位选择加强免疫策略的新型艾滋病疫苗以及其制备方法。
背景技术:
艾滋病(aids)是由感染人类免疫缺陷病毒(humanimmunodeficiencyvirus,hiv)引起人淋巴cd4t细胞大量死亡而导致的获得性免疫缺陷综合征(acquiredimmunodeficiencysyndrome,aids)。1981年发现首例艾滋病病例后,艾滋病迅速在全球范围内蔓延扩散。根据联合国艾滋病规划署的估计,截至2015年底,全球仍有约3670万艾滋病毒感染者。同年,约200万人新感染了艾滋病毒,120万人死于艾滋病毒相关原因,已经严重威胁全球的人类健康,严重危害社会进步和经济增长,是全球所面临的重大挑战之一。如何有效预防hiv感染,降低发病率和死亡率是我国乃至全球面临的紧迫任务。
疫苗是控制hiv传播和感染的有效手段。遗憾的是,目前尚无有效的疫苗被批准上市。rv144是目前唯一一个在临床试验上证明具有一定保护效果的疫苗,临床试验表明其有31.2%的保护效果(3)。随后的免疫分析发现其具有保护效果的原因(4)主要为:1)抗hiv保护率与疫苗接受者体内识别hiv包膜蛋白gp120v1v2区的igg抗体含量水平成正相关;2)抗hiv保护率与疫苗接受者体内血浆中识别hiv包膜蛋白iga的水平成负相关。血浆中该类iga可能跟该类igg竞争结合包膜蛋白,从而阻止该类igg发挥抗体依赖的细胞介导的细胞毒作用(antibody-dependentcell-mediatedcytotoxicity,adcc),降低对hiv感染细胞的杀伤作用而削弱疫苗的保护效果。并且,针对v1v2区的igg所具有的adcc效应被认为与rv144具有保护效果密切相关,可能起到了关键作用。因此,如何诱导出更高水平的识别hiv-1天然构象v1v2的特异性igg及该igg介导的adcc能力、同时减少刺激产生识别包膜蛋白的iga,是hiv疫苗设计的关键技术瓶颈之一。
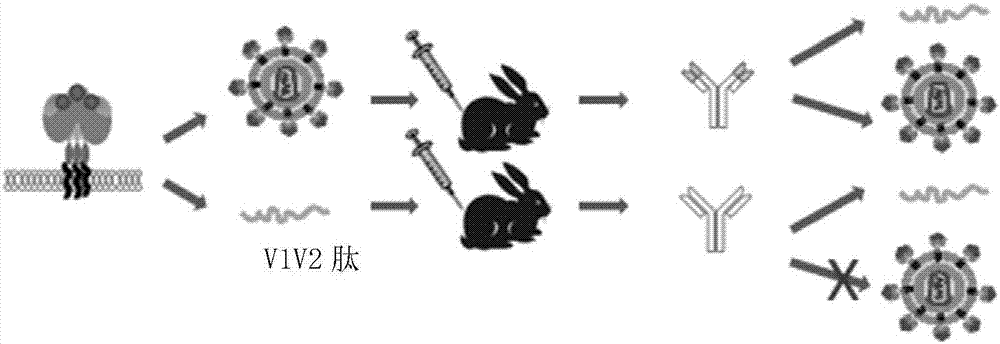
之前的研究表明,利用假病毒去免疫动物,免疫得到的抗体既能够识别病毒包膜蛋白也能够识别含有某一表位序列的多肽。但是,用含有某一表位序列的多肽作为抗原免疫动物所得到的抗体仅能识别该多肽抗原,而极难识别具有天然构象的病毒包膜蛋白(图1)。因此,单纯利用多肽免疫很难诱导产生识别结合天然构象病毒包膜蛋白的抗体,这是目前hiv疫苗研究中的共识。造成这一现象的原因可能是相同序列在多肽上的构象与在病毒上的天然构象不同。
目前这种以多肽为抗原的表位疫苗设计方案面临以下几个重要问题:1)表位多肽分子量相对小,免疫原性较弱;2)由于多肽抗原只包含关键表位的氨基酸序列,没有较多的周围辅助结构,所以很难具有类似于病毒上该表位的天然构象,因此有些多肽抗原很难诱导出能够识别具有天然构象相应表位的抗体。例如,之前的研究表明,利用hiv-1gp41上mper区的表位多肽,诱导产生的抗体仅能够识别该表位多肽,而对hiv的识别能力较差,没有中和活性(1,2)。因此,如何利用表位疫苗诱导出识别病毒上具有天然构象的相应表位的抗体是hiv疫苗设计的一个难题。
技术实现要素:
针对以上两个技术难点,我们在本发明中创新地提出了构象诱导加特异表位筛选的方法,来解决现有的hiv疫苗所存在的保护效果不高的问题。本发明提出的构象诱导加特异表位选择加强免疫的设计能够有效地解决利用线性表位疫苗难以诱导识别具有天然构象的该表位的抗体的难题,增强疫苗的抗病毒保护效果。
因此,一方面,本发明涉及一种艾滋病组合疫苗,其包含按以下顺序分别接种的组分:
(a)表达包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白的dna;
(b)包含hivgp120蛋白序列或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白;和
(c)包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽。
在本发明的第二方面,提供了一种用于预防艾滋病的试剂盒,其包括:
(1)本发明在第一方面的艾滋病组合疫苗;和
(2)接种所述艾滋病组合疫苗的说明书。
在本发明的第三方面,提供了本发明在第一方面的艾滋病组合疫苗在制备用于预防艾滋病的药物中的用途。
在本发明的第四方面,提供了一种对受试者进行免疫接种用于预防艾滋病的方法,包括以下步骤:
i.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(a)组分和任选的可药用佐剂对所述受试者进行初次免疫(初免);
ii.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(b)组分和任选的可药用佐剂对所述受试者进行第一次加强免疫,优选地在初次免疫(初免)两周后进行第一次加强免疫;并且
iii.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(c)组分和任选的可药用佐剂对所述受试者进行第二次加强免疫,优选地在第一次加强免疫两周后进行第二次加强免疫。
本发明的构象诱导加特异性表位选择加强免疫的策略显著提高了识别天然构象hiv-1gp120v1v2区的特异性igg抗体的水平,有效减少了免疫动物血浆中的识别hiv-1env的iga的产生;在此基础上,显著提高了adcc效应(图7,图8)。
附图说明
图1是现有技术中的多肽疫苗所遇到的技术难点的说明图。
图2是本发明的构象诱导加特异性表位选择加强免疫之设计原理的示意图。
图3是示出jrfl-v1v2ab(jr-fl假病毒免疫后纯化的v1v2特异性抗体)和pep-v1v2ab(v1v2多肽免疫后纯化的v1v2特异性抗体)与v1v2多肽的识别情况的柱状图。
图4是示出jrfl-v1v2ab识别细胞表达的天然构象的hiv-1包膜蛋白而pep-v1v2ab不识别该天然构象的hiv-1env的图表。
图5是示出构象诱导加特异性表位选择加强的免疫策略提高识别天然构象hiv-1v1v2区的igg的水平的柱状图。
图6是示出构象诱导加特异性表位选择加强的免疫策略降低识别天然hiv-1env的iga的水平的柱状图。
图7是示出构象诱导加特异性表位选择加强的免疫策略获得的特异性抗体具有更强adcc效应激活作用的柱状图。
图8是示出构象诱导加特异性表位选择加强的免疫策略获得的特异性抗体具有诱导更强adcc效应的柱状图。
具体实施方式
在本公开文本中提到的所有出版物均以全文引用的方式纳入本文,用于描述和公开出版物中所描述的方法,该方法可与本文中的描述联合使用。在本申请上下文中讨论的出版物仅仅由于其在本申请的申请日之前公布而被提供。此外,关于纳入引用文献中的类似或相同术语以及在本公开中明确定义的术语,在所有方面均以本公开文本中提供的术语定义为准。
除非另外定义,否则本文使用的所有技术和科学术语的含义与本公开所属领域的普通技术人员通常所了解的含义相同。本文描述了示例性的方法、装置和材料,但是与本文所述的方法和材料类似或同等的方法和材料都可用于所公开的方法和组合物的实施中。
在本文中,术语“包含”为开放式描述,表示除了该术语之后所列组分之外,还可以包含其它组分,前提条件是该其它组分不干扰或者不显著干扰想要获得的技术效果。类似的表述可以为例如“包括”、“含有”、“主要由……组成”、“基本由……组成”。另外,该术语“包含”还可以仅包含其后所列组分,类似的表述可以为例如“由……组成”、“仅包含”。
在本文中,术语“多肽”以其常规含义使用,即作为氨基酸序列使用。多肽不限于特定长度的产品。肽和蛋白质均包括在多肽的定义内,并且这三个术语可以在本文中互换使用,除非以其他方式具体指明。
本领域已知,动物或者人体内存在各种各样的淋巴细胞克隆。利用不同抗原进行免疫能够得到分泌针对所述不同抗原的抗体的多种淋巴细胞克隆。具体到本发明所涉及的人类免疫缺陷病毒(hiv),(a)当用v1v2多肽免疫时,能够诱导出可识别v1v2多肽的淋巴细胞克隆,然而该淋巴细胞克隆所分泌的抗体大多数仅可识别v1v2多肽而不能识别在细胞表面表达的天然构象env。(b)当利用表达天然构象的hivenv的dna免疫时,能够诱导出分泌针对env之不同表位的抗体的各种淋巴细胞克隆,并且即便进一步利用相同dna增强免疫,诱导分泌出的抗体仍然针对env不同表位,能够分泌针对某一有效表位的抗体的淋巴细胞比例依然很低,甚至由于该表位不是显性表位,多次免疫后的特异性抗体比例更低。(c)当利用表达天然构象env的dna免疫时,能够诱导出分泌针对env之不同表位的抗体的各种淋巴细胞克隆,进一步利用gp120单体免疫两次,能够诱导出分泌识别gp120单体的抗体的淋巴细胞克隆。相比于env,gp120上的表位要少得多,因此能够适当提高分泌有效抗体的淋巴细胞的比例,但是该比例依然较低(图2之(a)至(c))。
本申请发明人结合艾滋病疫苗领域的最新进展以及现有的rv144疫苗的经验,发现利用构象诱导加特异性表位加强免疫的策略,可以有效地解决以上难题,提升rv144疫苗提示的所有保护相关因素。
本发明人提出的构象诱导加特异性表位选择加强免疫的策略如下:首先利用表达天然构象env的dna进行初次免疫,然后用gp120单体蛋白加强免疫,最后利用v1v2多肽进一步选择和加强(图2之(d))。
具体地,在本发明中,发明人通过利用能够表达天然构象env的dna比如质粒进行初次免疫,能诱导产生识别天然构象env的抗体。随后,利用gp120蛋白加强免疫,从而激发产生出更多gp120特异性抗体。最后,利用含有v1v2区的多肽加强诱导针对v1v2区的抗体产生的免疫反应,由此可以产生识别天然构象v1v2的特异性抗体,并且其数量和比例得以选择性提升,达到刺激增强特异性有效抗体产生的目的。
本发明中的实验结果显示,通过本发明中的新策略显著增加了识别天然构象v1v2区的特异性igg抗体的产生,有效降低了免疫动物血浆中识别env的iga水平(图5-图6)。在此基础上,可以显著提高adcc效应(图7-图8)。adcc是指抗体依赖的细胞介导的细胞毒性作用,其被认为是rv144疫苗产生保护效应的关键因素(5)。
因此,本发明一方面涉及一种艾滋病组合疫苗,其包含按以下顺序分别接种的组分:
(a)表达包含hiv-1包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白的dna;
(b)包含hiv-1gp120蛋白序列或与所述hivgp120蛋白序列具有相同免疫原性且至少80%同源的氨基酸序列的蛋白;和
(c)包含hiv-1gp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽。
在一个实施方案中,所述hiv病毒可以为hiv-1或者hiv-2,优选为hiv-1。
在本文中,术语“包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白”是指除了包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列自身之外,任选地还包含其它不影响所述hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的表达和免疫原性的氨基酸序列。本领域技术人员根据其所掌握的普通技术知识可以很容易地确定可以包含的氨基酸序列。
在本文中,术语“与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列”是指与所述hiv包膜蛋白具有相同免疫原性且至少80%同源例如81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、99.5%或99.9%同源的氨基酸序列。
在一个实施方案中,所述hiv包膜蛋白的序列为seqidno:1,如下所示:
mrvkgirksyqylwkggtlllgilmicsaveklwvtvyygvpvwkeatttlfcasdakaydtevhnvwathacvptdpnpqevvlenvtehfnmwknnmveqmqediislwdqslkpcvkltplcvtlnckdvnatnttndsegtmergeikncsfnittsirdevqkeyalfykldvvpidnnntsyrliscdtsvitqacpkisfepipihycapagfailkcndktfngkgpcknvstvqcthgirpvvstqlllngslaeeevvirsdnftnnaktiivqlkesveinctrpnnntrksihigpgrafyttgeiigdirqahcnisrakwndtlkqiviklreqfenktivfnhssggdpeivmhsfncggeffycnstqlfnstwnnntegsnntegntitlpcrikqiinmwqevgkamyappirgqircssnitgllltrdgginengteifrpgggdmrdnwrselykykvvkieplgvaptkakrrvvqrekravgigavflgflgaagstmgaasmtltvqarlllsgivqqqnnllraieaqqrmlqltvwgikqlqarvlaverylgdqqllgiwgcsgklicttavpwnaswsnksldriwnnmtwmewereidnytseiytlieesqnqqekneqelleldkwaslwnwfditkwlwyikifimivgglvglrlvftvlsivnrvrqgysplsfqtllpaprgpdrpegieeegger。
在本文中,术语“包含hivgp120蛋白或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白”是指除了包含hivgp120蛋白或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列自身之外,任选地还包含其它不影响hivgp120蛋白或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列的免疫原性的氨基酸序列。本领域技术人员根据其所掌握的普通技术知识可以很容易地确定可以包含的氨基酸序列。
在本文中,术语“与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列”是指与所述hivgp120蛋白具有相同免疫原性且至少80%同源例如81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、99.5%或99.9%同源的氨基酸序列。
在一个实施方案中,所述hivgp120的序列为seqidno:2,其序列如下所示:
lwvtvyygvpvwkeatttlfcasdakaydtevhnvwathacvptdpnpqevvlenvtehfnmwknnmveqmqediislwdqslkpcvkltplcvtlnckdvnatnttndsegtmergeikncsfnittsirdevqkeyalfykldvvpidnnntsyrliscdtsvitqacpkisfepipihycapagfailkcndktfngkgpcknvstvqcthgirpvvstqlllngslaeeevvirsdnftnnaktiivqlkesveinctrpnnntrksihigpgrafyttgeiigdirqahcnisrakwndtlkqiviklreqfenktivfnhssggdpeivmhsfncggeffycnstqlfnstwnnntegsnntegntitlpcrikqiinmwqevgkamyappirgqircssnitgllltrdgginengteifrpgggdmrdnwrselykykvvkieplgvaptkakrrvvqrekr。
在本文中,术语“包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽”是指除了包含hivgp120v1v2区或与其具有相同免疫原性且至少80%同源的氨基酸序列自身之外,任选地还包含其它不影响hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的免疫原性的氨基酸序列。本领域技术人员根据其所掌握的普通技术知识可以很容易地确定可以包含的氨基酸序列。
在本文中,术语“与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列”是指与所述hivgp120v1v2区至少80%同源例如81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、99.5%或99.9%同源的氨基酸序列。
在一个实施方案中,所述hivgp120v1v2区的序列为seqidno:3,如下所示:
gtvkltplcvtlnckdvnatnttndsegtmergeikncsfnittsirdevqkeyalfykldvvpidnnntsyrliscdtsvitqa。
在一个具体实施方案中,所述hiv包膜蛋白的序列为seqidno:1,所述hivgp120的序列为seqidno:2,并且所述hivgp120v1v2区的序列为seqidno:3。
在一个实施方案中,所述表达包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白的dna为表达包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白的质粒、或者包含hiv包膜蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的病毒状颗粒。优选地,所述质粒可以是pcdna-jr-fl-env,以下简称penv,其来自于nihaidsresearchandreferencereagentprogram,参见wang等人(2010)(8)。
在一个实施方案中,所述包含hivgp120蛋白序列或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白仅包含hivgp120蛋白或与所述hivgp120蛋白具有相同免疫原性且至少80%同源的氨基酸序列。所述包含hivgp120蛋白或与所述hiv包膜蛋白具有相同免疫原性且至少80%同源的氨基酸序列的蛋白可以通过病毒分离、重组表达或者合成等方式产生,或者通过商购获得。
在一个实施方案中,所述包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽可以通过真核细胞表达或合成的方式产生,或者通过商购获得。例如,所述包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽是利用其中克隆有编码所述包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽的dna的载体在体外表达获得的。所述载体可以是,例如pcdna3。
在一个实施方案中,所述包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列的多肽可以仅包含hivgp120v1v2区或与所述hivgp120v1v2区具有相同免疫原性且至少80%同源的氨基酸序列作为直接免疫原或者作为组合免疫原的一部分。
在一个实施方案中,所述艾滋病组合疫苗可以进一步包含可药用佐剂。所述可药用佐剂包括但不限于弗氏佐剂、氢氧化铝佐剂、mf59、as02a、qa-21、短小棒状杆菌、脂多糖、细胞因子、明矾、以及油佐剂或水型佐剂。此外,与组分(a)、(b)和(c)组合使用的可药用佐剂可以相同也可以不同。
本发明的艾滋病组合疫苗可通过例如注射方式进行接种,所述注射方式例如肌肉注射、皮下注射、皮内注射等。本领域技术人员可以利用本领域公知的技术对其进行配方,以使其适合相应靶点进行特异性抗体的诱导和相应的给药方式。
在第二方面,本发明提供了一种用于预防艾滋病的试剂盒,其包括:1)本发明第一方面的艾滋病组合疫苗;和2)接种所述艾滋病组合疫苗的说明书。可以在该说明书上注明该艾滋病组合疫苗的各组分的免疫顺序、免疫时间间隔以及免疫有效剂量等信息。
在第三方面,本发明提供了根据本发明第一方面的艾滋病组合疫苗在制备用于预防艾滋病的药物中的用途。
在第四方面,本发明提供了一种对受试者进行免疫接种用于预防艾滋病的方法,包括以下步骤:
i.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(a)组分和任选的可药用佐剂对所述受试者进行初次免疫(初免);
ii.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(b)组分和任选的可药用佐剂对所述受试者进行第一次加强免疫;并且
iii.用免疫有效量的本发明第一方面的艾滋病组合疫苗中的(c)组分和任选的可药用佐剂对所述受试者进行第二次加强免疫。
此处所提及的“免疫有效量”是指在给予受试者之后能够在该受试者体内产生足以预防某种疾病例如对于本发明是艾滋病的中和抗体的疫苗量。
在一个实施方案中,所述受试者可以是,例如人。
对于上述初次免疫、第一次加强免疫和第二次加强免疫,其可以进行一次或者多次,没有具体次数限制,只要能达到或者实现所需的技术效果即可。优选地,所述初次免疫可以进行一次、两次或者三次,优选三次。优选地,所述第一次加强免疫可以进行一次或者两次,优选地进行两次。优选地,所述第二次加强免疫可以进行一次或者两次,优选地进行两次。
在一个优选的实施方案中,在初次免疫两周之后进行第一次加强免疫。
在另一个优选实施方案中,在第一次加强免疫两周之后进行第二次加强免疫。
如上所述,本发明的艾滋病组合疫苗包含联合使用的三种组分,将这三种组分用于有序免疫机体,诱导识别天然构象v1v2的igg抗体产生增强,与igg竞争的hiv-1env特异性iga水平下降,并使杀伤感染靶细胞的adcc效应显著地提高,从而获得比现有的rv144疫苗更优异的艾滋病疫苗效果。本发明的方法及策略可普遍用于艾滋病疫苗的研发以及其它传染性疾病。
实施例
本发明通过下述实施例进一步阐明,但任何实施例或其组合不应当理解为对本发明的范围或实施方式的限制。本发明的范围由所附权利要求书限定,结合本说明书和本领域一般常识,本领域普通技术人员可以清楚地明白权利要求书所限定的范围。在不偏离本发明的精神和范围的前提下,本领域技术人员可以对本发明的技术方案进行任何修改或改变,这种修改和改变也包含在本发明的范围内。
实施例1.不同疫苗的v1v2特异性抗体对v1v2多肽的识别
假病毒包装:用vigofect(vigofectinc.beijing,china)转染试剂,按照说明,每9.6cm2的培养皿分别转染5μgjr-fl-env质粒(penv)和5μgpnl4-3质粒。转染8h后更换新的培养基。3天后收集上清液,3000rpm×10min离心去除细胞碎片,上清液假病毒分装存储于-80℃。具体制备方法可参考sun等人(7)。
hiv-1jr-fl假病毒经试剂盒纯化后透析到pbs,使用p24检测试剂盒检测定量,每次免疫所用假病毒为16μg/只,辅以等体积odncpg佐剂。v1v2多肽按照常规的免疫接种方法,每次免疫所用多肽为50μg/只,首先配制多肽溶液,使用等体积的弗氏佐剂混合乳化。利用jr-fl假病毒(制备方法如上所述)和hiv-1v1v2多肽(购自江苏海元蛋白生物技术有限公司,其序列为seqidno:3,货号为pjw4303/gp70v1v2-jrfl)免疫新西兰大白兔,每隔两周进行加强免疫,每次免疫前取血。经过5次免疫后,采集兔血清并用elisa测定抗体滴度。首先利用proteing柱材(gehealthcare,sweden)提取血清中的总igg,然后利用v1v2多肽特异性偶联柱材(gehealthcare,sweden)按说明书提取v1v2-特异性抗体。利用酶联免疫吸附法(elisa)测定经纯化的特异性抗体对v1v2多肽的结合。elisa的具体操作如下:利用包被液(0.05mnahco3,ph9.6)稀释v1v2多肽为5μg/ml,并按照50μl/孔在96孔elisa板上4℃包被过夜。利用洗液(0.05%吐温的pbs溶液)洗两遍包被板,然后使用2%的脱脂牛奶溶液200μl/孔封闭包被板,37℃孵育2h。将纯化的v1v2特异性igg抗体用pbs进行50μl体系的梯度稀释,然后加入该elisa板,37℃孵育1h后用洗液洗3遍,加入辣根过氧化物酶(hrp)标记的抗兔igg抗体(dako,glostrup,denmark)(1:2500),37℃孵育1h后用洗液洗5遍,再用四甲基联苯胺(tmb)配制的显色液显色。
结果如图3所示,在v1v2-特异性igg抗体的浓度为5μg/ml时,jr-fl假病毒免疫后纯化的特异性抗体(jrfl-v1v2ab)与v1v2多肽结合的od450值为1.2,而v1v2多肽免疫后纯化的特异性抗体(pep-v1v2ab)与v1v2多肽结合的od450值为1.28。可见,jrfl-v1v2ab和pep-v1v2ab这两种抗体都能够很好地结合v1v2多肽。
实施例2.不同的特异性抗体对天然构象hiv-1env的识别
将5mlhiv-1jr-fl活病毒原液加入4×106个cem.nkr.ccr5细胞,轻轻吹打约60次,然后将细胞和病毒混合液在37℃co2培养箱内孵育2h,其中每隔30min轻轻晃动重悬细胞。之后将细胞和病毒混合液加入适当体积含10%fbs的1640培养基,移入培养瓶置于37℃co2培养箱中培养。为了保证细胞代谢需要,及时补液,感染后第四天的细胞即为表达hiv-1jr-flenv的cem.nkr.ccr5靶细胞(以下称靶细胞)(参见bruel等人(6))。
将10μg/ml的jrfl-v1v2ab和pep-v1v2ab各100μl(含1%bsa)分别与106个cem.nkr.ccr5靶细胞混匀,室温孵育1h。然后1000rpm×3min离心收集细胞,用200μlpbs重悬细胞,离心弃上清,重复三次。然后加入100μl546红色荧光标记的抗兔igg抗体(lifetechnologies,america)(1:500)重悬,室温孵育半个小时。之后1000rpm×3min离心收集细胞,用200μlpbs重悬细胞,离心弃上清,重复三次。利用accuric6(bd)检测被荧光标记的细胞数量。
如图4所示,jrfl-v1v2ab较强地结合cem.nkr.ccr5靶细胞(14.9%),而pep-v1v2ab基本不结合cem.nkr.ccr5靶细胞(0.6%)。
实施例3.对不同的免疫组抗体中识别天然构象hiv-1env的v1v2特异性igg含量的比较
将新西兰大白兔分六组,每组三只,进行如下处理:第一组用pbs免疫五次,每两周免疫一次,每次免疫1ml/只;第二组利用hiv-1gp120单体免疫五次,配制高浓度的蛋白溶液,使用pbs将其稀释,然后与等体积的弗氏佐剂混合乳化,每两周免疫一次,每次免疫50μg/只;第三组利用hiv-1v1v2多肽(购自江苏海元蛋白生物技术有限公司,其序列为seqidno:3,货号为pjw4303/gp70v1v2-jrfl)免疫五次,使用pbs稀释多肽溶液,然后与等体积的弗氏佐剂混合乳化,每两周免疫一次,每次免疫50μg/只;第四组利用表达jr-flenv的质粒(penv)免疫三次,使用pbs稀释质粒溶液,然后与等体积的弗氏佐剂混合乳化,每三周免疫一次,每次免疫50μg/只,然后利用hiv-1gp120单体蛋白加强免疫四次,每两周免疫一次,每次免疫50μg/只;第五组利用表达jr-flenv的质粒(penv)免疫三次后,然后利用hiv-1v1v2多肽进行加强和选择免疫四次,免疫方法同上;第六组先利用表达jr-flenv的质粒(penv)免疫三次后,然后利用hiv-1gp120单体蛋白加强免疫两次,最后再利用hiv-1v1v2多肽进行加强和选择免疫两次,免疫方法同上。
免疫完成后,收集血清并纯化igg,然后利用v1v2多肽特异性偶联柱材按说明书提取v1v2特异性igg抗体。将从前述第一组至第六组获得的抗体分别以组别标记为pbs组(pbs免疫完成后纯化的特异性抗体)、gp120组(gp120单体蛋白免疫完成后纯化的特异性抗体)、v1v2组(v1v2多肽免疫后纯化的特异性抗体)、penv+gp120组(用表达jr-flenv的质粒初免、再用gp120单体蛋白增强免疫后纯化的特异性抗体)、penv+v1v2组(用表达jr-flenv的质粒初免、再用v1v2多肽增强选择免疫后纯化的特异性抗体)、penv+gp120+v1v2组(用表达jr-flenv的质粒初免、再用gp120单体蛋白增强免疫、最后用v1v2多肽增强选择免疫纯化的特异性抗体)。
将10μg/ml的上述六种抗体各100μl(含1%bsa稀释)分别与106个表达jr-flenv的cem.nkr.ccr5靶细胞混匀室温孵育1小时。然后1000rpm×3min离心收集细胞,用200μlpbs重悬,离心弃上清,重复三次。加入100μl546红色荧光标记的抗兔igg抗体(1:500)重悬,室温温育半个小时。然后1000rpm×3min离心收集细胞,用200μlpbs重悬,离心弃上清,重复三次。利用accuric6(bd)检测被荧光标记的细胞数量。
结果如图5所示,gp120组和v1v2组这两组的抗体都较难结合cem.nkr.ccr5靶细胞表面表达的jr-flenv,分别为21.2%和10.3%。而在使用表达env的质粒初免进行构象诱导、gp120单体蛋白加强后产生的抗体,即penv+gp120组抗体,结合cem.nkr.ccr5靶细胞表面表达的jr-flenv明显加强,为46.1%。另外,先使用表达env的质粒初免进行构象诱导、然后直接利用v1v2表位多肽进行选择和加强后产生的抗体,即penv+v1v2组抗体,结合cem.nkr.ccr5靶细胞表面表达的jr-flenv的效果相对于gp120组和v1v2组有所提高,但效果不是很明显,为32.6%。这可能是因为经构象诱导后,虽然产生了分泌识别env不同表位的抗体的淋巴细胞克隆,但是这些克隆数目很低,以至于直接利用特异性表位v1v2多肽诱导,没有产生明显的效果。但在使用表达env的质粒初免进行构象诱导后,利用gp120单体蛋白加强选择那些能够分泌识别gp120不同表位的抗体的淋巴细胞克隆,然后利用特异性抗体表位v1v2多肽进一步选择那些能够分泌识别gp120上v1v2区表位的抗体的细胞后产生的抗体,即penv+gp120+v1v2组的抗体,对在cem.nkr.ccr5靶细胞表面表达的jr-fl天然构象env的识别明显提高,达到65.3%。
实施例4.对不同的免疫组抗体中识别天然构象hiv-1env的iga含量的比较
上述新西兰大白兔免疫完成后(实施例3),检测其抗体滴度并收集血清。使用proteinl/agarose(invivogen,america)柱材,按照说明书纯化血清中的igg和iga,再使用proteing柱材(gehealthcare,sweden)将其中的igg去除,即为血清中的iga抗体。pbs组(pbs免疫完成后纯化的iga抗体)、gp120组(gp120单体蛋白免疫完成后纯化的iga抗体)、v1v2组(v1v2多肽免疫后纯化的iga抗体)、penv+gp120组(用表达jr-flenv的质粒初免、再用gp120单体蛋白增强免疫后纯化的iga抗体)、penv+v1v2组(用表达jr-flenv的质粒初免、再用v1v2多肽增强选择免疫后纯化的iga抗体)、penv+gp120+v1v2组(用表达jr-flenv的质粒初免、再用gp120单体蛋白增强免疫、最后用v1v2多肽增强选择免疫纯化的iga抗体)。
本发明人检测了这些血清中识别jr-flenv的iga的含量。具体如下:将10μg/ml的上述六种iga抗体100μl(含1%bsa)分别与106个cem.nkr.ccr5靶细胞混匀室温孵育1小时。然后1000rpm×3min离心收集细胞,用200μlpbs重悬,离心弃上清,重复三次。之后加入100μl异硫氰酸荧光素(fitc)标记的抗兔iga二抗(abcam,england)(1:500稀释)重悬细胞,室温温育半小时。1000rpm×3min离心收集细胞,用200μlpbs重悬,离心弃上清,重复三次。利用accuric6(bd)检测荧光标记的靶细胞数量。
结果如图6所示,直接利用gp120单体蛋白免疫(gp120组)可以诱导出高水平的识别表达在cem.nkr.ccr5靶细胞表面的jr-flenv的iga(19%)。而使用表达env的质粒初免进行构象诱导、再经gp120单体蛋白加强后,penv+gp120组iga抗体中存在结合在cem.nkr.ccr5靶细胞的iga,但相对只用gp120单体蛋白免疫有所降低,为10.3%,这跟临床数据相一致(3)。进一步地,使用表达env的质粒初免进行构象诱导、再直接利用v1v2表位多肽进行选择和加强后,penv+v1v2组iga抗体中结合表达在cem.nkr.ccr5靶细胞表面的jr-flenv的iga较低,为2%。这可能是因为经构象诱导后,虽然产生了分泌识别env不同表位的抗体的淋巴细胞克隆,但是这些克隆数目很低,加之v1v2多肽的表位单一,接着利用特异性表位免疫诱导可能会导致识别env的iga的量较低。但是在使用表达env的质粒初免进行构象诱导后,利用gp120单体蛋白加强选择那些能够分泌识别gp120不同表位的抗体的淋巴细胞克隆,然后利用特异性抗体表位v1v2多肽进一步选择加强免疫后,penv+gp120+v1v2组iga抗体中识别表达在cem.nkr.ccr5靶细胞表面env的iga的含量明显降低,为3.5%。这可能是由于经构象诱导后,虽然能够产生分泌识别env不同表位的抗体的淋巴细胞克隆,但是这些克隆数目很低;另外,虽然通过gp120单体蛋白选择能够识别针对gp120的免疫反应,但继续利用v1v2多肽选择和加强,识别其他env和gp120表位的免疫反应不能够持续,而识别v1v2表位的免疫反应得以增强,因此可能导致识别env的iga的量较低。
实施例5.对不同免疫组抗体对adcc效应的激活作用检测
上述新西兰大白兔经免疫后(实施例3),检测其抗体滴度并收集血清。如实施例1所述,首先从血清中纯化igg,然后利用v1v2多肽特异性偶联柱材按说明书纯化血清中的特异性抗体:pbs免疫后得到的特异性抗体(pbs组)、经表达jr-flenv的质粒(penv)初免再经gp120单体蛋白增强免疫后得到的特异性抗体(penv+gp120组)、经表达jr-flenv的质粒(penv)初免再经gp120单体蛋白增强免疫后最后经v1v2多肽增强选择免疫后得到的特异性抗体(penv+gp120+v1v2组)。检测这些特异性抗体激活adcc效应的能力。adcc被认为是rv144疫苗产生保护效应的关键因素,因此我们选用该指标来评估所设计的新型疫苗的效果。
在本发明中,我们选用了promega公司的adccreporterbioassaypropagationmodel(promega,madison,wi),该模型可以较好地检测抗体对adcc效应的激活作用。在nature子刊等文章也使用该模型来研究抗体的adcc效应(6,7)。抗体对adcc效应的激活能力可通过检测荧光值间接地检测,其对adcc效应的激活能力越强,其所激活的adcc效应越强,其对应的荧光值越高。
对抗体所具有的adcc效应激活能力的检测方案具体如下:纯化出血清中的igg之后,利用偶联v1v2多肽的nhs柱材纯化v1v2特异性抗体,过滤除菌以进行激活adcc效应的试验。将单核细胞(jurkatcells)细胞铺板于96孔板(500,000细胞/孔)。靶细胞为感染hiv-1jr-fl活病毒后表达hiv-1env的cem.nkr.ccr5靶细胞。靶细胞(10,000细胞/孔)和不同浓度的抗体(5μg/ml,15μg/ml,30μg/ml)室温孵育30min之后加入效应细胞。将细胞板300g×5min离心后,置于37℃5%co2培养箱孵育24h。细胞上清(100μl)被转移至空白板,并加入adccreporterbioassaypropagationmodel(promega)显色试剂,100μl/孔。infinitem200pro酶标仪检测其荧光值。
如图7所示,随着抗体浓度升高,所诱发的荧光值也越高。直接用pbs免疫后,产生的pbs组特异性igg抗体(浓度为30μg/ml)可以诱发一定的荧光值(rlu:9365),对adcc效应的激活作用极弱;经构象诱导再经gp120单体蛋白加强后,产生的penv+gp120组特异性igg抗体(浓度为30μg/ml)诱发的荧光值明显增强(rlu:520131),对adcc效应的激活作用提高;经构象诱导再经gp120单体蛋白加强,然后利用v1v2多肽进一步选择加强免疫后,产生的penv+gp120+v1v2组特异性igg抗体(浓度为30μg/ml)诱发的荧光值更进一步提高(rlu:754498),说明其对adcc效应的激活作用显著增强。
实施例6.对不同免疫组抗体的adcc效应检测
上述新西兰大白兔经免疫后(实施例3),检测其抗体滴度并收集血清。如实施例1所述,首先从血清中纯化igg,然后利用v1v2多肽特异性偶联柱材按说明书纯化血清中的特异性抗体:pbs免疫后得到的特异性抗体(pbs组)、经表达jr-flenv的质粒(penv)初免再经gp120单体蛋白增强免疫后得到的特异性抗体(penv+gp120组)、经表达jr-flenv的质粒(penv)初免再经gp120单体蛋白增强免疫后最后经v1v2多肽增强选择免疫后得到的特异性抗体(penv+gp120+v1v2组)。检测这些特异性抗体介导的adcc效应。adcc被认为是rv144疫苗产生保护效应的关键因素,因此我们选用该指标来评估所设计的新型疫苗的效果。
对抗体所具有的adcc效应的检测方案具体如下:纯化出血清中的igg之后,利用偶联v1v2多肽的nhs柱材纯化v1v2特异性抗体,过滤除菌以进行adcc试验。将外周血单核细胞(pbmc,全细胞)细胞铺板于96孔板(500,000细胞/孔),37℃孵育3h使细胞贴壁,之后用温育的pbs洗两遍以去除未贴壁的细胞,以贴壁的细胞作为效应细胞。靶细胞为感染hiv-1jr-fl活病毒后表达hiv-1env的cem.nkr.ccr5靶细胞。将cem.nkr.ccr5靶细胞(10,000细胞/孔)和不同浓度的抗体(1.67μg/ml,5μg/ml,15μg/ml)室温孵育30min之后加入效应细胞。将细胞板300g×5min离心后,置于37℃5%co2培养箱孵育12h。细胞上清(100μl)被转移至空白板,并加入cytotox-onetmhomogeneousmembraneintegrityassay(promega)显色试剂,100μl/孔。裂解细胞乳酸脱氢酶(ldh)产生的乳酸脱氢酶转换为细胞色素氧化酶底物产生荧光(刃天青),通过荧光计检测该荧光(ex560nm/em590nm)。计算特异性杀伤的比例:(实验组-空白对照)/(阳性对照-空白对照)×100%。用2μl裂解液(cytotox-onehomogeneousmembraneintegrityassaykit)单独处理靶细胞作为阳性对照,靶细胞和效应细胞作用不加抗体的处理作为阴性对照。如图8所示,随着抗体浓度升高,所诱发的荧光值也越高。直接用pbs免疫后,产生的pbs组特异性igg抗体(浓度为15μg/ml)杀伤靶细胞的比例为0.6654%,介导极弱的adcc效应;经构象诱导再经gp120单体蛋白加强后,产生的penv+gp120组特异性igg抗体(浓度为15μg/ml)杀伤靶细胞的比例为14.03%,说明其诱导的adcc效应提高;经构象诱导再经gp120单体蛋白加强后,然后利用v1v2多肽进一步选择加强免疫,产生的抗体penv+gp120+v1v2组特异性igg抗体(浓度为15μg/ml)杀伤靶细胞的比例为19.73%,说明其诱导的adcc效应显著增强。
综合adcc效应的检测结果,这可能是由于penv免疫的构象诱导再经gp120单体加强免疫后,增加了识别天然构象hiv-1env的v1v2特异性igg含量(图5),从而使其激活adcc效应的能力和介导的adcc效应提高;然后利用v1v2多肽进一步选择加强免疫后,所得penv+gp120+v1v2组特异性igg抗体识别天然构象的igg含量显著增加,其激活adcc效应的能力和介导的adcc效应也呈显著增强。该指标表明,本发明人所设计的疫苗可在体内诱导出具有更强adcc效应的抗体。
对于本领域技术人员而言显而易见的是,本发明并不限于上述示例的细节,在不背离本发明的精神和宗旨的情况下,本领域技术人员能够想到本文所描述技术方案的变化方案,并且该变化方案也在本发明的保护范围内。本发明的保护范围由随附权利要求所限定。
另外,应当理解,虽然本说明书通过实施方式来对本发明进行了描述,但是并非每个实施方式仅包含一个独立的技术方案。本说明书的这种叙述方案仅为清楚起见,本领域技术人员应当将本说明书当作一个整体,各个实施方式中的技术方案可以适当组合,形成本领域技术人员可以理解的其它实施方式。
参考文献:
1.dongxn,wuy,chenyh.2005.theneutralizingepitopeeldkwaonhiv-1gp41:geneticvariabilityandantigenicity.immunollett.101:81-6.
2.wangz,liuz,chengx,chenyh.2005.therecombinantimmunogenwithhigh-densityepitopesofeldkwaandeldewainducedantibodiesrecognizingbothepitopesonhiv-1gp41.microbiolimmunol.49:703-9.
3.rerks-ngarms,pitisuttithump,nitayaphans,kaewkungwalj,chiuj,parisr,premsrin,namwatc,desouzam,adamse.2009.vaccinationwithalvacandaidsvaxtopreventhivinfectioninthailand.nengljmed.361:2209-2220.
4.haynesbf,gilbertpb,mcelrathmj,zolla-pazners,tomarasgd,alamsm,evansdt,montefioridc,karnasutac,sutthentr.2012.immune-correlatesanalysisofanhivvaccineefficacytrial.nengljmed.366:1275-1286.
5.nicolel.yatesetal.vaccine-inducedenvv1-v2igg3correlateswithlowerhiv-1infectionriskanddeclinessoonaftervaccination.scitranslmed.2014,6,228ra39.
6.bruelt,guivel-benhassinef,amraouisetal.eliminationofhiv-1-infectedcellsbybroadlyneutralizingantibodies.natcommun2016;7:10844.
7.sun,z.,zhu,y.,wang,q.,ye,l.,dai,y.,su,s.,yu,f.,ying,t.,yang,c.,jiang,s,lu,l.animmunogencontainingfourtandem10e8epitoperepeatswithexposedkeyresiduesinducedantibodiestoneutralizehiv-1andtoactivateadccreportergene.emergmicrobinfect.2016.5:e65.
8.wang,j.,tong,p.,lu,l.,zhou,l.,xu,l.,jiang,s.,chen,y.h.(2010).hiv-1gp41corewithexposedmembrane-proximalexternalregioninducingbroadhiv-1neutralizingantibodies.plosone.6(3):e18233.
序列表
<110>复旦大学
<120>hiv疫苗及其制备方法
<130>cp20160446
<160>3
<170>patentinversion3.5
<210>1
<211>731
<212>prt
<213>1型人类免疫缺陷病毒(humanimmunodeficiencyvirustype1)
<400>1
metargvallysglyilearglyssertyrglntyrleutrplysgly
151015
glythrleuleuleuglyileleumetilecysseralavalglulys
202530
leutrpvalthrvaltyrtyrglyvalprovaltrplysglualathr
354045
thrthrleuphecysalaseraspalalysalatyraspthrgluval
505560
hisasnvaltrpalathrhisalacysvalprothraspproasnpro
65707580
glngluvalvalleugluasnvalthrgluhispheasnmettrplys
859095
asnasnmetvalgluglnmetglngluaspileileserleutrpasp
100105110
glnserleulysprocysvallysleuthrproleucysvalthrleu
115120125
asncyslysaspvalasnalathrasnthrthrasnaspserglugly
130135140
thrmetgluargglygluilelysasncysserpheasnilethrthr
145150155160
serileargaspgluvalglnlysglutyralaleuphetyrlysleu
165170175
aspvalvalproileaspasnasnasnthrsertyrargleuileser
180185190
cysaspthrservalilethrglnalacysprolysileserpheglu
195200205
proileproilehistyrcysalaproalaglyphealaileleulys
210215220
cysasnasplysthrpheasnglylysglyprocyslysasnvalser
225230235240
thrvalglncysthrhisglyileargprovalvalserthrglnleu
245250255
leuleuasnglyserleualagluglugluvalvalileargserasp
260265270
asnphethrasnasnalalysthrileilevalglnleulysgluser
275280285
valgluileasncysthrargproasnasnasnthrarglysserile
290295300
hisileglyproglyargalaphetyrthrthrglygluileilegly
305310315320
aspileargglnalahiscysasnileserargalalystrpasnasp
325330335
thrleulysglnilevalilelysleuarggluglnphegluasnlys
340345350
thrilevalpheasnhisserserglyglyaspprogluilevalmet
355360365
hisserpheasncysglyglygluphephetyrcysasnserthrgln
370375380
leupheasnserthrtrpasnasnasnthrgluglyserasnasnthr
385390395400
gluglyasnthrilethrleuprocysargilelysglnileileasn
405410415
mettrpglngluvalglylysalamettyralaproproilearggly
420425430
glnileargcysserserasnilethrglyleuleuleuthrargasp
435440445
glyglyileasngluasnglythrgluilepheargproglyglygly
450455460
aspmetargaspasntrpargsergluleutyrlystyrlysvalval
465470475480
lysilegluproleuglyvalalaprothrlysalalysargargval
485490495
valglnargglulysargalavalglyileglyalavalpheleugly
500505510
pheleuglyalaalaglyserthrmetglyalaalasermetthrleu
515520525
thrvalglnalaargleuleuleuserglyilevalglnglnglnasn
530535540
asnleuleuargalaileglualaglnglnargmetleuglnleuthr
545550555560
valtrpglyilelysglnleuglnalaargvalleualavalgluarg
565570575
tyrleuglyaspglnglnleuleuglyiletrpglycysserglylys
580585590
leuilecysthrthralavalprotrpasnalasertrpserasnlys
595600605
serleuaspargiletrpasnasnmetthrtrpmetglutrpgluarg
610615620
gluileaspasntyrthrsergluiletyrthrleuileglugluser
625630635640
glnasnglnglnglulysasngluglngluleuleugluleuasplys
645650655
trpalaserleutrpasntrppheaspilethrlystrpleutrptyr
660665670
ilelysilepheilemetilevalglyglyleuvalglyleuargleu
675680685
valphethrvalleuserilevalasnargvalargglnglytyrser
690695700
proleuserpheglnthrleuleuproalaproargglyproasparg
705710715720
progluglyilegluglugluglyglygluarg
725730
<210>2
<211>470
<212>prt
<213>1型人类免疫缺陷病毒(humanimmunodeficiencyvirustype1)
<400>2
leutrpvalthrvaltyrtyrglyvalprovaltrplysglualathr
151015
thrthrleuphecysalaseraspalalysalatyraspthrgluval
202530
hisasnvaltrpalathrhisalacysvalprothraspproasnpro
354045
glngluvalvalleugluasnvalthrgluhispheasnmettrplys
505560
asnasnmetvalgluglnmetglngluaspileileserleutrpasp
65707580
glnserleulysprocysvallysleuthrproleucysvalthrleu
859095
asncyslysaspvalasnalathrasnthrthrasnaspserglugly
100105110
thrmetgluargglygluilelysasncysserpheasnilethrthr
115120125
serileargaspgluvalglnlysglutyralaleuphetyrlysleu
130135140
aspvalvalproileaspasnasnasnthrsertyrargleuileser
145150155160
cysaspthrservalilethrglnalacysprolysileserpheglu
165170175
proileproilehistyrcysalaproalaglyphealaileleulys
180185190
cysasnasplysthrpheasnglylysglyprocyslysasnvalser
195200205
thrvalglncysthrhisglyileargprovalvalserthrglnleu
210215220
leuleuasnglyserleualagluglugluvalvalileargserasp
225230235240
asnphethrasnasnalalysthrileilevalglnleulysgluser
245250255
valgluileasncysthrargproasnasnasnthrarglysserile
260265270
hisileglyproglyargalaphetyrthrthrglygluileilegly
275280285
aspileargglnalahiscysasnileserargalalystrpasnasp
290295300
thrleulysglnilevalilelysleuarggluglnphegluasnlys
305310315320
thrilevalpheasnhisserserglyglyaspprogluilevalmet
325330335
hisserpheasncysglyglygluphephetyrcysasnserthrgln
340345350
leupheasnserthrtrpasnasnasnthrgluglyserasnasnthr
355360365
gluglyasnthrilethrleuprocysargilelysglnileileasn
370375380
mettrpglngluvalglylysalamettyralaproproilearggly
385390395400
glnileargcysserserasnilethrglyleuleuleuthrargasp
405410415
glyglyileasngluasnglythrgluilepheargproglyglygly
420425430
aspmetargaspasntrpargsergluleutyrlystyrlysvalval
435440445
lysilegluproleuglyvalalaprothrlysalalysargargval
450455460
valglnargglulysarg
465470
<210>3
<211>85
<212>prt
<213>1型人类免疫缺陷病毒(humanimmunodeficiencyvirustype1)
<400>3
glythrvallysleuthrproleucysvalthrleuasncyslysasp
151015
valasnalathrasnthrthrasnaspsergluglythrmetgluarg
202530
glygluilelysasncysserpheasnilethrthrserileargasp
354045
gluvalglnlysglutyralaleuphetyrlysleuaspvalvalpro
505560
ileaspasnasnasnthrsertyrargleuilesercysaspthrser
65707580
valilethrglnala
85
- 还没有人留言评论。精彩留言会获得点赞!