大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制作方法
本发明涉及药物领域,具体而言,涉及一种大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物。
背景技术:
大驳骨为双子叶植物爵床科爵床属植物黑叶小驳骨(justiciaventricosawall.exsims.)的干燥全草,全年均可采收。黑叶小驳骨又名大驳骨,黑叶爵床、黑叶接骨草、大接骨、大驳骨丹、鸭仔花、逼迫树、大驳节等。其味辛;苦;性平。具有活血止痛;化瘀接骨;祛风除湿;消肿解毒。主治跌打伤肿;骨折;劳伤腰痛;风湿痹痛;胃气痛;肺痈;乳痈;无名肿毒;外伤红肿。有关大驳骨的药用记载,始见于《本草求原》,《陆川本草》等古籍亦有记载,《岭南采药录》,《南宁市药物志》,广州空军《常用中草药手册》等地方本草专著及全国性大型中药专著《中华本草》、《中药大辞典》、《中华药海》等均有收载,广西省中药材标准(1990年版),广东省中药材标准(2011年)和中华人民共和国卫生部药品标准中药成方制剂第八册,第十一册,第十九册,第二十册和国家中成药标准汇编骨伤科分册收载。
技术实现要素:
本发明的目的在于提供一种大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物,其旨在提供一种用于制备治疗中枢神经变性疾病药剂的药物;提供一种大驳骨的新的用途。
本发明提供一种技术方案:
大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用。
进一步地,上述大驳骨的提取物在制备预防和/或治疗神经退行性疾病的药物中的应用;
大驳骨的提取物主要通过以下步骤制得:将大驳骨采用溶剂进行提取,提取后分离得到提取液;其中,大驳骨与溶剂的重量比为1:5~20。
进一步地,上述神经退行性疾病包括帕金森病、阿尔兹海默病、亨廷顿病和tau蛋白病中的至少一种。
本发明还提供一种技术方案:
一种预防和/或治疗神经退行性疾病的药物,用于制备预防和/或治疗神经退行性疾病的药物,药物主要由包括大驳骨的原料制成。
进一步地,上述药物主要通过以下步骤制得:将大驳骨采用溶剂进行提取,提取后分离得到提取液;其中,大驳骨与溶剂的重量比为1:5~20。
进一步地,上述溶剂选自水、甲醇、乙醇、异丙醇、1-丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,3-丁二醇、丙酮、乙酸乙酯中的一种或者多种。
进一步地,上述溶剂为质量分数为30-95%乙醇水溶液。
进一步地,上述将大驳骨在30-90℃下超声提取15-60min。
进一步地,上述分离得到提取液后还包括对提取液浓缩、干燥。
进一步地,上述对提取液进行蒸发浓缩、减压浓缩或者膜浓缩;对浓缩后的提取液进行常压干燥、减压干燥、真空冷冻干燥或者喷雾干燥。
本发明提供的大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的有益效果是:
发明人发现大驳骨及其提取物新的用途,可以预防中枢神经元发生变性、凋亡;含有大驳骨的药物能够使ht-22神经细胞保持健康形态和增殖,保护ht-22神经细胞,抑制ht-22神经细胞的凋亡。本发明提供的药物在制备治疗、辅助治疗或预防神经退行性疾病的药物中具有较好的疗效。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
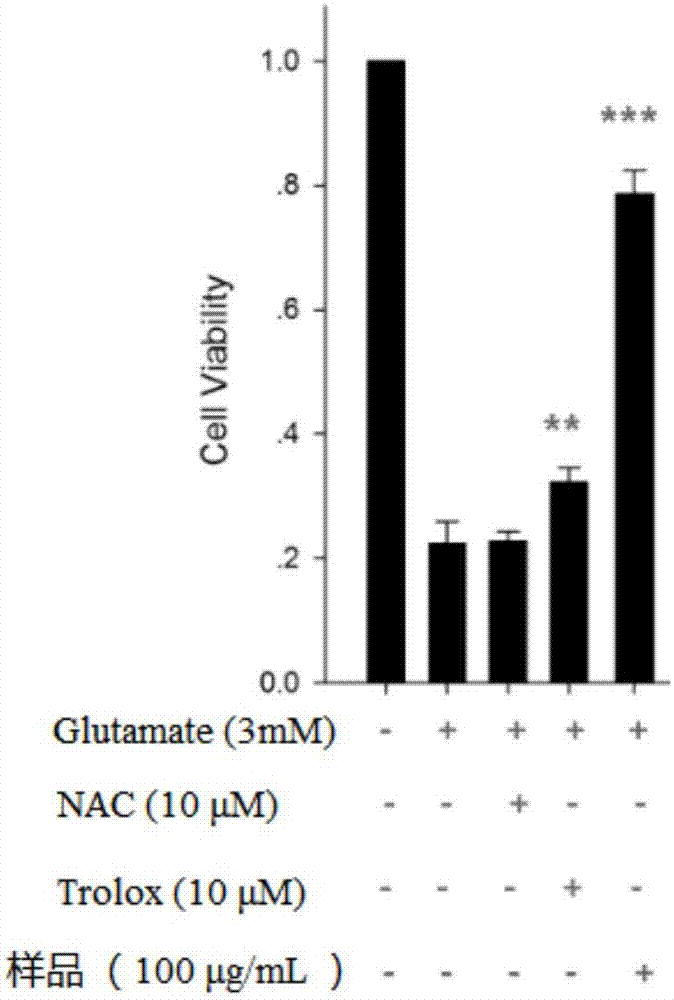
图1显示了mtt法检测的实施例1提供的药物对l-glutamate诱导ht-22细胞的保护作用。
图2显示了显微镜下观察的实施例1提供的药物对l-glutamate诱导ht-22细胞的保护作用。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
下面对本发明实施例的大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物进行具体说明。
进一步地,上述神经退行性疾病为中枢神经变性疾病。
进一步地,上述大驳骨的提取物在制备预防和/或治疗神经退行性疾病的药物中的应用;
大驳骨的提取物主要通过以下步骤制得:将大驳骨采用溶剂进行提取,提取后分离得到提取液;其中,大驳骨与溶剂的重量比为1:5~20。进一步地,大驳骨与溶剂的重量比为1:10-15。
上述溶剂选自水、甲醇、乙醇、异丙醇、1-丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,3-丁二醇、丙酮、乙酸乙酯中的一种或者多种。
进一步地,上述神经退行性疾病包括帕金森病、阿尔兹海默病、亨廷顿病和tau蛋白病中的至少一种。具体地,tau蛋白病包括额颞痴呆、皮层基底节变性、皮克氏病、进行性核上性麻痹等。
在本发明的其他实施例中,上述神经退行性疾病也包括威尔逊氏病、朊病毒病及其他痴呆包括血管性痴呆、肌萎缩侧索硬化(als)、急性中风(脑中风引起的神经损伤)及其他外伤性损伤;脑血管意外(如,年龄相关性黄斑变性);脑和脊髓外伤、周围神经病、视网膜病和青光眼。
中枢神经变性疾病是一组以中枢神经系统神经元逐渐发生变性、凋亡所导致的神经退行性疾病或神经病症。其病因大多不明,发病机制和病理表现复杂,临床表现各异。该组疾病多见于中老年,呈慢性或亚急性起病,进行性加重,病程较长,且多数疾病和病症之间相互重叠,如10%左右的帕金森病合并痴呆,太平洋关岛的阿尔茨海默、帕金森综合征等。由于缺乏特异的生化、影像学和病理生理学特征,往往主要依靠临床医生的经验作出诊断。除少数疾病(如帕金森病)依靠药物或手术可能暂时改善临床症状外,对大多数疾病目前尚无特效的治疗方法。例如缺血性中风的治疗策略主要包括溶栓治疗和神经保护治疗。溶栓药物阿替普酶(rt-pa)是首个也是迄今为止唯一被fda批准用于治疗中风的溶栓药物。尽管rt-pa已经被证实能有效治疗急性缺血性中风,但其治疗时间窗窄,作用机理不明确,有出血风险,因此只有少数病人能够及时接受rt-pa的有效治疗。复方左旋多巴是治疗pd的首选药物,但患者长期服用会出现开关现象、剂末恶化等严重并发症。因此开展神经保护性治疗,可能推迟发病时间或延缓病情的发展,已成为当前研究的热点。
神经保护治疗是通过阻碍缺血级联反应涉及的一种或多种机制,在初始阶段保护缺血引起的半暗带神经元损伤,从而阻止或延迟神经细胞死亡。可以通过药物实现血液迅速回流入缺血组织,从而抑制缺血所引起的生化水平、代谢水平和细胞水平上的损害。脑缺血触发了复杂的病理生化级联反应,神经保护治疗的途径多样,环节不同,神经保护的前景是很可观的。
经过发明人的研究以及探讨发现,大驳骨在制备治疗、辅助治疗或预防神经退行性疾病的药物中具有较好的疗效。大驳骨对中枢神经元逐渐发生变性、凋亡具有疗效。大驳骨有助于保护神经细胞免受细胞损伤和/或抵抗神经变性过程以及神经元功能损害的治疗剂或活性物质。
本发明还提供一种技术方案:
一种预防和/或治疗神经退行性疾病的药物,药物主要由包括大驳骨的原料制成。
进一步地,上述药物主要通过以下步骤制得:将大驳骨采用溶剂进行提取,提取后分离得到提取液;其中,大驳骨与溶剂的重量比为1:5~20。
进一步地,上述溶剂选自水、甲醇、乙醇、异丙醇、1-丁醇、乙二醇、1,2-丙二醇、1,3-丙二醇、1,3-丁二醇、丙酮、乙酸乙酯中的一种或者多种。
进一步地,上述溶剂为质量分数为30-95%乙醇水溶液。在本实施例中,为质量分数95%的乙醇水溶液。
进一步地,上述将大驳骨在30-90℃下超声提取15-60min。
进一步地,上述分离得到提取液后还包括对提取液浓缩、干燥。
进一步地,上述对提取液进行蒸发浓缩、减压浓缩或者膜浓缩;具体地,采用减压浓缩。在本发明较佳的实施例中,采用旋转蒸发仪蒸发浓缩。
对浓缩后的提取液进行常压干燥、减压干燥、真空冷冻干燥或者喷雾干燥。对浓缩后的提取液进行常压干燥、减压干燥、真空冷冻干燥或者喷雾干燥。具体地,在本发明中采用减压干燥。
大驳骨对中枢神经元逐渐发生变性、凋亡具有疗效。大驳骨的提取物或者药物具有保护神经元损伤,从而阻止或延迟神经细胞死亡的效果;能推迟发病时间或延缓病情的发展。大驳骨制备的药物能够细胞保持健康形态和增殖,抑制细胞凋亡;该药物对于神经细胞具有显著的保护作用。
此外,在其他实施例中,该药物还包括药学上可接受的载体或辅料。
例如:稀释剂与吸收剂,如淀粉、糊精、硫酸钙、乳糖、甘露醇、蔗糖、氯化钠、葡萄糖、尿素、碳酸钙、白陶土、微晶纤维素、硅酸铝等;湿润剂与粘合剂,如水、甘油、聚乙二醇、乙醇、丙醇、淀粉浆、糊精、糖浆、蜂蜜、葡萄糖溶液、阿拉伯胶浆、明胶浆、羧甲基纤维素钠、紫胶、甲基纤维素、磷酸钾、聚乙烯吡咯烷酮等;崩解剂,例如干燥淀粉、海藻酸盐、琼脂粉、褐藻淀粉、碳酸氢钠与枸橼酸、碳酸钙、聚氧乙烯、山梨糖醇脂肪酸酯、十二烷基磺酸钠、甲基纤维素、乙基纤维素等;崩解抑制剂,例如蔗糖、三硬脂酸甘油酯、可可脂、氢化油等;吸收促进剂,例如季铵盐、十二烷基硫酸钠等;润滑剂,例如滑石粉、二氧化硅、玉米淀粉、硬脂酸盐、硼酸、液体石蜡、聚乙二醇等。还可以将片剂进一步制成包衣片,例如糖包衣片、薄膜包衣片、肠溶包衣片,或双层片和多层片。
此外,为了将给药单元制成丸剂,可以广泛使用本领域公知的各种载体。如:葡萄糖、乳糖、淀粉、可可脂、氢化植物油、聚乙烯吡咯烷酮、gelucire、高岭土、滑石粉等;粘合剂如阿拉伯胶、黄蓍胶、明胶、乙醇、蜂蜜、液糖、米糊或面糊等;崩解剂,如琼脂粉、干燥淀粉、海藻酸盐、十二烷基磺酸钠、甲基纤维素、乙基纤维素等。为了将给药单元制成栓剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如聚乙二醇、卵磷脂、可可脂、高级醇、高级醇的酯、明胶、半合成甘油酯等。
此外,如需要,也可以向药物制剂中添加着色剂、防腐剂、香料、矫味剂、甜味剂或其它材料。
进一步地,本发明实施例的药物可以单位剂量形式给药,给药途径可为肠道或非肠道,如口服、肌肉、皮下、鼻腔、口腔粘膜、皮肤、腹膜或直肠等。给药剂型例如片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、脂质体、透皮剂、口含片、栓剂、冻干粉针剂等。可以是普通制剂、缓释制剂、控释制剂及各种微粒给药系统。为了将单位给药剂型制成片剂,可以广泛使用本领域公知的各种载体。
此外,本发明实施例的药物的给药剂量取决于许多因素,例如所要预防或治疗疾病的性质和严重程度,患者或动物的性别、年龄、体重及个体反应,所用的具体化合物,给药途径及给药次数等。上述剂量可以单一剂量形式或分成几个,例如二、三或四个剂量形式给药。
承上所述,在给药过程中,可改变药物组合物中各活性成分的实际剂量水平,以便所得的活性化合物量能有效针对具体患者、组合物和给药方式得到所需的治疗反应。剂量水平须根据具体化合物的活性、给药途径、所治疗病况的严重程度以及待治疗患者的病况和既往病史来选定。但是,本领域的做法是,化合物的剂量从低于为得到所需治疗效果而要求的水平开始,逐渐增加剂量,直到得到所需的效果。
发明人发现大驳骨及其提取物新的用途,可以预防中枢神经元发生变性、凋亡;含有大驳骨的药物能够使ht-22神经细胞保持健康形态和增殖,保护ht-22神经细胞,抑制ht-22神经细胞的凋亡。本发明提供的药物在制备治疗、辅助治疗或预防神经退行性疾病的药物中具有较好的疗效。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例提供一种药物,该药物主要由以下步骤制备:
称取大驳骨30g,置于三角瓶中,向三角瓶中加入300ml95%乙醇水溶液,于60℃超声提取30min,过滤,用旋转蒸发仪浓缩成浸膏状后置于蒸发皿中蒸干,于恒温烘箱内(50℃)烘至恒重。
实施例2
本实施例提供一种药物,该药物主要由以下步骤制备:
称取大驳骨10g,置于三角瓶中,向三角瓶中加入50ml30%乙醇水溶液,于30℃超声提取15min,过滤,减压浓缩成浸膏状后置于蒸发皿中蒸干,于恒温烘箱内(50℃)烘至恒重。
实施例3
本实施例提供一种药物,该药物主要由以下步骤制备:
称取大驳骨10g,置于三角瓶中,向三角瓶中加入200ml60%1,2-丙二醇水溶液,于90℃超声提取60min,过滤,减压浓缩成浸膏状后真空冷冻干燥至恒重。
实施例4
本实施例提供一种药物,该药物主要由以下步骤制备:
称取大驳骨10g,置于三角瓶中,向三角瓶中加入100ml乙酸乙酯,于60℃超声提取45min,过滤,膜浓缩后减压干燥至恒重。
实施例5
本实施例提供一种药物,该药物主要由以下步骤制备:
称取大驳骨10g,置于三角瓶中,向三角瓶中加入150ml水,于45℃超声提取60min,过滤,用旋转蒸发仪浓缩成浸膏状后置于蒸发皿中蒸干,于恒温烘箱内(50℃)烘至恒重。
试验例
本试验例对实施例1得到的药物进行神经保护测试。
1.ht-22神经细胞的培养
将(三批)ht-22细胞用胰酶(0.25%,1ml)从中皿消化下来(1min内),吹散成单细胞悬液,加入少量胎牛血清fbs(100μl)。1000rpm离心5min,去上清,将细胞沉淀分散在3ml完全培养基中,取1ml细胞悬液加入到24ml完全培养基中,来回颠倒10次混匀,取0.1ml用于计数。稀释至适当的细胞浓度(8×104cell/ml)后,48孔板先加50μl培养基,使培养基彻底分布于孔板边缘。种植在48孔板中(三批细胞三块板,100μl,8×104cell/ml)。边种边旋转离心管,种一半孔用力吹打细胞,使之均匀,同时让细胞悬液铺满孔板底部,全部种完后在显微镜下观察细胞分散是否均匀,十字摇匀使细胞在孔板底部分散均匀。放置24小时(细胞融合度约为30~40%)用于实验。
2.mtt法测试
将实施例1中获得药物200μg分散于2ml完全培养基中,用于3×48孔板换液,做mtt实验。取种好细胞的48孔板,分为control(对照组),glutamate(谷氨酸)组,nac(n-acetylcysteine)(n-乙酰半胱氨酸)组,trolox(水溶性维生素e)组和样品组(实施例1提供的药物组)。每组三个复孔,培养基换液,每孔200μl,每次换液前,吹打培养基,使药物分散均匀。换液完37℃孵育1h后加入谷氨酸使终浓度达到3mm(6μl)。摇匀后放置在37℃培养24h。观察细胞形态,并检测细胞存活率(mtt法),然后用20μl的mtt(5mg/ml)避光37℃孵育2h,轻轻吸去液体,每孔加200μl的dmso,摇床5min摇匀。然后用多功能酶标仪计算490nm下各吸光值(下面图中数据均为490nm下测得,损伤组细胞存活率约为control组的20%)。取三孔od值,求平均值,减去空白dmso的od值,然后除以对照组的平均值标准化。三批细胞的mtt的od值的平均值用sigmaplot12.5软件做统计差异。
统计结果如表1所示,表1示出了control组、glutamate组、nac组,trolox组和样品组中细胞存活率。
表1各实验组细胞存活率对比(
将表1中的实验数据绘制柱状图,结果如图1所示,具体地,图1显示了mtt法检测的大驳骨提取物对l-glutamate诱导ht-22细胞的保护作用。图中:“+”代表相应的试验组有相应的组分,“-”代表相应的试验组没有相应的组分。其中,**p<0.01,***p<0.001与谷氨酸组比较(单因素方差分析,dunnett法)。trolox(10μm)作为阳性对照使用。
由图1的结果显示,实施例1提供的药物对于ht-22神经细胞具有显著的保护作用。
3.显微镜下观察的大驳骨提取物的保护作用
实施例1提供的药物20μg分散于2ml完全培养基中,用于3×48孔板换液。取种好细胞的48孔板,分别是control组,glutamate组,glu(glutamate)+nac(n-acetylcysteine)组,glu+trolox和glu+样品组(实施例1提供的药物组),每组三个复孔,培养基换液,每孔200μl,每次换液前,吹打培养基,使药物分散均匀。换液完37℃孵育1h后加入谷氨酸使终浓度达到3mm(6μl)。摇匀后放置在37℃培养24h。最后在显微镜下观察细胞形态,并拍照,结果如图2所示。图2显示了显微镜下观察的大驳骨提取物对l-glutamate诱导ht-22细胞的保护作用。由图2可知,实施例1提供的药物可以使细胞保持健康形态和增殖,抑制了l-glutamate(l-谷氨酸)引起的细胞凋亡。
从本实验例可知,实施例1提供的药物能够细胞保持健康形态和增殖,抑制细胞凋亡;该药物对于ht-22神经细胞具有显著的保护作用。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- SeZn7MT3的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 纤维支架材料、其制备方法、及亚甲蓝负载量的调节方法与流程
- 大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 花叶假杜鹃在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 大脑内稳态调节蛋白的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 一种药物组合物及其制备方法和在制备防治神经退行性疾病的药物中的应用与流程
- 片层碳‑四氧化三铁复合体在抑制Aβ聚集中的应用的制造方法与工艺
- 一种干细胞球切割收集装置及干细胞球的切割分离传代方法与流程
- 一种具有改善记忆功效的多肽及其分离制备方法和应用与制造工艺
- 治疗或预防神经退行性病症的组合物和方法与制造工艺
- SeZn7MT3的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 纤维支架材料、其制备方法、及亚甲蓝负载量的调节方法与流程
- 大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 花叶假杜鹃在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 大脑内稳态调节蛋白的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 一种药物组合物及其制备方法和在制备防治神经退行性疾病的药物中的应用与流程
- 片层碳‑四氧化三铁复合体在抑制Aβ聚集中的应用的制造方法与工艺
- 一种干细胞球切割收集装置及干细胞球的切割分离传代方法与流程
- 一类抗氧化超短肽及其应用的制造方法与工艺
- 一种具有改善记忆功效的多肽及其分离制备方法和应用与制造工艺