一种基于3D打印的仿生软骨及其制造方法与流程
本发明属于生物医学工程技术领域,特别是涉及一种基于3d打印的仿生软骨及其制造方法。
背景技术:
由创伤或疾病造成的软骨退变或损伤在临床上较为常见,但由于关节软骨组织的特殊,内部没有血管、淋巴管和神经,创伤性损伤后只有极低或几乎没有有效的自修复能力,若治疗不及时或恰当,将导致严重的功能障碍。与其他的组织修复过程相同,软骨修复是通过纤维蛋白凝块的形成和随后缺损损周围的正常软骨、缺损下方的骨髓或者滑膜组织来源的成软骨细胞的级联反应,最终形成受损部位的修复组织。现有的几种软骨修复技术如软骨下钻孔、清理钻孔术或者微骨折,都是缺损接近软骨下有血供的组织和骨髓,通常联合应用清除软骨碎片,磨损关节成型和关节冲洗等操作。但传统技术是通过纤维软骨样组织修复软骨缺损,在成分构成、结构和力学性质方面,这种修复组织与正常软骨不同(正常关节软骨主要由透明软骨构成,作为缓冲垫抵抗外来应力),因而无法预测软骨修复的长期临床效果。通过传统方式治疗的患者,都会有一个短暂的疼痛缓解期;但是当修复组织发生退变,患者会出现进展性的症状。用适当的软骨填充材料修复缺陷,是快速恢复病态的或创伤性软骨缺损组织的有效方法。软骨组织工程为软骨损伤的治疗提供了一种理想的治疗途径,但是现有的技术难以制备出一种与正常软骨组织生理结构和生理性能相近的高质量的软骨修复材料,有许多问题有待解决,如新生软骨组织的固定、同种异体细胞移植后的免疫排斥反应、种子细胞和生长因子的选择,如何解决培养软骨的远期退化、是否能够忍受长期的负载和摩擦等等。
而近年来,研究者对组织工程支架的设计提出了4f准则:形状诉求(form)、性能诉求(function)、功能诉求(formation)和可植入性(fixation)。形状诉求是指支架材料必须能够完全填充复杂的三维缺陷,并且可以诱导组织再生;性能诉求是指支架的力学性能等可以在缺失组织修复前暂时起到缺失组织作用的需求;功能诉求是指材料需具有相应的生物活性,能够为细胞提供适宜的环境以促进组织再生;可植入性是指支架可通过手术植入人体,并起到预期功效。利用仿生学,体外构建适合组织细胞生长的显微结构,模拟体内环境,协调不同细胞的增殖、分化、迁移和凋亡等,是治疗组织缺损的发展方向。
利用3d打印技术制备的个性化支架,能够精确模拟天然组织复杂的三维微观结构,支架形状与缺损组织高度吻合,并能通过支持生长因子、细胞的共同打印赋予支架生物活性,通过梯度打印的方法模拟正常组织的生理结构,从而制备出一种与正常组织在结构和生理功能上无异的修复材料,是组织工程领域发展的必然趋势。
技术实现要素:
本发明的首要目的在于克服现有技术的缺点与不足,一种基于3d打印的仿生软骨的制备方法。
本发明的另一目的在于提供通过上述制备方法得到的一种基于3d打印的仿生软骨,其特征在于,所述的仿生软骨按重量份数计由改性ⅱ型胶原蛋白20-80份、改性透明质酸20-80份、纳米羟基磷灰石10-20份和软骨细胞0.1-0.5份通过梯度仿生3d打印所制得。
进一步的,所述仿生软骨由下至上依次由仿生软骨下骨、仿生钙化层、仿生软骨深层、仿生中间层和仿生浅表层通过3d打印机打印构建所得,整体呈多层的互穿网络结构。
所述的一种基于3d打印的仿生软骨及其制造方法,具体包括如下步骤;
(1)打印材料的制备:
①改性ⅱ型胶原蛋白的制备:将ⅱ型胶原蛋白加入到50℃的pbs磷酸盐中配制成质量浓度为10%的溶液,然后按体积比vⅱ型胶原蛋白pbs磷酸盐溶液:v甲基丙烯酸酐=10:0.75加入甲基丙烯酸酐在,50℃下搅拌反应4小时,反应结束后,将所得溶液置于截留分子量为10000的透析袋中透析7天,然后将得到的透析液置于-80℃冷冻干燥机中冷冻干燥48小时,即得改性ⅱ型胶原蛋白,置于室温下存储,备用;
②改性透明质酸的制备:将透明质酸溶解于蒸馏水中配制成质量浓度为2%的透明质酸溶液,然后加入摩尔浓度为1mol/l的氢氧化钠溶液调节溶液的ph至8.5得到透明质酸钠溶液,然后按质量比m透明质酸钠:m甲基丙烯酸二甲氨基乙酯=1:3.5加入甲甲基丙烯酸二甲氨基乙酯,在10℃下反应24h后,将所得溶液置于截留分子量为14000的透析袋中流水透析7天,然后将透析液置于-80℃冷冻干燥机中冷冻干燥48小时,即得改性透明质酸,置于室温下存储,备用;
③将软骨细胞消化后,加入到含有体积分数为10%的牛血清的软骨细胞培养基中,配制成细胞浓度为1×106—5×106ml-1的软骨细胞悬浮液,置于二氧化碳浓度为5%,温度为37℃的细胞培养箱中备用;所述软骨细胞为正常培养3代后的软骨细胞;
(2)各仿生层前驱体的制备:
①仿生软骨下骨前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,然后加入纳米羟基磷灰石,搅拌至纳米羟基磷灰石均匀分散在溶液中,得到仿生软骨下骨前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、纳米羟基磷灰石的浓度为5-10wt%,改性ⅱ型胶原蛋白的浓度为5-10wt%;
②仿生钙化层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸,每次加入的物质完全溶解后再加入下一种物质,然后加入纳米羟基磷灰石,搅拌至纳米羟基磷灰石均匀分散在溶液中,得到仿生钙化层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、纳米羟基磷灰石的浓度为1-5wt%,改性透明质酸的浓度为1-3wt%;
③仿生软骨深层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,然后加入等体积的步骤(1)所配制的软骨细胞悬浮液,轻柔搅拌至混合均匀,得到仿生软骨深层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性透明质酸的浓度为1-3wt%,改性ⅱ型胶原蛋白的浓度为10-15wt%,软骨细胞的浓度为5×105—2.5×106ml-1;
④仿生中间层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,得到仿生中间层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性透明质酸的浓度为2-5wt%,改性ⅱ型胶原蛋白的浓度为10-15wt%;
⑤仿生浅表层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,得到仿生浅表层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性ⅱ型胶原蛋白的浓度为10-15wt%;
(3)仿生软骨的仿生打印:
将步骤(2)制备所得的各仿生层前驱体按仿生软骨下骨前驱体、仿生钙化层前驱体、仿生软骨深层前驱体、仿生中间层前驱体、仿生浅表层前驱体的顺序
依次叠加打印,其中所述仿生软骨下骨的打印厚度设置为仿生软骨总厚度的5~10%、所述仿生钙化层的打印厚度设置为仿生软骨总厚度的2~5%、所述仿生软骨深层的打印厚度设置为仿生软骨总厚度的15~30%、所述仿生中间层的打印厚度设置为仿生软骨总厚度的40~55%、所述仿生浅表层的打印厚度设置为仿生软骨总厚度的10~20%,即得一种基于3d打印的仿生软骨;
优选的,所述的ⅱ型胶原蛋白的分子量为1×106kda;
优选的,所述的透明质酸的分子量为1.2~1.5×106kda;
优选的,所述的纳米羟基磷灰石,其粒径分布范围为150-250nm;
优选的,所述的所述的仿生软骨的仿生打印,采用3dsystems公司型号为3dsystemsprox800的立体光固化成型法3d打印机进行打印,设置每层仿生层的紫外光照射时间为30s,紫外光照射强度为10mw/cm2;
本发明的有益效果为:
(1)本发明公开的仿生软骨具有免疫原性低,原材料丰富,具有良好的生物相容性,良好的力学性能和血管化能力的优点。
(2)本发明以改性ⅱ型胶原蛋白、改性透明质酸、纳米羟基磷灰石和软骨细胞为基质,制备出3d仿生打印材料,然后利用三维打印技术进行仿生打印,制备出具有多层梯度结构的仿生软骨,不仅克服了传统软骨修复材料单相结构导致修复效果不佳的问题,而且通过将软骨细胞与打印材料复合后所打印出的仿生软骨能有效促进受损软骨部位的愈合。
(3)本发明制备的仿生软骨,是采用3d打印技术进行梯度仿生打印,相比于传统的组织工程软骨材料的制备方法,本发明所公开的制备方法具有支架微结构精确成型,有利于生长因子或细胞的黏附,且可以根据患者受损部位实际情况建模,能真正达到个性化治疗。
附图说明
图1为实施例1、2、3与对照组所做的力学性能检测实验结果对照图;
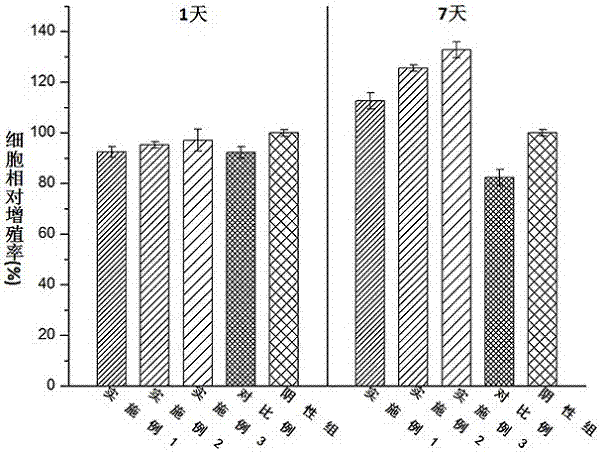
图2为实施例1、2、3与对照组所做的细胞毒性评价实验实验结果对照图;
图3为实施例1、2、3与对照组所做的碱性磷酸酶(alp)的检测实验结果对照图;
图4为实施例1、2、3与对照组所做的糖胺聚糖(gag)的分泌量的检测实验结果对照图。
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
本发明按如下步骤制备得到一种基于3d打印仿生软骨:
(1)打印材料的制备:
①改性ⅱ型胶原蛋白的制备:称取一定量的ⅱ型胶原蛋白(分子量为:1×106kda)加入到50℃的pbs磷酸盐中配制成质量浓度为10%的溶液,然后按体积比vⅱ型胶原蛋白pbs磷酸盐溶液:v甲基丙烯酸酐=10:0.75加入甲基丙烯酸酐,在50℃下搅拌反应4小时,反应结束后,将反应得到的溶液置于截留分子量为10000的透析袋中透析7天,然后将得到的透析液置于-80℃冷冻干燥机中冷冻干燥48小时,即得改性ⅱ型胶原蛋白,置于室温下存储,备用;
②改性透明质酸的制备:称取一定量的透明质酸(分子量为1.2~1.5×106kda)溶解于蒸馏水中配制成质量浓度为2%的透明质酸溶液,然后加入摩尔浓度为1mol/l的氢氧化钠溶液调节溶液的ph至8.5,然后按质量比m透明质酸钠:m甲基丙烯酸二甲氨基乙酯=1:3.5加入甲基丙烯酸二甲氨基乙酯,在10℃下反应24h后,加入到截留分子量为14000的透析袋中流水透析7天,然后将得到透析液置于-80℃冷冻干燥机中冷冻干燥48小时,即得改性透明质酸,置于室温下存储,备用;
③将软骨细胞消化后,加入含有体积分数10%牛血清的软骨细胞培养基,配制成细胞浓度为1×106—5×106ml-1的软骨细胞悬浮液,置于二氧化碳浓度为5%,温度为37℃的细胞培养箱中备用;所述软骨细胞为正常培养3代后的软骨细胞;
(2)各仿生层前驱体的制备:
①仿生软骨下骨前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,然后往所得的溶液中加入纳米羟基磷灰石(粒径分布范围为150-250nm),搅拌至纳米羟基磷灰石完全均匀分散在溶液中,得到仿生软骨下骨前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、纳米羟基磷灰石的浓度为5-10wt%,改性ⅱ型胶原蛋白的浓度为5-10wt%;
②仿生钙化层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸,每次加入的物质完全溶解后再加入下一种物质,然后往所得的溶液中加入纳米羟基磷灰石(粒径分布为150-250nm),搅拌至纳米羟基磷灰石完全分散在溶液中,得到仿生钙化层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、纳米羟基磷灰石的浓度为1-5wt%,改性透明质酸的浓度为1-3wt%;
③仿生软骨深层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,然后加入等体积的步骤(1)所配制的软骨细胞悬浮液,轻柔搅拌至混合均匀,得到仿生软骨深层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性透明质酸的浓度为1-3wt%,改性ⅱ型胶原蛋白的浓度为10-15wt%,软骨细胞的浓度为5×105—2.5×106ml-1;
④仿生中间层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性透明质酸、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,得到仿生中间层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性透明质酸的浓度为2-5wt%,改性ⅱ型胶原蛋白的浓度为10-15wt%;
⑤仿生浅表层前驱体的制备:往蒸馏水中依次加入光引发剂irgacure2959、步骤(1)制备的改性ⅱ型胶原蛋白,每次加入的物质完全溶解后再加入下一种物质,得到仿生浅表层前驱体溶液,备用;其中,光引发剂irgacure2959的浓度为0.5wt%、改性ⅱ型胶原蛋白的浓度为10-15wt%;
(3)仿生软骨的仿生打印:
将步骤(2)制备所得的各仿生层前驱体按仿生软骨下骨前驱体、仿生钙化层前驱体、仿生软骨深层前驱体、仿生中间层前驱体、仿生浅表层前驱体的顺序
依次叠加打印,其中仿生软骨下骨层的打印厚度设置为仿生软骨总厚度的5~10%、仿生钙化层为2~5%、仿生软骨深层为15~30%、仿生中间层为40~55%、仿生浅表层为10~20%,即得一种基于3d打印的仿生软骨;
实施例1
按本发明按上述方法制备一种基于3d打印的仿生软骨,其中:步骤打印材料的制备中所用的ⅱ型胶原蛋白的分子量为1×106kda,所用的透明质酸的分子量为1.2×106kda;步骤各仿生层前驱体的制备中所用到的纳米羟基磷灰石粒径分布范围为150-250nm;在仿生软骨下骨前驱体的制备步骤中纳米羟基磷灰石的用量份为5质量份、改性ⅱ型胶原蛋白的用量为5质量份、光引发剂irgacure2959的用量为0.5质量份;仿生钙化层前驱体的制备步骤中改性透明质酸的用量为30质量份、纳米羟基磷灰石的用为5质量份、光引发剂irgacure2959的用量为0.5质量份;仿生软骨深层前驱体的制备步骤中改性透明质酸的用量为25质量份、改性ⅱ型胶原蛋白的用量为5质量份、软骨细胞的用量为0.1质量份、光引发剂irgacure2959的用量为0.5质量份;仿生中间层前驱体的制备步骤中改性透明质酸的用量为25质量份、改性ⅱ型胶原蛋白的用量为5质量份、光引发剂irgacure2959的用量为0.5质量份;仿生浅表层前驱体的制备步骤中改性ⅱ型胶原蛋白的用量为5质量份、光引发剂irgacure2959的用量为0.5质量份;在仿生软骨的仿生打印步骤中其中仿生软骨下骨层的打印厚度设置为仿生软骨总厚度的10%、仿生钙化层为2%、仿生软骨深层为15%、仿生中间层为55%、仿生浅表层为18%;
实施例2
按本发明按上述方法制备一种基于3d打印的仿生软骨,其中:步骤打印材料的制备中所用的ⅱ型胶原蛋白的分子量为1×106kda,所用的透明质酸的分子量为1.2×106kda;步骤各仿生层前驱体的制备中所用到的纳米羟基磷灰石粒径分布为150-250nm;在仿生软骨下骨前驱体的制备步骤中纳米羟基磷灰石的用量份为10质量份、改性ⅱ型胶原蛋白的用量为10质量份、光引发剂irgacure2959的用量为0.5质量份;仿生钙化层前驱体的制备步骤中改性透明质酸的用量为10质量份、纳米羟基磷灰石的用为5质量份、光引发剂irgacure2959的用量为0.5质量份;仿生软骨深层前驱体的制备步骤中改性透明质酸的用量为15质量份、改性ⅱ型胶原蛋白的用量为10质量份、软骨细胞的用量为0.25质量份、光引发剂irgacure2959的用量为0.5质量份;仿生中间层前驱体的制备步骤中改性透明质酸的用量为15质量份、改性ⅱ型胶原蛋白的用量为10质量份、光引发剂irgacure2959的用量为0.5质量份;仿生浅表层前驱体的制备步骤中改性ⅱ型胶原蛋白的用量为10质量份、光引发剂irgacure2959的用量为0.5质量份;在仿生软骨的仿生打印步骤中其中仿生软骨下骨层的打印厚度设置为仿生软骨总厚度的5%、仿生钙化层为5%、仿生软骨深层为30%、仿生中间层为40%、仿生浅表层为20%;
实施例3
按本发明按上述方法制备一种基于3d打印的仿生软骨,其中:步骤打印材料的制备中所用的ⅱ型胶原蛋白的分子量为1×106kda,所用的透明质酸的分子量为1.2×106kda;步骤各仿生层前驱体的制备中所用到的纳米羟基磷灰石粒径分布为150-250nm;在仿生软骨下骨前驱体的制备步骤中纳米羟基磷灰石的用量份为10质量份、改性ⅱ型胶原蛋白的用量为20质量份、光引发剂irgacure2959的用量为0.5质量份;仿生钙化层前驱体的制备步骤中改性透明质酸的用量为10质量份、纳米羟基磷灰石的用为10质量份、光引发剂irgacure2959的用量为0.5质量份;仿生软骨深层前驱体的制备步骤中改性透明质酸的用量为5质量份、改性ⅱ型胶原蛋白的用量为20质量份、软骨细胞的用量为0.5质量份、光引发剂irgacure2959的用量为0.5质量份;仿生中间层前驱体的制备步骤中改性透明质酸的用量为5质量份、改性ⅱ型胶原蛋白的用量为20质量份、光引发剂irgacure2959的用量为0.5质量份;仿生浅表层前驱体的制备步骤中改性ⅱ型胶原蛋白的用量为20质量份、光引发剂irgacure2959的用量为0.5质量份;在仿生软骨的仿生打印步骤中其中仿生软骨下骨层的打印厚度设置为仿生软骨总厚度的5%、仿生钙化层为5%、仿生软骨深层为30%、仿生中间层为50%、仿生浅表层为10%;
实施例4
对比例:(一种基于3d打印的多层梯度仿生关节软骨材料制备工艺(参考申请号为cn201510752927.5实施例1制备得到)。
实验组1~3:为实施例1~3所得的一种基于3d打印的仿生软骨。
(1)力学性能的检测:将上述实施例1~3所制备的3d打印的抗菌水凝胶修复支架与对比例进行力学评价实验,采用instron5575力学试验机测试对比例和实验组的压缩性能,压缩速率设置为0.5mm/min,用于测试的样品的直径为6mm,高为4.5mm。测试前仪器按说明书调零,而且之后每次测试采用自动复位功能测试,每组样品设置5个平行样,实验结果如图1所示。
可以看到通过本发明所公开的方法所制得的仿生软骨实施例1~3的压缩强度明显较对比例要高,实施例3的压缩强度为对比例的2倍,压缩强度达5.16mpa。
(2)细胞毒性评价实验:将上述实施例1~3所制备的一种基于3d打印的仿生软骨与对比例进行细胞毒性评价实验(按国标gb/t16886.5-2003进行实验),对比实施例1~3和对比例对的实验结果如图2所示。
细胞毒性检测结果显示实施例1~3在与骨髓间充质细胞共培养1天和7天后其对应的细胞相对增殖率均在90%以上,细胞毒性评级为0级,证明其具有良好的细胞相容性,而对比例与骨髓间充质细胞共培养1天和7天后其对应细胞相对增殖率均分别为89.3%和87.5%,细胞毒性评级为1级,具有轻微的细胞毒性。此外,共培养时间的延长实施例1~3的相对相比增殖率均有明显提高,实施例2和3在7天后其细胞相对增殖率均较阴性组要高(均高于100%),证明采用本发明所公开的制备方法所制得的仿生软骨能促进骨髓间充质细胞的生长,有良好的生物相容性。
(3)碱性磷酸酶(alp)的检测
将上述实施例1~3所制备的一种基于3d打印的仿生软骨与对比例分别与骨髓间充质细胞进行共培养7天后采用其碱性磷酸酶试剂盒(alpassaykit,购自bioprotocol试剂盒公司)对其碱性磷酸酶值进行检测,对比实验组和对比例的骨诱导能力。实验结果如图3所示。
碱性磷酸酶(alkalinephosphatealp)是分化成骨细胞的标志物,能促进骨基质的矿化。从实验结果可知,与对比例相比,实施例1~3的alp值明显较对比例要高。由此可见,本发所制备的基于3d打印的仿生软骨具有较高的骨诱导能力,可以促进受损软骨组织的诱导再生。
(4)糖胺聚糖(gag)的分泌量的检测
将上述实施例1~3所制备的一种基于3d打印的仿生软骨与对比例分别与骨髓间充质细胞进行共培养7天和14天后采用二甲基亚甲基蓝试验试剂盒(dmmbassaykit,购自bioprotocol试剂盒公司)检测糖胺聚糖的分泌量,具体操作按试剂盒说明书进行操作。实验结果如图4示。
糖胺聚糖的分泌量多少与骨髓间充质细胞分化并形成成熟的软骨细胞的快慢有关。从实验结果显示,实施例1~3的糖胺聚糖的分泌量在7天和14天时均较对比例明显要高,且随培养时间增加实验组1~3的糖胺聚糖的分泌量均呈上升趋势,在14天时实施例3的糖胺聚糖分泌量达430.15,是对比例的糖胺聚糖的分泌量的2倍。由此可见,本发所制备的基于3d打印的仿生软骨具有较高的糖胺聚糖分泌量,可以促进骨髓间充质细胞分化为软骨细胞,有利于受损软骨组织的修复。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定;对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举;凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!