用于治疗皮肤损伤的内酰胺的制作方法
本发明涉及用于治疗皮肤损伤的方法的内酰胺。
背景技术:
尽管抗生素有所进展,持续感染仍然是一个主要问题,特别是在非常年轻的人、老年人和患有危害愈合过程的某些疾病的人中。
慢性伤口(即在12周内不愈合的伤口)代表特别的问题,特别是在患有糖尿病的人中,因为这些通常因细菌感染而复杂化。细菌感染的发生和持续通常使愈合过程复杂化。伤口可能变得严重和长期存在,使得周围的肉体发生坏死。有时,最终需要受影响的手脚趾或者肢体的部分的受影响组织的切除或者甚至截肢。
由于许多这些细菌感染的慢性特性,通常需要长期使用抗生素治疗。类似地,由于慢性伤口病况的危险,预防性地治疗患有病况如糖尿病的人是常见的,只要观察到或发生皮肤损伤。长期使用抗微生物剂可导致细菌进化以在特定患者伤口的局部环境和整个患者群体两者内产生抗性。
耐药细菌和真菌的出现带来了重大的医学和公共卫生问题。因此,迫切需要开发可以克服耐药性问题的抗微生物剂。细菌和真菌通常以四种方式产生耐药性:产生用于降解药物的代谢酶,改变其靶标以使药物无效,表达高水平的外排蛋白质,其将药物“泵出”以降低其浓度,和诱导生物膜形成以防止药物渗透到细菌中。
wo2007/085042(biosignallimited)描述了某些内酰胺结构及其在治疗细菌感染中的用途。
wo2014/118240(unilever)描述了包含内酰胺和助水溶物的抗微生物组合物。
wo2014/183164(kumar,perry和kit)描述了某些n-官能化二氢吡咯酮化合物和用于制备与二氢吡咯酮化合物连接的表面的方法。
技术实现要素:
本发明是基于发明人对某些内酰胺化合物的不寻常生物学性质的理解和见解,以及这些化合物由于其生物学特征而在治疗方法中的效用。
本文描述的内酰胺是抗细菌的。它们特别的生物学特性使它们令人惊讶地适用于皮肤损伤感染的治疗,特别是在皮肤损伤的长期治疗(包括预防性治疗)中。换句话说,内酰胺可用于治疗所谓的不愈合伤口。
在第一方面,本发明因此涉及用于治疗或预防受试者中的皮肤损伤的细菌感染的方法的内酰胺。
适合地,皮肤损伤是慢性的(在12周内未愈合)或被认为有成为慢性的风险的皮肤损伤。
适合地,感染是细菌感染,其中牵涉到假单胞菌(通常但不一定是铜绿假单胞菌)。
合适地,内酰胺是式i或式ii的内酰胺:
其中ar是任选取代的苯基,并且r1是h或c1-4烷基。
因此,在第一方面,本发明可提供用于治疗受试者中的慢性伤口的方法的式i或式ii的内酰胺,其中ar是任选取代的苯基,所述任选的取代基选自卤素和c1-4烷基。
在某些情况下,ar是未取代的。在某些情况下,ar被取代。在这种情况下,2、3、4、5和6位各自可被取代或未被取代。例如,ar可以是2,4-二取代的,3,4-二取代的,2,4,6-三取代的,3,4,5-三取代的,2,3,4-三取代的,2,4,5-三取代的,等等
合适的取代基r2包括卤素,c1-4烷基,oh,c1-4烷氧基,cf3,of3。
在某些情况下,ar在4-位具有取代基。在某些情况下,4-位的取代基是氯、氟或甲基,任选地氯或甲基。
例如,ar可以是
优选地,内酰胺是式ia或式iia的内酰胺:
其中,
r1为h或c1-4烷基(优选甲基);
r2选自h,卤素,c1-4烷基,oh,c1-4烷氧基,cf3,of3。
在某些情况下,内酰胺是式ia的内酰胺。在某些情况下,内酰胺是式iia的内酰胺。
优选地,r1是h。
优选地,r2是卤素(优选f、cl或br),或c1-4烷基(优选甲基)。
优选地,r2是卤素。卤素包括f、cl、br和i。例如,r2可以是氟或氯,例如氯。
优选的内酰胺可包括:
特别优选的内酰胺包括:4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488);5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491);和4-(4-氟苯基)-5-亚甲基-吡咯-2-酮(参考号310)。
内酰胺可用于治疗受试者的各种慢性皮肤损伤,但可特别用于治疗糖尿病性溃疡,例如糖尿病足溃疡。
式i和ii的内酰胺用于防止细菌生物膜的形成,延缓或阻止细菌生物膜的生长和发展,和/或降低细菌生物膜的程度。因此,本发明包括用于通过防止细菌生物膜的形成,延迟或阻止细菌生物膜的生长和发展,和/或降低细菌生物膜的程度来治疗受试者的细菌感染的式i和ii的内酰胺。假单胞菌,通常是铜绿假单胞菌,可以牵涉到细菌生物膜。
在本发明中,被治疗的受试者优选是哺乳动物受试者,最优选是人。
虽然内酰胺可用于治疗患有慢性皮肤损伤的各种受试者,但本文所述方法的优点是内酰胺的不寻常的生物学特征,其可使内酰胺特别适合于治疗糖尿病患者。因此,在一些情况下,受试者被诊断为患有糖尿病。糖尿病可以是i型或ii型。
在一些受试者中,特别是在被诊断患有糖尿病的受试者中,内酰胺可以预防性地用于防止皮肤损伤的细菌感染的发生或复发,即使当皮肤损伤不是明确的慢性时。
式i和ii的内酰胺可以用作皮肤损伤感染的一线治疗,或者可以用于已经用其他抗生素治疗相同感染的受试者,例如对那些其他抗生素没有表现出令人满意的响应的那些。
适当时,式i和ii的内酰胺可以与其他治疗一起施用,包括其他抗生素治疗。
在第二方面,本发明提供治疗皮肤损伤的细菌感染的方法,所述方法包括向受试者施用治疗有效量的式i或式ii的内酰胺。
在第三方面,本发明提供式i或式ii的内酰胺在制备用于治疗皮肤损伤的细菌感染的药物中的用途。
在第四方面,本发明提供了药物组合物,其包含式i或式ii的内酰胺,其中所述组合物被配制用于局部施用于皮肤,例如作为乳膏、凝胶或洗剂。
应当认识到,关于第一方面描述的所有优选适当时类似地适用于第二、第三、第四方面。
具体实施方式
现将参考以下附图描述本发明,其中:
lb培养基=lysogenybroth,来自sigmaaldrichuk。
内酰胺131=4-苯基-5-羟基-5-甲基-1h-吡咯-2-酮
内酰胺258=4-(4-氟苯基)-5-羟基-5-甲基-1h-吡咯-2-酮
内酰胺310=4-(4-氟苯基)-5-亚甲基-吡咯-2-酮
内酰胺316=4-(4-溴苯基)-5-羟基-5-甲基-1h-吡咯-2-酮
内酰胺488=4-(4-氯苯基)-5-亚甲基-吡咯-2-酮
内酰胺491=5-亚甲基-4-(对甲苯基)吡咯-2-酮
和
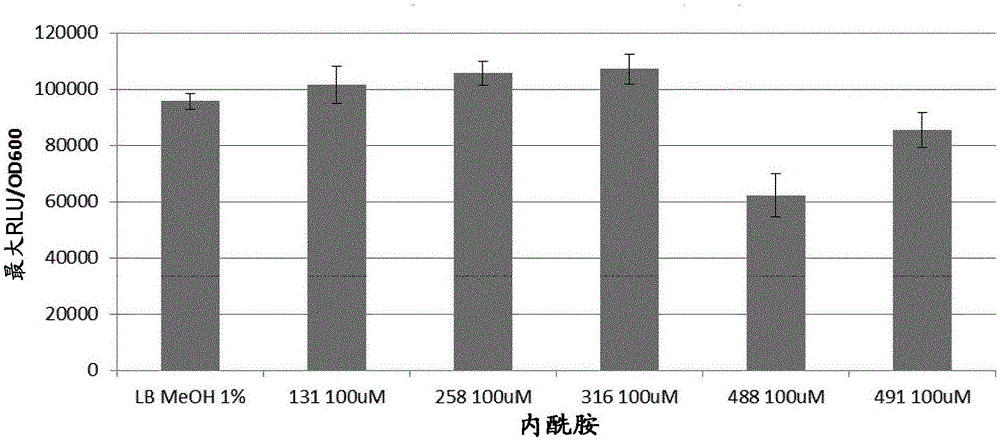
图1显示在100μm的内酰胺131,258,316,488和491存在和不存在时铜绿假单胞菌lasi::lux的表达的比较。对照:lb培养基+1%甲醇。
图2显示在100μm的内酰胺131,258,316,488和491存在和不存在时铜绿假单胞菌rhli::lux的表达的比较。对照:lb培养基+1%甲醇。
图3显示在100μm的unilever内酰胺131,258,316,488和491存在和不存在时铜绿假单胞菌pqsa::lux的表达的比较。对照:lb培养基+1%甲醇。
图4显示在100μm的unilever内酰胺131,258,316,488和491存在和不存在时铜绿假单胞菌tac::lux的表达的比较。对照:lb培养基+1%甲醇。
图5显示展示由在0(1),100(2)和10μm(3)的内酰胺488存在下生长的pao1-l产生绿脓素的小瓶。(4)是仅lb对照。
图6显示内酰胺488对铜绿假单胞菌pao1-l中pqsa::lux表达的影响。
图7显示内酰胺491对铜绿假单胞菌pao1-l中pqsa::lux表达的影响。
图8显示pqs在内酰胺488的存在下对pao1-lδpqsa中pqsa::lux表达的影响,pqs的ec50在488(215μm)存在下从2μm增加至31μm。
图9显示0,50,100,200μm的488对铜绿假单胞菌pao1-lδpqsa中pqsa’::lux的pqs依赖性表达的影响。数据显示在50μm但不是100μm或200μm的488存在下,pqs与488竞争pqsa::lux的pqsr依赖性激活,完全恢复光输出。
图10显示在0μm,10μm或40μm的pqs的存在下,内酰胺488对pao1δpqsa中pqsa’::lux表达的影响。
图11显示488的pqsr非依赖性活性对pao1-nδpqsahr中pqsa’::lux表达的影响。
图12显示488对铜绿假单胞菌中pqsa’::lux表达的抑制作用。
图13显示hhq生产的tlc分析。(图a)在312nm紫外光下的tlc板,显示pqs(泳道1上部斑点)和hhq(泳道1下部斑点)标准一起,488标准(泳道2),在不存在(泳道3)和存在(泳道4)化合物488的情况下生长的pao1-nδpqsahr的有机溶剂上清液提取物,和在不存在(泳道5)和存在488(泳道6)的情况下生长的pao1-nδpqsahrpqsabcd的有机溶剂上清液提取物。通过琼脂覆盖层中存在的pao1-lδpqsactx::pqsa’-luxcdabe发生绿脓素产生(图b)和光输出(图c)。绿脓素和光输出两者依赖于aq的存在。使用发光光子照相机捕获生物发光。uv照明的板(图a,泳道2,4和6)上的最亮点是488。
铜绿假单胞菌
铜绿假单胞菌是在某些细菌性皮肤感染中重要的病原体,并且与慢性伤口中的严重且通常是慢性的感染有关。存在许多铜绿假单胞菌菌株,包括pa01,pa7,usbpp-pa14和菌株2192的。除非另有说明,否则提到铜绿假单胞菌旨在指代任何和所有菌株。
本文描述的方法可以涉及治疗其中牵涉到铜绿假单胞菌的感染。铜绿假单胞菌可以是产生aq(烷基喹啉化合物)的菌株。铜绿假单胞菌可以是产生pqs(假单胞菌喹诺酮信号;2-庚基-3-羟基-4-(1h)-喹诺酮)和hhq(4-羟基-2-庚基喹啉)之一或两者的菌株。铜绿假单胞菌可以是属于两大铜绿假单胞菌基因组群组(pao1和pa14)之一的菌株。
皮肤损伤
如本文所用,术语皮肤损伤是指由例如伤害、其他皮肤创伤或诸如血液循环受限的病理原因引起的伤口或痛处。皮肤损伤的实例包括皮肤已被撕裂、切割或刺破的区域,溃疡(从溃疡前损伤到坏疽组织)。
皮肤损伤可以仅影响表皮和真皮,或者它们可以影响组织一直到筋膜。
群体感应
群体感应(qs)是藉此微生物特别是细菌通过分泌和检测称为自诱导物(ai)的化学信号而相互通信并表现出全社区性的行为协调的机制。群体感应已经在大量细菌物种/菌株中得到证实,并且在调节细菌毒力,抗药性,外排转运蛋白的表达和生物膜形成中是重要的,因此在抗微生物领域引起关注。(frontiersinmicrobiology6(1036),2015年9月)。
群体感应是基于细胞密度的调节集体行为的细胞间通信系统,其在细菌毒力和生物膜形成的调节中起关键作用。该过程依赖于称为自诱导肽(aip)的信号分子的产生、释放和全组性检测,其在革兰氏阴性细菌中通常是高丝氨酸内酯(hsl),尤其是n-酰基-高丝氨酸内酯(ahl)。已知其他群体感应分子,包括肾上腺素/去甲肾上腺素。
生物膜形成使细菌能够抵抗抗生素,因为一旦细菌感觉到生物膜的外层被破坏,内层将长得更强壮以重建社区。本发明是基于发明人对如本文所述的某些内酰胺的性质的研究以及他们对所述内酰胺影响革兰氏阴性细菌如铜绿假单胞菌中的qs的方式的见解。
铜绿假单胞菌的qs网络以由至少四个相互连接的信号传导机制组成的多层次结构组织,并展示可塑性,因为它可以响应细菌种群变化,也可能响应环境压力线索。铜绿假单胞菌通过依赖于两个qs系统(两者为luxl/r信号传导级联的一部分)即las和rh1系统,精心安排生物膜形成和毒力因子产生。
在铜绿假单胞菌中,酰基高丝氨酸内酯(ahl)和烷基喹诺酮(aq)qs系统对于毒力和生物膜形成是重要的。一种酰基-hslqs调节剂是lasr。由铜绿假单胞菌产生的非ahl信号传导分子称为pqs(假单胞菌喹诺酮信号),其为2-庚基-3-羟基-4-(1h)-喹诺酮。
生物膜
如本文所用的术语“生物膜”是指在水性环境中的界面处发展和持续的生物膜。这些生物膜由嵌入有机凝胶状基质中的微生物组成,所述有机凝胶状基质由一种或多种由驻留的微生物分泌的基质聚合物组成。生物膜可以发展成宏观结构,并且还能够捕获营养物和颗粒物,其可以促进其增强的发育和稳定性。生物膜还可以防止抗微生物剂的渗透,其可以导致持续感染。生物膜的形成为细菌提供了受保护的环境,例如在部分愈合和/或覆盖的伤口内,其可以承受各种应激,包括许多抗生素治疗。
药物组合物
本发明还提供了包含如本文所述的内酰胺的药物组合物。应理解,药物组合物将配制成适合于预期给药途径。包含式i或ii的内酰胺的药物组合物通常包含药学上可接受的载体,并且可任选地包含其他治疗成分。
合适地,将组合物配制成用于局部施用于皮肤,例如乳膏、凝胶或洗剂。在某些情况下,也可以使用全身施用,例如静脉内施用。因此,在一些情况下,组合物被配制用于肠胃外施用。
优选配制组合物以提供有效量的内酰胺。如本文所用的术语“有效量”是指内酰胺的量至少足以实现微生物群体的活性或生理学特性的期望调节。有效量至少部分地取决于所用化合物,存在的微生物种类,结构、系统或宿主,以及期望的调节水平。调节微生物群体的活性或生理特性包括但不限于减缓、减弱或抑制微生物群体的生长和/或表面的定殖;导致微生物群体部分或完全减少;抑制生物膜的形成、发展或生长,和部分或完全降低生物膜的程度,等等。
治疗方法
应当理解,本文所用的术语“治疗方法”包括预防,阻碍细菌菌落群体生长的治疗,保持细菌菌落群体稳定的治疗,以及减少或根除细菌群体的治疗。
本发明涉及皮肤损伤感染的治疗方法。这些通常被称为不愈合伤口。慢性病征的特征在于长持续时间或频繁复发,通常在伤口在第一次出现后12周内未愈合的情况下。
慢性细菌性伤口感染在糖尿病患者中带来特殊问题。因此,设想本发明用于治疗已被诊断患有糖尿病的患者的细菌性皮肤损伤感染。
由于它们不同寻常的生物学特性,式i和ii的内酰胺可用于长期治疗感染。这是因为,由于它们与细菌特别是铜绿假单胞菌的各种生物途径的选择性相互作用,内酰胺可以允许群体控制和减少,而不触发被认为导致进化抗性的机制。
在某些情况下,细菌感染是其中牵涉到假单胞菌的感染(通常但不一定是铜绿假单胞菌)。
本文描述的方法可适合长期使用。因此,该方法可包括将内酰胺定期施用于受试者至少数周,数月,至少1年,至少2年,至少3年,至少5年,至少8年,或至少10年的时间。
实施例
为了阐明本文所述化合物的作用机理,研究了每种内酰胺对铜绿假单胞菌中n-酰基高丝氨酸内酯(ahl)和2-烷基-4-喹诺酮-(aq)-依赖性群体感应(qs)的影响。
使用基于lux的lasi(图1)、rhli(图2)和pqsa(图3)染色体整合的启动子融合物,评估rhl和lasahl-和pqsaaq-合成酶基因的表达。将发光量化为细菌生长的函数。申请人进一步使用大量菌株确定,内酰胺均未在100μm下是生长抑制性的(图未显示)。
铜绿假单胞菌pao1-ntac::lux菌株被用作阳性对照生物传感器,因为它组成性地表达luxcdabe并因此表达光(图4)。在内酰胺存在下该菌株中光输出的任何降低将显示化合物是否对发光本身具有不利影响。tac::lux表达谱显示在化合物和参与光产生的酶之间没有干扰。因此,在qs报告菌株与内酰胺孵育时观察到的任何效应都将归因于启动子表达的改变。
然后研究了化合物4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)对pao1-l产生绿脓素的定性影响。
绿脓素是铜绿假单胞菌中的蓝色氧化还原活性次级代谢物和推定的信号传导分子(jayaseelan等,2014)。绿脓素生物合成(phz)基因受qs调节,并且部分是经由通过pqse起作用的转录调节因子pqsr(rampioni等,2011)。在存在和不存在化合物4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的情况下,在37℃下在铜绿假单胞菌菌株pao1-l中孵育8小时后,视觉评估绿脓素产生,其中图3显示是pqsr依赖性pqsa::lux启动子融合物的最有效抑制剂。图5显示在不存在或存在内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的情况下生长的pao1-l的培养物上清液。
由于小瓶2中的培养物上清液中不存在绿色色素沉着(图5),观察到内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)对绿脓素产生的抑制。虽然定性,但这一观察结果进一步证实了内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)对aq依赖性qs的抑制作用。
然后研究了本发明化合物对铜绿假单胞菌中aq依赖性qs的抑制特性。
在铜绿假单胞菌中,pqsabcde基因编码2-烷基-4-(1h)-喹诺酮(aq)的合成和作用所需的生物合成途径(heeb等,2010)。转录激活因子pqsr调节pqs生物合成途径的表达,其进而控制次级代谢物如弹性蛋白酶,绿脓素和磷脂酶以及生物膜成熟和群集运动(swarmingmotility)。在该qs系统中,主要的aq信号分子是4-羟基-2-庚基喹啉(hhq)和2-庚基-3-羟基-4-喹诺酮(pqs),两者充当pqsr的共诱导物(heeb等,2010;ilangovan等,2013)。
使用ahl和aq生物传感器菌株的第一次筛选实验的结果(图1-3)清楚地表明,对pqs-系统的抑制是内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)和5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491)对铜绿假单胞菌中的qs的主要作用。为了测定4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)和5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491)的相对抑制活性(ic50),使用相同的生物传感器菌株(铜绿假单胞菌pao1pqsa::lux;fletcher等,2007;ilangovan等,2013)构建剂量响应曲线。该菌株响应于aq(例如pqs和hhq)的内源性产生而产生光。获得的数据显示在图6和图7中,从其分别计算4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的ic50为22μm并且5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491)的ic50为44μm。虽然4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)在两种化合物中更有效,但5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491)显示期望的效果。还可以看出5-亚甲基-4-(对甲苯基)吡咯-2-酮(参考号491)在高浓度下不像4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)那样强烈地抑制pqsa表达,而4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)完全抑制光输出,因此完全抑制pqsa表达。
图6和7证实pqs群体感应在假单胞菌中的结合和抑制,化合物488显示完全敲除pqs的能力。图7中的491化合物虽然证明抑制,但在较高浓度下没有给出完全敲除。
研究了aq依赖性qs的作用模式。
pqs系统中的主要qs分子是aq、pqs及其前体hhq(williams&camara,2009)。它们的生物合成需要调节剂pqsr和生物合成蛋白pqsabcd和单加氧酶pqsh(heeb等,2010)。
4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的抑制作用可以涉及抑制aq生物合成,或者4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)可以表现得像拮抗剂并阻断pqs受体pqsr。这些实验不区分pqsr活化的抑制和aq生物合成的抑制,因为所使用的生物传感器菌株维持完整的aq依赖性qs系统。因此设计实验以确定4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)抑制活性的性质和程度。首先,探索了4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)是对于pqsabcde基因表达和因此aq生产必要的响应调节蛋白pqsr的抑制剂的可能性。
通过使用不产生aq的铜绿假单胞菌菌株pao1-lδpqsa,pqsa::lux,天然pqsr激动剂pqs的ec50值计算为~2μm(ilangovan等,2013)。在固定浓度的内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)和一系列pqs浓度的存在下,ec50值增加~15倍至31μm(图8)。这表明4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)充当aq信号传导的竞争性拮抗剂,潜在地抑制pqsr与其共诱导物pqs之间的相互作用。
然后使用0,50,100和200μm的4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)浓度重复图8中所示的实验。所得结果示于图9,其显示当4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)浓度增加时,最大光输出实质性降低。剂量响应曲线的形状表明4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)是竞争性拮抗剂,因为增加pqs浓度,恢复pqsa::lux表达。
这些数据证明了4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的选择性结合和竞争性拮抗剂活性。
进行基于pao1-lδpqsapqsa’::lux生物传感器的测定以确定内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)是否在更高浓度下表现出任何部分激动剂活性。部分激动剂是可以结合并激活受体,与完全激动剂相比导致非完全响应的分子。在图形上,也是部分激动剂的拮抗剂在高浓度下表现出激动剂活性。图10显示4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)没有部分激动剂活性,因为它在至多800μm的浓度下不能激活pqsa表达。这与其在10或40μmpqs存在下作为拮抗剂的活性形成对比。这证实在较高浓度下没有受体结合的激活,在较高剂量下提供低毒性或甚至无毒性。
pqs能够在不存在pqsr的情况下通过尚未完全了解,但似乎依赖于pqs的铁螯合特性的机制微弱地激活pqsa。该实验的目的是澄清内酰胺4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)是否也通过pqsr非依赖性途径而对pqsa表达是抑制性的。如先前所描述的,基于三重突变体pao1-nδpqsahr的pqsa’::lux生物传感器不可产生aq且缺乏pqsr,但仍然响应于外源性pqs。然而,该响应比pqsr依赖性响应弱得多。图11显示4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)在40μmpqs存在或不存在下对pqsa的pqsr非依赖性表达的影响。4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)对该pqsr非依赖性途径具有小的抑制作用。这表明虽然本发明化合物可以对不表达aq的铜绿假单胞菌具有一些影响,但它们在治疗牵涉到产生aq的菌株的病症中显示最大的希望。
实际上,对于4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488),pqs途径是占主导的抑制途径。考虑到群体感应在假单胞菌的毒性和毒力中的作用,则这种技术对那些能够进行群体感应的菌株最有效。
为了研究4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)对铜绿假单胞菌pa14的抑制作用,将pqsa’::lux融合物引入染色体上。观察到与先前对菌株pao1描述的那些类似的抑制作用。从图12中的抑制曲线外推的ic50计算为17.9μm。
为了确定4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)是否能够抑制参与aq生物合成的酶(pqsabcd),开发利用铜绿假单胞菌pao1-nδpqsahr。该突变体不可产生aq,因为已经删除编码关键生物合成酶(pqsa和pqsh)和调节(pqsr)的基因。为了在pao1-nδpqsa中恢复pqsr非依赖性方式的aq产生,将pqsabcd基因导入质粒(pbbrpqsabcd;niewerth等,2011)。铜绿假单胞菌pao1-nδpqsahr和铜绿假单胞菌pao1-nδpqsahrpbbrpqsabcd两者在lb中在有和没有4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)(200μm)的情况下温育过夜,重悬至od600为1.0。用酸化的乙酸乙酯萃取培养物,除去有机相,干燥并重悬于甲醇中,进行薄层色谱(tlc)。
表1
在使用二氯甲烷-甲醇流动相进行色谱后,用含有aq生物传感器菌株pao1-lδpqsactx::pqsa’-luxcdabe的薄琼脂层覆盖tlc板(fletcher等,2007),孵育并检查报告物输出(图13)。图13的图a显示色谱后在uv照射下的tlc板。生物传感器菌株响应于结合pqsr并激活pqsa启动子的aq产生光(图13的图c)和绿脓素(图13的图b)。
生物传感器揭示在不存在(图13的图b和c;泳道5)和存在(图13的图b和c;泳道6)化合物4-(4-氯苯基)-5-亚甲基-吡咯-2-酮(参考号488)的情况下pao1-nδpqsahrpbbr-pqsabcd的样品中都存在hhq,表明内酰胺不抑制hhq生物合成。
细菌菌株的来源
细菌菌株如下获得或制备:
*ddbj/embl/genbank登录号ayuc00000000
表2
生物活性概述
实施例证明本发明化合物已显示:
·抑制铜绿假单胞菌中的烷基喹诺酮(aq)依赖性群体感应(qs)。
·抑制属于主要铜绿假单胞菌基因组群组的代表性菌株中的pqsr(分别为pao1和pa14)。
·与lysr型调节剂pqsr拮抗地相互作用(以竞争性方式,没有部分激动剂活性)。
·似乎没有直接抑制aq生物合成,但通过充当pqsr拮抗剂阻断aq合成。
·可能与充当变构抑制剂的pqsr的共诱导物结合结构域(pqsrcbd)相互作用。
这提供了不寻常的生物学特征,其可以使本发明化合物能够可用于治疗源自细菌感染的慢性伤口并发症。特别地,本发明化合物的生物学特征提供了治疗糖尿病患者所经历的慢性伤口的效用。这是因为本发明化合物具有控制增殖和生物膜形成的生物活性特征,但不触发与产生抗菌抗性相关的生物途径。
参考文献
出于所有目的,本文引用的参考号文献通过引用整体并入:
aendekerks,digglesp,songz,
fletchermp,digglesp,cámaram&williams,p.(2007)biosensor-basedassaysforpqs,hhqandrelated2-alkyl-4-quinolonequorumsensingsignalmolecules.natureprotocols,2,1254-1262doi:10.1038/nprot.2007.158.
fletchermp,digglesp,cámaram.andwilliamsp.(2007)biosensor-basedassaysforpqs,hhqandrelated2-alkyl-4-quinolonequorumsensingsignalmolecules.natureprotocols,2,1254–62.
freschietal.(2015)clinicalutilizationofgenomicsdataproducedbytheinternationalpseudomonasaeruginosaconsortium.frontiersinmicrobiology6,article1036.
ilangovana,fletcherm,ramionig,pustelnyc,rumbaughk,heebs,camaram,trumana,chhabrasr,emsleyj&williamsp.(2013)structuralbasisfornativeagonistandsyntheticinhibitorrecognitionbythepseudomonasaeruginosaquorumsensingregulatorpqsr(mvfr).plospathogens9(7):e1003508.
niewerthh,berganderk,chhabras,williamsp,andfetzners.(2011)synthesisandbiotransformationof2-alkyl-4(1h)-quinolonesbyrecombinantpseudomonasputidakt2440,appliedmicrobiologyandbiotechnology,91,1399–1408.
rahmelg,stevensej,wolfortsf,shaoj,tompkinsrg,etal.(1995)commonvirulencefactorsforbacterialpathogenicityinplantsandanimals.science,268:1899–1902.
- 还没有人留言评论。精彩留言会获得点赞!