咪唑喹啉化合物及其应用的制作方法
相关申请本申请要求2018年9月7日提交的美国临时专利申请号62/728556的权益,其全部内容通过引用并入本申请。
背景技术:
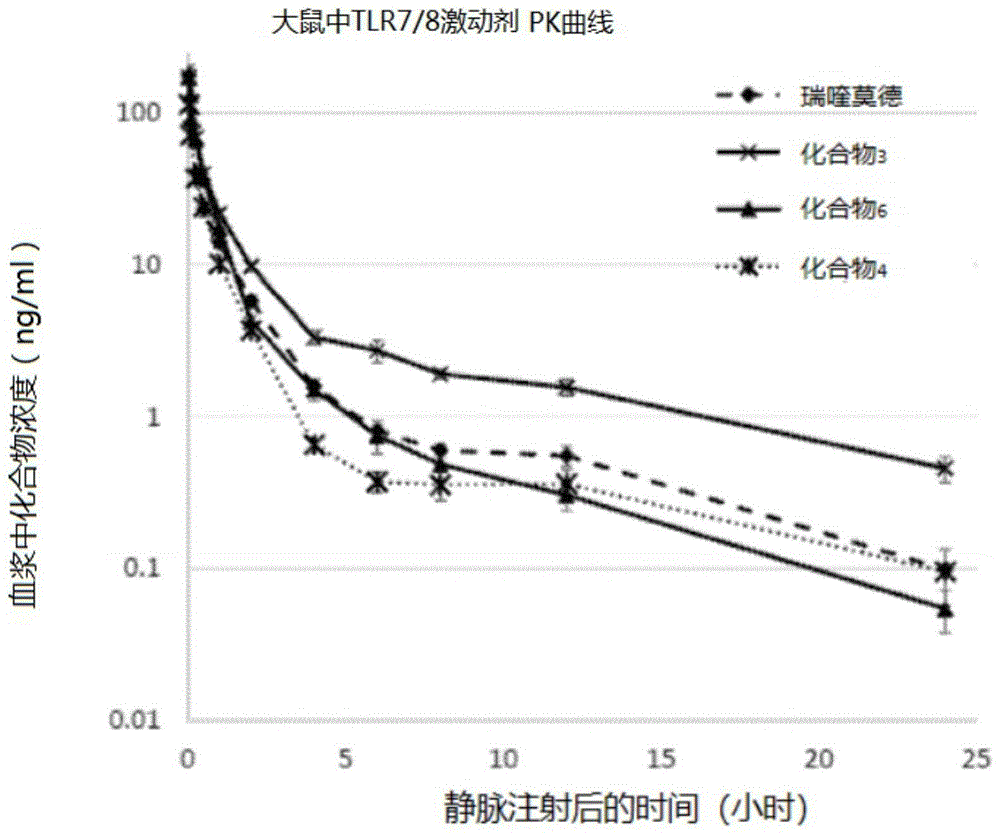
:toll样受体(tlrs)在病原体识别和先天免疫激活中具有根本性作用。tlr7和tlr8分别是toll样受体7和8,它们在人类x染色体上彼此紧邻。tlr7和tlr8均可识别诸如hiv和hcv的病毒的单链rna。已显示tlr7在自身免疫性疾病例如系统性红斑狼疮(sle)的发病机理以及抗病毒免疫调节中起重要作用。最近,tlr8的遗传变异与肺结核的易感性有关。tlr7在人类和小鼠中均起作用,而tlr8仅在人类中起作用,但似乎抵消了tlr7的活性。tlr7/8激动剂作为免疫应答增强剂的好处之一是可以同时刺激多种细胞类型。tlr7和tlr8主要在免疫细胞上表达,例如抗原呈递细胞,包括浆细胞样树突细胞(pdc)和髓样树突细胞(mdc),以及自然杀伤细胞和巨噬细胞。pdc和mdc上的tlr7/8激活会导致i型干扰素(ifn)、肿瘤坏死因子α(tnfα)和白介素12(il-12)的诱导和释放,这是启动先天性和适应性免疫杀死癌细胞的重要步骤。因此,需要开发作为抗病毒和抗肿瘤化合物的tlr7和tlr8的小分子激动剂。技术实现要素:本申请提供的化合物是咪唑喹啉衍生物或其药学上可接受的盐。所述化合物是toll样受体7和8(tlr7/8)的激动剂。可通过向受试者施用治疗有效量的本申请提供的咪唑喹啉衍生物来使用所述化合物治疗有需要的受试者的病毒感染(例如丙型肝炎(hcv))、癌症(例如her2阳性癌症)、变应性疾病或其组合。一方面,本申请提供了式(i)的化合物:或其药学上可接受的盐,其中每个r1独立为f、cl、br或i;r2为—o-(c3–5环烷基)、—o-(c1–3烷基)、—o-(c1–3卤代烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基);以及n为0、1、2、3或4。一些实施方式包括含有本申请所述化合物的药物剂型。本申请所述的化合物或组合物可用于活化tlr7/8。除了用作独立的免疫治疗剂,例如抗病毒和抗癌剂外,本申请所述的化合物或组合物还可以用作癌症疫苗或过继性t细胞转移方案中的佐剂。一些实施方式包括与tlr7/8激动剂有关的疾病或病症的治疗方法,该方法包括将有效量的本申请所述的化合物施用于有需要的哺乳动物。一些实施方式包括本申请所述的化合物在用于治疗与tlr7/8激动剂相关的疾病或病症的药物的制备中的用途。附图说明图1显示了实施例15中描述的tlr7/8激动剂的平均浓度与时间的大鼠的pk曲线。详细描述下面列出的是在本申请中使用的各种术语的定义。除非在特定情况下另有定义,否则这些定义适用于整个说明书和权利要求书中使用的术语,无论是单独使用还是作为较大组的一部分使用。本申请中,冠词“一种”或“一个”是指该冠词的语法对象中的一个或多个(即,至少一个)。举例来说,“一个元素”是指一个元素或一个以上元素。此外,用语“包括”以及其他形式(例如“包括”,“包含”和“含有”)的使用不是限制性的。本申请中,用语“施用”是指根据需要将本申请提供的化合物施用给细胞或受试者以获得期望的效果。本申请中,除非另有说明,用语“烷基”本身或作为另一取代基的一部分是指具有指定碳原子数的直链或支链烃(即,c1-3表示1-3个碳原子),并包括直链或支链取代基。本申请中,用语“组合物”或“药物组合物”是指至少一种化合物(如本申请所述的有用的)与药学上可接受的载体的混合物。所述药物组合物促进所述化合物向患者或受试者的给药。本领域存在多种施用化合物的技术,包括但不限于,静脉内、口服、喷雾、肠胃外、眼、肺、直肠、皮下和局部施用。本申请中,用语“控制疾病或病症”用于表示改变一种或多种激酶的活性以影响疾病或病症。本申请中,用语“环烷基”是指单环非芳香族基团,其中形成环的每个原子(即,骨架原子)是碳原子。在一个实施方式中,所述环烷基为饱和或部分不饱和的。环烷基包括具有3至5个环原子的基团(c3-5环烷基)。本申请中,用语“与激酶活性有关的疾病或病症”是指可通过抑制一种或多种激酶,全部或部分治疗的疾病、状况或病症。本申请中,用语“有效量”,“药学有效量”或“治疗有效量”是指无毒但足够剂量的试剂(例如,本申请提供的化合物或组合物)以提供所需的生物学结果,其结果可能是疾病的体征、症状或原因的减轻或缓和,或两者兼而有之,或生物学系统的任何其他所需改变,包括影响、降低或抑制激酶的活性或阻止其活化(例如,调节激酶活性)。在任何情况下,本领域普通技术人员可以使用常规实验确定适当的治疗量。本申请所用的这些用语还可以指有效地在动物中(其中在一些实施方式中,所述动物是人)产生期望的体内作用的量,包括但不限于葡萄膜炎,眼压降低或干眼症。本申请中,用语“赋形剂”是指可用于制备药物组合物的生理相容性添加剂。药学上可接受的载体和赋形剂的实例可以在例如《雷明顿药物科学》(remingtonpharmaceuticalscience),第16版中找到。本申请中,用语“卤代烷基”是指独立地被一个或多个氟、氯、溴或碘原子取代的烷基。在一些实施方式中,所述烷基独立地被一个或多个氟、氯或溴原子取代。在一些实施方式中,所述烷基独立地被一个或多个氟或氯原子取代。本申请中,用语“受试者”,“患者”或“个体”是指人或非人类哺乳动物。非人类哺乳动物包括,例如牲畜和宠物,例如羊、牛、猪、犬、猫和鼠类哺乳动物。在一些实施方式中,所述患者、受试者或个体是人。本申请中,用语“药学上可接受的”是指不消除化合物的生物学活性或特性并且相对无毒的材料,即,可以将所述材料施用于个体而不会引起不希望的生物学作用或与组合物中所含的任意成分以有害的方式相互作用。本申请中,用语“药学上可接受的载体”是指参与在患者体内或者向患者体内携带或运输本发明中有用的化合物从而使其可以执行其预期功能的药学上可接受的材料、组合物或载体,例如液体或固体填料、稳定剂、分散剂、悬浮剂、稀释剂、赋形剂、增稠剂、溶剂或包囊剂。通常,将此类构建体从一个器官或身体的一部分携带或运输到另一器官或身体的一部分。从与制剂的其他成分(包括本发明中有用的化合物)相容的意义上讲,每种载体必须是“可接受的”,并且对患者无害。在本申请中,“药学上可接受的载体”还包括与本发明中有用的化合物的活性相容并且患者生理上可接受的任意的以及所有的包衣、抗菌和抗真菌剂、吸收延迟剂等。用语“药学上可接受的载体”可以进一步包括在本发明中有用的化合物的药学上可接受的盐。在本发明的实践中,使用的药物组合物中可以包含的其他附加成分在例如雷明顿药物科学(remington'spharmaceuticalsciences)(genaro,ed.,mackpublishingco.,1985,easton,pa.)中有所描述,其通过引用并入本申请。“药学上可接受的载体”可用于制备药物组合物,该药物组合物通常与组合物的其他成分相容,对接受者无害,并且在生物学上或其他方面都无不利效果。“药学上可接受的载体”包括一种或多种载体。实施方式包括用于局部、眼、肠胃外、静脉内、腹膜内肌内、舌下、经鼻或口服给药的载体。“药学上可接受的载体”还包括用于制备水分散体的试剂和用于注射或分散的无菌粉末。本申请中,用语“药学上可接受的盐”是指本申请提供的化合物的衍生物,其中母体化合物的修饰是通过将现有的酸或碱部分转化为其盐形式。药学上可接受的盐的实例包括但不限于碱性残基例如胺的无机或有机酸盐;酸性残基例如羧酸的碱金属或有机盐等。本申请提供的化合物的药学上可接受的盐包括,例如由无毒的无机或有机酸形成的母体化合物的常规无毒盐。本申请提供的化合物的药学上可接受的盐可以通过常规化学方法由含有碱性或酸性部分的母体化合物合成。通常,可以在水中或在有机溶剂中或在两者的混合物中,通过将这些化合物的游离酸或碱形式与化学计算量的合适的碱或酸混合来制备这些盐;通常,可以使用非水介质,例如醚、乙酸乙酯、乙醇、异丙醇或乙腈。合适的盐的清单可见于《雷明顿药物科学》(remington'spharmaceuticalsciences),第17版,mackpublishingcompany,宾夕法尼亚州伊斯顿,1985年,第1418页和journalofpharmaceuticalscience,66,2(1977),它们中的每一个均通过引用整体并入本申请。本申请中,用语“预防”或“预防”是指在什么都没有发生的情况下疾病或疾病没有发展,或在已经有疾病或疾病的发展的情况下疾病或疾病没有进一步发展。还考虑了人预防与疾病或疾病有关的某些或全部症状的能力。本申请中,用语“治疗(名词)”或“治疗(动词)”是指将治疗剂,即本申请提供的化合物,应用于或施用给患者,或将治疗剂应用于或施用给患有某种疾病、有该疾病的症状或可能发展该疾病的患者中分离出的组织或细胞系(例如,用于诊断或体外应用),目的是治愈、缓解、减轻、改变、补救、改善、改进或影响该疾病、该疾病的症状或发展该疾病的可能性。基于从药物基因组学领域获得的知识,可以明确地定制或改进这样的治疗。化合物一方面,本申请提供了咪唑喹啉衍生物的化合物。在一个实施方式中,所述化合物是表1的化合物或其药学上可接受的盐。表1另一方面,本申请提供的是式(i)的化合物:或其药学上可接受的盐,其中每个r1独立为f、cl、br或i;r2为—o-(c3–5环烷基)、—o-(c1–3烷基)、—o-(c1–3卤代烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基);以及n为0、1、2、3或4。在一些实施方式中,式(i)的化合物为式(ii)的化合物:或其药学上可接受的盐。在一些实施方式中,式(i)的化合物为式(iii)的化合物:或其药学上可接受的盐。在一些实施方式中,r1为f、cl、br或i。在一些实施方式中,r1为f。在一些实施方式中,r1为h或f。在一些实施方式中,r1为h(即,n为0)。在一些实施方式中,r1为h、f、cl、br或i。在一些实施方式中,r2为—o-(c3–5环烷基)、—o-(c1–3烷基)、—o-(c1–3单卤代烷基)、—o-(c1–3二卤代烷基)、—o-(c1–3三卤代烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基)。在一些实施方式中,r2为—o-cf3、—o-ch2-cf3、—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基—s(o2)-甲基或—s(o2)-乙基。在一些实施方式中,所述卤代烷基卤素独立为f、cl、br或i。所述卤代烷基卤素为f。在一些实施方式中,r2为—o-(c3–5环烷基)、—o-(c1–3烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基)。在一些实施方式中,r2为—o-(c3–5环烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基)。在一些实施方式中,r2为—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基、—s(o2)-甲基或—s(o2)-乙基。在一些实施方式中,r2为—o-(c3–5环烷基)。在一些实施方式中,r2为—o-(c3–5环烷基),r1为f、cl、br或i。在一些实施方式中,r2为—o-(c3–5环烷基),r1为h或f。在一些实施方式中,r2为—o-(c3–5环烷基),r1为h。在一些实施方式中,r2为—o-(c3–5环烷基),r1为f。在一些实施方式中,r2为—o-(c3–5环烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为f、cl、br或i。在一些实施方式中,r2为—o-(c3–5环烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为h或f。在一些实施方式中,r2为—o-(c3–5环烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基),或—s(o2)(c1–3烷基),r1为f。在一些实施方式中,r2为—o-(c3–5环烷基)、—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为h。在一些实施方式中,r2为—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为f、cl、br或i。在一些实施方式中,r2为—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为h或f。在一些实施方式中,r2为—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为f。在一些实施方式中,r2为—s-(c1–3烷基)、—s(o)(c1–3烷基)或—s(o2)(c1–3烷基),r1为h。在一些实施方式中,r2为—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基—、s(o2)-甲基或—s(o2)-乙基,r1为f、cl、br或i。在一些实施方式中,r2为—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基—s(o2)-甲基或—s(o2)-乙基,r1为h或f。在一些实施方式中,r2为—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基—s(o2)-甲基或—s(o2)-乙基,r1为h。在一些实施方式中,r2为—o-环丙基、—s-甲基、—s-乙基、—s(o)-甲基、—s(o)-乙基—s(o2)-甲基或—s(o2)-乙基,r1为f。在一些实施方式中,n为0。在一些实施方式中,n为1。在一些实施方式中,n为2。在一些实施方式中,n为1、2、3或4。在一些实施方式中,n为0或1。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。在一些实施方式中,所述化合物为:或其药学上可接受的盐。本申请所述的化合物还包括同位素标记的化合物,其中一个或多个原子被具有相同原子序数,但原子质量或质量数不同于自然界常见的原子质量或质量数的原子取代。适用于包含在本申请所述化合物中的同位素的实例包括但不限于2h、3h、11c、13c、14c、36cl、18f、123i、125i、13n、15n、15o、17o、18o、32p和35s。在一个实施方式中,同位素标记的化合物可用于药物和/或底物组织分布研究。在另一个实施方式中,用较重的同位素例如氘取代具有更好的代谢稳定性(例如,体内半衰期增加或剂量要求降低)。在另一个实施方式中,用正电子发射同位素如11c、18f、15o和13n取代可用于正电子发射拓扑学(pet)研究中检查底物受体占有率。同位素标记的化合物可通过任何适当的方法或使用适当的同位素标记的试剂取代在其他方面使用的非标记试剂的方法制备。在一个实施方式中,本申请所述的化合物通过其他方式标记,包括但不限于使用发色团或荧光部分、生物发光标记或化学发光标记。本申请所述的化合物是使用本申请所述的技术和材料合成的,例如在fieserandfieser'sreagentsfororganicsynthesis,volumes1–17(johnwileyandsons,1991);rodd'schemistryofcarboncompounds,volumes1–5andsupplements(elseviersciencepublishers,1989);organicreactions,volumes1–40(johnwileyandsons,1991),larock'scomprehensiveorganictransformations(vchpublishersinc.,1989),march,advancedorganicchemistry4thed.,(wiley1992);careyandsundberg,advancedorganicchemistry4thed.,vols.aandb(plenum2000,2001),andgreeneandwuts,protectivegroupsinorganicsynthesis3rded.,(wiley1999)中所描述的(它们中的全部内容通过引用并入本申请)。通过使用适当的试剂和条件改变用于制备本申请所述化合物的一般方法来引入本申请提供的式中发现的各个基团。本申请还提供了包含本申请提供的化合物(即表1的化合物或其药学上可接受的盐)的组合物。本申请还提供了药物组合物,其包含本申请提供的化合物。方法另一方面,本申请提供了治疗有需要的受试者中癌症的方法,其包括向受试者施用本申请提供的化合物(即表1的化合物或其药学上可接受的盐)。在一些实施方式中,所述癌症是her2阳性癌症。在一些实施方式中,所述癌症是食道癌、胃癌、结肠癌、直肠癌、胰腺癌、肺癌、乳腺癌、子宫颈癌、子宫体、子宫癌、卵巢癌、膀胱癌、头颈癌、子宫内膜癌、骨肉瘤、前列腺癌、神经母细胞瘤或其组合。另一方面,本申请提供了治疗有需要的受试者中病毒感染、癌症、变应性疾病或其组合的方法,其包括向受试者施用本申请提供的化合物(即表1的化合物或药学上可接受的盐)。另一方面,本申请提供了治疗有需要的受试者中病毒感染的方法,其包括向受试者施用本申请提供的化合物(即表1的化合物或其药学上可接受的盐)。另一方面,本申请提供了治疗有需要的受试者中癌症的方法,其包括向受试者施用本申请提供的化合物(即表1的化合物或其药学上可接受的盐)。另一方面,本申请提供了治疗有需要的受试者中变应性疾病的方法,其包括向受试者施用本申请提供的化合物(即表1的化合物或其药学上可接受的盐)。在一些实施方式中,所述病毒感染包括丙型肝炎病毒(hcv)感染。在一些实施方式中,本申请提供了调节细胞中激酶活性的方法,包括使细胞与有效调节激酶活性量的本申请的化合物接触(即表1的化合物或其药学上可接受的盐)。在这些方法的一些实施方式中,所述受试者是人。另一方面,本申请提供了本申请提供的化合物(即表1的化合物或其药学上可接受的盐)、本申请提供的组合物或本申请提供的药物组合物在制备用于治疗病毒感染、癌症或过敏性疾病药物中的用途。另一方面,本申请提供了包含本申请提供的化合物和药学上可接受的载体的药物组合物。本申请提供的药物组合物中活性成分的实际剂量水平可以变化,以在对受试者无毒的情况下,得到对于特定受试者、组合物或给药方式获得期望的治疗反应的活性成分的有效量。在一些实施方式中,以剂量单位形式配制化合物是特别有利的,以易于给药和均一剂量。本申请中剂量单位形式是指适合作为待治疗受试者的单位剂量的物理上离散的单位;每个单元都包含预定量的治疗化合物,该化合物经计算可与所需的药物媒介结合以产生所需的治疗效果。本公开的剂量单位形式由以下因素决定,并直接取决于:(a)治疗化合物的独特特征和要实现的特定治疗效果,以及(b)混合/配制此类用于治疗有需要的受试者中本申请所指疾病的治疗化合物领域固有的局限性。在一个实施方式中,本申请提供的化合物或组合物是使用一种或多种药学上可接受的赋形剂或载体配制的。在一个实施方式中,本申请提供的药物组合物包含治疗有效量的本申请提供的化合物和药学上可接受的载体。在一个实施方式中,本公开内容提供了包装的药物组合物,其含有容器,该容器容纳至少一种治疗有效量的本申请提供的化合物以及使用该化合物治疗有需要的人中本申请所述的一种或多种疾病症状的说明书。本申请提供的任何组合物的施用途径包括口服、经鼻、经直肠、阴道内、肠胃外、经颊、舌下、局部或经眼。本申请提供的化合物的使用可以配制为通过任何合适的途径给药,例如眼、口服或肠胃外给药,例如透皮、透粘膜(例如舌下、舌、(经)颊、(经)尿道、阴道(例如,经阴道和引道周围)、鼻(内)和(经)直肠)、膀胱内、肺内、十二指肠内、胃内、鞘内、皮下、肌内、皮内、动脉内、静脉内、支气管内、吸入和局部给药。合适的组合物和剂型包括例如滴剂、片剂、胶囊剂、囊片、丸剂、软胶囊、锭剂、分散剂、混悬剂、溶液剂、糖浆剂、颗粒剂、珠子、透皮贴剂、凝胶剂、粉剂、丸剂、岩浆、喉糖、乳膏、糊剂、膏药、洗剂、圆盘(discs)、栓剂、用于鼻腔或口施用的液体喷雾剂,用于吸入的干粉或雾化制剂,用于眼内或膀胱内给药的组合物和制剂等。应当理解,如本申请所提供的有用的制剂和组合物不限于本申请描述的特定制剂和组合物。另一方面,本申请提供了适合施用于有需要的受试者的剂型,其包含本申请提供的化合物(即表1的化合物或其药学上可接受的盐)。另一方面,本申请提供了试剂盒,其包括含有本申请提供的化合物(即表1的化合物或其药学上可接受的盐)的组合物及其使用说明。在一些实施方式中,所述试剂盒还包括注射器、小瓶或剂型中的一种或多种。本领域技术人员仅使用常规实验就会认识到或能够确定本申请所述的具体程序、实施方式、权利要求和实施例的许多等同物。这样的等同物被认为在本公开的范围内,并由所附的权利要求书覆盖。例如,应当理解,具有本领域公认的替代方案并且仅使用常规实验进行的反应条件的改变,包括但不限于反应时间、反应大小或体积,以及实验试剂,例如溶剂、催化剂、压力、大气条件(例如氮气)以及还原或氧化剂,均在本申请的范围内。应当理解,本申请中提供数值和范围的任何地方,这些数值和范围所涵盖的所有数值和范围都包含在本公开的范围内。此外,本申请还考虑了落入这些范围内的所有值以及该值的范围的上限或下限。以下示例进一步说明了本公开的各方面。然而,它们绝不是对本申请所阐述的教导或本公开的限制。实施例在下面所示的合成方案中,除非另有说明,否则所有温度均以摄氏度表示,并且所有份数和百分数均以重量计。除非另有说明,否则试剂和溶剂均购自商业供应商,无需进一步纯化即可使用。无水四氢呋喃(thf)和n,n-二甲基甲酰胺(dmf)可从商业渠道购买,并直接使用。下面的反应通常在无水溶剂中在氩气或氮气的正压下在环境温度(除非另有说明)下进行。玻璃器皿是烘干的或加热干燥的。通过tlc测定反应或通过lc-ms分析反应,并根据原料的消耗判断反应的终止。分析薄层色谱(tlc)在预先涂有硅胶60f2540.25mm板(emscience)的玻璃板上进行,并用uv光(254nm)成像或用市售乙醇磷钼酸加热。制备薄层色谱(tlc)在预先涂有硅胶60f2540.5mm板(20×20cm,商购获得)的玻璃板上进行,并用uv光(254nm)成像。除非另有说明,通常通过以下方式进行反应的后处理:用反应溶剂或萃取溶剂将反应体积加倍,然后用25%(体积)萃取体积的指示水溶液洗涤。产物溶液经无水na2so4或mg2so4干燥,之后过滤,然后在旋转蒸发仪上减压蒸发溶剂,并记为真空下除去的溶剂。使用230-400目硅胶在正压下完成柱色谱分离。1h-nmr光谱和13c-nmr在以400mhz操作的varianmercury-vx400仪器上进行记录。nmr光谱以cdcl3溶液(以ppm为单位)获得,使用氯仿作为参考标准品(1h为7.27ppm,13c为77.00ppm),如果合适的话用cd3od(1h为3.4和4.8ppm,13c为49.3ppm),dmso-d6(1h为2.49ppm)或内四甲基硅烷(1h为0.00ppm)。根据需要使用其他nmr溶剂。实施例1:普通中间体a的合成实施例2:普通中间体b的合成实施例3:化合物1的合成实施例4:化合物2的合成实施例5:化合物3的合成实施例6:化合物4的合成实施例7:化合物5的合成实施例8:化合物6的合成实施例9:化合物10的合成实施例10:化合物11的合成实施例11:化合物12的合成实施例12:化合物13的合成实施例13:化合物14的合成实施例14:化合物15的合成实施例15:tlr7/8激动剂药代动力学研究spfsd大鼠购自biolasco台湾有限公司。动物在给药前被随机分为5组,每组3只雄性和3只雌性。所用动物的体重变动在每种性别的平均体重的±20%范围内。基本设计如表2所示。表2tlr7/8激动剂pk研究设计在给药前和给药后2分钟、5分钟、15分钟、30分钟、1小时、2小时、4小时、6小时、8小时、12小时和24小时通过尾静脉获得血样(200-350μl/时间点)。将血样收集到装有k2edta的试管中,并在冰上放置不超过30分钟,然后离心(1500-1750×g,15分钟,2-8℃)以进行血浆收集。平行制备研究样品并使用液相色谱-串联质谱法分析。在确定大鼠血浆中的浓度后进行药代动力学评估时,使用winnonlin(pharsightcorporation,版本6.3)和非隔离方法计算药代动力学参数。结果示于图1,并示于下表3(与瑞喹莫德组相比,斜体值显示出明显差异(p<0.05))。瑞喹莫德(resiquimod)是激活免疫系统的toll样受体(tlr)激动剂。表3tlr7/8激动剂的药代动力学参数实施例16:hek-bluehtlr7细胞中的tlr7/8激动剂效价测定hek-bluehtlr7细胞以3×104细胞/孔接种,并用9种浓度的阳性对照(cl264)和3种化合物(瑞喹莫德,化合物2,化合物3)处理。hek-bluetlr7细胞可通过在tlr7刺激后激活nf-κb时胚胎碱性磷酸酶(seap)的分泌来测量tlr7的生物活性。水用作阴性对照。在37℃、5%co2中孵育约16小时后,使用分光光度计在635nm下测定seap。剂量反应曲线与四参数对数曲线拟合(sigmaplot,版本9.0)。阳性对照(cl264)和受试化合物的ec50值计算值如下表4所示(与瑞喹莫德组比较,斜体值显示出显著差异(p<0.05))。表4tlr7/8激动剂的tlr7激动性ec50化合物ec50(ng/ml)cl264260.2±12.4瑞喹莫德59.9±9.0化合物236.2±3.6化合物340.5±2.2实施例17:hek-bluehtlr8细胞中的tlr7/8激动剂效价测定hek-bluehtlr8细胞以3×104细胞/孔接种,并用9种浓度的阳性对照(ssrna40)和4种测试样(瑞喹莫德,化合物2,化合物3)处理。hek-bluehtlr8细胞可通过在tlr8刺激后激活nf-κb时胚胎碱性磷酸酶(seap)的分泌来测量tlr8的生物活性。水用作阴性对照。在37℃、5%co2中孵育约16小时后,使用分光光度计在635nm下测定seap。剂量反应曲线与四参数对数曲线拟合(sigmaplot,版本9.0)。阳性对照(ssrna40)和受试化合物的ec50值的计算结果如下表5所示(与瑞喹莫德组比较,斜体值显示出显著差异(p<0.05))。表5tlr7/8激动剂的tlr8激动性ec50化合物ec50(ng/ml)ssrna402722.5±61.1瑞喹莫德375.9±1.9化合物2591.2±20.2化合物3515.5±10.5当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1