包括氧亚氨基甲苯衍生物作为活性成分的用于预防或治疗昼夜节律相关疾病的药物组合物
本发明涉及一种用于预防或治疗昼夜节律相关疾病的药物组合物,其包括氧亚氨基甲苯衍生物或其药学上可接受的盐作为活性成分。
背景技术:
像地球上所有的生物一样,人类也表现出一种昼夜节律,这种节律是根据昼夜在生理或行为方面的变化来调整的。人类最为人熟知的昼夜节律行为是睡眠,但除此之外,体温、饮食、激素、血糖水平等体内代谢活动,以及细胞分裂周期也受此昼夜节律的调节。当昼夜节律由于遗传或环境因素而被打破时,会引起各种生理或心理异常,称为昼夜节律相关障碍(circadianrhythm-relateddisorder)。尤其在工业化的现代社会,大多数人都暴露于各种原因造成的生物钟紊乱,如夜间照明过度、轮班工作等过度夜间活动、饮食模式异常等,并且,有关昼夜节律相关疾病的病因及治疗的研究的重要性也随之与日俱增。
生物体内有与昼夜节律控制相关的基因,而昼夜节律控制基因则调控着昼夜节律。通过最近的研究,控制昼夜节律的生物钟分子网络已被确定。哺乳动物昼夜节律调控基因包括period(per)基因(per1、per2、per3)、时钟基因、bmal基因(bmal1、bmal2)、cryptochrome(cry)基因(cry1、cry2)、rev-erb基因(rev-erbα、rev-erbβ)、ror基因(rora、rorb、rorc)等,它们形成一个分子网络。尤其,最高水平的时钟和bmal1蛋白的二聚体作为转录因子与位于较低水平的反馈基因per和cry基因启动子中的顺式元件(cis-element)e-box结合,并触发其表达,该基因产物抑制高水平转录因子的一系列分子循环结构是生物钟的核心,被称为生物钟核心环(coreloop)。这些分子网络通过触发受调控基因的昼夜节律来影响各种生理过程(非专利文献1)。此外,这些昼夜节律生物钟基因的分子网络不仅存在于哺乳动物中枢生物钟所在的下丘脑视交叉上核(scn,suprachiasmaticnucleus),而且还存在于各种外周器官,这些外周器官的细胞也以独立的昼夜节律周期性表达,其模式类似于视交叉上核。与中枢生物钟相比,在这样的各种外周器官中表达的生物钟分子网络被称为外周或局部时钟(peripheralorlocalclock)(非专利文献1)。
因为生物钟是控制行为和整体生理的通用控制机制,因此昼夜节律相关疾病的类型也非常广泛,包括睡眠障碍、癌症、代谢障碍、心血管疾病、免疫及炎症疾病、心境障碍、成瘾性障碍及退化性脑疾病等。
事实上,通过改变起床和睡眠的正常的24小时节律来轮班工作的急救人员等有患各种疾病的风险,包括糖尿病等代谢障碍(非专利文献2),通过对长期轮班工作的护士进行流行病学调查,发现护士轮班工作的次数和强度均高于乳腺癌发病正常人群(非专利文献3)。
到目前为止,已对很多有关各种环境和遗传生物钟紊乱而导致的昼夜节律相关疾病的病因和治疗的研究,其中之一就是通过磷酸化生物钟的关键基因来调节昼夜节律。在已被知晓哺乳动物酪蛋白激酶iε(ckiε)及酪蛋白激酶iδ(ckiδ)通过磷酸化生物钟的关键基因来调节昼夜节律后,已开始进行以cki蛋白为目标来调节昼夜节律的研究(非专利文献4)。然而,由于抑制cki基因并不直接影响生物钟分子网络,因此其作用并不显著。
另一个研究是有关rev-erbα/β(构成生物钟辅助环(auxiliaryloop)的基因)的研究,其涉及通过用于抑制bmal1表达的rev-erbα/β的激动剂(agonist)和拮抗剂(antagonist)来调节昼夜节律(非专利文献5),rev-erbα/β的主要作用是在生物钟分子网络中减缓时钟:bmal1二聚体的活性,从而进行微调,以使生物钟正常运行,然而其难以有效地调节昼夜节律。
最近发现2-乙氧基丙酸衍生物ks15可以通过抑制cry蛋白来提高时钟:bmal1二聚体的转录活性,并证实其减弱了昼夜分子生物学节律(非专利文献6)。
因此,在昼夜节律的生理和临床重要性已经显现的今天,对于预防及治疗各种与昼夜节律有关的疾病,迫切需要开发一种能够更直接有效地促进生物钟分子网络的药物。
非专利文献1:stratmannm,schibleru.properties,entrainment,andphysiologicalfunctionsofmammalianperipheraloscillators.jbiolrhythms.(2006)21(6):494-506.
非专利文献2:scheerfa,hiltonmf,mantzoroscs,sheasa.adversemetabolicandcardiovascularconsequencesofcircadianmisalignment.procnatlacadsciusa.(2009)106(11):4453-4458.
非专利文献3:schernhammeres,ladenf,speizerfe,willettwc,hunterdj,kawachii,colditzga.rotatingnightshiftsandriskofbreastcancerinwomenparticipatinginthenurses’healthstudy.jnatlcancerinst.(2001)93(20):1563-1568.
非专利文献4:chenz,yoosh,takahashijs.developmentandtherapeuticpotentialofsmall-moleculemodulatorsofcircadiansystems.annurevpharmacoltoxicol.(2018)58:231-252.
非专利文献5:kojetindj,burristp.rev-erbandrornuclearreceptorsasdrugtargets.natrevdrugdiscov.(2014)13(3):197-216.
非专利文献6:chunsk,jangj,chungs,yunh,kimnj,jungjw,songh,suhyg,kimk.identificationandvalidationofcryptochromeinhibitotsthatmodulatethemolecularcircadianclock.acschembiol.(2014)9(3):703-710.
非专利文献7:songh,chungs,choehk,kimhd,baiksm,leeh,leehw,chois,sunw,kimh,chos,leekh,kimk.adrenalperipheralclockcontrelstheautonomouscircadianrhythmofglucocorticoidbycausingrhythmicsteroidproduction.procnatlacadsciusa.(2008)105(52):20970-20975.
非专利文献8:schirmachera,horh,heidbredera,happes,kelschr,kuhlenbaumerg.meiβa
非专利文献9:wisorjp,o’harabf,teraoa,aelbycp,kilduffta,sancara,edgardm.frankenp.aroleforcryptochromesinsleepregulation.bmcneurosci.(2002)3:20.
非专利文献10:trachsell,edgardm,aeidelwf,hellerhc,dementwc.sleephomeostasisinsuprachiasmaticnuclei-lesionedrats:effectsofsleepdeprivationandtriazolamadministration.brainres.(1992)589(2):253-261.
非专利文献11:spiegelk,tasalie,leproultr,vancautere.effectsofpoorandshortsleeponglucosemetabolismandobesityrisk.natrevendocrinol.(2009)5(5):253-261.
非专利文献12:turekfw,joshuc,kohsakaa,line,ivanovag,mcdearmone,laposkya,losee-olsons,eastona,jensendr,eckelrh,takahashijs,bassj.obesityandmetabolicsyndromeincircadianclockmutantmice.science.(2005)308(5724):1043-1045.
非专利文献13:lamiaka,storchkf,weitzcj.physiologicalsignificanceofaperipheraltissuecircadianclock.procnatlacadsciusa.(2008)105(39):15172-15177.
非专利文献14:rudicrd,mcnamarap,curtisam,bostonrc,pandas,hogeneschjb,fitzgeraldga.bmallandclock,twoessentialcomponentsofthecircadianclock,areinvolvedinglucosehomeostasis.plosbiol.(2004)2(11):e377.
非专利文献15:shimbas,ishiin,ohtay,ohnot,watabey,hayashim,wadat,aoyagit,tezukam.brainandmusclearnt-likeprotein-1(bmal1),acomponentofthemolecularclock,regulatesadipogenesis.procnatlacadsciusa.(2005)102(34):12071-12076.
非专利文献16:burim,cohen-solalam,carmignacd,abecassispy,chauvetn,martinao,vanderhorstgt,robinsonic,maurelp,mollardp,bonnefontx.thecircadianclockcomponentscry1andcry2arenecessarytosustainsexdimorphisminmouselivermetabolism.jbiolchem.(2009)284(14):9066-9073.
非专利文献17:zhangee,liuy,dentinr,pongsawakulpy,liuac,hirotat,nusinowda,sunx,landaiss,kodamay,brennerda,montminym,kaysa.cryptochromemediatescircadianregulationofcampsignalingandhepaticgluconeogenesis.natmed.(2010)16(10):1152-1156.
非专利文献18:gouinjp,connorsj,kiecolt-glaserjk,glaserr,malarkeywb,atkinsonc,beversdorfd,quann.alteredexpressionofcircadianrhythmgenesamengindividualswithahistoryofdepression.jaffectdisord.(2010)126(1-2):161-166.
非专利文献19:mcclungca,sidiropoulouk,vitaternam,takahashijs,whitefj,cooperdc,nestlerej.regulationofdopaminergictransmissionandcocainerewardbytheclockgene.procnatlacadsciusa.(2005)102(26):9377-9381.
非专利文献20:chungs,leeej,yuns,choehk,parksb,sonhj,kimks,dluzende,leei,hwang0,songh,kimk.impactofcircadiannuclearreceptorrev-erbαonmidbraindopamineproductionandmoodregulation.cell.(2014)157(4):858-868.
非专利文献21:schnella,sandrellif,rancv,rippergerja,braie,alberil,rainerg,albrechtu.micelackingcircadianclockcomponentsdisplaydifferentmood-relatedbehaviorsanddonotresponduniformlytochroniclithiumtreatment.chronobiolint.(2015)32(8):1075-1089.
非专利文献22:moonjh,choch,songh,geumd,chungs,kimh,kangsg,parkym,yoonhk,kiml,jeehj,anh,kripkedf,leehj.advancedcircadianphaseinmaniaanddelayedcircadianphaseinmixedmaniaanddepressionreturnedtonormalaftertreatmentofbipolardisorder.ebiomedicine.(2016)11∶285-295.
非专利文献23:menculinig,verdolinin,murrua,pacchiarottii,volpeu,cervinoa,steardol,morettip,vietae,tortorellaa.depressivemoodandcircadianrhythmsdisturbancesasoutcomesofseasonalaffectivedisordertreatment:asystematicreview.jaffectdisord.(2018)241:608-626.
非专利文献24:hoods,amirs.neurodegenerationandthecircadianclock.frontagingneurosci.(2017)9:170.
非专利文献25:musiekea,limmm,yangg,baueraq,qil,leey,rohjh,ortiz-gonzalezx,dearbornjt,culverjp,herzoged,hogeneschjb,wozniakdf,dikraniank,giassonbi,weaverdr,holtzmandm,fitzgeraldga.circadianclockproteinsregulateneuronalredoxhomeostasisandneurodegeneration.jclininvest.(2013)123(12):5389-5400.
非专利文献26:laurettie,dimecoa,meralis,pratieod.circadianrhythmdysfunction:anovelenvironmentalriskfactorforparkinson’sdisease.molpsychiatry.(2017)22(2):280-286.
非专利文献27:gorbachevavy,kondratovrv,zhangr,cherukuris,gudkovav,takahashijs,antochmp.circadiansensitivitytothechemotherapeuticagentcyclophosphamidedependsonthefunctionalstatusoftheclock/bmal1transactivationcomplex.procnatlacadsciusa.(2005)102(9):3407-3412.
非专利文献28:ozturkn,leejh,gaddameedhis,sancara.lossofcryptochromereducescancerriskinp53mutantmice.procnatlacadsciusa.(2009)106(8):2841-2846.
非专利文献29:vanderhorstgt,muijtjensm,kobayashik,takanor,kannos,takaom,dewitj,verkerka,ekerap,vanleenend,buijsr,bootsmad,hoeijmakersjh,yasuia.mammaliancry1andcry2areessentialformaintenanceofcircadianrhythms.nature.(1999)398(6728):627-630.
非专利文献30:chunsk,chungs,kimhd,leejh,jangj,kimj,kimd,songh,ohyj,suhyg,leecs,kimk.asyntheticcryptochromeinhibitorinducesanti-proliferativeeffectsandincreaseschemosensitivityinhumanbreastcancercells.biochembiophysrescommun.(2015)467(2):441-446.
非专利文献31:yoosh,yamazakis,lowreypl,shimomurak,koch,buhred,siepkasm,honghk,ohwj,yoooj,menakerm,takahashijs.period2::luciferasereal-timereportingofcircadiandynamicsrevealspersistentcircadianoscillationsinmouseperipheraltissues.procnatlacadsciusa.(2004)101(15):5339-5346.
技术实现要素:
要解决的技术问题
在此背景下,本发明者在通过基于细胞的测试方法(测量时钟:bmal1的二聚体的活性)来开发直接作用于分子生物钟核心环的药物的过程中,发现氧亚氨基甲苯衍生物通过抑制cry的作用,增强生物钟分子网络的昼夜节律活性,由此完成了本发明。
因此,本发明的目的在于提供一种通过使用有机合成技术制备的氧亚氨基甲苯衍生物化合物及其药学上可接受的盐。
本发明的另一目在于提供一种用于预防或治疗昼夜节律相关疾病的药物组合物,其包括氧亚氨基甲苯衍生物或其药学上可接受的盐作为活性成分。
然而,本发明要解决的问题并非受限于上述言及的问题,未言及的其他问题能够通过以下记载由本领域普通技术人员所明确理解。
解决问题的技术方法
根据本发明的一实施例,提供一种用于预防或治疗昼夜节律相关疾病的药物组合物,其包括由以下化学式1表示的氧亚氨基甲苯衍生物或其药学上可接受的盐。
[化学式1]
(在所述化学式1中,
r1为c1至ci0的直链或支链烷基;c4-c10的环烷基;经添加碳、氧、氮或硫的5至7元取代或未取代的芳香族基,其中芳香族基表示呋喃基、苯硫基、苯基、噻唑基、吲哚基、异吲哚基、吡啶基、哌嗪基、哒嗪基、萘基、喹啉基,异喹啉基,其中取代基表示从由氢、卤素、氰基、硝基、羟基、c1至c10的直链或支链烷基、c1至ci0的烷氧基、c1至c10的卤代烷基、c1至c10的卤代烷氧基、c1至ci0的烷基硫代、cl至c10的烷基羰基及c1至c10的烷氧基羰基组成的群组中选择的1至4个取代基;
r2表示氢原子;从由c1至c10的直链或支链或环状烷基组成的群组中选择的取代基;
a、b、c、d、e分别独立地表示从由氢;卤素;氰基;硝基;羟基;c1至c10的直链或支链烷基;c1至c10的烷氧基;c1至c10的卤代烷基;c1至c10的卤代烷氧基;c1至c10的烷基硫代;c1至c10的烷基羰基;或c1至c10的烷氧基羰基组成的群组中选择的取代基,此时可以包括直链或支链c1至c10的烷基或烷氧基羧酸或其酯。)
根据一侧,由所述化学式1表示的氧亚氨基甲苯衍生物可以是从由以下组成的群组中选择的任一种化合物:
1)甲基{3-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
2){3-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
3)甲基(3-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
4)(3-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
5)甲基(3-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
6)(3-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
7)2-{3-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[(吡啶-2-基)甲基]乙酰胺;
8)2-{3-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[2-(1h-咪唑-2-基)乙基]乙酰胺;
9)甲基(3-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
10)(3-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
11)甲基{3-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
12){3-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
13)甲基(3-{(n-[(4-氟苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
14)(3-{n-[(4-氟苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
15)甲基{4-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
16){4-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
17)甲基(4-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
18)(4-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
19)甲基(4-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
20)(4-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
21)2-{4-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[(吡啶-2-基)甲基]乙酰胺;
22)2-{4-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[2-(1h-咪唑-2-基)乙基]乙酰胺;
23)甲基(4-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
24)(4-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
25)甲基{4-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;以及
26){4-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸。
根据一侧,所述昼夜节律相关疾病可以为睡眠障碍、代谢障碍、心血管疾病、免疫及炎症疾病、心境障碍、成瘾性障碍、退行性脑疾病或癌症。
根据一侧,所述睡眠障碍可以为时差综合征、轮班工作睡眠障碍、进行性睡眠相位综合征、睡眠相位后移症候群、呼吸相关睡眠障碍、不安腿综合征或rem睡眠行为障碍。
根据一侧,所述代谢障碍可以为肥胖、高血压、高脂血症、高血糖或多尿。
根据一侧,所述心境障碍可以为抑郁症、双相心境障碍、季节性情感障碍或焦虑性障碍。
根据一侧,所述退行性脑疾病可以为阿尔茨海默病、帕金森病、亨廷顿病或痴呆症。
根据一侧,所述心血管疾病可以为缺血性心脏病、急性心肌梗塞、脑梗塞或心房颤动。
根据一侧,所述癌症可以为大肠癌、胃癌、前列腺癌、乳腺癌、肾癌、肝癌、肺癌、子宫癌、结肠癌、胰腺癌、卵巢癌、血癌或脑瘤。
根据一侧,由所述化学式1表示的氧亚氨基甲苯衍生物可以通过抑制昼夜节律生物钟分子网络的转录调节因子crys的活性和增强时钟:bmal1二聚体的活性来增强昼夜节律的振幅,并稳定周期。
发明的效果
本发明的氧亚氨基甲苯衍生物可以通过抑制cry的作用来促进时钟:bmal1二聚体的活性,从而有效地增强生物钟分子网络的功能。因此,本发明的包括氧亚氨基甲苯衍生物或其药学上可接受的盐作为活性成分的药物组合物可以有效地用于预防或治疗与昼夜节律有关的疾病,如睡眠障碍、代谢障碍、心血管疾病、免疫及炎症疾病、心境障碍、退行性脑疾病及癌症等。
然而,本发明的效果并不限于上述效果,并且应当理解为包括可以从本发明的详细描述或权利要求中描述的本发明的配置推导出的所有效果。
附图说明
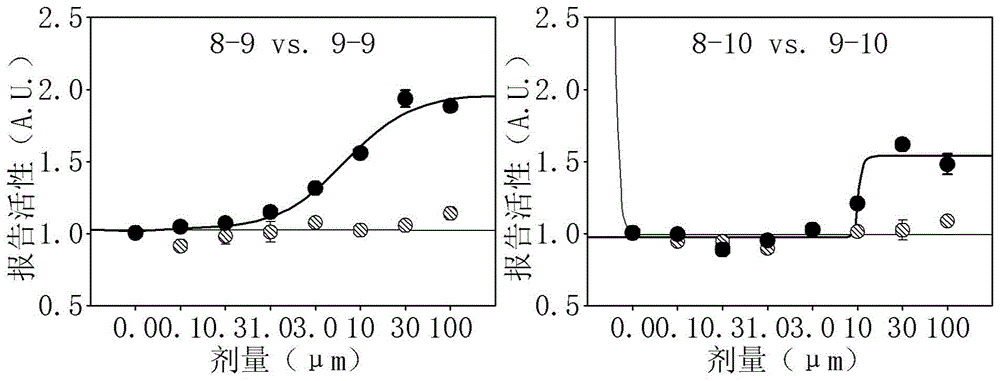
图1为评估氧亚氨基甲苯衍生物中化学式8-9、9-9、8-10及9-10的化合物对用于测量时钟:bmal1二聚体的活性e-box-luc的浓度依赖性影响,示出了化学式8-9及8-10的化合物以浓度依赖性方式增加e-box-luc的活性的结果。
图2示出时钟:bmal1二聚体(c/b)对e-box-luc报告活性的增加被cry1的过度表达所抑制,并且cry1对时钟:bmal1活性的抑制通过氧亚氨基甲苯衍生物中化学式8-9及8-10的化合物的处理,以浓度依赖性被恢复的结果。
图3a及图3b示出将氧亚氨基甲苯衍生物中化学式8-9及8-10化合物对在小鼠成纤维细胞系中观察到的per2-luc融合蛋白的昼夜节律表达的影响与作为2-乙氧基丙酸衍生物的cry抑制剂的ks15进行比较及评估的结果。图3a示出8-9、8-10的化合物及ka15对per2-luc融合蛋白的昼夜节律表达的影响,图3b示出将8-9、8-10的化合物及ks15对per2-luc融合蛋白的表达对昼夜节律的振幅(amplitude,左)、周期(period,中)及稳健性(robustness,右)的影响进行统计分析的结果。
图4a至图4c示出为小鼠提供高脂饮食(hfd,high-fatdiet)10周,化学式8-9的化合物在诱导肥胖过程中的肥胖抑制作用。在该过程中,以10mg/kg的剂量,每2天一次,通过腹腔注射向zt06注入化学式8-9的化合物,并从供应高脂饮食的第3周开始注入8周,并且作为对照组(veh,vehicle),注射包括0.1%dmso的相同体积(200μl)的盐水。
图4a示出接受10周高脂饮食及8周化学式8-9的化合物的小鼠的外观,图4b按每周示出提供高脂饮食及注入化学式8-9的化合物对小鼠体重的影响,图4c按试验组示出从开始注入化学式8-9的化合物到注入结束的时间点的体重增加量(weightgain)。
图5为在经历与图4所述相同的过程后的最后注入日后的第二天在zt02及zt12中,以scn为目标,使用定量rt-pcr技术来测量生物钟基因(bmall、npas2、rev-erbα、per2)的表达模式,并按处理组进行显示。使用tbp(tata-结合蛋白)mrna作为用于定量分析的内部对照(internalcontrol)。
图6a至6c分别示出,作为在经历与图4所述相同的过程后的最后注入日后的第二天在zt04至zt08之间的动物行为测试,每个处理组的蔗糖水偏嗜度(spt,sucrosepreferencetest)、悬尾实验(tst,tailsuspensiontest)及旷场实验(oft,openfieldtest)的结果。
具体实施方式
以下,参照附图对本发明的实施例进行详细说明。可以对以下实施例进行多种变更,因此本申请的权利范围并非受到以下实施例的限制或限定。对所有实施例的全部更改、其等同物乃至其替代物均包括在权利要求范围。
实施例中使用的术语仅用于说明特定实施例,并非用于限定实施例。在内容中没有特别说明的情况下,单数表达包括复数含义。在本说明书中,“包括”或者“具有”等术语用于表达存在说明书中所记载的特征、数字、步骤、操作、构成要素、配件或其组合,并不排除还具有一个或以上的其他特征、数字、步骤、操作、构成要素、配件或其组合,或者附加功能。
在没有其他定义的情况下,包括技术或者科学术语在内的在此使用的全部术语,都具有本领域普通技术人员所理解的通常的含义。通常使用的与词典定义相同的术语,应理解为与相关技术的通常的内容相一致的含义,在本申请中没有明确言及的情况下,不能过度理想化或解释为形式上的含义。
并且,在参照附图进行说明的过程中,与附图标记无关,相同的构成要素赋予相同的附图标记,并省略对此的重复的说明。在说明实施例的过程中,当判断对于相关公知技术的具体说明会不必要地混淆实施例时,省略对其详细说明。
根据本发明的一实施例,提供一种用于预防或治疗昼夜节律相关疾病的药物组合物,其包括由以下化学式1表示的氧亚氨基甲苯衍生物或其药学上可接受的盐。
[化学式1]
(在所述化学式1中,
r1为c1至c10的直链或支链烷基;c4-c10的环烷基;经添加碳、氧、氮或硫的5至7元取代或未取代的芳香族基,其中芳香族基表示呋喃基、苯硫基、苯基、噻唑基、吲哚基、异吲哚基、吡啶基、哌嗪基、哒嗪基、萘基、喹啉基,异喹啉基,其中取代基表示从由氢、卤素、氰基、硝基、羟基、c1至c10的直链或支链烷基、c1至c10的烷氧基、c1至c10的卤代烷基、c1至c10的卤代烷氧基、c1至c10的烷基硫代、c1至c10的烷基羰基及c1至c10的烷氧基羰基组成的群组中选择的1至4个取代基;
r2表示氢原子;从由c1至c10的直链或支链或环状烷基组成的群组中选择的取代基;
a、b、c、d、e分别独立地表示从由氢;卤素;氰基;硝基;羟基;c1至c10的直链或支链烷基;c1至c10的烷氧基;c1至c10的卤代烷基;c1至c10的卤代烷氧基;c1至c10的烷基硫代;c1至c10的烷基羰基;或c1至c10的烷氧基羰基组成的群组中选择的取代基,此时可以包括直链或支链c1至c10的烷基或烷氧基羧酸或其酯。)
更具体地,由所述化学式1表示的氧亚氨基甲苯衍生物可以是从由以下组成的群组中选择的任一种化合物:
1)甲基{3-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
2){3-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
3)甲基(3-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
4)(3-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
5)甲基(3-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
6)(3-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
7)2-{3-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[(吡啶-2-基)甲基]乙酰胺;
8)2-{3-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[2-(1h-咪唑-2-基)乙基]乙酰胺;
9)甲基(3-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
10)(3-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
11)甲基{3-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
12){3-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
13)甲基(3-{(n-[(4-氟苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
14)(3-{n-[(4-氟苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
15)甲基{4-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;
16){4-[n-{[3-(三氟甲基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸;
17)甲基(4-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
18)(4-{n-[(4-甲氧基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
19)甲基(4-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
20)(4-{n-[(4-溴苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
21)2-{4-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[(吡啶-2-基)甲基]乙酰胺;
22)2-{4-[n-(4-溴苯基)甲氧基乙亚胺基]苯氧基}-n-[2-(1h-咪唑-2-基)乙基]乙酰胺;
23)甲基(4-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸酯;
24)(4-{n-[(4-硝基苯基)甲氧基]乙亚胺基}苯氧基)乙酸;
25)甲基{4-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸酯;以及
26){4-[n-{[4-(甲磺酰基)苯基]甲氧基}乙亚胺基]苯氧基}乙酸。
由本发明的所述化学式1表示的氧亚氨基甲苯衍生物包括其药学上可接受的盐、水合物及溶剂化物。
在本说明书中,当提及由化学式1表示的化合物时,可以理解其意在包括其药学上可接受的盐,这种药学上可接受的盐可以通过制备常用盐的方法来制备。
所述“药学上可接受的盐”是指由药学上可接受的无毒碱或酸(包括无机或有机碱以及无机或有机酸)制备的盐。无机碱衍生的盐包括铝、铵、钙、铜、铁、铁、锂、镁、锰盐、锰、钾、钠、锌等。尤其,优选为铵、钙、镁、钾或钠盐。固体的盐可以存在于一个或多个晶体结构中,也可以以水合物的形式存在。从药学上可接受的无毒有机碱中提取的盐包括初级、二级或三级胺、取代胺(包括自然取代胺)、胺环或精氨酸、甜菜碱、咖啡因、胆碱、n、n’-二苯并乙基二胺、二乙胺、2-二乙基氨基乙醇、2-二甲基氨基乙醇、乙醇胺、乙二胺、n-乙基吗啉、n-乙基哌啶、葡萄糖胺、氨基葡萄糖、组氨酸、联氨酸、异丙基胺、赖氨酸、甲基葡萄糖胺、波波林、哌嗪、哌啶、聚酰胺树脂、普鲁卡因、嘌呤、可可碱、三乙胺,三甲胺、三丙胺、三甲基胺等和碱性离子交换树脂。
当本发明化合物为碱性时,盐可由药学上可接受的无毒酸(包括无机酸和有机酸)制备。所述酸包括乙酸、苯磺酸、苯甲酸、樟脑磺酸、柠檬酸、乙磺酸、富马酸、葡萄糖酸、谷氨酸、氢溴酸、盐酸、异硫氰酸、乳酸、马来酸、苹果酸、扁桃酸、甲磺酸、粘液酸(mucicacid)、硝酸、帕莫酸、泛酸,磷酸、琥珀酸、硫酸、酒石酸、对甲苯磺酸等。尤其,优选为柠檬酸、氢溴酸、盐酸、马来酸、磷酸、硫酸、富马酸或酒石酸。
可以理解,由所述化学式1表示的氧亚氨基甲苯衍生物化合物或其药学上可接受的盐的水合物包括由非共价分子间力结合的化学计量或非化学计量的量的水。所述水合物可以含有1当量以上的水,通常为1至5当量的水。这种水合物可以通过从水或含有水的溶剂中结晶本发明化学式1所表示的化合物或其药学上可接受的盐来制备。
可以理解,本发明的由所述化学式1表示的氧亚氨基甲苯衍生物化合物其药学上可接受的盐的溶剂化物包括由非共价分子间作用力结合的化学计量或非化学计量的量的溶剂。优选地,所述溶剂包括挥发性的、无毒的或适合人类施用的溶剂。
本发明的药物组合物含有作为活性成分的由化学式1表示的氧亚氨基甲苯衍生物化合物,并且向药物组合物中添加常规无毒的药学上可接受的载体、佐剂、赋形剂等,并由此可以制剂用于口服或肠外给药的磷制剂,例如片剂、胶囊剂、片剂、溶液、悬浮液等。
可用于本发明的药物组合物中的赋形剂可以包括甜味剂、粘合剂、增溶剂、增溶辅助剂、润湿剂、乳化剂、等渗剂、吸附剂、崩解剂、抗氧化剂、防腐剂、润滑剂、填充剂、香料等。例如,乳糖、葡萄糖、蔗糖、甘露醇、山梨醇、纤维素、甘氨酸、二氧化硅、滑石粉、硬脂酸、甾醇、硬脂酸镁、硅酸铝镁、淀粉、明胶、橡胶黄芩、海藻酸钠、甲基纤维素、羧甲基纤维素钠、琼脂、水、乙醇、聚乙二醇、聚乙烯吡咯烷酮、氯化钠、氯化钙、橘子香精、草莓香精、香草香精等。
本发明的药物组合物以药物有效量给药。在本发明中,“药物有效量”是指足以以适用于医疗的合理效益/风险比治疗疾病的量,有效剂量水平可以根据患者的疾病类型、严重程度、药物活性,对药物的敏感性、给药时间、给药途径及排泄率、治疗时间、包括药物同时使用因素以及在其他医学领域内有名的因素而决定。本发明的药物组合物可以作为单独的治疗剂施用或与其他治疗剂联合使用,可以与常规治疗剂按顺序或同时施用,并且可以单次或多次给药。考虑到所有上述因素,重要的是以能够以最小量获得最大效果而没有副作用的量给药,这是本领域技术人员可以容易地确定的。
具体地,根据本发明的药物组合物的有效量可根据患者的年龄、性别、状况、体重、活性成分在体内的吸收程度、失活率和排泄率、疾病类型以及将组合使用的药物而改变。例如,可以以每天0.1mg/kg至100mg/kg的量施用,优选地,以1至30mg/kg的量施用,并且可以每天施用一次或多次。
本发明的药物组合物可通过各种途径施用于受试者。所有的给药方式都是可以预期的,可以通过口服、直肠或静脉注射、肌肉注射、皮下注射、宫内硬膜注射或脑血管注射等方式给药。本发明的药物组合物根据作为活性成分的药物类型以及各种相关因素(例如,待治疗的疾病、给药途径、患者的年龄、性别和体重以及疾病的严重程度等)来确定。
本发明的药物组合物抑制cry分子的活性,从而增强分子生物钟中心的昼夜节律。因此,本发明的药物组合物包括作为活性成分的氧亚氨基甲苯衍生物化合物及其药学上可接受的盐,使得通过所述衍生物所具有的cry活性抑制作用或昼夜分子生物钟中心环增强作用来有效地用于与昼夜节律相关疾病的治疗。
所述昼夜节律相关疾病可以包括睡眠障碍、代谢障碍、心血管疾病、免疫及炎症疾病、心境障碍、成瘾性障碍、退行性脑疾病及癌症,但并不限于此。
在本发明中,“昼夜节律相关疾病”是指由于遗传或环境因素而通过抑制生物钟分子网络而表现为各种生理和心理异常的原因的疾病,并且,作为昼夜节律相关疾病,例如有包括时差和轮班工作综合征的睡眠障碍、包括肥胖和糖尿病的代谢障碍、心血管疾病、免疫和炎症性疾病、心境障碍、退化性脑疾病及癌症等。此外,疾病的类型也非常多样,这些疾病可以通过控制生物钟分子网络来预防或治疗。
例如,本发明的药物组合物具有预防、控制或治疗昼夜节律相关疾病的有效作用,例如睡眠障碍、代谢疾病、心血管疾病、免疫和炎症疾病、心境障碍、退行性脑疾病及癌症等。
此外,本发明的药物组合物可单独用于预防和治疗诸如睡眠障碍、代谢疾病、心血管疾病、免疫和炎症疾病、心境障碍、退行性脑疾病和癌症等疾病,或用于外科手术、激素治疗、药物治疗及与使用生物反应调节剂的方法结合使用。
在本发明中,术语“昼夜节律相关的睡眠障碍”是指由于施加到生物钟的遗传或环境干扰而使睡眠/觉醒节律以异常模式出现的障碍。睡眠障碍患者在社会需要的时候难以入睡或醒来,因此他们很容易抱怨睡眠不足造成的障碍,而其发病原因在于作为生物钟网络的下位基因的cry导致的睡眠障碍。根据最近对睡眠障碍患者进行的遗传学研究表明,cry1基因内含子中rs17289712的遗传多态性与该疾病的症状显着相关。这意味着cry在生物钟调节睡眠/觉醒节律中起着独特的作用(非专利文献8)。
另外,在另一个有关cry(生物钟下位基因)对睡眠的影响的研究中发现,与正常小鼠相比,同时缺陷cry1和cry2基因的小鼠增加了非快速眼动睡眠(nrems,non-remsleep),并且,非快速眼动睡眠期间δ波的强度也表现出增加的趋势(非专利文献9)。这意味着深度睡眠增加,缺陷cry1和cry2基因的小鼠的这种睡眠模式与动物模型中看到的症状不同,后者通过人为破坏下丘脑视神经间质核来破坏昼夜节律。当上核被破坏时,总睡眠时间没有变化,但睡眠模式是碎片化的,δ波的强度趋于降低(非专利文献10)。这表明,除了cry在昼夜节律钟中扮演的角色外,在睡眠稳态的调节中可以起到独立的角色。
因此,为了验证根据本发明的由化学式1表示的氧亚氨基甲苯衍生物的cry蛋白活性调节,进行了实验例1至3,结果表明,氧亚氨基甲苯衍生物化合物不仅对抑制时钟:bmal1二聚体活性的cry蛋白具有优异的抑制效果,而且对通过per2-luc融合蛋白在细胞水平上增加了昼夜分子生物节律的振幅,其增强活性效果优异。因此,本发明的包括由上述化学式1表示的氧亚氨基甲苯衍生物或其药学上可接受的盐的药物组合物可以容易地用于预防或治疗与生物钟的关键基因相关的昼夜节律相关的睡眠障碍。
有研究表明,代谢障碍是一种与昼夜节律相关的疾病,可由遗传或环境因素引起的生物钟功能异常引起。长期轮班工作或睡眠不足等不正常的生活方式会减缓体内生长激素和褪黑激素分泌的昼夜节律,并会增加皮质醇水平(非专利文件11),这些激素的变化导致类似于肥胖的初始症状的体重增加。
此外,通过基因工程动物模型的分析结果,生物钟系统与代谢障碍的关系更为明显。在时钟突变小鼠中,发现瘦素活性和胰岛素分泌减少,并出现高脂血症和高血糖症状(非专利文献12)。此外,bmal1基因缺陷小鼠的脂肪细胞生长和分化受损,肝脏碳水化合物代谢也出现异常症状(非专利文献13-15)。此外,最近的研究表明,cry在肝脏葡萄糖合成(gluconeogenesis)过程中起着重要的调节作用,而肝脏葡萄糖合成是导致高血糖的原因。与正常小鼠相比,cry缺陷小鼠血糖控制异常,这是因为cry与糖皮质激素受体(gr,glucocorticoidreceptor)结合并调节激素诱导的葡萄糖血管生成基因的表达(非专利文件16)。此外,cry不仅通过与gr结合,而且通过与g-蛋白偶联受体(g-proteincoupledreceptor)的g亚单位(gsubunit)结合来调节腺苷酸环化酶的活性,通过这一点,显示了调节作用于环磷酸腺苷(camp,cyclicadenosinemonophosphate)诱导的葡萄糖合成的基因表达的效果(非专利文献17)。
这一研究结果更清楚地表明,代谢障碍不仅与生物钟的相移有关,而且生物钟、bmal1的缺陷及cry1的异常表达也可引起代谢障碍。此外,这些结果表明,通过表达时钟和bmal1,对增强时钟:bmal1二聚体的活性及抑制cry的活性有效。
因此,为了确认根据本发明的由化学式1表示的氧亚氨基甲苯衍生物化合物的时钟:bmal1的二聚体的活性及抑制cry活性的效果,进行了实验例1至3,氧亚氨基甲苯衍生物不仅对抑制时钟:bmal1二聚体活性的cry蛋白具有优异的抑制效果,而且对通过per2-luc融合蛋白在细胞水平上增加了昼夜分子生物节律的振幅,其增强活性效果优异。
并且,通过以下实验例4的结果,对通过供应高脂肪饮食诱导肥胖的小鼠反复注入本发明化学式1所表示的氧亚氨基甲苯衍生物,结果证实具有统计显著性的减肥功效。另外,在实验例5中,当通过高脂饮食对具有位于视交叉上核中的昼夜节律中心生物钟的相位异常以及肥胖的小鼠重复注入氧亚氨基甲苯衍生物时,能够确认恢复昼夜分组节律的效果。
因此,包括根据本发明的由化学式1所表示的氧亚氨基甲苯衍生物或其可接受盐的药物组合物可有用地用于预防或治疗由生物钟的功能紊乱引起的代谢疾病。
其中,与所述昼夜节律相关的代谢障碍可以为肥胖、高血压、高脂血症、高血糖或多尿,但并不限于此。
由于昼夜节律的变化,心境障碍和成瘾性障碍也会发生,对此的研究正在积极进行中。与代谢活动和细胞分裂等生理功能类似,情绪变化(大脑的高级功能之一)也表现出昼夜节律性,在调节这些情绪中,生物钟的作用在表现出病理症状的各种类型的情绪障碍的发作和发展中也很重要。
为探讨心境障碍与昼夜节律的关系,对30名抑郁症患者和30名非抑郁症患者的血液标本进行了分析,以探讨4种昼夜节律基因的mrna表达模式。mrna表示基因活性,有抑郁症史的参与者比没有抑郁症的参与者具有更高的时钟基因活性,由此可以预测抑郁症与生物钟中的关键基因时钟的活性有关(非专利文献18)。
在心境障碍中,双相心境障碍,即狂躁性抑郁症与生物钟的关系最为显著。各种生物钟基因的基因命中率,如clock、rev-erbα、per、cry等不仅在小鼠中表现出类似于躁狂抑郁症的行为表型(非专利文献19-21),特别是在躁狂抑郁症患者出现躁狂发作前一个周期,已报告生物节律相位的调制(非专利文献22)。上述结果有力地表明,昼夜节律生物钟的活性和稳健性的减弱是躁狂抑郁症发病的关键机制。
此外,生物钟和心境障碍之间的关系可以通过光疗法(lighttherapy)来了解。作为通过除药物治疗之外还可以控制生物钟的人工刺激来治疗心境障碍的广泛使用的方法之一,光疗法被认为在季节性心境障碍中特别有效。季节性心境障碍是最常见的精神障碍之一,其中生活在四季分明的温带气候区的人口中有5-10%会出现此症状,类似于抑郁症的症状出现在冬季,太阳升起得晚,白天变短。此时,当季节性心境障碍患者被人为地暴露在强光下时,抑郁症状得到缓解,并且在清晨进行的光治疗比在晚上进行的光治疗更有效(非专利文献23)。这不仅说明季节性心境障碍的症状与生物钟的相位调节有关,而且生物钟的关键基因时钟和bmal1的表达在白天有光时被激活,而生物钟的活性:bmal1二聚体对治疗有效。
考虑到这些事实,确认了根据本发明的由化学式1表示的氧亚氨基甲苯衍生物化合物的时钟:bmal1的二聚体的活性及昼夜分子生物节律的增强效果。作为进行实验例1至3的实验结果表明,氧亚氨基甲苯衍生物不仅对抑制时钟:bmal1二聚体活性的cry蛋白具有优异的抑制效果,而且对通过per2-luc融合蛋白在细胞水平上增加了昼夜分子生物节律的振幅,其增强活性效果优异。此外,通过实验例6评估与心境障碍(如抑郁、焦虑和愉悦反应等)相关的行为表型在小鼠中的功效,其结果表明,注入氧亚氨基甲苯衍生物具有抗抑郁和抗焦虑作用。因此,本发明的包括由上述化学式1表示的氧亚氨基甲苯衍生物或其药学上可接受的盐的药物组合物可以有效地用于通过对生物钟的药理学控制来预防或治疗与心境障碍相关的疾病。
其中,与所述昼夜节律相关的心境障碍可以为抑郁症、双相心境障碍、季节性情感障碍或焦虑性障碍,但并不限于此。
由于昼夜节律的改变,各种退行性脑疾病也会发生,对此的研究正在积极进行中。在患有各种退行性脑疾病(如阿尔茨海默病、帕金森病、亨廷顿病等)的患者中,从发病开始就有包括睡眠障碍在内的昼夜节律异常的报道(非专利文献24),这成为降低退行性脑疾病患者的生活质量的主要原因。尤其,昼夜节律异常和与其相关的睡眠障碍有时被认为是帕金森病和亨廷顿病的代表性非运动症状。在最近一项使用动物模型的研究中,已经证明生物钟的活性减弱是增加患退化性脑疾病的风险并恶化症状的主要原因(非专利文献25-26)。
考虑到这些事实,执行了实验例1和实验例3,以确认根据本发明的由化学式1表示的氧亚氨基甲苯衍生物化合物的时钟:bmal1的二聚体的活性及昼夜分子生物节律的增强效果,其结果表明,昼夜分子生物节律的刺激效果优异,如提高per-luc融合蛋白表达的昼夜节律振幅以及提高时钟:bmal1二聚体的活性等。因此,本发明的包括氧亚氨基甲苯衍生物或其药学上可接受的盐的药物组合物可以有效地用于通过对生物钟的药理学控制来预防或治疗与退化性脑疾病相关的疾病。
其中,与所述昼夜节律相关的退行性脑疾病可以为阿尔茨海默病、帕金森病或亨廷顿病,但并不限于此。
癌症是一种与昼夜节律相关的疾病,其对抗癌药物敏感性的昼夜节律变化清楚地显示了生物钟关键基因与肿瘤的关系。在任何时候,cry基因打靶小鼠均表现出比正常小鼠更高的抗癌药耐药性。这种耐药性的差异在于正常小鼠和昼夜节律基因工程小鼠的肝细胞中时钟:bmal1二聚体的功能状态不同,并发现这原因在于肝脏处理抗癌药物毒性能力上的差异(非专利文献27)。本研究表明,生物周期关键基因时钟:bmal1二聚体和作为下位基因的cry对抗癌药物的作用起到重要影响。
生物钟基因除了影响抗癌药物敏感性的昼夜变化外,还更直接抑制肿瘤的形成和生长。当在肿瘤诱导的动物模型之一的p53基因缺陷小鼠中额外缺失cry时,肿瘤的形成和生长将被抑制(非专利文献28)。由于cry的基因缺陷会完全破坏个体固有的昼夜节律(非专利文献29),对生物钟的干扰和导致肿瘤发展的进展路径不一定一致,这表明可能存在更复杂的相关性。
尤其,这提示生物钟核心基因不仅在维持昼夜节律方面具有独立功能,而且在细胞周期和肿瘤发展过程中也具有独立功能,并且,其为考虑在抗癌作用中cry的暂时抑制的新可能性提供了空间。事实上,作为持续性cry抑制剂的ks15,其虽然昼夜节律增强作用不大,但对乳腺癌细胞系显示出抗癌作用(非专利文献30)。
由本发明的化学式1表示的氧亚氨基甲苯衍生物化合物具有优异的抑制cry作用的效果,如实验例1的结果所示,因此通过使用其来药理抑制cry活性,由此可以通过限制在特定时间段内的药物来提高药物的功效并降低毒性。此外,由于其抑制肿瘤细胞的生成和生长,因此含有其作为活性成分的药物组合物可以用于预防或治疗因昼夜节律改变而引起的癌症。
其中,与所述昼夜节律相关的癌症可以为大肠癌、胃癌、前列腺癌、乳腺癌、肾癌、肝癌、肺癌、子宫癌、结肠癌、胰腺癌、卵巢癌、血癌或脑瘤,但并不限于此。
制备由本发明化学式1表示的氧亚氨基甲苯衍生物的方法如下。
[反应式1]
(在所述反应式1中,a至e、r1及r2分别如上文所定义。)
更具体地,将通常可以获得的由所述化学式2表示的r1取代的胺类化合物或其盐,以及通常可以获得的由所述化学式3表示的a至e、r2取代的醛或酮化合物进行反应,从而合成由化学式1表示的氧亚氨基甲基化合物。
下面,给出优选实施例以帮助理解本发明。然而,提供以下实施例仅用于更容易理解本发明,本发明的内容并不受以下实施例的限制。
实施例1:氧亚氨基甲苯衍生物化合物(化学式8-9、化学式8-10化合物)的合成
[反应式2]
步骤1:苯乙酮衍生物(化学式6)的制备
如所述反应式2所示,将可商购的3-羟基苯乙酮(化学式4,1g)放入反应器中,并添加n,n-二甲基甲醛。将反应器冷却至0℃后,缓慢添加碳酸钾(3当量,3g)和甲基氯乙酸甲酯(化学式5,1.2当量,0.767ml),并将所述反应液的温度升高至室温,然后搅拌12小时。反应完成后,过滤所述反应液,并在减压下浓缩滤液。将所述浓缩化合物以乙酸乙酯和己烷作为流动相进行硅胶色谱,以获得目标化合物,即苯乙酮衍生物(化学式6,1453mg,产率95%)。
1h-nmr(cdcl3,500mhz)δ7.60(m,1h),7.48(m,1h),7.40(dd,j=8.1,7.5hz,1h),7.15(m,1h),4.70(s,2h),3.82(s,3h),2.60(s,3h).
[反应式3]
步骤2:氧亚氨基甲苯衍生物(化学式8-9)的制备
如所述反应式3所示,将苯乙酮衍生物(化学式6,208mg)和可商购的烷氧基胺化合物(化学式7,1.2当量,246mg)放入反应器中,并添加吡啶。将所述反应液搅拌5小时,同时加热回流。反应完成后,将所述反应液冷却至室温并进行减压浓缩。将所述浓缩化合物以乙酸乙酯和己烷作为流动相进行硅胶色谱,以获得目标化合物,即氧亚氨基甲苯衍生物化合物(化学式8-9,197mg,产率55%)。
[反应式4]
步骤3:氧亚氨基甲苯衍生物水解物(化学式8-10)的制备
如所述反应式4所示,将氧亚氨基甲苯衍生物化合物(化学式8-9,20mg)放入反应器中,并添加四氢呋喃、水和甲醇。将反应器冷却到0℃后,缓慢添加氢氧化锂(3当量,7mg),并将所述反应液的温度升高至室温,然后搅拌8小时。反应完成后,使用稀盐酸中和所述反应液,然后进行减压浓缩。使用乙酸乙酯来稀释残留物,并使用水进行洗涤,再使用无水硫酸镁进行干燥并过滤。在减压下浓缩滤液,并使用乙酸乙酯和己烷作为流动相进行硅胶色谱,以获得目标化合物,即氧亚氨基甲苯衍生物水解产物(化学式8-10,19mg,产率99%)。
除了如下[表1]所述在化学式1所表示的化合物中进行a至e、r1及r2之外,以与上述实施例1相同的方式将含有水解物的氧亚氨基甲苯衍生物(8-1至14、9-1至12)进行合成。合成的氧亚氨基甲苯衍生物化合物的结构及分析结果总结如下[表1]。
[表1]
实验例1、对时钟:bmal1二聚体的转录活性的功效评估
为了评价氧亚氨基甲苯衍生物对e-box介导的时钟:bmal1二聚体的转录活性的影响,使用了表达e-box-luc报告基因的nih-3t3成纤维细胞系(非专利文献6)。表达报告基因的成纤维细胞系使用添加有10%血清(fetalbovineserum)、1%青霉素/链霉素(streptomycin,invitrogen)和1%l-谷氨酰胺的达尔伯克(氏)改良伊格尔(氏)培养基(dulbecco’smodifiedeaglemedium,dmem),并将其维持在保持5%二氧化碳和37℃湿润状态的培养箱中进行培养。
在处理化合物前24小时,将报告表达细胞系分配到48-well培养板中培养。接着针对所培养的细胞进行化合物处理,使得最终浓度为0.1、0.3、1.0、3.0、10、30或100μm。作为对照组(0μm),使用等量的二甲基亚砜(dmso,dimethylsulfoxide)处理细胞。处理化合物36小时后,使用1xd-pbs来洗涤细胞两次,并按每个well使用100μl的细胞溶液缓冲液(possivelysisbuffer,promega)来溶解15分钟。将溶解物中20μl的样品与等量的萤光素酶活性评估试剂(lucigaseassayreagent,promega)进行反应,之后使用光度计(td-20/20luminometer,turnersystems)来测量萤光素酶活性。通过溶解物的蛋白质含量来校正所测得的荧光素酶活性,并且使用bio-rad公司的bradford染色试剂来测量蛋白质含量。
通过四参数logistic方程(fourparameterlogisticequation)将每种衍生物的浓度-反应相关性转换为标准曲线,并对其进行分析,而在计算过程采用了由sigmaplot10.0(sigmaplot8.0,systat软件公司)所提供的统计分析功能。根据浓度-反应曲线,计算每种衍生物的最大活性(max)和ec50值,并将其输入所述[表1]。在化合物中诱导细胞死亡的情况下,在ec50区显示细胞毒性(tox.)发生。作为代表性示例,化学式8-9、9-9、8-10及9-10的化合物的浓度-反应相关曲线如图1所示。
如图1和表1所示,在实施例1的化合物中,化学式8-9的化合物与对照组相比具有193.04%的最大活性,ec50值为6.44μm,在100μm内未观察到明显的细胞毒性,在最大活性、ec50和细胞毒性方面表现最佳。具有类似于化学式8-9结构的化学式8-10的化合物也显示出显著水平的最大活性(161.26%)和ec50值(10.17μm)。
实验例2、根据复合治疗的cry依赖性验证
为了验证上述实施例1中制备的化合物(8-9及8-10)是否实际上通过cry调节e-box介导的转录活性,进行了以下实验。
本实验中使用的hek293细胞系使用添加有10%血清、1%青霉素/链霉素和1%l-谷氨酰胺的达尔伯克(氏)改良伊格尔(氏)培养基(dulbecco’smodifiedeaglemedium,dmem),并将其维持在保持5%二氧化碳和37℃湿润状态的培养箱中进行培养。在转染24小时前将hek293细胞分配到48-well培养板中,除e-box-luc荧光素酶报告基因(50ng/well)和prl-mtk报告基因(100ng/well)外,将小鼠时钟表达载体(600ng/well)和小鼠bmal1表达载体(200ng/well)的混合物,或等量pcdna3.1质粒和flag-cry1表达载体(20ng/well),或等量pcdna3.1质粒导入细胞。脂质体(lipofectamine3000,invitrogen)用于转染(transfection),并且按照制造商手册进行程序。
在转染48小时后,最终处理化学式9-9或8-10的化合物,使得最终达到1、3或10μm的浓度。作为对照组(0μm),使用等量的经二甲基亚砜处理的。处理化合物36小时后,使用1xd-pbs来洗涤细胞两次,并按每个well使用100μl的细胞溶液缓冲液来溶解15分钟。将溶解物中20μl的样品与等量的萤光素酶活性评估试剂进行反应,之后使用光度计来测量萤光素酶活性。使用一起导入的prl-mtkranilla萤光素酶活性,对测定的e-box-luc荧光素酶活性进行了校正。
将每个实验组中每个衍生物处理的e-box-luc报告基因活性变化的程度转换为与对照组(仅导入e-box-luc荧光素酶报告基因、prl-mtk报告基因及pcdna3.1,并标记为经二甲基亚砜处理的组,ctl)平均值的比值,并如图2所示。结果,cry1的表达显著抑制了时钟:bmal1的e-box介导的转录活性,这种cry的作用对于化学式8-9及8-10化合物的处理以浓度依赖性方式被抑制。
如图2所示,在实施例1的化合物中,化学式8-9、8-10的化合物以cry依赖的方式促进时钟:bmal1的转录活性,因此,本发明的氧亚氨基甲苯衍生物可以作为cry蛋白的抑制剂。
实验例3、对per2-luc融合蛋白昼夜表达的衍生功效评估
评估了上述实施例1中制备的化合物(8-9及8-10)通过抑制cry和增强时钟:bmal1的转录活性对细胞表达的分子生物钟的昼夜节律表达的影响。为此,使用了突变体成纤维细胞系(per2-lucknock-infibroblast),其从per2基因的终止密码子所在位置连接荧光素酶基因,从而表达per2-luc融合蛋白。该细胞系是在出生后1周从per2-lucknock-in突变小鼠(非专利文献31)的肺组织建立的。per2-lucknock-in(ki)成纤维细胞使用添加有10%血清、1%青霉素/链霉素和1%l-谷氨酰胺的达尔伯克(氏)改良伊格尔(氏)培养基(dulbecco’smodifiedeaglemedium,dmem),并将其维持在保持5%二氧化碳和37℃湿润状态的培养箱中进行培养。
在化合物处理24小时前,将per2-luc-ki细胞分装于35mm培养皿中进行培养。将培养的细胞与200nm地塞米松(以下简称dex,dexamethasone)同步2小时后,将其替换为包括20μm的化学式8-9或8-10的化合物及荧光素酶的底物的荧光素(最终浓度0.1mm)的培养基。作为对照组,使用了等量的经二甲基亚砜(veh)处理的细胞,而不是化合物,作为另一个对照组,使用了ks15(最终浓度20μm),一种基于2-乙氧基丙酸的cry抑制剂(非专利文献6)。对照组和ks15处理的细胞也被含有相同浓度的荧光素的培养基所取代。
使用实时生物磷光测量设备(kronos-dio,atto)对培养在含有该化合物和荧光素的培养基中的细胞产生的生物磷光信号进行连续测量(间隔10分钟,持续最多5天),并对其结果通过统计趋势(detrending)进行了确认。采用cosinor分析程序(http://www.circadian.org)来分析per2-luc融合蛋白的昼夜节律表达模式,从而计算周期性的振幅(amplitude)、周期(period)及稳健性(robustness),并根据通过4次重复实验获得的结果,验证了根据化合物处理的变化的统计显着性。
结果,如图3a和图3b所示,化学式8-9或8-10的化合物处理将per2-luc融合蛋白的昼夜节律表达的幅度增加到显著水平,但对周期和稳健性没有显著影响。这与ks15形成了鲜明的对比,尽管ks15的处理增强了时钟:bmal1二聚体的转录活性,但其降低了昼夜分子节律的振幅,并将其稳健性降低到显著水平。即,与诸如ks15的2-乙氧基丙酸衍生物不同,本发明的氧亚氨基甲苯衍生物对昼夜分子生物钟的活性具有增强作用。
实验例4、衍生物对高脂饮食诱导的肥胖症的功效评估
验证上述实施例1中制备的化合物(8-9)对高脂肪饮食引起的肥胖的作用。含有相当于总热量60%的脂质的高脂饮食可引起小鼠肥胖和各种代谢异常,是应用最广泛的代谢障碍动物模型(非专利文献15)。
实验开始后,将小鼠(共28头)分为两个实验组,分别提供正常饮食(normalchow,nc,含15.2%的蛋白质和2.9%的脂质)或高脂饮食(high-fatdiet,hfd,含20.3%的蛋白质和27.0%的脂质)2周。在第3周开始时,将每个饮食组再次分为两个实验组,并将其作为注入化学式8-9化合物的组或作为对照组。对于每个饮食组的注入组,每2天一次通过腹腔内注射注入8-9化合物(每次10mg/kg体重,注入200μl),共8周,并以相同的方式向对照组注入溶剂(veh,含0.5%的二甲基亚砜的等量的生理盐水)。每周测量两次体重(1周中第一日和第四日),每天中在zt06-07时期进行测量,并将两次测量的平均值记录为相应周的体重,如图4所示。
图4a为显示在共为10周的实验结束后每个实验组的小鼠(每个7头)的外观的代表性照片,图4b示出了1周间隔体重的变化。图4c示出在8周内注入8-9或溶剂期间体重变化的结果。
如图4a至图4c所示,注入化学式8-9化合物显示出肥胖抑制作用,例如与对照组相比,将高脂肪饮食引起的体重增加减少约40%。相反地,在给予正常饮食的小鼠中,处理组和对照组之间没有统计学上的显著差异,这意味着在诱发肥胖的特定情况下出现化学式8-9化合物的注入效果,尤其化学式8-9化合物的减肥效果不是由潜在的化合物的毒性引起的。
实验例5、衍生物对高脂饮食诱导的昼夜节律异常的功效评估
如上所述,基于包括肥胖在内的代谢障碍非常频繁地伴随着昼夜节律异常的事实,验证了所述实施例1中制备的化合物(8-9)对由高脂饮食引起的视交叉上核的中枢生物钟的昼夜节律功能的影响。
为此,在完成所述实验例4所述的饮食和化合物注入的第二天,在zt02(每个实验组3头)和zt12(每个实验组4头)时处死小鼠,然后切除大脑并制备1mm厚的脑组织切片,将位于下丘脑的视交叉上核区域提取到一定的大小(宽2mm、长1mm、厚1mm)。使用被商用化的rna分离试剂盒(microrneasy,qiagen),从视交叉上核中分离rna,并使用被商用化的cdna合成试剂盒(cdnasynthesiskit,takara)为每500ng的rna样本合成cdna。对于该cdna,使用sybrgreenipcr试剂盒(invitrogen)通过定量实时pcr(quantitativereal-timepcr)来测量靶基因mrna的表达水平。生物钟基因bmal1、npas2、rev-erbα、per2的基因表达水平,以管家(house-keeping)基因之一的tata-box结合蛋白(tbp,tata-boxbindingprotein)mrna的表达水平进行校正,并且将整体结果表示为与标准rna样品中测得的基因水平的比率。测量结果如图5所示。
如图5所示,当通过高脂饮食诱导肥胖(hfd及veh)时,与接受正常饮食并注入溶剂的对照组的小鼠(nc及veh)不同,bmal1及reverbα的昼夜节律表达会消失,并且npas2mrna的表达模式逆转。相反地,尽管提供了高脂肪饮食,但在注入实施例1的化合物的小鼠(hfd及8-9)中,这些生物钟基因的表达保持正常。如实验例4所示,即使在接受正常饮食并注入化合物8-9的小鼠组(nc及8-9)中,生物钟基因的昼夜节律表达模式也呈正常。
上述结果与实验例3的培养细胞模型的结果一致,实施例1的衍生物(8-9)的注入有助于增强体内昼夜分子生物钟,因此这结果表明,即使在伴随着昼夜节律紊乱的肥胖动物模型中,不仅可以减轻体重,还可以维持中枢生物钟的昼夜节律功能。
实验例6、衍生物对脑功能的情绪及成瘾性控制的功效评估
如上所述,基于情绪和成瘾性障碍频繁伴随昼夜节律异常的事实,验证了根据本发明的上述实施例1中制备的化合物(8-9)对小鼠情绪和成瘾相关行为造成的影响。
为此,将化合物(8-9)或溶剂以实验例4中所述的相同剂量(每2天一次,10mg/kg体重,注入200μl)反复注入6周,然后依次进行以下三种动物的行为测试,结果如图6a至6c所示。在行为测试期间,以相同的方式注入化合物和溶剂。
蔗糖水偏嗜度(sucrosepreferencetest)(以下简称spt)是一种用于测量与成瘾风险和抑郁相关的愉悦反应的行为测试方法(非专利文献20)。将普通饮用水和2%的糖水分别放入同一形式的饮用水瓶中,给受试小鼠饮用48小时。在第3天改变两个饮用水瓶的位置后,测量24小时间内所消耗的普通饮用水和2%的糖水的重量。糖水偏嗜度表示为糖水消耗量相对于总消耗量(一般饮用水和糖水消耗量之和)的百分比,但两组小鼠之间没有显著差异(图6a)。虽然许多显示出代谢和情绪改善效果的物质具有很高的成瘾风险,但本实验例的结果意味着,化学式8-9化合物的治疗不会在愉悦反应中引起大问题。
悬尾实验(tailsuspensiontest)(以下简称tst)是一种测量诱发抑郁风险的行为测试方法(非专利文献20)。将受试小鼠的尾部固定到预先安装的支架上后,对小鼠的运动进行6分钟的拍摄。除呼吸外没有其他动作被定义为“不动性(immobility)”,6分钟内出现不动性的时间表示为%,抑郁程度越高,不动时间越长,而具有抗抑郁作用的药物越可以缩短不动反应的时间。与对照组相比,注入化学式8-9化合物的小鼠的不动时间减少到具有统计学意义的水平,这意味着化学式8-9化合物具有抗抑郁作用(图6b)。
旷场实验(openfieldtest)(以下简称oft)是一种测量小鼠焦虑的行为测试方法(非专利文献20)。当受试小鼠被单独留在一个顶部开放的房间(宽、长和深各45cm)时,它们本能地倾向于停留在墙壁的边缘,而不是开放空间的中心区域。因此,在拍摄小鼠行为15分钟后,停留在中心区域的时间(占总面积的25%)表示为%,焦虑程度越高,在中心区停留的时间越短,而当注入具有抗焦虑作用的药物时,它们留在中心区域的时间会增加。与对照组相比,注入化学式8-9化合物的小鼠在中心区域停留的时间增加到具有统计学意义的水平,这意味着化学式8-9化合物具有抗焦虑作用(图6c)。注入组和对照组在试验箱内15分钟的总移动距离没有显示出显著差异,这不是由于tst不动性时间或oft中心区占用时间的差异导致的运动功能调节,事实上,这是由焦虑差异引起的特征(图6c)。
另外,根据本发明的所述化学式1所表示的氧亚氨基甲苯衍生物可以根据用途以各种形式制剂。以下说明几种制剂方法,其中包括根据本发明的所述化学式1表示的化合物作为活性成分。
制剂例1、片剂的制备(加压法)
作为活性成分,筛选由本发明化学式1表示的化合物5.0mg,然后与乳糖14.1mg、交聚维酮usnf0.8mg及硬脂酸镁0.1mg进行混合,并压制成片剂。
制剂例2、片剂的制备(湿法造粒)
作为活性成分,筛选由本发明化学式1表示的化合物5.0mg,然后与乳糖16.0mg和淀粉4.0mg进行混合。将0.3mg的聚山梨酯80溶解在纯水中后,添加适量的该溶液,然后雾化。干燥后,筛分细颗粒,并与胶态二氧化硅2.7mg及硬脂酸镁2.0mg进行混合。将细颗粒压制成片剂。
制剂例3、粉末及胶囊剂的制备
作为活性成分,筛选由本发明化学式1表示的化合物5.0mg,然后与乳糖14.8mg、聚乙烯吡咯烷酮10.0mg及硬脂酸镁0.2mg进行混合。使用合适的装置将混合物填充在稳固的no.5明胶胶囊中。
制剂例4、注射剂的制备
作为活性成分,包括由本发明化学式1表示的化合物100mg,并且另外包括甘露醇180mg、na2hpo4、12h2o26mg及蒸馏水2974mg以制备注射剂。
综上,通过有限的实施例及附图对实施例进行了说明,本领域的普通技术人员能够对上述记载进行多种修改与变形。例如,所说明的技术以与所说明的方法不同的顺序执行,和/或所说明的构成要素以与所说明的方法不同的形态结合或组合,或者,由其他构成要素或等同物进行替换或置换也能够获得相同的效果。
由此,其他体现、其他实施例及权利要求范围的均等物全部属于专利权利要求的范围。
- 还没有人留言评论。精彩留言会获得点赞!