靶向CD371的抗原识别受体及其用途的制作方法
中的一种或多种包含在具有异源序列的融合蛋白中以形成细胞外抗原结合结构域。
11.在某些实施方式中,细胞外抗原结合结构域包含:
12.(a)重链可变区cdr1,其包含seq id no:28所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:29所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:30所示的氨基酸序列或其保守修饰;
13.(b)重链可变区cdr1,其包含seq id no:34所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:35所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:36所示的氨基酸序列或其保守修饰;
14.(c)重链可变区cdr1,其包含seq id no:40所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:42所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:43所示的氨基酸序列或其保守修饰;
15.(d)重链可变区cdr1,其包含seq id no:462所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:47所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:48所示的氨基酸序列或其保守修饰;
16.(e)重链可变区cdr1,其包含seq id no:52所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:53所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:54所示的氨基酸序列或其保守修饰;或
17.(f)重链可变区cdr1,其包含seq id no:58所示的氨基酸序列或其保守修饰;重链可变区cdr2,其包含seq id no:59所示的氨基酸序列或其保守修饰;和重链可变区cdr3,其包含seq id no:60所示的氨基酸序列或其保守修饰。
18.在某些实施方式中,细胞外抗原结合结构域包含:重链可变区cdr1,其包含seq id no:28所示的氨基酸序列;重链可变区cdr2,其包含seq id no:29所示的氨基酸序列;和重链可变区cdr3,其包含seq id no:30所示的氨基酸序列。
19.在某些实施方式中,细胞外抗原结合结构域包含:
20.(a)轻链可变区cdr1,其包含seq id no:31所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:32所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:33所示的氨基酸序列或其保守修饰;
21.(b)轻链可变区cdr1,其包含seq id no:37所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:38所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:39所示的氨基酸序列或其保守修饰;
22.(c)轻链可变区cdr1,其包含seq id no:43所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:44所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:45所示的氨基酸序列或其保守修饰;
23.(d)轻链可变区cdr1,其包含seq id no:49所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:50所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:51所示的氨基酸序列或其保守修饰;
24.(e)轻链可变区cdr1,其包含seq id no:55所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:56所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:57所示的氨基酸序列或其保守修饰;或
25.(f)轻链可变区cdr1,其包含seq id no:61所示的氨基酸序列或其保守修饰;轻链可变区cdr2,其包含seq id no:62所示的氨基酸序列或其保守修饰;和轻链可变区cdr3,其包含seq id no:63所示的氨基酸序列或其保守修饰。
26.在某些实施方式中,细胞外抗原结合结构域包含:重链可变区cdr1,其包含seq id no:28所示的氨基酸序列;重链可变区cdr2,其包含seq id no:29所示的氨基酸序列;和重链可变区cdr3,其包含seq id no:30所示的氨基酸序列。
27.在某些实施方式中,细胞外抗原结合结构域包含:
28.(a)重链可变区cdr1,其包含seq id no:28所示的氨基酸序列;重链可变区cdr2,其包含seq id no:29所示的氨基酸序列;重链可变区cdr3,其包含seq id no:30所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:31所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:32所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:33所示的氨基酸序列;
29.(b)重链可变区cdr1,其包含seq id no:34所示的氨基酸序列;重链可变区cdr2,其包含seq id no:35所示的氨基酸序列;重链可变区cdr3,其包含seq id no:36所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:37所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:38所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:39所示的氨基酸序列;
30.(c)重链可变区cdr1,其包含seq id no:40所示的氨基酸序列;重链可变区cdr2,其包含seq id no:41所示的氨基酸序列;重链可变区cdr3,其包含seq id no:42所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:43所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:44所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:45所示的氨基酸序列;
31.(d)重链可变区cdr1,其包含seq id no:46所示的氨基酸序列;重链可变区cdr2,其包含seq id no:47所示的氨基酸序列;重链可变区cdr3,其包含seq id no:48所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:49所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:50所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:51所示的氨基酸序列;
32.(e)重链可变区cdr1,其包含seq id no:52所示的氨基酸序列;重链可变区cdr2,其包含seq id no:53所示的氨基酸序列;重链可变区cdr3,其包含seq id no:54所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:55所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:56所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:57所示的氨基酸序列;或
33.(f)重链可变区cdr1,其包含seq id no:58所示的氨基酸序列;重链可变区cdr2,其包含seq id no:59所示的氨基酸序列;重链可变区cdr3,其包含seq id no:60所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:61所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:62所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:63所示的氨基酸序列。
34.在某些实施方式中,细胞外抗原结合结构域包含:重链可变区cdr1,其包含seq id no:28所示的氨基酸序列;重链可变区cdr2,其包含seq id no:29所示的氨基酸序列;重链
可变区cdr3,其包含seq id no:30所示的氨基酸序列;轻链可变区cdr1,其包含seq id no:31所示的氨基酸序列;轻链可变区cdr2,其包含seq id no:32所示的氨基酸序列;和轻链可变区cdr3,其包含seq id no:33所示的氨基酸序列。。
35.在某些实施方式中,细胞外抗原结合结构域包含重链可变区,该重链可变区包含与seq id no:1、seq id no:3、seq id no:5、seq id no:7、seq id no:9或seq id no:11所示的氨基酸序列具有至少约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含重链可变区,该重链可变区包含seq id no:1、seq id no:3、seq id no:5、seq id no:7、seq id no:9或seq id no:11所示的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含重链可变区,该重链可变区包含seq id no:1所示的氨基酸序列。
36.在某些实施方式中,细胞外抗原结合结构域包含轻链可变区,该轻链可变区包含与seq id no:2、seq id no:4、seq id no:6、seq id no:8、seq id no:10或seq id no:12所示的氨基酸序列具有至少约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含轻链可变区,该轻链可变区包含包含seq id no:2、seq id no:4、seq id no:6、seq id no:8、seq id no:10或seq id no:12所示的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含轻链可变区,该轻链可变区包含seq id no:2所示的氨基酸序列。
37.在某些实施方式中,细胞外抗原结合结构域包含:(a)重链可变区,其包含与seq id no:1、seq id no:3、seq id no:5、seq id no:7、seq id no:9或seq id no:11所示的氨基酸序列具有至少约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%同源性或同一性的氨基酸序列;和(b)轻链可变区,其包含与seq id no:2、seq id no:4、seq id no:6、seq id no:8、seq id no:10或seq id no:12所示的氨基酸序列具有至少约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含:(a)重链可变区,其包含seq id no:1、seq id no:3、seq id no:5、seq id no:7、seq id no:9或seq id no:11所示的氨基酸序列;和(b)轻链可变区,其包含seq id no:2、seq id no:4、seq id no:6、seq id no:8、seq id no:10或seq id no:12所示的氨基酸序列。
38.在某些实施方式中,细胞外抗原结合结构域包含:
39.(a)包含seq id no:1所示的氨基酸序列的重链可变区,和包含seq id no:2所示的氨基酸序列的轻链可变区;
40.(b)包含seq id no:3所示的氨基酸序列的重链可变区,和包含seq id no:4所示的氨基酸序列的轻链可变区;
41.(c)包含seq id no:5所示的氨基酸序列的重链可变区,和包含seq id no:6所示的氨基酸序列的轻链可变区;
42.(d)包含seq id no:7所示的氨基酸序列的重链可变区,和包含seq id no:8所示
的氨基酸序列的轻链可变区;
43.(e)包含seq id no:9所示的氨基酸序列的重链可变区,和包含seq id no:10所示的氨基酸序列的轻链可变区;或
44.(f)包含seq id no:11所示的氨基酸序列的重链可变区,和包含seq id no:12所示的氨基酸序列的轻链可变区。
45.在某些实施方式中,细胞外抗原结合结构域包含重链可变区,其包含seq id no:1所示的氨基酸序列;和轻链可变区,其包含seq id no:2所示的氨基酸序列。
46.在某些实施方式中,细胞外抗原结合结构域包含细胞外抗原结合结构域的重链可变区和轻链可变区之间的接头。在某些实施方式中,接头具有seq id no:13、seq id no:14、seq id no:91、seq id no:92、seq id no:93或seq id no:94所示的氨基酸序列。在某些实施方式中,接头具有seq id no:13或seq id no:14所示的氨基酸序列。
47.在某些实施方式中,细胞外抗原结合结构域包含共价连接至细胞外抗原结合结构域的5’末端的信号肽。在某些实施方式中,细胞外抗原结合结构域包含重链可变区和轻链可变区,重链可变区和轻链可变区位置从n末端到c末端为:v
h-v
l
。
48.在某些实施方式中,细胞外抗原结合结构域以低结合亲和力结合cd371。在某些实施方式中,细胞外抗原结合结构域以1
×
10-8
m或更高的解离常数(kd)结合cd371。
49.在某些实施方式中,跨膜结构域包含cd28多肽。在某些实施方式中,细胞内信号传导结构域包含cd3ζ多肽。在某些实施方式中,细胞内信号传导结构域还包含至少一个共刺激信号传导区。在某些实施方式中,至少一个共刺激信号传导区包含cd28多肽、4-1bb多肽、ox40多肽、icos多肽、dap-10多肽、或其组合。在某些实施方式中,至少一个共刺激信号传导区包含cd28多肽或4-1bb多肽。
50.在某些实施方式中,抗原识别受体是嵌合抗原受体(car)、t细胞受体(tcr)或t细胞样融合蛋白。在某些实施方式中,抗原识别受体是car。
51.在某些实施方式中,抗原识别受体重组表达。在某些实施方式中,抗原识别受体由载体表达。在某些实施方式中,载体是γ-逆转录病毒载体。
52.本公开的主题提供包含本公开的抗原识别受体的细胞。在某些实施方式中,用抗原识别受体转导细胞。在某些实施方式中,抗原识别受体在细胞表面上组成型表达。
53.在某些实施方式中,对细胞工程化以表达细胞因子或其片段。在某些实施方式中,细胞还包含细胞因子或其片段的外源多肽。在某些实施方式中,细胞还包含编码细胞因子或其片段的核酸分子。在某些实施方式中,细胞因子选自il-18、il-33、il-36、及其组合。在某些实施方式中,细胞因子是il-18。
54.在某些实施方式中,细胞是免疫应答细胞。在某些实施方式中,细胞是淋巴谱系的细胞或骨髓谱系的细胞。在某些实施方式中,细胞选自t细胞、自然杀伤(nk)细胞和可分化成淋巴样细胞的干细胞。
55.在某些实施方式中,细胞是t细胞。在某些实施方式中,t细胞是细胞毒性t淋巴细胞(ctl)或调节性t细胞。在某些实施方式中,干细胞是多能干细胞。在某些实施方式中,多能干细胞是胚胎干细胞或诱导的多能干细胞。
56.本公开的主题还提供了编码本公开的抗原识别受体的核酸分子。
57.在某些实施方式中,核酸分子包含seq id no:22、seq id no:23、seq id no:24、
seq id no:25、seq id no:26或seq id no:27所示的核苷酸序列。在某些实施方式中,核酸分子包含seq id no:22所示的核苷酸序列。本公开的主题还提供包含本公开的核酸分子的载体。在某些实施方式中,载体是病毒载体。在某些实施方式中,载体是γ-逆转录病毒载体。
58.此外,本公开的主题提供表达本文公开的核酸分子的宿主细胞。
59.在某些实施方式中,宿主细胞是t细胞。
60.本公开的主题还提供包含本文公开的细胞的组合物。在某些实施方式中,该组合物是还包含药学上可接受的载体的药物组合物。
61.本公开的主题还提供减少受试者中肿瘤负荷的方法。在某些实施方式中,该方法包括向受试者施用有效量的本公开的细胞或组合物。
62.在某些实施方式中,该方法减少受试者中的肿瘤细胞的数量、减小受试者中的肿瘤大小、和/或根除受试者中的肿瘤。本公开的主题还提供增加或延长患有肿瘤或瘤形成的受试者的生存期的方法。在某些实施方式中,该方法包括向受试者施用有效量的本公开的细胞或组合物。本公开的主题还提供治疗和/或预防受试者中肿瘤或瘤形成的方法。在某些实施方式中,该方法包括向受试者施用有效量的本公开的细胞或组合物。在某些实施方式中,肿瘤或瘤形成选自急性髓性白血病(aml)、多发性骨髓瘤、非霍奇金氏淋巴瘤、霍奇金氏淋巴瘤、慢性淋巴细胞性白血病(cll)、胶质母细胞瘤、骨髓增生异常综合征(mds)和慢性髓细胞性白血病(cml)。在某些实施方式中,肿瘤或瘤形成是急性髓性白血病(aml)。
63.本公开的主题还提供用于产生包含靶向cd371的抗原识别受体的本公开的细胞的方法。在某些实施方式中,该方法包括将编码抗原识别受体的核酸分子引入细胞中。
64.此外,本公开的主题提供用于减少受试者中肿瘤负荷、治疗和/或预防受试者中肿瘤或瘤形成、和/或增加或延长患有肿瘤或瘤形成的受试者的生存期的试剂盒。在某些实施方式中,试剂盒包含本文所述的细胞。在某些实施方式中,该试剂盒还包含使用该细胞用于减少受试者中肿瘤负荷、治疗和/或预防受试者中肿瘤或瘤形成、和/或增加或延长患有肿瘤或瘤形成的受试者的生存期的书面说明。
附图说明
65.以下详细说明以实例的方式给出,但不旨在将本发明限制于所描述的特定实施方式,可以结合附图来理解。
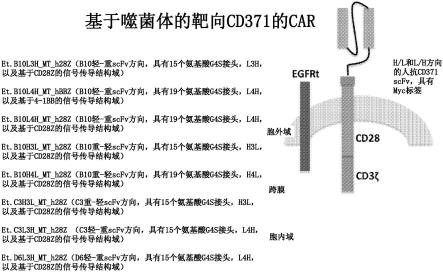
66.图1描述根据本公开的主题的抗原识别受体的结构。
67.图2描述在转导的人t细胞表面上检测到靶向cd371的car。针对egfrt(cetuximab-apc)和myc-标签(9b11-pe)的抗体检测基于b10的car构建体中egfrt和人抗-人car的表面表达。对照包括不表达egfrt或myc-标签的非转导人t细胞,以及含有非myc-标签的car构建体etah19h28z(抗-人cd19 car t细胞)和etc1hvh28z(衍生自小鼠的抗-人cd371抗体107537的抗-cd371 car t细胞)。
68.图3描述靶向cd371的car t细胞的肿瘤细胞裂解活性。休息4天(4dr),将靶向人cd371的car t细胞与表达gfp和萤火虫荧光素酶(u937gl)的cd33
+
/cd371
+
u937细胞以不同的效应物:肿瘤(e:t)比共培养。24小时后测量生物发光并将其绘制为在非功能性car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号
百分比。et.c1hvh28z代表衍生自小鼠抗-人cd371抗体1075.7的靶向cd371的car,并且etm195mth28z代表衍生自鼠抗-cd33抗体m195的靶向cd33的car t细胞(参见zhao等,haematologica(2010):95:71
–
78(2010))。
69.图4描述靶向cd371的car t细胞在24小时杀伤试验中的肿瘤细胞裂解活性。健康供体来源(称为“供体c”)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶(u937gl)的cd33
+
/cd371
+
u937细胞以不同的效应物:肿瘤(e:t)比共培养。24小时后测量生物发光并将其绘制为在非功能性car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。et.c1hvh28z代表衍生自小鼠抗-人cd371抗体1075.7的靶向cd371的car,并且etm195mth28z代表衍生自鼠抗-人cd33抗体m195的靶向cd33的car t细胞。
70.图5描述靶向cd371的car t细胞在24小时杀伤试验中的肿瘤细胞裂解活性。健康供体来源(称为“供体d”)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶(u937gl)的cd33
+
/cd371
+
u937细胞以不同的效应物:肿瘤(e:t比)共培养。24小时后测量生物发光并将其绘制为在非功能性car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。et.c1hvh28z代表衍生自小鼠抗-人cd371抗体1075.7的靶向cd371的car,并且etm195mth28z代表衍生自鼠抗-人cd33抗体m195的靶向cd33的car t细胞。
71.图6描述靶向cd371的car t细胞在递归刺激测定中的活性。健康供体来源(称为“供体c”)靶向cd371的car t细胞与cd33
+
/cd371
+
u937gl细胞以1:12.5的e:t比和30,000car阳性/ml的浓度共培养。大约每4-5天对car t细胞进行计数,并通过流式细胞术进行表征,然后将初始数量的肿瘤细胞添加回培养物中(如箭头所示)。et.b10lhdel代表无功能的car t细胞(缺少信号传导结构域);et.c1hvh28z代表衍生自小鼠抗-人cd371抗体1075.7的靶向cd371的car,etm195mth28z代表衍生自鼠抗人cd33抗体m195的靶向cd33的car t细胞。
72.图7描述靶向cd371的car t细胞在递归刺激测定中的活性。健康供体来源(称为“供体d”)靶向cd371的car t细胞与cd33
+
/cd371
+
u937gl细胞以1:12.5的e:t比和30,000car阳性/ml的浓度共培养。大约每4-5天对car t细胞进行计数,并通过流式细胞术进行表征,然后将初始数量的肿瘤细胞添加回培养物中(如箭头所示)。et.b10lhdel代表无功能的car t细胞(缺少信号传导结构域);et.c1hvh28z代表衍生自小鼠抗-人cd371抗体1075.7的靶向cd371的car,并且etm195mth28z代表衍生自鼠抗-人cd33抗体m195的靶向cd33的car t细胞。
73.图8a和8b描述来自不同健康供体的靶向cd371的car t细胞(第二代基于b10hl的car t细胞和基于b10lh的car t细胞)在u937gl 24小时杀伤试验中的体外抗肿瘤活性。健康人供体来源(称为“供体a”和“供体b”)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶的cd371阳性u937细胞(u937gl)以不同的效应物:肿瘤比共培养。24小时后测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。图8a显示供体a的结果。图8b显示供体b的结果。
74.图9a和9b描述来自不同健康供体的靶向cd371的car t细胞(第二代基于b10hl的car t细胞和基于b10lh的car t细胞)在hl60gl 24小时杀伤试验中的体外抗肿瘤活性。健
康人供体来源(称为“供体a”和“供体b”)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶的cd371阳性hl60细胞(hl60gl)以不同的效应物:肿瘤比共培养。24小时后测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和hl60gl的共培养物中检测到的信号百分比。图9a显示供体a的结果。图9b显示供体b的结果。
75.图10a和10b描述人cd371(hcd371)crispr敲除细胞系的产生。用crispr从hl60gl(图10a)和u937gl(图10b)中敲除人cd371。使用抗人cd371 apc偶联抗体通过流式细胞术确认敲除。图10a显示hl60gl的敲除。图10b显示u937gl的敲除。
76.图11a和11b描述来自不同的健康供体的靶向cd371的car t细胞(第二代基于b10的car t细胞,即基于b10-hl和b10lh的car t细胞)在24小时杀伤试验中对抗原阴性u937gl的细胞毒性活性。健康人供体来源(称为“供体a”和“供体b”)靶向cd371的car t细胞与表达rfp和海萤荧光素酶(u937rfpcyp.371ko)的cd371阴性u937细胞以不同的效应物:肿瘤比共培养。24小时后测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937rfpcyp.371ko的共培养物中检测到的信号百分比。图11a显示供体a的结果。图11b显示供体b的结果。
77.图12a和12b描述来自不同的健康供体的靶向cd371的car t细胞(第二代基于b10的car t细胞,即基于b10-hl和b10lh的car t细胞)在24小时杀伤试验中对抗原阴性hl60gl的细胞毒性活性。健康人供体来源(称为“供体a”和“供体b”)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶(hl60l.371ko)的cd371阴性hl60细胞以不同的效应物:肿瘤比共培养。24小时后测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和hl60gl.371ko的共培养物中检测到的信号百分比。图12a显示供体a的结果。图12b显示供体b的结果。
78.图13a和13b描述靶向cd371的car t细胞(第二代基于b10的car t细胞,即基于b10-hl和b10lh的car t细胞)的干扰素γ(ifn-γ)分泌。靶向人cd371的car t细胞单独与cd371阴性u937细胞或与cd371+u937细胞以1:1的效应物:肿瘤比(e:t)(200μl中4.0
×
104:4.0
×
104个细胞)共培养。24小时后,收集上清液并使用基于珠的多重测定测量ifn-γ。图13a显示供体a的结果。图13b显示供体b的结果。
79.图14a和14b描述靶向cd371的car t细胞(第二代基于b10的car t细胞,即基于b10-hl和b10lh的car t细胞)的白细胞介素-2(il-2)分泌。靶向人cd371的car t细胞单独与cd371阴性u937细胞或与cd371+u937细胞以1:1的效应物:肿瘤比(e:t)(200μl中4.0
×
104:4.0
×
104个细胞)共培养。24小时后,收集上清液并使用基于珠的多重测定测量il-2。图14a显示供体a的结果。图14b显示供体b的结果。
80.图15a和15b描述靶向cd371的car t细胞(第二代基于b10的car t细胞,即基于b10-hl和b10lh的car t细胞)的肿瘤坏死因子α(tnf-α)分泌。靶向人cd371的car t细胞单独与cd371阴性u937细胞或与cd371+u937细胞以1:1的效应物:肿瘤比(e:t)(200μl中4.0
×
104:4.0
×
104个细胞)共培养。24小时后,收集上清液并使用基于珠的多重测定测量tnf-α。图15a显示供体a的结果。图15b显示供体b的结果。
81.图16a和16b描述基于b10的car t细胞在递归刺激测定中的细胞增殖。靶向cd371的car t细胞由两名健康供体(供体a和供体b)产生。car t细胞与cd371+u937gl以1:5的e:t
比和50,000car阳性/ml的浓度共培养。大约每5天,通过流式细胞术对car t细胞进行计数和表征。将初始数量的肿瘤细胞添加回培养物中(如箭头所示)。图16a显示供体a的结果。图16b显示供体b的结果。
82.图17示出aml的鼠异种移植模型。ncg小鼠通过尾静脉接种5
×
104u937glamlfab-m5细胞系。三天后,将靶向cd371的car t细胞施用于小鼠。大约每5天用生物发光成像无创测量肿瘤动力学,并监测存活率。
83.图18描述用靶向人cd371的car t细胞治疗的aml细胞系异种移植小鼠(供体1)的存活率。ncg小鼠接种5
×
104u937gl肿瘤细胞,三天后用大约1.25
×
106个靶向人cd371的car t细胞治疗。监测小鼠的存活率。
84.图19描述用靶向人cd371的car t细胞治疗的aml细胞系异种移植小鼠(供体2)的存活率。ncg小鼠接种u937gl肿瘤细胞,并在三天后用大约1.25
×
106个靶向人cd371的car t细胞治疗。监测小鼠的存活率。
85.图20描述基于b10的car t细胞的体内活性。ncg小鼠接种5
×
104u937gl肿瘤细胞,并在三天后用不同剂量的靶向cd371的car t细胞(1.25
×
105、2.5
×
105、5.0
×
105和1.0
×
106)处理。在55天(图20a)和60天(图20b)内监测小鼠的存活率。图21描述scfv与表达人cd371的hek293细胞的结合。
86.图22描述第二代基于b10hl的car t细胞对cd371阳性靶标的体外细胞毒性。基于b10hl的car t细胞具有不同长度的g4s接头。健康人供体来源(包括供体a和b)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶的抗原阳性u937细胞(u937gl)以不同的效应物:肿瘤比共培养。24小时后测量生物发光,并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。
87.图23描述基于b10的car t细胞的体内活性。ncg小鼠接种5
×
104u937gl肿瘤细胞,并用5
×
105car t细胞治疗。监测小鼠的存活率。b10h3l、b10h5l和分泌il33的b10h4l靶向人cd371的car t细胞在体内优于基于b10h4l的car t细胞。
88.图24描述基于b10的car t细胞的体内活性。ncg小鼠接种5
×
104u937gl肿瘤细胞,并用2.5
×
105car t细胞治疗。监测小鼠的存活率。分泌il18和il33的b10h4l靶向人cd371的car t细胞在体内优于基于b10h4l的car t细胞。
89.图25描述基于b10的car t细胞的体内活性。ncg小鼠接种5
×
104u937gl肿瘤细胞,并用1.0
×
105car t细胞治疗。监测小鼠的存活率。在1.0
×
105的低剂量下,分泌il18的b10h4l靶向人cd371的car t细胞在体内优于所有其他构建体。
具体实施方式
90.本公开的主题提供特异性靶向cd371的抗原识别受体(例如,嵌合抗原受体(car)或t细胞受体(tcr))。本公开的主题还提供包含这种受体的细胞。该细胞可以是免疫应答细胞,例如,遗传修饰的免疫应答细胞(例如,t细胞或nk细胞)。本公开的主题还提供使用这种细胞用于治疗的方法,例如,用于治疗和/或预防肿瘤或瘤形成(例如,aml)。
91.本公开的非限制性实施方式通过本说明书和实施例进行描述。
92.出于使本公开清楚的目的,而不是通过限制的方式,将详细描述分为以下小节:
93.5.1.定义;
94.5.2.cd371;
95.5.3.抗原识别受体;
96.5.4.细胞;
97.5.5.组合物和载体;
98.5.6.多肽;
99.5.7.剂型和给药;
100.5.8.治疗方法;和
101.5.9.试剂盒。
102.5.1.定义
103.除非另有定义,本文使用的所有技术和科学术语具有本发明所属领域的技术人员通常理解的含义。以下参考文献为本领域技术人员提供本发明中使用的许多术语的一般定义:singleton等,dictionary of microbiology and molecular biology(第二版,1994);the cambridge dictionary of science and technology(walker编,1988);the glossary of genetics,第五版,r.rieger等(编),springer verlag(1991);和hale&marham,the harper collins dictionary of biology(1991)。除非另有说明,本文使用的以下术语具有下文给出的含义。
104.本文使用的术语“约”或“大约”是指在由本领域普通技术人员确定的特定值的可接受误差范围内,这将部分地取决于如何测量或确定该值,即测量系统的局限性。例如,根据本领域的惯例,“约”可以指在3个或多于3个标准偏差内。或者,“约”可以表示给定值的高达20%、优选高达10%、更优选高达5%、再更优选高达1%的范围。或者,特别是关于生物系统或过程,该术语可以表示在数值的一个数量级内、优选在5倍以内、更优选在2倍以内。
[0105]“免疫应答细胞”是指在免疫应答中起作用的细胞或其祖细胞或其后代。在某些实施方式中,免疫应答细胞是淋巴谱系的细胞。淋巴谱系细胞的非限制性实例包括t细胞、自然杀伤(nk)细胞、b细胞和可分化成淋巴样细胞的干细胞。在某些实施方式中,免疫应答细胞是骨髓谱系细胞。
[0106]“激活免疫应答细胞”是指信号转导的诱导或细胞中蛋白质表达的变化,导致免疫应答的启动。例如,当cd3链响应于配体结合和基于免疫受体酪氨酸的抑制基序(itam)聚集时,就会产生信号转导级联反应。在某些实施方式中,当内源性tcr或外源性car与抗原结合时,发生免疫突触的形成,其包括在结合受体(例如,cd4或cd8,cd3γ/δ/ε/ζ等)附近的许多分子的聚集。膜结合信号分子的这种聚集使cd3链中包含的itam基序磷酸化。该磷酸化反过来启动了t细胞激活通路,最终激活转录因子,例如nf-κb和ap-1。这些转录因子诱导t细胞的整体基因表达,从而增加il-2的产生,促进主调节t细胞蛋白的增殖和表达,进而启动t细胞介导的免疫应答。
[0107]“刺激免疫应答细胞”是指导致强烈和持续的免疫应答的信号。在各种实施方式中,这发生在免疫细胞(例如,t细胞)激活之后或通过包括但不限于cd28、cd137(4-1bb)、ox40、cd40和icos的受体同时介导。接收多种刺激信号对于建立强烈且长期的t细胞介导的免疫应答可能很重要。t细胞可以迅速被抑制并且对抗原无应答。尽管这些共刺激信号的作用可能有所不同,但它们通常会导致基因表达增加,从而产生长寿命、增殖性和抗凋亡性t
细胞,其对抗原应答强烈,可彻底和持续根除。
[0108]
如本文所用,术语“抗原识别受体”是指能够识别靶抗原(例如,cd371)的受体。在某些实施方式中,抗原识别受体在其与靶抗原结合后能够激活免疫或免疫应答细胞(例如,t细胞)。
[0109]
本文使用的术语“抗体”不仅指完整的抗体分子,而且指保留免疫原结合能力的抗体分子片段。此类片段在本领域中也是众所周知的,并且在体外和体内常规使用。因此,本文使用的术语“抗体”不仅指完整的免疫球蛋白分子,而且指众所周知的活性片段f(ab')2和fab。缺少完整抗体的fc片段的f(ab')2和fab片段,更快地从循环中清除,并且可能具有更少的完整抗体的非特异性组织结合(wahl等,nucl med(1983);24:316-325)。如本文所用,包括完整天然抗体、双特异性抗体;嵌合抗体;fab、fab’、单链v区片段(scfv)、融合多肽和非常规抗体。在某些实施方式中,抗体是糖蛋白,其包含通过二硫键相互连接的至少两个重(h)链和两个轻(l)链。每条重链由重链可变区(在本文中简称为vh)和重链恒定(ch)区组成。重链恒定区由三个结构域ch1、ch2和ch3组成。每条轻链由轻链可变区(在本文中简称为v
l
)和轻链恒定c
l
区组成。轻链恒定区由一个结构域c
l
组成。vh区和v
l
区可进一步细分为高变区,称为互补决定区(cdr),其间散布有更保守的区,称为框架区(fr)。每个vh和v
l
由三个cdr和四个fr组成,它们从氨基端到羧基端按以下顺序排列:fr1,cdr1,fr2,cdr2,fr3,cdr3,fr4。重链和轻链的可变区包含与抗原相互作用的结合结构域。抗体的恒定区可以介导免疫球蛋白与宿主组织或因子的结合,所述宿主组织或因子包括免疫系统的各种细胞(例如,效应细胞)和经典补体系统的第一组分(c1q)。
[0110]
如本文所用,“cdr”定义为抗体的互补决定区氨基酸序列,其是免疫球蛋白重链和轻链的高变区。参见,例如,kabat等,sequences of proteins of immunological interest,第4版,美国国立卫生研究院卫生与公共服务部(1987)或imgt编号系统(lefranc,the immunologist(1999);7:132-136;lefranc等,dev.comp.immunol.(2003);27:55-77)。通常,抗体在可变区中包含三个重链和三个轻链cdr或cdr区。cdr提供大多数接触残基,以使抗体与抗原或表位结合。在某些实施方式中,使用imgt编号系统勾勒cdr区域。在某些实施方式中,使用可在http://www.imgt.org/imgt_vquest/input访问的imgt编号系统来勾勒cdr区域。
[0111]
本文使用的术语“单链可变片段”或“scfv”是免疫球蛋白(例如小鼠或人)的重链(vh)和轻链(v
l
)的可变区的融合蛋白,其共价连接形成vh::vl异源二聚体。重链(vh)和轻链(v
l
)直接连接或通过肽编码接头(例如,10、15、20、25个氨基酸)连接,其将vh的n末端与v
l
的c-末端连接或将vh的c末端与v
l
的n末端连接。接头通常富含用于柔性的甘氨酸,以及用于溶解性的丝氨酸或苏氨酸。接头可以连接细胞外抗原结合结构域的重链可变区和轻链可变区。接头的非限制性实例公开于shen等,anal.chem.80(6):1910-1917(2008)和wo2014/087010,其内容整体并入本文以供参考。在某些实施方式中,接头是g4s接头。
[0112]
在某些实施方式中,接头包含seq id no:13所示的氨基酸序列,其在下文提供:
[0113]
ggggsggggsgggsggggs[seq id no:13]
[0114]
在某些实施方式中,接头包含seq id no:14所示的氨基酸序列,其在下文提供:
[0115]
ggggsggggsggggs[seq id no:14]
[0116]
在某些实施方式中,接头包含seq id no:91所示的氨基酸序列,其在下文提供:
[0117]
ggggsggggsggggsgggsggggs [seq id no:91]
[0118]
在某些实施方式中,接头包含seq id no:92所示的氨基酸序列,其在下文提供:
[0119]
ggggsggggsggggsggggsgggsggggs [seq id no:92]
[0120]
在某些实施方式中,接头包含seq id no:93所示的氨基酸序列,其在下文提供:
[0121]
ggggs [seq id no: 93]
[0122]
在某些实施方式中,接头包含seq id no:94所示的氨基酸序列,其在下文提供:
[0123]
ggggsggggs[seq id no:94]
[0124]
尽管去除了恒定区并引入了接头,scfv蛋白仍保留了原始免疫球蛋白的特异性。单链fv多肽抗体可以由如huston等proc.nat.acad.sci.usa,(1988);85:5879-5883;美国专利第5,091,513号、第5,132,405号和第4,956,778号以及美国专利公开号20050196754和20050196754所述的包括vh和v
l
编码序列的核酸表达。已经描述了具有抑制活性的拮抗scfv(参见,例如,zhao等,hyrbidoma(larchmt)(2008);27(6):455-51;peter等,j cachexia sarcopenia muscle(2012);8月12日;shieh等,j imunol(2009);183(4):2277-85;giomarelli等,thromb haemost(2007);97(6):955-63;fife等,j clin invst(2006);116(8):2252-61;brocks等,immunotechnology 1997 3(3):173-84;moosmayer等,ther immunol 1995 2(10:31-40))。已经描述了具有刺激活性的激动性scfv(参见,例如,peter等,j bioi chern 2003 25278(38):36740-7;xie等,nat biotech 1997 15(8):768-71;ledbetter等,crit rev immunol 1997 17(5-6):427-55;ho等,biochim biophys acta 2003 1638(3):257-66)。
[0125]
如本文所用,术语“嵌合抗原受体”或“car”是指包含与能够激活或刺激免疫应答细胞的细胞内信号传导结构域融合的细胞外抗原结合结构域和跨膜结构域的分子。在某些实施方式中,car的细胞外抗原结合结构域包含scfv。scfv可以源自融合抗体的可变重和轻区。替代地或另外,scfv可以衍生自fab’s(而不是抗体,例如获自fab文库)。在某些实施方式中,将scfv融合至跨膜结构域,然后融合至细胞内信号传导结构域。“基本同一性”或“基本同源性”是指与参考氨基酸序列(例如,本文所述的任意氨基酸序列)或参考核酸序列(例如,本文描述的任意核酸序列)表现出至少约50%同源性或同一性的多肽或核酸分子。在某些实施方式中,这样的序列与用于比较的氨基酸或核酸的序列具有至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约99%或至少约100%同源性或同一性。
[0126]
序列同一性可以通过使用序列分析软件(例如,威斯康星大学生物技术中心遗传学计算机组的序列分析软件包,威斯康星州麦迪逊市53705大学大道1710号,blast、bestfit、gap或pileup/prettybox程序)进行测量。这样的软件通过将同源性程度分配给各种取代、缺失和/或其它修饰来匹配相同或相似的序列。保守取代通常包括以下组内的取代:甘氨酸、丙氨酸;缬氨酸、异亮氨酸、亮氨酸;天冬氨酸、谷氨酸、天冬酰胺、谷氨酰胺;丝氨酸、苏氨酸赖氨酸、精氨酸;和苯丙氨酸、酪氨酸。在确定同一性程度的示例性方法中,可以使用blast程序,其中e-3和e-100之间的概率得分指示密切相关的序列。
[0127]“有效量”是足以在治疗时影响有益或期望的临床结果的量。可以以一个或多个剂量向受试者施用有效量。在某些实施方式中,有效量可以是足以减轻、改善、稳定、逆转或减缓疾病进展或以其他方式降低疾病的病理后果的量。有效量可以由医生根据具体情况确定
并且在本领域技术人员的技能范围内。当确定合适的剂量以达到有效量时,通常要考虑几个因素。这些因素包括受试者的年龄、性别和体重、所治疗的疾病、疾病的严重程度以及所施用的细胞的形式和有效浓度。
[0128]
如本文所用,术语“内源性”是指核酸分子或多肽通常在细胞或组织中表达。
[0129]
如本文所用,术语“外源性”是指核酸分子或多肽不是内源性存在细胞中的。因此,术语“外源性”将涵盖在细胞中表达的任何重组核酸分子或多肽,例如外源、异源和过表达的核酸分子和多肽。“外源性”核酸是指天然野生型细胞中不存在的核酸。例如,外源性核酸可通过序列、位置/定位或两者而不同于内源性对应物。为了清楚起见,外源性核酸相对于其天然内源性对应物可以具有相同或不同的序列。可以通过遗传工程将其引入细胞本身或其祖细胞,并且可以任选地将其连接至替代控制序列,例如非天然启动子或分泌序列。
[0130]“异源核酸分子或多肽”是指通常不存在于细胞或得自细胞的样品中的核酸分子(例如cdna、dna或rna分子)或多肽。该核酸可以来自另一个生物,或者可以是例如通常不在细胞或样品中表达的mrna分子。
[0131]“调节”是指正或负改变。示例性调节包括约1%、约2%、约5%、约10%、约25%、约50%、约75%或约100%的变化。
[0132]“增加”是指正改变至少约5%。改变可以为约5%、约10%、约25%、约30%、约50%、约75%、约100%或更多。
[0133]“减少”是指负改变至少约5%。改变可以为约5%、约10%、约25%、约30%、约50%、约75%或甚至约100%。
[0134]
术语“分离的”、“纯化的”或“生物学上纯净的”是指物质在不同程度上不含在其原始状态下通常与其伴随的组分。“分离”表示与原始来源或环境的分离度。“纯化”表示分离度高于分离。“纯化的”或“生物纯净的”蛋白质充分不含其它物质,以使任何杂质均不会实质性地影响蛋白质的生物学特性或引起其它不利后果。也就是说,如果核酸或肽通过重组dna技术生产而基本不含细胞材料、病毒材料或培养基,或者通过化学合成而基本不含化学前体或其它化学品,则其是纯化的。纯度和均质性通常使用分析化学技术确定,例如聚丙烯酰胺凝胶电泳或高效液相色谱法。术语“纯化的”可以表示核酸或蛋白质在电泳凝胶中产生基本上一个条带。对于可以进行修饰(例如磷酸化或糖基化)的蛋白质,不同的修饰可以产生不同的分离的蛋白质,可以将其分别纯化。
[0135]“分离的细胞”是指与天然伴随细胞的分子和/或细胞组分分离的细胞。
[0136]
如本文所用,术语“抗原结合结构域”是指能够特异性结合细胞上存在的特定抗原决定簇或抗原决定簇组的结构域。
[0137]“瘤形成”是指以细胞或组织的病理性增生及其随后向其它组织或器官的迁移或侵袭为特征的疾病。瘤形成的生长通常是不受控制的和进行性的,并且在不引起正常细胞增殖或者导致正常细胞增殖停止的条件下发生。瘤形成可影响多种细胞类型、组织或器官,包括但不限于选自以下的器官:膀胱、骨骼、大脑、乳房、软骨、神经胶质、食道、输卵管、胆囊、心脏、肠、肾脏、肝脏、肺、淋巴结、神经组织、卵巢、胰腺、前列腺、骨骼肌、皮肤、脊髓、脾脏、胃、睾丸、胸腺、甲状腺、气管、泌尿生殖道、输尿管、尿道,子宫和阴道、或其组织或细胞类型。瘤形成包括癌症,例如肉瘤、肿瘤或浆细胞瘤(浆细胞的恶性肿瘤)。瘤形成可以是原发性肿瘤或原发性癌症。此外,瘤形成可能处于转移状态。
[0138]“受体”是指存在于细胞膜上的选择性地结合一个或更多个配体的多肽或其一部分。
[0139]“识别”是指选择性地结合靶标。识别肿瘤的t细胞可以表达与肿瘤抗原结合的受体(例如tcr或car)。
[0140]“参考”或“对照”是指比较的标准。例如,可以将表达car和scfv的细胞的scfv-抗原结合水平与仅表达car的相应细胞的scfv-抗原结合水平进行比较。
[0141]“分泌的”是指多肽通过分泌通路通过内质网、高尔基体、以及作为在细胞质膜上瞬时融合从而将蛋白质释放到细胞外的囊泡而从细胞释放。
[0142]“信号序列”或“前导序列”是指存在于新合成的蛋白质的n-末端,指导它们进入分泌通路的肽序列(例如5、10、15、20、25或30个氨基酸)。
[0143]“特异性结合”或“与
…
特异性结合”或“特异性靶向”是指识别并/或结合目的生物分子(例如多肽,例如cd371多肽)但基本上不识别并/或结合样品例如生物样品中其它分子的多肽或其片段,其自然包括本公开的多肽(例如cd371多肽)。
[0144]
术语“包含”,“包括”旨在具有美国专利法中赋予它们的广义含义,并且可以表示“含有”,“包含”等。
[0145]
如本文所用,“治疗”是指试图改变所治疗的个体或细胞的疾病进程的临床干预,并且可以用于预防或在临床病理过程中进行。治疗的治疗作用包括但不限于预防疾病的发生或复发、减轻症状、减少疾病的任何直接或间接病理后果、预防转移、降低疾病进展的速度、改善或减轻疾病状态、和缓解或改善预后。通过预防疾病或病症的进展,治疗不仅可以预防在受影响或诊断的受试者或怀疑患有该病症的受试者中由于病症引起的恶化,而且治疗可以在有患病症或怀疑患有该病症风险的受试者中预防该病症的发作或该病症的症状。
[0146]
本文中的“个体”或“受试者”是脊椎动物,例如人或非人动物,例如哺乳动物。哺乳动物包括但不限于人、灵长类动物、农场动物、运动动物、啮齿动物和宠物。非人动物受试者的非限制性实例包括啮齿动物,如小鼠、大鼠、仓鼠和豚鼠;兔子;狗;猫;绵羊;猪;山羊;牛;马;和非人灵长类动物,例如猿和猴子。如本文所用,术语“免疫受损的”是指具有免疫缺陷的受试者。该受试者非常容易遭受机会性感染,这种感染是由通常不会在免疫系统健康的人中引起疾病的生物体引起的,但是会影响免疫系统功能差或免疫系统受抑制的人。
[0147]
在以下公开中描述了本发明公开主题的其它方面,并且在本发明公开主题的范围内。
[0148]
5.2.cd371
[0149]
cd371(cec12a)也称为dcal-2、micl或cll-1,是一种30kd c型凝集素跨膜糖蛋白。它在单核细胞、粒细胞、自然杀伤(nk)细胞和嗜碱性粒细胞上表达。cd371是一种免疫抑制受体,可将src同源磷酸酶shp-1和shp-2募集到其磷酸化的细胞质免疫受体酪氨酸抑制基序(itim)(sancho等,annu rev.immunol(2012);30:491-529;yan等,front immunol(2015);6:408;lahoud等,j immunol(2011);187:842)。cd371被认为是一种负调节性尿酸晶体(尿酸单钠,msu)受体,可控制自身免疫和炎症性疾病(neumann等,immunity(2014);40:389-99)。cd371是粒细胞和单核细胞功能的负调节剂(marshall等,j biol chem(2004);279(15):14792-802;pyz等,eur j immunol(2008);38(4):1157-63)。
[0150]
在某些实施方式中,cd371是人cd371,其包含或由具有ncbi参考号:np_612210.4
(seq id no:15)的氨基酸序列或其片段组成。
[0151]
seq id no:15在下文提供:
[0152][0153]
在某些实施方式中,cd371包含与seq id no:15所示的氨基酸序列具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、或至少约99%、至少约100%同一性的氨基酸序列或其片段,或由其组成。
[0154]
5.3.抗原识别受体
[0155]
本公开的抗原识别受体特异性靶向或结合cd371。在某些实施方式中,抗原识别受体是嵌合抗原受体(car)。在某些实施方式中,抗原识别受体是t细胞受体(tcr)。在某些实施方式中,抗原识别受体是tcr样融合分子。
[0156]
本公开的主题还提供编码本公开的抗原识别受体的核酸分子。在某些实施方式中,核酸分子包含编码本文公开的靶向cd371的抗原识别受体的多肽的核苷酸序列。
[0157]
5.3.1.t细胞受体(tcr)
[0158]
在某些实施方式中,抗原识别受体是tcr。tcr是二硫键连接的异二聚体蛋白,其由两条可变链组成,这些可变链表达为与不变cd3链分子复合物的一部分。tcr在t细胞的表面上发现,并负责将抗原识别为与主要组织相容性复合物(mhc)分子结合的肽。在某些实施方式中,tcr包含α链和β链(分别由tra和trb编码)。在某些实施方式中,tcr包括γ链和δ链(分别由trg和trd编码)。
[0159]
tcr的每条链均由两个细胞外结构域组成:可变(v)区和恒定(c)区。恒定区靠近细胞膜,其后是跨膜区和短的胞质尾区。可变区结合肽/mhc复合物。两条链的可变结构域均具有三个互补决定区(cdr)。
[0160]
在某些实施方式中,tcr可以与三个二聚体信号传导模块cd3δ/ε、cd3γ/ε和cd247ζ/ζ或ζ/η形成受体复合物。当tcr复合物与其抗原和mhc(肽/mhc)结合时,表达tcr复合物的t细胞被激活。
[0161]
在某些实施方式中,tcr是内源性tcr。在某些实施方式中,抗原识别受体是天然存在的tcr。
[0162]
在某些实施方式中,抗原识别受体是外源性tcr。在某些实施方式中,抗原识别受体是重组tcr。在某些实施方式中,抗原识别受体是非天然存在的tcr。在某些实施方式中,非天然存在的tcr与任何天然存在的tcr的区别在于至少一个氨基酸残基。在某些实施方式中,非天然存在的tcr与任何天然存在的tcr相差至少约2、约3、约4、约5、约6、约7、约8、约9、约10、约11、约12、约13、约14、约15、约20、约25、约30、约40、约50、约60、约70、约80、约90、约100个或更多个氨基酸残基。在某些实施方式中,非天然存在的tcr由天然存在的tcr通过至少一个氨基酸残基修饰获得。在某些实施方式中,非天然存在的tcr由天然存在的tcr通过至少约2、约3、约4、约5、约6、约7、约8、约9、约10、约11、约12、约13、约14、约15、约20、约25、约30、约40、约50、约60、约70、约80、约90、约100个或更多个氨基酸残基修饰获得。
[0163]
5.3.2.嵌合抗原受体(car)
[0164]
在某些实施方式中,抗原识别受体是car。car是工程改造受体,其将目的特异性移植或赋予免疫效应细胞。car可用于将单克隆抗体的特异性移植到t细胞上;通过逆转录病毒载体促进其编码序列的转移。
[0165]
共有三代car。“第一代”car通常由胞外抗原结合结构域(例如scfv)组成,该结构域与跨膜结构域融合,而跨膜结构域与细胞质/细胞内信号传导结构域融合。“第一代”car可以提供从头抗原识别,并通过单个融合分子中的cd3ζ链信号传导结构域激活cd4
+
和cd8
+
t细胞,而与hla介导的抗原呈递无关。“第二代”car将来自各种共刺激分子(例如cd28、4-1bb、icos、ox40)的细胞内信号传导结构域添加到car的胞质尾区,以向t细胞提供其它信号。“第二代”car包括提供共刺激(例如cd28或4-1bb)和激活(cd3ζ)的car。“第三代”car包括提供多重共刺激(例如,cd28和4-1bb)和激活(cd3ζ)的那些。在某些实施方式中,抗原识别受体是第一代car。在某些实施方式中,抗原识别受体是不包含共刺激分子或其片段的细胞内信号传导结构域的car。在某些实施方式中,抗原识别受体是第二代car。
[0166]
在某些实施方式中,car包含特异性结合cd371的细胞外抗原结合结构域、跨膜结构域和细胞内信号传导结构域。
[0167]
5.3.2.1.car的细胞外抗原结合结构域
[0168]
在某些实施方式中,细胞外抗原结合结构域是scfv。在某些实施方式中,scfv是人scfv。在某些实施方式中,scfv是人源化scfv。在某些实施方式中,scfv是鼠scfv。在某些实施方式中,通过用抗原-fc融合蛋白筛选scfv噬菌体文库来鉴定scfv。
[0169]
在某些实施方式中,细胞外抗原结合结构域是fab。在某些实施方式中,fab是交联的。在某些实施方式中,细胞外抗原结合结构域是f(ab)2。
[0170]
任何前述分子可以包含在具有异源序列的融合蛋白中以形成细胞外抗原结合结构域。在某些非限制性实施方式中,car的细胞外抗原结合结构域(体现为例如scfv或其类似物)以约1
×
10-6
m或更小,例如约1
×
10-7
m或更小、约1
×
10-8
m或更小、约1
×
10-9
m或更小、约1
×
10-10
m或更小、或约1
×
10-11
m或更小的解离常数(kd)结合cd371(例如人cd371)。在某些实施方式中,car的细胞外抗原结合结构域以约1
×
10-7
m或更小的kd结合cd371(例如人cd371)。在某些实施方式中,car的细胞外抗原结合结构域以约1
×
10-8
m或更小的kd结合cd371(例如人cd371)。在某些实施方式中,car的细胞外抗原结合结构域以约1.5
×
10-8
m或约1
×
10-8
m的kd结合cd371(例如人cd371)。在某些实施方式中,car的细胞外抗原结合结构域以约1
×
10-8
m和约1
×
10-7
m之间的kd结合cd371(例如人cd371)。
[0171]
在某些实施方式中,car的细胞外抗原结合结构域以低结合亲和力结合cd371(例如人cd371)。在某些实施方式中,car的细胞外抗原结合结构域以约1.5
×
10-8
m或更大、约1
×
10-8
m或更大、约1
×
10-7
m或更大、或约1
×
10-6
m或更大的kd结合cd371(例如人cd371)。
[0172]
car的细胞外抗原结合结构域的结合可以通过例如酶联免疫吸附测定法(elisa)、放射免疫测定法(ria)、facs分析法、生物测定法(例如生长抑制)、或western blot测定法来测定。这些测定法中的每一种通常通过采用对目标复合物具有特异性的标记试剂(例如抗体或scfv)来检测特定目标蛋白质-抗体复合物的存在。例如,scfv可以被放射性标记并用于放射免疫测定法(ria)(参见,例如,weintraub,b.,放射免疫测定的原理,放射配体测定技术的第七培训课程,内分泌学会,1986年3月,并入本文以供参考)。放射性同位素可通过诸如使用γ计数器或闪烁计数器的方法或通过放射自显影来检测。在某些实施方式中,
id no:1所示的氨基酸序列;和v
l
,其包含seq id no:2所示的氨基酸序列。在某些实施方式中,vh和v
l
经由接头连接。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。
[0181]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,scfv包含seq id no:107所示的氨基酸序列,其提供于表1。在某些实施方式中,将scfv命名为“b10h4l”。
[0182]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。在某些实施方式中,scfv包含seq id no:16所示的氨基酸序列。在某些实施方式中,将scfv命名为“b10l4h”。编码seq id no:16的氨基酸序列的示例性核苷酸序列如seq id no:22所示。seq id no:16和seq id no:22提供于下表1。
[0183]
表1
[0184][0185]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:3所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约
95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:3所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含vh,其包含seq id no:3所示的氨基酸序列。seq id no:3提供于下表2。
[0186]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:4所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:4所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含v
l
,其包含seq id no:4所示的氨基酸序列。seq id no:4提供于下表2。
[0187]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含seq id no:3所示的氨基酸序列,如表2所示。在某些实施方式中,抗cd371 scfv包含v
l
,其包含seq id no:4所示的氨基酸序列。在某些实施方式中,抗cd371 scfv包含vh,其包含seq id no:3所示的氨基酸序列;和v
l
,其包含seq id no:4所示的氨基酸序列。
[0188]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:34所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:35所示的氨基酸序列或其保守修饰;和v
h cdr3,其包含seq id no:36所示的氨基酸序列或其保守修饰。seq id no:34-36提供于表2。
[0189]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l cdr1,其包含seq id no:37所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:38所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:39所示的氨基酸序列或其保守修饰。seq id no:37-39提供于表2。
[0190]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:34所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:35所示的氨基酸序列或其保守修饰;v
h cdr3,其包含seq id no:36所示的氨基酸序列或其保守修饰;v
l cdr1,其包含seq id no:37所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:38所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:39所示的氨基酸序列或其保守修饰。
[0191]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:34所示的氨基酸序列;v
h cdr2,其包含seq id no:35所示的氨基酸序列;v
h cdr3,其包含seq id no:36所示的氨基酸序列;v
l cdr1,其包含seq id no:37所示的氨基酸序列;v
l cdr2,其包含seq id no:38所示的氨基酸序列;和v
l cdr3,其包含seq id no:39所示的氨基酸序列。
[0192]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含seq id no:3所示的氨基酸序列;和v
l
,其包含seq id no:4所示的氨基酸序列。在某些实施方式
中,vh和v
l
经由接头连接。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。
[0193]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,scfv包含seq id no:108所示的氨基酸序列,其提供于表2。在某些实施方式中,将scfv命名为“c3h4l”。
[0194]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。在某些实施方式中,scfv包含seq id no:17所示的氨基酸序列。在某些实施方式中,将scfv命名为“c3l4h”。编码seq id no:17的氨基酸序列的示例性核苷酸序列如seq id no:23所示。seq id no:17和seq id no:23提供于下表2。
[0195]
表2
[0196][0197]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:5所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:5所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约
85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含vh,其包含seq id no:5所示的氨基酸序列。seq id no:5提供于下表3。
[0198]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:6所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:6所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含v
l
,其包含seq id no:6所示的氨基酸序列。seq id no:6提供于下表3。
[0199]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:40所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:41所示的氨基酸序列或其保守修饰;和v
h cdr3,其包含seq id no:42所示的氨基酸序列或其保守修饰。seq id no:40-42提供于表3。
[0200]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l cdr1,其包含seq id no:43所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:44所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:45所示的氨基酸序列或其保守修饰。seq id no:43-45提供于表3。
[0201]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:40所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:41所示的氨基酸序列或其保守修饰;v
h cdr3,其包含seq id no:42所示的氨基酸序列或其保守修饰;v
l cdr1,其包含seq id no:43所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:44所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:45所示的氨基酸序列或其保守修饰。
[0202]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:40所示的氨基酸序列;v
h cdr2,其包含seq id no:41所示的氨基酸序列;v
h cdr3,其包含seq id no:42所示的氨基酸序列;v
l cdr1,其包含seq id no:43所示的氨基酸序列;v
l cdr2,其包含seq id no:44所示的氨基酸序列;和v
l cdr3,其包含seq id no:45所示的氨基酸序列。
[0203]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含seq id no:5所示的氨基酸序列;和v
l
,其包含seq id no:6所示的氨基酸序列。在某些实施方式中,vh和v
l
经由接头连接。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。
[0204]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,scfv包含seq id no:109所示的氨基酸序列,其提供于表3。在某些实施方式中,将scfv命名为“d6h4l”。
[0205]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。在某些实施方式中,scfv包含seq id no:18所示的氨基酸序列。在某些实施方式中,将scfv命名为“d6l4h”。编码seq id no:18的氨基酸序列的示例性核苷酸序列如seq id no:24所示。seq id no:18和seq id no:24提供于下表3。
[0206]
表3
[0207][0208][0209]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:7所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:7所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含vh,其包含seq id no:7所示的氨基酸序列。seq id no:7提供于下表4。
[0210]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与
id no:19和seq id no:25提供于下表4。
[0218]
表4
[0219][0220]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:9所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:9所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含vh,其包含seq id no:9所示的氨基酸序列。seq id no:9提供于下表5。
[0221]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:10所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:10所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含v
l
,其包含seq id no:10所示的氨基酸序列。seq id no:10
提供于下表5。
[0222]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:52所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:53所示的氨基酸序列或其保守修饰;和v
h cdr3,其包含seq id no:54所示的氨基酸序列或其保守修饰。seq id no:52-54提供于表5。
[0223]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l cdr1,其包含seq id no:55所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:56所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:57所示的氨基酸序列或其保守修饰。seq id no:55-57提供于表5。
[0224]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:52所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:53所示的氨基酸序列或其保守修饰;v
h cdr3,其包含seq id no:54所示的氨基酸序列或其保守修饰;v
l cdr1,其包含seq id no:55所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:56所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:57所示的氨基酸序列或其保守修饰。
[0225]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:52所示的氨基酸序列;v
h cdr2,其包含seq id no:53所示的氨基酸序列;v
h cdr3,其包含seq id no:54所示的氨基酸序列;v
l cdr1,其包含seq id no:55所示的氨基酸序列;v
l cdr2,其包含seq id no:56所示的氨基酸序列;和v
l cdr3,其包含seq id no:57所示的氨基酸序列。
[0226]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含seq id no:9所示的氨基酸序列;和v
l
,其包含seq id no:10所示的氨基酸序列。在某些实施方式中,vh和v
l
经由接头连接。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。
[0227]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,scfv包含seq id no:111所示的氨基酸序列,其提供于表5。在某些实施方式中,将scfv命名为“e4h4l”。
[0228]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。在某些实施方式中,scfv包含seq id no:20所示的氨基酸序列。在某些实施方式中,将scfv命名为“e4l4h”。编码seq id no:20的氨基酸序列的示例性核苷酸序列如seq id no:26所示。seq id no:20和seq id no:26提供于下表5。
[0229]
表5
[0230]
[0231][0232]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:11所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含与seq id no:11所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含vh,其包含seq id no:11所示的氨基酸序列。seq id no:11提供于下表6。
[0233]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:12所示氨基酸序列具有至少约80%(例如至少约85%、至少约90%、或至少约95%)同源性或同一性的氨基酸序列。例如,car的细胞外抗原结合结构域(例如scfv)包含v
l
,其包含与seq id no:12所示氨基酸序列具有约80%、约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列。在某些实施方式中,细胞外抗原结合结构域包含v
l
,其包含seq id no:12所示的氨基酸序列。seq id no:12提供于下表6。
[0234]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:58所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:59所示的氨基酸序列或其保守修饰;和v
h cdr3,其包含seq id no:60所示的氨基酸序列或其保守修饰。seq id no:58-60提供于表6。
[0235]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
l cdr1,其包含seq id no:61所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:62所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:63所示的氨基酸序列或其保守修饰。seq id no:61-63提供于表6。
[0236]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:58所示的氨基酸序列或其保守修饰;v
h cdr2,其包含seq id no:59所示的氨基酸序列或其保守修饰;v
h cdr3,其包含seq id no:60所示的氨基酸序列或其保守修饰;v
l cdr1,其包含seq id no:61所示的氨基酸序列或其保守修饰;v
l cdr2,其包含seq id no:62所示的氨基酸序列或其保守修饰;和v
l cdr3,其包含seq id no:63所示的氨基酸序列或其保守修饰。
[0237]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含v
h cdr1,其包含seq id no:58所示的氨基酸序列;v
h cdr2,其包含seq id no:59所示的氨基酸序列;v
h cdr3,其包含seq id no:60所示的氨基酸序列;v
l cdr1,其包含seq id no:61所示的氨基酸序列;v
l cdr2,其包含seq id no:62所示的氨基酸序列;和v
l cdr3,其包含seq id no:63所示的氨基酸序列。
[0238]
在某些实施方式中,car的细胞外抗原结合结构域(例如scfv)包含vh,其包含seq id no:11所示的氨基酸序列;和v
l
,其包含seq id no:12所示的氨基酸序列。在某些实施方式中,vh和v
l
经由接头连接。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。
[0239]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,scfv包含seq id no:112所示的氨基酸序列,其提供于表6。在某些实施方式中,将scfv命名为“e8h4l”。
[0240]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。在某些实施方式中,scfv包含seq id no:21所示的氨基酸序列。在某些实施方式中,将scfv命名为“e8l4h”。编码seq id no:21的氨基酸序列的示例性核苷酸序列如seq id no:27所示。seq id no:21和seq id no:27提供于下表6。
[0241]
表6
[0242][0243][0244]
如本文所用,术语“保守序列修饰”是指不显著影响或改变本公开的包含氨基酸序列的间皮素-靶向car(例如,car的细胞外抗原结合结构域)的结合特征的氨基酸修饰。保守修饰可以包括氨基酸取代、添加和缺失。可以通过本领域已知的标准技术(例如定点诱变和pcr介导的诱变)将修饰引入本公开的car的细胞外抗原结合结构域中。氨基酸可根据其物理化学性质(例如电荷和极性)分为几组。保守氨基酸取代是其中氨基酸残基被相同组内的氨基酸取代的氨基酸取代。例如,氨基酸可以按电荷分类:带正电荷的氨基酸包括赖氨酸、精氨酸、组氨酸,带负电荷的氨基酸包括天冬氨酸、谷氨酸,中性电荷氨基酸包括丙氨酸、天冬酰胺、半胱氨酸、谷氨酰胺、甘氨酸,异亮氨酸、亮氨酸、蛋氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸和缬氨酸。另外,氨基酸可以按极性分类:极性氨基酸包括精氨酸(碱性极性)、天冬酰胺、天冬氨酸(酸性极性)、谷氨酸(酸性极性)、谷氨酰胺、组氨酸(碱性极性)、赖氨酸(碱性极性)、丝氨酸、苏氨酸和酪氨酸;非极性氨基酸包括丙氨酸、半胱氨酸、甘氨酸、异亮氨酸、亮氨酸、蛋氨酸、苯丙氨酸、脯氨酸、色氨酸和缬氨酸。因此,cdr区内的一个或更多个氨基酸残基可以被来自相同组的其它氨基酸残基替换,并且可以使用本文所述的功能测定法测试改变的抗体的保留功能(即,上述(c)至(l)中列出的功能)。在某些实施方式中,在指定序列或cdr区内不超过一个、不超过两个、不超过三个、不超过四个、不超过五个残基被改变。
[0245]
相对于指定序列,含有与指定序列(例如,seq id no:1、seq id no:2、seq id no:
3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、或seq id no:12)具有至少约80%、至少约80%、至少约85%、至少约90%或至少约95%(例如,约81%、约82%、约83%、约84%、约85%、约86%、约87%、约88%、约89%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%同源性或同一性的vh和/或v
l
氨基酸序列可以包含取代(例如,保守取代)、插入或缺失,但保留结合靶抗原(例如,间皮素)的能力。在某些实施方式中,在指定序列(例如,seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、或seq id no:12)中,总共1至10个氨基酸被取代、插入和/或缺失。在某些实施方式中,取代、插入或缺失发生在细胞外抗原结合结构域的cdr之外的区(例如,在fr中)。在某些实施方式中,细胞外抗原结合结构域包含选自seq id no:1-12(包括该序列(seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、或seq id no:12)的翻译后修饰)中的vh和/或v
l
序列。
[0246]
如本文所用,两个氨基酸序列之间的同源性百分比等同于两个序列之间的同一性百分比。两个序列之间的同一性百分比是该序列共享的相同位置数的函数(即,%同源性=相同位置数#/位置总数#
×
100),其中考虑了空位数和每个空位的长度,需要引入这些空位以实现两个序列的最佳比对。序列的比较和两个序列之间同一性百分比的确定可以使用数学算法来完成。
[0247]
可以使用e.meyers和w.miller(comput.appl.biosci.,4:11-17(1988))的算法确定两个氨基酸序列之间的同源性百分比,该算法已合并到align程序(2.0版)中),使用pam120重量残基表,空位长度罚分为12,空位罚分为4。此外,两个氨基酸序列之间的同源性百分比可以使用needleman和wunsch(j.mol.biol.48:444-453(1970))算法来确定,该算法已被整合到gcg软件包(可从www.gcg.com获得)中的gap程序中,使用blossum 62矩阵或pam250矩阵,并且空位权重为16、14、12、10、8、6或4,长度权重为1、2、3、4、5或6。
[0248]
另外或可替代地,本公开的主题的氨基酸序列可以进一步用作“查询序列”以对公共数据库进行搜索以例如识别相关序列。可以使用altschul等((1990)j.mol.biol.215:403-10)的xblast程序(2.0版)执行此类搜索。可以使用xblast程序进行blast蛋白质搜索,得分=50,字长=3,以获得与本文公开的指定序列(例如,scfv m903,m904,m905,m906和m900的重链和轻链可变区序列)同源的氨基酸序列。为了获得用于比较目的的空位比对,可以如altschul等,(1997)nucleic acids res.25(17):3389-3402中所述使用gapped blast。当使用blast和gapped blast程序时,可以使用各个程序(例如xblast和nblast)的默认参数。
[0249]
在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合片段交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合片段包含例如任何一种本公开的scfv(例如,v10、c3、d6、a11、e4和d8)的v
h cdr1、cdr2和cdr3序列和v
l cdr1、cdr2和cdr3序列。在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合部分包含例如任何一种本公开的scfv(例如,v10、c3、d6、a11、e4和d8)的vh和v
l
序列。
[0250]
在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原
结合部分交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合部分包含scfv b10的v
h cdr1、cdr2和cdr3序列以及v
l cdr1、cdr2和cdr3序列。例如,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合部分包含v
h cdr1,其包含seq id no:28所示的氨基酸序列;v
h cdr2,其包含seq id no:29所示的氨基酸序列;v
h cdr3,其包含seq id no:30所示的氨基酸序列;v
l cdr1,其包含seq id no:31所示的氨基酸序列;v
l cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列。在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合部分包含scfv b10的vh和v
l
序列。例如,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分交叉竞争结合cd371(例如人cd371),该参考抗体或其抗原结合部分包含vh,其包含seq id no:1所示的氨基酸序列;和v
l
,其包含seq id no:2所示的氨基酸序列。
[0251]
在某些实施方式中,细胞外抗原结合结构域与参考抗体或其抗原结合部分结合cd371(例如人cd371)上的相同表位。例如,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分结合cd371(例如人cd371)上的相同表位,该参考抗体或其抗原结合片段包含例如任何一种本公开的scfv(例如,b10、c3、d6、a11、e4和e8)的v
h cdr1、cdr2和cdr3序列和v
l cdr1、cdr2和cdr3序列。在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合部分结合emr2(例如人emr2)上的相同表位,参考抗体或其抗原结合部分包含例如任何一种本公开的scfv(例如,b10、c3、d6、a11、e4和e8)的vh和v
l
序列。
[0252]
在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合片段结合cd371(例如人cd371)上的相同表位,该参考抗体或其抗原结合片段包含scfv b10的v
h cdr1、cdr2和cdr3序列以及v
l cdr1、cdr2和cdr3序列。例如,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合片段结合cd371(例如人cd371)上的相同表位,该参考抗体或其抗原结合片段包含v
h cdr1,其包含seq id no:28所示的氨基酸序列;v
h cdr2,其包含seq id no:29所示的氨基酸序列;v
h cdr3,其包含seq id no:30所示的氨基酸序列;v
l cdr1,其包含seq id no:31所示的氨基酸序列;v
l cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列。在某些实施方式中,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合片段结合cd371(例如人cd371)上相同或基本相同的表位,该参考抗体或其抗原结合片段包含scfv b10的vh和v
l
序列。例如,本公开的car的细胞外抗原结合结构域与参考抗体或其抗原结合片段结合cd371(例如人cd371)上的相同表位,该参考抗体或其抗原结合片段包含vh,其包含seq id no:1所示的氨基酸序列;和v
l
,其包含seq id no:2所示的氨基酸序列。
[0253]
与参考抗体或其抗原结合部分交叉竞争或竞争结合cd371(例如人cd371)的细胞外抗原结合结构域可通过使用本领域已知的常规方法来鉴定,包括但不限于,elisa、放射免疫测定(ria)、biacore、流式细胞术、蛋白质印迹和任何其他合适的定量或定性抗体结合测定。竞争elisa描述于morris,“epitope mapping of protein antigens by competition elisa”,the protein protocols handbook(1996),pp 595-600,j.walker著,其整体并入以供参考。在某些实施方式中,抗体结合测定包括测量参考抗体与cd371多肽的初始结合,将参考抗体与测试细胞外抗原结合结构域混合,测量参考抗体与cd371多肽
的第二次结合。测试细胞外抗原结合结构域的存在,并将参考抗体的初始结合与第二次结合进行比较,其中与初始结合相比,参考抗体与cd371多肽的第二次结合降低表明测试细胞外抗原结合结构域与参考抗体交叉竞争结合cd371,例如抗体识别相同或基本相同表位、重叠表位或相邻表位。在某些实施方式中,参考抗体例如用荧光染料、生物素或过氧化物酶标记。在某些实施方式中,cd371多肽在细胞中表达,例如在流式细胞术测试中。在某些实施方式中,cd371多肽被固定在表面上,包括biacore ship上(例如,在biacore测试中),或适用于表面等离子体共振分析的其他介质上。在完全不相关的抗体(不与cd371结合)存在下参考抗体的结合可以作为对照高值。可以通过将标记的参考抗体与未标记的参考抗体一起孵育来获得对照低值,其中标记的参考抗体的竞争和结合减少将会发生。在某些实施方式中,测试细胞外抗原结合结构域将参考抗体与cd371多肽的结合降低至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或至少约95%被认为是与参考抗体交叉竞争结合cd371的细胞外抗原结合结构域。在某些实施方式中,测定在室温下进行。
[0254]
在某些实施方式中,抗体结合测定包括测量测试细胞外抗原结合结构域与cd371多肽的初始结合,将测试细胞外抗原结合结构域与参考抗体混合,在参考抗体存在的情况下测量测试细胞外抗原结合结构域与cd371多肽的第二次结合,并将测试细胞外抗原结合结构域的初始结合与第二次结合进行比较,其中与初始结合比较,测试细胞外抗原结合结构域与cd371多肽的第二次结合降低表明测试细胞外抗原结合结构域与参考抗体交叉竞争结合cd371,例如参考抗体识别相同或基本相同表位、重叠表位或相邻表位。在某些实施方式中,测试细胞外抗原结合结构域例如用荧光染料、生物素或过氧化物酶标记。在某些实施方式中,cd371多肽在细胞中表达,例如在流式细胞术测试中。在某些实施方式中,cd371多肽被固定在表面上,包括biacore ship上(例如,在biacore测试中),或适用于表面等离子体共振分析的其他介质上。在完全不相关的抗体(不与cd371结合)存在下测试细胞外抗原结合结构域的结合可以用作对照高值。可以通过将标记的测试细胞外抗原结合结构域与未标记的测试细胞外抗原结合结构域一起孵育来获得对照低值,其中标记的测试细胞外抗原结合结构域的竞争和结合减少将会发生。在某些实施方式中,在参考抗体存在的情况下,测试细胞外抗原结合结构域与cd371多肽的结合降低至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或至少约95%被认为是与参考抗体交叉竞争结合cd371的细胞外抗原结合结构域。在某些实施方式中,测定在室温下进行。
[0255]
在某些非限制性实施方式中,本公开的car的细胞外抗原结合结构域包含连接细胞外抗原结合结构域的重链可变区和轻链可变区的接头。在某些实施方式中,接头包含seq id no:13所示的氨基酸序列。在某些实施方式中,接头包含seq id no:14所示的氨基酸序列。在某些实施方式中,接头包含seq id no:91所示的氨基酸序列。在某些实施方式中,接头包含seq id no:92所示的氨基酸序列。在某些实施方式中,接头包含seq id no:93所示的氨基酸序列。在某些实施方式中,接头包含seq id no:94所示的氨基酸序列。
[0256]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个重链可变区(vh)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
h-v
l
。
[0257]
在某些实施方式中,car的细胞外抗原结合结构域内的可变区必须一个接一个地连接,使得在细胞外抗原结合结构域的n端,定位一个轻链可变区(v
l
)。在某些实施方式中,如果car的细胞外抗原结合结构域是scfv,可变区位置从n末端到c末端为:v
l-vh。
[0258]
此外,细胞外抗原结合结构域可以包含引导新生蛋白进入内质网的前导肽或信号肽。如果car要被糖基化并锚定在细胞膜中,信号肽或前导肽可能是必不可少的。信号序列或前导序列可以是存在于新合成的蛋白质的n端的肽序列(长约5、约10、约15、约20、约25或约30个氨基酸),指导它们进入分泌通路。在某些实施方式中,信号肽共价连接至细胞外抗原结合结构域的5’末端。在某些实施方式中,信号肽包含cd8多肽,例如,car包含截短的cd8信号肽。
[0259]
5.3.2.2.car的跨膜结构域
[0260]
在某些非限制性实施方式中,car的跨膜结构域包含跨越膜的至少一部分的疏水性α螺旋。不同的跨膜结构域导致不同的受体稳定性。抗原识别后,受体聚集并将信号传递给细胞。根据本公开的主题,car的跨膜结构域可以包含cd8的天然或修饰的跨膜结构域或其片段,cd28的天然或修饰的跨膜结构域或其片段,cd3ζ的天然或修饰的跨膜结构域或其片段,cd4的天然或修饰的跨膜结构域或其片段,4-1bb的天然或修饰的跨膜结构域或其片段,ox40的天然或修饰的跨膜结构域或其片段,icos的天然或修饰的跨膜结构域或其片段,cd84的天然或修饰的跨膜结构域或其片段,cd166的天然或修饰的跨膜结构域或其片段,cd8a的天然或修饰的跨膜结构域或其片段,cd8b的天然或修饰的跨膜结构域或其片段,icam-1的天然或修饰的跨膜结构域或其片段,ctla-4的天然或修饰的跨膜结构域或其片段,cd27的天然或修饰的跨膜结构域或其片段,cd40的天然或修饰的跨膜结构域或其片段,nkgd2或其片段,或其组合。
[0261]
在某些实施方式中,car的跨膜结构域包含cd8多肽(例如,cd8的跨膜结构域或其片段)。
[0262]
在某些实施方式中,car的跨膜结构域包含cd8多肽(例如,cd8的跨膜结构域或其片段)。在某些实施方式中,car的跨膜结构域包含cd8多肽(例如,人cd8的跨膜结构域或其片段)。在某些实施方式中,cd8多肽包含与具有ncbi参考号:np_001139345.1(seq id no:64)的氨基酸序列具有至少约85%、约90%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,cd8多肽包含作为seq id no:64的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50且至多235个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd8多肽包含seq id no:64的氨基酸1至235、1至50、50至100、100至150、150至200、137至209或200至235的氨基酸序列,或由其组成。在某些实施方式中,car的跨膜结构域包含cd8多肽,其包含seq id no:64的氨基酸137至209或由其组成。seq id no:64在下文提供。
[0263][0264]
在某些实施方式中,car的跨膜结构域包含cd8多肽(例如,小鼠cd8的跨膜结构域或其片段)。在某些实施方式中,cd8多肽包含与具有ncbi参考号:aaa92533.1(seq id no:
65)的氨基酸序列具有至少约85%、约90%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,cd8多肽包含作为seq id no:65的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50、或至少60、或至少70、或至少100、或至少200且至多247个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd8多肽包含seq id no:65的氨基酸1至247、1至50、50至100、100至150、150至200、151至219、或200至247的氨基酸序列或由其组成。在某些实施方式中,car的跨膜结构域包含cd8多肽,其包含seq id no:65的氨基酸151至219或由其组成。seq id no:65在下文提供。
[0265][0266]
在某些实施方式中,本公开的car的跨膜结构与包含cd28多肽(例如,cd28的跨膜结构域或其片段)。
[0267]
在某些实施方式中,car的跨膜结构域包含cd28多肽(例如,人cd28的跨膜结构域或其片段)。在某些实施方式中,cd28多肽包含与具有ncbi参考号:np_006130(seq id no:66)的氨基酸序列具有至少约85%、约90%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,cd28多肽包含作为seq id no:66的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50且至多220个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd28多肽包含seq id no:66的氨基酸1至220、1至50、50至100、100至150、150至200、153至179、或200至220的氨基酸序列或由其组成。在某些实施方式中,car的跨膜结构域包含cd28多肽,其包含seq id no:66的氨基酸153至179或由其组成。seq id no:66提供如下:
[0268][0269]
编码seq id no:66的氨基酸153至179的示例性核苷酸序列如seq id no:67所示,其在下文提供。
[0270][0271]
在某些实施方式中,car的跨膜结构域包含cd28多肽(例如,小鼠cd28的跨膜结构域或其片段)。在某些实施方式中,cd28多肽包含与具有ncbi参考号:np_031668.3(seq id no:68)的氨基酸序列具有至少约85%、约90%、约95%、约96%、约97%、约98%、约99%或约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些实施方式中,cd28多肽包含作为seq id no:66的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50且至多218个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd28多肽包含seq id no:68的氨基酸1至220、1至50、50至100、100至150、150至200、151至177或200
至218的氨基酸序列或由其组成。在某些实施方式中,car的跨膜结构域包含cd28多肽,其包含seq id no:68的氨基酸151至177或由其组成。seq id no:68提供如下:
[0272][0273]
在某些非限制性实施方式中,car还可以包含将细胞外抗原结合结构域连接至跨膜结构域的间隔区。间隔区可以足够柔韧性以允许抗原结合结构域在不同方向上定向以促进抗原识别同时保留car的激活活性。
[0274]
在某些实施方式中,car的铰链/间隔区包含cd8的天然或修饰的铰链区或其片段,cd28的天然或修饰的铰链区或其片段,cd3ζ的天然或修饰的铰链区或其片段,cd40的天然或修饰的铰链区或其片段,4-1bb的天然或修饰的铰链区或其片段,ox40的天然或修饰的铰链区或其片段,cd84的天然或修饰的铰链区或其片段,cd166的天然或修饰的铰链区或其片段,cd8a的天然或修饰的铰链区或其片段,cd8b的天然或修饰的铰链区或其片段,icos的天然或修饰的铰链区或其片段,icam-1的天然或修饰的铰链区或其片段,ctla-4的天然或修饰的铰链区或其片段,cd27的天然或修饰的铰链区或其片段,cd40的天然或修饰的铰链区或其片段,nkgd2的天然或修饰的铰链区或其片段,合成多肽(不基于与免疫应答相关的蛋白质),或其组合。铰链/间隔区可以是来自igg1的铰链区、或者是免疫球蛋白的ch2ch3区和cd3的一部分、cd28多肽的一部分(例如,seq id no:66或seq id no:68的一部分)、cd8多肽的一部分(例如seq id no:64或seq id no:65的一部分)、前述任一项的变体,该变体与其具有至少约80%、至少约85%、至少约90%、至少约95%或至少约100%的同源性或同一性、或合成的间隔序列。
[0275]
5.3.2.3.car的细胞内信号传导结构域
[0276]
在某些实施方式中,car包含细胞内信号传导结构域。在某些非限制性实施方式中,car的细胞内信号传导结构域包含cd3ζ多肽,cd3ζ可以激活或刺激细胞(例如淋巴谱系的细胞,例如t细胞)。野生型(“天然”)cd3ζ包含三个基于功能性免疫受体酪氨酸的激活基序(itam)、三个功能性富碱性拉伸(brs)区域(brs1、brs2和brs3)。cd3ζ在抗原结合后将激活信号传递至细胞(例如,淋巴谱系的细胞,例如t细胞)。cd3ζ-链的细胞内信号传导结构域是来自内源性tcr的信号的主要传递者。
[0277]
在某些实施方式中,car的细胞内信号传导结构域包含天然cd3ζ。在某些实施方式中,cd3ζ多肽包含与具有ncbi参考号:np_932170(seq id no:69)的氨基酸序列具有至少约85%、约90%、约95%、约96%、约97%、约98%、约99%、或约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,cd3ζ多肽包含作为seq id no:69的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50且至多164个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd3ζ多肽包含seq id no:69的氨基酸1至164、1至50、50至100、52至164、100至150、或150至164的氨基酸序列或由其组成。在某些实施方式中,car的细胞内信号传导结构域包含cd3ζ多肽,其包含seq id no:69的氨基酸52至164或由其组成。seq id no:69在下文提供:
[0278][0279]
在某些实施方式中,car的细胞内信号传导结构域包含cd3多肽,其包含seq id no:89中所示的氨基酸序列或由其组成。seq id no:89在下文提供。
[0280][0281]
编码seq id no:89的氨基酸序列的示例性核苷酸序列如seq id no:90所示,其在下文提供。
[0282][0283]
在某些非限制性实施方式中,car的细胞内信号传导结构域还包含至少一个共刺激性信号传导区。在某些实施方式中,共刺激信号传导区包含至少一种共刺激分子或其片段。在某些实施方式中,共刺激信号传导区包含至少一种共刺激分子或其片段的胞内结构域。
[0284]
如本文所用,“共刺激分子”是指除抗原受体或其配体之外的细胞表面分子,其可以提供淋巴细胞对抗原的有效应答。在某些实施方式中,共刺激分子可以提供最佳的淋巴细胞活化。共刺激分子的非限制性实例包括cd28、4-1bb、ox40、icos、dap-10、cd27、cd40、nkgd2、cd2、fn14、hvem、ltbr、cd28h、tnfr1、tnfr2、baff-r、bcma、taci、troy、rank、cd40、cd27、cd30、edar、xedar、gitr、dr6和ngfr,及其组合。共刺激分子可以与共刺激配体结合,该配体是一种在细胞表面表达的蛋白质,在与其受体结合后会产生共刺激应答,即当抗原识别受体(例如嵌合抗原受体(car))与其靶抗原结合时影响所提供刺激的细胞内应答。作为一个实例,4-1bb配体(即,4-1bbl)可以结合4-1bb以提供细胞内信号,其与car信号组合诱导car
+
t细胞的效应细胞功能。
[0285]
在某些实施方式中,car的细胞内信号传导结构域包含含有cd28多肽例如cd28的细胞内结构域或其片段的共刺激信号传导区。cd28多肽可包含或具有与seq id no:66所示的氨基酸序列具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、至少约100%同源性或同一性的氨基酸序列或其片段,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,cd28多肽包含作为seq id no:66的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50且至多220个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd28多肽包含seq id no:66的氨基酸1至220、1至50、50至100、100至150、114至220、150至200、180至220或200至220的氨基酸序列或由其组成。在某些实施方式中,car的细胞内信号传导结构域包含共刺激信号传导区,其包含cd28多肽,该cd28多肽包含seq id no:66的氨基酸180至220的氨基酸序列或由其组成。
[0286]
编码seq id no:66的氨基酸180至220的示例性核酸序列如seq id no:70所示,其在下文提供。
[0287][0288]
在某些实施方式中,cd28多肽可包含与seq id no:68所示的氨基酸序列具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、至少约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,cd28多肽包含作为seq id no:68的连续部分的氨基酸序列或由其组成,其为至少约20、或至少约30、或至少约40、或至少约50且至多218个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,cd28多肽包含seq id no:68的氨基酸1至218、1至50、50至100、100至150、150至218、178至218、或200至218的氨基酸序列或由其组成。在某些实施方式中,本公开的car的共刺激信号传导区包含cd28多肽,该cd28多肽包含seq id no:68的氨基酸178至218的氨基酸序列或由其组成。
[0289]
在某些实施方式中,car的细胞内信号传导结构域包含含有4-1bb多肽例如4-1bb的细胞内结构域或其片段的共刺激信号传导区。4-1bb多肽可包含与具有ncbi参考号:np_001552(seq id no:71)所示的氨基酸序列具有至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、至少约100%同源性或同一性的氨基酸序列或其片段,或由其组成,和/或可以任选地包含至多一个或至多两个或至多三个保守氨基酸取代。在某些非限制性实施方式中,4-1bb多肽包含作为seq id no:71的连续部分的氨基酸序列或由其组成,其为至少20、或至少30、或至少40、或至少50、或至少100、或至少150、或至少150且至多255个氨基酸长度。可替代地或另外地,在非限制性的各种实施方式中,4-1bb多肽包含seq id no:71的氨基酸1至255、1至50、50至100、100至150、150至200或200至255的氨基酸序列或由其组成。在某些实施方式中,car的细胞内信号传导结构域包含共刺激信号传导区,其包含4-1bb多肽,该4-1bb多肽包含seq id no:71的氨基酸214至255的氨基酸序列或由其组成。seq id no:71在下文提供。
[0290][0291]
编码seq id no:71的氨基酸214至255的示例性核酸序列如seq id no:72所示,其在下文提供。
[0292][0293]
在某些实施方式中,car的细胞内信号传导结构域包含共刺激信号传导区,该共刺激信号传导区包含两种或多种共刺激分子的细胞内结构域或其部分,例如cd28的细胞内结构域或其片段和4-1bb的细胞内结构域或其片段,或cd28的细胞内结构域或其片段和ox40的细胞内结构域或其片段。
[0294]
5.3.2.4.示例性car
[0295]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,
cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其片段),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其片段)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:14所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
l-vh。在某些实施方式中,将car命名为“et.b10l3h_mt_h28z”。在某些实施方式中,car包含seq id no:73所示的核苷酸序列,其在下文提供。
[0296][0297]
seq id no:73的氨基酸序列的示例性核酸序列如seq id no:74所示,其在下文提供。
[0298]
[0299][0300]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含4-1bb多肽(例如,人4-1bb的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:13所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
l-vh。在某些实施方式中,将car命名为“et.b10l4h_mt_hbbz”。在某些实施方式中,car包含seq id no:75所示的核苷酸序列,其在下文提供。
[0301][0302]
seq id no:75的氨基酸序列的示例性核酸序列如seq id no:76所示,其在下文提供。
[0303]
[0304][0305]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:13所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
l-vh。在某些实施方式中,将car命名为“et.b10l4h_mt_h28z”。在某些实施方式中,car包含seq id no:77所示的核苷酸序列,其在下文提供。
[0306][0307]
[0308]
seq id no:77的氨基酸序列的示例性核酸序列如seq id no:78所示,其在下文提供。
[0309][0310][0311]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,
cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:14所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h3l_mt_h28z”。在某些实施方式中,car包含seq id no:79所示的核苷酸序列,其在下文提供。
[0312][0313][0314]
seq id no:79的氨基酸序列的示例性核酸序列如seq id no:80所示,其在下文提供。
[0315][0316]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)
跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:13所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h4l_mt_h28z”。在某些实施方式中,car包含seq id no:81所示的核苷酸序列,其在下文提供。
[0317][0318]
seq id no:81的氨基酸序列的示例性核酸序列如seq id no:82所示,其在下文提供。
[0319]
[0320][0321]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:34所示的氨基酸序列,cdr2,其包含seq id no:35所示的氨基酸序列;和v
h cdr3,其包含seq id no:36所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:37所示的氨基酸序列,cdr2,其包含seq id no:38所示的氨基酸序列;和v
l cdr3,其包含seq id no:39所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传
导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:14所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.c3h3l_mt_h28z”。在某些实施方式中,car包含seq id no:83所示的核苷酸序列,其在下文提供。
[0322][0323]
seq id no:83的氨基酸序列的示例性核酸序列如seq id no:84所示,其在下文提供。
[0324]
[0325][0326]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:34所示的氨基酸序列,cdr2,其包含seq id no:35所示的氨基酸序列;和v
h cdr3,其包含seq id no:36所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:37所示的氨基酸序列,cdr2,其包含seq id no:38所示的氨基酸序列;和v
l cdr3,其包含seq id no:39所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:14所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
l-vh。在某些实施方式中,将car命名为“et.c3l3h_mt_h28z”。在某些实施方式中,car包含seq id no:85所示的核苷酸序列,其在下文提供。
[0327][0328]
seq id no:85的氨基酸序列的示例性核酸序列如seq id no:86所示,其在下文提供。
[0329]
[0330][0331]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:40所示的氨基酸序列,cdr2,其包含seq id no:41所示的氨基酸序列;和v
h cdr3,其包含seq id no:42所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:43所示的氨基酸序列,cdr2,其包含seq id no:44所示的氨基酸序列;和v
l cdr3,其包含seq id no:45所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其部分),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其部分)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:14所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
l-vh。在某些实施方式中,将caqr命名为“et.d6l3h_mt_h28z”。在某些实施方式中,car包含seq id no:87所示的核苷酸序列,其在下文提供。
[0332][0333]
seq id no:87的氨基酸序列的示例性核酸序列如seq id no:88所示,其在下文提供。
[0334]
[0335][0336]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其片段),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其片段)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:93所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h1l_mt_h28z”。在某些实施方式中,car包含seq id no:95所示的核苷酸序列,其在下文提供。
[0337][0338][0339]
seq id no:95的氨基酸序列的示例性核酸序列如seq id no:96所示,其在下文提
供。
[0340][0341][0342]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含
seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其片段),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其片段)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:94所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h2l_mt_h28z”。在某些实施方式中,car包含seq id no:97所示的核苷酸序列,其在下文提供。
[0343][0344]
seq id no:97的氨基酸序列的示例性核酸序列如seq id no:98所示,其在下文提供。
[0345][0346]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)
跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其片段),和(c)细胞内信号传导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其片段)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:91所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h5l_mt_h28z”。在某些实施方式中,car包含seq id no:99所示的核苷酸序列,其在下文提供。
[0347][0348]
seq id no:99的氨基酸序列的示例性核酸序列如seq id no:100所示,其在下文提供。
[0349]
[0350][0351]
在某些实施方式中,car是靶向cd371的car。在某些实施方式中,car包含(a)细胞外抗原结合结构域,其包含(i)vh,其包含cdr1,其包含seq id no:28所示的氨基酸序列,cdr2,其包含seq id no:29所示的氨基酸序列;和v
h cdr3,其包含seq id no:30所示的氨基酸序列,和(ii)v
l
,其包含cdr1,其包含seq id no:31所示的氨基酸序列,cdr2,其包含seq id no:32所示的氨基酸序列;和v
l cdr3,其包含seq id no:33所示的氨基酸序列;(b)跨膜结构域,其包含cd28多肽(例如,人cd28的跨膜结构域或其片段),和(c)细胞内信号传
导结构域,其包含(i)cd3ζ多肽,和(ii)共刺激信号传导区,其包含cd28多肽(例如,人cd28的细胞内结构域或其片段)。在某些实施方式中,vh和v
l
经由接头连接,该接头包含seq id no:92所示的核苷酸序列或由其组成。在某些实施方式中,vh和v
l
的位置从n末端到c末端为:v
h-v
l
。在某些实施方式中,将car命名为“et.b10h6l_mt_h28z”。在某些实施方式中,car包含seq id no:101所示的核苷酸序列,其在下文提供。
[0352][0353]
seq id no:101的氨基酸序列的示例性核酸序列如seq id no:102所示,其在下文提供。
[0354]
[0355][0356]
在某些实施方式中,本公开的car还包含诱导型启动子,用于在人细胞中表达核酸序列。用于表达car基因的启动子可以是组成型启动子,例如泛素c(ubic)启动子。
[0357]
5.3.3.tcr样融合分子
[0358]
在某些实施方式中,抗原识别受体是tcr样融合分子。tcr融合分子的非限制性实例包括不依赖hla的基于tcr的嵌合抗原受体(也称为“hit-car”,例如国际专利申请号pct/us19/017525中公开的那些,将其全部并入以供参考)和t细胞受体融合构建体(truc)(例如,在baeuerle等,“synthetic truc receptors engaging the complete t cell receptor for potent anti-tumor response,”nature communications第10卷,文章编号:2087(2019)中公开的那些,将其全部并入以供参考)。
[0359]
在某些实施方式中,tcr样融合分子包含抗原结合链,该抗原结合链包含细胞外抗原结合结构域和恒定结构域,其中tcr样融合分子以不依赖hla的方式结合抗原。在某些实施方式中,恒定结构域包含选自天然或修饰的trac肽、天然或修饰的trbc肽、天然或修饰的
trdc肽、天然或修饰的trgc肽和其任何变体或功能片段的t细胞受体恒定区。在某些实施方式中,恒定结构域包含天然或修饰的trac肽。在某些实施方式中,恒定域包含天然或修饰的trbc肽。在某些实施方式中,恒定结构域能够与另一个恒定结构域形成同二聚体或异二聚体。在某些实施方式中,抗原结合链能够与cd3ζ多肽缔合。在某些实施方式中,抗原结合链在与抗原结合后能够激活与抗原结合链结合的cd3ζ多肽。在某些实施方式中,cd3ζ多肽的激活能够激活免疫应答细胞。在某些实施方式中,tcr样融合分子能够与cd3复合物整合并提供不依赖hla的抗原识别。在某些实施方式中,tcr样融合分子替代cd3/tcr复合物中的内源性tcr。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域能够与另一个细胞外抗原结合结构域二聚化。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含细胞表面受体的配体、细胞表面配体的受体、抗体的抗原结合部分或其片段、或tcr的抗原结合部分。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含一个或两个免疫球蛋白可变区。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含抗体的重链可变区(vh)。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含抗体的轻链可变区(v
l
)。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域能够与另一个细胞外抗原结合结构域二聚化。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含抗体的vh,其中vh能够与包含抗体v
l
的另一个细胞外抗原结合结构域二聚化并形成可变片段(fv)。在某些实施方式中,tcr样融合分子的细胞外抗原结合结构域包含抗体的v
l
,其中v
l
能够与包含抗体vh的另一个细胞外抗原结合结构域二聚化并形成可变片段(fv)。
[0360]
tcr样融合分子可以结合肿瘤抗原或病原体抗原。在某些实施方式中,tcr样融合分子结合肿瘤抗原。
[0361]
5.4.细胞
[0362]
本公开的主题提供包含本公开的靶向cd371的抗原识别受体(例如,在第5.3节中公开的一种)的细胞。在某些实施方式中,细胞选自淋巴谱系的细胞和骨髓谱系的细胞。在某些实施方式中,细胞是免疫应答细胞。在某些实施方式中,免疫应答细胞是淋巴谱系的细胞。
[0363]
在某些实施方式中,细胞是淋巴谱系的细胞。淋巴谱系的细胞可以提供抗体的产生、细胞免疫系统的调节、血液中外来物质的检测、宿主外来细胞的检测等。淋巴谱系细胞的非限制性实例包括t细胞、自然杀伤(nk)细胞、b细胞、树突细胞、可分化成淋巴样细胞的干细胞。在某些实施方式中,干细胞是多能干细胞(例如,胚胎干细胞)。
[0364]
在某些实施方式中,细胞是t细胞。t细胞可以是在胸腺中成熟的淋巴细胞,主要负责细胞介导的免疫。t细胞参与适应性免疫系统。本发明公开主题的t细胞可以是任何类型的t细胞,包括但不限于辅助t细胞、细胞毒性t细胞、记忆t细胞(包括中央记忆t细胞、干细胞样记忆t细胞(或干样记忆t细胞)、和两种效应记忆t细胞:例如t
em
细胞和t
emra
细胞)、调节性t细胞(也称为抑制性t细胞)、肿瘤浸润淋巴细胞(til)、自然杀伤性t细胞、粘膜相关性不变t细胞和γδt细胞。细胞毒性t细胞(ctl或杀伤性t细胞)是能够诱导被感染的体细胞或肿瘤细胞死亡的t淋巴细胞的一个子集。患者自身的t细胞可以被基因改造以通过抗原识别受体(例如car或tcr)的引入靶向特定的抗原。在某些实施方式中,免疫应答细胞是t细胞。t细胞可以是cd4
+
t细胞或cd8
+
t细胞。在某些实施方式中,t细胞是cd8
+
t细胞。
[0365]
在某些实施方式中,细胞是nk细胞。自然杀伤(nk)细胞可以是淋巴细胞,它是细胞介导的免疫力的一部分,并在先天免疫应答中起作用。nk细胞不需要事先激活即可对靶细胞执行细胞毒作用。
[0366]
本发明公开主题的人淋巴细胞的类型包括但不限于外周供体淋巴细胞,例如在sadelain等,nat rev cancer(2003);3:35-45(公开了经遗传修饰以表达car的外周供体淋巴细胞),在morgan,r.a.等,2006science 314:126-129(公开了经遗传修饰以表达包含α和β异二聚体的全长肿瘤抗原识别性t细胞受体复合物的外周供体淋巴细胞),在panelli,等.j immunol(2000);164:495-504;panelli,等.j immunol(2000);164:4382-4392(公开了在肿瘤活组织检查中衍生自肿瘤浸润淋巴细胞(til)的淋巴细胞培养物)和在dupont,等.cancer res(2005):65:5417-5427;papanicolaou,等.blood(2003):102:2498-2505(选择性地公开了使用人工抗原呈递细胞(aapc)或脉冲树突状细胞在体外扩增的抗原特异性外周血白细胞)中公开的那些。
[0367]
细胞(例如,t细胞)可以是自体的、非自体的(例如,同种异体的)、或者是体外从工程化的祖细胞或干细胞衍生的。
[0368]
本发明的细胞可以是骨髓谱系的细胞。骨髓谱系细胞的非限制性实例包括单核细胞、巨噬细胞、嗜中性粒细胞、树突状细胞、嗜碱性粒细胞、嗜中性粒细胞、嗜酸性粒细胞、巨核细胞、肥大细胞、红细胞、血小板和可分化成骨髓细胞的干细胞。在某些实施方式中,干细胞是多能干细胞(例如,胚胎干细胞或诱导的多能干细胞)。
[0369]
在某些实施方式中,本公开的细胞能够调节肿瘤微环境。肿瘤具有对宿主免疫应答敌对的微环境,该微环境涉及恶性细胞保护自身免受免疫识别和消除的一系列机制。这种“敌对的肿瘤微环境”包含多种免疫抑制因子,其包括浸润性调节性cd4
+
t细胞(tregs)、髓样衍生抑制细胞(mdsc)、肿瘤相关巨噬细胞(tam)、包括tgf-b在内的免疫抑制细胞因子、以及靶向由活化的t细胞表达的免疫抑制受体(ctla-4和pd-1)的配体的表达。这些免疫抑制机制在维持耐受性和抑制不适当的免疫应答中起作用,但是在肿瘤微环境内,这些机制阻止了有效的抗肿瘤免疫应答。这些免疫抑制因子在遇到目标肿瘤细胞后,可以共同诱导过继转移的car修饰的t细胞明显的无反应性或凋亡。
[0370]
在某些实施方式中,可以用本公开的靶向cd371的抗原识别受体转导细胞,使得细胞表达抗原识别受体。
[0371]
在某些实施方式中,细胞还包含可溶性单链可变片段(scfv),其结合具有免疫抑制活性或免疫刺激活性的多肽。在某些实施方式中,免疫抑制活性是指诱导细胞(例如,活化的免疫应答细胞)中的信号转导或蛋白质表达的变化,从而导致免疫应答降低。已知通过它们的结合抑制或降低免疫应答的多肽包括cd47、pd-1、ctla-4及其相应的配体,包括sirpa、pd-l1、pd-l2、b7-1和b7-2。这种多肽存在于肿瘤微环境中并抑制对肿瘤细胞的免疫应答。在各种实施方式中,抑制、阻断或拮抗免疫抑制多肽和/或其配体的相互作用增强免疫应答细胞的免疫应答。
[0372]
在某些实施方式中,免疫刺激活性是指诱导细胞(例如,活化的免疫应答细胞)中的信号转导或蛋白质表达的变化,从而导致免疫应答的增加。免疫刺激活性可以包括促炎活性。已知通过它们的结合刺激或增加免疫应答的多肽包括cd28、ox-40、4-ibb及其相应的配体,包括b7-1、b7-2、ox-40l和4-1bbl。这种多肽存在于肿瘤微环境中并激活对肿瘤细胞
的免疫应答。在各种实施方式中,促进、刺激或激动促炎多肽和/或其配体增强免疫应答细胞的免疫应答。
[0373]
包含抗原识别受体(例如,car)和结合具有免疫抑制活性或免疫刺激活性的多肽的可溶性scfv的细胞公开于国际专利公开号wo2014/134165,将其整体并入以供参考。
[0374]
在某些实施方式中,细胞还包含外源cd40l。包含抗原识别受体(例如,car)和外源cd40l的细胞公开于国际专利公开号wo2014/134165。
[0375]
此外,在某些实施方式中,将细胞工程化以表达il-18。在某些实施方式中,细胞还包含外源il-18多肽。在某些实施方式中,外源il-18多肽包含以下提供的seq id no:103所示的氨基酸序列或由其组成。
[0376][0377]
在某些实施方式中,细胞还包含编码il-18多肽的核酸分子。在某些实施方式中,核酸分子包含以下提供的seq id no:104所示的核苷酸序列。
[0378][0379]
或者,在某些实施方式中,细胞在il-18基因座处还包含修饰的启动子/增强子,其可以增加il-18基因表达,例如,放置组成型或诱导型启动子以驱动il-18基因表达。
[0380]
包含抗原识别受体(例如,car)并工程化以表达il-18,例如包含外源il-18多肽或在il-18基因座处修饰的启动子/增强子的细胞公开于国际专利公开号wo2018/027155,将其全部并入本文以供参考。
[0381]
另外地或替代地,将细胞工程化以表达il-33。在某些实施方式中,细胞还包含外源il-33多肽。在某些实施方式中,外源il-33多肽包含以下提供的seq id no:105所示的氨基酸序列或由其组成。
[0382][0383]
在某些实施方式中,细胞还包含编码il-33多肽的核酸分子。在某些实施方式中,核酸分子包含以下提供的seq id no:106所示的核苷酸序列。
[0384][0385]
或者,在某些实施方式中,细胞在il-33基因座处还包含修饰的启动子/增强子,其可以增加il-33基因表达,例如,放置组成型或诱导型启动子以驱动il-33基因表达。包含抗原识别受体(例如,car)并工程化以表达il-33(例如,包含外源il-33多肽或在il-33基因座处的修饰启动子/增强子)的细胞公开于国际专利公开号wo2019/099479,将其全部并入以供参考。
[0386]
另外地或替代地,将细胞工程化以表达il-36。在某些实施方式中,细胞还包含外源il-36多肽。在某些实施方式中,细胞在il-36基因座处还包含修饰的启动子/增强子,其可以增加il-36基因表达,例如,放置组成型或诱导型启动子以驱动il-36基因表达。包含抗原识别受体(例如,car)并工程化以表达il-36,例如包含外源il-36多肽或在il-36基因座处修饰的启动子/增强子的细胞公开于国际专利公开号wo2019/099483,将其全部并入本文以供参考。
[0387]
5.5.组合物和载体
[0388]
本公开的主题提供包含本公开的靶向cd371的抗原识别受体(例如,在第5.3节中公开的一种)的组合物。还提供包含这种组合物的细胞。
[0389]
在某些实施方式中,本公开的靶向cd371的抗原识别受体与启动子可操作地连接。
[0390]
此外,本公开的主题提供核酸组合物,其包含编码本公开的靶向cd371的抗原识别受体(例如,第5.3节中公开的一种)的多核苷酸。还提供包含这种核酸组合物的细胞。
[0391]
在某些实施方式中,核酸组合物还包含与本公开的靶向cd371的抗原识别受体有效连接的启动子。
[0392]
在某些实施方式中,启动子是内源的或外源的。在某些实施方式中,外源启动子选自延伸因子(ef)-1启动子、巨细胞病毒立即早期启动子(cmv)启动子、猿病毒40早期启动子(sv40)启动子、磷酸甘油酸激酶(pgk)启动子、和金属硫蛋白促进剂。在某些实施方式中,启动子是诱导型启动子。在某些实施方式中,诱导型启动子选自nfat转录反应元件(tre)启动子、cd69启动子、cd25启动子和il-2启动子。
[0393]
组合物和核酸组合物可以通过本领域已知的方法或如本文所述的方法施用于受试者或和/或递送到细胞中。细胞(例如,t细胞或nk细胞)的遗传修饰可以通过用重组dna构建体转导基本上均质的细胞组成来完成。在某些实施方式中,逆转录病毒载体(例如γ-逆转录病毒载体或慢病毒载体)用于将dna构建体引入细胞。例如,可以将编码抗原识别受体的多核苷酸克隆到逆转录病毒载体中,并且可以从其内源启动子、逆转录病毒长末端重复序列或对目的靶细胞类型特异性的启动子驱动表达。也可以使用非病毒载体。
[0394]
对于细胞的初始遗传修饰以包括本公开的靶向cd371的抗原识别受体(例如,car或tcr),逆转录病毒载体可以用于转导,然而可以使用任何其它合适的病毒载体或非病毒递送系统。可以在单个多顺反子表达盒、单个载体的多个表达盒或多个载体中构建抗原识别受体。产生多顺反子表达盒的元件的实例包括但不限于各种病毒和非病毒内部核糖体进入位点(ires,例如,fgf-1ires、fgf-2ires、vegf ires、igf-ii ires、nf-κb ires、runx1 ires、p53 ires、甲型肝炎ires、丙型肝炎ires、瘟病毒ires、无杆状病毒ires、小核糖核酸病毒ires、脊髓灰质炎病毒ires和脑心肌炎病毒ires)和可裂解的接头(例如2a肽,例如p2a、t2a、e2a和f2a肽)。逆转录病毒载体和合适的包装系的组合也是合适的,其中衣壳蛋白将具有感染人细胞的功能。已知各种产生两性病毒的细胞系,包括但不限于pa12(miller等,(1985)mol cell biol(1985);5:431-437);pa317(miller等,mol cell biol(1986);6:2895-2902);和crip(danos等,proc natl acad sci usa(1988);85:6460-6464)。非两性粒子也是合适的,例如,用vsvg、rd114或galv包膜和本领域已知的任何其它假型化的粒子。
[0395]
可能的转导方法还包括细胞与生产细胞的直接共培养(bregni等.blood(1992);80:1418-1422),或单独用病毒上清液或含有或不含有适当生长因子和聚阳离子的浓缩载体原种培养(xu,等.exp.hemat.(1994);22:223-230);和hughes,等.j.clin.invest.(1992);89:1817)。
[0396]
其它转导病毒载体可用于修饰细胞。在某些实施方式中,所选择的载体表现出高的感染效率和稳定的整合和表达(参见,例如,cayouette等,human gene therapy 8:423-430,1997;kido等,current eye research 15:833-844,1996;bloomer等,journal of virology71:6641-6649,1997;naldini等,science 272:263-267,1996;和miyoshi等,proc.natl.acad.sci.u.s.a.94:10319,1997)。可以使用的其它病毒载体包括,例如,腺病毒、慢病毒和与腺相关的病毒载体、牛痘病毒、牛乳头瘤病毒或疱疹病毒,例如爱泼斯坦-巴尔病毒(也参见例如miller,human gene thera(1990);15-14;friedman,science 244:1275-1281,1989;eglitis等,biotechniques(1988);6:608-614;tolstoshev等,cur opin biotechnol(1990);1:55-61;sharp,the lancet(1991);337:1277-78;cornetta等,nucleic acid research and molecular biology 36:311-22,1987;anderson,science(1984);226:401-409;moen,blood cells17:407-16,1991;miller等,biotechnol(1989);7:980-90;legal la salle等,science(1993);259:988-90;和johnson,chest(1995)107:77s-83s的载体)。逆转录病毒载体发展地特别好,并已用于临床(rosenberg等,n.engl.j.med(1990);323:370,1990;anderson等,美国专利第5,399,346号)。
[0397]
非病毒方法也可以用于细胞的遗传修饰。例如,可以通过在脂质转染(feigner等,proc natl acad sci u.s.a.(1987);84:7413;ono等,neurosci lett(1990);17:259;brigham等,am j med sci(1989);298:278;staubinger等,methods in enzymol(1983);101:512;wu等,j biol chem(1988);263:14621;wu等,j biol chem(1989);264:16985),或手术条件下的微注射(wolff等,science(1990);247:1465)的情况下施用核酸来将核酸分子引入细胞中。其它非病毒的基因转移方法包括使用磷酸钙、deae葡聚糖、电穿孔和原生质体融合的体外转染。脂质体也可能对将dna递送到细胞中有益。也可以通过将正常核酸转移到可离体培养的细胞类型(例如,自体或异源原代细胞或其后代)中来完成将正常基因移植到受试者的受影响组织中,之后,将细胞(或其后代)注射到目标组织中或全身注射。重组受
体也可以使用转座酶或靶向核酸酶(例如锌指核酸酶、大范围核酸酶或tale核酸酶、crispr)衍生或获得。瞬时表达可通过rna电穿孔获得。
[0398]
任何靶向基因组编辑方法也可用于将本公开的抗原识别受体递送至细胞或受试者。在某些实施方式中,crispr系统用于递送本文公开的本公开的抗原识别受体。在某些实施方式中,锌指核酸酶用于递送本公开的抗原识别受体。在某些实施方式中,talen系统用于递送本公开的抗原识别受体。
[0399]
成簇的规律间隔的短回文重复序列(crispr)系统是在原核细胞中发现的基因组编辑工具。当用于基因组编辑时,该系统包括cas9(一种能够使用crrna作为其向导来修饰dna的蛋白质),crispr rna(crrna,包含cas9用来引导其到达宿主dna正确片段的rna,以及与tracrrna结合的区域(通常以发夹环形式),与cas9形成活性复合物),反式激活crrna(tracrrna,与crrna结合,与cas9形成活性复合物),以及dna修复模板的可选片段(可指导细胞修复过程允许插入特定的dna序列的dna)。crispr/cas9通常采用质粒转染靶细胞。crrna需要针对每种应用进行设计,因为这是cas9用来识别并直接结合细胞中靶dna的序列。携带car表达盒的修复模板还需要针对每种应用进行设计,因为它必须与切口两侧的序列重叠,并为插入序列编码。多个crrna和tracrrna可以包装在一起以形成单向导rna(sgrna)。该sgrna可以与cas9基因连接在一起并制成质粒,以便被转染到细胞中。
[0400]
锌指核酸酶(zfn)是一种人工限制性酶,通过将锌指dna结合结构域与dna裂解结构域结合而产生。锌指结构域可以被工程化以靶向特定的dna序列,其允许锌指核酸酶靶向基因组内的期望序列。各个zfn的dna结合结构域通常包含多个独立的锌指重复序列,并且每个都可以识别多个碱基对。产生新的锌指结构域的最常见方法是结合已知特异性的较小锌指“模块”。zfn中最常见的裂解结构域是来自ii型限制性核酸内切酶foki的非特异性裂解结构域。使用内源性同源重组(hr)机器和带有car表达盒的同源dna模板,zfn可以用于将car表达盒插入基因组。当靶序列被zfn酶切后,hr机器搜索受损染色体与同源dna模板之间的同源性,然后在染色体的两个断裂末端之间复制模板的序列,从而将同源dna模板整合到基因组。
[0401]
转录激活因子样效应物核酸酶(talen)是限制性酶,可以工程化为切割dna的特定序列。talen系统的工作原理几乎与zfn相同。它们是通过将转录激活因子样效应物dna结合结构域与dna裂解结构域结合而产生的。转录激活因子样效应物(tale)由具有两个可变位置的33-34个氨基酸重复基序组成,这些位置对特定核苷酸有很强的识别能力。通过组装这些tale的阵列,可以对tale dna结合结构域进行改造以结合所需的dna序列,从而指导核酸酶切割基因组中的特定位置。用于多核苷酸疗法的cdna表达可以从任何合适的启动子(例如人巨细胞病毒(cmv)、猿猴病毒40(sv40)或金属硫蛋白启动子)中进行指导,并由任何适当的哺乳动物调节元件或内含子(例如延伸因子1a增强子/启动子/内含子结构)调节。例如,如果需要的话,已知优先在特定细胞类型中指导基因表达的增强子可以用于指导核酸的表达。所使用的增强剂可以包括但不限于被表征为组织或细胞特异性增强子的那些。或者,如果将基因组克隆用作治疗构建体,则可以通过同源调控序列或,如果需要,通过衍生自包括上述任何启动子或调控元件的异源的调控序列来介导调控。
[0402]
用于递送基因组编辑剂/系统的方法可以根据需要而变化。在某些实施方式中,选择的基因组编辑方法的组分作为dna构建体在一个或多个质粒中递送。在某些实施方式中,
通过病毒载体递送组分。常见的递送方法包括但不限于电穿孔、显微注射、基因枪、穿刺(impalefection)、流体静压力、连续输注、超声处理、磁转染、腺相关病毒、病毒载体的包膜蛋白假型、可复制的载体顺式和反式元件、单纯疱疹病毒和化学媒介物(例如寡核苷酸、脂复合物、聚合物小体、多复合物、树状聚合物、无机纳米颗粒和穿透细胞的肽)。
[0403]
5.6.多肽
[0404]
本公开的主题提供通过产生序列改变来优化氨基酸序列或核酸序列的方法。这样的改变可以包括某些突变、缺失、插入或翻译后修饰。本公开的主题还包括本文公开的任何天然存在的多肽(包括但不限于cd371、cd8、cd28、4-1bb和cd3ζ)的类似物。类似物可以通过氨基酸序列差异、通过翻译后修饰或通过两者与本文公开的天然存在的多肽不同。类似物可表现出与本公开主题的全部或部分天然存在的氨基酸序列具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更多的同源性或同一性。序列差异的长度是至少5、10、15或20个氨基酸残基,例如至少25、50或75个氨基酸残基,或超过100个氨基酸残基。同样,在确定同一性程度的示例性方法中,可以使用blast程序,其概率得分在e-3
和e-100
之间,指示密切相关的序列。修饰包括多肽的体内和体外化学衍生,例如乙酰化、羧化、磷酸化或糖基化;这样的修饰可以在多肽合成或加工过程中或在用分离的修饰酶处理之后发生。类似物也可以通过天然序列的改变而不同于天然存在的多肽。这些包括天然和诱导的遗传变异(例如,如sambrook,fritsch和maniatis,《分子克隆:实验室手册》(第2版),csh出版社,1989,或ausubel等,同上,中所述,是由于通过辐射或暴露于乙烷甲基硫酸盐中的随机诱变或通过位点特异性诱变而产生的)。还包括环化的肽、分子和类似物,其含有除l-氨基酸以外的残基,例如d-氨基酸或非天然存在的或合成的氨基酸,例如β或γ氨基酸。
[0405]
除了全长多肽,本公开主题还提供本文公开的任何多肽的片段。如本文所用,术语“片段”是指至少5、10、13或15个氨基酸。在某些实施方式中,片段包含至少20个连续氨基酸、至少30个连续氨基酸或至少50个连续氨基酸。在某些实施方式中,片段包含至少60至80、100、200、300或更多个连续氨基酸。片段可以通过本领域技术人员已知的方法产生,或者可以由正常的蛋白质加工产生(例如,从新生多肽中去除生物活性不需要的氨基酸,或者通过替代性的mrna剪接或替代性蛋白质加工事件去除氨基酸))。
[0406]
5.7.剂型和给药
[0407]
本公开的主题还提供包含本公开的细胞的组合物。包含本公开的细胞的组合物可以方便地以无菌液体制剂的形式提供,例如等渗水溶液剂、悬浮液、乳剂,分散剂或粘性组合物,其可以缓冲至选定的ph。液体制剂通常比凝胶、其它粘性组合物和固体组合物更容易制备。另外,液体组合物在某种程度上更方便施用,尤其是通过注射。另一方面,可以在适当的粘度范围内配制粘性组合物以提供与特定组织的更长的接触时间。液体或粘性组合物可以包含载体,所述载体可以是溶剂或分散介质,其包含例如水、盐水、磷酸盐缓冲盐水、多元醇(例如甘油、丙二醇、液体聚乙二醇等)及其合适的混合物。
[0408]
可以通过将遗传修饰的细胞掺入所需量的适当溶剂中,并根据需要掺入不同量的其它成分来制备无菌注射溶液。这样的组合物可以与合适的载体、稀释剂或赋形剂例如无菌水、生理盐水、葡萄糖、右旋糖等混合。组合物也可以冻干。所述组合物可包含辅助物质,例如润湿剂、分散剂或乳化剂(例如,甲基纤维素)、ph缓冲剂、胶凝剂或增粘剂、防腐剂、矫
味剂、颜料等,这取决于给药途径和所需制剂。可以参考标准文本,例如“remington's pharmaceutical science”,1985年第17版,以引用方式并入本文,以制备合适的制剂,而无需进行过多的实验。
[0409]
可以添加增强组合物的稳定性和无菌性的各种添加剂,包括抗微生物防腐剂、抗氧化剂、螯合剂和缓冲剂。可以通过各种抗细菌和抗真菌剂,例如对羟基苯甲酸酯、三氯叔丁醇、苯酚、山梨酸等来确保防止微生物的作用。可通过使用延迟吸收的试剂例如单硬脂酸铝和明胶来延长可注射药物形式的吸收。然而,根据本公开的主题,所使用的任何媒介物、稀释剂或添加剂将必须与遗传修饰的细胞相容。
[0410]
该组合物可以是等渗的,即它们可以具有与血液和泪液相同的渗透压。组合物的所需等渗性可以使用氯化钠或其它药学上可接受的试剂例如葡萄糖、硼酸、酒石酸钠、丙二醇或其它无机或有机溶质来实现。氯化钠可以是特别适用于含有钠离子的缓冲剂。
[0411]
如果需要,可使用药学上可接受的增稠剂将组合物的粘度保持在选定水平。例如,甲基纤维素容易且经济地获得并且易于使用。其它合适的增稠剂包括,例如,黄原胶、羧甲基纤维素、羟丙基纤维素、卡波姆等。增稠剂的浓度可以取决于选择的试剂。重要的是要使用能够达到所选粘度的用量。显然,合适载体和其它添加剂的选择将取决于确切的给药途径和特定剂型的性质,例如液体剂型(例如,是否将组合物配制成溶液剂、悬浮液、凝胶剂或其它液体形式,例如定时释放形式或液体填充形式)。
[0412]
可以将包含本公开的细胞的组合物系统地或直接提供给受试者,以诱导和/或增强对抗原的免疫应答和/或治疗和/或预防肿瘤。在某些实施方式中,将本公开的免疫应答细胞或包含其的组合物直接注射到目的器官(例如,受肿瘤影响的器官)中。或者,例如通过向循环系统(例如,肿瘤脉管系统)给药,将本公开的细胞或包含其的组合物间接地提供给目的器官。可以在施用细胞或组合物之前,之中或之后提供扩增和分化剂,以增加体外或体内细胞(例如t细胞或nk细胞)的产生。
[0413]
可以在任何生理上可接受的载体中通常在血管内施用本公开的细胞,然而它们也可以被引入骨骼或其它方便的部位,在这些部位细胞可以找到合适的再生和分化部位(例如胸腺)。
[0414]
对于所治疗的受试者,要施用的细胞数量可以有所不同。在某些实施方式中,向受试者(例如,人受试者)施用的本公开的细胞为约104至约10
10
之间、约104至约107之间、约105至约107、约105至约109之间、或约106至约108之间。可以以更少的数量施用更有效的细胞。通常,至少会施用约l
×
l05个细胞,最终达到约l
×
l0
10
或更多。在某些实施方式中,将至少约1
×
105、5
×
105、1
×
106、约5
×
106、约1
×
107、约5
×
107、约1
×
108或约5
×
108的本公开的细胞施用于受试者。在某些实施方式中,将约1
×
106个本公开的细胞施用于受试者。可以根据每个受试者的个体因素,包括其大小、年龄、性别、体重和具体受试者的状况,来确定有效剂量的精确确定。本领域技术人员从本公开和本领域知识中可以容易地确定剂量。
[0415]
本公开的细胞可以包含纯化的细胞群体。本领域技术人员可以使用各种众所周知的方法,例如荧光激活细胞分选(facs),容易地确定群体中本公开的细胞的百分比。在包含本公开的免疫应答细胞的群体中,纯度的合适范围是约50%至约55%、约5%至约60%、以及约65%至约70%。在某些实施方式中,纯度为约70%至约75%、约75%至约80%或约80%至约85%。在某些实施方式中,纯度为约85%至约90%,约90%至约95%或约95%至约
100%。剂量可以由本领域技术人员容易地调节(例如,纯度降低可能需要增加剂量)。可以通过注射、导管等引入细胞。
[0416]
本领域技术人员可以容易地确定组合物中和在方法中施用的细胞和任选的添加剂、媒介物和/或载体的量。通常,任何添加剂(除一种或多种活性细胞和/或一种或多种试剂外)在磷酸盐缓冲盐水中的存在量为0.001%至50%(重量)溶液,并且活性成分按微克至毫克的顺序存在,例如约0.0001wt%至约5wt%、约0.0001wt%至约1wt%、约0.0001wt%至约0.05wt%或约0.001wt%至约20wt%、约0.01wt%至约10wt%或约0.05wt%至约5wt%。对于要施用于动物或人的任何组合物,可以确定以下结果:毒性,例如通过在合适的动物模型例如啮齿类动物如小鼠中确定致死剂量(ld)和ld50;组合物的剂量,其中的组分浓度和施用组合物的时间,引起合适的反应。根据技术人员,本公开和本文引用的文献的知识,这种确定不需要过度的实验。并且,可以确定连续给药的时间而无需过多的实验。
[0417]
在某些实施方式中,组合物是药物组合物,其包含本文公开的细胞和药学上可接受的载体。
[0418]
组合物的施用可以是自体的或异体的。例如,细胞可以从一名受试者获得,并施用于同一受试者或不同的、相容的受试者。可以施用外周血衍生细胞或其后代(例如,体内、离体或体外衍生的)。当施用本公开的组合物(例如,包含本公开的细胞的药物组合物)时,可以将其配制成单位剂量的可注射形式(溶液、悬浮液、乳剂)。
[0419]
本公开的细胞和组合物可以通过本领域已知的任何方法施用,包括但不限于口服施用、静脉内施用、皮下施用、结内施用、瘤内施用、鞘内施用、胸膜内施用、骨内施用、腹膜内施用、胸膜施用和直接施用于受试者。
[0420]
5.8.治疗方法
[0421]
本公开主题的细胞和包含其的组合物可用于治疗和/或预防肿瘤或瘤形成。可以将这种细胞施用于有需要的受试者(例如,人受试者)以治疗和/或预防肿瘤或瘤形成(例如,急性髓性白血病(aml)、多发性骨髓瘤、非霍奇金淋巴瘤、霍奇金淋巴瘤、慢性淋巴细胞性白血病(cll),胶质母细胞瘤)。在某些实施方式中,细胞是t细胞。t细胞可以是cd4
+
t细胞或cd8
+
t细胞。在某些实施方式中,t细胞是cd4
+
t细胞。
[0422]
本公开的主题提供用于在有需要的受试者中诱导和/或增加免疫应答的方法。本公开的细胞和包含其的组合物可用于疗法或药物。本公开的主题提供使用细胞(例如,t细胞)或包含其的组合物的各种方法。例如,本公开的细胞和包含其的组合物可用于减少受试者的肿瘤负荷。本公开的细胞可以减少受试者的肿瘤细胞数量、减小肿瘤大小和/或根除肿瘤。本公开的细胞和包含其的组合物可用于治疗和/或预防受试者的肿瘤或瘤形成。本公开的细胞和包含其的组合物可用于延长患有肿瘤或瘤形成的受试者的生存期。这些方法包括施用本文公开的细胞或包含其的组合物(例如药物组合物)以实现期望的效果,例如缓解现有病症或预防复发。为了治疗,施用的量是有效产生所需效果的量。可以一次或多次给药来提供有效量。可以大剂量或通过连续灌注来提供有效量。
[0423]
本公开的主题提供使用细胞(例如,t细胞)或包含其的组合物的各种方法。例如,本公开的主题提供减少受试者中的肿瘤负荷的方法。在某些实施方式中,减少肿瘤负荷的方法包括将本发明公开的细胞或包含其的组合物施用于受试者。本公开的细胞可以减少受试者的肿瘤细胞数量、减小肿瘤大小和/或根除肿瘤。
[0424]
肿瘤或瘤形成可以是实体瘤。实体瘤的非限制性实例包括间皮瘤、肺癌、胰腺癌、卵巢癌、乳腺癌、结肠癌、胸膜瘤、成胶质细胞瘤、食管癌、胃癌(gastric cancer)、滑膜肉瘤、胸腺癌、子宫内膜癌、胃癌(stomach cancer)和胆管癌。
[0425]
本公开的主题还提供增加或延长患有肿瘤或瘤形成的受试者的生存期的方法。在某些实施方式中,增加或延长患有肿瘤或瘤形成的受试者的生存期的方法包括向受试者施用本发明公开的免疫应答细胞或包含其的组合物。该方法可以减少或根除受试者的肿瘤负担。此外,本公开的主题提供增加受试者的免疫应答的方法,包括向受试者施用本公开的细胞或包含其的组合物。本公开的主题还提供用于治疗和/或预防受试者的肿瘤或瘤形成的方法,其包括向受试者施用本公开的细胞或包含其的组合物。
[0426]
瘤形成或肿瘤的非限制性实例包括急性髓性白血病(aml)、多发性骨髓瘤、慢性淋巴细胞性白血病(cll)、淋巴瘤(霍奇金淋巴瘤、非霍奇金淋巴瘤)、胶质母细胞瘤、骨髓增生异常综合征(mds)和慢性髓细胞性白血病(cml)、骨癌、肠癌、肝癌、皮肤癌、头或颈癌、黑素瘤(皮肤或眼内恶性黑素瘤)、肾癌(例如透明细胞癌)、喉癌、前列腺癌(例如激素难治性前列腺腺癌)、血癌(例如白血病、淋巴瘤和骨髓瘤)、子宫癌、直肠癌、肛区癌、膀胱癌、脑癌、胃癌(stomach cancer)、睾丸癌、输卵管癌、子宫内膜癌、子宫颈癌、阴道癌、外阴癌、白血病(例如急性白血病、急性淋巴细胞性白血病、急性髓细胞白血病、急性成淋巴细胞性白血病、急性早幼粒细胞性白血病、急性单核细胞性白血病、急性红白血病、慢性白血病、慢性髓细胞白血病、真性红细胞增多症、小肠癌、内分泌系统癌、甲状腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道癌、阴茎癌、儿童实体瘤、淋巴细胞淋巴瘤、膀胱癌、肾或输尿管癌、肾盂癌、中枢神经系统(cns)肿瘤、原发性cns淋巴瘤、肿瘤血管生成、脊髓轴肿瘤、脑干胶质瘤、垂体腺瘤、卡波西氏肉瘤(kaposi’s sarcoma)、表皮样癌、鳞状细胞癌、t细胞淋巴瘤、环境诱导的癌症包括由石棉诱导的癌症、包括瓦尔登斯特伦巨球蛋白血症(waldenstrom’s macroglobulinemia)、重链病和实体瘤比如肉瘤和癌(carcinoma)(例如纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨源性肉瘤、脊索瘤、血管肉瘤、内皮肉瘤、淋巴管肉瘤、淋巴管内皮肉瘤(lymphangioendotheliosarcoma)、滑膜瘤、间皮瘤、尤文氏瘤(ewing’s tumor)、平滑肌肉瘤、横纹肌肉瘤、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、支气管癌、肝细胞瘤、胆管癌、绒毛膜癌、精原细胞瘤、胚胎性癌、肾母细胞瘤(wilm’s tumor)、子宫颈癌、唾液腺癌、子宫癌、睾丸癌、膀胱癌、上皮癌、神经胶质瘤、星形细胞瘤、成神经管细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、成血管细胞瘤、听神经瘤、少突神经胶质瘤、许旺氏细胞瘤、脑膜瘤、黑素瘤、成神经细胞瘤和视网膜母细胞瘤)。
[0427]
在某些实施方式中,肿瘤或瘤形成选自急性髓性白血病(aml)、多发性骨髓瘤、慢性淋巴细胞性白血病(cll)、霍奇金淋巴瘤、非霍奇金淋巴瘤、胶质母细胞瘤、骨髓增生异常综合征(mds)和慢性髓细胞性白血病(cml)。在某些实施方式中,肿瘤或瘤形成是aml。
[0428]
受试者可以患有疾病的晚期形式,在这种情况下,治疗目标可以包括缓解或逆转疾病进展和/或减轻副作用。受试者可以具有已经对其进行过治疗的病史,在这种情况下,治疗目标通常包括降低或延迟复发风险。
[0429]
由于本公开的靶向cd371的抗原识别受体的表面表达,过继转移细胞(例如,免疫应答细胞,例如t细胞或nk细胞)在肿瘤部位被赋予增强的和选择性的溶细胞活性。此外,在其定位于肿瘤或病毒感染及其增殖之后,细胞将肿瘤或病毒感染位点转变成高传导性环
境,以用于广泛涉及生理抗肿瘤或抗病毒应答的多种免疫细胞(肿瘤浸润淋巴细胞、nk细胞、nkt细胞、树突状细胞和巨噬细胞)。
[0430]
可以对本公开的细胞(例如,t细胞)进行进一步修饰,以避免或最小化免疫并发症(称为“恶性t细胞转化”),例如移植物抗宿主病(gvhd),或当健康组织表达与肿瘤细胞相同的靶抗原时,会导致类似于gvhd的结果的风险。该问题的潜在解决方案是将自杀基因改造到本公开的细胞中。合适的自杀基因包括但不限于单纯疱疹病毒胸苷激酶(hsv-tk)、诱导型caspase 9自杀基因(icasp-9)和截短的人表皮生长因子受体(egfrt)多肽。在某些实施方式中,自杀基因是egfrt多肽。egfrt多肽可通过施用抗egfr单克隆抗体(例如西妥昔单抗)来使t细胞消除。egfrt可以共价连接至抗原识别受体(例如car)的上游。自杀基因可以包含在包含编码本公开的抗原识别受体(例如car)的核酸的载体内。以此方式,在恶性t细胞转化(例如,gvhd)过程中施用旨在激活自杀基因的前药(例如,前药(例如,可以激活icasp-9的ap1903)),可以触发由自杀基因激活的表达抗原识别受体(例如car)的细胞的凋亡。将自杀基因掺入本公开的car中可提高安全性,并能够在很短的时间内消除大部分受体表达细胞。可以在细胞输注后的给定时间点抢先消除掺入了自杀基因的本公开的细胞(例如,t细胞),或在毒性的最早迹象时将其消除。
[0431]
5.9.试剂盒
[0432]
本公开的主题提供用于在受试者中诱导和/或增强免疫应答、治疗和/或预防受试者的肿瘤或瘤形成、减少受试者的肿瘤负荷和/或增加或延长受试者体内有肿瘤或瘤形成的受试者的生存期的试剂盒。在某些实施方式中,试剂盒包含本公开的细胞或包含其的组合物。在某些实施方式中,试剂盒包括无菌容器;这样的容器可以是盒子、安瓿、瓶、小瓶、管、袋、小袋、泡罩包装或本领域已知的其它合适的容器形式。这样的容器可以由塑料、玻璃、层压纸、金属箔或其它适合于容纳药物的材料制成。在某些非限制性实施方式中,试剂盒包含编码本公开的靶向cd371的抗原识别受体(例如,car或tcr)的核酸分子。
[0433]
如果需要的话,将细胞和/或核酸分子与将细胞或核酸分子施用于患有肿瘤或病原体或免疫疾病或有发展成肿瘤或瘤形成的受试者的说明书一起提供。说明书通常包括有关组合物用于治疗和/或预防肿瘤或瘤形成的信息。在某些实施方式中,说明书包括以下至少一项:治疗剂的描述;用于治疗或预防肿瘤或瘤形成的剂量表和给药;注意事项;警告;适应症;不适应症;用药信息;不良反应;动物药理学;临床研究;和/或参考。这些说明书可以直接打印在容器上(如果有的话),或者作为粘贴在容器上的标签,或者作为单独的纸页、小册子、卡片或文件夹提供在容器内或与容器一起。
[0434]
实施例
[0435]
除非另有说明,否则本公开的实践采用分子生物学、微生物学、细胞生物学、生物化学和免疫学的常规技术(包括重组技术),其在技术人员的能力范围内。在诸如“分子克隆:实验室手册”,第二版(sambrook,1989);“寡核苷酸合成”(gait,1984);“动物细胞培养”(freshney,1987);“酶学方法”“实验免疫学手册”(weir,1996);“哺乳动物细胞的基因转移载体”(miller和calos,1987年);“分子生物学的当前方法”(ausubel,1987年);“pcr:聚合酶链反应”,(mullis,1994年);“免疫学的当前方法”(coligan,1991年)中充分地解释了这些技术。这些技术适用于本文公开的多核苷酸和多肽的产生,并且因此可以在制备和实施本文公开的主题中考虑。在以下部分中将讨论用于具体实施例的特别有用的技术。
[0436]
提出以下实施例以向本领域普通技术人员提供有关如何制备和使用本公开的细胞和组合物的完整公开和描述,而不旨在限制发明人视为其发明的范围。
[0437]
实施例1
–
靶向cd371的car的生成
[0438]
生成了以下六种靶向cd371的car:“et.b10l3h_mt_h28z”、“et.b10l4h_mt_hbbz”、“et.b10l4h_mt_h28z”、“et.b10h3l_mt_h28z”、“et.b10h4l_mt_h28z”、“et.c3h3l_mt_lht28z”、“et.c3l3h_mt_h28z”和“et.d6l3h_mt_h28z”。car的结构如图1所示。
[0439]
如图2所示,通过egfr和myc-tag在转导的人t细胞表面检测到car。针对egfrt(西妥昔单抗-apc(cetuximab-apc))和myc-tag(9b11-pe)的抗体用于检测基于b10的构建体中egfrt和人抗人car的表面表达。对照包括不表达egfrt或myc标签的非转导人t细胞,以及含有car构建体的非myc标签etah19h28z(抗人cd19 car t细胞)和etc1hvh28z(源自小鼠抗人cd371抗体1075.7的抗cd371 car t细胞)。
[0440]
实施例2
–
靶向cd371的cat t细胞的体外细胞毒性活性
[0441]
t细胞用许多靶向cd371的car(即“et.c1hvh28z”、“et.b10lh_mt_h28z”、“et.b10lhg4s_mt_h28z”、“et.b10hl_mt_h28z”、“et.c3hl_mt_h28z”、“et.c3lh_mt_h28z”和“et.d6lh_mt_h28z”)转染。et.c1hvh28z用作阳性对照,来源于小鼠抗人cd371抗体1075.7。“et.b10lhg4s_mt_hdel”是一种非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)。这些靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶(u937gl)的cd371+u937细胞以不同的效应物:肿瘤比共培养。24小时后,测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。结果显示在图3中。如图3所示,靶向cd371的car t细胞能够裂解表达cd371的细胞。
[0442]
实施例3
–
靶向cd371的cat t细胞的体外细胞毒性活性
[0443]
t细胞用许多靶向cd371的car(即“et.c1hvh28z”、“et.b10l4h_mt_h28z”、“et.b10l3h_mt_h28z”、“et.b10l4h_mt_hbbz”、“et.b10h3l_mt_h28z”、“et.c3hl_mt_h28z”、“et.c3lh_mt_h28z”和“et.m195_mt_h28z”)转染。et.c1hvh28z用作阳性对照,来源于小鼠抗人抗体1075.7)。“et.m195mth28z”代表源自鼠抗人cd33抗体m195的靶向cd33的car t细胞。“et.m195mth28z”用作阳性对照,因为u937细胞也表达cd33。健康人供体来源(即供体c和供体d)靶向cd371的car t细胞与表达gfp和萤火虫荧光素酶的cd33+/cd371+u937细胞(u937gl)以不同的效应物:肿瘤比共培养。24小时后,测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养物中检测到的信号百分比。结果显示在图4(供体c)和图5(供体d)中。如图4和5所示,基于b10的car(hl/lh二者)t细胞优于基于c3的car t细胞。
[0444]
实施例4
–
靶向cd371的car t细胞的抗原刺激
[0445]
健康人供体来源(即供体c和供体d)靶向cd371的car t细胞与cd33+/cd371+u937gl以1:12.5的e:t比和30,000car+/ml的浓度共培养。大约每4-5天,对car t细胞进行计数并通过流式细胞术对其进行表征,然后将初始数量的肿瘤细胞添加回培养物中(如箭头所示)。结果显示在图6(供体c)和图7(供体d)中。“et.b10lhdel”代表无功能的car t细胞(缺乏信号传导结构域)。“et.c1hvh28z”代表源自小鼠抗人cd371抗体1075.7)的靶向cd371的car,而“etm195mth28z”或“m19528”代表源自鼠抗人cd33抗体m195的靶向cd33的car t细
胞。如图6和7所示,在长期重复刺激试验中,基于b10的car t细胞优于基于c3的car t细胞。
[0446]
实施例5
–
靶向cd371的cat t细胞的体外细胞毒性活性
[0447]
健康人供体来源(即供体a和供体b)靶向cd371的car t细胞与cd371阳性u937细胞或表达gfp和萤火虫荧光素酶(u937gl或hl60gl)的hl60细胞以不同的效应物:肿瘤比共培养。在共培养24小时后测量生物发光,并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937gl的共培养中检测到的信号百分比。结果显示在图8a和8b(对于u937gl细胞)以及图9a和9b(对于hl 60细胞)中。如图8a-8b和9a-9b所示,基于b10hl的靶向cd371的car t细胞优于基于b10lh的靶向cd371的car t细胞。
[0448]
实施例6
–
靶向cd371的car t细胞的抗原特异性细胞毒性活性
[0449]
评估了靶向cd371的car t细胞的细胞毒性活性是否对cd371具有特异性。产生了人cd371(hcd371)crispr敲除细胞系。人cd371用crispr从hl60gl和u937gl中敲除,并使用抗人cd371 apc偶联抗体通过流式细胞术确认敲除。请参见图10。
[0450]
健康人供体来源(即供体a和供体b)靶向cd371的car t细胞与表达rfp和海萤荧光素酶的抗原阴性u937细胞或hl60(u937rfpcyp.371ko或hlgl.371ko)以不同的效应物:肿瘤比共培养。24小时后,测量生物发光并将其绘制为在非功能性靶向cd371的car t细胞(基于b10l4h,但没有cd28或cd3ζ信号传导结构域)和u937rfpcyp.371ko的共培养物中检测到的信号百分比。结果显示在图11a-11b(对于u937细胞)和图12a-12b(对于hl60细胞)中。如图11a-11b和12a-12b所示,基于b10hl和基于b10lh的靶向cd371的car t细胞对cd371阴性u937细胞均未显示出显著的细胞毒性,并且对cd371阴性hl60细胞显示出有限的细胞毒性。
[0451]
实施例7
–
靶向cd371的car t细胞的细胞因子分泌
[0452]
评估了靶向cd371的car t细胞产生细胞因子的能力。靶向cd371的car t细胞单独与cd371阴性肿瘤细胞或cd371阳性u937细胞以1:1的效应物:肿瘤比(200μl中40,000:40,000个细胞)共培养。24小时后,从培养物中收集上清液,并使用基于珠的多重测定测量ifn-γ、il-2和tnf-α的分泌水平。结果显示在图13a-13b(对于ifn-γ)、图14a-14b(对于il-2)和图15a-15b(对于tnf-α)中。如图13a-13b、图14a-14b和图15a-15b所示,与基于b10lh的car t细胞相比,基于b10hl的caqr t细胞以抗原依赖性方式产生更多的细胞因子。
[0453]
实施例8
–
靶向cd371的car t细胞的增殖能力
[0454]
car t细胞由两个健康的供体(即供体a和供体b)产生。靶向cd371的car t细胞与cd371+u937gl以1:5的e:t比和50,000car+/ml的浓度共培养。大约每5天对car t细胞进行计数,并通过流式细胞术进行表征。在箭头指示的时间点将初始数量的肿瘤细胞添加回培养物中。结果显示在图16中。如图16所示,基于b10hl和基于b10-lh的靶向cd371的car t细胞在体外显示出接近可比的扩增能力。
[0455]
实施例9
–
靶向cd371的car t细胞的体内抗肿瘤活性
[0456]
评估了基于b10的靶向cd371的car t细胞的体内抗肿瘤活性。图17示出aml的异种移植模型。ncg小鼠通过尾静脉接种5.0
×
104u937gl肿瘤细胞、aml fab-m5细胞系,并在三天后用大约1.25
×
106car t细胞治疗。监测小鼠存活率。结果显示在图18(供体1)和图19(供体2)中。如图18和19所示,与基于b10lh的car t细胞相比,基于b10hl的car t细胞在aml异种移植小鼠中显示出更高的存活率。
[0457]
接下来,评估了体内活性是否具有剂量依赖性。ncg小鼠接种5.0
×
104u937gl肿瘤
细胞,三天后用不同剂量的car t细胞(1.25
×
105、2.5
×
105、5.0
×
105和1.0
×
106)治疗。结果显示在图20中。如图20所示,在剂量反应治疗模型中,基于b10hl的car t细胞优于基于b10lh的car t细胞。
[0458]
实施例10:b10 scfv与表达cd371的细胞系的结合
[0459]
评估了两种方向(v
h-v
l
或v
l-vh)的b10(也称为“1b10”)scfv与表达cd371的细胞的结合。结果显示在图21中。如图21所示,检测到v
l-vh方向的b10 scfv与细胞的结合。然而,流式细胞术未观察到v
h-v
l
方向的b10 scfv的结合,表明亲和力较低,因此需要二价结合。
[0460]
实施例11:b10 scfv与溶液中的重组cd371结合
[0461]
对于scfv亲和力测量,用链霉亲和素捕获生物素化的cd371,并使用可溶性scfv作为分析物。表8示出不同scfv形式的解离常数(kd)、开启率(k
on
)和关闭率(k
off
)。与流式细胞术结果一致,观察到v
h-v
l
方向的1b10 scfv的弱结合,但解离常数无法通过任何曲线拟合方法计算。
[0462]
因此,令人惊讶的是,包含较低结合亲和力scfv的car在体外和体内优于包含较高结合亲和力scfv的car,如实施例5、7和9中所示。
[0463]
表8.v
h-v
l
或v
l-vh方向上的b10 scfv对可溶性cd371的结合亲和力
[0464][0465]
实施例12:基于b10hl的第二代car t细胞的体内和体外活性
[0466]
成功生成了具有截短的egfr(et)、myc-标签(mt)和g4s接头的基于b10hl的第二代car t细胞:
[0467]
·
et.b10h4l_mt_h28z描述于实施例1。
[0468]
·
et.b10h1l_mt_h28z包含具有v
h-v
l
方向的基于b10的scfv(命名为b10h1l),和5个氨基酸长的g4s接头(ggggs[seq id no:93]),以及基于cd28z的信号传导结构域。
[0469]
·
et.b10h2l_mt_h28z包含具有v
h-v
l
方向的基于b10的scfv(命名为b10h2l)和10个氨基酸长的g4s接头(ggggsggggs[seq id no:94]),以及基于cd28z的信号传导结构域。
[0470]
·
et.b10h5l_mt_h28z包含具有v
h-v
l
方向的基于b10的scfv(命名为b10h5l)和24个氨基酸长的g4s接头(ggggsggggsggggsgggsggggs[seq id no:91]),以及基于cd28z的信号传导结构域。
[0471]
·
et.b10h6l_mt_h28z包含具有v
h-v
l
方向的基于b10的scfv(命名为b10h6l)和29个氨基酸的g4s接头(ggggsggggsggggsggggsgggsggggs[seq id no:92]),以及基于cd28z的信号传导结构域。
[0472]
产生了另外的基于b10h4l的第二代car t细胞,该细胞包括组成型il18(命名为“et.b10h4lmt28zpil18”)或il33(命名为“et.b10h4lmt28zpil33”)分泌。包含et.b10h4lmt28zpil18的t细胞包含命名为“et.b10h4l_mt_h28z”的car和外源il-18多肽(例如,包含seq id no 103所示氨基酸序列的外源il-18多肽)。包含et.b10h4lmt28zpil33的t细胞包含命名为“et.b10h4l_mt_h28z”的car和外源il-33多肽(例如,包含seq id no 105所示氨基酸序列的外源il-33多肽)。
[0473]
如图22所示,具有v
h-v
l
方向的scfv的car t细胞对u937细胞的细胞毒性优于具有vl-vh方向的scfv的car t细胞。为了评估这些基于b10的car t细胞的体内活性,将ncg小鼠接种5
×
104u937gl肿瘤细胞,并用不同剂量的car t细胞进行治疗。监测记录治疗过的小鼠的存活率。如图23所示,在5
×
105car t细胞的剂量下,基于b10h3l、b10h5l和分泌il33的b10h4l的靶向人cd371的car t细胞优于基于b10h4l的car t细胞。如图24所示,在2.5
×
105car t细胞的剂量下,基于分泌il18和分泌il33的b10h4l的靶向人cd371的car t细胞优于基于b10h4l的car t细胞。如图25所示,在1.0
×
105car t细胞的低剂量下,分泌il18的b10h4l靶向人cd371的car t细胞优于其他car t细胞。
[0474]
本公开的主题的实施方式
[0475]
从前面的描述中,将显而易见的是,可以对本公开的主题进行变型和修改以将其应用于各种用途和条件。这样的实施方式也在所附权利要求的范围内。
[0476]
本文所述变量定义中的元素列表包括将变量定义为列出的元素的任何单个元素或组合(或子组合)。本文所述实施方式包括将该实施方式作为任何单一实施方式或与任何其它实施方式或其部分相结合。
[0477]
本说明书中提到的所有专利和出版物都以相同的程度并入本文以供参考,就如同每个独立的专利和出版物都被具体地和单独地指出以并入而供参考一样。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1