叶酸-普朗尼克-MXenes肿瘤靶向载药体系及其制备方法
本发明涉及一种靶向纳米技术领域,特别是涉及一种叶酸-普朗尼克-mxenes肿瘤靶向载药体系及其制备方法。
背景技术:
癌症的治疗一直以来都面临着诸多挑战,近年来,人们致力于开发更有效的用于癌症治疗的药物递送系统,目的是在减少副作用的同时确保其出色的疗效。随着纳米技术的成熟,肿瘤靶向药物载体的优势逐渐显露,该药物载体对肿瘤具有高选择性,同时可以缓慢释放活性抗癌剂。肿瘤靶向药物载体是指通过包封或者吸附等手段,将药物小分子整合于纳米材料中,形成药物纳米颗粒,实现有效的药物递送。不同于小分子药物,纳米药物递送系统能够通过肿瘤疏松的血管孔隙进入肿瘤组织,在肿瘤内部实现高渗透和滞留效应,因此具有高载药率、被动靶向功能以及药物控制释放等特殊的优越性。
纳米技术是提高药效的有效手段,但传统纳米粒子进入体内后大部分迅速被网状内皮系统吞噬,使到达肿瘤细胞的纳米粒子数量减少,降低了药效,这极大限制了纳米粒子在医药领域中的研究和应用。叶酸受体在大部分恶性肿瘤细胞中高度表达,利用叶酸受体进行肿瘤靶向治疗是有效手段。在正常生理条件下,抗肿瘤药物在水溶液中的溶解度较低,无法直接通过体内注射的方式进行给药,叶酸与纳米技术结合是一种有效的提高生物利用度的方式。因此,寻找恰当的叶酸与药物偶联方式以提高生物利用度具有极为重要的应用价值。
肿瘤的多药耐药性(multidrugresistance,mdr)是指肿瘤细胞经化疗药物治疗后对不同抗肿瘤药物产生交叉耐药的性质。在恶性肿瘤的临床治疗中,多药耐药性会严重影响化疗药物的抗肿瘤效果,进而导致肿瘤的恶化和转移。引起肿瘤细胞多药耐药性的分子机制很多并且十分复杂,其中p-糖蛋白(p-gp)在肿瘤细胞表面过度表达是产生多药耐药性主要原因之一。普朗尼克是一种三嵌段共聚物(聚氧乙烯-聚氧丙烯-聚氧乙烯),由于其同时具备亲水性和疏水性,所以具有较好的生物偶联性,利用普朗尼克对mxenes进行表面修饰可增加其水溶性和生物相容性。而且,普朗尼克能够显著的抑制肿瘤细胞的p-gp活性。通过抑制p-糖蛋白的活性,从而降低了肿瘤细胞的多药耐药性,提高了肿瘤细胞对抗肿瘤药物的敏感性,进而杀伤肿瘤细胞。
技术实现要素:
本发明的目的是克服现有技术的上述不足而提供一种叶酸-普朗尼克-mxenes肿瘤靶向载药体系及其制备方法,以新型纳米材料mxenes作为药物缓释载体,利用载体本身生物相容性好、无细胞毒性、载药量高和自身缓慢降解而达到药物缓释等优点,对其表面改性从而与叶酸分子结合,制备出既能和肿瘤细胞特异性结合,同时能抑制肿瘤的多药耐药性的靶向给药的纳米药物给药体系。
本发明的技术方案是:叶酸-普朗尼克-mxenes肿瘤靶向载药体系,通过n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐活化叶酸;利用活化后叶酸的羧基与mxenes上的羟基发生酯化反应合成叶酸-mxenes,并使用透析法进行纯化;纯化的叶酸-mxenes的羧基在n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐存在的条件下与普朗尼克上含有的羟基发生酯化反应得到结合物,即形成叶酸-普朗尼克-mxenes肿瘤靶向载药体系。
本发明进一步的技术方案是:所述的普朗尼克为聚醚l65,聚醚f68,聚醚f188,聚醚f124或聚醚f127。
本发明提供的另一技术方案是:叶酸-普朗尼克-mxenes肿瘤靶向载药体系的制备方法,包括以下步骤,
(a)mxenes的制备:称量ti3alc2粉末置于聚四氟乙烯材质的容器中,加入浓度为9~12mol/l的hcl溶液形成反应溶液;称取lif在10min内缓慢加入反应溶液中,搅拌反应24~36h;反应完成后超声震荡反应溶液15~30min,以6000~10000r/pm离心反应物,弃去上清液,用去离子水反复清洗反应物,保留上清液,所得产物为多层ti3c2溶液,将所得的上层清液置于惰性气体中保存待用。
其中,所述ti3alc2与lif的质量比为1:1~2,lif与hcl物质的量之比为1:2.5~3.5。
(b)叶酸的活化:称取叶酸溶于二甲基亚砜,将其置于20℃~45℃下搅拌至完全溶解;然后依次加入n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐混合均匀,混合均匀后的溶液置于室温环境下避光反应6~12h,得到活化叶酸。
其中,所述叶酸、二甲基亚砜比例为每溶解0.1mol的叶酸使用20ml的二甲基亚砜,叶酸和n-羟基琥珀酰亚胺的质量比为2~2.5:1,n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:1.5~2.5。
(c)叶酸-mxenes体系的构建:称取mxenes加入到的去离子水中形成分散液,将分散液超声分散均匀;在20℃~45℃搅拌的条件下将分散液缓慢滴加至活化叶酸溶液中得到叶酸-mxenes溶液,置于惰性气体保护的条件下反应18h~36h,其中mxenes与去离子水的质量比为2~3:1。
(d)叶酸-mxenes体系的纯化:量取浓度为0.3~1g/ml的乙二胺四乙酸溶液,往溶液中添加nahco3将其ph值调至8,将透析袋置于此溶液中煮沸10min~30min;将步骤(c)制备的叶酸-mxenes溶液放入该透析袋中,用去离子水透析2~3d,每隔12h更换透析液;将透析过的叶酸-mxenes溶液置于离心管中,以4000r/min离心30min~60min,离心后的溶液去除上清液,然后加入去离子水振荡,弃去上清液,如此反复3~5次,除去残留的二甲基亚砜;然后加入丙酮振荡,弃去上清液,如此反复3~5次,除去未反应原料得到纯化的叶酸-mxenes,将纯化后的叶酸-mxenes移入表面皿,置于35~45℃条件下真空干燥待用。
(e)叶酸-普朗尼克-mxenes的制备及纯化:称取普朗尼克溶于二甲基亚砜溶液,在室温下搅拌至完全溶解得到普朗尼克溶液;然后称取n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐溶于水中形成混合液,将该混合液滴加至普朗尼克溶液中,滴加过程中不断搅拌,滴加完成后搅拌活化30min~60min得到活化后的普朗尼克溶液;将该活化后的普朗尼克溶液滴加至步骤d纯化后的叶酸-mxenes中,滴加过程中不断搅拌,滴加完成后搅拌12h~24h进行酯化反应;反应完成后将反应液置于透析袋中透析2~4d,透析介质为蒸馏水,每隔12h更换透析介质以除去未反应的n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐;将透析后的溶液用超声波分散均匀,并置于离心管中以4000~4500r/min离心10~20min,取上清液,即得纯化后的叶酸-普朗尼克-mxenes。
所述普朗尼克与二甲基亚砜比例为每溶解400mg的普朗尼克使用10ml的二甲基亚砜,所述n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:1.5~2.5,所述活化后的普朗尼克溶液与纯化的叶酸-mxenes的质量比为1:10~12。
本发明与现有技术相比具有如下特点:
1、本发明以mxenes为药物载体,叶酸为肿瘤靶向配体,普朗尼克为表面修饰物构建的叶酸-普朗尼克-mxenes肿瘤靶向载药体系,具有靶向性的同时又具有抗肿瘤多药耐药性。
2、本发明叶酸-普朗尼克-mxenes肿瘤靶向载药体系载药量大,缓释效果好,所用材料无毒无害且易得。
3、本发明合成方法简单易操作,可重复性强,适合工业化生产,在生物医药方面的应用开发提供了全新的研究思路。
以下结合附图和具体实施方式对本发明的详细结构作进一步描述。
附图说明
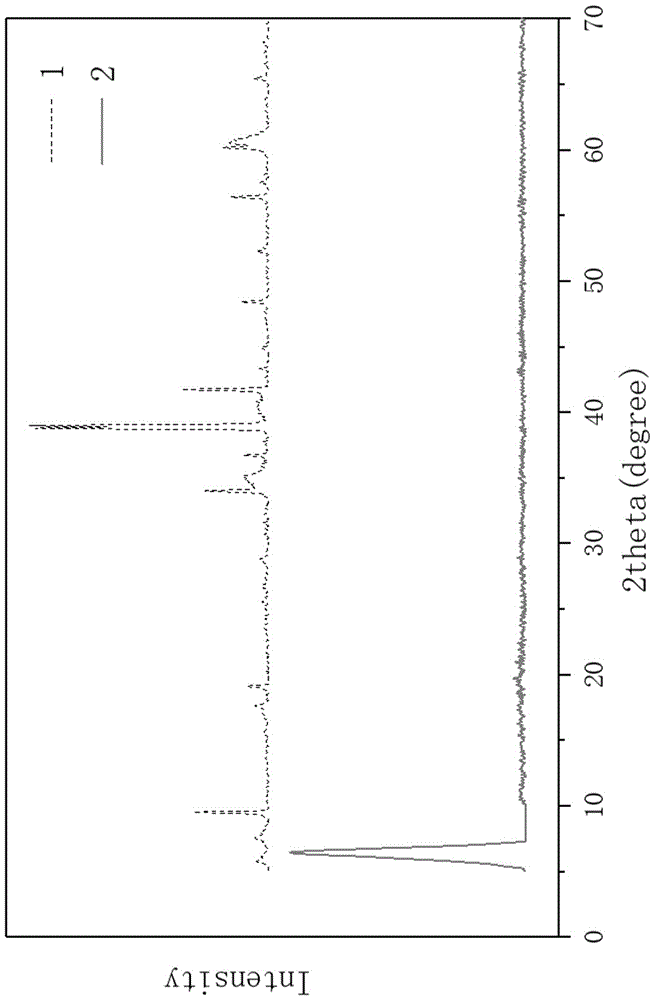
图1为mxenes制备时ti3alc2与ti3c2的xrd对比图;
图2中实线部分为mxenes氨基化后的fi-ir图、虚线部分为纯化后的叶酸-mxenes的fi-ir图;
图3为纯化后的普朗尼克-叶酸-mxenes的fi-ir图。
具体实施方式
实施例一,叶酸-普朗尼克-mxenes肿瘤靶向载药体系,通过n-羟基琥珀酰亚胺(nhs)和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc·hcl)活化叶酸;利用活化后叶酸的羧基与mxenes上的羟基发生酯化反应合成叶酸-mxenes,并使用透析法进行纯化;纯化的叶酸-mxenes的羧基在缩合剂存在的条件下与普朗尼克上含有的羟基发生酯化反应得到结合物,即形成叶酸-普朗尼克-mxenes肿瘤靶向载药体系。
其中,所述的普朗尼克包括聚醚l65,聚醚f68,聚醚f188,聚醚f124,聚醚f127。
实施例二,叶酸-普朗尼克-mxenes肿瘤靶向载药体系的制备方法,包括以下步骤:
(a)mxenes的制备:称量ti3alc2粉末置于聚四氟乙烯材质的容器中,加入浓度为10mol/l的hcl溶液形成反应溶液;称取lif在5min内缓慢加入反应溶液中,搅拌反应24h;反应完成后超声震荡反应溶液30min,以6000r/pm离心反应物,弃去上清液,用去离子水反复清洗反应物,保留上清液,所得产物为多层ti3c2溶液,将所得的上层清液置于惰性气体中保存待用。其中,所述ti3alc2与lif的质量比为1:1,lif与hcl物质的量之比为1:3.5。
(b)叶酸的活化:称取叶酸溶于二甲基亚砜,将其置于20℃下搅拌至完全溶解;然后依次加入n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐混合均匀,混合均匀后的溶液置于室温环境下避光反应6h,得到活化叶酸。其中,所述叶酸、二甲基亚砜比例为每溶解0.1mol的叶酸使用20ml的二甲基亚砜,叶酸和n-羟基琥珀酰亚胺的质量比为2:1,n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:1.5。
(c)叶酸-mxenes体系的构建:称取mxenes加入到的去离子水中形成分散液,将分散液超声分散均匀;在20℃搅拌的条件下将分散液缓慢滴加至活化叶酸溶液中得到叶酸-mxenes溶液,置于惰性气体保护的条件下反应18h,其中mxenes与去离子水的质量比为2:1。
(d)叶酸-mxenes体系的纯化:量取浓度为0.3g/ml的乙二胺四乙酸溶液,往溶液中添加nahco3将其ph值调至8,将透析袋置于此溶液中煮沸10min;将步骤(c)制备的叶酸-mxenes溶液放入该透析袋中,用去离子水透析2d,每隔12h更换透析液;将透析过的叶酸-mxenes溶液置于离心管中,以4000r/min离心30min,离心后的溶液去除上清液,然后加入去离子水振荡,弃去上清液,如此反复5次,除去残留的二甲基亚砜;然后加入丙酮振荡,弃去上清液,如此反复3次,除去未反应原料得到纯化的叶酸-mxenes,将纯化后的叶酸-mxenes移入表面皿,置于35℃条件下真空干燥待用。
(e)叶酸-普朗尼克-mxenes的制备及纯化:称取普朗尼克溶于二甲基亚砜溶液,在室温下搅拌至完全溶解得到普朗尼克溶液;然后称取n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐溶于水中形成混合液,将该混合液滴加至普朗尼克溶液中,滴加过程中不断搅拌,滴加完成后搅拌活化30min得到活化后的普朗尼克溶液;将该活化后的普朗尼克溶液滴加至步骤d纯化后的叶酸-mxenes中,滴加过程中不断搅拌,滴加完成后搅拌12h进行酯化反应;反应完成后将反应液置于透析袋中透析2d,透析介质为蒸馏水,每隔12h更换透析介质以除去未反应的n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐;将透析后的溶液用超声波分散均匀,并置于离心管中以4000r/min离心10min,取上清液,即得纯化后的叶酸-普朗尼克-mxenes。所述普朗尼克选用普朗尼克f68,普朗尼克f68与二甲基亚砜比例为每溶解400mg的普朗尼克f68使用10ml的二甲基亚砜,所述n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:1.5,所述活化后的普朗尼克溶液与纯化的叶酸-mxenes的质量比为1:10。
实施例三,叶酸-普朗尼克-mxenes肿瘤靶向载药体系的制备方法,包括以下步骤:
(a)mxenes的制备:称量ti3alc2粉末置于聚四氟乙烯材质的容器中,加入浓度为12mol/l的hcl溶液形成反应溶液;称取lif在5min内缓慢加入反应溶液中,搅拌反应30h;反应完成后超声震荡反应溶液15min,以8000r/pm离心反应物,弃去上清液,用去离子水反复清洗反应物,保留上清液,所得产物为多层ti3c2溶液,将所得的上层清液置于惰性气体中保存待用。其中,所述ti3alc2与lif的质量比为1:2,lif与hcl物质的量之比为1:2.5。
(b)叶酸的活化:称取叶酸溶于二甲基亚砜,将其置于40℃下搅拌至完全溶解;然后依次加入n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐混合均匀,混合均匀后的溶液置于室温环境下避光反应10h,得到活化叶酸。其中,所述叶酸、二甲基亚砜比例为每溶解0.1mol的叶酸使用20ml的二甲基亚砜,叶酸和n-羟基琥珀酰亚胺的质量比为2.2:1,n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:2。
(c)叶酸-mxenes体系的构建:称取mxenes加入到的去离子水中形成分散液,将分散液超声分散均匀;在25℃搅拌的条件下将分散液缓慢滴加至活化叶酸溶液中得到叶酸-mxenes溶液,置于惰性气体保护的条件下反应30h,其中mxenes与去离子水的质量比为2.5:1。
(d)叶酸-mxenes体系的纯化:量取浓度为1g/ml的乙二胺四乙酸溶液,往溶液中添加nahco3将其ph值调至8,将透析袋置于此溶液中煮沸20min;将步骤(c)制备的叶酸-mxenes溶液放入该透析袋中,用去离子水透析3d,每隔12h更换透析液;将透析过的叶酸-mxenes溶液置于离心管中,以4000r/min离心50min,离心后的溶液去除上清液,然后加入去离子水振荡,弃去上清液,如此反复3次,除去残留的二甲基亚砜;然后加入丙酮振荡,弃去上清液,如此反复5次,除去未反应原料得到纯化的叶酸-mxenes,将纯化后的叶酸-mxenes移入表面皿,置于40℃条件下真空干燥待用。
(e)叶酸-普朗尼克-mxenes的制备及纯化:称取普朗尼克溶于二甲基亚砜溶液,在室温下搅拌至完全溶解得到普朗尼克溶液;然后称取n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐溶于水中形成混合液,将该混合液滴加至普朗尼克溶液中,滴加过程中不断搅拌,滴加完成后搅拌活化50min得到活化后的普朗尼克溶液;将该活化后的普朗尼克溶液滴加至步骤d纯化后的叶酸-mxenes中,滴加过程中不断搅拌,滴加完成后搅拌24h进行酯化反应;反应完成后将反应液置于透析袋中透析2d,透析介质为蒸馏水,每隔12h更换透析介质以除去未反应的n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐;将透析后的溶液用超声波分散均匀,并置于离心管中以4000r/min离心20min,取上清液,即得纯化后的叶酸-普朗尼克-mxenes。所述所述普朗尼克选用普朗尼克f188,普朗尼克f188与二甲基亚砜比例为每溶解400mg的普朗尼克f188使用10ml的二甲基亚砜,所述n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:2,所述活化后的普朗尼克溶液与纯化的叶酸-mxenes的质量比为1:11。
实施例四,叶酸-普朗尼克-mxenes肿瘤靶向载药体系的制备方法,包括以下步骤:
(a)mxenes的制备:称量ti3alc2粉末置于聚四氟乙烯材质的容器中,加入浓度为9mol/l的hcl溶液形成反应溶液;称取lif在5min内缓慢加入反应溶液中,搅拌反应36h;反应完成后超声震荡反应溶液24min,以10000r/pm离心反应物,弃去上清液,用去离子水反复清洗反应物,保留上清液,所得产物为多层ti3c2溶液,将所得的上层清液置于惰性气体中保存待用。其中,所述ti3alc2与lif的质量比为1:1.5,lif与hcl物质的量之比为1:3。
(b)叶酸的活化:称取叶酸溶于二甲基亚砜,将其置于45℃下搅拌至完全溶解;然后依次加入n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐混合均匀,混合均匀后的溶液置于室温环境下避光反应12h,得到活化叶酸。其中,所述叶酸、二甲基亚砜比例为每溶解0.1mol的叶酸使用20ml的二甲基亚砜,叶酸和n-羟基琥珀酰亚胺的质量比为2.5:1,n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:2.5。
(c)叶酸-mxenes体系的构建:称取mxenes加入到的去离子水中形成分散液,将分散液超声分散均匀;在45℃搅拌的条件下将分散液缓慢滴加至活化叶酸溶液中得到叶酸-mxenes溶液,置于惰性气体保护的条件下反应36h,其中mxenes与去离子水的质量比为3:1。
(d)叶酸-mxenes体系的纯化:量取浓度为0.7g/ml的乙二胺四乙酸溶液,往溶液中添加nahco3将其ph值调至8,将透析袋置于此溶液中煮沸30min;将步骤(c)制备的叶酸-mxenes溶液放入该透析袋中,用去离子水透析3d,每隔12h更换透析液;将透析过的叶酸-mxenes溶液置于离心管中,以4000r/min离心60min,离心后的溶液去除上清液,然后加入去离子水振荡,弃去上清液,如此反复4次,除去残留的二甲基亚砜;然后加入丙酮振荡,弃去上清液,如此反复4次,除去未反应原料得到纯化的叶酸-mxenes,将纯化后的叶酸-mxenes移入表面皿,置于45℃条件下真空干燥待用。
(e)叶酸-普朗尼克-mxenes的制备及纯化:称取普朗尼克溶于二甲基亚砜溶液,在室温下搅拌至完全溶解得到普朗尼克溶液;然后称取n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐溶于水中形成混合液,将该混合液滴加至普朗尼克溶液中,滴加过程中不断搅拌,滴加完成后搅拌活化60min得到活化后的普朗尼克溶液;将该活化后的普朗尼克溶液滴加至步骤d纯化后的叶酸-mxenes中,滴加过程中不断搅拌,滴加完成后搅拌24h进行酯化反应;反应完成后将反应液置于透析袋中透析3d,透析介质为蒸馏水,每隔12h更换透析介质以除去未反应的n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐;将透析后的溶液用超声波分散均匀,并置于离心管中以4500r/min离心15min,取上清液,即得纯化后的叶酸-普朗尼克-mxenes。所述普朗尼克选用普朗尼克f127,普朗尼克f127与二甲基亚砜比例为每溶解400mg的普朗尼克f127使用10ml的二甲基亚砜,所述n-羟基琥珀酰亚胺和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的质量比为1:2.5,所述活化后的普朗尼克溶液与纯化的叶酸-mxenes的质量比为1:12。
图1示出了步骤(a)中ti3alc2与ti3c2的xrd对比图,从图1中可以看出ti3alc2在38处有峰,这个峰是al的特征峰,ti3c2在38处的峰已经完全消失,由此可知经过步骤(a)已经成功的制备出了mxenes材料。
图2实线部分示出了mxenes氨基化(mxenes-nh2)后的fi-ir图,从图2实线部分中能够看出mxenes-nh2材料在3400cm-1处有明显的峰值,此处是-oh的特征峰,由此可知合成出来的mxenes材料表面含有丰富的羟基;在1402cm-1处为-oh的弯曲振动;在2970cm-1为-nh3+的振动;在1616cm-1为-nh2的弯曲振动,由此可知mxenes已经氨基化成功。
图2虚线部分示出了步骤(d)纯化后的叶酸-mxenes(mxenes-nh2-fa)的fi-ir图,从图2虚线部分中能够看出在1511cm-1和1697cm-1处为二级酰胺-conh-的振动,固相中出现酰胺ⅰ和ⅱ带,说明mxenes-nh2与叶酸上的羧酸基团发生反应形成了酰胺键;在1604cm-1处的振动为叶酸中芳环的骨架振动,能够知道叶酸已经接枝到了mxenes材料中。
图3示出了步骤(e)纯化后的普朗尼克-叶酸-mxenes的fi-ir图,从图3中能够看出在1103cm-1的峰为c-o醚键的伸缩振动,在2930cm-1为-ch2-或-ch3伸缩振动的峰,在1515cm-1为二级酰胺-conh-的振动,在1605cm-1处的振动为叶酸中芳环的骨架振动,由此可知已经成功合成了普朗尼克-叶酸-mxenes。
- 还没有人留言评论。精彩留言会获得点赞!