葡萄糖响应的多孔二氧化硅复合可注射凝胶及其制备方法
本发明属于高分子材料技术领域的一种凝胶及其制备方法,具体涉及一种葡萄糖响应的多孔二氧化硅复合可注射凝胶及其制备方法。
背景技术:
糖尿病是一种代谢类的疾病,表现为胰岛素分泌缺陷或胰岛素受体缺陷或二者兼有,现如今并没有根治糖尿病的方法。糖尿病患者的血糖浓度显著高于正常水平,如果长时间血糖过高可能会导致一系列的并发症,如心血管疾病、肾病、神经损伤等。因此,现在对于i型糖尿病的主要治疗途径为定期皮下注射胰岛素,然而,这样的方法往往会引起疼痛从而导致患者的不服从。虽然现如今一些其他的胰岛素递药方式被开发出来,如口服、鼻腔吸收、皮肤吸收、眼部给药等,但仍然解决不了血糖水平控制不连续的问题,除此之外,这种胰岛素递药方式容易出现剂量控制不当从而导致低血糖的发生,从而引起意识不清、脑损伤等健康问题,甚至休克或者死亡。
因此,为了改善对于糖尿病患者的血糖控制,葡萄糖响应的胰岛素递送体系被提出,该体系本质上为胰岛素载体,致力于实现随着葡萄糖浓度的变化自适应的调节自身胰岛素的释放量,从而达到一次给药长时间稳定血糖的目的。基于硼酸酯键的可注射的凝胶由于能够被注射到生物体内表现出了巨大的应用潜力。由于苯硼酸能够与二醇结构可逆动态结合形成硼酸酯键,因此,利用硼酸酯键交联能够很方便地制备可注射凝胶,同时,由于葡萄糖含有二醇结构,葡萄糖能够破坏凝胶中的硼酸酯键交联点从而导致凝胶降解从而导致胰岛素释放。
技术实现要素:
本发明提供了一种葡萄糖响应的多孔二氧化硅复合可注射凝胶。葡萄糖响应的多孔二氧化硅复合可注射凝胶在中性ph环境下的不同葡萄糖浓度溶液中具有不同的胰岛素释放速率,凝胶具有自愈和性能,硬度可调,制备简单,原料易得。
本发明采用氨基化的多孔二氧化硅作为胰岛素载体,具有良好的生物相容性和生物降解性,具有可调的载药量,通过将胰岛素溶液与氨基化的多孔二氧化硅混合使胰岛素被负载到多孔二氧化硅上,将负载有胰岛素的多孔二氧化硅、苯硼酸修饰的海藻酸、瓜尔豆胶三者混合制得葡萄糖响应的多孔二氧化硅复合可注射凝胶。
本发明由以下技术方案实现:
一、一种葡萄糖响应的多孔二氧化硅复合可注射凝胶
所述的多孔二氧化硅复合可注射凝胶主要由氨基化的多孔二氧化硅和两种聚合物混合制备得到。
所述的两种聚合物,其中一种聚合物含有苯硼酸基团,另一种聚合物含有二羟基。
所述的氨基化的多孔二氧化硅在ph=7.4下zeta电位大于20mv。
所述的氨基化的多孔二氧化硅的粒径为10-1000nm。
二、一种葡萄糖响应的多孔二氧化硅复合可注射凝胶的制备方法,包括以下步骤:
1)向十六烷基三甲基氯化铵和三乙醇胺的水溶液中加入正硅酸乙酯的甲苯溶液得到反应体系a,以150rpm的搅拌速率进行搅拌,使得反应体系a呈现水相和油相两相分离状态,然后继续于60℃反应12h后,将水相依次经离心、洗涤、冷冻干燥和煅烧后得到多孔二氧化硅固体;
2)将多孔二氧化硅固体分散于无水甲苯中,超声分散后在110℃回流1h,然后加入3-氨丙基三乙氧基硅烷(aptes)得到悬浊液b,将悬浊液b依次经离心、洗涤和冷冻干燥得到氨基化的多孔二氧化硅固体;
3)向经1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐和n-羟基琥珀酰亚胺活化的海藻酸钠水溶液中加入2-氨基苯硼酸的氢氧化钠溶液得到反应体系c,调整反应体系c的ph至8搅拌4h,反应结束后再将盐酸溶液加入反应体系c中得到悬浊液d,将悬浊液d离心后得到白色固体,然后将白色固体洗涤后溶于氢氧化钠溶液中,并调整ph至7-8之间,然后再加入盐酸溶液重复沉淀、离心和洗涤步骤后得到固体e,将固体e冷冻干燥得到2-氨基苯硼酸修饰的海藻酸钠;
4)将胰岛素负载到氨基化的多孔二氧化硅固体中,得到负载胰岛素的氨基化的多孔二氧化硅;
5)将负载胰岛素的氨基化的多孔二氧化硅与瓜尔豆胶水溶液中混合后,再加入2-氨基苯硼酸修饰的海藻酸钠搅拌后得到葡萄糖响应的多孔二氧化硅复合可注射凝胶。
所述步骤4)中,氨基化的多孔二氧化硅和胰岛素的质量比为(4:1)-(1:1)。
所述步骤5)中,2-氨基苯硼酸修饰的海藻酸钠和瓜尔豆胶的质量比为(1:4)-(3:2)。
所述步骤4)中,胰岛素的负载时间为0.5-2h,负载环境为ph中性。
胰岛素负载的多孔二氧化硅在多孔二氧化硅复合可注射凝胶中的含量小于32mg/cm3。
本发明材料的胰岛素负载效率较高,这归结于多孔二氧化硅在中性ph下正的zeta电位以及其大的比表面积。
本发明的有益效果:
本发明制备的多孔二氧化硅复合可注射凝胶可以通过灵活调节氨基化多孔二氧化硅的加入量从而在一定范围内调节凝胶的模量,进而调节凝聚的释药性能和可注射性能等;
本发明的多孔二氧化硅复合可注射凝胶具有自愈合性能,凝胶网络被破坏后能够在短时间内恢复原来的性能;
本发明的多孔二氧化硅复合可注射凝胶具有可注射性能,能够顺利通过直径0.6mm的针头;
本发明的多孔二氧化硅复合可注射凝胶具有良好的胰岛素缓释效果,在生理ph环境下12h内能持续不断释放出胰岛素;
本发明材料具有葡萄糖响应性能,在生理ph的环境下,在0g/l与1g/l的葡萄糖溶液中胰岛素的累计释放量相差不大,在4g/l的葡萄糖溶液中胰岛素的累计释放量增大。
总述,本发明的多孔二氧化硅复合可注射凝胶具有自愈合性能和可注射性能,具有良好的胰岛素缓释效果,且可以通过灵活调节氨基化多孔二氧化硅的加入量在一定范围内调节凝胶的模量,进而调节凝聚的释药性能和可注射性能等。
附图说明
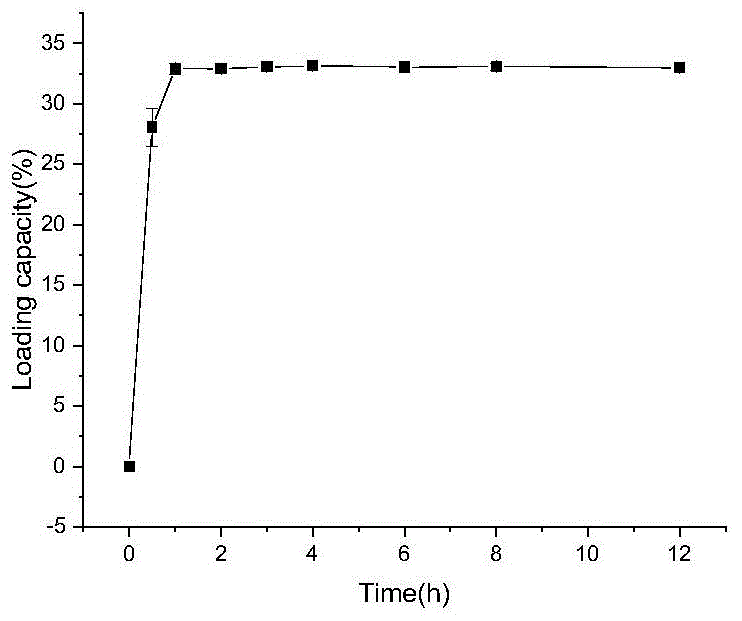
图1为本发明实施例1中dmsn-nh2负载胰岛素过程中胰岛素负载率随时间的变化曲线图;
图2为本发明实施例1中负载有胰岛素的dmsn-nh2的胰岛素累积释放曲线图;
图3为本发明实施例1在不同糖浓度下的胰岛素累积释放曲线图;
图4为本发明实施例2的流变性能曲线图;
图5为本发明实施例2的愈合过程示意图;
图6为本发明实施例3的注射过程示意图。
具体实施方式
下面结合实施例对本发明做更详尽的说明,但本发明不局限于此,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围之内。本说明书中未作详细描述的内容属于本领域专业技术人员公知的现有技术。
实施例1:
1)称取8.0112g(25mmol)的十六烷基三甲基氯化铵(ctac)和0.1856g(1.2mmol)三乙醇胺(teoa)置于24ml去离子水中,搅拌直至完全溶解后,再加入36ml去离子水并在60℃保持低速搅拌(150rpm)1h,随后配置体积分数为10%(8.9mmol)的正硅酸乙酯(teos)的甲苯溶液并缓慢将其加入水体系,使得反应体系呈现两相分相的状态,两相为水相和油相,继续在60℃下保持低速搅拌12h后,取水相乳白色液体离心(15000rpm,1h),将得到的白色固体用水洗涤三遍后冷冻干燥,并用马弗炉在550℃下焙烧5h得到多孔二氧化硅(dmsn-t)。
2)称取75.1mgdmsn-t于40ml无水甲苯中,超声分散10min后在110℃回流1h,加入78μl(44.4mmol)3-氨丙基三乙氧基硅烷(aptes)后,继续在110℃回流12h,然后离心以离心速率15000rpm离心10min后收集固体产物,并用乙醇和水洗涤三遍固体产物,随后冷冻干燥24h得到氨基化的多孔二氧化硅(dmsn-nh2)。
3)称取0.9997g海藻酸钠(50.5mmolunit)溶于水中并定质量至50g左右得到2%的海藻酸钠水溶液,然后称取1.9353g1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc·hcl)(101mmol)和2.2307mgn-羟基琥珀酰亚胺nhs(202mmol)溶于海藻酸钠水溶液中,并于常温下搅拌30min得到活化的海藻酸钠水溶液待用;随后称取690.7mg2-氨基苯硼酸(2-apba)(50.5mmol)溶于1.6ml1mol/l的naoh溶液中,并用水稀释至5ml,将该2-apba的naoh溶液滴加到活化的海藻酸钠水溶液中,并调整ph至8左右,继续搅拌4h后,再将25ml高速搅拌的0.1mol/l的盐酸溶液加入到活化的海藻酸钠水溶液中得到悬浊液,将悬浊液离心后得到白色固体,将该固体用水洗涤三遍后用naoh溶液溶解并调整ph至7-8左右,然后再加入25ml高速搅拌的0.1mol/l的盐酸溶液并重复上述沉淀、离心和洗涤步骤后得到固体,将所得固体冷冻干燥后得到的淡褐色粉末即为2-氨基苯硼酸修饰的海藻酸(sa-apba)。
4)称取一定量胰岛素溶于0.01mol/l的盐酸中并定容得到4mg/ml的胰岛素溶液,并用1mol/l的naoh溶液调ph至7左右,再用标准pbs缓冲液稀释得到2mg/ml的胰岛素溶液待用。称取1.0mgdmsn-nh2于离心管中,加入0.5ml2mg/ml的胰岛素溶液并用pbs缓冲液稀释至2ml,随后将分散液超声5min后置于常温下搅拌2h,再将分散液离心并取样上清液用于吸光度测试,将剩余固体冷冻干燥后得到白色粉末即为负载有胰岛素的dmsn-nh2。
5)称取8.0mg负载有胰岛素的dmsn-nh2置于玻璃瓶中,加入0.6ml2%的瓜尔豆胶水溶液,常温下搅拌1h使得负载有胰岛素的dmsn-nh2与瓜尔豆胶混合均匀,随后在搅拌下缓慢滴入0.4ml2%的sa-apba溶液,并继续搅拌1h后得到的凝胶块即为葡萄糖响应的多孔二氧化硅复合可注射凝胶。
如图1所示为实施例1中dmsn-nh2负载胰岛素的胰岛素负载率随时间的变化关系,可以观察到在0.5h是胰岛素负载率已经达到较高水平,在1h时胰岛素已经几乎达到负载最高值。
如图2所示为实施例1中负载有胰岛素的dmsn-nh2在ph=7.4,温度为37℃下的胰岛素累积释放曲线,可以观察到在2h时胰岛素已经几乎达到平衡释放量。
如图3所示为实施例1在ph=7.4,温度为37℃,不同糖浓度下(0g/l,1g/l和4g/l)的胰岛素累积释放曲线。其中,体系表现出了良好的胰岛素缓释行为,同时,可以观察到葡萄糖浓度为4g/l时的胰岛素释放曲线高于其他两组曲线,说明了材料存在一定的葡萄糖响应释药行为。
实施例2:
实施例2的步骤1)-步骤4)与实施例1相同,步骤5)如下:
5)称取4.0mg负载有胰岛素的dmsn-nh2置于玻璃瓶中,加入0.6ml2%的瓜尔豆胶水溶液,常温下搅拌1h以使得负载有胰岛素的dmsn-nh2与瓜尔豆胶混合均匀。随后在搅拌下缓慢滴入0.4ml2%的sa-apba溶液,并继续搅拌1h后得到的凝胶块即为葡萄糖响应的多孔二氧化硅复合可注射凝胶。
将凝胶块置于旋转流变仪上进行时间扫描,频率固定为1hz,应变在1%与700%之间反复,每个应变持续1min,测试进行三个循环。
如图4所示为实施例2的流变性能。应变调整至700%是为了模拟凝胶网络被破坏的过程,可以观察到凝胶在三个循环内表现出了相似的储能模量和耗散模量,说明了该凝胶良好的自愈合性能。
如图5所示为实施例2愈合现象的图,现将制备好的一个多孔二氧化硅复合可注射凝胶分为两个,即图中的多孔二氧化硅复合可注射凝胶a和多孔二氧化硅复合可注射凝胶b,经过一段时间可以观察到多孔二氧化硅复合可注射凝胶a和多孔二氧化硅复合可注射凝胶b愈合到一起,说明本发明制备的多孔二氧化硅复合可注射凝胶具有良好的自愈合性能。
实施例3:
实施例3的步骤1)-步骤4)与实施例1相同,步骤5)如下:
5)称取16.0mg负载有胰岛素的dmsn-nh2置于玻璃瓶中,加入0.6ml2%的瓜尔豆胶水溶液,常温下搅拌1h以使得负载有胰岛素的dmsn-nh2与瓜尔豆胶混合均匀。随后在搅拌下缓慢滴入0.4ml2%的sa-apba溶液,并继续搅拌1h后得到的凝胶块即为dmsn-nh2复合凝胶(葡萄糖响应的多孔二氧化硅复合可注射凝胶)。
将dmsn-nh2复合凝胶用罗丹明b染色后置于2ml注射器内,推动注射器使凝胶从0.6mm针头被挤出到水中。
如图6为凝胶从注射器中被推出的过程图,可以观察到凝胶顺利从针口被推出,且被推出后仍然保留了其凝胶的状态。
- 还没有人留言评论。精彩留言会获得点赞!