人血白蛋白在制备放射性碘标金丝桃素药物制剂中的应用
本发明属于药物制剂领域,特别是涉及人血白蛋白在制备放射性碘标金丝桃素药物制剂中的应用。
背景技术:
金丝桃素(hypericin,简写为hyp)是一种来自贯叶连翘的提取物,有抗炎、抗病毒、抗aids的功效,甚至有报导说其还能抗癌。近二三十年前,hyp优越的“坏死靶向性”被比利时华人科学家yichengni教授发现,然后也的确开辟了其在恶性实体瘤诊疗领域的独到应用,但并非是直接治疗肿瘤,而是与其他药物联合:在其他药物(例如康普瑞汀磷酸二钠)消灭了大部分癌细胞并造成大量的肿瘤坏死灶后,hyp在自身标记上放射性131i(即形成131i-hyp)、依据其特有的坏死靶向性,将131i携带至坏死肿瘤灶上、利用131i的高能β射线杀灭近距离的、残余的活瘤细胞,而对更远距离的正常组织细胞没有危害,充分做到的癌症治疗的靶向性。同时131i-hyp释放低能量γ射线,可用于核医学影像肿瘤定位诊断和疗效评价。
hyp难溶与水,因此不容易制备成溶液注射、而是常溶于油脂制备成口服制剂。然而如想注入机体的是131i-hyp而非hyp,则必不能经口服(肠道的碱性环境会引起脱标,131i会与hyp分离,导致131i不会在聚集在坏死肿瘤部位、失去靶向治疗特性),因此静脉注射又唯一的、最好的选择。临床前研究中,一开始是采用万能溶剂dmso对hyp进行溶解、标记131i、然后稀释、制备成溶液后经静脉注射的。然而,dmso具有极易渗透皮肤的特殊性质,可引起使用者出现恶心、呕吐、皮疹等不良反应;并且,dmso存在一定毒性作用,与蛋白质疏水基团发生作用,导致蛋白质变性,具有血管毒性、溶血和肝肾毒性等。因此,dmso并不在药典许可的注射用药之列,不是一个最为理想的金丝桃素类的溶解剂。中国专利cn201310111593.4采用胆酸盐增溶放射性碘标金丝桃类药物,但是胆酸盐作为辅料药物进行静脉注射暂时没有获得相关辅料批件。中国专利cn107308455b采用环糊精作为制备131i-hyp的溶剂、且羟丙基-β-环糊精是药典批准的静脉注射用辅料,但所需环糊精剂量较大、毕竟是非体内成分的外来物,使用时也需慎重;在一些非学术期刊的讨论版上,也有人对羟丙基-β-环糊精用于静脉注射的安全性持否定态度。因此还有必要进一步改进hyp的溶剂。
过去我们仅通过研究经验了解到:131i-hyp静脉入血后应该是与血浆蛋白结合运载。是以当131i-hyp注射过快时、会因浓度过大、不溶于血液而发生自聚现象,沉积在肝脾肺等单核巨噬系统,因此过去给药(131i-hyp)时总是尽可能缓慢注射,增加其与血浆蛋白结合的几率。最近,我们经研究确定,无论哪种溶剂、其(hyp/131i-hyp)静脉入血后都是结合在白蛋白上的,因此提出设想:为何又一定要通过缓慢注射,而不能让其在体外就与白蛋白充分结合呢?
用白蛋白替代dmso或者羟丙基-β-环糊精、助溶hyp,并在体外进行131i标记、产生131i-hyp,这一操作尚无先例。推测原因之一,可能是有可查文献提出“白蛋白可被碘标记(如被125i标记)”,进而似乎可以推论:在hyp/白蛋白溶液中,加入131i进行标记,会同时产生131i-hyp与131i-白蛋白,而后者不光是杂质成分、也是对肿瘤治疗不利的。但其实,二者进行放射性碘标记的标记条件是不同的,可以利用化学反应条件的差异只标记hyp、而白蛋白不被标记。
技术实现要素:
本发明解决现有技术中存在的上述技术问题,提出人血白蛋白在制备放射性碘标hyp药物制剂中的应用、运用人血白蛋白制备放射性碘标hyp药物制剂的方法以及放射性碘标hyp制剂。
人血白蛋白在制备放射性碘标hyp药物制剂中的应用,作为hyp、碘标记的hyp的溶剂,用于人体血管(如静脉、动脉)内注射。
优选地,所述人血白蛋白为浓度在5%~25%(5~25g/100ml)的人血白蛋白。
一种放射性碘标hyp药物制剂,包括人血白蛋白、hyp和131i标记的hyp;人血白蛋白作为溶剂,增加hyp溶解度,可用于人体静脉注射、人体动脉注射。
一种制备放射性碘标hyp药物制剂的方法,包括以下步骤:
1)将hyp与5%~25%(5~25g/100ml)的人血白蛋白溶液混合,每毫升所述人血白蛋白溶液加入0.01~1mghyp,在4℃~37℃温度下不断超声、混匀,8小时后,高速离心、取上清、0.22μm微孔滤膜过滤,得到人血白蛋白-hyp溶液;
2)所购核素-na131i溶液,比活度为20~1000mci/ml,用pbs缓冲液调节至中性。
3)人血白蛋白-hyp溶液与步骤2)制备得到的溶液在催化剂存在下,34℃~40℃水浴不断混匀,直至标记率到达90%以上。所述人血白蛋白-hyp溶液和na131i溶液的量均按制备标记物所需的量加入。
优选地,所述催化剂为iodogen或氯胺t,剂量为3~10μg/mcina131i。
相对于现有技术,本发明的优点如下,
本发明首次将人血白蛋白应用于制备“放射性碘标hyp”制剂。由于人血白蛋白是人体血液的固有成分、无毒无害,不存在像辅料那样作为体外添加的成分需要在药典收录的范围内、或者需药监局批准的情况;同时,作为大多数药物的血液内载体,白蛋白可大大提到hyp水溶性;而且在本专利标记条件下、增溶了的hyp可被碘高效标记、而人血白蛋白本身尚未被标记,标记后产物无需在进行纯化、也不会改变原有的碘标hyp的靶向性和体内代谢模式。因此,人血白蛋白可作为dmso、环糊精的替代物,应用于放射性碘标hyp制剂;
本发明的放射性碘标hyp制剂,与dmso或羟丙基-β-环糊精作为溶剂的131i-hyp注射液相比,更加可被医学界接受,且可以保证hyp的标记效率,标记物的坏死靶向性基本未改变,在正常肝、脾、肾及血液内的分布更低,可用于肿瘤治疗;
本发明制备碘标hyp制剂的方法,工艺简单,成本低廉,制备效率高,适用于产业化操作。
附图说明
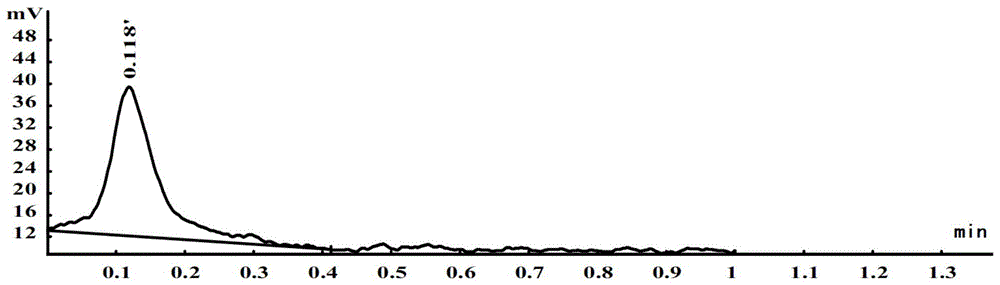
图1为人血白蛋白-hyp溶液加入调节ph值的131i标记后的放射性薄层扫描仪检测结果;
图2为人血白蛋白溶液加入调节ph值的131i标记后,与人血白蛋白-hyp溶液在相同的条件下进行标记的放射性薄层扫描仪检测结果;
图3为hyp在人血白蛋白溶液(左)、dmso溶液(中)、羟丙基-β-环糊精溶液(右)进行131i标记后,131i-hyp溶液注射入坏死动物模型体内,由spect-ct检测所得的放射性在体分布;
图4为hyp在人血白蛋白溶液(左)、dmso溶液(中)、羟丙基-β-环糊精溶液进行131i标记后(右)、131i-hyp溶液注射入坏死动物模型体内,处死剖检获得坏死肝叶(上行);采用磷屏自显影分析所得的、放射性分布的体外分析结果(下行);说明放射性仅分布在肝叶的坏死组织内。
具体实施方式
说明,以下ci为以活度来描述放射源大小的单位,居里;
131i-hyp为131i标记的hyp。
实施例1:
以人血白蛋白为溶剂的131i-hyp溶液的制备:称取1mghyp,配比加入1ml的20%(20g/100ml)人血白蛋白溶液,在4℃~37℃下(可适当加热不超过37℃)、超声、不断混匀、避光过夜8小时后,10000g离心15min,取上清、经0.22μm微孔滤膜过滤,得到“人血白蛋白-hyp”溶液。将催化剂iodogen事先涂管于1.5mlep管(最佳为配比为3~10μgiodogen:1mcina131i),加入“人血白蛋白-hyp”溶液约1ml,再加入约10μl的na131i溶液(比活度在20~1000mci/ml,同位素从生产到使用不超过1个半衰期,加入前用pbs缓冲液调节至中性),34℃~40℃水浴,不断混匀并用薄层层析法(thin-layerchromatography,tlc)、配合放射性薄层扫描仪检测131i标记率,直至标记率到达98%以上(图1),得“131i-hyp/人血白蛋白”溶液。空白对照组为相应的不含hyp的人血白蛋白溶液,实验表明,人血白蛋白溶液本身不能被131i标记(图2)。将“131i-hyp/人血白蛋白”溶液用10~50ml的人血白蛋白溶液进行稀释,用于下一步注射。
实施例2:
制备大鼠部分肝坏死再灌注模型:雄性sd大鼠(250-300g)术前24小时开始服用0.5%ki溶液代替饮水,以封闭甲状腺对游离碘的摄取。手术当天,麻醉开腹,进行右肝叶坏死再灌注手术,24小时内磁共振扫描,检测肝脏局部是否坏死。
将部分肝坏死大鼠模型分为三组,分别注射“131i-hyp/人血白蛋白”溶液、传统制剂“131i-hyp/dmso”溶液、“131i-hyp/羟丙基-β-环糊精”溶液(三种溶液标记条件相同)。注射后48h,检测131i的放射性分布。首先将大鼠麻醉,进行在体核素扫描(spect-ct)(见图3),结果显示:1)各组的131i放射性聚集于进行过坏死造模的肝叶部位,以白蛋白为溶剂并未影响放射性的坏死靶向分布(即未影响131i-hyp的分布);2)另一个放射性聚集的部位在肠道(因多余的未结合坏死部位的131i-hyp经肝脏代谢、由胆汁排入肠道,并与食糜混合后、逐渐随粪便排出体外);3)其他部位几乎无放射性分布,符合131i-hyp的生理分布,且不存在131i-白蛋白分布的可能性(图3左)。然后过量麻醉处死大鼠,采集手术中的坏死肝叶,进行冰冻切片,通过磷屏自显影检测放射性是否仅附着于肝叶中的坏死组织部位(图4),结果显示:三个处理组的肝叶的坏死部位经磷屏自显影显示有放射性分布,肝叶尚未坏死的部位无放射性分布,符合131i-hyp坏死靶向分布特征。
上述实施例仅为本发明的优选技术方案,而不应视为对于本发明的限制,本发明的保护范围应以权利要求记载的技术方案,包括权利要求记载的技术方案中技术特征的等同替换方案为保护范围,即在此范围内的等同替换改进,也在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!