多酸化合物、其制备方法和医药用途与流程
本发明属于医药领域,特别是抗病毒药物领域。具体而言,本发明涉及多酸化合物、其制备方法和医药用途,特别是预防和/或治疗艾滋病的用途。
背景技术:
艾滋病(acquiredimmunedeficiencysyndrome,aids)是人类免疫缺馅病毒(humanimmunodeficiencyvirus,hiv)引起的致死性传染病。1981年在法国发现首位患者,后在美国被首次确诊为艾滋病以来,已在全球广泛流行,但是尚无有效的疫苗和能根治的药物。针对hiv复制周期的不同阶段,治疗hiv感染的靶点包括:1、针对hiv毒粒:可溶性cd4、中和抗体;2、针对病毒进入:进入/融合抑制剂,其靶点包括宿主细胞膜受体(cd4分子、辅助受体ccr5和cxcr4)和病毒外膜蛋白(gp120和gp41);3、整合前的早期阶段:逆转录酶抑制剂;4、整合过程:整合酶抑制剂;5、整合后:蛋白酶抑制剂;6、细胞成熟、出芽:成熟抑制剂,作用于gag蛋白,阻止hiv的成熟和释放。目前fda批准用于治疗艾滋病的药物约有30多种,主要是针对gp41、ccr5、逆转录酶、整合酶和蛋白酶等靶点。上世纪九十年代中期开始,人们开始应用harrt疗法(高效抗逆转录病毒疗法)治疗艾滋病,该疗法是以两种逆转录酶抑制剂和一种蛋白酶抑制剂,合并或轮流使用,但这些药物都存在着易产生抗药性、有较严重的长期毒性、价格昂贵等缺点。针对hiv-1病毒极易耐药的特性,更多的关注病原体本身与机体细胞因子之间的关系,寻找新的靶点势在必行。广大科研工作者们正致力于寻找针对hiv复制周期中不同靶点的有效的抗hiv-1药物,以期能够联合发挥作用,减少病毒的耐药、降低毒性、节约成本,实现有效的治疗作用。
多酸化合物又称多金属氧酸盐(polyoxometalates),是一类金属-氧簇合物,是由d0组态的过渡金属离子(如moⅵ,wⅵ,vⅵ,ndⅴ,taⅴ等)与氧高度聚合形成的具有空间网络结构的无机高分子聚合物。上世纪80年代中期杂多化合物(nh4)17na[nasb9w21086]·14h2o被发现具有抑制艾滋病病毒逆转录酶的作用,并很快作为抗艾滋病候选药物先后在法国和美国进行临床研究。但后期由于其对骨髓细胞的抑制作用,在给药剂量及给药时间上均受到限制。
本发明提供的kxhypti2w10o40·mh2o的式(i)化合物毒性低,抗hiv活性强,且未见有关其抑制hiv-1复制,预防和/或治疗艾滋病的相关报道。
技术实现要素:
在第一方面,本发明提供一种式(i)化合物:
kxhypti2w10o40·mh2o(i)
其中:
m=0~20的整数,优选0~15的整数,
x=1~5的整数,
y=1~6的整数,并且
x+y=7。
在本发明的一个优选的实施方案中,式(i)化合物选自:k6hpti2w10o40·5h2o、k4h3pti2w10o40·8h2o和k2h5pti2w10o40·6h2o。
在第二方面,本发明提供一种制备上述式(i)化合物的方法,其包括以下步骤:将二水钨酸钠、磷酸二氢钠溶解在蒸馏水中,滴加的四氯化钛,回流反应,冷却过滤,调节滤液ph值,加入过量的氯化钾得白色固体的式(i)化合物,任选地热水重结晶。
在本发明的一个优选的实施方案中,所述制备方法包括以下步骤:将二水钨酸钠91mmol、磷酸二氢钠43mmol溶解在100ml的蒸馏水中,滴加16mmol的四氯化钛,回流反应30min,冷却过滤,调节滤液ph值,加入适量的氯化钾得白色固体,热水重结晶。
在本发明的另一个优选的实施方案中,通过加入稀盐酸调节滤液ph值至1~8,优选3~7。根据调节不同ph值得到分子中含不同数量k和h的化合物。
第三方面,本发明提供一种预防和/或治疗艾滋病的药物组合物,其包含治疗有效量的上述式(i)化合物以及药学上可接受的赋形剂或载体。本文使用术语“赋形剂”、“载体”来描述任何非本发明化合物的成分。赋形剂、载体的选择主要取决于例如特定的施用模式,赋形剂、载体对溶解度和稳定性的影响和剂型的性质等因素。
有利地,所述药物组合物进一步包含另一种治疗艾滋病的药物,优选齐多夫定。
第四方面,本发明涉及上述式(i)化合物或包含其的药物组合物在制备用于预防和/或治疗艾滋病的药物中的用途。
第五方面,本发明涉及上述式(i)化合物,其用作药物。
第六方面,本发明涉及上述式(i)化合物,其用于预防和/或治疗艾滋病。
第七方面,本发明涉及上述式(i)化合物,其用于预防和/或治疗艾滋病,并以每日的0.01mg/kg至50mg/kg体重的量向需要其的受试者施用。
第八方面,本发明涉及上述式(i)化合物,其与另一种治疗艾滋病的药物联合用于预防和/或治疗艾滋病,优选地,所述另一种治疗艾滋病的药物为齐多夫定。
第九方面,本发明涉及一种用于预防和/或治疗艾滋病的方法,其包括向需要其的受试者施用治疗有效量的上述式(i)化合物。
在本发明的一个优选的实施方案中,所述化合物以每日的0.01mg/kg至50mg/kg体重的量向需要其的受试者施用。
第十方面,本发明涉及一种用于预防和/或治疗艾滋病的方法,其包括向需要其的受试者施用治疗有效量的上述式(i)化合物和另一种治疗艾滋病的药物,优选地,所述另一种治疗艾滋病的药物为齐多夫定。
在本发明的另一个优选的实施方案中,所述化合物或药物组合物以片剂、胶囊、栓剂、粉末剂、颗粒剂、混悬剂、喷雾剂、膏剂或丸剂形式施用。
本发明人进行了一系列实验,结果显示:
所述式(i)化合物通过作用于病毒进入细胞阶段发挥抑制病毒复制的作用;
所述式(i)化合物通过封闭cd4受体发挥抑制病毒复制的作用;和/或
所述式(i)化合物通过保护a3g免受vif的降解从而发挥抑制病毒复制的作用。
本发明的化合物可以作为晶体或无定型产品施用。它们也可以与一种或多种药学上可接受的赋形剂或载体联合作为药物组合物施用。
根据本发明的药物组合物可以与一种或多种其它活性剂如其他作用靶点的抗艾滋病药联合应用,与抗癌药一起施用,或者与放射治疗或外科治疗联合,或者与放射治疗和外科治疗组合。施用可以是与其它治疗同时的、分开的或交错的。
根据本发明的药物组合物被制备以施用于人类。可以通过经口、舌下、经皮、局部或直肠或鼻腔内途径施用根据本发明的药物组合物。在这种情况下,可以单一剂型(与常规药学载体混合)向人类施用活性成分。合适的单一剂型包括口服形式如片剂、胶囊、粉末剂、颗粒剂和口服溶液或混悬剂、舌下和口腔剂型、皮下或经皮、外部、肌肉内、鼻腔内或眼内剂型、直肠剂型。
当制备片剂形式的固体组合物时,将主要活性成分与药学载体混合,例如明胶、淀粉、乳糖、硬脂酸镁、滑石粉、阿拉伯胶、二氧化硅或等价物。可以用蔗糖或其它合适的材料将片剂包衣,或可以处理片剂以使其具有持续的或延缓的活性并且不断地释放预定量的活性成分。
通过将活性成分与稀释剂混合并将获得的混合物倒入软或硬胶囊中获得胶囊制剂。
糖浆或酏剂形式的制剂可以含有活性成分连同甜味剂、防腐剂以及提供香味的试剂和合适的着色剂。
水可分散性粉末剂或颗粒剂可以含有与分散剂或湿润剂、或混悬剂、以及香味物质或甜味剂混合的活性成分。
对于直肠施用,使用栓剂,其用在直肠温度熔化的粘合剂,例如可可油或聚乙二醇制得。
还可以将活性成分任选与一种或多种添加载体一起制成微囊形式。
有利地,根据本发明的药物组合物旨在经口或直肠施用。
根据本发明的药物组合物可以进一步含有起到另外的或任选的协同效应的活性成分。
可以调整式(i)化合物在根据本发明的组合物中的剂量以获得一定量的物质,其能够有效地获得施用方法下特定组合物所寻求的治疗应答。通常预期每日的有效量为0.01mg/kg至50mg/kg体重,更优选0.1mg/kg至10mg/kg体重。在一天内以适当的间隔以两个、三个、四个或多个亚剂量施用所需的剂量可能是适当的。所述亚剂量可以被配制成单位剂型,例如,每单位剂型包含1至1000mg,特别是5至200mg活性成分。
确切的剂量和施用频率取决于所使用的特定的式(i)化合物、待治疗的特定病情、待治疗的病情的严重程度、特定患者的年龄、重量和大体身体情况以及个体可能采用的其它药物,正如本领域技术人员所熟知的那样。另外,显然可以降低或增加有效量,这取决于所治疗受试者的响应和/或取决于开出本发明化合物的医师的评估。因此,以上提及的有效量范围仅是指导,且并不旨在限制本发明的范围或用途至任何程度。
本发明中对上述式(i)化合物进行了一系列实验以验证其抑制hiv复制的活性和机理,包括有细胞水平的毒性实验和抗hiv活性实验,结果显示本发明化合物具有很高的安全性和很好的体外抑制hiv-1的活性;动物水平的抗siv活性实验,对恒河猴直肠给药,再攻毒感染sivmac251,结果显示本发明化合物具有明显的体内抑制病毒复制的作用,对抑制hiv复制的机制也做了系统深入的研究,证明本发明化合物可通过作用于病毒进入细胞阶段、封闭cd4受体、以及影响vif-a3g相互作用等途径发挥抗hiv作用,另外本发明化合物还可以与上市公认有效的治疗艾滋病的阳性药物产生多靶点联合治疗,协同增效的作用,有望成为一种高效、低毒、对多个靶点均发挥作用的预防和/或治疗艾滋病的药物。其具有抗病毒活性高、低毒性、制备方便、价格低廉的特点。
附图说明
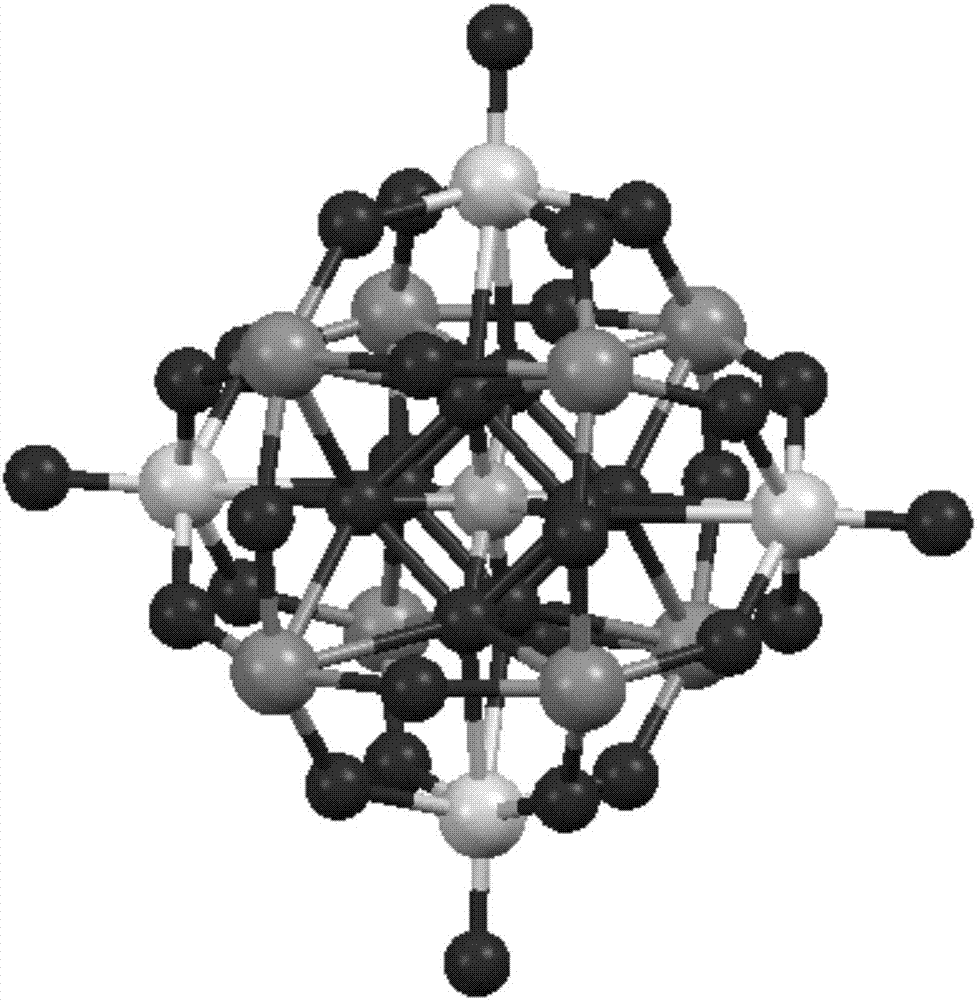
图1显示杂多阴离子pti2w10o407-的结构图。
图2显示kc-01在tzm-bl细胞上抗hiv-1药效。
图3显示kc-01在胸腺细胞上抗hiv-1药效。
图4显示cck8法细胞毒性结果。
图5显示病毒sivmac251直肠途径感染中国恒河猴血浆病毒载量结果。
图6显示病毒sivmac251直肠途径感染中国恒河猴外周血cd4+/cd8+结果。
图7显示magitest药效学实验结果。
图8显示kc-01对病毒进入细胞的抑制作用。
图9显示kc-01对细胞表面cd4受体的封闭作用。
图10显示kc-01对hiv-1vif降解a3g的保护作用。
图11显示kc-01与azt联合用药的协同/拮抗曲面图。
具体实施方式
下面将结合实施例和附图详细描述本发明,但是实施例不应解释为对本发明范围的限制。
实施例中使用的主要材料、仪器及其来源为:
实施例1、k6hpti2w10o40·5h2o的制备
二水钨酸钠91mmol、磷酸二氢钠43mmol溶解在100ml的蒸馏水中,滴加16mmol的四氯化钛,回流反应30min,冷却过滤,调节滤液ph值为7,向滤液中加入过量kcl得白色固体,热水重结晶。根据元素分析和热重分析结果(%,计算值):k8.04(8.01),p1.05(1.06),ti3.26(3.27),w62.70(62.72),h2o3.10(3.07),及x射线单晶衍射分析,确定化合物组成为k6hpti2w10o40·5h2o。其中,杂多阴离子pti2w10o407-的晶体结构见图1,晶体基本参数见表1。
表1.杂多阴离子pti2w10o407-的晶体基本参数
实施例2、k4h3pti2w10o40·8h2o的制备
二水钨酸钠91mmol、磷酸二氢钠43mmol溶解在100ml的蒸馏水中,滴加16mmol的四氯化钛,回流反应30min,冷却过滤,调节滤液ph值为5,向滤液中加入过量kcl得白色固体,热水重结晶。根据元素分析和热重分析结果(%,计算值):k5.35(5.38),p1.04(1.06),ti3.32(3.29),w63.24(63.20),h2o4.96(4.95),及x射线单晶衍射分析,确定化合物组成为k4h3pti2w10o40·8h2o(在本文中用代号kc-01表示)。其中,杂多阴离子pti2w10o407-的晶体结构见图1,晶体基本参数见表1。
实施例3、k2h5pti2w10o40·6h2o的制备
二水钨酸钠91mmol、磷酸二氢钠43mmol溶解在100ml的蒸馏水中,滴加16mmol的四氯化钛,回流反应30min,冷却过滤,调节滤液ph值为3,向滤液中加入过量kcl得白色固体,热水重结晶。根据元素分析和热重分析结果(%,计算值):k2.82(2.80),p1.14(1.11),ti3.42(3.43),w65.77(65.74),h2o3.84(3.86),及x射线单晶衍射分析,确定化合物组成为k2h5pti2w10o40·6h2o。其中,杂多阴离子pti2w10o407-的晶体结构见图1,晶体基本参数见表1。
实施例4、kc-01颗粒剂、胶囊剂的制备
kc-01干燥粉末每5g与淀粉44g,羧甲基淀粉钠5g混合,用60~80%乙醇湿法制粒,干燥后,按每袋4~5g装袋即得颗粒剂;亦可以60~80%乙醇湿法制粒后,干燥的颗粒按照每粒0.5g装入空胶囊得含有效成分kc-01约50mg/粒的胶囊剂。
实施例5、kc-01片剂的制备
kc-01片剂1000片制备处方:kc-01固体粉末50g、淀粉36g、糊精25g、羧甲基淀粉纳1g、10%淀粉浆60g、硬脂酸镁1g,混合压片得到含有效成分kc-0150mg/片的片剂。
实施例6、kc-01栓剂的制备
kc-01栓剂100枚处方为:kc-01粉末30g,甘油190g,明胶54g,加纯化水至300ml。取处方量的明胶置蒸发皿,加入2倍与明胶重量的纯化水浸泡约30min,使明胶膨胀变软,再加入甘油,在水浴上加热使明胶溶解,继续加热并轻轻搅拌使内容物质量达到约50g为止。另取处方量kc-01溶于水,所得溶液加至上述明胶溶液中,搅拌均匀,趁热注入已涂有润滑剂的栓模中,冷却,削去溢出部分,脱模,即得栓剂。
实施例7、kc-01在细胞水平的抗hiv-1药效学实验
以tzm-bl细胞、mt4细胞和胸腺细胞三种细胞株为模型,用hiv-1分别感染细胞,对染毒细胞给药后观察化合物kc-01对病毒复制的抑制作用。
tzm-bl细胞:将tzm-bl细胞(hela细胞表达cd4、cxcr4和ccr5,含tat启动的荧光素酶和lacz基因)接种于96孔板,37℃培养箱培养24h后,弃去上清,加入psg3假病毒上清,病毒上清中加入deae(终浓度10μg/ml),同时加入系列浓度分别为10、1、0.1、0.01、0.001μg/ml的化合物kc-01溶液,培养48h后,弃去上清,加入固定液室温固定5min,pbs清洗后加入显色液(含4mm氰亚铁酸钾,4mm氰铁酸钾,2mmmgcl2,0.4mg/mlx-gal),37℃培养箱中培养50min,pbs清洗,在显微镜下计数蓝斑数,计算得ic50为144ng/ml,显示其抑制病毒复制的活性很高,结果见图2。
mt4细胞:实验设病毒对照组、细胞对照组、azt阳性对照组和化合物kc-01不同浓度给药组,每组设三个复孔。azt给药浓度为1μg/ml,kc-01各给药浓度分别为10、2、0.4、0.08、0.016μg/ml。取状态良好的mt4细胞,配制1000tcid50/ml的病毒稀释液(hiv-1r3a病毒1:100稀释)。细胞离心去培养基后,每管加入病毒稀释液,37℃、co2培养箱内培养2h,每半小时摇晃一次。pbs洗涤细胞3次,1500rpm,离心5分钟,弃上清,加入新鲜培养基重悬,重悬液加入u底96孔板中,每孔100μl,其中细胞对照组加入未加毒的mt4细胞。向96孔板中加入对应药物液,每孔100μl,细胞对照和病毒对照组加入100μl无血清培养基,每组设3个复孔。培养5天,在培养3天时采用半换液(保持药物浓度不变)换液一次。在培养5天后(即第6天),每孔取上清50μl进行p24检测。荧光素酶检测:各孔取上清50μl加入到前1天已铺板的tzmbl细胞中,继续培养48h,使用brightglo检测试剂盒进行荧光素酶检测。
结果,药物kc-01在p24和荧光素酶两种方法检测效果与阳性药物azt相当,计算得到其半数抑制浓度ic50分别为8ng/ml和3ng/ml。
胸腺细胞:采用胸腺器官培养法(thymusorganculture,toc)法,dmem培养基,20%胎牛血清原代培养胸腺细胞。取50μl胸腺细胞与等体积pnl4.3野生毒株混合培养,分别加入4μg/ml和40μg/ml的化合物kc-01共培养,培养3天后收集胸腺细胞,加入抗cd4-pe和抗cd3-apc抗体,冰浴30min,低速离心并经pbs洗涤两次后,制备单细胞悬液,流式细胞仪检测胸腺中t细胞亚群的比例,计数加药前后cd4细胞数,结果发现加药40μg/ml时显著的抑制感染cd4t细胞数(见图3)。
实施例8、kc-01在细胞水平的毒性实验
mt4细胞毒性实验:按照实施例1中mt4细胞药效学实验方法,于96孔板加入药液及正常细胞(未感染病毒),三天后用mtt法测定细胞毒性,计算出半数毒性浓度tc50=537μg/ml。
cck-8细胞毒性试验:用三种不同的细胞株(293ft细胞、hela细胞、tzm-bl细胞)分别验证了化合物kc-01的细胞毒性。分别将不同细胞接种于96孔板,37℃培养箱培养24h后,加入不同梯度浓度的化合物kc-01。继续培养48h后,采用cck-8细胞增殖检测试剂,培养30min,酶标仪检测od值。计算化合物kc-01对细胞增殖的抑制率,结果见图4。
两种方法的细胞水平毒性实验结果均显示该化合物具有较低的细胞毒性,安全性高。
实施例9、kc-01经直肠给药在恒河猴体内药效学实验
kc-01溶于水制成溶液,将s40基质于70℃水浴融化,以1n的naoh调ph值至7.0,将kc-01水溶液与融化的s40基质按4:6比例混合,搅拌均匀,使kc-01在乳膏中的浓度为2mg/g;4℃保存,用前加温至37℃。取健康状况良好的恒河猴,3-5岁,4kg左右,雌雄各半;血清学和pcr法排除特定病原体(siv/srv/stlv/bv/tb)后,进入动物房适应1周后开始进行实验。制备好的kc-01的乳膏按照1g/kg的剂量给药两只恒河猴(分别称给药组1和给药组2),相当于每kg体重给予该化合物6mg;另有两只恒河猴先行直肠给予相同质量和性状的不含药的空白乳膏剂(分别称对照组1和对照组2)。给药和对照两组动物均给药半小时后攻毒,以病毒sivmac251直肠攻毒一次,剂量为5×104tcid50。给药攻毒后第0、3、6、10、13、17、20、24、31、42、56、72、90天取血,测定预防效果。
给药组与不给药的对照组实验结果对比显示,对照组的恒河猴病毒载量于攻毒后3~6天可以检测到,此后不断上升,于2周左右达到峰值,为7.51和7.35,此后逐渐下降,实验结束时仍为3.72和4.46。而给药组的恒河猴则在第六天可检测到病毒,但是低于对照组,此后逐渐缓慢升高,到72天达到最高值,为4.31和4.45,到实验结束时降低到2.0和3.13,见图5。cd4/cd8比值结果:各组在攻毒后均有反应性下降,但是给药组逐渐升高,在第三周时达到1.0以上,并一直持续。而对照组的比值一直低于1.0,并持续到实验结束,见图6。
本实验采用较大剂量病毒攻毒,且仅一次直肠给药,以上结果显示该化合物在较低的剂量(6mg/动物)下已经显示对染毒的恒河猴体内sivmac251病毒的复制有很强的抑制作用。
实施例10、kc-01抑制hiv-1复制机制的研究
艾滋病毒的生活周期包括病毒进入细胞、逆转录酶、整合酶、转录、蛋白酶等阶段,每个不同阶段都对应用药物作用的靶点。了解药物作用的靶点对于药物作用机制的阐明,药效作用的更好发挥都起着至关重要的作用。进入细胞的阶段,包括病毒、cd4受体、ccr5辅助受体(m细胞)、cxcr4辅助受体(t细胞)几个部位;逆转录酶和蛋白酶靶点最好的应用就是“鸡尾酒疗法”。本发明中化合物可作用于hiv-1病毒周期中的不同阶段,从而更好的发挥抑制病毒复制的作用。
magitest:本发明中应用病毒基因重组的“单一生活周期(singlelifecycle)”模型,研究药物作用的靶点。感染后2-6h是病毒进入细胞阶段,10-14h为逆转录阶段,20h以后是整合、转录、蛋白合成阶段。药物在何时间段产生作用,则表明作用于何靶点。
用24孔板接种hela-cd4+-ltr-x-gel细胞0.4×105cell/孔,放置24h,使之吸附,贴壁。第二天,吸去孔中上清,加入定量hiv(nl4),0、6、12、18、24、36h分别于不同孔各加入100μl不同浓度的化合物kc-01溶液或阳性对照药溶液,培养基对照,37℃,5%co2培养,3h后再加入200μl相同药液,37℃,5%co2培养48h,收集上清以备检测,各孔吸去上清加入固定液1ml,再以k4[fe(cn)6]、k3[fe(cn)6]及x-gel染色,显微镜下蓝色细胞表示带有病毒基因。根据每孔蓝色细胞数计算抑制率。结果表明化合物kc-01主要作用于病毒进入细胞的阶段(图7)。
辅助受体作用部位的分析:病毒进入细胞与三个部位有关,既病毒的gp120蛋白,细胞膜上的cd4受体,及辅助受体ccr5(嗜m细胞)及cxcr4(嗜t细胞)。
方法同以上的magitest,不同的辅助受体应用不同的细胞株及病毒,cxcr4用的病毒株为nl4,细胞株为hela-cd4+-ltr-x-gel(嗜t);ccr5用的病毒株为yu2,细胞株为293t(嗜m),48h后同法检测,结果见下表。kc-01对两种辅助受体均有抑制作用,说明不是对辅助受体本身有作用,而可能作用于cd4或病毒脱壳等,尚有待进一步分析。
细胞进入抑制:向tzm-bl细胞中分别加入100tcid50/ml的hiv-1包膜和水疱性口炎病毒g蛋白(vsv-g)包膜的假病毒质粒(psg3),同时加入不同浓度的化合物kc-01,共同培养48h后,固定染色,检测蓝斑数,计算抑制率。结果显示,化合物kc-01对hiv-1包膜的假病毒具有选择性的抑制作用,表明化合物kc-01可以抑制病毒进入细胞(图8)。
封闭细胞表面cd4受体:将tzm-bl细胞与化合物kc-01共培养30min,离心,pbs清洗2次,加入cd4-pe抗体孵育30min,pbs清洗2次,流式细胞仪检测cd4的荧光强度,结果显示化合物kc-01与tzm-bl细胞共孵育,可以封闭细胞表面的cd4受体(减少71%),从而阻止env包膜通过cd4受体进入细胞(图9)。
对vif-a3g相互作用的影响:载脂蛋白bmrna编辑酶催化多肽样蛋白(apolipoproteinbmrna-editingenzymecatalyticpolypeptideprotein,apobec)家族的成员apobec3g(a3g)可以通过胞嘧啶脱氨机制抑制hiv-1的复制,发挥固有免疫的作用;hiv-1的病毒感染因子vif(viralinfectivityfactor)能与a3g结合并引发a3g的降解,使hiv-1的感染率增加100倍以上。本发明设计实验以vif-a3g为靶点研究化合物kc-01对hiv-1的抑制作用,具体如下:将293t细胞接种于6孔板板中,细胞贴壁后共转染pcdna3.1-vif和pcdna3.1-a3g质粒,共转6h后加入化合物kc-01,共同孵育24h后,裂解细胞提取总蛋白,采用westernblot分析vif和a3g的蛋白表达,结果显示vif降解a3g蛋白的表达,但加入化合物kc-01后可以有效保护部分a3g60%不被vif降解,从而降低病毒的感染率,结果见图10。
实施例11、kc-01与azt的协同作用研究
齐多夫定(azt)为目前临床上广泛应用的治疗hiv感染的阳性药物,属于核苷类逆转录酶抑制剂。本发明设计实验将kc-01与azt联合给药,利用macsynergyii软件检测其协同、拮抗作用水平。通过软件可得到联合用药的水平累积平面,从图中协同容量值(单位nm2%)的大小反应药物协同、拮抗的大小。如果药物效果仅仅是相加作用,则合成平面将呈现完全水平;累积平面上若出现峰即表示协同作用;累积平面下的的谷则表示拮抗作用。其协同、拮抗水平定义见下表。
消化tzm-bl细胞,在96孔板中按7,000个/孔的细胞数接种tzm-bl细胞,37℃,5%co2培养箱中培养至细胞汇合度达40-50%。取psg3假病毒一支,500μl病毒至10ml含deae的完全培养基混匀。各加药实验孔加入50μl毒液;细胞对照孔加入50μl含deae的完全培养基;病毒对照孔加入50μl毒液。药物5倍比稀释,每种药物设6个剂量,每个剂量3个复孔,每孔加稀释药液体积为25μl,至加药后kc-01的终浓度分别为:500ng/ml、100ng/ml、20ng/ml、4ng/ml、0.8ng/ml;azt的终浓度分别为:5ng/ml、1ng/ml、0.2ng/ml、0.04ng/ml、0.008ng/ml),37℃,5%co2培养箱中继续培养48h。弃去96孔板中的培养基,每孔加入200μl固定液(37%甲醛675μl,25%戊二醛200μl,pbs24.1ml配制而成),于37℃,5%co2培养箱中孵育5min;弃固定液,pbs缓冲液洗涤细胞2次;避光条件下每孔加入100μl染色液(0.2m亚铁氰化钾240μl,0.2m铁氰化钾240μl,2.0mmgcl212μl,40mg/mlx-gal120μl,pbs11.4ml配制而成),放置在37℃,5%co2培养箱中孵育50min;弃染色液,pbs缓冲液洗涤细胞2次后,利用显微镜计数细胞蓝斑数。按照以下公式(1)计算病毒抑制率:
抑制率结果导入macsynergyii软件,拟合得出如图11的结果和如下表的kc-01与azt协同/拮抗容量(nm2%)值。由结果可见kc-01和azt不同浓度组合,呈现不同的相互作用,kc-01与azt协同/拮抗容量为71.46/-39.69nm2%,表明在本实验选用的浓度范围内,kc-01与azt呈现协同作用。且kc-01浓度为20ng/ml,azt浓度为5ng/ml时,kc-01与azt协同作用最强。azt是针对hiv逆转录酶靶点的有效药物,kc-01的作用靶点与其不同,二者联合应用,推测会起到针对不同靶点的协同作用,而使药效进一步增加。
kc-01与azt协同/拮抗容量(nm2%)
本发明对所涉及化合物进行了一系列的体内和体外药效学实验以及机制分析,结果显示本发明的化合物具有很高的安全性和明显的抑制hiv-1(siv)的活性;同时实验证明本发明的化合物可通过作用于病毒进入细胞阶段、封闭cd4受体、以及影响vif-a3g相互作用等途径发挥抗hiv作用,另外本发明化合物还可以上市公认有效的治疗艾滋病的阳性药物产生多靶点联合治疗,协同增效的作用,有望成为一种高效、低毒、对多个靶点均发挥作用的预防和/或治疗艾滋病的药物。
- 还没有人留言评论。精彩留言会获得点赞!