一种硅酸锰微球的绿色一步水热合成方法及应用与流程
[0001]
本发明涉及无机材料化工领域,具体涉及硅酸锰微球的绿色一步水热合成及应用。
背景技术:
[0002]
现今,随着工业进步和社会发展,水污染日趋严重,已成了世界性的头号环境治理难题。工业引起的水污染,含污染物多,成分复杂,不易在水中净化,处理起来也比较困难。为此,人们尝试开发高效、实用和经济的纳米材料作为催化剂或吸附剂,以解决水污染问题。高级氧化法(aops)在降解有机污染物方面具有广阔的应用前景。最著名的催化剂包括芬顿和类芬顿型催化剂。锰化合物特别是锰氧化物是典型的芬顿型催化剂,具有毒性低、来源丰富、成本低、环境友好等优点。此外,锰的多价态不仅可以提高反应活性,还可以产生更多种类的化合物,从而使得应用多样化。过渡金属硅酸锰作为一种具有高比表面、多级结构硅酸盐材料,已被广泛应用于吸附、催化、储能、药物传递等领域。更重要的是,与金属和金属氧化物相比,其成本更低、来源更丰富、结构更稳定。特别是层状结构硅酸锰,结合了锰化合物的高化学活性和层状硅酸盐的结构稳定性,作为类芬顿型催化剂有着显著的发展前景,具有很高的研究价值。
[0003]
目前,已有大量文献报道关于硅酸锰微球材料的合成。例如,christopher cheung yec等以st
ö
ber法为基础,将teos在氨水催化下水解缩聚,得到粒径为270 nm 的sio2微球作硬模板,mn(ac)2·
4h2o为锰源,在180
º
c条件下反应12.0 h,得到以braunite-1q (mn
2+
mn
63+
sio
12
或mn
2+
mn
3+6
[o8|sio4],jcpds no. 89-5661)为主物相的中空微球,其比表面积为316.1 m
2 g-1
,将其应用于染料的降解(acs nano,2014);shu meng hao等以碳纳米管(cnts)为模板,在乙醇溶剂中加入阳离子表面活性剂ctab,并在碱性条件下催化teos水解缩聚,得到硅包覆的碳纳米管(cnt@snts),之后将cnt@snts在空气氛围中煅烧,最终得到snts,并以snts为硅源,mncl2·
4h2o为锰源,加入氨水、氯化铵,水热10 h,得到mn7o8(sio4)中空纳米管,比表面积为438 m
2 g-1
,将其应用于亚甲基蓝(meb)染料的降解,在最佳降解条件下,k=1.717 min-1
,q=81.9 g l
−1g
−1(adv. funct. mater. 2016);中国专利文献(cn201711134136.1)公开了一种基于摇铃形模板双层中空纳米硅酸锰的合成方法。首先模板zif-8@msio2以硅酸四丁酯、zif-8为原料,水和甲醇为溶剂,加入表面活性剂,在碱性条件下合成。其次先将锰盐溶于去离子水中,并依次加入氯化铵和氨水,将形成的锰离子络合物加入到zif-8@msio2溶胶体系中,在10-35
º
c或50-180
º
c条件下反应4.0-48.0 h,得到双层中空的纳米硅酸锰mn(sio4);中国专利文献(cn201710422359.1)公开了一种空心硅酸锰材料及其合成方法。其同样以st
ö
ber法为基础,以teos为原料,在有机溶剂和碱性缓冲溶液中水解缩聚得到粒径小于等于50 nm sio2微球作模板,随后加入高锰酸钾,在水热/溶剂热反应釜中170-200
º
c下反应,制得空心硅酸锰(mn5si3o
12
,jcpds no. 37-0221)材料。
[0004]
然而,上述硅酸锰材料的合成,均是采用teos水解合成sio2微球或纳米管作为硬模板,再加入锰盐水热合成硅酸锰材料,其合成过程至少经过两步(acs nano,2014)甚至多
步步骤(adv. funct. mater. 2016),有的体系还需要高分子表面活性剂(cn201711134136.1& adv. funct. mater. 2016),合成工艺繁琐,且有机硅teos水解合成sio2微球价格昂贵,有的体系水热过程中还需再次使用有机溶剂(cn201710422359.1),不符合环境友好、绿色工艺的要求,而已报道的硅酸锰材料用于染料降解效果一般。
技术实现要素:
[0005]
针对现阶段硅酸锰材料的合成工艺繁琐、不够绿色、成本高等缺陷,本发明提供了一种硅酸锰微球的绿色一步水热合成方法,通过将可溶性金属锰盐、可溶性硅酸盐、铵盐在碱性条件下进行水热反应,即可得到硅酸锰微球;而且制备的硅酸锰微球能够用于污水处理,降解效果好,可多次循环利用,提供了成本廉价、简单有效的污水处理办法。
[0006]
本发明的技术方案如下:一种硅酸锰微球的绿色一步水热合成方法,所述的方法为:将可溶性金属锰盐、可溶性硅酸盐、铵盐在碱性条件下进行水热反应,得到所述硅酸锰微球。
[0007]
上述硅酸锰微球的绿色一步水热合成方法,具体步骤为:1) 将所述可溶性金属锰盐与所述铵盐溶于去离子水中,混合均匀,得到溶液a;2) 将所述溶液a和碱源混合均匀,得到溶液b;3) 将所述可溶性硅酸盐溶解得到的硅酸盐溶液滴加到所述溶液b中,混合均匀,得到悬浮液c;4) 将所述悬浮液c进行水热反应,冷却至室温得到水热产物;5) 将所述水热产物进行洗涤、过滤、干燥,得到所述硅酸锰微球。
[0008]
上述硅酸锰微球结构为braunite-1q,mn
+2
mn
6+3
sio
12
,粒径为100-500 nm,其次级结构为3-6 nm粒子,比表面积为350-450 m
2 g-1
,孔容为0.54-0.78 cc g-1
。
[0009]
所述可溶性金属锰盐为氯化锰、硫酸锰、乙酸锰中的至少一种;所述铵盐为氯化铵或硫酸铵中的至少一种;所述碱源为氨水、乙二胺中的至少一种;所述可溶性硅酸盐为硅酸钠或硅酸钾中的至少一种。
[0010]
在所述可溶性金属锰盐、铵盐、可溶性硅酸盐中,锰离子、铵离子、硅酸根的摩尔比为:0.70:1-4:0.10-0.50,所述锰离子与碱源的摩尔比为:0.70:0.01-0.04。
[0011]
所述步骤4)中,以5-10
º
c min-1
的速率升温至120-200
º
c,反应6.0-24.0 h,冷却至室温,得到水热产物。
[0012]
所述步骤5)中,将所述水热产物依次用去离子水洗涤,然后用乙醇洗涤,洗涤后抽滤。
[0013]
上述任一所述的方法合成的硅酸锰微球。
[0014]
上述合成方法得到的硅酸锰微球,在污水处理上的应用。
[0015]
优选地,上述应用,方法为:将所述硅酸锰微球置于含有机染料的污水中,在25-60
º
c下,加入30 wt% h2o2进行催化降解。
[0016]
优选地,所述的有机染料污水所含的有机染料为:亚甲基蓝(阳离子染料)、罗丹明b(阳离子染料)、甲基蓝(阴离子染料)。
[0017]
本发明技术方案,具有如下优点:1、本发明提供硅酸锰微球的绿色一步合成方法,分别利用可溶性金属锰源为锰源,以
可溶性硅酸盐为硅源,以铵盐为矿化剂,在碱性条件下进行水热反应,得到组成纯净、尺寸均一、粒径分布范围较窄的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球,粒径为100-500 nm,其次级结构为3-6 nm粒子,比表面积为350-450 m
2 g-1
,孔容为0.54-0.78 cc g-1
,采用一步水热法,绿色环保、操作简单、条件温和、能耗低、工艺易控,适宜大规模工业推广。
[0018]
2、本发明提供的硅酸锰微球能够用于污水处理,采用高级氧化技术(aops),将硅酸锰微球置于含有有机染料的污水中,加入h2o2,进行类芬顿型催化降解有机染料,降解效果好,可多次循环利用,提供了成本廉价、简单有效的污水处理办法。
附图说明
[0019]
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在无需付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0020]
图1为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球的sem图谱;图2为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球的xrd图谱;图3为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球的tem照片;图4为实施例4合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球的sem照片;图5为实施例6合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球的xrd照片;图6为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球在25
º
c,加入h2o2,t (min)时刻亚甲基蓝紫外-可见光谱(uv-vis)图。
[0021]
图7为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球在60
º
c,加入h2o2,t (min)时刻亚甲基蓝紫外-可见光谱(uv-vis)图。
[0022]
图8为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球在25
º
c,加入h2o2,t (min)时刻罗丹明b紫外-可见光谱(uv-vis)图。
[0023]
图9为实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球在25
º
c,加入h2o2,t (min)时刻甲基蓝紫外-可见光谱(uv-vis)图。
具体实施方式
[0024]
提供下述实施例是为了更好地理解本发明,但并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征组合而得出的任何与本发明相同或近似的产品,均落在本发明的保护范围之内。
[0025]
实施例中未注明具体实验步骤或条件者,按照本领域内文献所描述的常规实验步骤的操作或条件即可进行。所有试剂或仪器未注明生产厂商,均为可通过市售获得的常规试剂产品。
[0026]
实施例1一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mncl2和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶
液a;(2) 将2 ml nh3·
h2o快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应12.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0027]
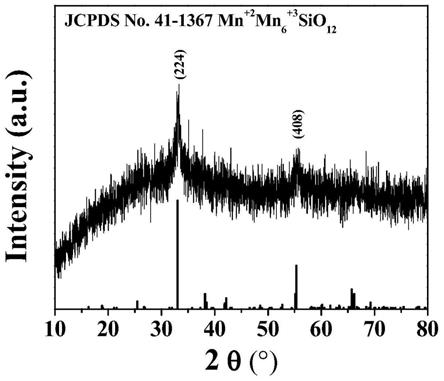
本实施例制得的样品,使用miniflex600型x-射线衍射(xrd)仪器得到的xrd图谱如图1所示,由图1可以看出braunite-1q,mn
+2
mn
6+3
sio
12
微球的xrd图与xrd标准卡片号jcpds no. 41-1367匹配较好,说明产物组成较纯。
[0028]
本实施例制得的braunite-1q,mn
+2
mn
6+3
sio
12
微球使用jem-2010型透射电子显微镜(tem)得到的tem照片如图2所示,由图2可以看出braunite-1q,mn
+2
mn
6+3
sio
12
微球由纳米粒子组装而成,粒径在110-220 nm,粒径分布均匀。
[0029]
实施例2一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mncl2和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml nh3·
h2o快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应18.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0030]
实施例2得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在180-300 nm,粒径分布均匀。
[0031]
实施例3一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mncl2和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml nh3·
h2o快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b
中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应24.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0032]
实施例3得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在280-500 nm,粒径分布均匀。
[0033]
实施例4一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mn(ac)2和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml nh3·
h2o快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应24.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0034]
实施例4得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在90-210 nm,粒径分布均匀。
[0035]
实施例5一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mnso4和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml nh3·
h2o快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应24.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0036]
实施例5所得硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在60-100 nm,粒径分布均匀。
[0037]
实施例6一种硅酸锰微球的合成方法,操作如下:
(1) 将1.30 mmol mnso4和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml 乙二胺快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的na2sio3溶于20 ml去离子水中,将得到的na2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应24.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0038]
实施例6得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在120-230 nm,粒径分布均匀。
[0039]
实施例7一种硅酸锰微球的合成方法,操作如下:(1) 将1.30 mmol mncl2和10 mmol nh4cl固体分别溶于10 ml、10 ml去离子水中,将得到的nh4cl溶液滴加到10 ml mncl2溶液中,250 rpm磁力搅拌10 min后得到无色透明的溶液a;(2) 将2 ml 乙二胺快速滴加至无色透明溶液a中,得到溶液b,250 rpm磁力搅拌10 min;(3) 将0.37 mmol的k2sio3溶于20 ml去离子水中,将得到的k2sio3滴加到溶液中b中,250 rpm磁力搅拌10 min后得到悬浮液c;(4) 将悬浮液c置于水热釜内,以8
º
c min-1
的升温速率升温至120
º
c,恒温反应24.0 h后,自然冷却至室温,得到水热产物;(5) 将水热产物依次经过去离子水及无水乙醇各洗涤三次并布氏漏斗过滤,60
º
c下干燥18.0 h,即得样品。
[0040]
实施例7得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)粒径在200-480 nm,粒径分布均匀。
[0041]
实验例一、实验目的检验实验例1合成得到的硅酸锰微球对有机染料的吸附-降解效果。
[0042]
二、实验方法配置浓度为50 mg l-1
的亚甲基蓝(罗丹明b或甲基蓝)溶液,量筒量取50 ml 有机染料溶液,0.1 m naoh溶液将(或0.1 m hcl 溶液)调节ph值后,置于100 ml锥形瓶中;称取10 mg实施例1合成得到的硅酸锰(braunite-1q,mn
+2
mn
6+3
sio
12
)微球,加入到上述盛有有机染料溶液的锥形瓶中;置于磁力搅拌器上,25
º
c或60
º
c、黑暗条件吸附1.0 h达吸附平衡后,向锥形瓶内加入5 ml h2o2,每隔一段时间在锥形瓶内取3 ml溶液,用一次性针头过滤器过滤,得到的滤液置于紫外-可见光谱(uv-vis)仪进行表征,得到t 时刻下,对应的有机染料溶液吸光度。
[0043]
动力学数据拟合如下动力学方程:-dc
t
/dt=kc
t
,然后ln(c0/c
t
)=kt,式中,c
t
和k分别为有机染料废水在t时刻的浓度和速率常数。催化效率也可以用q来评价:q=(c
0-c)v0/v
′
m,式中,q (g l
−1g
−1)为1 g催化剂和1 l 30 wt% h2o2溶液对有机染料的降解量;c
0 (g l
−1)和c (g l
−1)分别为有机染料的初始浓度和最终浓度;v
0 (ml)和v’(ml)分别为染料溶液的体积和30 wt% h2o2溶液的体积。染料去除率的计算方法为:在664 nm(554 nm或598 nm) 处用紫外分光光度计测量染料废水的吸光度,去除率(%)=(a
0-a)/a0×
100%,a0为染料废水反应前的吸光度值,a为反应后的吸光度值。根据公式,计算得出降解速率常数k、q值和去除率。
[0044]
三、实验结果如图6所示,黑暗条件吸附1.0 h达吸附平衡后,在室温下,加入5 ml h2o2,20 min时,亚甲基蓝去除率为97.7%,此时k=0.169 min-1
,q=50.3 g l
−1g
−1。30 min时,亚甲基蓝去除率为99.9%,在664 nm处亚甲基蓝最大吸收峰吸光度趋近于0。
[0045]
如图7所示,黑暗条件吸附1.0 h达吸附平衡后,在60
º
c,加入1 ml h2o2,3 min时,亚甲基蓝去除率为98.0%,此时k=0.979 min-1
,q=248.8 g l
−1g
−1。4 min时,亚甲基蓝去除率为99.1%,在664 nm 处亚甲基蓝最大吸收峰吸光度趋近于0。
[0046]
braunite-1q,mn
+2
mn
6+3
sio
12
微球作为催化剂,采用高级氧化技术aops降解亚甲基蓝废水效果明显高于中空管状braunite-1q,mn
+2
mn
6+3
sio
12 (25
º
c,10 ml h2o2时,k=0.060 min-1
,q=24.7 g l
−1g
−1,60
º
c,3 ml h2o2时,k=0.828 min-1
,q=81.9 g l
−1g
−1,adv. funct. mater. 2016)和纳米圆盘状mntio
3 (30
º
c,1.5 ml h2o2时,k=0.168 min-1
,q=131.4 g l
−1g
−1,acs appl. nano mater. 2018)。基于此本发明合成的braunite-1q,mn
+2
mn
6+3
sio
12
微球作为类芬顿型催化剂降解亚甲基蓝表现处良好的降解效果。
[0047]
如图8所示,黑暗条件吸附1.0 h达到吸附平衡后,在室温下,加入5 ml h2o2,60 min时,罗丹明b去除率为94.2%,在554 nm 处罗丹明b最大吸收峰吸光度趋近于0。
[0048]
如图9所示,黑暗条件吸附1.0 h达到吸附平衡后,在室温下,加入5 ml h2o2,15 min时,甲基蓝去除率为97.8%,在598 nm 处甲基蓝最大吸收峰吸光度趋近于0。
[0049]
显然,上述实施里仅仅是为了清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里,无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动处于本发明创造的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1