心脏重塑和其它心脏病状的治疗的制作方法
本申请要求2013年11月5日提交的美国临时专利申请序列号61/900,007的优先权,这个专利以全文引用的方式并入本文中,如同在本文中完整阐述一样。
背景技术:
心脏最初通过起始心脏重塑来响应心脏损伤或病理应力。这类心脏重塑变化抵制不同的心脏应力情形,但长远地导致心脏功能障碍并且最终导致心脏衰竭。心脏重塑是在心肌细胞内发生的一系列复杂的转录、信号传导、结构以及功能事件的顶点。心脏重塑还涉及心室内的其它细胞要素,包括成纤维细胞、冠状动脉血管结构以及侵润性发炎细胞(Bisping,2014)。心脏重塑包涵细胞变化,包括肌细胞肥大、坏死、凋亡、纤维化、纤维状胶原蛋白增加以及成纤维细胞增殖。
当前,五百万美国人罹患慢性心脏衰竭,许多形式的心脏功能障碍的最终共同路径。预测随着我们的人口老龄化,所有形式的心脏病治疗的直接医疗成本将从2010年的2720亿美元三倍升至2030年的8180亿美元(Heidenreich,2011)。约50%的心脏衰竭诊断在不存在缺血性心脏病的情况下涉及心脏重塑和相关的收缩功能障碍。当前,不存在特定的疗法用于这种形式的心脏衰竭,其在人口老龄化下流行率迅速增长。
尽管仅旨在校正低心输出量或减少的血流量的许多疗法的功效,包括血管紧张素转化酶(ACE)抑制剂、血管紧张素受体阻断剂(ARB)、醛固酮拮抗剂以及β-肾上腺素能受体阻断剂(β-阻断剂),提供症状缓解,但其不一定减缓心脏衰竭进程或降低死亡率(Cohn,2000)。为了遏制对个人和社会的这种巨大负担,在本领域中需要靶向心脏重塑的治疗。
某些组蛋白脱乙酰化酶(HDAC)抑制剂展示减少心脏重塑的潜力。这些强效的泛HDAC抑制剂,包括曲古抑菌素A(Trichostatin A,TSA)、斯克瑞泰(Scriptaid)以及SAHA,在低纳摩尔浓度范围内抑制HDAC。然而,HDAC抑制剂的治疗效益必须仔细权衡其引起毒性的潜力。除了恶心和疲劳外,关于HDAC抑制剂治疗已经报道了血液毒性和QT延长(McKinsey,2011)。泛HDAC抑制可以引起短暂性血小板减少并且在一些情况下引起骨髓抑制。QT延长已经在使用泛HDAC抑制剂的试验中作为剂量限制性毒性而报道。因此,在本领域中需要可以抑制心脏重塑而无毒性副作用的新化合物。
技术实现要素:
本发明的一个方面涉及可以在本文所公开的方法中使用的一种或多种化合物。在一个实施方案中,一种或多种化合物可以包含式I的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物,其中:
A和B环独立地选自由苯基和吡啶基环组成的群组;
R1-R5各自独立地选自由氯和卤素组成的群组;
X1和X2各自独立地选自-NHC(=O)-或-C(=O)-NH-;并且
L1是-(CH2)n-,其中n是4、5或6。
在另一个实施方案中,一种或多种化合物可以包含式II的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物,其中:
R1-R5各自独立地选自由氢和卤素组成的群组;
X1和X2各自独立地选自-NHC(=O)-或-C(=O)-NH-;并且
L1是-(CH2)n-,其中n是4、5或6。
在另一个实施方案中,一种或多种化合物可以包含7MI或8MI的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物。
本发明的另一个方面涉及一种改善受试者的心脏功能的方法,其包括向受试者施用治疗有效量的本文所公开的一种或多种化合物。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以改善受试者的心脏功能的药物。
本发明的另一个方面涉及一种治疗受试者的心脏重塑的方法,其包括向受试者施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的心脏重塑的药物。
在一些实施方案中,心脏重塑可以表现为包括以下的症状:心脏收缩力减小、心脏后壁的厚度增大和/或心室质量增加。在一些实施方案中,心脏重塑可以表现为心脏纤维化、肌细胞肥大、肌细胞坏死、肌细胞凋亡、成纤维细胞增殖增加和/或纤维状胶原蛋白增加。
在某个实施方案中,心脏重塑可以表现为一种或多种症状,其独立地选自由以下组成的群组:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、左心室(LV)舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
本发明的另一个方面涉及一种治疗受试者的心脏纤维化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的心脏纤维化的药物。
本发明的另一个方面涉及一种治疗受试者的左心室功能障碍的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的左心室功能障碍的药物。
在一些实施方案中,左心室功能障碍可以表现为一种或多种症状,其独立地选自由以下组成的群组:左心室的舒张功能减小、左心室的收缩功能减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、LV收缩期直径增大、LV舒张末期压力增大、LV收缩期容积增大、LV舒张期容积增大和/或LV质量增加。
本发明的另一个方面涉及一种抑制受试者的肌细胞凋亡的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制受试者的肌细胞凋亡的药物。
本发明的另一个方面涉及一种抑制表现心脏重塑症状的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制表现心脏重塑症状的受试者的MEF2乙酰化的药物。
在一些实施方案中,症状可以是一种或多种症状,其独立地选自包含以下的群组:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
本发明的另一个方面涉及一种抑制具有左心室功能障碍的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制具有左心室功能障碍的受试者的MEF2乙酰化的药物。
本发明的另一个方面涉及一种抑制具有心脏纤维化的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制具有心脏纤维化的受试者的MEF2乙酰化的药物。
在涉及本文所论述的所有方法的一些实施方案中,受试者可以具有一种或多种症状,其独立地选自由以下组成的群组:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
在涉及本文所论述的所有方法的一些实施方案中,受试者可以已经诊断患有一种或多种病状,其独立地选自由以下组成的群组:心脏纤维化、高血压、主动脉狭窄、心肌梗塞、心肌炎、心肌病、瓣膜反流、瓣膜病、左心室功能障碍、心脏缺血、舒张期功能障碍、慢性心绞痛、心动过速以及心动过缓。
在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中B型利钠肽(BNP)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中心房利钠肽(ANP)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中α-肌球蛋白重链(α-MHC)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中β-肌球蛋白重链(β-MHC)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中肌质网(内质网)Ca2+-ATPase(SERCA)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中I型胶原蛋白(Col 1)或3型胶原蛋白(Col 3)的表达。
在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物可以抑制MEF2乙酰化。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物可以促使IIa类HDAC从细胞核重定位至细胞质中。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物可以抑制MEF2结合至其辅因子(即,IIa类HDAC)。
在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物对于HDAC6抑制可以具有大于50μM的IC50。在涉及本文所论述的所有方法的一些实施方案中,与HDAC1相比,一种或多种化合物可以优先或选择性地抑制HDAC3。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物对于HDAC抑制可以具有在检测HeLa细胞核提取物中总组蛋白脱乙酰化的抑制的检验中测定的大于1μM的IC50。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物对于HDAC抑制可以具有在检测HeLa细胞核提取物中总组蛋白脱乙酰化的抑制的检验中测定的大于0.5μM的IC50。
附图说明
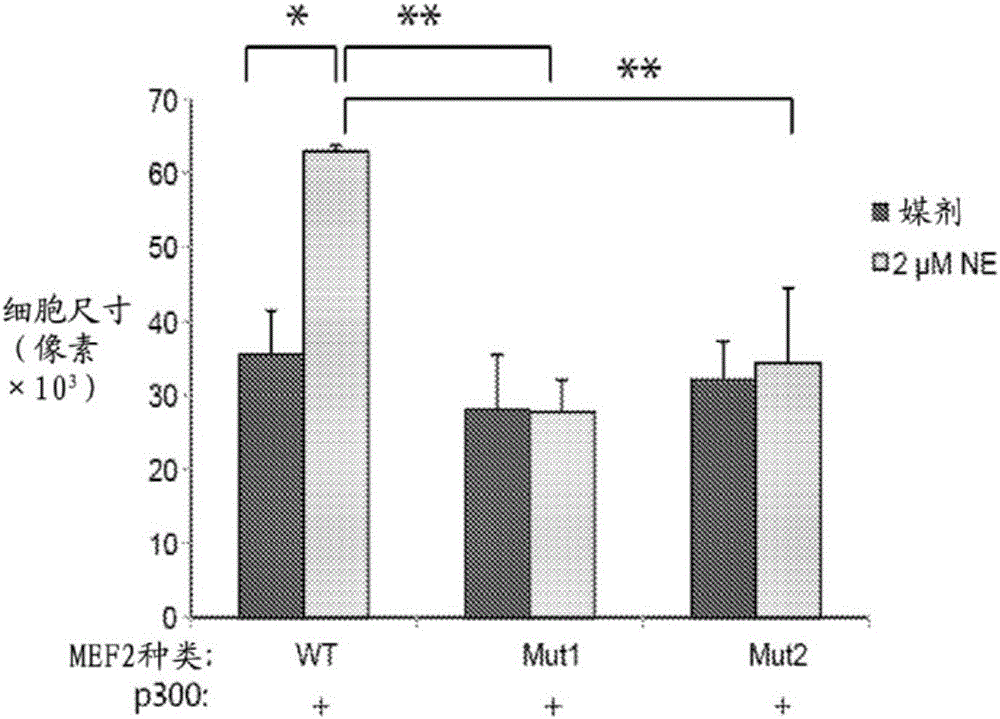
图1说明了乙酰化缺陷MEF2D突变体减小肌细胞肥大反应并且充当肥大的显性阴性抑制剂。用媒剂(暗灰条)或2μM去甲肾中腺素(NE)(亮灰条)处理新生大鼠心室肌细胞(NRVM)。在NRVM培养物中由NE在野生型(WT)或2种不同乙酰化缺陷MEF2突变体之一(Mut1,MEF2D K424R或Mut2,MEF2D I423A)存在下诱导肥大。
图2说明了MEF2抑制剂抑制血清诱导的肥大。图2A示出了在使用NRVM的体外检验中所用的MEF2抑制剂(7MI和8MI)和对照抑制剂(曲古抑菌素A)的化学结构。图2B示出了接受MEF2抑制剂(7MI(黑条)、8MI(白条)或TSA(条纹条))的NRVM对胎牛血清(FBS)展现减低的生长反应。还用DMSO(亮灰条)或媒剂(暗灰条)作为阴性对照来处理细胞。抑制剂效力的次序是DMSO<7MI<TSA<8MI。生存力无变化(末示出)。
图3示出了MEF2抑制剂阻断通过横向主动脉缩窄(TAC)产生的压力超负荷诱导的心脏肥大。在横向主动脉结扎之后立即开始通过每日注射指定浓度的MEF2抑制剂8MI持续两周来处理小鼠。N=每种病状至少3只。使小鼠经受假手术(暗灰条)或TAC(亮灰条)。图3A示出了在处死时测量的心脏重量与胫骨长度的比率的结果。图3B示出了左心室射血分数(LVEF)的结果。在两周时在处死之前通过超声心动描记术在Vevo770超声系统上测定作为收缩功能的量度的射血分数。
图4说明了MEF2乙酰化在表现心脏重塑的人类心脏中增加。图4A示出了在一系列人类左心室心肌样品中测定的MEF2的乙酰化状态的代表性墨点,其代表3个对照心脏(对照)和9个心肌病心脏(心脏重塑)。图4B示出了来自图4A中的免疫墨点的数据的图形,其定量为针对乙酰基-赖氨酸标准化的密度计量单位(n.d.u.,标准化的密度计量单位)。
图5示出了在8MI处理的小鼠中在TAC之后心脏质量的标准化。在TAC或假手术之后21天并且接受指定剂量的8MI的小鼠中测定心脏重量与胫骨长度的比率(HW/TL)(n=每组4-5只)。图5B说明了在8MI处理的小鼠中在TAC之后来自如图5A中处理的小鼠的心脏的代表性曼森氏三色(Masson′s Trichrome)染色的四腔室横切片的心脏几何形状的标准化。原始放大率=1倍。图5C示出了在如图5A中使用指定剂量的8MI处理的小鼠中超声心动描记术的后壁厚度的标准化。图5D示出了来自如图5A中并且如所指示处理的小鼠的心肌的代表性麦胚凝集素(WGA)染色的切片的体内肌细胞尺寸的标准化。图5E示出了在来自每种病状3只小鼠的至少4个心肌切片中来自细胞的WGA染色的切片中的细胞尺寸的定量。
图6示出了8MI减少与压力超负荷相关的纤维化。图6A示出了来自使用指定处理的小鼠的心肌的代表性切片的曼森氏三色染色。图6B示出了相对于总组织面积定量和表达的纤维化面积。数据总结了来自每组3只小鼠的至少4个切片。
图7示出了8MI阻断与压力超负荷相关的转录和功能变化。图7A-7G示出了在获自如实施例4中处理的小鼠的心肌样品中如通过定量实时PCR测量的来自指定基因的mRNA转录物。图7A示出了1型胶原蛋白(Col 1)的表达。图7B示出了3型胶原蛋白(Col 3)的表达。图7C示出了心房利钠肽(ANP)的表达。图7D示出了B型利钠肽(BNP)的表达。图7E示出了肌质网(内质网)Ca2+-ATPase(SERCA)的表达。图7F示出了β-肌球蛋白重链(β-MHC)的表达。图7G示出了α-肌球蛋白重链(α-MHC)的表达。n.d.u.=标准化的转录单位。
图8示出了在8MI处理的小鼠中在TAC之后心脏功能的保留。图8A示出了射血分数(EF)。图8B示出了%缩短分数。图8C示出了心搏量(ml)。图8D示出了舒张末期的左心室内径(LViDd)。图8E示出了收缩末期的左心室内径(LViDs)。图8F示出了左心室收缩期容积(LV Vs)。图8G示出了左心室舒张期容积(LV Vd)。图8H示出了心率。在图8A-H中,在接受8MI(5、20以及40mg/kg)或其媒剂的小鼠中在TAC或假手术之后21天进行超声心动描记术。
图9示出了8MI减少压力超负荷相关的MEF2乙酰化。如实施例9中所描述在如所指示用指定剂量的8MI或其媒剂(0)处理的TAC或假手术小鼠的心肌溶解产物中测定乙酰基-MEF2和乙酰基-GATA4。用8MI处理并不降低无应力心脏中的乙酰基-MEF2水平。MEF2乙酰化由TAC增加并且由8MI减少。用抗泛MEF2或GATA4抗体使心肌溶解产物免疫沉淀,并且用针对MEF2、GATA4或乙酰基-赖氨酸(对照)的抗体探测。图9中所示的定量数据来自每组3只小鼠并且针对总乙酰基-赖氨酸标准化(西方墨点未示出)。
图10示出了8MI在TAC期间以剂量依赖性方式防止肌细胞凋亡。图10示出了肌细胞凋亡在TAC手术小鼠中与假手术小鼠相比增加。用8MI处理小鼠降低肌细胞凋亡水平。
图11示出了7MI和8MI比BML-210或TSA更好地被肝代谢。
具体实施方式
以下描述提供了对于本公开的实施方案的透彻理解并且能够描述本公开的实施方案的特定细节。然而,本领域的技术人员应了解,本公开可以在没有这些细节的情况下实施。在其它情况下,众所周知的结构和功能并未详细地示出或描述以避免不必要地模糊本公开的实施方案的描述。
心脏重塑可以在临床上表现为在心脏损伤或应力后心脏的尺寸、形状以及功能的变化。用以评价左心室重塑的量度包括心脏尺寸、形状和质量、射血分数、舒张末期和收缩末期容积以及峰值力收缩。心脏重塑可以描述为可以在心肌梗塞、心脏缺血、压力超负荷(主动脉狭窄、高血压)、发炎性心肌疾病(心肌炎)、特发性扩张型心肌病或容积超负荷(瓣膜反流)之后发生的生理病状。心脏对如高血压和主动脉狭窄中的持续负荷增加的反应导致超负荷腔室中的肌肉质量增加。
作为损伤或应力的结果,肌细胞数目减少并且存活的肌细胞作为初始补偿过程的一部分变得伸长或肥大以在收缩性组织损失之后维持心搏量。心室壁的厚度也增大。成纤维细胞当由应力或损伤活化时通过增加胶原蛋白合成,从而引起心室的纤维化来促成重塑。
重塑的常见情形是在心肌梗塞或急性缺血之后。存在心脏的心肌坏死(细胞死亡)和不成比例的变薄。这种薄的削弱区域不能以与其它健康组织相同的方式经受住心脏上的压力和容积负荷。因此,存在由梗塞区引起的腔室扩张。在心肌梗塞之后的初始重塑期引起坏死区域和心肌疤痕的修复,这在一定程度上可以被视为有益的,因为存在左心室功能和心输出量的改善或维持。经过一段时间,随着心脏经历进行中的重塑,其变得不太像椭圆形并且更像球形。心室质量和容积增加,其一起不利地影响心脏功能。最终,舒张功能或心脏在收缩之间松弛的能力可能变得受损,进一步引起衰退。
在McKinsey中总结的先前报道显示MEF2的转录活性响应心脏中的病理应力而上调,继而诱导心脏重塑(McKinsey,2011)。在小鼠心脏中组成活性形式的MEF2的异位过度表达引起扩张型心肌病(McKinsey,2011)。在培养的大鼠心肌细胞中HDAC4或HDAC9的异位过度表达协调地抑制MEF2依赖性转录和激动剂依赖性心脏肥大。相比之下,小鼠中编码HDAC9的基因的破坏导致心脏MEF2活性的超活化,并且敲除HDAC5或HDAC9基因的小鼠响应压力超负荷发展过大的心脏肥大并且随着年龄的增长发展自发的病理性肥大。在McKinsey中总结的这些先前报道显示IIa类HDAC通过结合MEF2并压制MEF2依赖性转录而作为心脏肥大的内源抑制剂。
给出这种背景知识下,并不预期本文所公开的化合物减少或抑制心脏重塑,因为Jayathiliaka先前报道了本文所公开的化合物破坏MEF2结合至IIa类HDAC(Jayathiliaka,2012)。Jayathiliaka先前报道了化合物促使IIa类HDAC从细胞核重定位至细胞质中。在细胞质中,IIa类HDAC可能不再抑制位于细胞的细胞核中的MEF2。如果化合物破坏MEF2结合至IIa类HDAC,那么MEF2依赖性转录将不再受IIa类HDAC压制,而替代地将上调。上调的MEF2依赖性转录诱导心脏重塑。因此,预测本文所公开的化合物诱导或增加心脏重塑而不是抑制心脏重塑,因为其破坏IIa类HDAC对MEF2依赖性转录的压制。
本文中的某些实施方案涉及本文在下面的实施例中提供的意想不到的结果,这些实施例显示本文所公开的化合物如何显著降低心脏重塑的作用。令人惊讶的是,本文所公开的化合物的卤索取代基与另一种类BML-210或类PAOA化合物相比引起血清刺激的新生大鼠心室肌细胞中肌细胞的细胞尺寸显著减小(数据未公开)。
I.化合物
在一个实施方案中,可以在本文所公开的方法中使用的一种或多种化合物可以包含7MI或8MI的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物。
在另一个实施方案中,本文所公开的一种或多种化合物可以包含式I的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物,其中:
A和B环独立地选自由苯基和吡啶基环组成的群组;
R1-R5各自独立地选自由氢和卤素组成的群组;
X1和X2各自独立地选自-NHC(=O)-或-C(=O)-NH-;并且
L1是-(CH2)n-,其中n是4、5或6。
在一些实施方案中,-X1-L1-X2-是-NHC(=O)-L1-C(=O)NH-。
在一些实施方案中,-X1-L1-X2-是-C(=O)-NH-L1-C(=O)NH-。
在一些实施方案中,R3、R4以及R5中的至少一者是卤素(例如,Cl、Br以及F)。
在一些实施方案中,A是苯基环并且B是吡啶基环。
在一些实施方案中,A是苯基环,B是吡啶基环,R1-R3以及R5是氢,并且R4是卤素(例如,Cl、Br以及F)。
在一些实施方案中,A是苯基环,B是吡啶基环,R1、R2、R4以及R5是氢,并且R3是卤素(例如,Cl、Br以及F)。
在另一个实施方案中,本文所公开的一种或多种化合物可以包含式II的结构:
包括其医药学上可接受的溶剂化物、医药学上可接受的前药、医药学上可接受的盐以及医药学上可接受的立体异构体,并且进一步包括其所有比率的混合物,其中R1-R5、X1、X2以及L1与上文一样定义。
在一些实施方案中,R3、R4以及R4中的至少一者是卤素(例如,Cl、Br以及F)。
在一些实施方案中,-X1-L1-X2-是-NHC(=O)-L1-C(=O)NH-。
在一些实施方案中,-X1-L1-X2-是-C(=O)-NH-L1-C(=O)NH-。
除非另有规定,否则所有取代基意图包括任选地被取代的取代基,即,进一步被取代或未被取代。
在一些实施方案中,本文所公开的一种或多种化合物可以抑制MEF2乙酰化。
在一些实施方案中,本文所公开的一种或多种化合物可以抑制IIa类HDAC的功能。
在一些实施方案中,本文所公开的一种或多种化合物可以促使IIa类HDAC从细胞的细胞核重定位至细胞质。
在一些实施方案中,本文所公开的一种或多种化合物对于HDAC6抑制可以具有大于50μM的IC50。
在一些实施方案中,与HDAC1相比,一种或多种化合物可以优先或选择性地抑制HDAC3。
在一些实施方案中,一种或多种化合物在检测HeLa细胞核提取物中总组蛋白脱乙酰化的抑制的检验中可以具有大于0.5μM的IC50。
令人惊讶的是,本文所公开的化合物似乎比泛HDAC抑制剂毒性更小。实施例2和4中的实验结果展示,小鼠可以耐受100mg/kg的8MI日剂量持续四周而没有肾或肝病的任何征象或者其它不良作用。相比之下,在小鼠中对于TSA先前所报道的耐受日剂量是1mg/kg并且并非所有小鼠都存活。较弱的HDAC抑制活性以及抑制某些HDAC的优先性或特异性可能促成本文所公开的化合物的优良毒性型态。
具有7MI、8MI、式I以及式II的结构式的化合物在肝中比曲古抑菌素A(TSA)或BML-210显著地代谢更稳定(参看实施例11和图11):
尽管BML-210与7MI和8MI的结构是相关的,但苯环上的卤素取代基经过一段时间与BML-210相比令人惊讶地增加7MI和8MI在肝中的代谢稳定性(图11)。因此,庚二酰苯胺类邻氨基酰苯胺化合物上的卤素取代基意想不到地并且显著地增强药物的生物利用度并且降低CYP介导的药物-药物相互作用的可能性。类似地,7MI和8MI在肝中与TSA相比也显著地代谢更稳定。
如本文所用的“医药学上可接受的”的化合物或组合物适合用于与生物受试者的组织或器官接触而没有过度的毒性、刺激性、过敏反应、免疫原性或者其它问题或并发症,与合理的效益/风险比相称。如果所述化合物或组合物将要与其它成分一起使用,那么所述化合物或组合物也与所述其它成分相容。
如本文所用的术语“溶剂化物”指的是由溶质(例如,本文所公开的化合物)和溶剂形成的可变化学计量的复合物。用于本发明的目的的这类溶剂可能不干扰溶质的生物活性。适合溶剂的实例包括(但不限于)水、水溶液(例如,缓冲液)、甲醇、乙醇以及乙酸。优选地,所使用的溶剂是医药学上可接受的溶剂。适合的医药学上可接受的溶剂的实例包括(但不限于)水、水溶液(例如,缓冲液)、乙醇以及乙酸。适合溶剂化物的实例是根据本发明的化合物的单水合物或二水合物或醇化物。
如本文所用的化合物的医药学上可接受的盐指的是化合物(例如,本文所公开的化合物)的任何医药学上可接受的酸和/或碱加成盐。
适合的酸包括有机和无机酸。适合的碱包括有机和无机碱。适合无机酸的实例包括(但不限于):盐酸、氢氟酸、氢溴酸、氢碘酸、硫酸以及硼酸。适合有机酸的实例包括(但不限于):乙酸、三氟乙酸、甲酸、草酸、丙二酸、琥珀酸、酒石酸、马来酸、富马酸、甲磺酸、三氟甲磺酸、苯甲酸、乙醇酸、乳酸、柠檬酸以及扁桃酸。适合无机碱的实例包括(但不限于):氨、羟乙胺以及肼。适合有机碱的实例包括(但不限于)甲胺、乙胺、三甲胺、三乙胺、乙二胺、羟乙胺、吗啉、哌嗪以及胍。本发明进一步提供了本文所描述的所有化合物的水合物和多晶型物。
II.组合物
本文所公开的化合物可以含有一个或多个手性原子,或可以按其它方式能够作为两个或更多个立体异构体存在,其通常是对映体和/或非对映体。因此,包含本文所公开的化合物的组合物可以包括立体异构体的混合物或对映体的混合物,以及纯化的立体异构体、纯化的对映体、立体异构体富集的混合物或对映体富集的混合物。本文所提供的组合物还包括由上文所描述的结构表示的化合物的个别异构体以及其任何全部或部分平衡的混合物。本文所公开的组合物还涵盖由上文所描述的结构表示的化合物的个别异构体与其一个或多个手性中心反转的异构体的混合物。而目,应了解,上文所描述的结构的所有互变异构体和互变异构体的混合物包括于这些结构的范围内并且优选其所对应的结构。
所获得的外消旋体可以通过本身已知的方法机械地或化学地拆分成异构体。非对映体优选地从外消旋混合物通过与光学活性拆分剂反应而形成。适合拆分剂的实例是光学活性酸,诸如酒石酸、二乙酰基酒石酸、二苯甲酰基酒石酸、扁桃酸、苹果酸、乳酸或各种光学活性樟脑磺酸(诸如樟脑磺酸)的D和L形式。还有利的是借助于用光学活性拆分剂填充的柱的对映体拆分。非对映体拆分也可以通过标准纯化工艺来进行,诸如色谱法或分步结晶。
还可能通过上文所描述的方法经由使用已经是光学活性的起始物质获得包含本文所公开的化合物的结构的光学活性化合物。
III.医药配方
如本文所用的医药配方包含治疗有效量的本文所公开的化合物或其组合物中的一者或多者。在某些实施方案中,医药配方进一步包含医药学上可接受的载剂。
如本文所用的“治疗有效量”、“治疗有效浓度”或“治疗有效剂量”是如下量:如与尚未接受这种量的对应受试者相比,其使得治疗、治愈、预防改良,或疾病、病症或副作用改善,或疾病或病症的进展速率下降。
这种量将取决于多种因素而变化,包括(但不限于)化合物、其组合物或医药配方的特征(包括其活性、药物动力学、药效学以及生物利用度)、所治疗的受试者(包括年龄、性别、疾病类型和期数、一般身体状况、对给定剂量的响应性以及药物的类型)或细胞的生理状况、配方中医药学上可接受的载剂的性质,以及施用途径。此外,有效或治疗有效量可以取决于化合物、其组合物或医药配方单独还是与其它药物、其它疗法或其它治疗方法或模态组合施用而变化。临床和药理学领域的技术人员将能够经由常规实验,即通过监测细胞或受试者对施用一种或多种化合物、其组合物或医药配方的反应并且相应地调节剂量来确定有效量或治疗有效量。典型剂量可以在约0.1mg/kg至约100mg/kg或更大的范围内,这取决于上文所提及的因素。在其它实施方案中,剂量可以在约0.1mg/kg至约100mg/kg;或约1mg/kg至约100mg/kg;或约5mg/kg至约100mg/kg的范围内。对于额外指导,参看《雷明顿:药剂学科学与实践(Remington:The Science and Practice of Pharmacy)》,第21版,Univ.of Sciences in Philadelphia(USIP),Lippincott Williams&Wilkins,Philadelphia,PA,2005,其特此以引用的方式并入,如同在本文中完整阐述用于确定治疗有效量的额外指导一样。
如本文所用的术语“约”指的是±10%、±5%或±1%的在“约”之后的值。
“医药学上可接受的载剂”是医药学上可接受的材料、组合物或媒剂,诸如液体或固体填充剂、稀释剂、赋形剂、溶剂或囊封材料,其涉及携带或运输活性成分从一个位置、体液、组织、器官(内部或外部)或身体部分至另一个位置、体液、组织、器官或身体部分。每种载剂在与配方的其它成分,例如本文所描述的化合物或其它成分相容的意义上是“医药学上可接受的”并且适合用于与生物受试者的组织或器官接触而没有过度的毒性、刺激性、过敏反应、免疫原性或者其它问题或并发症,与合理的效益/风险比相称。
医药学上可接受的载剂在本领域中是众所周知的并且包括(但不限于)(1)糖,诸如乳糖、葡萄糖以及蔗糖;(2)淀粉,诸如玉米淀粉和马铃薯淀粉;(3)纤维素和其衍生物,诸如羧甲基纤维素钠、乙基纤维素以及乙酸纤维素;(4)粉末状黄蓍胶;(5)麦芽;(6)明胶;(7)滑石;(8)赋形剂,诸如可可脂和栓剂蜡;(9)油,诸如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油以及大豆油;(10)二元醇,诸如丙二醇;(11)多元醇,诸如甘油、山梨糖醇、甘露糖醇以及聚乙二醇;(12)酯,诸如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,诸如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液(Ringer′s solution);(19)醇,诸如乙醇和丙醇;(20)磷酸盐缓冲溶液;以及(21)在医药配方中所采用的其它无毒相容性物质。
本文所公开的医药配方可以含有如适当的生理状况所需的医药学上可接受的辅助物质,诸如pH调节和缓冲剂、毒性调节剂等等,例如乙酸钠、氯化钠、氯化钾、氯化钙、乳酸钠等等。
医药配方中本文所公开的一种或多种化合物的浓度可以广泛变化,并且将主要基于流体体积、粘度、体重等等根据所选的特定施用模式和生物受试者的需要而选择。举例来说,本文所公开的化合物的浓度可以为约0.0001%至约100%、约0.001%至约50%、约0.01%至约30%、约0.1%至约20%、或约1%至约10%wt。
可以考虑到所选的施用模式以及化合物的物理和化学特性来选择适合的医药学上可接受的载剂。
本领域的技术人员应认识到,含有本文所公开的一种或多种化合物或其组合物的医药配方可以通过各种途径施用于受试者,这些途径包括(但不限于)经口或肠道外,诸如静脉内。组合物还可以经由皮下注射、皮下包埋、胃内、局部和/或阴道施用来施用。组合物还可以通过注射或插管来施用。
在一个实施方案中,医药载剂可以是液体并且医药配方将呈溶液的形式。在另一个实施方案中,医药学上可接受的载剂是固体并且医药配方呈粉末、片剂、丸剂或胶囊的形式。在另一个实施方案中,医药载剂是凝胶并且医药配方呈栓剂或乳膏的形式。
固体载剂可以包括一种或多种物质,其也可以充当调味剂、润滑剂、增溶剂、悬浮剂、填充剂、助流剂、压缩助剂、粘合剂或片剂崩解剂,其也可以是囊封材料。在粉末中,载剂是细碎的固体,其与细碎的活性成分混合。在片剂中,活性成分与具有必需的压缩特性的载剂以适合的比例混合并且以所需的形状和尺寸压实。粉末和片剂优选地含有高达约99%的本文所公开的一种或多种化合物。适合的固体载剂包括例如磷酸钙、硬脂酸镁、滑石、糖、乳糖、糊精、淀粉、明胶、纤维素、聚乙烯吡咯烷酮、低熔点蜡以及离子交换树脂。
除了含有有效量的本文所描述的一种或多种化合物或其组合物以外,本文所提供的医药配方还可以包括适合的稀释剂、防腐剂、增溶剂、乳化剂、佐剂和/或载剂。
医药配方可以按无菌溶液或悬浮液的形式施用,其含有其它溶质或悬浮剂,例如,使溶液等渗的足够盐水或葡萄糖、胆汁盐、阿拉伯胶、明胶、单油酸脱水山梨糖醇、聚山梨醇酯80(与环氧乙烷共聚的山梨糖醇和其酸酐的油酸酯)等等。
额外的医药配方将为本领域的技术人员显而易见,包括涉及持续或控制递送配方中的结合剂分子的配方。用于配制多种其它持续或控制递送工具,诸如脂质体载剂、生物溶蚀性微粒或多孔小珠以及积存注射剂的技术也为本领域的技术人员所知。参看例如PCT/US93/0082948,其以引用的方式并入本文中,如同在本文中完整阐述用于递送医药配方的多孔聚合微粒的控制释放的技术一样。持续释放制剂的额外实例包括呈成形物品的形式的半渗透聚合物基质,例如膜或微胶囊。持续释放基质可以包括聚酯、水凝胶、聚乳酸、L-谷氨酸和L-谷氨酸γ-乙酯的共聚物、聚(甲基丙烯酸2-羟乙酯)、乙烯乙酸乙烯酯或聚-D-(-)-3-羟基丁酸。持续释放组合物还包括脂质体,其可以通过本领域中已知的若干方法中的任一者制备。
IV.治疗方法
本发明的一个方面涉及一种治疗受试者的心脏重塑的方法,其包括向受试者施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的心脏重塑的药物。
在一些实施方案中,心脏重塑可以表现为心脏收缩力减小、心脏后壁的厚度增大和/或心室质量增加。在一些实施方案中,心脏重塑可以表现为心脏纤维化、肌细胞肥大、肌细胞坏死、肌细胞凋亡、成纤维细胞增殖增加和/或纤维状胶原蛋白增加。
在一些实施方案中,心脏重塑可以表现为一种或多种症状,其独立地选自由以下组成的群组:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、左心室(LV)舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
本发明的另一个方面涉及一种改善受试者的心脏功能的方法,其包括向受试者施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以改善受试者的心脏功能的药物。
在一些实施方案中,心脏功能可以通过增强心脏收缩力来改善。在某个实施方案中,心脏功能可以通过减少受试者的心脏纤维化来改善。在一些实施方案中,心脏功能可以通过减小心脏后壁的厚度来改善。在一些实施方案中,心脏功能可以通过减少心室质量来改善。在一些实施方案中,心脏功能可以通过改善左或右心室的舒张和/或收缩功能来改善。在其它实施方案中,心脏功能可以通过增加心搏量、缩短分数和/或射血分数来改善。在某个实施方案中,心脏功能可以通过减小LV舒张期和/或收缩期直径来改善。在一些实施方案中,心脏功能可以通过减小LV舒张末期压力来改善。在一些实施方案中,心脏功能可以通过减小LV收缩末期和/或舒张末期容积来改善。在某些实施方案中,心脏功能可以通过减小心室壁应力和/或心室壁张力来改善。
在一些实施方案中,心脏功能可以通过降低循环B型利钠肽(BNP)水平来改善。编码B型利钠肽的基因的表达在心室肌细胞中在病理性心脏肥大期间增强,并且循环BNP水平在临床上用作心脏衰竭的替代量度。在一些实施方案中,心脏功能可以通过减少α-肌球蛋白重链和/或β-肌球蛋白重链的表达来改善。
本发明的另一个方面涉及一种治疗受试者的心脏纤维化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的心脏纤维化的药物。
本发明的另一个方面涉及一种治疗受试者的左心室功能障碍的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的左心室功能障碍的药物。
在一些实施方案中,左心室功能障碍可以表现为一种或多种症状,其独立地选自由以下组成的群组:左心室的舒张功能减小、左心室的收缩功能减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、LV收缩期直径增大、LV舒张末期压力增大、LV收缩期容积增大、LV舒张期容积增大和/或LV质量增加。
本发明的另一个方面涉及一种治疗受试者的右心室功能障碍的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的右心室功能障碍的药物。
在一些实施方案中,右心室功能障碍可以表现为一种或多种症状,其独立地选自由以下组成的群组:右心室的舒张功能减小、右心室的收缩功能减小、心搏量减小、缩短分数减小、射血分数减小、右心室(RV)舒张期直径增大、RV收缩期直径增大、RV舒张末期压力增大、RV收缩期容积增大、RV舒张期容积增大和/或RV质量增加。
本发明的另一个方面涉及一种治疗受试者的心脏肥大的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗受试者的心脏肥大的药物。
本发明的另一个方面涉及一种抑制受试者的肌细胞凋亡的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制受试者的肌细胞凋亡的药物。
本发明的另一个方面涉及一种抑制表现心脏重塑症状的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制表现心脏重塑症状的受试者的MEF2乙酰化的药物。
在一些实施方案中,症状可以是一种或多种症状,其独立地选自包含以下的群组:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
本发明的另一个方面涉及一种抑制具有左心室功能障碍的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制具有左心室功能障碍的受试者的MEF2乙酰化的药物。
本发明的另一个方面涉及一种抑制具有心脏纤维化的受试者的MEF2乙酰化的方法,其包括施用治疗有效量的本文所公开的一种或多种化合物、组合物或医药配方。另一个实施方案涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以抑制具有心脏纤维化的受试者的MEF2乙酰化的药物。
在涉及本文所公开的所有方法的一些实施方案中,受试者可以具有独立地选自由以下组成的群组的一者或多者:左心室的舒张功能减小、左心室的收缩功能减小、心脏收缩力减小、心搏量减小、缩短分数减小、射血分数减小、LV舒张期直径增大、左心室收缩期直径增大、LV舒张末期压力增大、心室壁应力增大、心室壁张力增大、LV收缩期容积增大、LV舒张期容积增大、心室质量增加以及心脏后壁的厚度增大。
在涉及本文所公开的所有方法的一些实施方案中,受试者可以已经诊断患有一种或多种病状,其独立地选自由以下组成的群组:心脏纤维化、高血压、主动脉狭窄、心肌梗塞、心肌炎、心肌病、瓣膜反流、瓣膜病、左心室功能障碍、心脏缺血、舒张期功能障碍、慢性心绞痛、心动过速以及心动过缓。
在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中B型利钠肽(BNP)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中心房利钠肽(ANP)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中α-肌球蛋白重链(α-MHC)的表达。在涉及此处所公开的所有方法的一些实施方案中,种或多种化合物可以抑制肌细胞中β-肌球蛋白重链(β-MHC)的表达。在涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中肌质网(内质网)Ca2+-ATPase(SERCA)的表达。涉及此处所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制肌细胞中I型胶原蛋白(Col 1)或3型胶原蛋白(Col 3)的表达。
在涉及本文所公开的所有方法的一些实施方案中,一种或多种化合物可以抑制MEF2乙酰化。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物可以促使IIa类HDAC从细胞核重定位至细胞质中。在涉及本文所论述的所有方法的其它实施方案中,一种或多种化合物可以抑制MEF2结合至其辅因子(即,IIa类HDAC)。
在涉及本文所公开的所有方法的一些实施方案中,一种或多种化合物对于HDAC6抑制可以具有大于50μM的IC50。在涉及本文所论述的所有方法的一些实施方案中,与HDAC1相比,一种或多种化合物可以优先或选择性地抑制HDAC3。在涉及本文所论述的所有方法的一些实施方案中,一种或多种化合物对于HDAC抑制可以具有在检测HeLa细胞核提取物中总组蛋白脱乙酰化的抑制的检验中测定的大于1μM的IC50。在涉及本文所论述的所有方法的其它实施方案中,一种或多种化合物对于HDAC抑制可以具有在检测HeLa细胞核提取物中总组蛋白脱乙酰化的抑制的检验中测定的大于0.5μM的IC50。
在涉及本文所公开的所有方法的一些实施方案中,施用可以包括一种或多种化合物的经口施用。如实施例11中所说明,8MI在肝中比BML-210或TSA更稳定,从而增加其在经口施用的剂量中的生物利用度和有效性。
在涉及本文所公开的所有方法的一些实施方案中,施用可以包括静脉内施用。
将要施用的最佳剂量可以由本领域的技术人员确定,并且将随着所使用的特定化合物、组合物或配方、制剂的强度、施用模式以及疾病病状的进展而变化。取决于所治疗的特定受试者的额外因素包括(但不限于)受试者的年龄、体重、性别、饮食、施用时间、施用的时间和频率、药物组合、反应敏感度以及对疗法的响应。化合物、组合物或医药配方的施用可以连续地或间歇地实现。在任何治疗方案中,化合物、组合物或医药配方可以单独地或在混合液中施用于受试者,这种混合液含有两种或更多种化合物或其组合物、其它治疗剂、组合物等等,包括(但不限于)耐受诱导剂、增效剂以及副作用缓解剂。所有这些药剂在普遍接受的有效剂量范围内施用,诸如《医师案头参考(Physician′s Desk Reference)》,第41版,Publisher Edward R.Barnhart,N.J.(1987)中所公开的那些,其以引用的方式并入本文中,如同在本文中完整阐述一样。在某些实施方案中,适当的剂量水平一般将为每天每公斤受试者体重约0.001至约50mg,其可以按单次或多次剂量施用。优选地,剂量水平将为每天约0.005至约25mg/kg;更优选地每天约0.01至约10mg/kg;并且甚至更优选地每天约0.05至约1mg/kg。在一些实施方案中,日剂量可以介于约10-6g/kg至约5g/kg体重之间。
病状的“治疗(treat/treatment)”可以指的是预防病状,减缓病状的发作或发展速率,降低发展病状的风险,预防或延迟与病状相关的症状的发展,减轻或终止与病状相关的症状,产生病状的完全或部分消退,或其某种组合。
在一些实施方案中,本文所公开的一种或多种化合物或其组合物或医药配方可以与一种或多种额外治疗剂组合在本文所提供的方法中施用。如本文所用的“组合”或“与……组合”意指在治疗相同受试者的相同心脏肥大的过程中按任何次序使用两种或更多种药剂、药物、治疗方案、治疗模态或其组合。这包括同时施用(在相同或独立的配方中),以及按隔开至多数天的时间上间隔的次序施用。这种组合治疗还可以包括药剂、药物、治疗方案或治疗模态中的任一者或多者的多于单次施用。此外,两种或更多种药剂、药物、治疗方案、治疗模态或其组合的施用可以通过相同或不同的施用途径。
可以与本文所公开的化合物或其组合物或医药配方组合施用的治疗剂的实例包括(但不限于)β-肾上腺素能受体阻断剂、抗高血压药、芳氧基烷酸/纤维酸衍生物、树脂/胆汁酸螯合剂、HMG CoA还原酶抑制剂、烟酸衍生物、甲状腺激素和类似物、抗高脂蛋白血症药、抗动脉硬化药、抗血栓形成/纤维蛋白溶解剂、抗凝剂、抗血小板剂、血栓溶解剂、促凝血剂、抗凝剂拮抗剂、血栓溶解剂拮抗剂和抗血栓形成剂、抗心律失常剂、钠通道阻断剂、β阻断剂、复极化延长剂、钙通道阻断剂/拮抗剂、抗心律失常剂、α阻断剂、α/β阻断剂、抗血管紧张素II剂、交感神经阻滞药、血管舒张药、血管加压药、充血性心脏衰竭的治疗剂、后负荷-前负荷降低剂、利尿剂、变力剂和/或抗心绞痛剂。
在另一个实施方案中,治疗剂是抗癌剂。可以根据本文所描述的某些实施方案使用的抗癌剂通常在性质上是细胞毒性或细胞抑制的并且可以包括(但不限于)烷化剂;抗代谢物;抗肿瘤抗生素;拓扑异构酶抑制剂;有丝分裂抑制剂;激素(例如,皮质类固醇);靶向治疗剂(例如,选择性雌激素受体调节剂(SERM));毒素;免疫佐剂、免疫调节剂以及其它免疫治疗剂(例如,治疗抗体和其片段、重组细胞因子以及免疫刺激分子-合成的或来自完整微生物或微生物组分);酶(例如,使前药在肿瘤部位裂解成细胞毒性剂的酶);核酸酶;反义寡核苷酸;核酸分子(例如,mRNA分子、cDNA分子或RNAi分子,诸如siRNA或shRNA);螯合剂;硼化合物;光活性剂和染料。可以根据本公开的某些实施方案用作治疗剂的抗癌剂的实例包括(但不限于)13-顺式维甲酸(13-cis-retinoic acid)、2-氯脱氧腺苷、5-阿扎胞苷(5-azacitidine)、5-氟尿嘧啶、6-巯基嘌呤、6-硫鸟嘌呤、放线菌素D(actinomycin-D)、阿霉素(adriamycin)、阿地白介素(aldesleukin)、阿利维甲酸(alitretinoin)、全反式维甲酸、α干扰素、六甲蜜胺(altretamine)、氨甲蝶呤(amethopterin)、氨磷汀(amifostine)、阿那格雷(anagrelide)、阿那曲唑(anastrozole)、阿糖胞嘧啶(arabinosylcytosine)、三氧化二砷、安吖啶(amsacrine)、氨基喜树碱(aminocamptothecin)、氨鲁米特(aminoglutethimide)、天冬酰胺酶、氮杂胞苷、卡介苗(bacillus calmette-guerin,BCG)、苯达莫司汀(bendamustine)、贝沙罗汀(bexarotene)、比卡鲁胺(bicalutamide)、硼替佐米(bortezomib)、博莱霉素(bleomycin)、白消安(busulfan)、甲酰四氢叶酸钙(calcium leucovorin)、嗜橙菌因子(citrovorum factor)、卡培他滨(capecitabine)、卡奈替尼(canertinib)、卡铂(carboplatin)、卡莫司汀(carmustine)、苯丁酸氮芥(chlorambucil)、顺铂(cisplatin)、克拉屈滨(cladribine)、可的松(cortisone)、环磷酰胺、阿糖孢苷(cytarabine)、阿法达贝泊汀(darbepoetin alfa)、达沙替尼(dasatinib)、道诺霉素(daunomycin)、地西他滨(decitabine)、地尼白介素(denileukin diftitox)、地塞米松(dexamethasone)、德克塞索恩(dexasone)、右雷佐生(dexrazoxane)、放线菌素D(dactinomycin)、柔红霉素(daunorubicin)、达卡巴嗪(decarbazine)、多烯紫杉醇(docetaxel)、多柔比星(doxorubicin)、脱氧氟尿苷(doxifluridine)、恩尿嘧啶(eniluracil)、表柔比星(epirubicin)、阿法依泊汀(epoetin alfa)、埃罗替尼(erlotinib)、依维莫司(everolimus)、依西美坦(exemestane)、雌莫司汀(estramustine)、依托泊苷(etoposide)、非格司亭(filgrastim)、氟甲睾酮(fluoxymesterone)、氟维司群(fulvestrant)、夫拉平度(flavopiridol)、氟尿苷(floxuridine)、氟达拉滨(fludarabine)、氟尿嘧啶(fluorouracil)、氟他胺(flutamide)、吉非替尼(gefitinib)、吉西他滨(gemcitabine)、奥佐米星(ozogamicin)、戈舍瑞林(goserelin)、粒细胞集落刺激因子、粒细胞巨噬细胞集落刺激因子、六甲蜜胺(hexamethylmelamine)、氢化可的松(hydrocortisone)、羟基脲、干扰素α、白介素-2、白介素-11、异维甲酸(isotretinoin)、伊沙匹隆(ixabepilone)、伊达比星(idarubicin)、甲磺酸伊马替尼(imatinib mesylate)、异环磷酰胺(ifosfamide)、伊立替康(irinotecan)、拉帕替尼(lapatinib)、来那度胺(lenalidomide)、来曲唑(letrozole)、甲酰四氢叶酸(leucovorin)、亮丙瑞林(leuprolide)、脂质体Ara-C、洛莫司汀(lomustine)、二氯甲基二乙胺(mechlorethamine)、甲地孕酮(megestrol)、美法仑(melphalan)、颈基嘌呤、美司那(mesna)、甲氨蝶呤(methotrexate)、甲基泼尼松龙(methylprednisolone)、丝裂霉素C(mitomycin C)、米托坦(mitotane)、米托蒽醌(mitoxantrone)、奈拉滨(nelarabine)、尼鲁米特(nilutamide)、奥曲肽(octreotide)、奥普瑞白介素(oprelvekin)、奥沙利铂(oxaliplatin)、太平洋紫杉醇(paclitaxel)、帕米膦酸钠(pamidronate)、培美曲塞(pemetrexed)、PEG干扰素、培门冬酶(pegaspargase)、培非格司亭(pegfilgrastim)、PEG-L-天冬酰胺酶、喷司他丁(pentostatin)、普卡霉素(plicamycin)、泼尼松龙(prednisolone)、强的松(prednisone)、丙卡巴肼(procarbazine)、雷洛昔芬(raloxifene)、罗米司亭(romiplostim)、雷替曲塞(ralitrexed)、沙帕他滨(sapacitabine)、沙格司亭(sargramostim)、沙铂(satraplatin)、索拉非尼(sorafenib)、舒尼替尼(sunitinib)、司莫司汀(semustine)、链脲菌素(streptozocin)、他莫昔芬(tamoxifen)、替加氟(tegafur)、替加氟-尿嘧啶、替西罗莫司(temsirolimus)、替莫唑胺(temozolamide)、替尼泊苷(teniposide)、沙利度胺(thalidomide)、硫鸟嘌呤(thioguanine)、噻替哌(thiotepa)、拓扑替康(topotecan)、托瑞米芬(toremifene)、维甲酸(tretinoin)、三甲曲沙(trimitrexate)、阿鲁比星(alrubicin)、长春新碱(vincristine)、长春碱(vinblastine)、长春地辛(vindestine)、长春瑞滨(vinorelbine)、伏立诺他(vorinostat)以及唑来膦酸(zoledronic acid)。
可以根据本公开的某些实施方案用作抗癌剂的治疗抗体和其功能片段包括(但不限于)阿仑单抗(alemtuzumab)、贝伐单抗(bevacizumab)、西妥昔单抗(cetuximab)、依决洛单抗(edrecolomab)、吉妥珠单抗(gemtuzumab)、替伊莫单抗(ibritumomab tiuxetan)、帕尼单抗(panitumumab)、利妥昔单抗(rituximab)、托西莫单抗(tositumomab)和曲妥珠单抗(trastuzumab)以及与本文所列的特定疾病相关的其它抗体。
可以根据本公开的某些实施方案用作抗癌剂的毒素包括(但不限于)蓖麻毒素、相思豆毒素、核糖核酸酶(RNase)、DNase I、葡萄球菌肠毒素A、美洲商陆抗病毒蛋白、白树毒素(gelonin)、白喉毒素、假单胞菌外毒素以及假单胞菌内毒素。
可以根据本公开的某些实施方案用作治疗剂的放射性同位素包括(但不限于)32p、89Sr、90Y、99mTc、99Mo、131I、153Sm、177Lu、186Re、213Bi、223Ra以及225Ac。
给药频率将取决于所使用的医药配方中的治疗剂(例如,本文所公开的一种或多种化合物)的药物动力学参数。通常,施用医药配方直至达到达成所需作用的剂量。配方可以因此以单次剂量,或经过一段时间以多次剂量(在相同或不同的浓度/剂量下),或以连续输注来施用。常规地进行适当剂量的进一步细化。适当剂量可以经由使用适当的剂量反应数据来确定。长效医药配方可以取决于特定配方的半衰期和清除速率每3至4天、每周或每两周施用。
另一个方面涉及本文所公开的一种或多种化合物或其组合物或医药配方的用途,其用于制造用以治疗由一个或多个转录因子和/或辅因子可调控的病状的药物。对于这个方面,一种或多种化合物或其组合物或医药配方、转录因子和/或辅因子以及由转录因子和/或辅因子可调控的病状与上文所公开的相同,并且病状的治疗与前文所描述的相同。
除非上下文另有明确要求,否则贯穿描述和权利要求书,词语“包含”等等应以包括性的意义(就是说,以“包括(但不限于)”的意义)解释,与排他的或详尽的意义相反。词语“本文”、“上文”、“下文”、“前文”以及类似含义的词语当在本申请中使用时,指的是作为整体的本申请并且不是指本申请的任何特定部分。在上下文允许的情况下,上述具体实施方式中使用单数或复数的词语还可以分别包括复数或单数。关于两个或更多个项目的清单的词语“或”以及“和/或”涵盖这个词语的所有以下解释:清单中的任一项目、清单中的所有项目以及清单中的项目的任何组合。
以下实施例意图说明本发明的各种实施方案。这样的话,所论述的特定实施方案不应解释为限制本发明的范围。本领域的技术人员将显而易见,在不脱离本发明的范围的情况下可以作出各种等效物、变化以及修改,并且应了解,这类等效实施方案应包括于本文中。此外,本公开中所引用的所有参考文献特此以全文引用的方式并入,如同在本文中完整阐述一样。
实施例
实施例1:7MI和8MI抑制体外心肌细胞肥大
缺乏被p300乙酰化的能力的两个不同MEF2突变体构建体Mut1和Mut2用作MEF2信号传导的有效中断的阳性对照。在p300存在下这些突变体中的任一者而不是野生型MEF2(WT)的转染完全阻断去甲肾上腺素诱导的心肌细胞肥大(图1)。
接下来,测试7MI和8MI抑制体外肥大的能力(图2A)。许多激动剂,包括α1-肾上腺素能化合物(诸如去甲肾上腺素)、血管紧张素II以及生长因子(包括IGF-1),先前已经显示在本文所用的体外系统中诱导肥大。然而,含有多种丰富的生长因子的胎牛血清被选作心肌细胞生长可用的最稳固和多因子刺激物,原因在于将需要类似稳固和强力的抑制剂阻断这种肥大。用一定剂量范围的测试化合物对新生大鼠心室肌细胞(NRVM)的预处理以类似于其先前所观测的体外转录压制活性的效力次序减少血清刺激的肌细胞生长(图2B和末示出的数据)。总之,这些结果显示使用化合物7MI和8MI抑制心肌细胞中的MEF2活化足以响应狭窄的与广泛作用的生长信号来阻断肌细胞肥大。
实施例2:7MI和8MI抑制体内心肌细胞肥大
基于实施例1中的结果,在通过横向主动脉缩窄(TAC)产生的压力超负荷的体内检验中测试最强效的抑制剂(8MI)。TAC已经广泛地用于对高血压、主动脉瓣疾病以及其它类型的压力超负荷的临床肥大刺激建模。在野生型C57/B16中通过如Wei等2008中所描述建立右侧与左侧颈动脉的起点之间的横向主动脉的手术限制来建立体内压力超负荷。使对照同窝出生仔经受假手术。手术死亡率<5%。通过使用在右心房的水平上调零的Statham压力传感器(型号P23XL,Viggo-Spectramed,Oxnard,CA)从右侧和左侧颈动脉同时测量来确定跨主动脉梯度。如Wei等2008中所描述连续地记录压力。在手术之后按规定的时间间隔处死成对的TAC和对照动物并且移出心脏以供分析。
用8MI处理C57/B16小鼠两周,并且通过超声心动描记术评估心脏功能并且在处死后使用心脏重量/胫骨长度(HW/TL)的标准指数评估心脏质量。TAC使得在手术之后两周心脏质量显著增加>50%(图3A,0μg/g 8MI,亮灰条)。用8MI处理以剂量依赖性方式显著减弱这种增加(图3A,20μg/g和40μg/g 8MI,亮灰条)。TAC相关的肥大伴随有如左心室射血分数(LVEF)从约80%降至约50%所反映的收缩性心脏衰竭的发展(图3B,比较0μg/g 8MI,暗灰条(约80%)与0μg/g 8MI,亮灰条(约50%))。意想不到地,用8MI处理很大程度上预防这种功能受损,甚至在最低剂量下仍观察到有益作用(图3B,5μg/g、20μg/g以及40μg/g 8MI,亮灰条)。8MI在多种细胞的培养物中直至20μM未显示明显的毒性。每天用100mg/Kg 8MI处理持续四周的小鼠未显示肾或肝损伤的征象或者其它不良作用,表明8MI在动物模型中耐受良好。另外,在任一组中未观察到死亡率。
这些发现展示靶向MEF2活化以减少对血液动力学应力的肥大反应的效益。此外,这些结果显示通过这种机制减弱肥大在适应压力负荷期间不使收缩功能受损。实际上,显示相反的情况:阻断肥大性生长与改善的功能相关,这提供了靶向肥大以延迟或预防心脏衰竭的强有力的理论基础。
实施例3:MEF2乙酰化在经历心脏重塑的人类心脏中增加
在一系列人类左心室心肌样品中确定MEF2的乙酰化状态,这些样品代表没有心脏重塑或心脏衰竭症状的3个心脏(对照)以及显示心脏重塑和心脏衰竭症状的9个心脏。表1提供了对照心脏和9个有症状心脏的特征。
表1.所分析的人类受试者的特征
人类左心室心肌样品经由人类组织合作网(Cooperative Human Tissue Network)从匿名捐赠者获得并且维持于-80℃下直至使用。在死后4小时内收集组织。使样品均化,并且用抗乙酰基-赖氨酸抗体(Upstate,Charlottesville,Virginia,USA)使后续溶解产物免疫沉淀。电泳分离免疫沉淀物并且用抗MEF2抗体(Santa Cruz Biotechnology,Santa Cruz,CA,USA)和抗乙酰基-赖氨酸作为上样对照进行免疫墨点分析。代表性墨点示于图4A中。图4B中的图形以针对乙酰基-Lys标准化的密度计量单位(n.d.u.,标准化的密度计量单位)定量来自免疫墨点的数据。MEF2种类的乙酰化在显示心脏重塑症状的心脏样品中相对于对照心脏样品升高(图4B)。结果显示MEF2乙酰化在经历心脏重塑的心脏病状中增加。
实施例4:8MI预防体内心脏重塑
在中等压力超负荷的模型中进一步测试8MI对肥大的影响(图5A-5E)。在即将横向主动脉缩窄(TAC)之前和之后持续21天施用一定浓度范围的8MI或其媒剂(DMSO)。对2-3月龄的野生型C57/BL/6小鼠进行所有实验。如Wei等2008中所描述通过TAC诱导心脏肥大。通过脉冲波多普勒超声心动描记术在术后评估通过TAC诱导的压力梯度以确认所有动物中的等效梯度(45±5mmHg)。在手术介入前一天经由尾静脉注射递送8MI并且然后每天递送持续21天。在手术之后第21天在处死时获得血液样品,并且在80℃下冷冻血清直至分析。
曼森氏三色用于显现心脏四腔室解剖结构。石蜡包埋切片用于染色(图5B)。制备来自小鼠的心肌的代表性麦胚凝集素(WGA)染色切片。对于超声心动描记术(图5C),用40mg/kg氯胺酮(ketamine)和5mg/kg利多卡因(xylocaine)将小鼠置于麻醉下并且紧固于仰卧位。使用40赫兹传感器在Visual Sonics 770高分辨率成像系统上评估小鼠。在心室的短和长轴观中的B型用于评估心室的壁运动缺陷,并且在长轴观中的M型用于收缩期和舒张期的心室间间隔厚度、后壁厚度以及左心室尺寸。
苏木精和伊红(HE)以及FITC偶联的WGA(来自Invitrogen)用于评估心肌细胞尺寸(图5D和5E)。测量来自每种病状3只小鼠的至少4个心肌切片的细胞的尺寸(图5E)。用DAPI对WGA样品进行复染并且从DAPI和FITC通道合并图像。
在21天结束时,在媒剂处理的动物中,TAC诱导标准化的心脏重量(心脏重量/胫骨长度,HW/TL)与经历假手术的小鼠相比增加50%(图5A)。在图5A中,白条代表进行假手术的小鼠,并且黑条代表进行TAC手术的小鼠。8MI的施用以剂量依赖性方式减弱心脏重量的增加,在所使用的最高剂量(40mg/kg)下基本上降低HW/TL至如白条所指示的正常水平(图5A)。与先前所公布的TSA结果相比,8MI显示显著优良的作用。
心脏的四腔室切片展示用8MI处理再次以剂量依赖性方式还预防心肌重塑(图5B)。确认这些发现,超声心动描记术的壁厚度在媒剂处理的动物中增加35.9%±1.0%,但在8MI的最高剂量下的小鼠中仅增加6.9%±1.4%(图5C)。肌细胞横切面积响应TAC增加2.2倍(TAC,319±22μm2对比假手术,146±17);用8MI处理有效地消除这种2.2倍增加(图5D和5E)。再次,与先前所公布的TSA结果相比,8MI在减小肌细胞横切面积中显示显著优良的作用。
实施例5:8MI抑制体内心室纤维化
使用获自在实施例4中所描述的实验条件下处理的相同小鼠的心脏组织样品,曼森氏三色用于将纤维化组织染色(图6A)。相对于总组织面积定量和表达纤维化面积(图6B)。心室纤维化在TAC之后21天的小鼠中是明显的,但在假手术小鼠中不明显(图6A和6B)。引人注目地,这种纤维化反应由最高剂量的8MI消除并且以剂量依赖性方式显著降低(图6A和6B)。
实施例6:8MI在体内耐受良好
在处死之前,从如实施例4中所描述而处理的小鼠的血液中提取血清。血清化学的分析揭示在3只对照小鼠中有2只(#4和#6),但在接受任何剂量的8MI的9只小鼠中仅1只(#14)通过TAC诱导显著的肾和/或肝功能障碍(表I)。这些结果显示8MI耐受良好。
表2:经受TAC或假手术并且用8MI处理的小鼠中的血清化学
如上文实施例2中所论述,8MI在多种细胞的培养物中直至20μM未显示明显的毒性。而且,如实施例2中所描述每天用8MI(100mg/Kg)处理持续四周的小鼠未显示肾或肝损伤的征象或者其它不良作用。另外,在任一组(假手术或TAC手术)中未观察到死亡率,这支持8MI在动物模型中比更强效的泛HDAC抑制剂更加耐受的论断。
实施例7:8MI减弱与心脏重塑相关的转录
在来自实施例4中所描述的实验的平行样品中,定量一组心脏结构和肥大相关的基因的表达。使用TRIzol试剂(Invitrogen,Carlsbad,CA)从左心室组织提取总RNA。使用TaqMan Universal PCR主混合试剂(Applied Biosystems,Foster City,CA)在下列条件下扩增cDNA:在50℃下2分钟,在95℃下10分钟,40个循环:在ABI 7900HT热循环仪中在95℃下15秒并且在60℃下1分钟。将mRNA表达水平针对内部参考18S rRNA的那些标准化。所有样品一式两份运作。使用下列引物组:ANP、BNP、SERCA、MHC以及18S。使用来自Applied Biosystems的软件RQ manager1.2分析数据。
与实施例4和5中所公开的形态数据一致,1型胶原蛋白和3型胶原蛋白(Col1和Col3)图7A和7B)、心房利钠肽(ANP)图7C)、B型利钠肽(BNP)图7D)、SERCA2(图7E)以及α-肌球蛋白重链和β-肌球蛋白重链(图7F和7G)的应力诱导的表达通过8MI处理明显削弱。
实施例8:8MI保留TAC手术之后小鼠中的心脏功能
对小鼠进行超声心动描记术研究以在实施例4中所描述的实验条件下检查收缩功能。超声心动描记术研究揭示在基线处的所有小鼠中以及在用DMSO或8MI处理的假手术小鼠中的正常心脏功能(图8A-8H)。正如预期,TAC诱导在21天射血分数下降37%(假手术,82.4±1.8%对比TAC,51.7±5.1%)(图8A)。用8MI处理尽管有持续压力超负荷仍以剂量依赖性方式保留收缩功能。小鼠在8MI的最高剂量下维持75.4%的接近正常射血分数(图8A)。缩短分数(FS)(图8B)和心搏量(图8C)通过TAC减低并且在8MI存在下类似地恢复。LV舒张末期直径(LViDd)(图8D)、LV收缩末期直径(LViDs)(图8E)、LV收缩期容积(LV Vs)(图8F)以及LV舒张期容积(LV Vd)(图8G)通过TAC增大并且在8MI存在下减小。这些结果与如图4B中注意到的减少的心脏重塑一致。心率在所有小鼠中不受影响(图8H)。
实施例9:8MI抑制体内压力超负荷相关的MEF2乙酰化
在实施例4中所描述的实验条件下,在媒剂或8MI存在下在来自假手术和TAC手术小鼠的心肌组织中测定MEF2乙酰化。在RIPA(Sigma)中收集蛋白质样品。将500ng蛋白质样品与5μg乙酰基赖氨酸或GATA4抗体(Upstate,Charlottesville,Virginia)或MEF2抗体(Santa Cruz Biotechnology,Santa Cruz,CA)(5μg)一起孵育。使用TrueBlot琼脂糖小珠捕获免疫复合物并且经受西方分析。在SDS-PAGE上拆分免疫复合物并且转移至硝酸纤维素膜。在室温下在0.5%TBS-T中用5%牛奶阻断膜1小时,继而在一级抗体中在适当稀释度下孵育过夜。在室温下在HRP偶联的二级抗体中将膜孵育2小时并且使用化学发光显色。
总乙酰基-MEF2含量在接受最大剂量(40mg/kg)的8MI的假手术小鼠中对比接受媒剂(DMSO)的那些并无不同,表明对基底MEF2乙酰化的影响缺乏(图9)。然而,TAC诱导乙酰基-MEF2含量显著增加。如图9中所指示的渐增剂量的8MI使乙酰基-MEF2含量降至处于或低于假手术小鼠的那些的水平。在相同条件下,总水平和Ac-GATA4水平也增加,但用8MI未观察到显著变化。
实施例10:8MI在TAC期间防止肌细胞凋亡
在来自实施例4中所描述的实验的平行样品中,在媒剂或8MI存在下在来自假手术和TAC手术小鼠的心肌组织中定量凋亡。遵循用于可商购的末端脱氧核苷酰转移酶介导的dUTP缺口末端标记(TUNEL)检验试剂盒(Cardiotacs,Trevigne,Gaithersburg,Md)的推荐方案检测凋亡。凋亡在TAC样品中与假样品相比显著增强(图10)。凋亡在TAC手术小鼠中由8MI以剂量依赖性方式减少(图10)。在8MI的最高剂量(40mg/kg)下,凋亡减至与假手术小鼠所观测到的凋亡水平近似相同(图10)。
实施例11:7MI和8MI在肝中比BML-210或TSA显著地代谢更稳定
药物清除率是身体或器官从血液循环中消除药物的能力的量度。全身清除率是整个身体消除药物的能力的量度。器官清除率是特定器官(肝或肾)消除药物的能力的量度。对于肝清除率,肝是药物代谢的主要器官和药物清除的关键器官。用NADPH加强的人肝微粒体(HLM)是用以测量体外代谢并且预测体内清除率的标准方式。CLint(固有清除率)是体外与体内研究之间的联系,其可以基于单指数衰减模型来估计:Ct=C×e-kt。
用NADPH加强的人肝微粒体是用以体外评估由CYP(细胞色素P450)酶介导的代谢稳定性的标准方法。反应混合物(0.4mL)含有0.5mg/mL人肝微粒体、100mM磷酸盐缓冲液(pH 7.4)以及5mM测试化合物。首先在37℃振荡水浴中使混合物升温5分钟,并且然后添加1mM最终浓度的NADPH以起始反应。在指定的时间点获取等分试样(50mL)并且与冰冷甲醇(含有内部标准)混合以停止反应。使混合物短暂涡旋并且离心用于蛋白质沉淀。使10mL上清液的等分试样经受LC-MS/MS分析。化合物消失的百分比用于计算代谢速率。
表3:与BML-210和TSA相比7MI或8MI从肝中的底物消失.
结果提供了给定的化合物将如何经受肝代谢清除的指示。尽管BML-210与7MI和8MI共享结构相似性,但当前数据显示其将比7MI或8MI代谢清除快得多,表明BML-210是高清除率化合物(图11)。表3显示BML-210具有比7MI高4.3倍并且比8MI高2.5倍的固有清除(Clint)速率。类似地,TSA比7MI或8MI代谢清除快得多(图11),其具有比7MI高3.2倍并且比8MI高1.9倍的Clint速率(表3)。在肝中代谢不稳定的化合物通常展现低的口服生物利用度并且倾向于发生CYP介导的药物-药物相互作用。这些结果显示7MI和8MI可能展现比BML-210或TSA更高的口服生物利用度并且可能不太倾向于发生CYP介导的药物-药物相互作用。
参考文献
以下所列的参考文献、专利和公布的专利申请以及上述说明书中所引用的所有参考文献特此以全文引用的方式并入,如同在本文中完整阐述一样。
1.Berry,J.M.,Cao,D.J.,Rothermel,B.A.以及Hill,J.A.(2008)在心脏病治疗中的组蛋白脱乙酰化酶抑制(Histone deacetylase inhibition in the treatment of heart disease).《药物安全性专家见解(Expert Opin.Drug Saf.)》7(1):53-67。
2.Bisping E.,Wakula,P.,Poteser,M.以及Heinzel,F.R.(2014)靶向心脏肥大:朝着病因性心脏衰竭疗法的方向(Targeting Cardiac Hypertrophy:Toward a Causal Heart Failure Therapy).《心血管药理学杂志(J.Cardiovasc.Pharmacol.)》64:293-305。
3.Cheng S,Xanthakis V,Sullivan LM,Lieb W,Massaro J,Aragam J,Benjamin EJ,Vasan RS(2010)在成人生命过程中超声心动描记术的心脏重塑指数的关联:来自弗雷明汉心脏研究的纵向观测(Correlates of echocardiographic indices of cardiac remodeling over the adult life course:longitudinal observations from the Framingham Heart Study).《循环(Circulation)》122(6):570-578。
4.Cohn JN,Ferrari R,Sharpe N(2000)心脏重塑--概念和临床意义:来自心脏重塑的国际论坛的共识论文(Cardiac remodeling--concepts and clinical implications:a consensus paper from an international forum on cardiac remodeling).《美国心脏病学会杂志(J Am Coll Cardiol)》35(3):569-582。
5.Cox DM,Du M,Marback M,Yang EC,Chan J,Siu KW,McDermott JC(2003)调控肌细胞增强因子2A的稳定性和功能的磷酸化基序(Phosphorylation motifs regulating the stability and function of myocyte enhancer factor 2A).《生物化学杂志(The Journal of biological chemistry)》278(17):15297-15303。
6.Dorn GW,2nd,Robbins J,Sugden PH(2003)肥大分型:避免混淆(Phenotyping hypertrophy:eschew obfuscation).《循环研究(Circ Res)》92(11):1171-1175。
7.Heidenreich,P.A.等,(2011)预测美围心血管疾病的未来:美国心脏协会的政策声明(Forcasting the future of cardiovascular disease in the United States:a policy statement from the American Heart Association).《循环(Circulation)》(123)(8):933-944。
8.Jayathiliaka,N.,Han,A.,Gaffney,K.J.,Dey,R.,Jarusiewicz,J.A.,Noridomi,K.,Philips,M.A.,Lei,X.,He,J.,Ye,J.,Gao,T.,Petasis,N.A.以及Chen,L.(2012)通过阻断IIa类HDAC与MEF2的相互作用抑制IIa类HDAC的功能(Inhibition of the function of class IIa HDACs by blocking their interaction with MEF2).《核酸研究(Nucleic Acids Research)》40(12):5378-5388。
9.Kane GC,Karon BL,Mahoney DW,Redfield MM,Roger VL,Burnett JC,Jr,Jacobsen SJ,Rodeheffer RJ(2011)左心室舒张期功能障碍的进程和心脏衰竭的风险(Progression of left ventricular diastolic dysfunction and risk of heart failure).《美围医学会杂志(JAMA)》306(8):856-863。
10.Kannel WB(2000)心脏衰竭的发生率和流行病学(Incidence and epidemiology of heart failure).《心脏衰竭评论(Heart Fail Rev)》5(2):167-173。
11.Kong Y.,Tannous,P.,Lu,G.,Berenji,K.Rothermel,B.A.,Olson,E.N.以及Hill,J.A.(2006)I类和II类组蛋白脱乙酰化酶的抑制减弱压力超负荷心脏肥大(Suppressio of Class I and II Histone Deacetylases Blunts Pressure-Overload Cardiac Hypertrophy).《循环(Circulation)》113:2579-2588。
12.Lam CS,Donal E,Kraigher-KrainerE,Vasan RS(2011)保留射血分数的心脏衰竭的流行病学和临床病程(Epideniology and clinical course of heart failure with preserved ejection fraction).《欧洲心脏衰竭杂志(Eur J Heart Fail)》13(1):18-28。
13.Maron BJ,Bonow RO,Cannon RO,3rd,Leon MB,Epstein SE.(1987)肥大型心肌病的临床表现、病理生理学以及疗法的相互关系(Hypertrophic cardiomyopathy.Interrelations of clinical manifestations,pathophysiology,and therapy).《新英格兰医学杂志(N Engl J Med.)》3月26日;316(13):780-789。
14.McKinsey,T.A.(2011)心脏中HDAC的生物学和治疗意义(The Biology and Therapeutic Implications of HDACs in the Heart).《实验药理学手册(Handbook of Experimental Pharmacology)》,206:57-77。
15.McKinsey,T.A.(2012)心脏中HDAC抑制剂的治疗潜力(Therapeutic Potential for HDAC Inhibitors in the Heart).《药理学与毒理学年评(Annu.Rev.Pharmacol.Toxicol.)》52:303-19。
16.《医师案头参考(Physician′s Desk Reference)》,第41版,Publisher Edward R.Barnhart,N.J.(1987)。
17.PCT/US93/0082948。
18.《雷明顿:药剂学科学与实践(Remington:The Science and Practice of Pharmacy)》,第21版,Univ.of Sciences in Philadelphia(USIP),Lippincott Williams&Wilkins,Philadelphia,PA,2005。
19.Samuel JL,Swynghedauw B(2008)心脏肥大是不是压力超负荷心脏中的所需补偿机制?(Is cardiac hypertrophy a required compensatory mechanism in pressure-overloaded heart?)《高血压杂志(J Hypertens)》26(5):857-858。
20.Spirito P,Chiarella F,Carratino L,Berisso MZ,Bellotti P,Vecchio C.(1989)《新英格兰医学杂志(Journal N Engl J Med.)》门诊患者群体中肥大型心肌病的临床病程和预后(Clinical course and prognosis of hypertrophic cardiomyopathy in an outpatient population).23;320(12):749-55。
21.Wei JQ,Shehadeh LA,Mitrani JM,Pessanha M,Slepak TI,Webster KA,Bishopric NH(2008)乙酰转移酶p300对适应性心脏肥大的定量控制(Quantitative control of adaptive cardiac hypertrophy by acetyltransferase p300).《循环(Circulation)》118(9):934-946。
- 还没有人留言评论。精彩留言会获得点赞!