使用PNA探针的熔解曲线分析、使用熔解曲线分析用于分析核苷酸多态性的方法和试剂盒与流程
本发明涉及用于检测靶基因的核苷酸多态性的修饰的PNA探针、使用包含报告物(reporter)和与其偶联的淬灭物(quencher)的PNA探针的熔解曲线分析方法,使用所述PNA探针分析靶基因的核苷酸多态性的方法,和包含PNA探针的用于检测靶基因的核苷酸多态性的试剂盒,且更具体地,涉及使用PNA探针的熔解曲线分析方法,通过熔解曲线分析的核苷酸多态性分析方法,和核苷酸多态性分析试剂盒,其中所述PNA探针含有负电荷分子。
背景技术:
单核苷酸多态性(SNP)是由DNA核苷酸中一个核苷酸的取代引起的基因变异,其为每个人带来在疾病原因、对治疗剂的反应等方面的个体差异。注意力已聚焦于SNP的检测和确认上,因为它们与新药开发以及个体化用药相关联。
为了迅速检测SNP,已使用了多种检测方法,其中应用实时PCR技术。作为多种检测方法的代表性实例,存在使用DNA嵌入式荧光材料的分析方法、使用DNA探针的方法、使用PNA探针的方法等。
使用DNA嵌入式荧光材料的单核苷酸多态性分析方法可通过DNA嵌入式荧光材料的饱和浓度来区分PCR扩增子的核苷酸中的变化而无需对实施PCR反应后获得的产物进行额外操作。然而,该方法在使用DNA嵌入式荧光材料中具有局限,且具有的劣势在于仅一个单核苷酸能够被分析且应使用用于分析熔解曲线的程序[Kirk M.Ririe等,ANALYTICAL BIOCHEMISTRY 245:154160,1997;U.Hladnik等,Clin Exp Med 2:105108,2002]。
作为用于熔解曲线分析的DNA探针,存在MGB Taqman探针、Molecular Beacon(分子信标)(MB)探针和二元探针。上述方法具有的优势在于显示了优异的SNP区分能力,但具有的劣势在于因为DNA探针的最小长度长约20~40聚物因此难以通过一个反应检测邻近的SNP[Hidefumi Sasaki等,Clin Cancer Res 11:2924-2929,2005;Manna Zhang等,HEPATOLOGY 36:3,2002]。
使用特征在于含有负电荷分子的PNA探针的熔解曲线分析方法具有的优势在于,相比已有PNA探针,PNA探针能够迅速而强烈地与靶DNA偶联,且由于强偶联能力,能够使用具有长度较短的探针,使得邻近的单核苷酸多态性能够被检测。
相关领域的文献
非专利文献
(非专利文献1)Chen,C.Y.等,Clin.Chem 50:481-489,2004
(非专利文献2)M Beau-Faller等,British Journal of Cancer 100:985-992,2009
概述
本发明的一个目的是提供能够检测靶基因的核苷酸多态性的PNA探针。具体地,其特征在于PNA探针含有负电荷分子。
本发明的另一目的是提供使用PNA探针用于检测靶基因的核苷酸多态性的熔解曲线分析方法和包括所述PNA探针的核苷酸多态性分析方法。
本发明的另一目的是提供含有所述PNA探针的用于检测靶基因的核苷酸多态性的试剂盒。
附图简述
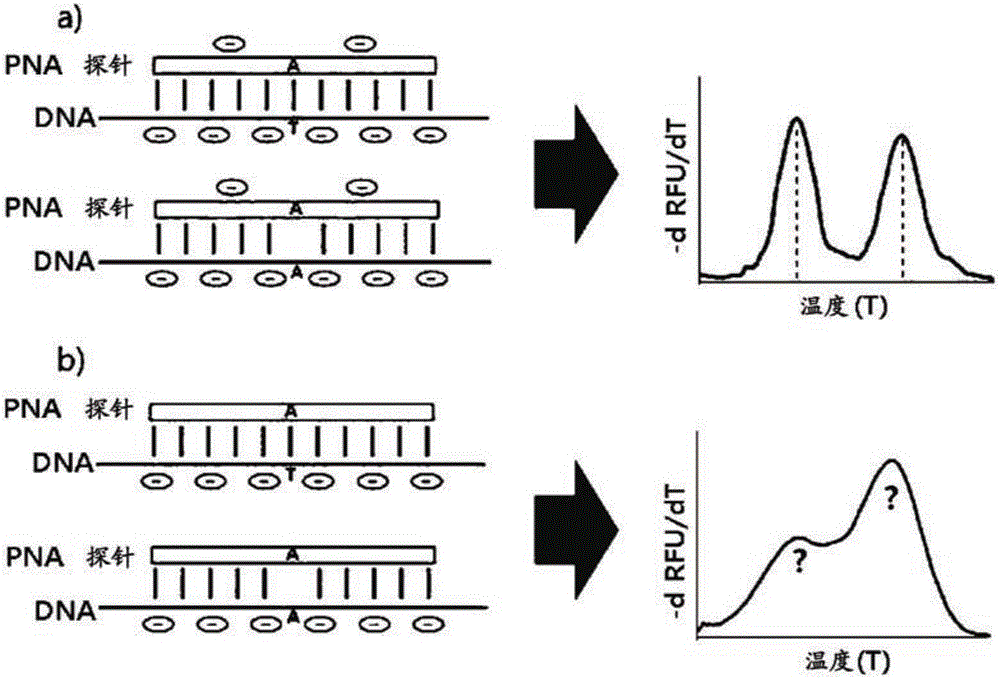
图1是显示与靶DNA偶联的PNA探针的示意图和熔解曲线图;
(a)使用与具有负电荷的氨基酸侧链偶联的PNA探针的情况。
(b)使用未修饰的PNA探针的情况。
图2显示通过将PNA探针与具有单核苷酸多态性的杂合样品偶联而获得的熔解曲线图;
(a)使用含有未修饰的PNA探针和以1:1比例混合的表2中的SEQ ID NO:10和11的DNA寡聚物的样品的情况。
(b)使用含有与γ-谷氨酸偶联的PNA探针和以1:1比例混合的表2中的SEQ ID NO:10和11的DNA寡聚物的样品的情况。
(c)使用含有未修饰的PNA探针和以1:1比例混合的表2中的SEQ ID NO: 10和12的DNA寡聚物的样品的情况。
(d)使用含有与γ-谷氨酸偶联的PNA探针和以1:1比例混合的表2中的SEQ ID NO:10和12的DNA寡聚物的样品的情况。
(e)使用含有未修饰的PNA探针和以1:1比例混合的表2中的SEQ ID NO:10和13的DNA寡聚物的样品的情况。
(f)使用含有与γ-谷氨酸偶联的PNA探针和以1:1比例混合的表2中的SEQ ID NO:10和13的DNA寡聚物的样品的情况。
图3显示通过将PNA探针与具有单核苷酸多态性的杂合样品偶联获得的熔解曲线图;
(a)未与γ-谷氨酸偶联的PNA探针的情况。
(b)与两个γ-谷氨酸偶联其间具有两个核苷酸的PNA探针的情况。
(c)与两个γ-谷氨酸连续偶联而其间无两个核苷酸的PNA探针的情况。
(d)与两个γ-谷氨酸偶联其间具有一个核苷酸的PNA探针的情况。
图4显示使用与γ-谷氨酸偶联的三个PNA探针的多重检测,黑线指示通过SEQ ID NO:2的PNA探针的熔解曲线,蓝线指示通过SEQ ID NO:7的PNA探针的熔解曲线,且红线指示通过SEQ ID NO:8的PNA探针的熔解曲线。
(a)使用由三个PNA探针和与每个探针互补结合的靶DNA寡聚物组成的纯合样品的实验情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
(b)使用由三个PNA探针和由于单核苷酸多态性所致的与每个探针错配的靶DNA寡聚物组成的纯合样品的实验情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
(c)使用含有三个PNA探针和彼此以1:1的比例混合的上述(a)和(b)中使用的靶DNA寡聚物的杂合样品的实验情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
图5显示多重检测,该情况中包含与其偶联γ-谷氨酸的三个PNA探针与单核苷酸多态性相邻;且黑线指示SEQ ID NO:2的PNA探针的熔解曲线,蓝线指示SEQ ID NO:7的PNA探针的熔解曲线,且红线指示SEQ ID NO:8的PNA探针的熔解曲线。
(a)使用三个PNA探针和表2中SEQ ID NO:19的DNA寡聚物的情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
(b)使用三个PNA探针和表2中SEQ ID NO:20的DNA寡聚物的情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
(c)使用三个PNA探针和彼此以1:1的比例混合的表2中SEQ ID NO:19和20的DNA寡聚物的情况,其中所述三个PNA探针包含与其偶联的γ-谷氨酸。
图6显示通过将PNA探针与具有单核苷酸多态性的多个杂合样品偶联而获得的熔解曲线图;
(a)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:21和22的DNA寡聚物的样品的情况。
(b)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:25和26的DNA寡聚物的样品的情况。
(c)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:21和23的DNA寡聚物的样品的情况。
(d)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:25和27的DNA寡聚物的样品的情况。
(e)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:21和24的DNA寡聚物的样品的情况。
(f)使用含有表1中SEQ ID NO:9的PNA探针和彼此以1:1的比率混合的表2中的SEQ ID NO:25和28的DNA寡聚物的样品的情况。
发明详述
本发明提供用于检测靶基因的核苷酸多态性的PNA探针,其包含报告物和与其偶联的淬灭物。
其特征在于PNA探针包含负电荷分子,其中所述负电荷分子可为选自由所有的酸组成的组的至少一种,所有的酸包括氨基酸、氨基酸侧链、磷酸、羧酸、磺酸、硝酸和硼酸。
此外,负电荷分子可与PNA探针的N末端、C末端,或PNA骨架的α、β和γ位置偶联,且至少一种负电荷分子可与探针的碱基连续或间歇偶联。
本发明提供使用PNA探针的熔解曲线分析方法,所述PNA探针包含报告物和与其偶联的淬灭物。
其特征在于所述熔解曲线分析方法中使用的PNA探针含有负电荷分子,且由于使用含有负电荷分子的PNA探针,熔解曲线的解析/分辨率(resolution)增加,从而易于分析杂合样品。
根据本发明含有负电荷分子的PNA探针可含有选自由所有的酸组成的组的至少一种负电荷分子,所有的酸包括氨基酸、氨基酸侧链、磷酸、羧酸、磺酸、硝酸和硼酸。负电荷分子可与PNA探针的N末端、C末端,或PNA骨架的α、β和γ位置偶联,且至少一种负电荷分子可与探针的碱基连续或间歇偶联。
此外,PNA探针可含有荧光材料。荧光材料可以是报告物、淬灭物或嵌入式荧光材料。
本发明提供使用含有负电荷分子的PNA探针的靶基因的核苷酸多态性分析方法。
可通过分析熔解曲线使用靶基因的核苷酸多态性分析方法。
由于PNA具有优异的热稳定性和生物稳定性,及与DNA相比对靶DNA的高识别能力和与靶DNA的高偶联能力,PNA可用作实时PCR技术的探针用于检测单核苷酸多态性(SNP)。然而,由于实时PCR方法使用荧光材料检测样品中的靶DNA,为了检测在一个位置的SNP,存在的问题是需要具有两种荧光材料(其具有不同波长)的探针。上述问题在实施多重检测中是显著的限制,而本发明可通过荧光探针的熔解曲线分析解决了所述问题。然而,在其中使用未修饰的PNA探针实施熔解曲线分析的情况中,由于在熔解曲线图一半最大值处的半宽度是大的,存在的劣势是用杂合样品的分析结果并不精确。因此,本发明的发明人尝试将PNA探针的骨架与具有负电荷的氨基酸的侧链偶联,从而随着温度增加,PNA探针和靶DNA迅速解离,由此能够精确分析熔解曲线。因此简化的示意图示于图1。
由于在熔解曲线图的半最大值处较小的半宽度,根据本发明的PNA探针可应用于多种分子诊断技术,如下述实例。例如,在其中核苷酸多态性发生于短核苷酸序列中多个位置处的密码子的情况中,由于熔解曲线的解析/分辨率很高,可使用一个PNA探针检测核苷酸多态性是否在一个位置或在两个或多个位置发生。此外,由于高解析/分辨率,熔解曲线可根据核苷酸多态性发生的位置处的碱基而区分,且因此,具有修饰的核苷酸序列可简单地得出而无需单独的分析(如序列分析)。
由于增加的熔解曲线解析/分辨率,根据本发明使用PNA探针用于检测核苷酸多态性的熔解曲线分析方法可使得实施核苷酸多态性的多重检测成为可能,且此外,甚至在其中SNP彼此相邻的情况中,可实施多重检测。
此外,甚至其中引入根据本发明与具有负电荷的氨基酸的侧链偶联的PNA探针以及在并非靶DNA的SNP修饰位置的不同位置形成错配的碱基的情况中,可获得与上述情况类似的效果。
本发明提供靶DNA的核苷酸多态性分析方法,其包括:
从测试样品分离靶DNA;
将靶DNA与PNA探针杂交,所述PNA探针含有报告物和与其偶联的淬灭物;
通过熔解由杂交获得的产物同时改变温度而获得熔解曲线;并
分析获得的熔解曲线。
其特征在于靶基因的核苷酸多态性分析方法中使用的PNA探针,和熔解曲线分析方法含有负电荷分子,其中含有负电荷分子的PNA探针可含有选自由所有的酸组成的组的至少一种负电荷分子,所有的酸包括氨基酸、氨基酸侧链、磷酸、羧酸、磺酸、硝酸和硼酸。负电荷分子可与PNA探针的N末端、C末端,或PNA骨架的α、β或γ位置偶联,且至少一种负电荷分子可与PNA探针的每个碱基连续或间歇偶联。
此外,在根据本发明的核苷酸多态性分析方法和熔解曲线分析方法中使用的PNA探针可包含荧光材料。探针可具有报告物和淬灭物的荧光材料,所述淬灭物能够淬灭与其两末端都偶联的报告物的荧光,并可包含嵌入式荧光材料。报告物可为选自下组的至少一种:FAM(6-羧基荧光素)、德州红(Texas red)、JOE、TAMRA、CY5和CY3,且淬灭物优选是TAMRA(6-羧基四甲基-罗丹明)、BHQ1、BHQ2或Dabysyl,但本发明不限于此。嵌入式荧光材料可选自下组:吖啶同二聚体及其衍生物、吖啶橙及其衍生物、7-氨基放线菌素D(7-AAD)及其衍生物、放线菌素D及其衍生物、9-氨基-6-氯-2-甲氧基吖啶(ACMA)及其衍生物、DAPI及其衍生物、二氢乙锭及其衍生物、溴化乙锭及其衍生物、乙锭同型二聚体-1(EthD-1)及其衍生物、乙锭同型二聚体-2(EthD-2)及其衍生物、乙锭单叠氮化物(ethidium monoazide)及其衍生物、碘化己啶及其衍生物、双苯酰亚胺(bisbenzimide)、Hoechst 33258及其衍生物、Hoechst 33342及其衍生物、Hoechst 34580及其衍生物、羟芪巴脒(hydroxystilbamidine)及其衍生物、LDS751及其衍生物、碘化丙啶(PI)及其衍生和Cy-染料衍生物。
用于靶基因的核苷酸多态性分析方法的PNA探针可含有报告物和淬灭物,其中所述PNA探针含有与其偶联的负电荷分子。含有负电荷分子、报告物和淬灭物的PNA探针与靶DNA杂交且随后生成荧光信号,且随温度增加,由于负电荷效应,PNA探针和靶DNA在探针的最佳熔解温度迅速熔解,从而淬灭荧光信号。与无负电荷的PNA探针相比,含有负电荷的PNA探针迅速从靶DNA解离以增加熔解曲线的解析/分辨率。通过从根据温度变化的荧光信号获得的具有高解析/分辨率的熔解曲线分析,可分析靶DNA的核苷酸多态性。
此外,用于靶基因的核苷酸多态性的PNA探针可含有嵌入式荧光材料,其中所述PNA探针含有与其偶联的负电荷分子。含有与其偶联的嵌入式荧光材料和负电荷分子的探针与靶DNA杂交且随后生成荧光信号,且由于负电荷效应,PNA探针和靶DNA在探针的最佳熔解温度迅速熔解,从而淬灭荧光信号。通过根据荧光信号的温度获得的具有高解析/分辨率的熔解曲线分析,可分析靶DNA的核苷酸多态性。
此外,根据本发明的靶基因的核苷酸多态性分析方法可包括分析通过使用荧光信号检测获得的熔解曲线而不将嵌入式荧光材料与探针直接偶联。
本发明提供使用PNA探针的熔解曲线分析方法用于分析靶基因的核苷酸多态性的试剂盒,所述PNA探针包含报告物和与其偶联的淬灭物。
其特征在于PNA探针含有负电荷,且试剂盒优选含有PNA探针,所述PNA探针包含报告物和与其偶联的淬灭物,但本发明不限于此。
用于分析核苷酸多态性的试剂盒可通过分析多重靶DNA或单靶DNA的核苷酸多态性而使用。
此后,将参照下述实施例详细描述本发明。这些实施例仅用于例示本发明,且根据本发明的精髓对于本领域的技术人员显而易见的是,本发明的范围不应理解为受限于这些实施例。
实施例1熔解曲线分析实验中使用的PNA探针、靶DNA寡聚物合成和熔解曲线分析方法
为了实施本发明的熔解曲线分析,合成了如下表1所示的PNA探针来使用。
[表1]本发明中使用的PNA探针的序列
在上文表1中,O指示接头,粗体字母指示γ-谷氨酸-PNA单体且K指示赖氨酸。
根据韩国专利公开号464261[Lee等,Org.Lett.,9:3291-3293,2007]所述的方法,通过固相合成通过从苯并噻唑磺酰基(Bts)保护的PNA单体和官能化的树脂合成PNA寡聚物而制备PNA探针。除上述的方法外,PNA探针可使用9-芴基甲氧基羰基(Fmoc)或叔丁氧基羰基(t-Boc)合成方法合成[Kim L.等,J.Org.Chem.59:5767-5773,1994;Stephen A.等,Tetrahedron,51:6179-6194,1995]。根据本领域广泛已知的方法在PNA探针上标记报告物材料和淬灭物材料。
作为将与PNA探针偶联的靶DNA寡聚物,使用了由Bioneer Corporation(韩国)合成的DNA寡聚物。
[表2]本发明中使用的DNA寡聚物的序列
添加了1.25μM上表1中所列的PNA探针、0.25μM上表2中所列的DNA寡聚物和PCR扩增溶液(Enzynomics Co.,Ltd.,Korea)并彼此混合,然后是使用实时PCR仪(CFX96TM实时PCR系统)在95℃反应5分钟,温度以0.1℃/秒的速率减少直至40℃并将反应物保持5分钟,然后测量荧光同时从40℃以0.5℃将温度增加至95℃,由此实施熔解曲线分析。
实施例2使用包含与其偶联的γ-谷氨酸的PNA探针进行的具有单核苷酸多态性的杂合样品的熔解曲线分析
为了比较包含与其偶联的γ-谷氨酸的PNA探针与未修饰的PNA探针之间的熔解曲线中的差异,通过实施例1的方法,通过实验分析了熔解曲线,所述实验使用包含表1中的SEQ ID NO:1和2的PNA探针和寡聚物的样品,所述寡聚物通过将表2中SEQ ID NO:10的DNA寡聚物以1:1的比例分别与表2中的SEQ ID NO:11至13的DNA寡聚物之一混合而制备。
其结果示于图2。可以理解的是在其中使用了包含与其偶联的γ-谷氨酸的PNA探针(即,包含引入其中的负电荷分子的PNA探针)的情况中,由于负电荷效应,根据温度的增加,PNA探针从靶DNA迅速解离,从而具有SNP的杂合样品中熔解曲线的解析/分辨率显著增加。
实施例3根据与PNA探针偶联的γ-谷氨酸的位置具有单苷酸多态性的杂合样品的熔解曲线分析
为根据γ-谷氨酸(其为与PNA探针偶联的负电荷分子)的位置比较熔解曲线的差异,通过上述实施例1的方法,使用样品通过实验分析了熔解曲线,所述样品分别包含表1中的SEQ ID NO:3、4、5和6的PNA探针和以1:1的比例彼此混合的表2中的NO:13至14的DNA寡聚物。其结果示于图3。
在使用与两个γ-谷氨酸偶联、其间具有两个核苷酸的PNA探针的情况中,将两条熔解曲线在具有SNP的杂合样品中最精确地彼此分开。
实施例4含有三个不同PNA探针的三个不同的纯合样品或包含单核苷酸多态性的杂合样品的熔解曲线分析,其中三个不同PNA探针含有与其偶联的γ-谷氨酸
通过确认上述实施例2是否能够用于多重检测,进行了实施例4。通过上述实施例1的方法,分别使用下述样品通过实验分析熔解曲线:包含表1中SEQ ID NO:2的PNA探针与靶寡聚物的组合的样品,所述靶寡聚物通过包含表2中SEQ ID NO:10或11的DNA寡聚物或通过以1:1的比率彼此混合两种DNA寡聚物而制备;包含表1中SEQ ID NO:7的PNA探针与靶寡聚物的组合的样品,所述靶寡聚物通过包含表2中SEQ ID NO:15或16的DNA寡聚物或通过以1:1的比率彼此混合两种DNA寡聚物而制备;和包含表1中SEQ ID NO:8的PNA探针与靶寡聚物的组合的样品,所述靶寡聚物通过包含表2中SEQ ID NO:17或18的DNA寡聚物或通过以1:1的比率彼此混合两种DNA寡聚物而制备。
其结果示于图4。确认了多重检测能够使用PNA探针执行,所述PNA探针包含与其偶联的γ-谷氨酸。
实施例5使用三个不同的PNA探针在具有相邻的不同的单核苷酸多态性的杂合样品中的熔解曲线分析,其中三个不同的PNA探针包含与其偶联γ-谷氨酸
通过确认由上述实施例4确认的多重检测能力是否能够甚至在SNP彼此相邻的情况中进行,进行了实施例5。使用包含表1中的SEQ ID NO:2、7和8的三个PNA探针和靶寡聚物的样品通过实验分析了熔解曲线,所述靶寡聚物通过包含表2中的SEQ ID NO:19或20的DNA寡聚物或通过以1:1的比率将两者DNA寡聚物彼此混合而制备。
其结果示于图5。通过使用包含与其偶联的γ-谷氨酸的PNA探针,确认了多重检测甚至在SNP彼此相邻的情况中能够执行。
实施例6使用PNA探针在具有不同的单核苷酸多态性的杂合样品中的熔解曲线分析,所述PNA探针具有引入其中的碱基,所述碱基在并非靶DNA的SNP修饰位置的不同位置处形成错配
为比较具有引入其中的在并非靶DNA的SNP修饰位置的不同位置处形成错配的碱基的PNA探针的效果,通过实施例1的方法,分别使用下述样品通过实验分析了熔解曲线:包含表1中SEQ ID NO:9的PNA探针和靶寡聚物的样品,所述靶寡聚物通过将SEQ ID NO:21的DNA寡聚物与表2中的SEQ ID NO:22至24的DNA寡聚物之一以1:1比例混合而制备,包含表1中SEQ ID NO:9的PNA探针和靶寡聚物的样品,所述靶寡聚物通过将SEQ ID NO:25的DNA寡聚物与表2中的SEQ ID NO:26至28的DNA寡聚物之一以1:1比例混合而制备。
其结果示于图6。通过使用具有引入其中的在并非靶DNA的SNP修饰位置的不同位置处形成错配的碱基的PNA探针,确认了两条熔解曲线在具有SNP的杂合样品中最精确地彼此分开。
在本发明中开发的PNA荧光探针不仅可用于上文实施例清楚描述的熔解曲线分析方法,还可用于能够使用荧光探针分析靶DNA的所有方法,例如,实时PCR方法;然而,其仅通过实施例的方式描述,且本发明并不限于此。本领域的技术人员可以理解的是可使用所有已知的方法。
工业实用性
根据本发明的PNA探针的骨架可与具有负电荷的氨基酸的侧链偶联,从而PNA探针可具有对于靶DNA的高识别能力和对于靶DNA的高偶联能力且可通过热迅速解离。因此,本发明的使用包含负电荷的PNA探针的核苷酸多态性分析方法具有的优势在于甚至在显示两条熔解曲线图的杂合样品中可相对容易地进行核苷酸多态性分析,且可同时分析两个和更多个邻近的单核苷酸多态性。此处,容易实施的熔解曲线分析不限于杂合样品,还可应用于包括纯合样品的所有样品。
已基于其具体特征详细描述了本发明,而且对于本领域的技术人员显而易见的是这些特定的技术仅为优选的实施方案且因此本发明的范围不限于所述实施方案。因此,本发明实质的范围由所附的权利要求及其等同物限定。
序列表自由文本
附于本文件。
序列表
<110> 帕纳金股份有限公司(PANAGENE INC.)
<120> 使用PNA探针的熔解曲线分析、使用熔解曲线分析用于分析核苷酸多态性的方法和试剂盒
<130> PF-B1787
<140> PCT/KR2014/002909
<141> 2014-04-04
<160> 28
<170> PatentIn version 3.2
<210> 1
<211> 12
<212> DNA
<213> 人工的
<220>
<223> 861-F71
<400> 1
caaacagctg gg 12
<210> 2
<211> 12
<212> DNA
<213> 人工的
<220>
<223> 861-glu2-71-65
<400> 2
caaacagctg gg 12
<210> 3
<211> 11
<212> DNA
<213> 人工的
<220>
<223> 858-F-78
<400> 3
ttgggcgggc c 11
<210> 4
<211> 11
<212> DNA
<213> 人工的
<220>
<223> 858-glu2-70
<400> 4
ttgggcgggc c 11
<210> 5
<211> 11
<212> DNA
<213> 人工的
<220>
<223> 858-glu270
<400> 5
ttgggcgggc c 11
<210> 6
<211> 11
<212> DNA
<213> 人工的
<220>
<223> 858-glu-270
<400> 6
ttgggcgggc c 11
<210> 7
<211> 14
<212> DNA
<213> 人工的
<220>
<223> 18-2-3
<400> 7
tagttgggat gtac 14
<210> 8
<211> 14
<212> DNA
<213> 人工的
<220>
<223> K13_melt
<400> 8
acgccaccag ctcc 14
<210> 9
<211> 13
<212> DNA
<213> 人工的
<220>
<223> K
<400> 9
gagcttggtg gcg 13
<210> 10
<211> 30
<212> DNA
<213> 人工的
<220>
<223> 58T-61T
<400> 10
cgcacccagc tgtttggcct gcccaaaatc 30
<210> 11
<211> 30
<212> DNA
<213> 人工的
<220>
<223> 58T-61A
<400> 11
cgcacccagc agtttggcct gcccaaaatc 30
<210> 12
<211> 30
<212> DNA
<213> 人工的
<220>
<223> 58T-61G
<400> 12
cgcacccagc ggtttggcct gcccaaaatc 30
<210> 13
<211> 30
<212> DNA
<213> 人工的
<220>
<223> 58C-61C
<400> 13
cgcacccagc cgtttggcct gcccaaaatc 30
<210> 14
<211> 30
<212> DNA
<213> 人工的
<220>
<223> 58A-61C
<400> 14
cgcacccagc cgtttggcca gcccaaaatc 30
<210> 15
<211> 21
<212> DNA
<213> 人工的
<220>
<223> Tm-13-04
<400> 15
catgtacgtc ccaactacat g 21
<210> 16
<211> 21
<212> DNA
<213> 人工的
<220>
<223> Tm-13-01
<400> 16
catgtacgtc acaactacat g 21
<210> 17
<211> 26
<212> DNA
<213> 人工的
<220>
<223> 2120758-G(W)
<400> 17
aaggttggag atggtggcgt aggcta 26
<210> 18
<211> 26
<212> DNA
<213> 人工的
<220>
<223> 2120758-C
<400> 18
aaggttggag atgctggcgt aggcta 26
<210> 19
<211> 71
<212> DNA
<213> 人工的
<220>
<223> 3Target_W
<400> 19
cacccagctg tttggaagca tggtacgcca ctaagctcca aggaatcggt tggagatggt 60
ggcgtaggct a 71
<210> 20
<211> 71
<212> DNA
<213> 人工的
<220>
<223> 3Target_M
<400> 20
cacccagcag tttggaagca tggtacgcca gtaagctcca aggaatcggt tggagatgct 60
ggcgtaggct a 71
<210> 21
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)
<400> 21
catgcgccac caagctccat g 21
<210> 22
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-0A
<400> 22
catgcgccac taagctccat g 21
<210> 23
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-0C
<400> 23
catgcgccac gaagctccat g 21
<210> 24
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-0T
<400> 24
catgcgccac aaagctccat g 21
<210> 25
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-0A
<400> 25
catgcgccac taagctccat g 21
<210> 26
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-1A
<400> 26
catgcgccaa taagctccat g 21
<210> 27
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-2A
<400> 27
catgcgccag taagctccat g 21
<210> 28
<211> 21
<212> DNA
<213> 人工的
<220>
<223> K(D)-3A
<400> 28
catgcgccat taagctccat g 21
- 还没有人留言评论。精彩留言会获得点赞!