用于改善哺乳动物血糖控制的肽及其组合物的制作方法
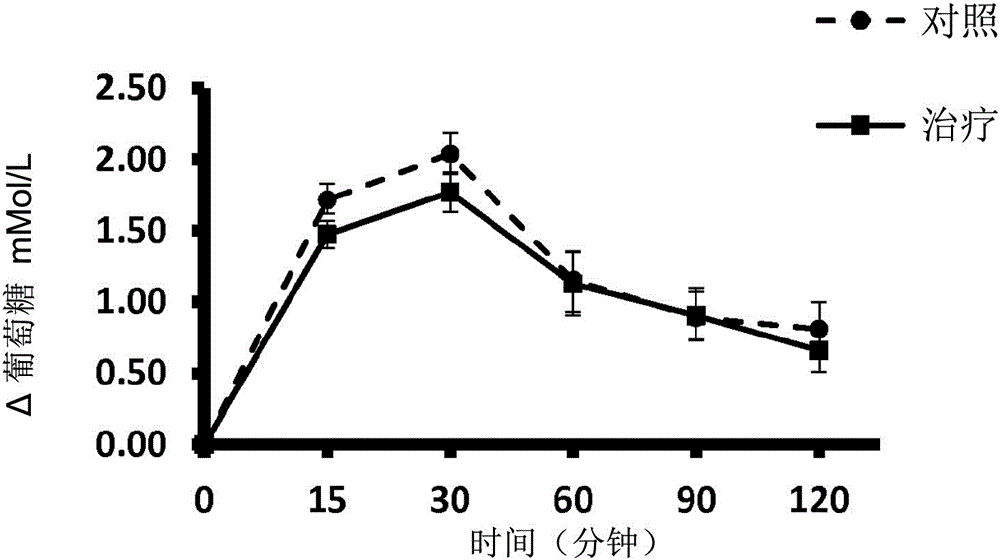
由于全世界的肥胖程度螺旋式上升,高血糖水平(高血糖症)越来越普遍。世界卫生组织估计,年龄在20岁以上的成年人当中有超过14亿人超重/肥胖,而三分之一的美国成年人和1.08亿亚洲人被诊断有糖尿病。高血糖现在和高血压以及高胆固醇血症一样重要,这导致提升了需要有助于餐后血糖水平产品的卫生专业人员和注重健康的消费者的意识。US2005/0089969公开了胰岛素模拟肽。本发明的目的是解决至少一个上述提及的问题。技术实现要素:广泛地,申请人已经鉴定了肽,SEQIDNO:11,及其生物活性片段,它们有改善哺乳动物血糖控制/状态的功效,特别是在口服后增加胰岛素分泌。所述SEQIDNO:11的肽与US2005/0089969中的SEQIDNO:2有大约94%的序列一致性,并且在重要的功能位点上有许多不同的残基。具体地,申请人已经鉴定了,所述肽,以及包括所述肽的组合物,能在体外增加胰岛β细胞的胰岛素分泌(图7A-7C)。申请人也已经表明了包括所述肽的组合物的急性治疗在ob/ob小鼠的葡萄糖耐量试验期间有降低葡萄糖的效果,以及引起小鼠肝脏脂肪含量的减少(图8和9)。使用饮食诱导的肥胖模型,在高脂喂养的情况下用包括所述肽的组合物治疗动物12周,与单独的高脂喂养相比,改善了在葡萄糖耐量试验(GTT)期间的葡萄糖清除率(图11)。另外,申请人已经证明,当在临床研究中包括本发明的肽的组合物与碳水化合物膳食一起给予人时,会引起血糖水平降低和胰岛素水平升高(图1和2)。所述肽是或者包括下面的SEQIDNO:11及其生物活性片段,所述生物活性片段通常包含SEQIDNO:1或5或两者都有的序列。YPVEPFTESQSLTLTDVENLHLPLPLLQSWMHQPHQPLPPTVMFPPQSVLSLSQSK(SEQUENCEIDNO:11)特定的生物活性片段包含以下SEQIDNO1至10。HQPHQPLPPTVMFPPQSVL(SEQUENCEIDNO:1)HQPHQPLPPTVMFPPQSVLSLSQSK(SEQUENCEIDNO:2)LQSWMHQPHQPLPPTVMFPPQSVL(SEQUENCEIDNO:3)LQSWMHQPHQPLPPTVMFPPQSVLSLSQSK(SEQUENCEIDNO:4)PPQSVLSLSQSK(SEQUENCEIDNO:5)MHQPHQPLPPTVMFPPQSVL(SEQUENCEIDNO:6)MHQPHQPLPPTVMFPPQSVLSLSQSK(SEQUENCEIDNO:7)SWMHQPHQPLPPTVMFPPQSVL(SEQUENCEIDNO:8)SWMHQPHQPLPPTVMFPPQSVLSLSQSK(SEQUENCEIDNO:9)YPVEPFTESQSLTLTDVENLHLPLPLLQSWMHQPHQPLPPTVMFPPQSVL(SEQUENCEIDNO:10)一方面,本发明涉及的肽包含(a)SEQIDNO:11的序列,或(b)其生物活性片段,优选地包含SEQIDNO:1或5的序列(下文称为“本发明的肽”)。另一方面,本发明涉及用于改善哺乳动物血糖控制和代谢综合征方面的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆血糖水平,特别是餐后血糖水平的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防高血糖症(特别是高脂饮食或肥胖诱发的高血糖症)的本发明的肽。在一个实施例中,本发明涉及用于增加哺乳动物餐后胰岛素分泌的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中调节葡萄糖平衡的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或减轻胰岛素抵抗的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆胆固醇水平的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或降低肝脏脂肪含量的本发明的肽。在一个实施例中,本发明涉及用于促进哺乳动物抗炎反应的本发明的肽。在一个实施例中,本发明涉及用于减少高脂饮食或肥胖诱发的炎症的本发明的肽。在一个实施例中,本发明涉及用于治疗或预防哺乳动物炎症性疾病的方法的本发明的肽。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆血糖水平,特别是餐后血糖水平,以及增加胰岛素分泌,特别是餐后胰岛素分泌的本发明的肽。另一方面,本发明也涉及包括多种不同的本发明的肽的组合物,例如至少2、3、4、5、6、7、8、9、10或11种本发明不同的肽。优选地,每一种本发明的肽包含SEQIDNO:11的序列,或其包含SEQIDNO:1或5序列的片段。另一方面,本发明也涉及包括基本上所有的SEQIDNO:1或11的肽的组合物。合适地,该组合物是牛酪蛋白产品的水解物。该组合物可以是药物、食品、食品补充剂、膳食补充剂、特殊食品(用于糖尿病患者或婴儿或老年患者)。另一方面,本发明涉及用于改善哺乳动物血糖控制的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆血糖水平,特别是餐后血糖水平的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防高血糖症(特别是高脂饮食或肥胖诱发的高血糖症)的本发明的组合物。在一个实施例中,本发明涉及用于增加哺乳动物餐后胰岛素分泌的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中调节葡萄糖体内平衡的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或减轻胰岛素抵抗的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆胆固醇水平的本发明的组合物。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或降低肝脏脂肪含量的本发明的组合物。在一个实施例中,本发明涉及用于促进哺乳动物抗炎反应的本发明的组合物。在一个实施例中,本发明涉及用于减少高脂饮食或肥胖诱发的炎症的本发明的组合物。另一方面,本发明涉及包括本发明的组合物的食品。典型地,该食品是特殊药用食品(FSMP)。在一个实施例中,该食品是奶制品。I另一方面,本发明涉及用于改善哺乳动物血糖控制的本发明的食品。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防高血糖症(特别是高脂饮食或肥胖诱发的高血糖症)的本发明的食品。在一个实施例中,本发明涉及用于增加哺乳动物餐后胰岛素分泌的本发明的食品。在一个实施例中,本发明涉及用于在哺乳动物中调节葡萄糖平衡的本发明的食品。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或减轻胰岛素抵抗的本发明的食品。在一个实施例中,本发明涉及用于在哺乳动物中降低血浆胆固醇水平的本发明的食品。在一个实施例中,本发明涉及用于在哺乳动物中治疗或预防或降低肝脏脂肪含量的本发明的食品。在一个实施例中,本发明涉及用于促进哺乳动物抗炎反应的本发明的食品。在一个实施例中,本发明涉及用于减少高脂饮食或肥胖诱发的炎症的本发明的食品。另一方面,本发明涉及用于预防或治疗选自代谢紊乱或肥胖症的本发明的组合物或肽。因此,本发明也涉及用于预防或治疗人类代谢紊乱的方法,包括对人体施用治疗有效量的本发明组合物或肽的步骤。另一方面,本发明提供包括结合有合适药物载体的本发明的肽或组合物的药物组合物。本发明提供包括多种不同的本发明的肽的牛酪蛋白产品衍生的水解物,例如包括至少2、3、4、5、6、7、8、9、10或11种本发明不同的肽。合适地,至少1%、10%、20%、30%、40%、50%、60%、70%、80%或者90%(w/w)的所述水解物包括本发明的肽。典型地,本发明的水解物通过在30℃至60℃的温度范围内使用胃-肠道酶制剂对牛酪蛋白产品进行水解得到。本发明所述的组合物可以包括本发明的水解物。本发明也涉及制备本发明牛酪蛋白产品衍生的水解物的方法,包括步骤:提供牛酪蛋白衍生产品,使用胃肠道蛋白酶制剂在30℃至60℃对牛酪蛋白衍生产品酶解合适的时间。该牛酪蛋白产品通常包括酪蛋白盐,其实例为本领域技术人员熟知以及包含酪蛋白酸钠。典型地,所述牛酪蛋白产品(和/或所述酪蛋白水解物)基本不含(即低于5%、4%、3%、2%、1%、0.5%、0.2%、0.1%(w/w)其它乳蛋白,例如乳清蛋白。典型地,蛋白酶与酪蛋白底物的比率(w.w)为0.1-1.0%,优选地0.2-2.0%。合适地,所述酪蛋白底物的水解用蛋白酶制剂在温度30℃至60℃进行。定义在本说明书中,术语“改善血糖控制”应该被理解为以下的一种或多种:治疗或预防高血糖、增加餐后胰岛素分泌、调节葡萄糖体内平衡、减轻胰岛素抵抗、增加胰高血糖素样肽的水平、降低肝脂肪含量、防范HFD或肥胖诱发的炎症。术语“改善代谢健康”应该被理解为降低血浆胆固醇水平、降低肝脏脂肪含量,或促进抗炎反应或它们的任何组合。在本说明书中,术语“哺乳动物”应该被理解为高等哺乳动物,特别是人。典型地,所述人患有选自代谢紊乱比如糖尿病或肥胖的紊乱症。本文使用的术语“肽”是指通过肽键联结起来的多达60个氨基酸单体组成的聚合物。本发明使用的肽(包含其变体和片段)可以全部或部分通过化学合成或通过核酸表达而产生。例如,本发明的和用于本发明的肽容易根据本领域熟知的已经建立的标准液体或优选固相肽合成方法制备(参见,例如,J.M.Stewart和J.D.Young,SolidPhasePeptideSynthesis,2ndedition,PierceChemicalCompany,Rockford,Illinois(1984),inM.BodanzskyandA.Bodanzsky,ThePracticeofPeptideSynthesis,SpringerVerlag,NewYork(1984)。必要时,本发明使用的任何肽可以被化学修饰以增加它们的稳定性。化学修饰的肽或肽类似物包含所述肽的任何功能性化学等价物,其特征在于,关于本发明的实践,其在体内或体外增加稳定性和/或功效。所述术语肽类似物也指本文描述的任何肽的氨基酸衍生物。通过程序可以产生肽类似物,所述程序包括但不限于对侧链的修饰、在肽合成期间掺入非天然氨基酸和/或它们的衍生物以及使用交联剂和对肽或它们的类似物施加构象约束的其它方法。侧链修饰的实例包含氨基修饰,比如通过用醛反应接着用NaBH4还原进行还原烷基化;用甲基乙酰亚胺酯酰胺化;用乙酸酐乙酰化;用氰酸酯进行氨基的氨基甲酰化;用2,4,6-三硝基苯磺酸(TNBS)进行氨基的三硝基苄基化;用丁二酸酐和四氢邻苯二甲酸酐对氨基进行烷基化;以及用吡哆醛-5'-磷酸进行赖氨酸的吡哆酰基化,接着用NaBH4还原。精氨酸残基的胍基可以通过与试剂比如2,3-丁二酮、苯甲酰甲醛和乙二醛形成杂环缩合产物来修饰。羧基可以通过碳化二亚胺活化进行修饰,通过邻酰基异脲形成,然后随之衍生化成,例如,相应的酰胺。巯基可以通过以下方法进行修饰,比如用碘乙酸或碘乙酰胺进行羧甲基化;过甲酸氧化成磺基丙氨酸;与其它硫醇化合物形成混合二硫化物;与马来酰亚胺反应;马来酸酐或其它的取代马来酰亚胺;使用4-氯高汞苯甲酸、4-氯苯甲酰苯磺酸、苯基氯化汞、2-氯汞-4-硝基酚和其它汞形成汞衍生物;用氰酸酯在碱性pH进行氨甲酰化。色氨酸残基可以通过,例如,N-溴代丁二酰亚胺进行氧化或用2-羟基-5-硝基苯甲溴或磺酰卤进行吲哚环的烷基化来修饰。酪氨酸残基可以用四硝基甲烷硝化形成3-硝基酪氨酸衍生物来改变。组氨酸残基的咪唑环的修饰可以通过用碘乙酸衍生物进行烷基化或用焦碳酸二乙酯进行N-乙酰基化来完成。在肽合成期间掺入非天然氨基酸和衍生物的实例包含但不限于使用正亮氨酸、4-氨基丁酸、4-氨基-3-羟基-5-苯基戊酸、6-氨基己酸、叔丁基甘氨酸、正缬氨酸、苯基甘氨酸、鸟氨酸、肌氨酸、4-氨基-3-羟基-6-甲基庚酸、2-噻吩基丙氨酸和/或氨基酸的D-异构体。肽结构修饰包含产生包括由D-氨基酸编码的反向序列的反转肽。在本说明书中,术语“本发明的肽”是指包含SEQIDNO:11序列或其生物活性片段或生物活性变体的肽。应用于SEQIDNO:11中的术语“其生物活性片段”是指具有至少10个氨基酸的SEQIDNO:11的片段以及参考图7B在下文中描述的与体外试验的对照相比,该片段能够增加胰岛β细胞的胰岛素分泌。公开的实例中SEQIDNO:11的生物活性片段具有至少12个氨基酸并包含序列PPQSVLSLSQSK(SEQIDNO:5)或序列HQPHQPLPPTVMFPPQSVL(SEQIDNO:1)。特定实例中SEQIDNO:11的生物活性片段包含SEQIDNO:1至11的序列(图7B)。应用于给定参考肽的术语“生物活性变体”是指所述肽的变体具有至少80%序列同源性,并且通常在肽的全长上具有至少90%,优选地至少95%,理想地至少96%、97%、98%或99%序列同源性,并且参考图7B在下文中描述的与体外试验的对照相比,能够增加胰岛β细胞的胰岛素分泌。在本文中,序列同源性包括序列一致性和相似性,即与SEQIDNO:11共有90%氨基酸同源性的变体,是在变体序列的全长上任何90%的比对残基与SEQIDNO:11的相应残基相同或是对SEQIDNO:11的相应残基的保守替换。本发明的组合物包括不同肽的混合物,其至少包括2种肽,例如2、3、4、5、6、7、8、9、10或11种不同的肽,其中所述的肽选自于SEQIDNO:11或其生物活性片段。在一个实施例中,所述组合物包括SEQIDNO:1至11的基本上所有的肽,例如8、9或10种肽。术语“包括SEQIDNO1至11的基本上所有的肽的组合物”应该被理解为包括至少8、9或10种肽的组合物。所述组合物也可以包含另外的肽、多肽或蛋白质,或其它组分,例如难消化的碳水化合物。所述组合物可以通过使用胃肠道蛋白酶制剂在合适的温度水解牛酪蛋白产品(例如酪蛋白酸钠)充足的时间,以提供包括SEQIDNO:1至11中的至少两种肽的水解物而制备。本文所用的术语“牛酪蛋白产品”应该被理解为主要由酪蛋白组成的牛奶衍生产品,例如凝乳酶酪蛋白酸盐和酸酪蛋白酸盐(酪蛋白酸钠、钙和钾)。本文所用的术语“胃肠道蛋白酶制剂”应该被理解为包含胰蛋白酶、糜蛋白酶和弹性蛋白酶的蛋白酶制剂。典型地,所述水解在30℃至60℃下进行。在一个实施例中,本发明所述组合物是包括SEQIDNO:1至11的一系列肽的酪蛋白衍生的水解物,以下称为“LFC24”。当根据下文描述的临床研究条件给予成年人时,本发明所述的组合物通常能降低餐后血糖水平,增加餐后胰岛素分泌水平,或二者都可以。本发明也涉及到包括一种或多种本发明的肽的组合物。术语“组合物”可以指食品、药物、膳食补充剂或营养补充剂。所述食品可以是固体食物或液体。食品的实例包含乳制品(比如牛奶饮料、酸奶、酸奶饮料、奶酪、涂抹酱)、饮料、烘焙食品、肉制品、早餐谷物、零食食品。所述膳食补充剂可以以任何形式提供,包含粉末、颗粒、薄片或以单位剂量形式提供,比如一袋粉末、丸剂、胶囊、片剂、锭剂等等。本发明也涉及到食用产品,例如包括本发明组合物的食品。所述食品可以是固体食物或液体。食品的实例包括乳制品(比如牛奶饮料、酸奶、酸奶饮料、奶酪、涂抹酱)、饮料、烘焙食品、肉制品、早餐谷物、零食食品。所述食品可以包括任何量的本发明组合物,例如从0.1%到30%(w/w)。所述食品可以是特殊药用食品(FSMP),其被定义为特定配制、加工和旨在用于对处于医疗监护下治疗的个体的疾病、紊乱或医学情况进行膳食管理的食品。这些食品旨在用于正常食物不能满足营养需求的人的专属或部分喂养。“炎症性疾病”是指影响人的免疫介导的炎症病症,并且通常特征在于一种或多种细胞因子的失调表达。炎症性疾病的实例包含皮肤炎症性疾病、关节炎症性疾病、心血管系统炎症性疾病、某些自身免疫疾病、肺和气道炎症性疾病、肠道炎症性疾病。皮肤炎症性疾病的实例包含皮炎,例如过敏性皮炎和接触性皮炎,寻常痤疮和牛皮癣。关节炎症性疾病的实例包含类风湿性关节炎。心血管系统炎症性疾病的实例是心血管疾病和动脉粥样硬化。自身免疫疾病的实例包括1型糖尿病、格雷夫斯病、格林-巴利疾病、狼疮、牛皮癣关节炎和溃疡性结肠炎。肺和气道炎症性疾病的实例包含哮喘、囊性纤维化、COPD、肺气肿和急性呼吸窘迫综合征。肠道炎症性疾病的实例包含结肠炎和炎症性肠病。其它炎症性疾病包括癌症、花粉热、牙周炎、过敏、超敏反应、缺血、抑郁、系统性疾病、感染后炎症和支气管炎。在本说明书中,术语“代谢紊乱”应该被理解为包括前期糖尿病、糖尿病;1型糖尿病;2型糖尿病;代谢综合征;肥胖;糖尿病血脂异常;高脂血症(hyperlipidemia);高血压;高甘油三酯血症;高脂肪酸血症(hyperfattyacidemia);高胆固醇血症;高胰岛素血症、MODY和HNF1A-MODY。本发明也提供包括结合合适的药物赋形剂的本发明的肽或组合物的药物组合物。所述术语“赋形剂”是指与所述肽或组合物一起给药的稀释剂、佐药、赋形剂或载体。这样的药物赋形剂可以是无菌液体,比如水和油,包括石油、动物、植物或合成来源的那些,比如花生油、大豆油、矿物油、芝麻油等等。当所述药物组合物静脉内给药时,水是优选的赋形剂。盐水溶液和葡萄糖水溶液以及甘油溶液也可以用作液体赋形剂,特别是用作注射溶液。合适的药物赋形剂包括淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂乳粉、甘油、丙二醇、水、乙醇等等。必要时,所述组合物也可以含有少量的润湿剂或乳化剂或pH缓冲剂。这些组合物可以采用溶液、悬浮液、乳液、片剂、丸剂、胶囊、粉剂、缓释制剂等形式。附图说明图1:用酪蛋白酸钠或LFC24治疗后120分钟内葡萄糖的平均变化(Δ变化,mmol/L)。数据基于n=62个健康成年人呈现,其中误差线表示平均值的标准误差(SEM)。治疗效果显著:p<0.05。图2:用酪蛋白酸钠或LFC24治疗后120分钟内胰岛素的平均变化(Δ变化,mU/L)。数据基于n=62个健康成年人呈现,其中误差线表示平均值的标准误差(SEM)。治疗效果显著:p<0.05。图3:用酪蛋白酸钠或水解的酪蛋白(LFC24)治疗后120分钟GIP的平均变化(Δ变化,pg/ml)。治疗效果显著:ns。数据基于n=62个健康成年人呈现,其中误差线表示平均值的标准误差(SEM)。GIP(胰高血糖素样肽)显著增加,其中用LFC24治疗导致浓度在15分钟时上升高于对照水平之上17.1%,例如增加25.95pg/ml。图4:用酪蛋白酸钠或LFC24治疗后120分钟未酯化的脂肪酸的平均变化(Δ变化,mMol/L)。数据基于n=62个健康成年人呈现,其中误差线表示平均值的标准误差。治疗效果显著:p<0.001。消耗LFC24与消耗完整的酪蛋白酸钠相比,未酯化的脂肪酸(NEFA)的响应明显降低。图5:暴露在LFC24之后,BRINBD11细胞的胰岛素分泌(n=3/4)。数值为平均值±SD。**p<0.01。细胞暴露于(1)16.7mM葡萄糖(2)16.7mM葡萄糖和10mM丙氨酸以及(3)16.7mM葡萄糖和LFC24(1mg/ml)。图6:胰岛β细胞(BRIN-BD11)的胰岛素分泌。用3T3-L1脂肪细胞条件培养基和具有LFC24的3T3-L1培养基(n=4)培养2小时后BRIN-BD11细胞的胰岛素分泌。数值为平均值±SD。暴露于LFC24预防了胰岛β细胞功能障碍。**p<0.01,***p<0.001图7A:暴露于16.7mmol/l葡萄糖和编号10的合成肽之后胰岛β细胞(BRINBD11)(n=3/4)的胰岛素分泌。数值为平均值±SD。阳性对照是16.7mM葡萄糖和加有10mM丙氨酸的16.7mM葡萄糖。****p<0.0001图7B:暴露于16.7mmol/l葡萄糖和合成肽之后诱导的胰岛β细胞(BRINBD11)(n=3/4)的胰岛素分泌。数值为平均值±SD。阳性对照是16.7mM葡萄糖和加有10mM丙氨酸的16.7mM葡萄糖。*与葡萄糖对照相比P<0.05。图7C:暴露于16.7mmol/l葡萄糖和所述合成肽的组合之后胰岛β细胞(BRINBD11)(n=3)的胰岛素分泌。阳性对照是16.7mM葡萄糖和16.7mM葡萄糖以及10mM丙氨酸。肽1、3、4、5、9、10和11的合并样品比合成肽2、6、7和8的组合更有效。图8:与对照治疗组相比,在ob/ob小鼠葡萄糖耐量试验期间用LFC24进行急性治疗,在15分钟(*p<0.05)和120分钟(*p<0.05)具有葡萄糖降低效果。结果表示为±SD。(对照n=5,治疗n=6)。虚线表示对照组以及实线表示用LFC24治疗。图9:用LFC24长期治疗引发ob/ob小鼠整个肝脏脂肪百分比在12周的治疗后明显下降。对照表示对照治疗的小鼠以及治疗表示用LFC24治疗。与对照小鼠的肝脏相比,用酪蛋白衍生的水解物治疗引起肝脏脂肪减少43%。结果表示为±SD,每个肝脏6个独立的40×图像。(对照n=6,LFC24治疗n=5),(p<0.05)。用LFC24长期治疗引发ob/ob小鼠平均肝脏脂肪球粒径在12周的治疗后明显下降。平均脂肪球粒径从对照肝脏平均39微米的粒径下降到治疗肝脏的28微米。结果表示为平均值±SD,每个肝脏6个独立的40×图像。(对照n=6,LFC24治疗n=5),(*p<0.05)。图10:用酪蛋白衍生的水解物长期治疗引起ob/ob小鼠肝脏脂肪球粒径和整个肝脏脂肪含量在12周的治疗后明显下降。A&B表示对照ob/ob小鼠喂水12周后的肝脏H&E染色切片。C&D表示用LFC24治疗的ob/ob小鼠的肝脏H&E染色切片。比例尺=300μm图11:GTT期间的葡萄糖水平。数值是平均值±SEM。LFC24防止高脂饮食(HFD)诱发葡萄糖不耐受症。补充LFC24防止了小鼠HFD诱发葡萄糖不耐受症。HFD+LFC24喂养的小鼠明显降低了对GTT的血糖响应,与HFD喂养的小鼠相比,明显降低葡萄糖挑战(challenge)后的血糖水平(p<0.001,p<0.05)。与HFD喂养的小鼠相比,HFD+LFC24喂养的小鼠的曲线下的GTT面积(AUC)也显著下降。血糖控制的这种改善是独立于体重的,因两种HFD均引发等同的体重增加。图12:LFC24防止高脂饮食(HFD)诱发脂肪组织中pAKT水平的降低。在处死小鼠之前15分钟用1.5U/kg胰岛素注射小鼠。立即将脂肪组织快速冷冻。(A)磷酸化AKT水平通过蛋白质印迹分析确定。(B)pAKT水平的光密度分析相对于GAPDH归一化,并用任意单位(AU)表示。(**p<0.01w.r.t食物+胰岛素;++p<0.01w.r.tHFD+胰岛素)(n=10只小鼠/组)图13:LFC24防止高脂饮食(HFD)诱发炎症,用LFC24对比不用LFC24的HDF喂养C57Bl/6小鼠,骨髓巨噬细胞(BMM)减少TNF-、IL-1和IL-18的分泌。从各研究组雄性C57Bl/6小鼠中获得BMM。将BMM培养7天,接种密度1×105个细胞/ml,用LPS(10ng/ml)刺激3-24h±ATP(5mM)。收集上清液并通过ELISA测定TNF-、IL-1和IL-18的浓度(***p<0.001;**p<0.01w.r.t食物+LPS;###p<0.001;##p<0.01;#p<0.05HFD+LFC24+LPS/ATP相对于HFD(不含LFC24)+LPS/ATP)(n=3只小鼠/组)。图14:LFC24改善脂肪组织的炎症,用具有LFC24的HDF喂养C57Bl/6小鼠,脂肪组织外植体减少IL-1、IL-6和TNF-的分泌。给小鼠喂养食物或补充HFD的食物±LFC24处理过的水,获取附睾的脂肪组织。所述组织用培养基±ATP(5mM)培养24h。收获培养基,并测定IL-1β(A)IL-6(B)和TNF-α(C)细胞因子的分泌(**p<0.01w.r.t食物+ATP;+p<0.05w.r.tHFD+ATP)(n=9-10只小鼠/组)。图15:LFC24特异性抑制IL-1和TNF-α对3T3-L1脂肪细胞IL-6表达的促炎性作用;与改善的胰岛素信号标记pAKT和GLUT4一致。3T3-L1脂肪细胞用±LFC24(1mg/mL)和NaCAS(1mg/mL)预处理72小时,接着用IL1β/TNFα(0.5ng/mL+0.5ng/mL)处理24小时。培养基和细胞收集起来进行分析。(A)IL-6细胞因子水平通过ELISA测定(***p<0.001w.r.t.对照;++p<0.01w.r.tIL1β/TNFα)。(B)在用±胰岛素(100nM)处理15分钟的3T3-L1细胞中,磷酸化AKT通过蛋白质印迹分析测定。(C)GLUT-4mRNA的表达通过RT-qPCR测定(***p<0.001w.r.t.对照;**p<0.01w.r.t对照;++p<0.01IL-1β/TNFαw.r.tLFC24+IL-1β/TNFα)。具体实施例牛酪蛋白衍生的酶水解物(LFC24)的制备将牛奶的酪蛋白组分用胃肠道蛋白酶制剂(胰蛋白酶、糜蛋白酶和弹性蛋白酶)在30℃-60℃温度范围内进行蛋白水解消化。在反应完成后,将该溶液加热使酶失活,并且将该消化物进行蒸发和喷雾干燥。产生的粉末制剂按照下文描述进行生物活性分析并通过反相固相萃取(SPE)分离进行肽的分析。人体研究研究人群通过海报和电台广告在都柏林地区招募健康的受试者。该研究由都柏林大学人类伦理研究委员会(UniversityCollegeDublinHumanEthicsResearchCommittee)批准。对感兴趣的候选人进行了筛选,并且一旦接受,为他们的参与提供书面的知情同意书。入选标准要求受试者年龄在40-65岁,BMI>25kg/m2,并且无疾病、未服处方药、没有怀孕或者不在哺乳期。表1.研究人群的基线特征(显示的数据表示62名受试者(32名女性,30名男性)的平均值和标准偏差(SD))平均值SD年龄(岁)53.66.5BMI(kg/m2)31.34.6身体脂肪%37.08.2腰围(cm)93.710.6收缩压(mmHg)128.916.9舒张压(mmHg)82.38.3研究设计和干预该研究是随机交叉设计摄入完整的酪蛋白酸钠和包括SEQIDNO:1至11的所有的肽的酪蛋白衍生的水解物(以下简称“LFC24”)。从KerryIngredients公司获得完整的酪蛋白酸钠。每种蛋白饮料通过在120ml矿泉水(Ballygowan)中重构12g干燥的LFC24或完整的酪蛋白酸钠而制备,得到10%w/v溶液。达到空腹条件的受试者被指示在10分钟内吃掉含有75g碳水化合物和蛋白饮料的膳食。在时间点t=0、15、30、60、90和120分钟时采集血样。统计数据表示为平均值±SEM。使用SPSS18.0(美国,伊利诺伊州,芝加哥,SPSS公司)执行线性混合模型分析,对所有分析物进行对照组和治疗组的响应的比较。0.05或更低的p值就认为是显著的。结果总共有30名男性和32名女性成功完成了该研究(表1)。LFC24组和酪蛋白酸钠组的葡萄糖和胰岛素响应显著不同(图1和图2)。体外研究LFC24可以促进胰岛β细胞的胰岛素分泌(图5)。试验最初在细胞系中实施并且使用主要胰岛证实(数据未显示)。LFC24拯救胰岛β细胞功能的能力使用脂肪细胞条件培养基-β细胞功能模型检验。暴露于LFC24拯救了所述β细胞胰岛素分泌的能力(图6)。在LFC24中被鉴定存在一系列肽。鉴定所述肽后,合成一系列合成肽。测试了促进胰岛素分泌的能力,结果如图7所示。动物模型研究进行了三次动物研究。研究1和2使用ob/ob小鼠模型,研究3使用饮食诱导的肥胖小鼠模型。研究1和2在葡萄糖耐量测试期间酪蛋白衍生的水解物(LFC24)对葡萄糖和胰岛素水平的急性效果为了评估LFC24的急性效果,在ob/ob和C57BL/6野生型小鼠中执行GTT。在ob/ob小鼠中发现葡萄糖降低效果,与ob/ob对照组相比,观察到在15分钟(*p<0.05)和120分钟(*p<0.05)时葡萄糖水平下降(图8)。在GTT期间为ob/ob小鼠测量胰岛素;与对照条件相比,在GTT之前用酪蛋白衍生的水解物处理一个小时,在0、15和60分钟时对胰岛素水平没有效果。补充酪蛋白衍生的水解物(LFC24)对肝脏脂肪的效果肝脏组织学研究表明,用酪蛋白衍生的水解物(LFC24)治疗引起了肝脏总体脂肪含量显著(p<0.05)减少,脂肪滴尺寸显著(p<0.05)减少(图9)。与对照小鼠的肝脏相比,用酪蛋白衍生的水解物治疗引起了总体肝脏脂肪减少43%和平均脂肪球粒径减少28%(图9)。视觉观察肝脏的H&E染色图像揭示了治疗后肝脏脂肪鲜明的改变(图10)。研究3血糖控制和胰岛素信号用LFC24治疗使用饮食诱发肥胖模型的动物12周。在GTT期间,与单独的高脂喂养相比,在高脂喂养的情况下用LFC24治疗改善了葡萄糖清除率。在食物喂养期间,LFC24没有效果(图11)。这种血糖控制的改善可以通过脂肪组织(图12)、骨骼肌和肝脏(数据未显示)中pAKT表达的上调解释。pAKT是调节血糖控制的关键胰岛素信号分子。炎症和血糖控制在饮食诱导的肥胖模型中,LFC24诱发抗炎效果,其中用具有LFC24的HFD预防了单独HFD的促炎、胰岛素过敏效应。LFC24显著减少从骨髓巨噬细胞分泌的TNFα、IL-1β和IL-18(图13)。此外,LFC24显著减少离体脂肪组织IL-6、IL-1β和TNFα分泌(图14)。炎症-血糖控制交互作用为了明确LFC24对促炎胰岛素敏化轴(sensitisingaxis)效果的特异性,我们证明了,LFC24通过减少3T3-L1脂肪细胞分泌IL-6能防止IL-1β和TNFα的促炎效果,这伴随着胰岛素信号分子pAKT和葡萄糖转运GLUT4的改善(图15)。本发明并不限于以上描述的实施例,在结构和细节上的变化并不脱离本发明的精神。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1