用于样本的自动转移的装置、系统及方法与流程
本说明书的实施例涉及样本转移,并且更具体地涉及自动样本转移。
背景技术:
在来自哺乳动物细胞的重组蛋白的制造中,冷藏保存的细胞的种子培养扩张是开始新的生产活动所需的重要步骤。该扩大过程或种子培养扩张为重要的,因为培养液的质量通常确定了生产活动的成功。
典型地,在种子培养扩张过程中,细胞(如,用于蛋白质疗法的细胞)最初从少量(例如,1ml或更多)的冷藏保存的样本培养。在实例中,待冷藏保存的样本置于冷冻瓶中,并且冷却到大约-80℃或更低的冷冻冷却温度来保存样本中的细胞。此外,在接种需要时,大约1.0ml到大约5.0ml的少量冷藏保存的样本解冻,以在冷冻瓶中获得细胞的悬液。随后,解冻的样本细胞转移到常规使用的培养器皿中,如方瓶(T-flasks)或转瓶。此外,培养器皿例行地在CO2受控的培养器中培养。
此外,培养器皿中的细胞与生长介质混合来便于细胞生长。细胞的悬液基于细胞生长到相同尺寸的附加培养器皿或较大细胞培养器皿中来亚培养(sub-cultivate)。随着细胞量的增长,细胞转移到具有更多生长介质的逐渐更大体积的培养器皿中。添加生长介质、细胞转移和细胞生长的该过程继续,直到获得确定的细胞质量。当确定的细胞质量累积时,细胞悬液收集并且用于灌注生物反应器,该生物反应器可用于开始新的生产活动。在一个实例中,确定的细胞质量可用于对器皿如WAVE™袋和Xcellerex™生物反应器中的生产接种。
典型地,种子培养扩张过程需要复杂的手动操作,并且使用多个培养器皿,导致了细胞污染可能性增大。此外,种子培养扩张过程的活动到活动的可变性可由缺少活性pH或溶解氧和用于在扩大期间控制的其它相似的指示物而引起。
通常,种子培养扩张过程需要由熟练操作者执行。在细胞培养和扩张的初始阶段中,操作者需要使冷冻瓶在水浴或恒温珠浴中解冻。此外,操作者需要净化瓶的外表面。经由实例,冷冻瓶的表面净化可通过喷洒化学制品如乙醇或消毒液来执行。在表面净化之后,冷冻瓶在层流罩中开启。此外,移液管用于从冷冻瓶回收培养液样本,并且将样本转移到细颈瓶,其预先填充有确定量的生长介质。随后,细颈瓶放置到培养器中,以完成初始细胞培养操作程序。因此,用以从细胞的冷藏保存样本开始细胞培养的、与种子培养扩张过程相关联的现有过程和设置是劳动和基础设施密集的。
技术实现要素:
根据本说明书的方面,提供了一种构造成使用第一容器和第二容器形成样本通路组件的联接装置。样本通路组件包括第一隔间和第二隔间。此外,样本通路组件构造成收纳样本。联接装置包括构造成加热样本的至少一部分的加热构件。此外,联接装置包括分离构件,其构造成使第一容器的至少一部分和第二容器的至少一部分与第一容器和第二容器的其余部分分离,以形成样本通路组件的第一隔间和第二隔间。此外,联接装置构造成转移样本的至少一部分,同时至少在联接第一隔间和第二隔间期间保持用于样本的无菌环境。
根据本说明书的另一个方面,提供了一种用于样本转移的自动系统。自动系统包括联接装置和操作性地联接于联接装置的收集装置。联接装置构造成使用第一容器和第二容器形成样本通路组件。样本通路组件包括第一隔间和第二隔间。此外,样本通路组件构造成收纳样本。联接装置包括构造成加热样本的至少一部分的加热构件。此外,联接装置包括分离构件,其构造成使第一容器的至少一部分和第二容器的至少一部分与第一容器和第二容器的其余部分分离,以形成样本通路组件的第一隔间和第二隔间。此外,联接装置构造成转移样本的至少一部分,同时至少在联接第一隔间和第二隔间期间保持用于样本的无菌环境。此外,自动系统包括收集装置,其操作性地联接于第二隔间的出口通路,以接收样本的至少一部分。
根据本说明书的又一个方面,提供了一种用于自动样本转移的方法。该方法包括提供具有第一保持器单元和第二保持器单元的联接装置。该方法还包括将具有样本的第一容器设置在联接装置的第一保持器单元中,以及将具有入口通路和出口通路的第二容器设置在联接装置的第二保持器单元中。此外,该方法包括使第一容器的至少一部分和第二容器的至少一部分与第一容器和第二容器的其余部分分离,以形成第一隔间和第二隔间。该方法还包括联接第一隔间和第二隔间来形成样本通路组件,以及将样本的至少一部分加热至确定温度。此外,该方法包括将样本的至少一部分从样本通路组件转移至收集装置。
附图说明
当参照附图阅读下列详细描述时,将更好地理解本公开的这些和其它的特征、方面和优点,在该附图中,相似的标记在所有附图中表示相似的部件,其中:
图1为根据本说明书的方面的示例性样本通路组件的示意图;
图2-8为根据本说明书的方面的使用联接装置组装图1的样本通路组件的示例性方法的示意图;
图9为根据说明书的方面的组装样本通路组件的方法的示意图;
图10为根据本说明书的方面的操作性地联接于第一容器或样本通路组件的加热构件的截面视图;
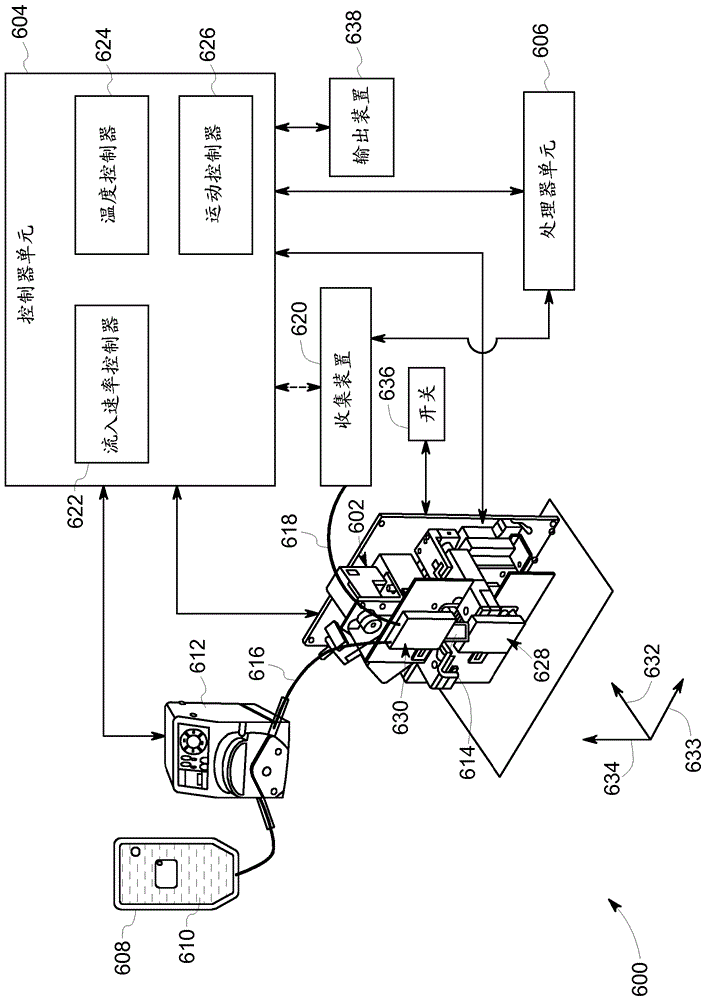
图11为根据本说明书的方面的用于样本转移的示例性自动系统的示意图;以及
图12为根据本说明书的方面的样本的自动转移的方法的示例性流程图的示意图。
具体实施方式
本说明书的实施例涉及用于自动样本转移的系统和方法。在某些实施例中,用于自动样本转移的系统和方法可形成用于细胞的种子培养扩张的部分。此外,这些实施例中的一些可用于提供用于冷藏保存的样本细胞自动接种转移至收集装置(如,但不限于培养器皿)的系统和方法。在一个实例中,哺乳动物细胞的群体可使用本说明书的系统和方法来转移。
图1为本说明书的样本通路组件100的示意图。在一个实施例中,样本通路组件100可在用于样本传递的自动系统中形成和使用。在特定实施例中,样本通路组件100可在用于以自动方式执行种子培养扩张的自动系统中形成以及使用。此外,如本文中详细所述,样本通路组件100的一部分可由冷冻瓶的至少一部分形成。具体而言,构造成收纳样本的冷冻瓶的一部分可形成样本通路组件100的部分。
在所示实施例中,样本通路组件100包括第一隔间102和第二隔间104。第一隔间102可构造成接收样本106。在一个实施例中,第一隔间102可为标准冷冻瓶的一部分,并且第二隔间104可为类似尺寸的管的一部分。此外,第二隔间104可操作性地联接于第一隔间102,使得第一隔间102和第二隔间104与彼此流体连通。
在某些实施例中,使用样本通路组件100的自动系统可构造成以最小操作者介入来操作。具体而言,一旦样本106经由第一隔间102设置在自动系统中,并且自动系统通电,则系统可构造成执行样本的解冻,通过联接第一隔间102和第二隔间104以产生样本通路组件100来接近样本,并且转移样本,而没有另外的操作者介入。
在一个实施例中,第一隔间102和第二隔间104可使用接头105联接。此外,在一个实施例中,接头105可为熔合接头。在非限制性实例中,接头105可通过热熔合、化学熔合或两者形成。在一个实施例中,接头105可通过将第一隔间102和第二隔间104热熔合在一起以形成样本通路组件100来形成。在特定实例中,接头105可通过热熔合第一隔间102和第二隔间104的界面来形成。在一个实施例中,接头105可为气密性密封接头,以防止样本106污染。
此外,在所示实施例中,第二隔间104可包括入口通路108和出口通路110。此外,在样本通路组件100中,设置在第一隔间102中的样本106可能够经由第二隔间104的入口通路108和/或出口通路110接近。因此,样本通路组件100可用于收纳、接近和转移样本106。另外,在一个实施例中,样本通路组件100可具有一个以上的入口通路108和出口通路110。此外,入口通路108和/或出口通路110可具有一个或更多个端口。
在一个实施例中,样本通路组件100可构造成将样本106转移至收集装置(图1中未示出),如培养器皿,其在样本通路组件100的外部。在该实施例中,样本通路组件100的出口通路110可联接于培养器皿。在一个实施例中,培养器皿可用于培养样本中的细胞。在一些实施例中,样本通路组件100可构造成使用入口通路108来接收生长介质(图1中未示出)。此外,样本通路组件100还可构造成使用出口通路110将样本106转移出样本通路组件100。
在某些实施例中,第二隔间104内的入口通路108和出口通路110的长度可取决于合乎需要的结果而变化。经由实例,设置在样本通路组件100中的入口通路108的一部分的长度可大于设置在样本通路组件100中的出口通路110的一部分的长度,以使入口通路108的端部关于出口通路110的端部更接近接头105,以便于样本106和生长介质的混合。可注意的是,样本和生长介质的混合物可称为"样本混合物"。
有利地,样本通路组件100可构造成在样本的处理期间保持用于样本106的无菌环境。如本文中使用的,用语"无菌环境"是指大致没有不合乎需要的微生物的环境。具体而言,样本通路组件100可构造成至少在样本106设置在样本通路组件100中时的持续时间内保持用于样本106的无菌环境。此外,样本通路组件100可构造成至少在样本106从样本通路组件100转移至收集装置时的持续时间内保持用于样本106的无菌环境。
图2-8示出了用于形成样本通路组件260(见图8)以便于转移样本(图2中未示出)的联接装置200。联接装置200可形成用于样本转移的自动系统的部分,如图11中所示的自动系统。此外,联接装置200构造成形成样本通路组件260,其中样本通路组件260构造成收纳样本的至少一部分。在某些实施例中,联接装置200包括加热构件201(见图2)和分离构件203(见图3-8)。在所示实施例中,联接装置200还可包括构件位置框架。在某些实施例中,构件位置框架可为可选的。构件位置框架可构造成向联接装置200提供机械完整性和稳健性。此外,构件位置框架可构造成收纳和/或保持各种一次性流体路径构件。此外,构件位置框架可包括用以收纳第一容器206和/或第二容器214的提供物(provision)。经由实例,操作者可经由构件位置框架将第一容器206和/或第二容器214设置在联接装置200中。此外,构件位置框架可构造成在样本通路组件260形成之前和之后保持联接装置200的两个或更多个构件的相对位置。
在某些实施例中,加热构件201构造成在样本通路组件260形成之前和/或之后加热样本的至少一部分。此外,分离构件203构造成联接第一隔间266和第二隔间268(见图7-8)来形成样本通路组件260。在一些实施例中,联接装置200可构造成转移样本的至少一部分,同时保持用于样本的无菌环境,例如在第一隔间和第二隔间的联接期间或之后。在一个实施例中,用于接收样本混合物的收集装置(图2中未示出)可设置在联接装置200中。在另一个实施例中,收集装置可设置在联接装置200外。
在所示实施例中,联接装置200包括第一保持器单元202和操作性地联接于第一保持器单元202的第二保持器单元204。此外,可注意到,图2示出了其中联接装置200开启来从内部示出保持器单元202和204的细节的实施例。图3-8示出了使用图2-8中所示的联接装置200形成样本通路组件260的示例性步骤。
在图2的所示实施例中,第一保持器单元202构造成收纳第一容器206的至少一部分。此外,第一容器具有第一侧208和第二侧210。此外,第一容器206的第一侧208和第二侧210可构造成闭合。经由实例,第一容器206可为样本瓶,并且瓶的第一侧208可闭合,并且瓶的第二侧210可具有盖212。盖212的非限制性实例可包括密封剂膜。
此外,第二保持器单元204构造成收纳第二容器214的至少一部分。第二容器214包括第一侧216和第二侧218。第二容器214可或可不具有相当大的容积。在一个实施例中,第二容器214可具有瓶,而在另一个实施例中,第二容器214可为闭合容器,而没有任何相当大的容积。此外,第二容器214的第二侧218可至少部分地闭合。此外,第二容器214的第一侧216包括入口通路220和出口通路222。在一个实施例中,入口通路220和出口通路222可为入口管和出口管。在非限制性实例中,入口通路220和出口通路222可使用双内腔管路形成。入口管220和出口管222可为柔性管或刚性管。
尽管图3-8中未示出,但在一些实施例中,在将第二容器214设置在第二保持器单元204中之前,入口通路220操作性地联接于生长介质源、泵或两者。在一个实施例中,入口通路220可经由泵(如但不限于蠕动泵)联接于生长介质源。此外或作为备选,蠕动泵还可联接于出口通路222。具体而言,入口通路220的端部可联接于生长介质源的出口,并且泵可操作性地联接在生长介质源与第二容器214之间。此外,泵可构造成便于合乎需要量的生长介质在预定速率下流入在样本通路组件260中。在一些实施例中,收集装置可预先附接于第二容器214。在一个实施例中,收集装置可通过出口通路222的管路预先联接于第二容器214并且与第二容器214流体连通。在另一个实施例中,收集装置可使用适当的无菌技术紧接在由操作者使用之前操作性地联接于第二容器214。此外,可注意的是,收集装置为细胞培养兼容器皿,其构造成接收样本混合物,同时保持用于样本的无菌环境。收集装置的非限制性实例可包括灭菌细颈瓶、灭菌生物反应器或两者。
在某些实施例中,第一保持器单元202和第二保持器单元204可包括夹具或其它类似的结构,用于分别机械地保持第一容器206和第二容器214。然而,第一保持器单元202、第二保持器单元204或两者可具有关于彼此的一个或更多个自由度。在非限制性实例中,第一保持器单元202和第二保持器单元204可具有关于彼此的三个自由度。此外,第一保持器单元202和第二保持器单元204可构造成对准和熔合第一容器206和第二容器214的部分,以形成样本通路组件206,同时保持用于设置在第一容器206中的样本的无菌环境。
在所示实施例中,第一保持器单元202和第二保持器单元204可包括构造成分别保持第一容器206和第二容器214的特征224和226。此外,特征224和226可构造成在容器206和214的加载和容器206和214加载之后的保持器单元202和204的闭合期间,将第一容器206和第二容器214固持在它们的相应位置。经由实例,特征224和226可构造成在容器206和214的加载和保持器单元202和204的闭合期间,将第一容器206和第二容器214分别固持在第一保持器单元202和第二保持器单元204中的它们的相应槽口228和230中。在所示实施例中,特征示为叉形元件,然而,在备选实施例中,特征224和226可具有适合于将第一容器206和第二容器214保持就位的任何其它形状。此外,特征224和226和槽口228和230可构造成收纳变化形状和尺寸的第一容器206和第二容器214。例如,可容易操作的调整件可提供成调整特征224和226和/或槽口228和230,以符合第一容器206和第二容器214的物理大小。
此外,特征224和226和槽口228和230(见图3-4)可构造成定位第一容器206和第二容器214,使得第一容器206和第二容器214的至少一部分可沿第一方向242重叠。此外,在联接在一起来形成样本通路组件260之前,第一容器206和第二容器214可设置成沿第二方向244远离彼此。在所示实施例中,第一容器206和第二容器214的重叠部分大体上由附图标记246代表。
在一些实施例中,特征224和226可包括用以提高联接装置200的人体工程学和相容性的若干结构。经由实例,特征224和226的叉形形状可便于第一容器206和第二容器214在联接装置200中的容易安装。在这些实施例中的一些中,叉设计成适应各种直径以及截面几何形状的小瓶,如但不限于,圆形、正方形、矩形或任何其它几何形状或非几何形状。保持器单元202和204沿方向242的相对运动用于闭合联接装置200。
在一个实施例中,联接装置200可首先在开始时处于开启状态,并且使用者可需要将第一容器206和第二容器214简单地设置或落入在对应的开口232和234中,并且接着闭合联接装置200来实现用于联接装置200的加载程序。图2-4示出了处于开启状态的联接装置200,并且图5-8示出了处于闭合状态的联接装置200。在加载程序期间,第一容器206和第二容器214可自动地锁定在正确位置。在另一个实施例中,可不需要开启和闭合联接装置200来执行加载程序。例如,在该实施例中,第一容器206和第二容器214可使用开口232和234简单地落在处于联接装置200的闭合状态的联接装置200中。在一个实施例中,第一容器206和第二容器214可在使用联接装置200时由使用者设置在构件位置框架上。在一些实施例中,第一保持器单元202和第二保持器单元204可操作性地联接于一个或更多个促动器,如线性和/或旋转促动器,以便于第一保持器单元202和第二保持器单元204的移动用于操作联接装置200。
在某些实施例中,加热构件201可构造成加热设置在第一容器206和/或样本通路组件206的一部分中的样本的至少一部分。在一个实例中,加热构件201可构造成使设置在第一容器206和/或样本通路组件260中的样本解冻至确定温度。因此,加热构件201可设置在第一保持器单元202中,使得加热构件201操作性地联接于第一容器206的至少一部分。在其中第一容器206为冷冻瓶的一个实例中,在操作中,具有在冷冻温度下的样本的冷冻瓶可直接地设置在联接装置200中。加热元件201可接着将冷冻瓶中的样本解冻至合乎需要温度。有利地,加热构件201构造成以合乎需要的加热速率加热设置在第一容器206中的冻结的样本。在特定实例中,加热构件201构造成使设置在冷冻瓶中的冷藏保存的样本快速解冻。
在某些实施例中,加热构件201可包括多层结构,如将关于图10详细描述的。加热构件201可围绕第一容器206的一部分设置。在图2的所示实施例中,加热构件201包括薄膜加热器258,以及设置在第一容器206附近的导热泡沫261。导热泡沫261构造成提供第一容器206的表面的至少一部分上的一致的热通量。该一致的热通量可通过导热泡沫261中的顺应性来实现,导热泡沫261便于消除薄膜加热器258与第一容器206的表面之间的气隙。此外,在薄膜加热器258用作加热构件201的情况中,导热泡沫261的导热性质有助于减少热点。尽管未示出,但预想的是,在一些实施例中,另一个加热构件可类似地围绕第二容器214的至少一部分设置。围绕第二容器214的部分设置的该其它加热构件可构造成在使生长介质与样本混合之前加热生长介质的至少一部分。在一个实施例中,加热构件201可至少部分地设置在槽口228和230中。在一个实施例中,在加热构件201包括两个半部的情况下,加热构件201的两个半部可设置在存在于联接装置200的两个部分中的槽口228和230中,使得在联接装置200闭合时,加热构件201的两个半部围绕第一容器206的至少一部分设置。此外,在一些实施例中,加热构件201可为电池操作的加热器或化学加热器。
此外,在一些实施例中,分离构件203可构造成使第一容器206和第二容器214的至少一部分分离以形成样本通路组件260的第一隔间266和第二隔间268。此外,分离构件203可定位成使得分离构件203与第一容器206和第二容器214的重叠部分246对准或沿第一方向242与其重叠。此外,分离构件203可构造成在样本通路组件260形成期间放置成与第一容器206和第二容器214物理接触。在特定实施例中,分离构件203可构造成同时、几乎同时或快速相继地与第一容器206和第二容器214物理接触。在一些实施例中,分离构件203可铰接,以便能够绕着联接装置200中的确定点或轴线至少部分地旋转。
此外,在某些实施例中,分离构件203可构造成加热至确定温度。在这些实施例中的一些中,分离构件203可构造成通过使电流穿过分离构件203的部分来加热至确定温度。
在一些实施例中,分离构件203可为刀片。此外,刀片可具有连续结构或有图案的结构。在一个实施例中,有图案的结构可包括多个条、线、线缆或它们的组合。此外,在一些实施例中,分离构件203可包括激光束。激光束可单独使用或与刀片组合使用。此外,在一些实施例中,灭菌环境可在第一容器206和第二容器214的相应部分的分离动作以形成样本通路组件260的第一隔间266和第二隔间268时提供在联接装置200内。
此外,分离构件203可具有适于将非翘曲特征给予刀片的机械强度和厚度。有利地,连同分离构件203的合乎需要温度的分离构件203的非翘曲特征可导致第一容器206和第二容器214的完全切割,导致刀片与第一容器206和第二容器214的接触点处的光滑界面。如可注意到的,第一容器206和第二容器214的光滑界面或完全切割便于第一容器206和第二容器214的增强熔合,并且提供样本通路组件的气密性密封。在一个实施例中,分离构件203可具有从大约0.01英寸到大约0.03英寸到大约0.03英寸的范围中的厚度。在另一个实施例中,203可涂覆有聚四氟乙烯(PTFE)或其它材料,以产生润滑表面,其可导致容器的较高质量的分离。此外,在这些或其它实施例中,分离构件203可由高温材料制成,如但不限于,铂、钨、镍铬铁合金、镍(合金HX)或它们的组合。在一个实施例中,分离构件203可由导电材料制成,如但不限于钨、镍铁铬合金、镍(合金HX)或它们的组合。此外,在一个实施例中,分离构件203可在确定温度下加热和保持达高达几秒,以使分离构件203灭菌。
此外,在加热分离构件203之后,分离构件203的运动可开始,以便于沿第一容器206和第二容器214的横向方向(也表示为方向245)切割第一容器206和第二容器214的部分。在一个实施例中,分离构件203可用于几乎同时分离第一容器206和第二容器214的重叠部分246来形成第一隔间和第二隔间。在一个实施例中,分离构件203可构造成在分离构件203的单次刷过中切割第一容器206和第二容器214的部分。
在分离步骤的快速相继中,第一隔间266和第二隔间268可对准。经由实例,具有第一隔间266和第二隔间268的第一保持器单元202和第二保持器单元204可关于彼此移动,以使第一隔间266和第二隔间268对准来形成样本通路组件260。例如,第一保持器单元202和第二保持器单元204可关于彼此沿第二方向244移动,以使第一隔间266和第二隔间268对准。此外,第一保持器单元202和/或第二保持器单元204可朝彼此沿第一方向242移动,并且压靠彼此,以形成第一容器206和第二容器214的其余部分之间的接头。在一个实施例中,接头可为热接头,其由于第一容器206和第二容器214的材料在第一容器206和第二容器214的界面处的熔化和熔合而形成。此外,在一个实施例中,分离构件203可构造成在接头形成在第一容器206和第二容器214的其余部分之间或样本通路组件260的第一隔间266和第二隔间268之间之前缩回。
可注意到,各种运动,包括分离构件203的运动,以及保持器单元202和204沿一个或更多个方向的运动可同时或以最小时间延迟发生,以防止设置在第一容器206中的样本暴露于环境。在一个实施例中,紧接在第一容器206和第二容器214的部分的分离之后,保持器单元202和204中的一个或两者可开始关于彼此移动,以使第一容器206和第二容器214的部分对准。
在某些实施例中,联接装置200可具有用于执行四个主要操作的三个促动自由度,即,(1)分离构件203沿第三方向245的运动,以便分离第一容器和第二容器,(2)由第一保持器单元202和/或第二保持器单元204沿第二方向244的运动实现的第一容器206和第二容器214的对准运动,(3)分离构件203沿第三方向245的运动,以及(4)用于形成第一容器206与第二容器214之间的机械联接或接头的、第一保持器单元202和第二保持器单元204沿第一方向242的联接运动。在一个实施例中,操作(3)和(4)可同时执行。在一些实施例中,在第一容器206和第二容器214安装之后,操作者可接通联接装置200,以开始样本混合物的自动转移程序。
在一些实施例中,保持器单元202和204的对准运动可用于使第一容器206和第二容器214的部分对准来形成样本通路组件260。在一些实施例中,在保持器单元202和204的对准运动之后,第一容器206和第二容器214可停留在分离构件203上达一些时间,以增强第一容器206和第二容器214的第一隔间和第二隔间的界面之间的连结。具体而言,第一容器206和第二容器214可停留在分离构件203上达合乎需要的时间段,以允许第一隔间和第二隔间的界面处的足够量的塑料熔化,由此增加可用于连结第一隔间和第二隔间的材料。随后,保持器单元202和204的联接运动可用于使保持器单元202和204朝彼此沿第一方向242移动,以形成第一容器206和第二容器214的部分之间的接头。此外,保持器单元202和204的该联接运动可执行,同时分离构件在分离第一容器206和第二容器214的部分之后移动远离第一容器206和第二容器214。
有利地,联接装置200的一个或更多个构件在性质上为一次性的,由此减小两个或更多个样本污染的机会。此外,本申请的联接装置200构造成有效且高效地解冻,接近,并且将内容物(样本)从第一容器204如冷冻瓶以无菌方式在最小使用者介入下以时间有效的方式转移至合乎需要的收集装置。此外,联接装置200构造成以无菌方式将样本混合物转移到生物反应器中,同时设置在可位于生物安全柜的界限外的任何非无菌环境中。
图3示出了在将第一容器206和第二容器214设置在联接装置200的它们的相应槽口228和230中之前的图2的联接装置200的实施例250。如所示,槽口230构造成收纳第二容器214。此外,如图4的实施例251中所示,槽口228构造成收纳第一容器206。分离构件203和第一容器206和第二容器214的相对位置使得分离构件203的刀片沿方向245的运动分离第一容器206和第二容器214的部分,以形成样本通路组件260的隔间266和268。如图5中所示,在加载第一容器206和第二容器214之后,联接装置闭合。闭合的联接装置大体上由附图标记254代表。现在参照图6,在所示实施例255中,分离构件203的温度使用温度传感器252监测。为了确保用于样本的无菌环境,分离构件203在第一容器206和第二容器214的部分分离期间保持在高温下,并且与第一容器206和第二容器214紧密接触。
分离构件203沿大体上由箭头257代表的方向的刷过动作执行成使第一容器206和第二容器214的部分262和264分别从第一容器206和第二容器214的部分266和268分出。
参照图7的实施例270,在分离构件203使第一容器206和第二容器214的部分分出之后,第一容器206和第二容器214的部分266和268与彼此对准。在所示实例中,第一保持器单元202和第二保持器单元204可关于彼此沿第二方向244移动,以对准部分266和268,它们形成样本通路组件260的第一隔间和第二隔间。
此外,如图8的实施例272中所示,第一保持器单元202和/或第二保持器单元204可朝彼此沿第一方向242移动,并且压靠彼此来形成第一容器206和第二容器214的部分266和268之间的接头,以形成具有第一隔间266和第二隔间268的样本通路组件260。在一个实施例中,接头可为热接头274,其由于第一容器206和第二容器214的部分266和268的界面处的第一容器206和第二容器214的材料的熔化和熔合而形成。可注意到的是,在分离动作完成之后和在形成热接头274之前,分离构件203可缩回,如图8中所示。可选地,第一容器206和第二容器214的部分262和264可使用机械方法或其它方法来从连接装置200除去。
图9为组装样本通路组件400,如图1的样本通路组件100的方法的示意图。在所示实施例中,样本通路组件400从第一容器402和第二容器410的部分组装。此外,第一容器402包括第一侧404和第二侧406。此外,第一容器402的第一侧404闭合,然而第一容器402的第二侧406构造成按需要开启或闭合。经由实例,第二侧406可包括开口端和对应的帽408,其中帽408构造成设置在开口端上来闭合第一容器402。在一个实例中,第一容器402可为具有可除去的螺纹盖的瓶。在一个实施例中,帽408可除去或卸下来将样本409设置在第一容器402中。随后,帽408可置于第一容器上,以闭合第一容器402的第二端406。在一个实例中,第一容器402可为冷冻瓶、聚合物管或两者。
此外,第二容器410可包括第一侧412和第二侧414。第二容器410的第一侧412和第二侧414可闭合。此外,第二容器410的第一侧412可至少包括入口通路416和出口通路418。在一些实施例中,设置在第二容器410内的入口通路416的一部分可比设置在第二容器410内的出口通路418的一部分更长。在一些实施例中,第二容器410可在联接第二容器410和第一容器402之前预先灭菌。第二容器410可为管、瓶,或构造成提供可构造成联接于第一容器402的界面的任何其它容器。
此外,入口通路416和出口通路418可在联接第一容器402和第二容器410之前灭菌。此外,在一个实施例中,第二容器410可在联接第一容器402和第二容器410的部分来形成样本通路组件400之前联接于一个或更多个其它构件。在一个实施例中,这些其它构件可在样本通路组件400外。经由实例,第二容器410可联接于培养器皿,如构造成收集样本的生物反应器,或构造成泵送样本通路组件400中的生长介质的泵。在一个实施例中,第二容器410的入口通路416可在联接第一容器402和第二容器410之前操作性地联接于生长介质源(图9中未示出)。此外,出口通路418可在联接第一容器402和第二容器410之前联接于收集装置(图9中未示出)。收集装置的非限制性实例可包括细颈瓶或生物反应器。
在一个实施例中,样本通路组件400可为一次性装置。此外,如所示,样本通路组件400可通过使设置成更接近第一容器402和第二容器410的相应的第二侧406和414的、第一容器402和第二容器410的相应部分420和422分离,同时随后分别联接第一容器402和第二容器410的其余部分424和426的界面来形成样本通路组件400来形成。
此外,在一个实施例中,第一容器402和第二容器410的部分424和426分别可关于彼此移动来使第一容器402和第二容器410的其余部分424和426关于彼此对准,使得第一容器402和第二容器410的其余部分424和426设置在彼此上。尽管在所示实施例中,第一容器402和第二容器410示为具有各处的相似截面面积,然而在一些实施例中,只有接触来形成样本通路组件400的第一容器402和第二容器410的其余部分424和426的界面可具有相似截面。经由实例,第一容器402可为袋形,具有设置在袋的第二侧处的喷口状结构,其中该喷口状结构可具有与第二容器410的界面的截面相似的截面。在特定实施例中,第一容器402可为冷冻袋。
此外,第一容器402和第二容器410可压靠彼此来形成第一容器402和第二容器410的其余部分424和426之间的接头,以形成样本通路组件400。步骤如下:(1)分离第一容器402和第二容器410的部分420和422,以及(2)使其余部分424和426对准,以及(3)联接其余部分424和426可在分离构件427仍在合乎需要温度下的同时执行,以防止样本409不合乎需要地暴露于第一容器402和第二容器410外的环境。
此外,接头432可由于第一容器402和第二容器410的其余部分424和426的界面的联接而形成。此外,第一容器402和第二容器410的其余部分424和426可形成样本通路组件400中的第一隔间428和第二隔间430。在一个实施例中,接头432可为热熔合接头、化学熔合接头或两者。在一个实例中,热熔合接头可为气密性密封的接头。热熔合接头可在第一容器402和第二容器410的部分420和422使用在加热状态中的分离构件427与部分424和426分离,并且其余部分424和426的界面紧接在使部分420和422与第一容器402和第二容器410分离之后接触时形成。部分424和426的界面处的熔化材料可熔合在一起来形成热接头。因此,合乎需要的是,材料至少存在于适合于形成热接头的部分424和426的界面处。在一些实施例中,第一容器402和第二容器410或至少第一容器402和第二容器410的部分424和426的界面处的材料可由热塑性塑料制成。热塑性塑料的非限制性实例包括聚乙烯、乙烯醋酸乙烯酯(EVA)、聚氯乙烯(PVC)、聚丙烯、尼龙或它们的组合。此外,联接装置200的构件位置框架可由聚氧化乙烯(POM)、酚醛塑料、聚醚醚酮(PEEK)、尼龙、聚丙烯、聚苯硫醚(PPS)、聚对苯二甲酸乙二醇酯(PET)等制成。
此外,在样本通路组件400中,入口通路416可设置成关于出口通路418更接近第一隔间402的第一侧404。随后,在操作中,入口通路416相比于出口通路418的位置更接近样本409,以便于样本409和生长介质的混合。然而,在备选实施例中,出口通路418可设置成相比于入口通路416相对更接近于样本409,以提供样本409的有效转移。此外,生长介质在样本通路组件400中如由箭头434所示经由入口通路416引入。与生长介质混合的样本409从样本通路组件400抽取,如由箭头436表示。此外,出口通路418用于将样本和生长介质的混合物(样本混合物)抽取至收集装置。
此外,生长介质以确定速率引入在样本通路组件400中。样本通路组件400中的生长介质的引入的速率保持在合乎需要的值下,以便于生长介质与样本的混合(箭头439)。样本混合物的抽取速率大致类似于样本通路组件400中的生长介质的引入速率。此外,引入和抽取的速率保持成以便便于样本409与到来的生长介质的混合,以便于样本混合物从样本通路组件400至收集装置的有效转移。然而,可注意到的是,生长介质的相对高的流率可不合乎需要地引起剪切。因此,可合乎需要的是保持生长介质的引入速率,其类似于不在细胞上引起过大剪切的样本混合物的抽取的速率。在一个实施例中,转移出样本通路组件400的样本的体积可在从大约1vol%到大约100vol%、80vol%到大约100vol%,或90vol%到大约100vol%的范围中。可注意到的是,在有效混合的情况下,转移出样本通路组件400的样本的百分比可由引入到样本通路组件400中的生长介质的体积导出。由于样本通路组件400的容积为恒定的,并且假定引入在样本通路组件400中的生长介质的量类似于从样本通路组件抽取的样本混合物的量,用于稀释(或细胞回收)的等式可为指数函数。经由实例,关于引入在样本通路组件中的1ml体积的样本和50ml体积的生长介质,在一些实施例中,来自样本通路组件400的样本(具有合乎需要的混合)的回收可高达大约99.99%。
有利地,样本通路组件400便于样本409从第一容器402如瓶或冷冻瓶以最小操作者介入转移至收集装置。此外,样本通路组件400便于样本409回收方面和从第一容器402转移到收集装置所需的时间方面的有效转移。此外,样本通路组件400便于以无菌方式接近样本409,而与样本接近组件400设置在其中的环境无关。
图10示出了具有加热构件502的加热组件500的一部分的截面俯视图,加热构件502构造成加热本体508的至少一部分,如第一容器(图10中未示出),或样本通路组件的一部分(图10中未示出),或第二容器的一部分(未示出)。经由实例,最初,加热构件502可构造成加热样本、样本混合物和/或生长介质。在特定实例中,样本可为冷藏保存的样本。在该实例中,加热构件502可构造成使冷藏保存的样本解冻来形成液体细胞悬液以实现培养液转移。
可注意到的是,生长介质通常在大约4℃下储存。然而,使用具有大约4℃或更低的温度的生长介质可消极地影响细胞生长。结果,可合乎需要的是将生长介质预热至少至室温。在一些实施例中,在转移样本混合物时,加热构件502可用于使冷藏保存的样本解冻并且加热生长介质。在一个实施例中,加热构件502可用作用于冷生长介质的联机加热器。
在所示实施例中,加热构件502包括加热器504和导热器506。在一个实例中,加热器504可具有柔性且可顺应的结构。在非限制性实例中,加热器504可为薄膜加热器。加热器504的其它非限制性实例可包括非接触式加热器,如红外(IR)加热器、具有在器皿内循环的温度调节流体的弹性器皿,或两者。
此外,导热器506可构造成便于热从加热器504到本体508的一致传递。此外,导热器506可便于热至本体508的一致分配。导热器506的非限制性实例可包括掺杂有导热颗粒的导热泡沫和/或橡胶。导热器506的其它非限制性实例可包括加热的(或温度受控的)囊,其可符合第一容器。在一个实施例中,加热构件502可为可顺应的结构。此外,加热构件502可由一个或更多个部分制成。加热构件502的一个或更多个部分可构造成围绕本体508的确定部分可顺应地设置。
在所示实施例中,加热组件500可包括温度传感器510,其操作性地联接于加热构件502或本体508。然而,在其中加热组件500使用两个或更多个温度传感器的情况下,两个或更多个温度传感器可操作性地联接于加热构件502和本体508两者。结果,温度传感器510可构造成感测加热构件和/或本体508的温度。温度传感器510的非限制性实例可包括热电偶、热敏电阻、电阻温度装置(RTD)或它们的组合。加热组件500还可包括温度控制器512,其操作性地联接于温度传感器510,以控制加热构件504和/或本体508的温度。
图11示出了具有联接装置602、控制器单元604和处理器单元606的示例性自动系统600。此外,联接装置602操作性地联接于生长介质源608。具体而言,生长介质源608可使用样本通路组件614的入口通路616操作性地联接于样本通路组件614。在所示实施例中,样本通路组件614可构造成使用泵612来接收设置在生长介质源608中的生长介质610。在非限制性实例中,泵612可为蠕动泵。泵612可构造成便于生长介质610从生长介质源608至设置在联接装置602中的样本通路组件614的转移。此外,泵612可构造成便于生长介质610在预定速率下至样本通路组件614的转移。具体而言,生长介质610可用于将内容物冲出样本通路组件614。具体而言,在操作中,生长介质610可用于将内容物冲出样本通路组件614的第一容器(图11中未示出)。
在一些实施例中,生长介质610可在将生长介质610转移至样本通路组件614之前或当时加热至确定温度。在一个实施例中,生长介质610的确定温度可构造成便于收集装置620中的细胞生长。此外,样本通路组件614的出口通路618可操作性地联接于外部装置,如收集装置620。在一些实施例中,收集装置620可构造成接收与生长介质610混合的样本混合物。在非限制性实例中,收集装置可为生物反应器。
此外,控制单元604可用于共同地代表在自动系统600中使用的各种控制装置,其中控制装置构造成控制和调节自动系统600的操作。经由实例,在所示实施例中,控制单元604可构造成使用流入控制器622来控制生长介质610的输入流。
此外,一个或更多个温度控制器624可用于控制样本或样本混合物的温度。在非限制性实例中,温度控制器624可构造成控制设置在第一容器(例如,瓶)中的样本、生长介质610中的一个或更多个的温度,以及加热构件(图11中未示出)的温度。可注意的是,在某些实施例中,可合乎需要的是在形成样本通路组件614之前使样本解冻。
在一些实施例中,附加的温度控制器624可用于控制在联接装置602中使用的分离构件(图11中未示出)的温度。在一些实施例中,控制器单元604可使用传感器来感测控制的参数。经由实例,控制器单元604可使用红外温度传感器用于感测分离构件的温度,或使用热电偶以感测加热构件和/或样本通路组件614的温度。此外,尽管未示出,但在一些实施例中,一个或更多个温度传感器可操作性地联接于收集装置620,以感测收集装置620的温度。在一个实例中,热电偶可联接于收集装置620的外表面。
此外,控制器单元604可包括运动控制器626,其中运动控制器626可构造成控制自动系统600的一个或更多个构件沿一个或更多个方向632,633和634的运动。在一些实施例中,运动控制器626可构造成控制一个或更多个保持器单元628和630、分离构件或两者的运动。
此外,自动系统600的处理器单元606可构造成处理来自控制器单元604的数据。在某些实施例中,处理器单元606还可联接于一个或更多个使用者输入输出装置(未示出),用于接收来自使用者的命令和输入。例如,输入输出装置可包括如键盘、触摸屏、麦克风、鼠标、控制面板、显示装置、脚动开关、手动开关和/或按钮的装置。此外,处理器单元606和/或控制器单元604可构造成联接于其它装置,如但不限于收集装置620、生长介质源608、泵612或它们的组合,以控制或监测这些装置的操作。在一个实施例中,处理器单元606和控制器单元604可集成到单个单元中。
在备选实施例中,控制器单元604的各个控制器可具有相应的独立处理器。在一些实施例中,处理器单元606和/或控制器单元604可构造成将相关数据储存在储存库(未示出)中。在一个实施例中,储存库可包括装置,如硬盘驱动器、软盘驱动器、光盘读/写(CD-R/W)驱动器、数字多功能盘(DVD)驱动器、闪速驱动器和/或固态储存装置。
此外,自动系统600可包括输出装置638,其可构造成显示代表自动转移的发展或自动种子培养过程的数据,或关于自动系统600的操作的任何其它参数。在一个实例中,输出装置638可构造成显示由在自动系统600中使用的一个或更多个传感器感测的感测数据。
有利地,自动系统600可包括提供物,其用于将第一容器和第二容器简单地设置在联接装置602中的指定位置,并且例如通过使用开关636来开始联接装置602的操作,以开始样本混合物的转移或开始自动种子培养过程。因此,自动系统600以最小操作者介入执行种子培养过程,由此减小人为误差和与其相关联的非可预计的结果的可能性。此外,用于自动系统600的周围环境可或可不为无菌的。在一个实施例中,第一容器和第二容器、入口和出口管路等可在性质上是一次性的,由此通过防止来自前一批次等的污染物的引入来使自动系统600甚至不太易于污染。
此外,自动系统600可由未训练的操作者操作。由于自动系统600能够在非无菌环境中无菌地接近瓶的内容物,故可不需要层流罩或清洁室,这可显著地减小底板空间要求和基础设施成本。此外,自动系统600是全自动的,并且第二容器在功能上闭合,这相比于手动过程显著地降低了污染的风险。
在一些实施例中,自动系统600可构造成以自动方式有效地操作。此外,自动系统600可在无菌或非无菌环境中以相同或相似的结果操作。在特定实施例中,在第一容器为冷冻瓶的情况下,自动系统600构造成接收冻结或冷藏保存的冷冻瓶或预先解冻或部分地冻结的冷冻瓶,其中冷冻瓶包括具有由使用者提供的几千万细胞的样本。此外,自动系统构造成使冷冻瓶解冻,接近,并且将细胞从冷冻瓶转移至收集装置,如生物反应器。有利地,与自动系统设置在其中的环境无关,系统600构造成实现无菌接近和样本从冷冻瓶转移到生物反应器用于进一步处理。在特定实例中,样本通路组件中的样本可接近和转移用于将细胞培养成几十亿,以灌注较大规模的生物反应器。
在某些实施例中,样本通路组件和使用样本通路组件用于转移样本或样本混合物的自动系统可向生物制药客户提供自动生产底板解决方案,以利用冻结或冷藏保存的瓶原料来开始,并且产生扩张的培养液以备下一生产器皿(例如,生物反应器,如但不限于WAVE袋®或Xcellerex®生物反应器)。
此外,在某些实施例中,设置在样本通路组件中的冷藏保存的样本细胞可转移至适合的培养器皿用于细胞生长。此外,在这些实施例中,以解冻冷藏保存的样本开始并且包括解冻冷藏保存的样本的步骤并且以将样本转移至适合的培养器皿结束的步骤可为自动的。此外,包括解冻冷藏保存的样本细胞、接近样本细胞和将样本细胞转移至适合的培养器皿的步骤的过程可在过程期间以最小操作者介入需要为自动的。在一个实施例中,样本通路组件可为容器,如但不限于冷冻瓶。然而,在其它实施例中,第一容器可为瓶、管、移液管、细颈瓶,或构造成将样本收纳在无菌环境中的任何其它容器。此外,在一些实施例中,培养器皿可用作接种反应器,其用作用于生产规模活动的种子源。在备选实施例中,收集装置可简单地为灭菌袋、灭菌细颈瓶,或构造成收集样本的任何其它适合的器皿。在一个实施例中,在使用联接装置之前,收集装置可无菌地联接于联接装置。作为备选,收集装置可预先联接于联接装置。经由实例,收集装置可预先联接于第二容器。
图12为将样本如冷藏保存的样本自动转移至收集装置(如,生物反应器或细颈瓶)作为用于细胞生长或接种的种子培养过程的一部分的示例性方法700。
在框702处,方法以提供具有样本的第一容器开始。样本可为冷藏保存或冻结的细胞样本。在一个实例中,细胞可为哺乳动物细胞。第一容器可为仅包含感兴趣的微生物的器皿,即,冷冻瓶或具有细胞样本的瓶。在框704处,可提供具有入口通路和出口通路的第二容器。在一个实施例中,第二容器可与入口通路和出口通路预先配合,并且预先灭菌。
此外,在框705处,可提供具有加热构件和分离构件的联接装置。此外,联接装置可包括第一保持器单元,其操作性地联接于加热构件,并且构造用于收纳第一容器。此外,联接装置可包括第二保持器单元。在一个实施例中,联接装置可预先灭菌。
可选地,在框706处,第二容器可操作性地联接于一个或更多个外部装置,如但不限于生长介质源、泵、收集装置或它们的组合。此外,第二容器也可联接于加热构件,其中加热构件可构造成在将生长介质引入在第一容器中之前预先加热生长介质。
此外,在框708处,第一容器可设置在联接装置的第一保持器单元中。具体而言,第一容器可设置在第一保持器单元中的指定槽口中。此外,加热构件可设在槽口中,并且加热构件可构造成操作性地联接于第一容器,以在样本转移之前和期间将样本加热至确定温度。在非限制性实例中,第一容器可为具有冷藏保存的样本的冷冻瓶。在该实施例中,加热构件可构造成将最初可处于-80℃或更低的冷藏保存的样本解冻和加热至大约37℃的温度。作为备选,水浴或恒温珠浴可用于在第一容器设置在联接装置的第一保持器中之前加热设置在第一容器中的样本。
此外,在框710处,第二容器可设置在联接装置的第二保持器单元中。具体而言,第二容器可设置在第二保持器单元中的相应槽口中。在一个实施例中,构造成收纳第二容器的槽口可包括加热构件。加热构件可构造成将第二容器和穿过第二容器的生长介质加热至合乎需要的温度。结果,引入至样本的生长介质可处于适合于接种和细胞生长的合乎需要温度。
此外,温度传感器(例如,热电偶)可用于感测第一容器和/或加热构件的温度。此外,温度控制器可用于将第一容器的温度或加热构件的温度调制成大约37℃来使样本解冻。将温度保持在37℃或低于37℃确保了样本的细胞不过热。加热构件可用于主要取决于第一容器的尺寸来在确定量的时间内使第一容器解冻。在一些实施例中,加热构件可构造成使第一容器快速解冻,同时保持与常规使用但耗时的程序(如,水浴和恒温珠浴)相当的细胞活性和生长。
此外,在框712处,在将第一容器和第二容器设置在它们的相应槽口中之后,第一容器和第二容器的部分可使用分离构件与第一容器和第二容器的其余部分分离。
此外,在框714处,紧接在第一容器和第二容器的部分的分离之后,第一容器和第二容器的其余部分可对准。此外,在框716处,在分离期间或紧接在分离之后,第一容器和第二容器的其余部分可压靠彼此,以在分离构件缩回的同时或之后物理地联接其余部分来形成样本通路组件。在其中加热刀片用作分离构件的一个实施例中,其余部分可热熔合。然而,在备选实施例中,其它联接技术也可使用。
此外,在框718处,在形成样本通路组件之后,生长介质可提供至样本通路组件,并且随后至操作性地联接于样本通路组件的收集装置。在特定实例中,在形成样本通路组件之后,蠕动泵可打开,以通过样本通路组件将生长介质提供到生物反应器中。生长介质和样本的有效混合由样本通路组件的设计,如入口和出口通路的定位,以及设置在样本通路组件内的入口通路的大小促进,以最大化样本的回收。
在某些实施例中,生长介质的流率和生长介质提供至样本通路组件的量可基于以下中的一个或更多个计算:a)合乎需要的细胞回收,2)合乎需要的剪切,以及3)为下一次扩张接种的样本混合物中的合乎需要细胞密度。此外,生长介质的流率可以便防止细胞上的过大剪切和确保良好混合。结果,在框720处,样本可从样本通路组件有效地回收,并且从样本通路组件转移至收集装置。
此外,步骤712到718或712到720可利用由操作者提供到系统的最少信息执行。经由实例,操作者可仅需要输入瓶类型和/或瓶中的样本的合乎需要体积。在一些实施例中,假定收集装置已经连接于第二容器,一旦提供第一容器和第二容器,则对于形成样本通路组件的步骤而言,可不需要另外的操作者介入。系统可从加热样本的步骤直到将样本混合物转移到收集装置的步骤为自动的。作为备选,可在样本通路组件形成之后需要的最小操作者介入伴有操作开关来向泵和样本混合物转移到收集装置中涉及的其它构件供能。
此外,流程图700中描述的方法的步骤702-720可或可不按如所示的相同顺序进行。经由实例,第二容器可提供在第一容器之前,或者生长介质源可在将第二容器设置在联接装置中之前预先联接。
有利地,样本转移的装置、系统和方法设计成灵活的,容易操作并且基础实施友好(例如,不需要无菌环境)。此外,自动系统可置于工作台或推车上,由此提高了整个细胞生产底板的灵活性。另外,自动系统可不需要技术人员来操作系统。此外,样本通路组件和收集装置的一次性性质允许生产设施中的快速转换。此外,本说明书的系统和方法在第一容器和第二容器的安装之后在较大程度上为自动的,并且由此较不劳动密集。
尽管本文中示出和描述了本公开的仅某些特征,但本领域技术人员将想到许多改型和变化。因此,将理解的是,所附权利要求旨在覆盖落入本公开的真实精神内的所有此类改型和变化。
- 还没有人留言评论。精彩留言会获得点赞!