一类大环内酯化合物及其在制备抗肿瘤药物中的应用的制作方法
本发明属于天然产物领域,具体涉及五个大环内酯类化合物及其在制备抗肿瘤药物中的应用。
背景技术:
:
长期以来,恶性肿瘤已成为严重危害人类生命和生活质量的主要疾病之一。据报道,恶性肿瘤已经成为我国居民首要死因,而且,随着经济的发展以及人们对环境保护的不力,恶性肿瘤的致死率还在不断增长。世界卫生组织预测,到2020年,将有2000万新发恶性肿瘤病例,其中死亡人数达1200万,且绝大部分将发生在发展中国家。对于恶性肿瘤的治疗,天然产物及其衍生物药物发挥着重要作用。据报道,1981年到2008年间,天然产物来源的抗肿瘤药物占上市抗肿瘤药物的60%以上,而且,新型天然产物及其衍生物作为新的抗肿瘤药物所占数量还在不断增加。
技术实现要素:
:
本发明的第一个目的是提供五个具有抗肿瘤活性的大环内酯类化合物及其药用盐。
本发明的大环内酯类化合物或其药用盐,其结构如式(Ⅰ)、(Ⅱ)和(Ⅲ)所示:
式(Ⅰ)中,化合物1:β-OH;或化合物2:α-OH;或式(Ⅱ)中,化合物3:β-OH;或化合物4:α-OH;或式(Ⅲ)中,化合物5。
本发明人通过对海洋放线菌Streptomyces sp.SCSIO ZJ89发酵提取物的HPLC-DAD图谱分析,发现其所产次级代谢产物紫外吸收特征鲜明,通过摇床放大发酵和提取纯化,得到5个紫外吸收基本一致的同类化合物。经结构分析,其被确定为大环内酯类化合物,具体结构如式(Ⅰ)、(Ⅱ)和(Ⅲ)所示,化合物1:β-OH;或化合物2:α-OH;或式(Ⅱ)中,化合物3:β-OH;或化合物4:α-OH;或式(Ⅲ)中,化合物5。
通过对化合物1、化合物2、化合物3、化合物4和化合物5的抗肿瘤活性评价,发现化合物1-5对人肺癌(A549)、人鼻咽癌(CNE2)、人宫颈癌(HeLa)、人肝癌(HepG2)、人乳腺癌(MCF-7)具有明显抑制作用。
因此,本发明的第二个目的是提供化合物1、化合物2、化合物3、化合物4或化合物5在制备抗肿瘤药物中的应用。
优选,所述的抗肿瘤药物为抗人肺癌、人鼻咽癌、人宫颈癌、人肝癌或人乳腺癌的药物。
本发明的第三个目的是提供一种抗肿瘤药物,其特征在于,包括有效量的作为活性成份的如式(Ⅰ)、(Ⅱ)和(Ⅲ)所示的化合物1、化合物2、化合物3、化合物4或化合物5,或其药用盐,和药学上可以接受的载体。
优选,所述的抗肿瘤药物为抗人肺癌、人鼻咽癌、人宫颈癌、人肝癌或人乳腺癌的药物。
本发明的第四个目的是提供一种制备化合物1、化合物2、化合物3、化合物4和化合物5的方法,其特征在于,所述的化合物1、化合物2、化合物3、化合物4和化合物5是从海洋放线菌Streptomyces sp.SCSIO ZJ89的发酵产物中制备分离得到的。
优选,具体步骤如下:
A、制备海洋放线菌Streptomyces sp.SCSIO ZJ89的发酵产物;
B、将海洋放线菌Streptomyces sp.SCSIO ZJ89的发酵产物进行离心分离,获得发酵液和菌丝体,发酵液用丁酮萃取,丁酮萃取液浓缩得发酵液浸膏;菌丝体用丙酮萃取,丙酮萃取液经浓缩得菌体浸膏,该浸膏用硅胶分离,采用氯仿/甲醇从100/0,98/2,96/4,94/6,92/8,90/10,80/20,50/50,0/100,v/v梯度洗脱顺序得9个组分A1-A9;
氯仿/甲醇94/6洗脱得馏份-组分A4用氯仿/甲醇100/0,98/2,96/4,94/6,92/8,90/10,v/v梯度洗脱顺序得6个组分B1-B6,氯仿/甲醇96/4洗脱得馏份-组分B3用氯仿/甲醇100/0,98/2,96/4,94/6,92/8,v/v得5个组分C1-C5;
氯仿/甲醇92/8洗脱得馏份-组分A5、氯仿/甲醇94/6洗脱得馏份-B4合并,然后用石油醚/乙酸乙酯P/E,80/20,70/30,60/40,55/45,50/50,40/60,30/70,20/80,v/v梯度洗脱顺序得到组分D1-D8,合并氯仿/甲醇94/6洗脱得馏份-组分C4、石油醚/乙酸乙酯40/60洗脱得馏份-D6和石油醚/乙酸乙酯30/70洗脱得馏份-D7,经高效液相纯化得到化合物5,合并组分氯仿/甲醇98/2洗脱得馏份-C2和氯仿/甲醇96/4洗脱得馏份-组分C3,经高效液相纯化得到化合物1、化合物4、化合物3和化合物2。
所述的制备海洋放线菌Streptomyces sp.SCSIO ZJ89的发酵产物是以海洋放线菌Streptomyces sp.SCSIO ZJ89作为发酵菌株在放大发酵培养基中培养得到海洋放线菌Streptomyces sp.SCSIO ZJ89的发酵产物;所述的放大发酵培养基,按总质量分数100%计,包括可溶性淀粉0.5%,大豆粉0.5%,葡萄糖2%,酵母膏0.2%,蛋白胨0.2%,K2HPO40.05%,MgSO4·7H2O 0.05%,NaCl 0.4%,CaCO3 0.2%,粗海盐3%,pH 7.2-7.4,余量为水。
本发明的大环内酯类化合物-化合物1、化合物2、化合物3、化合物4和化合物5对肿瘤细胞具有明显的抑制作用,可以用于制备抗肿瘤药物,用于治疗肿瘤,因此本发明为开发新的抗肿瘤药物提供了备选化合物,对开发中国海洋药物资源具有重要的意义。
本发明的海洋放线菌Streptomyces sp.SCSIO ZJ89于2016年11月22日保藏于中国普通微生物菌种保藏管理中心(CGMCC),地址:北京市朝阳区北辰西路1号院中科院微生物研究所,其保藏编号为:CGMCC NO.13322。
附图说明:
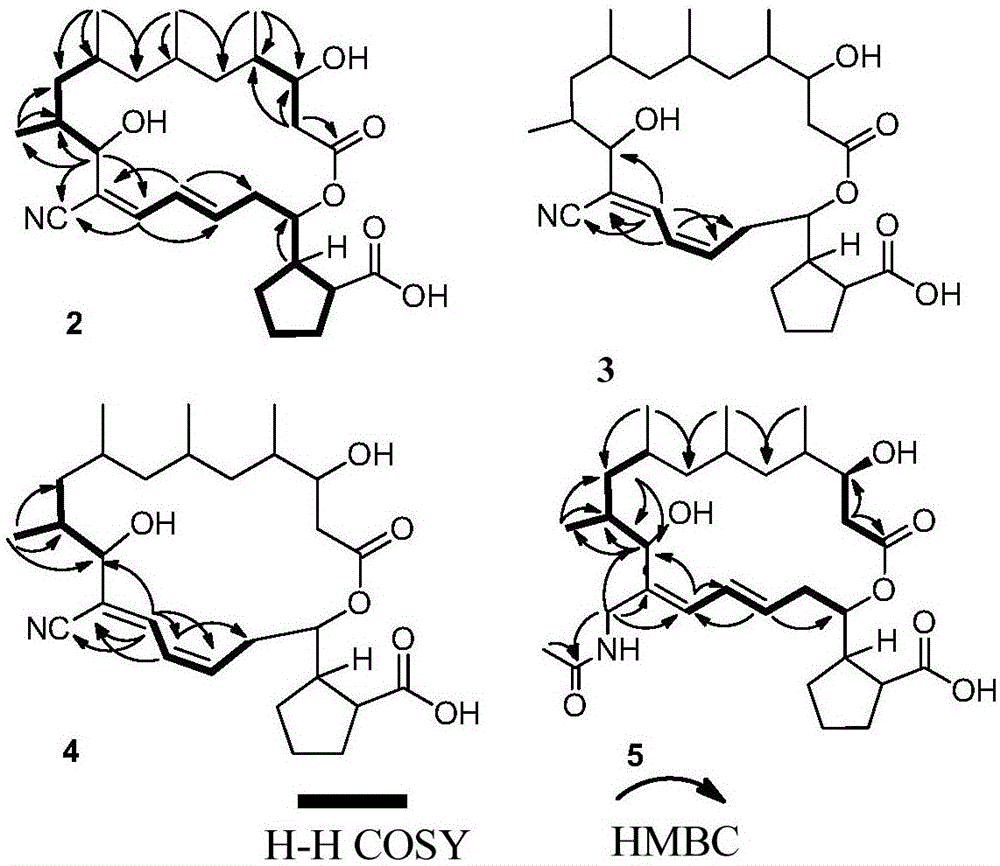
图1是化合物2-5的1H-1H COSY和部分HMBC相关信息,其中2代表化合物2,3代表化合物3,4代表化合物4,5代表化合物5。
具体实施方式:
以下实施例是对本发明的进一步说明,而不是对本发明的限制。
实施例1:
如式(Ⅰ)、(Ⅱ)和(Ⅲ)所示的化合物1、化合物2、化合物3、化合物4或化合物5的制备和结构鉴定
一、如式(Ⅰ)、(Ⅱ)和(Ⅲ)所示的化合物1、化合物2、化合物3、化合物4或化合物5的制备
1.种子培养:
(1)种子培养基配方:按质量分数100%计,包括可溶性淀粉0.5%,大豆粉0.5%,葡萄糖2%,酵母膏0.2%,蛋白胨0.2%,K2HPO4 0.05%,MgSO4·7H2O 0.05%,NaCl 0.4%,CaCO3 0.2%,粗海盐3%,pH 7.2-7.4,余量为水。按照配方将上述物质混合在一起,配好后分装于250mL的锥形瓶中,每瓶装50mL,121℃灭菌20分钟,做为备用的种子培养基。
(2)种子的培养:将海洋放线菌Streptomyces sp.SCSIO ZJ89的菌丝体或孢子接入到上述种子培养基中,以200rpm的转速、在28℃下、摇床培养36小时得种子培养液。
2.放大发酵培养:
(1)放大发酵培养基配方:按总质量分数100%计,包括可溶性淀粉0.5%,大豆粉0.5%,葡萄糖2%,酵母膏0.2%,蛋白胨0.2%,K2HPO4 0.05%,MgSO4·7H2O 0.05%,NaCl 0.4%,CaCO3 0.2%,粗海盐3%,pH 7.2-7.4,余量为水。按照配方将上述物质混合在一起,分批配好后共计21.8L放大发酵培养基,配好后分装于1000mL的锥形瓶中,每瓶装200mL,121℃灭菌20分钟,做为备用的放大发酵培养基。
(2)发酵培养:
在无菌操作下,将培养好的种子培养液分别接种于放大发酵培养基中,每1000ml锥形瓶(含200mL放大发酵培养基)接种一瓶种子培养液(50mL)。每50ml种子培养液接入装有200mL放大发酵培养基的1000mL锥形瓶中,以200rpm的转速、在28℃下、摇床培养7天得海洋放线菌Streptomyces sp.SCSIO ZJ89发酵产物。
3.提取分离:
将上述海洋放线菌Streptomyces sp.SCSIO ZJ89发酵产物,以3600rpm离心,得上清发酵液和沉淀菌丝体。上清发酵液用丁酮等体积萃取3次,丁酮萃取液在低于40℃减压浓缩得发酵液浸膏;沉淀菌丝体用共计3L丙酮反复萃取三次,丙酮萃取液在低于40℃下减压浓缩得菌体浸膏;经HPLC-DAD检测后,合并发酵液浸膏和菌体浸膏共计得约31.22g浸膏。该浸膏用100-200目硅胶分离,经拌样、干法装柱后,采用氯仿/甲醇(100/0,98/2,96/4,94/6,92/8,90/10,80/20,50/50,0/100,v/v)梯度洗脱顺序得9个组分(A1-A9)。组分A4(氯仿/甲醇94/6洗脱的馏份)用氯仿/甲醇(100/0,98/2,96/4,94/6,92/8,90/10,v/v)梯度洗脱顺序得6个组分(B1-B6)。组分B3(氯仿/甲醇96/4洗脱的馏份)用氯仿/甲醇(100/0,98/2,96/4,94/6,92/8,v/v)得5个组分(C1-C5)。组分A5(氯仿/甲醇92/8洗脱的馏份)、B4(氯仿/甲醇94/6洗脱的馏份)合并,然后用石油醚/乙酸乙酯(P/E,80/20,70/30,60/40,55/45,50/50,40/60,30/70,20/80,v/v)梯度洗脱顺序得到组分D1-D8。合并组分C4(氯仿/甲醇94/6洗脱的馏份)、D6(石油醚/乙酸乙酯40/60洗脱的馏份)和D7(石油醚/乙酸乙酯30/70洗脱的馏份),以254nm波长做检测、采用2.5ml/min的流速、以42/58(水/乙腈,v/v)用反相柱YMC-Pack ODS-A column(250×10mm,5μm)进行半制备高压液相分离(SP-HPLC)洗脱,在保留时间为26min得到化合物5(39.9mg),同样,合并组分C2(氯仿/甲醇98/2洗脱的馏份)-C3(氯仿/甲醇96/4洗脱的馏份),以254nm波长做检测、采用2.5ml/min的流速、以40/60(水/乙腈,v/v)用反相柱YMC-Pack ODS-A column(250×10mm,5μm)进行半制备高压液相分离(SP-HPLC)洗脱,将在17.8min、20.4min、22.7min、24.7min得到化合物1(139.1mg)、化合物4(3.7mg)、化合物3(3.6mg)和化合物2(14.3mg)。
二、化合物1、化合物2、化合物3、化合物4和化合物5的结构鉴定
对化合物1、化合物2、化合物3和化合物4和化合物5进行结构分析测试,得到以下理化性质数据,其核磁数据如表1和2所示:
化合物1:白色无定形粉末;[α]25D-18.0(c12.1,ethanol);(+)-HR-ESI-MS m/z490.3171[M+H]+(calcd for C28H44NO6,490.3163)and 512.2986[M+Na]+(calcd for C28H43NNaO6,512.2983)。
化合物2:白色无定形粉末;[α]25D+14.1(c 3.0,ethanol);(+)-HR-ESI-MS m/z 490.3161[M+H]+(calcd for C28H44NO6,490.3169)and 512.2987[M+Na]+(calcd for C28H43NNaO6,512.2988)
化合物3:白色无定形粉末;[α]25D+41.1(c 2.6,ethanol);(+)-HR-ESI-MS m/z 490.3162[M+H]+(calcd for C28H44NO6,490.3163)and 512.2980[M+Na]+(calcd for C28H43NNaO6,512.2983)
化合物4:白色无定形粉末;[α]25D-35.8(c 3.1,ethanol);(+)-HR-ESI-MS m/z 490.3161[M+H]+(calcd for C28H44NO6,490.3163)and 512.2986[M+Na]+(calcd for C28H43NNaO6,512.2983)
化合物5:白色无定形粉末;[α]25D-4.7(c 8.8,ethanol);(+)-HR-ESI-MS m/z536.3566[M+H]+(calcd for C30H50NO7,536.3582)and 558.3389[M+Na]+(calcd for C30H49NNaO7,558.3401)
表1:化合物1-3在CD3OD.中的1H(500MHz)和13C NMR(125HMz)数据
*Resonances overlapped
表2:化合物4-5在CD3OD.中的1H(500MHz)和13C NMR(125HMz)数据
化合物2、化合物3、化合物4和化合物5的2D NMR相关信息如图1所示:
根据以上理化数据分析可知,化合物1、化合物2、化合物3、化合物4和化合物5的具体结构如式(Ⅰ)和(Ⅱ)所示。
式(Ⅰ)中,化合物1:β-OH;或化合物2:α-OH;或式(Ⅱ)中,化合物3:β-OH;或化合物4:α-OH;或式(Ⅲ)中,化合物5。
实施例2:
对实施例1的大环内酯类化合物-化合物1、化合物2、化合物3、化合物4和化合物5的抗肿瘤细胞的实验。
采用国际通用的肿瘤细胞株,即:人肺癌细胞株(A549)、人鼻咽癌细胞株(CNE2)、人宫颈癌细胞株(HeLa)、人肝癌细胞株(HepG2)、人乳腺癌细胞株(MCF-7)和正常人肝细胞(L02)和正常人脐静脉内皮细胞(Huvect-12)。试验方法为CCK-8法:
1)细胞培养:根据细胞生长速度,将处于对数生长期的肿瘤细胞和正常细胞以100μL/孔接种于96孔板,贴壁生长24小时。
2)加样品(药品):每孔加10μL不同浓度的化合物1、化合物2、化合物3、化合物4和化合物5的培养基稀释溶液,并设相应浓度的培养基溶媒对照及无细胞凋零孔。
3)加药细胞培养:肿瘤细胞在37℃、5%的CO2条件下培养48小时。
4)活性测试:经培养后的细胞,每孔加入10μL的CCK-8溶液,继续培养2小时,酶标仪450nm波长测定OD值。以多柔比星、顺铂作为阳性对照。
5)活性报告。每株细胞系做五个平行实验,实验结果见表3:
表3:化合物1、2、3、4和5对肿瘤细胞株和正常细胞的的抑制作用(IC50,μM)
a阳性对照
上述实验结果表明,化合物1、化合物2、化合物3和化合物4对肿瘤细胞有明显抑制作用,尤其是化合物4,不但对肿瘤细胞的抑制活性明显较强,而且相比于肿瘤细胞,对正常细胞的抑制活性明显较弱,对正常细胞的毒性较小。
综上所述,本发明为研制新的抗肿瘤药物提供了新的先导化合物,对开发中国海洋药物资源具有重要的意义。
- 还没有人留言评论。精彩留言会获得点赞!