一种通用荧光探针及其检测方法和应用与流程
本发明涉及实时荧光PCR领域,尤其涉及一种通用荧光探针及其检测方法和应用。
背景技术:
现有技术中,荧光素标记方法在PCR中的应用,主要体现在荧光引物或荧光探针两个方面。
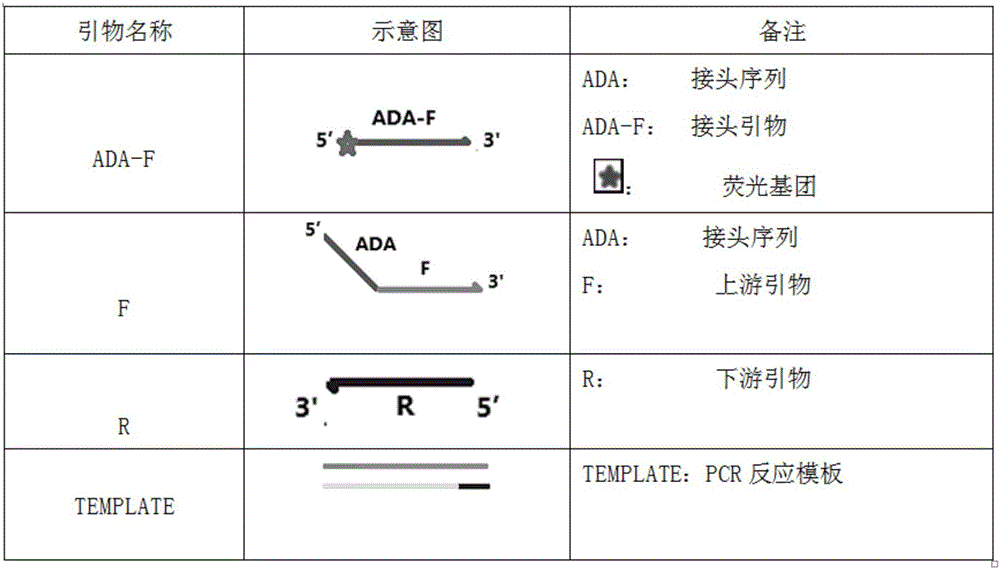
其中,荧光引物的方法,主要有直接标记引物或者标记接头引物,而PCR产物采用遗传分析仪,如ABI遗传分析仪310、3130、3130xl、3730等,通常用于检测微卫星及基因分型,例如中国专利公告号为CN104178566的发明专利,即公开了一种可用于微卫星检测的多重荧光PCR通用接头及检测方法和应用,其引物设计图和检测流程图分别如图1和图2所示。该技术的缺点包括:a)不能实现实时检测;b)图谱结果分析难,易误判;c)PCR产物需后处理,易污染检测环境。
荧光探针又可分为水解探针和杂交探针,其荧光信号检测主要通过实时荧光定量PCR仪进行。其中,1)水解探针:如图3所示,以TaqMan探针为例进行说明,水解探针的5'端和3'端分别标记了一个报告荧光基团和一个淬灭荧光基团,在探针完整时,系统激发供体而产生的荧光信号被临近的淬灭基团吸收,所以此时检测不到供体荧光信号;而当PCR过程中Taq DNA聚合酶扩增到探针结合模版的位点时,其5'-3'核酸外切酶的活性切割掉探针5'端的报告基团——游离的报告基团远离淬灭基团,打破能量的传递,激发报告基团产生的荧光信号就可以被荧光检测系统检测到,检测的是信号的积累。这种TaqMan探针技术,需要针对目的基因或突变位点设计特异性探针,不同基因或突变位点需重新设计、合成,存在成本高且费时的问题。2)杂交探针,复性时两条特异探针杂交到模板上,相互靠近而产生检测信号,到升温变性探针远离模板,无信号,检测的是实时荧光信号。
分子信标(Molecular beacon,MB)是一种呈发夹结构的茎环双标记寡核苷酸探针,两端的核酸序列互补配对,荧光基团与标记在另一端的淬灭基团紧紧靠近,在复性温度下,模板不存在时,形成茎环结构,当加热变性会使互补配对的茎环双链解开,如图4所示,如果有模板存在环序列,分子信标将与模板配对。与模板配对后,分子信标将成链状而非发夹状,使得荧光基团与淬灭剂分开。当荧光基团被激发时,淬灭作用被解除,发出激发光子。这种分子信标技术,需要针对目的基因或突变位点设计特异性探针,不同基因或突变位点需重新设计、合成,存在成本高且费时的问题;另外需通过熔解曲线Tm峰值进行检测,检测灵敏度有限。
技术实现要素:
为解决上述技术问题,本发明的目的是提供一种实现实时检测、无需PCR后续处理、节省设计和合成时间、降低成本、结果稳定性好且易于分析的通用荧光探针及其检测方法和应用。
本发明第一方面提供一种通用荧光探针,包括正链探针、负链探针以及特异性下游引物;其中,
所述正链探针包括由5’端至3’端依次相连的寡聚核苷酸正链序列(UAP)、连接序列和特异性上游引物序列(ASO);
所述负链探针包括与寡聚核苷酸正链序列互补的寡聚核苷酸负链序列,所述寡聚核苷酸负链序列的5’端和3’端分别连接有荧光基团(R)和淬灭基团(Q);
所述特异性上游引物序列(ASO)和特异性下游引物(LSO)与目标基因的靶点序列相互互补。
进一步的,所述连接序列包括TA Box序列,所述TA Box序列为包括但不限于AA、TT、AAA、TTT、AT、TA、ATA、TAT、AAT、TAA、ATTT、TAAA、TATT、AATA、TTAT、TATA、ATAT、ATATA、TATATA、TTTAA、TATTT、TTATT、TTTAT、TAATT、TTAAT、AAATT、ATAAA、AATAA或AAATA的序列。
应当说明的是,为了实现通用荧光探针在某一类目的生物中的通用检测,所述寡聚核苷酸正链序列与采用该通用荧光探针进行检测的目的生物的序列相比无同源性或序列相似度小于30%。
应当说明的是,同源性是指进化过程中源于同一祖先的分支之间的关系,同源性是来描述物种之间的进化关系的,所谓同源序列,是指从某一共同祖先经趋异进化而形成的不同序列。相似性是指序列比对过程中用来描述检测序列和目标序列之间相同DNA碱基或氨基酸残基顺序所占比例的高低。一般认为,序列之间的相似性(similarity)越高,序列之间同源的可能性越大。当相似程度高于50%时,比较容易推测检测序列和目标序列可能是同源序列;而当相似性程度低于20%时,就难以确定或者根本无法确定两者具有同源性。
关于通用荧光探针的设计,若目的生物为真核生物,则所述寡聚核苷酸正链序列可根据酵母菌基因组序列设计而成。
进一步的,所述寡聚核苷酸正链序列采用如SEQ ID NO:1-6中任一项所示的核苷酸序列,相应的,所述寡聚核苷酸负链序列采用如SEQ ID NO:7-12中所示的核苷酸序列。其序列信息具体如下:
GCGTGTTGAGTGTGCGGCGTAGA(SEQ ID NO:1)
GCGAAAGCCTGACGGAGCGAG(SEQ ID NO:2)
AGATGTAGCGATAGCCTGAGCGAGCGA(SEQ ID NO:3)
GATGAGTGTGTTGCGGCGTAGATGAGTG(SEQ ID NO:4)
TAGCGATAGCCTGAGCGAGCGA(SEQ ID NO:5)
GCGATGCGTGACGGAGAGTGAG(SEQ ID NO:6)
R-TCTACGCCGCACACTCAACACGC-Q(SEQ ID NO:7)
R-CTCGCTCCGTCAGGCTTTCGC-Q(SEQ ID NO:8)
R-TCGCTCGCTCAGGCTATCGCTACATCT-Q(SEQ ID NO:9)
R-CACTCATCTACGCCGCAACACACTCATC-Q(SEQ ID NO:10)
R-TCGCTCGCTCAGGCTATCGCTA-Q(SEQ ID NO:11)
R-CTCACTCTCCGTCACGCATCGC-Q(SEQ ID NO:12)
其中,R代表荧光基团,Q代表淬灭基团。
进一步的,所述荧光基团包括但不限于FAM、TET、Texas Red、VIC或Cy5,所述淬灭基团包括但不限于BHQ1或BHQ2。
本发明第二方面提供一种采用前述通用荧光探针的检测方法,包括以下步骤:
S1、提取样品的基因组DNA;
S2、将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合;
S3、配制PCR反应体系,进行实时荧光PCR扩增;
S4、根据实时检测的荧光信号强度进行结果分析。
应当说明的是,对于低丰度目标样品或者低回收率的核酸样本,在步骤S1之后还包括采用上游引物(FP)和下游引物(RP)对样品的基因组DNA预扩增的步骤,然后再将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合,然后进行PCR扩增;对于高丰度目标样品或者高回收率的核酸样本,可以直接将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合,然后进行PCR扩增。
进一步的,所述上游引物和下游引物、以及通用荧光探针均设置为多组以同时检测多个目标基因,或者,所述通用荧光探针设置为多组以检测多个目标基因、或单个目标基因的多个基因型。
本发明第三方面提供一种前述通用荧光探针,在基因分型和突变基因检测上的应用。
借由上述方案,本发明至少具有以下优点:
1)通用荧光探针序列特异,通用性较高;
2)通用荧光探针可用于SNP位点检测;
3)UAP序列和ASO序列引入TA Box,消除荧光基团与相邻模板碱基引起的荧光淬灭效应,避免影响检测;
4)UAP序列灵活变动,消除引物自身二级机构对检测结果的影响;
5)一步法检测,无需后续处理即可获得实时检测结果,快速、准确,无污染。
上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,并可依照说明书的内容予以实施,以下以本发明的较佳实施例并配合附图详细说明如后。
附图说明
图1是现有技术中多重荧光PCR通用接头引物设计图;
图2是现有技术中用于微卫星检测的多重荧光PCR通用接头的检测方法流程图;
图3是现有技术中TaqMan探针的工作原理图;
图4是现有技术中分子信标的工作原理图;
图5是本发明第一实施例中通用荧光探针设计图;
图6是本发明第一实施例中通用荧光探针PCR扩增原理;
图7是采用BIO-RAD荧光定量PCR仪和通用荧光探针对等位基因中的突变型基因位点检测结果图;
图8是采用ABI7500荧光定量PCR仪和通用荧光探针对等位基因中的突变型基因位点检测结果图;
图9是本发明第二实施例中基因分型结果图;
图10是本发明第三实施例中基因分型结果图;
图11是本发明第四实施例中基因分型结果图;
图12是本发明第五实施例中基因分型结果图;
图13是本发明第六实施例中基因分型结果图。
具体实施方式
下面结合附图和实施例,对本发明的具体实施方式作进一步详细描述。以下实施例用于说明本发明,但不用来限制本发明的范围。
实施例一
本发明一较佳实施例提供一组通用荧光探针,如图5所示,包括正链探针、负链探针以及特异性下游引物;其中,正链探针包括由5’端至3’端依次相连的寡聚核苷酸正链序列(UAP)、连接序列(TA Box)和特异性上游引物序列(ASO);负链探针包括与寡聚核苷酸正链序列互补的寡聚核苷酸负链序列(UP),寡聚核苷酸负链序列的5’端和3’端分别连接有荧光基团(R)和淬灭基团(Q),荧光基团可选用FAM、TET、Texas Red、VIC或Cy5,淬灭基团可选用BHQ1或BHQ2;特异性上游引物序列(ASO)和特异性下游引物(LSO)与目标基因的靶点序列相互互补。
采用该通用荧光探针的检测方法,包括以下步骤:
S1、提取样品的基因组DNA;
S2、将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合;
S3、配制PCR反应体系,进行实时荧光PCR扩增;
S4、根据实时检测的荧光信号强度进行结果分析。
通用荧光探针的PCR扩增原理,如图6所示:
第一步:正链探针UAP-TA Box-ASO与特异性下游引物LSO分别以基因组DNA为模板扩增,产生互补链;
第二步:特异性下游引物LSO以第一步扩增产物为模板,延伸至负链探针UP位置,水解负链探针5’端的荧光基团,产生游离的荧光基团;
第三步:荧光检测,分析检测结果。
对于低丰度目标样品或者低回收率的核酸样本,在步骤S1之后还包括采用上游引物(FP)和下游引物(RP)对样品的基因组DNA预扩增的步骤,然后再将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合,然后进行PCR扩增;对于高丰度目标样品或者高回收率的核酸样本,可以直接将通用荧光探针中正链探针、负链探针以及特异性下游引物按一定比例混合,然后进行PCR扩增。
进一步的,所述上游引物和下游引物、以及通用荧光探针均设置为多组以同时检测多个目标基因,或者,所述通用荧光探针设置为多组以检测多个目标基因、或单个目标基因的多个基因型。
以通用荧光探针设置为多组以检测单个目标基因的多个基因型为例,作进一步说明,荧光基团和淬灭基团标记在UP序列的5’端和3’端,并可与其任意组合,但是同时使用的不同通用荧光探针的荧光基团和淬灭基团不能重复,需建立一一对应关系。现有的荧光基团(FAM、TET、Texas Red、VIC、Cy5等)和淬灭基团(BHQ1、BHQ2等),根据仪器检测通道及检测类型进行选择,避免光谱重叠。
以检测等位基因中的突变型基因位点为例,具体实验流程如下:
S1、设计通用荧光探针,包括正链探针(UAP-TA Box-ASO)、负链探针(UP)、特异性上游引物(FP)以及特异性下游引物(RP/LSO);
S2、特异性上游引物(FP)以及特异性下游引物(RP)配置反应体系,进行DNA模板预扩增;
S3、将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按一定比例混合为混合引物,配置反应体系,以预扩增产物进行实时荧光定量PCR检测;
反应体系为10μL,包括2X TaKaRa TaqTM HS Perfect Mix 5ul、混合引物1.2μL、荧光标记接头0.5μL、去离子水1μL、DNA 20ng。
S4、结果分析,生成检测报告,基于现有荧光定量PCR仪器,通过检测荧光信号强度,进行基因型检测,不同仪器分型图7和8所示,分别为BIO-RAD荧光定量PCR仪和ABI7500荧光定量PCR仪,可以准确检测等位基因中的突变型基因位点。
其中,寡聚核苷酸正链序列(UAP)和寡聚核苷酸负链序列(UP)的序列可分别设计如表1所示。
表1 UAP和UP序列表
其中,TA Box序列组合方式如表2所示。
表2 TA Box序列设计图
实施例二
本发明提供一种实时荧光PCR仪运用通用荧光探针进行rs2294008位点基因分型的方法,具体步骤如下:
S1、合成正链探针(等位基因特异性引物1、等位基因特异性引物2)、与正链探针相互补的负链探针(等位基因特异性引物1、等位基因特异性引物2)以及特异性下游引物(LSO);
表3 rs2294008基因分型检测引物设计表
表中,标记下划线的部分为寡聚核苷酸正链序列(UAP),方框标记的为连接序列(TA Box),未标记的为特异性上游引物序列(ASO),对应检测rs2294008位点的野生型和突变型。
S2、选取人唾液样本,提取样本的基因组DNA;
S3、选取新合成的rs2294008位点的上游引物(FP)及下游引物(RP)对DNA模板进行预扩增;
S4、采用表3中的通用荧光探针,将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按照一定比例(摩尔比)混合,在涡旋混合器上混匀组成混合引物;
S5、将混合引物配置成PCR反应体系,以预扩增产物进行实时荧光PCR扩增;
S6、根据实时检测的荧光信号强度进行结果分析;根据荧光检测结果进行基因分型,其结果如图9所示,可见通用荧光探针可以很好地将待测目的基因的突变型和野生型分开。
实施例三
本发明提供一种实时荧光PCR仪运用通用荧光探针进行rs6010620位点基因分型的方法,具体步骤如下:
S1、合成正链探针(等位基因特异性引物1、等位基因特异性引物2)、与正链探针相互补的负链探针(等位基因特异性引物1、等位基因特异性引物2)以及特异性下游引物(LSO);
表4 rs6010620基因分型检测引物设计表
表中,标记下划线的部分为寡聚核苷酸正链序列(UAP),方框标记的为连接序列(TA Box),未标记的为特异性上游引物序列(ASO),对应检测rs6010620位点的野生型和突变型。
S2、选取人唾液样本,提取样本的基因组DNA;
S3、选取新合成的rs6010620位点的上游引物(FP)及下游引物(RP)对DNA模板进行预扩增;
S4、采用表4中的通用荧光探针,将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按照一定比例(摩尔比)混合,在涡旋混合器上混匀组成混合引物;
S5、将混合引物配置成PCR反应体系,以预扩增产物进行实时荧光PCR扩增;
S6、根据实时检测的荧光信号强度进行结果分析;根据荧光检测结果进行基因分型,其结果如图10所示,可见通用荧光探针可以很好地将待测目的基因的突变型和野生型分开。
实施例四
本发明提供一种实时荧光PCR仪运用通用荧光探针进行rs339331位点基因分型的方法,具体步骤如下:
S1、合成正链探针(等位基因特异性引物1、等位基因特异性引物2)、与正链探针相互补的负链探针(等位基因特异性引物1、等位基因特异性引物2)以及特异性下游引物(LSO);
表5rs339331基因分型检测引物设计表
表中,标记下划线的部分为寡聚核苷酸正链序列(UAP),方框标记的为连接序列(TA Box),未标记的为特异性上游引物序列(ASO),对应检测rs339331位点的野生型和突变型。
S2、选取人唾液样本,提取样本的基因组DNA;
S3、选取新合成的rs339331位点的上游引物(FP)及下游引物(RP)对DNA模板进行预扩增;
S4、采用表5中的通用荧光探针,将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按照一定比例(摩尔比)混合,在涡旋混合器上混匀组成混合引物;
S5、将混合引物配置成PCR反应体系,以预扩增产物进行实时荧光PCR扩增;
S6、根据实时检测的荧光信号强度进行结果分析;根据荧光检测结果进行基因分型,其结果如图11所示,可见通用荧光探针可以很好地将待测目的基因的突变型和野生型分开。
实施例五
本发明提供一种实时荧光PCR仪运用通用荧光探针进行rs17728461位点基因分型的方法,具体步骤如下:
S1、合成正链探针(等位基因特异性引物1、等位基因特异性引物2)、与正链探针相互补的负链探针(等位基因特异性引物1、等位基因特异性引物2)以及特异性下游引物(LSO);
表6 rs17728461基因分型检测引物设计表
表中,标记下划线的部分为寡聚核苷酸正链序列(UAP),方框标记的为连接序列(TA Box),未标记的为特异性上游引物序列(ASO),对应检测rs17728461位点的野生型和突变型。
S2、选取人唾液样本,提取样本的基因组DNA;
S3、选取新合成的rs17728461位点的上游引物(FP)及下游引物(RP)对DNA模板进行预扩增;
S4、采用表6中的通用荧光探针,将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按照一定比例(摩尔比)混合,在涡旋混合器上混匀组成混合引物;
S5、将混合引物配置成PCR反应体系,以预扩增产物进行实时荧光PCR扩增;
S6、根据实时检测的荧光信号强度进行结果分析;根据荧光检测结果进行基因分型,其结果如图12所示,可见通用荧光探针可以很好地将待测目的基因的突变型和野生型分开。
实施例六
本发明提供一种实时荧光PCR仪运用通用荧光探针进行rs11903757位点基因分型的方法,具体步骤如下:
S1、合成正链探针(等位基因特异性引物1、等位基因特异性引物2)、与正链探针相互补的负链探针(等位基因特异性引物1、等位基因特异性引物2)以及特异性下游引物(LSO);
表7 rs11903757基因分型检测引物设计表
表中,标记下划线的部分为寡聚核苷酸正链序列(UAP),方框标记的为连接序列(TA Box),未标记的为特异性上游引物序列(ASO),对应检测rs11903757位点的野生型和突变型。
S2、选取人唾液样本,提取样本的基因组DNA;
S3、选取新合成的rs11903757位点的上游引物(FP)及下游引物(RP)对DNA模板进行预扩增;
S4、采用表7中的通用荧光探针,将正链探针(UAP-TA Box-ASO)、负链探针(UP)、和特异性下游引物(LSO)按照一定比例(摩尔比)混合,在涡旋混合器上混匀组成混合引物;
S5、将混合引物配置成PCR反应体系,以预扩增产物进行实时荧光PCR扩增;
S6、根据实时检测的荧光信号强度进行结果分析;根据荧光检测结果进行基因分型,其结果如图13所示,可见通用荧光探针可以很好地将待测目的基因的突变型和野生型分开。
以上所述仅是本发明的优选实施方式,并不用于限制本发明,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和变型,这些改进和变型也应视为本发明的保护范围。
SEQUENCE LISTING
<110> 健路生物科技(苏州)有限公司
<120> 一种通用荧光探针及其检测方法和应用
<130> 2016
<160> 27
<170> PatentIn version 3.3
<210> 1
<211> 23
<212> DNA
<213> 人工序列
<400> 1
gcgtgttgag tgtgcggcgt aga 23
<210> 2
<211> 21
<212> DNA
<213> 人工序列
<400> 2
gcgaaagcct gacggagcga g 21
<210> 3
<211> 27
<212> DNA
<213> 人工序列
<400> 3
agatgtagcg atagcctgag cgagcga 27
<210> 4
<211> 28
<212> DNA
<213> 人工序列
<400> 4
gatgagtgtg ttgcggcgta gatgagtg 28
<210> 5
<211> 22
<212> DNA
<213> 人工序列
<400> 5
tagcgatagc ctgagcgagc ga 22
<210> 6
<211> 22
<212> DNA
<213> 人工序列
<400> 6
gcgatgcgtg acggagagtg ag 22
<210> 7
<211> 23
<212> DNA
<213> 人工序列
<400> 7
tctacgccgc acactcaaca cgc 23
<210> 8
<211> 21
<212> DNA
<213> 人工序列
<400> 8
ctcgctccgt caggctttcg c 21
<210> 9
<211> 27
<212> DNA
<213> 人工序列
<400> 9
tcgctcgctc aggctatcgc tacatct 27
<210> 10
<211> 28
<212> DNA
<213> 人工序列
<400> 10
cactcatcta cgccgcaaca cactcatc 28
<210> 11
<211> 22
<212> DNA
<213> 人工序列
<400> 11
tcgctcgctc aggctatcgc ta 22
<210> 12
<211> 22
<212> DNA
<213> 人工序列
<400> 12
ctcactctcc gtcacgcatc gc 22
<210> 13
<211> 46
<212> DNA
<213> 人工序列
<400> 13
gcgtgttgag tgtgcggcgt agaatataca gcccaccagt gaccac 46
<210> 14
<211> 46
<212> DNA
<213> 人工序列
<400> 14
gcgaaagcct gacggagcga gatatacaca gcccaccagt gaccat 46
<210> 15
<211> 19
<212> DNA
<213> 人工序列
<400> 15
gccaagcctg ccatcaaca 19
<210> 16
<211> 48
<212> DNA
<213> 人工序列
<400> 16
tagcgatagc ctgagcgagc gaatacaacc agatcatgca aagcaggt 48
<210> 17
<211> 46
<212> DNA
<213> 人工序列
<400> 17
gcgatgcgtg acggagagtg agataaccag atcatgcaaa gcaggc 46
<210> 18
<211> 25
<212> DNA
<213> 人工序列
<400> 18
ctgttttccc tttttgagac ctggg 25
<210> 19
<211> 59
<212> DNA
<213> 人工序列
<400> 19
agatgtagcg atagcctgag cgagcgaaat cctcctagtc actaaagata aacctcata 59
<210> 20
<211> 60
<212> DNA
<213> 人工序列
<400> 20
gatgagtgtg ttgcggcgta gatgagtgaa tcctcctagt cactaaagat aaacctcatg 60
<210> 21
<211> 27
<212> DNA
<213> 人工序列
<400> 21
gtacactttg catgaactct ctctccc 27
<210> 22
<211> 52
<212> DNA
<213> 人工序列
<400> 22
gcgtgttgag tgtgcggcgt agataacctc agtggagaag ttttatctgc ac 52
<210> 23
<211> 50
<212> DNA
<213> 人工序列
<400> 23
gcgaaagcct gacggagcga gtaacctcag tggagaagtt ttatctgcag 50
<210> 24
<211> 27
<212> DNA
<213> 人工序列
<400> 24
gtacactttg catgaactct ctctccc 27
<210> 25
<211> 54
<212> DNA
<213> 人工序列
<400> 25
agatgtagcg atagcctgag cgagcgattt ctggacttgt aactggtgtt tgca 54
<210> 26
<211> 54
<212> DNA
<213> 人工序列
<400> 26
gatgagtgtg ttgcggcgta gatgagtgtt ttggacttgt aactggtgtt tgcg 54
<210> 27
<211> 27
<212> DNA
<213> 人工序列
<400> 27
gtacactttg catgaactct ctctccc 27
- 还没有人留言评论。精彩留言会获得点赞!