启动子及其用途的制作方法
本发明涉及医学领域,尤其涉及与视网膜神经节细胞或感光细胞变性相关的疾病的治疗和预防。
背景技术:
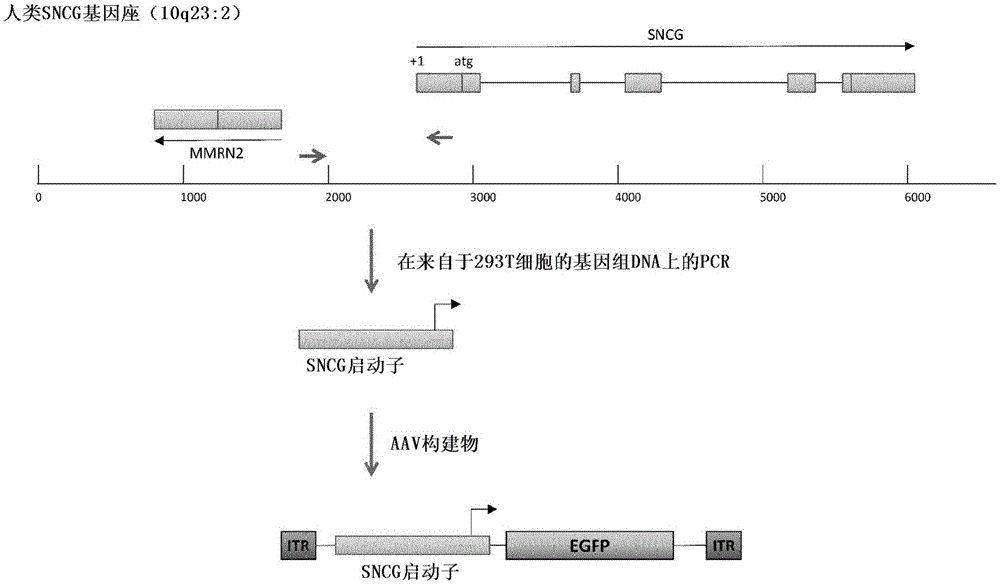
:人们可以将视网膜分成两个部分,视网膜色素上皮(rpe)和视网膜神经感觉层。rpe主动参与维持视网膜神经感觉层的功能。视网膜神经感觉层被组织成包括感光细胞和视网膜神经节细胞(rgc)的神经网络。感光细胞将光信息转变成电信息并将其导向rgc,后者负责将视觉信息从视网膜传输到视觉皮层。在这些不同的细胞类型之中,我们也可以发现具有调控功能的细胞例如水平细胞,其引起负反馈,允许视网膜应答适应于各种不同的光强度条件并提高对比度信息。rgc主要是谷氨酸能神经元,其位于视网膜的内表面(神经节细胞层)中。它们的轴突形成视神经。存在大约15至20种类型的rgc。rgc在视觉加工中发挥关键作用,并且rgc功能障碍或变性可能引起失明。被称为视神经病的广泛类型的疾病由主要缺乏rgc引起。它们中的一些是遗传疾病,例如由线粒体基因突变造成的利伯氏遗传性视神经病(leberhereditaryopticneuropathy)(lhon)。然而,获得性神经病更加普遍,例如青光眼,它是发达国家中失明的第二最重要的病因,在全世界影响7千万人。造成这些疾病的基因的健康版本或编码神经保护因子的基因在神经节细胞中的靶向表达,可以允许治疗这些视神经病。因此,能够在这些细胞中获得强烈且特异性的基因表达以提供基因疗法,是至关重要的。此外,rgc可以构成治疗靶点,而不直接牵涉变性过程。例如,在感光细胞由于遗传性(即色素性视网膜炎)或获得性疾病而丧失的疾病中,rgc在感光细胞变性后仍长期存留,因此构成了使用光遗传学工具恢复视网膜的治疗靶点。在这种情形中,rgc是独立于变性细胞的细胞靶点,其中光敏蛋白以强烈且受限的方式表达对于视力恢复的成功来说是必不可少的。研究rgc的功能也是极为有趣的,因为它们的尺寸、形状和每种rgc类型的投影都是与众不同的,并且据认为它们在视觉功能中发挥相当不同且可能独立的作用,但目前关于这个问题了解得相当少。可以在这些细胞中驱动基因表达的启动子序列将允许识别或追踪rgc,通过遗传编码的电压或钙敏感性蛋白(即gcamp)的表达监测它们的活性。在现有技术中,在rgc中的基因表达已经通过使用遍在启动子或组织特异性启动子来获得。遍在启动子在组织中提供强烈但不受限制的基因表达模式。遍在真核启动子源自于鸡β肌动蛋白(cba)基因或磷酸甘油酸激酶(pgk)或延伸因子1α(ef1α)的启动子。其他病毒起源的遍在启动子包括源自于巨细胞病毒(cmv)的启动子或合成的启动子序列例如cag。然而,已证实cmv启动子的调控依赖于许多能够改变转入基因的表达的细胞信号传导途径。此外,这些启动子不限于给定的细胞类型,并在它们被递送到其中的所有细胞例如视网膜色素上皮(rpe)、视网膜和视网膜之外的其他眼组织例如睫状体、虹膜、角膜等的müller神经胶质细胞中引起表达。已经使用在rpe或感光细胞中引起表达的组织特异性启动子获得了受限于视网膜细胞的基因表达。启动子例如基于rpe65、vmd2和oa1的启动子在rpe细胞中引起基因表达,而人(rk)或牛(rho)视紫红质激酶的启动子或小鼠视蛋白(mop)的启动子,引起受限于感光细胞的表达。这些启动子受限于视网膜,但在rgc中效率不高。几种蛋白质已被描述为表达在视网膜的rgc中。在这些蛋白质中,thy1-1(胸腺细胞抗原1-1)或brn3-a蛋白被常规用作神经节细胞的标志物。然而,thy1-1蛋白对rgc没有特异性,因为它也在巨噬细胞和小胶质细胞中表达。此外,thy-1和brn3-a两者只在一部分神经节细胞中表达。因此,这些标志物的启动子区不允许转入基因在整个神经节细胞群体中的特异性表达。最近,已描述了几个在递送到视网膜后在视网膜神经节细胞中引起受限表达的启动子序列。一个2.8kb的基于人连接蛋白36(cx36)的序列,驱动在小鼠中在特定亚型的rgc中和在非人类灵长动物中在窝周(peri-foveaolar)rgc中的表达(yin等,iovs,2011;52(5):2775–8;dalkara等,scitransmed,2013;5(189):189ra76)。simpson和同事描述了其他超过3.3kb的在rgc中驱动表达的启动子元件(ple25、ple53和ple67)(deleeuw等,molthermethandclindev,2014;1:5)。γ-突触核蛋白基因(sncg)已被描述为在视网膜中表达,更特别地,描述了γ-突触核蛋白与brn3-a蛋白在人和鼠rgc中的共定位(surgucheva等,molvis,2008,14,1540-8)。然而,作者还注意到了γ-突触核蛋白在视网膜丛状细胞中以及在未被作者鉴定并且不表达brn3-a蛋白的细胞中的免疫反应性。此外,作者展示,在非rgc细胞系中,γ-突触核蛋白启动子活性受到γ-突触核蛋白基因的2,195-bp的片段支持,所述片段包括起始atg密码子上游的1,260bp的非编码5’侧翼区以及外显子1和内含子1,其被描述为同样在所研究的非rgc细胞系中,在调控sncg基因的表达中具有必不可少的作用(surgucheva等,jmolneurosci,2008,35:267-71)。许多重组病毒载体被描述为允许在体内高效的基因转移,以用于基因疗法应用。其中,腺相关病毒(aav)由于其非致病性、非插入性和低免疫原性特征,可能是关键的递送机制。此外,aav已被描述为允许在啮齿动物rgc中非常高效地转导。事实上,不同研究团队已显示,aav血清型2(aav2)或其酪氨酸突变的形式在小鼠中的玻璃体内注射,引起报告基因在rgc中非常高效的表达(petrs-silva等,molther.2009mar;17(3):463-71;petrs-silva等,molther.2011feb;19(2):293-301)。然而,由于其尺寸小,aav的dna有效载荷严重受限,并且与大型启动子例如现有技术中描述的rgc特异性启动子的使用不相容。因此,对开发允许转入基因在rgc中强烈、稳定且特异地表达,并且特别适合于使用aav载体的基因转移的紧凑型启动子,存在着强烈需求。技术实现要素:本发明人在本文中提供了一种新的转录启动子,其长度短并因此适合于与aav载体相组合使用,并且可以在视网膜神经节细胞(rgc)中特异性地驱动高水平的基因表达。因此,在第一种情况下,本发明涉及一种在视网膜神经节细胞中具有启动子活性的分离的核酸,其中所述核酸具有小于1.5kb的长度,并包含选自下述各项的序列:-seqidno:1的序列,-与seqidno:1具有至少80%同一性的序列,-包含seqidno:1的至少500个连续核苷酸的序列,以及-能够在中等严紧条件下与seqidno:1的核酸序列或其互补链杂交的序列。优选地,所述分离的核酸具有视网膜神经节细胞特异性启动子活性。优选地,本发明的核酸具有小于1.5kb的长度,并包含选自seqidno:1的序列及其与seqidno:1具有至少80%同一性的功能性变体的序列,或由所述序列构成。特别地,本发明的核酸可以包含与seqidno:1具有至少80%或90%同一性的序列或由所述序列构成,或者可以包含seqidno:1的序列或由所述序列构成。优选地,本发明的核酸具有小于1.2kb、更优选地小于1kb的长度。在第二种情况下,本发明涉及一种表达盒,其包含可操作地连接到编码目标多肽或目标核酸、优选为目标多肽的核酸的本发明的核酸。特别地,所述目标多肽可以是治疗性蛋白、光遗传学驱动剂(optogeneticactuator)或报告蛋白。优选地,所述目标多肽是治疗性蛋白或光遗传学驱动剂。特别地,所述治疗性蛋白可以选自mt-nd4、mt-nd1、mt-nd6、mt-cyb、mt-co3、mt-nd5、mt-nd2、mt-coi、mt-atp6、mt-nd4l、opa1、opa3、opa7和aco2,或者可以是优选地选自gdnf、vegf、cntf、fgf2、bdnf和epo的神经营养因子,优选地选自bcl2和bcl2l1的抗凋亡蛋白,优选地选自内皮抑素、血管抑素和sflt的抗血管生成因子,优选地选自il10、il1r1、tgfbi和il4的抗炎因子,或视杆细胞来源的视锥细胞活性因子(rod-derivedconeviabilityfactor)(rdcvf)。所述光遗传学驱动剂可以是光遗传学激活剂,其优选地选自视紫红质,光视蛋白,黑视蛋白,松果体视蛋白,松果体旁视蛋白,va视蛋白,周视蛋白,神经视蛋白,脑视蛋白,视网膜色素,rgr视蛋白,具有红移的光谱性质的微生物视蛋白例如reachr、chrimson或chrimsonr,可以召集gi/o信号传导的脊椎动物视蛋白例如短波长脊椎动物视蛋白或长波长脊椎动物视蛋白,来自于衣藻属(chlamydomonas)微藻的通道视紫红质例如通道视紫红质-1和通道视紫红质-2(来自于莱茵衣藻(chlamydomonasreinhardtii)),及其变体;或者光遗传学抑制剂,其优选地选自嗜盐菌视紫红质例如嗜盐菌视紫红质(nphr)、增强的嗜盐菌视紫红质(enphr2.0和enphr3.0)和红移的嗜盐菌视紫红质halo57,古菌视紫红质-3(ar-3),古菌视紫红质(arch),细菌视紫红质例如增强的细菌视紫红质(ebr),变形菌视紫红质,黄单胞菌视紫红质,斑点小球腔菌(leptosphaeriamaculans)真菌视蛋白(mac),大白鲨交叉嗜盐菌视紫红质(cruxhalorhodopsinjaws),及其变体。所述目标多肽也可以是报告蛋白,其优选地选自荧光蛋白、钙指示剂、碱性磷酸酶、β-半乳糖苷酶、β-内酰胺酶、辣根过氧化物酶及其变体。在优选实施方式中,所述目标多肽不是sncg蛋白和/或不是萤光素酶。或者,本发明的核酸可以可操作地连接到编码目标核酸的核酸,所述目标核酸优选地选自sirna、shrna、rnai、mirna、反义rna、核酶和脱氧核酶(dnazyme)。在第三种情况下,本发明涉及一种包含本发明的表达盒的载体,优选为病毒载体,更优选为反转录病毒载体,特别是慢病毒载体或非致病性细小病毒。所述载体可以是腺相关病毒(aav)载体,并且可以包含侧接于编码目标多肽或目标核酸的核酸的两个itr。在另一种情况下,本发明涉及一种包含本发明的载体的病毒粒子,特别是包含所述载体和aav来源的衣壳的aav粒子,所述衣壳优选地选自aav-2、aav-5、aav-7m8(aav2-7m8)、aav-9和aav-8血清型衣壳,更优选为aav-2来源的衣壳例如aav-2或aav2-7m8衣壳。在另一种情况下,本发明还涉及用本发明的表达盒、载体或病毒粒子转化的细胞,优选为视网膜神经节细胞。在另一种情况下,本发明还涉及一种药物组合物,其包含本发明的核酸、表达盒、载体、病毒粒子或细胞以及可药用赋形剂。在另一种情况下,本发明涉及本发明的表达盒、载体、病毒粒子或细胞的用途,其用于眼病的治疗。优选地,所述眼病选自与视网膜神经节细胞变性相关的疾病,更优选地选自遗传性视神经病例如利伯氏遗传性视神经病或显性视神经萎缩,以及与感光细胞变性相关的疾病例如年龄相关性黄斑变性、视锥细胞-视杆细胞营养不良、利伯氏先天性黑朦(lebercongenitalamaurosis)、斯特格氏病(stargardt’sdisease)、糖尿病性视网膜病、视网膜脱离、贝斯特氏病(best’sdisease)、色素性视网膜炎、无脉络膜症或视网膜毯层变性。在另一种情况下,本发明还涉及本发明的核酸、表达盒、载体或病毒粒子的用途,其用于在视网膜神经节细胞中表达编码目标多肽或目标核酸的核酸,优选地用于视网膜神经节细胞中的特异性表达。它还涉及一种在视网膜神经节细胞中表达目标多肽或目标核酸、优选地在视网膜神经节细胞中特异性表达目标多肽或目标核酸的方法,所述方法包括将本发明的核酸、表达盒、载体或病毒粒子引入到视网膜神经节细胞中。附图说明图1.sncg基因和启动子序列的示意图。sncg基因位于10号染色体(10q23.3)上。它含有5个外显子,从+1转录位点到第5个外显子的末端延伸跨越3.5kb。第一个外显子multimerine2基因(mmrn2)位于+1sncg转录位点下游863bp。为了提取人类sncg启动子的序列,从hek293t细胞扩增-785至+163区域(用箭头指示)。然后将所述pcr产物亚克隆到pentr-d/topo中并测序。所述序列与genebank序列geneid6623一致。然后产生在sncg启动子序列(seqidno:1)的控制之下表达egfp报告基因的aav载体。图2.上图:hsncg启动子在小鼠rgc中引起高表达。玻璃体内注射aav2-y444f-hsncg-gfp后四周,小鼠视网膜的眼底图像(a)、视网膜平放固定物(b)和冷冻切片(c)。下图:pgk启动子在视网膜中的多种细胞类型中引起高表达。玻璃体内注射aav2-y444f-pgk-gfp后四周,小鼠视网膜的眼底图像(d)、视网膜平放固定物(e)和冷冻切片(f)。图3.玻璃体内注射aav2-cmv-gfp(上)和aav2-hsncg-gfp(下)后小鼠视网膜的视网膜平放固定物的共聚焦显微镜图像(a),以及玻璃体内注射aav2-hsncg-gfp后小鼠视网膜的横截面(b)。图4.通过眼底荧光成像评估食蟹猴(cynomolgusmacaque)视网膜的黄斑区中的gfp表达。通过玻璃体内注射来给药含有sncg启动子(a)、cmv启动子(b)的aav-gfp载体。具有gfp表达的区域在暗背景上显白色。相机自动调整曝光时间,并且gfp表达强度最大的图4a上的图像具有最暗的背景颜色,但对于gfp表达强度最弱的图4b上的图像来说,在转导区域(窝周环)与背景之间几乎没有差异。图5.在小鼠rgc中,sncg启动子与cmv启动子相比驱动更高水平的hcatch-gfp表达。a)用5x109vg的aav2-sncg-hcatch-gfp(右)或aav2-cmv-hcatch-gfp(左)注射的代表性rd1小鼠视网膜的眼底图像。b)从同一注射系列获得的视网膜平放固定物,示出了在sncg启动子(右)和cmv启动子(左)之下获得的catch-gfp荧光。c)在用aav2-sncg-hcatch-gfp或aav2-cmv-hcatch-gfp注射的rd1小鼠视网膜中,brn3a阳性、gfp阳性和双标记的细胞的定量。在视网膜的中央和外周区域中的所选视野上,用于细胞计数的跨神经节细胞层的共聚焦堆叠投影。在每个象限中选择区域并将细胞计数平均以获得每mm2的brn3a阳性、gfp阳性和共标记的细胞。误差条表示sem。d)用sncg-catch-gfp转导的rd1小鼠视网膜的跨rgc层的代表性共聚焦堆叠投影,用brn3a(红色)和抗gfp(绿色)抗体共标记。e)从注射sncg-catch-gfp的视网膜中的一个代表性视网膜平放固定物获得的横截面,用bnr3a(红色)和抗gfp抗体(绿色)共标记,并且细胞核用dapi(蓝色)标记。图6.rd1小鼠的视网膜和皮层中的功能性catch响应。在每只眼(n=4)5x107、5x108和5x109vg的cmv(黑色)或sncg(灰色)控制下表达catch的视网膜中,在a)1014个光子/cm2/s或b)1017个光子/cm2/s下在480nm处显示出光响应的具有自发活性的细胞的百分率。c)在5x109个病毒粒子剂量(n=4,155个细胞)下,在cmv启动子控制下表达catch的视网膜中,响应幅度(归一化到在最大照度下获得的响应)随光强度的变化。d)在每只眼5x107个病毒粒子剂量(浅灰色,n=4个视网膜,158个细胞)、5x108(深灰色,n=4个视网膜,221个细胞)和5x109(黑色,n=4个视网膜,261个细胞)个病毒粒子(vg)剂量下,在sncg启动子控制下表达catch的视网膜中,响应幅度(归一化到在最大照度下获得的响应)随光强度的变化。e)光栅图和刺激前后时间直方图(psth),示出了在sncg启动子控制下表达catch的视网膜中,在480nm的全视野闪光期间的光响应或动作电位(spike)频率的提高。注意在使用sncg启动子时,曲线在最大aav载体剂量下达到平台。(f、g、h)表达sncg-catch的rd1小鼠的视觉皮层神经元在3种不同的增加的光强度(1015、1016和1017个光子/cm2/s)下对475nm全视野闪光做出响应的psth(顶部)和相应的光栅图(底部)。i)在以5x109vg的剂量用sncg-catch处理的rd1视网膜中记录的视觉诱发电位(vep)与未处理的rd1视网膜和野生型小鼠视网膜的比较。j)在475nm下,归一化的皮层活动性(动作电位和vep)随光强度的变化(n=3只小鼠)。误差条表示sem。图7.aav-catch注射的nhp的体内眼科检查。a)从弱到强的后葡萄膜炎等级;b)从极小到严重的玻璃体混浊等级。图8.来自于用高剂量aav2-catch注射的nhp的眼在注射后3个月时的组织病理学检查。a)以40x的分辨率成像的横跨眼的竖直经线的视网膜切片。(b-f)在来自于(a)的放大区域上,在小梁网状结构(b)、睫状体(c)、视神经(d)、虹膜(e)和视网膜(f)中不存在可检测的淋巴细胞、巨噬细胞或眼结构的损伤。图9.a)解剖之前nhp1的黄斑区,示出了注射后3个月时窝周环中的catch表达。b)mea记录和rgc免疫标记后的半个同一窝区。视网膜平放固定物用brn3a(红色)和gfp抗体(绿色)染色。c)来自于以相同剂量注射的另一只恒河猴的视网膜在注射后3个月时的窝区。视网膜平放固定物用针对通道视紫红质的抗体染色(绿色)。细胞核用dapi染色。d)在以10e12vg/眼的剂量用aav2-sncg-catch(上图)或aav2-cmv-catch(下图)注射后6个月时,恒河猴视网膜的窝上的代表性切片。视网膜平放固定物用针对通道视紫红质的抗体染色(绿色)。图10.catch介导的单细胞光响应的特征。a)视网膜切片,示出了用aav2-hcatch(无gfp标签)注射的nhp2的窝周区域,其中光响应性神经节细胞被修补。b)在细胞附着状态下的rgc记录,示出了在光刺激期间的动作电位和它们的频率增加,正如在所述记录上方的动作电位频率曲线上看到的。c)在-60mv膜片钳下的细胞的光电流响应。d)修补的rgc的动作电位谱,在450nm左右显示出光电流幅度峰值。e)在2至22hz范围内的提高的频率下的闪烁刺激。在l-ap4灌注下,使用1.461016个光子/cm2/s的光强度,在470nm下从(a)中示出的区域记录(b-e)中的细胞。(f-g)用aav2-hcatch-gfp注射的nhp1的窝周区域的双光子图像,显示出具有膜结合表达的高密度的转染细胞,h)在-60mv下使用膜片钳处理并表现出光电流(左)或在细胞附着状态下记录并在光刺激期间显示出增加的动作电位频率(右)的2种代表性细胞的响应。图11.来自于注射后6个月时nhp视网膜中表达catch的rgc的单细胞记录(细胞附着和膜片钳)。在以每只眼5x1011vg的浓度用aav2-cmv-hcatch(左)或aav2-sncg-hcatch(右)注射的灵长动物视网膜中,在注射后6个月时窝周记录到的表现出或没有表现出光响应的细胞的总数。b)与a)相同,但浓度为每只眼1x1012vg。c)响应细胞的百分率随病毒剂量(每只眼5x1011或1x1012vg)和启动子(cmv或sncg)的变化。d)在注射后6个月时,在增加的强度下,对光响应的rgc的最大放电频率。在图上示出了四组不同的响应性细胞,代表了在低和高剂量下试验的两种启动子。e)在注射后6个月时,在增加的强度下对光响应的rgc的峰值光电流(在-60mv下记录的内向电流)。两条曲线代表在每只眼1x1012vg下试验的两种启动子。图12.来自于在注射后3和6个月时在nhp视网膜中表达catch的rgc的mea记录。a)在以每只眼5x1011vg用aav2-sncg-hcatch-gfp(顶部)和aav2-sncg-hcatch(底部)注射的灵长动物视网膜中,在注射后3个月时,基于在增加的光强度下响应神经元的放电率(表示成它们的自发性放电活动的百分率)的灰度图。在图中黄斑区用虚线椭圆指示。b)在用aav2-sncg-hcatch-gfp注射的灵长动物视网膜中,在施用l-ap4后,对于480nm下的全视野闪光的神经节细胞响应的光栅图和刺激前后时间直方图。c)在表达hcatch的灵长动物视网膜中,在施用l-ap4后,在1017个光子/cm2/s下的平均光谱调制。d)对不同刺激强度的平均的归一化响应。e)在注射后6个月时,对强度增加的光响应的rgc的放电频率。每条线表示在对于高剂量组的n=2个视网膜和对于低剂量组的n=3个视网膜之间归一化的放电频率。图13:用aav2-7m8-cag-chrimsonr-tdtomato双侧注射的2只恒河猴的荧光眼底图像。图像在注射当天、注射后1个月和2个月时获取,并且在这些时间点没有显示任何可检测的荧光。le:左眼,re:右眼。图14:用aav2-7m8-sncg-chrimsonr-tdtomato双侧注射的2只恒河猴的荧光眼底图像。图像在注射当天、注射后1个月和2个月时获取,从注射后1个月开始显示出与chrimson-tdtomato相关的强烈荧光(白色)。le:左眼,re:右眼。图15.a-c-e-g对cag启动子(a&c)和sncg启动子(e&g)来说,在多电极阵列上灵长动物半窝的图像,黑点是由电极阵列造成的(间隔100μm)。b-d-f-h对cag(b&d)和sncg(f&h)启动子来说,所有记录位点的对10msec全视野刺激(强度:x1017个光子.cm2.sec-1)的颜色编码的响应。所有图使用相同的色标。图16.使用落射荧光(a-b-c)和双光子显微术(d)观察的灵长动物半窝的本源荧光的图像。a)cag启动子:图像来自于不同放大倍数下的两只灵长动物的左和右半窝(顶部,nhp4灵长动物;底部:nhp3灵长动物)。b)sncg启动子:图像来自于不同放大倍数下的nhp1灵长动物左半窝和窝周边中的区域,示出了chrimsonr-tdtomato表达的荧光斑点。c)与b)相同,但使用nhp1灵长动物的右半窝(箭头表示)。d)来自于具有两种不同启动子(左,cag;右,sncg)的两只猴的近窝区的代表性活体双光子图像。具体实施方式发明人在本文中鉴定到一种源自于人γ-突触核蛋白基因的调控区的启动子序列。该启动子具有小于1kb的长度,并且可以在视网膜神经节细胞(rgc)中特异性驱动高水平基因表达。得益于它的短长度,这种启动子可以容易地用于aav介导的基因递送,并且特别适合于递送长基因。发明人证实,这种启动子与aav衣壳相组合,在小鼠和非人类灵长动物两者中在rgc中引起强烈且特异性的转入基因表达。事实上,在相同的aav剂量下,这种启动子在rgc中提供比遍在cmv启动子更强的转入基因表达。此外,发明人显示,在灵长动物中,这种启动子也比cmv启动子更强。定义当在本文中使用时,术语“核酸”或“多核苷酸”是指任何长度的核苷酸的聚合形式,所述核苷酸可以是核糖核苷酸或脱氧核糖核苷酸。因此,该术语包括但不限于单链、双链或多链dna或rna、基因组dna、cdna、dna-rna杂合体或包含嘌呤和嘧啶碱基或其他天然、化学或生物化学修饰的非天然或衍生的核苷酸碱基的聚合物。所述多核苷酸的骨架可以包含糖和磷酸酯基团(正如通常可以存在于rna或dna中的)或者修饰或取代的糖或磷酸酯基团。或者,所述多核苷酸的骨架可以包含合成的子单元例如氨基磷酸酯的聚合物,并因此可以是寡脱氧核苷氨基磷酸(p-nh2)或混合的氨基磷酸酯-磷酸二酯寡聚物。本发明的核酸可以通过本领域技术人员已知的任何技术来制备,包括化学合成、重组和突变。在优选实施方式中,本发明的核酸是dna分子,其优选地通过本领域技术人员公知的重组方法来合成。当在本文中使用时,术语“分离的核酸”是指已被鉴定并从其天然环境的组分中分离和/或回收的核酸分子。特别地,该术语是指与其天然来源中存在的其他核酸分子分离开的核酸分子。例如,对于基因组dna来说,术语“分离的”包括从与所述基因组dna天然结合的染色体分离出的核酸分子。优选地,“分离的”核酸分子不含在所述核酸分子所源自的生物体的基因组dna中与所述核酸分子天然地侧接的序列。当在本文中使用时,术语“启动子”指的是指导与其可操作地连接的核酸的转录的调控元件。启动子可以调控可操作地连接的核酸的转录速率和效率两者。启动子也可以可操作地连接到增强(“增强子”)或阻遏(“阻遏物”)核酸的启动子依赖性转录的其他调控元件。当在本文中使用时,术语“启动子活性”是指启动子引发与其可操作地连接的核酸的转录的能力。启动子活性可以使用本领域中已知的或实施例中所描述的程序来测量。例如,启动子活性可以通过使用例如rna印迹或聚合酶链反应(pcr),作为转录的mrna的量被测量。或者,启动子活性可以例如通过蛋白质印迹、elisa、比色测定法和各种不同的活性测定法,包括报告基因测定法和本领域中已知的或实施例中所描述的其他程序,作为翻译的蛋白质产物的量被测量。术语“可操作地连接”当在本文中使用时,是指单一核酸分子上的核酸序列的关联,使得一者的功能受到另一者影响。例如,当启动子能够影响编码序列的表达,即所述编码序列在所述启动子的转录控制之下时,所述启动子与所述编码序列可操作地连接。术语“多肽”和“蛋白质”可互换使用,是指氨基酸残基的聚合物,并且不限于最小长度。这些氨基酸残基的聚合物可以含有天然或非天然的氨基酸残基,并且包括但不限于肽、寡肽、氨基酸残基的二聚体、三聚体和多聚体。全长蛋白质及其片段两者都被该定义涵盖。所述术语还包括多肽的翻译后修饰,例如糖基化、唾液酸化、乙酰化、磷酸化等。此外,出于本发明的目的,“多肽”可以是指包括对本源序列的修饰例如缺失、添加和替换(通常在本质上是保守的)的蛋白质,只要所述蛋白质维持所需活性即可。这些修饰可以是通过定点突变精心设计的,或者可以是偶然的,例如通过生产所述蛋白质的宿主的突变或由pcr扩增造成的错误。当在本文中使用时,术语“视网膜神经节细胞”或“rgc”是指视网膜最内层的神经元,不包括移动性无长突细胞。它们通过视网膜的双极细胞整合来自于感光细胞的信息,并投射到脑中,在那里它们在丘脑、下丘脑和上丘处形成突触。发现神经转录因子brn3a(geneid:5457)在rgc中特异性表达,并且针对这种蛋白质的抗体被认为是鉴定和定量rgc的可靠标志物(quina等,j.neurosci.2005;25(50):11595–11604)。因此,在特定实施方式中,术语“视网膜神经节细胞”或“rgc”是指表达brn3a的视网膜的最内层的神经元。当在本文中使用时,术语“序列同一性”或“同一性”是指从两个多核苷酸序列的比对获得的位置匹配(同一核酸残基)的数目(%)。通过在对齐以便最大化重叠和同一性并同时最小化序列间隙时比较所述序列来确定序列同一性。特别地,可以根据两个序列的长度,使用多种数学全局或局部比对算法中的任一种来确定序列同一性。长度相近的序列优选地使用在整个长度上最佳地比对所述序列的全局比对算法(例如needleman和wunsch算法;needleman和wunsch,1970)来比对,而长度显著不同的序列优选地使用局部比对算法(例如smith和waterman算法(smith和waterman,1981)或altschul算法(altschul等,1997;altschul等,2005))来比对。出于确定核酸序列同一性百分数目的的比对可以以本领域技术之内的各种不同方式来实现,例如使用可以在因特网网站例如http://blast.ncbi.nlm.nih.gov/或http://www.ebi.ac.uk/tools/emboss/上获取的可公开获得的计算机软件。本领域技术人员可以确定用于测量比对的适合参数,包括在所比较的序列的全长范围内获得最大比对所需的任何算法。出于本发明的目的,核酸序列同一性百分数值是指使用成对序列比对程序embossneedle产生的值,所述程序使用needleman-wunsch算法产生两个序列的最佳全局比对,其中所有搜索参数被设定到缺省值,即评分矩阵=blosum62,间隙开放=10,间隙延伸=0.5,末端间隙罚分=错误,末端间隙开放=10,末端间隙延伸=0.5。术语“对象”或“患者”是指具有视网膜的动物,优选是指哺乳动物,甚至更优选是指人类,包括成人、儿童和处于出生前阶段的人类。在第一种情况下,本发明涉及一种核酸,优选为分离的核酸,其在视网膜神经节细胞中具有启动子活性,具有小于2kb的长度,并且包含选自seqidno:1的序列及其功能性变体的序列或由所述序列构成。seqidno:1的核苷酸序列源自于人γ-突触核蛋白基因(符号:sncg;geneid:6623)的调控区。该基因编码据信参与神经变性疾病的病理发生的突触核蛋白家族蛋白质的一个成员。进一步发现,所述基因中的突变与乳腺肿瘤发生相关。所述基因位于10号染色体上(10q23.2-q23.3)(genebank登记号nc_000010.11,从86958531位至86963260位)。如图1中所示,seqidno:1的启动子包含sncg基因的5’调控区的953个核苷酸(从-789位至+164位,所述蛋白质的起始密码子在+168位)。本发明的核酸在rgc中,即在被引入rgc中时表现出启动子活性,它可以引发与其可操作地连接的核酸的转录。优选地,所述启动子活性是rgc特异性的。术语“rgc特异性的”应该被理解为意味着主要在视网膜神经节细胞中有活性的启动子。应该理解,不能完全排除在其他组织或细胞中通常较低的残余表达。在优选实施方式中,本发明的启动子在双极、无长突、水平、muller细胞中或在感光细胞中无活性。在一个实施方式中,本发明的启动子包含seqidno:1的序列或由所述序列构成。在另一个实施方式中,本发明的启动子包含seqidno:1的功能性变体或由其构成。当在本文中使用时,术语“变体”是指与原始序列不同但保留其基本性质的核苷酸序列。一般来说,变体与原始多核苷酸总体密切相似,并且在许多区域中一致。变体的序列可能差别在于序列中一个或多个核苷酸的核苷酸替换、缺失或插入,其不损害所述启动子活性。变体可能具有与原始序列相同的长度,或者可能更短或更长。术语“功能性变体”是指表现出seqidno:1的启动子活性,即在rgc中表现出启动子活性、优选为rgc特异性启动子活性的seqidno:1的变体。在一个实施方式中,本发明的启动子包含选自下述序列的seqidno:1的功能性变体或由其构成:-与seqidno:1具有至少80%同一性的序列,-包含seqidno:1的至少100个连续核苷酸的序列,以及-能够在低、中等或高严紧条件下与seqidno:1的核酸序列或其互补链杂交的序列。在特定实施方式中,本发明的启动子包含优选地在seqidno:1的整个序列上与seqidno:1具有至少80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98或99%同一性的功能性变体,或由其构成。本发明的启动子与seqidno:1的多核苷酸可以相差1、2、3、4、5、6、7、8、9、10、11、12、13、14或15个替换、缺失和/或插入。在另一个特定实施方式中,本发明的启动子包含下述功能性变体或由其构成,所述功能性变体具有包含seqidno:1的至少100、200、300、400、500、600、700、800、900个连续核苷酸的序列。优选地,它包含下述功能性变体或由其构成,所述功能性变体具有包含seqidno:1的至少500个连续核苷酸的序列。在另一个特定实施方式中,本发明的启动子包含其序列能够在低、中等或高严紧条件下、优选地在中等严紧条件下、更优选地在高严紧条件下与seqidno:1的核酸序列或其互补链杂交的功能性变体,或由其构成。当在本文中使用时,术语“低严紧条件”意味着长度为至少100个核苷酸的探针,在42℃下在5xsspe,0.3%sds,200微克/ml剪切且变性的鲑鱼精子dna和25%甲酰胺中预杂交和杂交,然后进行12至24小时的标准dna印迹程序。最后将载体材料用2xssc,0.2%sds在50℃下清洗三次,每次15分钟。术语“中等严紧条件”意味着长度为至少100个核苷酸的探针,在42℃下在5xsspe,0.3%sds,200微克/ml剪切且变性的鲑鱼精子dna和35%甲酰胺中预杂交和杂交,然后进行12至24小时的标准dna印迹程序。最后将载体材料用2xssc,0.2%sds在55℃下清洗三次,每次15分钟。术语“高严紧条件”意味着长度为至少100个核苷酸的探针,在42℃下在5xsspe,0.3%sds,200微克/ml剪切且变性的鲑鱼精子dna和50%甲酰胺中预杂交和杂交,然后进行12至24小时的标准dna印迹程序。最后将载体材料用2xssc,0.2%sds在65℃下清洗三次,每次15分钟。本发明的启动子序列的主要优点之一在于它的尺寸小。事实上,本发明的启动子具有小于2kb的长度,因此特别适用于在dna有效载荷严重受限的aav载体中使用。在优选实施方式中,本发明的启动子的长度小于1.5kb,优选地小于1.4、1.3、1.2、1.1或1kb,更优选地小于990、980、970或960个碱基。在某些实施方式中,本发明的启动子没有可操作地连接到sncg基因,特别是人类sncg基因。在某些其他实施方式中,本发明的启动子没有可操作地连接到编码报告蛋白的基因,特别是编码萤光素酶的基因。优选地,本发明的启动子没有可操作地连接到sncg基因或编码萤光素酶的基因。在第二种情况下,本发明涉及一种表达盒,其包含可操作地连接到目标核酸的本发明的启动子。所述可操作地连接到本发明的启动子的核酸可以编码目标多肽或目标核酸。当在本文中使用时,术语“表达盒”是指包含编码序列和所述编码序列的表达所需的一个或多个控制序列的核酸构建物。特别地,这些控制序列之一是本发明的启动子。通常,所述表达盒包含表达选定基因产物所需的编码序列和在所述编码序列之前(5'非编码序列)和之后(3'非编码序列)的调控序列。因此,表达盒通常包含启动子序列、编码序列和通常含有多腺苷化位点和/或转录终止子的3′非翻译区。所述表达盒还可以包含其他调控元件,例如增强子序列、便于dna片段在载体内的插入的多接头序列和/或剪接信号序列。表达盒通常被包含在载体内,以便于克隆和转化。优选地,本发明的启动子被可操作地连接到异源核酸。当在本文中使用时,术语“异源的”意味着除了在天然存在的基因组中所述启动子可操作地连接到的核酸之外的核酸。特别地,在某些实施方式中,本发明的启动子没有可操作地连接到sncg基因,特别是人类sncg基因。在某些其他实施方式中,本发明的启动子没有可操作地连接到编码萤光素酶的基因。优选地,本发明的启动子既没有可操作地连接到sncg基因也没有可操作地连接到编码萤光素酶的基因。在一个实施方式中,所述可操作地连接到本发明的启动子的核酸编码目标多肽。所述目标多肽可以是需要在rgc中表达的任何多肽。特别地,所述目标多肽可以是治疗性多肽、报告蛋白或光遗传学驱动剂。在一个实施方式中,所述可操作地连接到本发明的启动子的核酸是治疗性基因,即编码治疗性多肽。当在本文中使用时,术语“治疗性基因”是指编码在病理状况的治疗中有用的治疗性蛋白的基因。所述治疗性基因在表达时,对它存在于其中的细胞或组织或所述基因在其体内表达的患者提供有益效果。有益效果的实例包括病症或疾病的征兆或症状的改善,病症或疾病的预防或抑制,或所需特征的提供。治疗性基因包括在患者中部分或完全校正遗传缺陷的基因。特别地,所述治疗性基因可以是但不限于编码在基因疗法中有用的蛋白质的核酸序列,以在对象的细胞或组织中缓解由所述蛋白质的缺失、缺损或亚最适水平而造成的缺陷。所述治疗性多肽可以例如提供在rgc中不存在、缺陷或以亚最适水平存在的多肽和/或酶活性,提供在rgc中间接抵消不平衡的多肽和/或酶活性。所述治疗性多肽也可用于通过例如充当显性失活多肽来降低多肽的活性。优选地,所述治疗性多肽提供在rgc中不存在、缺陷或以亚最适水平存在的多肽和/或酶活性,更优选为在rgc中不存在或缺陷的多肽和/或酶活性。治疗性基因的实例包括但不限于用于替换已知引起视网膜疾病的缺失或突变基因的核酸,例如mt-nd4(geneid:4538)、mt-nd1(geneid:4535)、mt-nd6(geneid:4541)、mt-cyb(geneid:4519)、mt-co3(geneid:4514)、mt-nd5(geneid:4540)、mt-nd2(geneid:4536)、mt-coi(geneid:4512)、mt-atp6(geneid:4508)、mt-nd4l(geneid:4539)、opa1(geneid:4976)、opa3(geneid:80207)、opa7(geneid:84233)、aco2和(geneid:50)。所述治疗性基因也可以编码神经营养因子,例如gdnf(geneid:2668)、cntf(geneid:1270)、fgf2(geneid:2247)、bdnf(geneid:627)和epo(geneid:2056),抗凋亡基因例如bcl2(geneid:596)和bcl2l1(geneid:598),抗血管生成因子例如内皮抑素、血管抑素和sflt,抗炎因子例如il10(geneid:3586)、il1r1(geneid:3554)、tgfbi(geneid:7045)和il4(geneid:3565),或视杆细胞来源的视锥细胞活性因子(rdcvf)(geneid:115861)。优选地,所述治疗性基因选自mt-nd4(geneid:4538)、mt-nd1(geneid:4535)、mt-nd6(geneid:4541)、mt-cyb(geneid:4519)、mt-co3(geneid:4514)、mt-nd5(geneid:4540)、mt-nd2(geneid:4536)、mt-coi(geneid:4512)、mt-atp6(geneid:4508)和mt-nd4l(geneid:4539)。更优选地,所述治疗性基因选自mt-nd4(geneid:4538)、mt-nd1(geneid:4535)和mt-nd6(geneid:4541)。可以向治疗性蛋白添加另外的信号肽,特别是以便将它们输入到某些细胞器(例如线粒体)内,将它们从细胞分泌出去,或将它们插入到细胞膜中。在另一个实施方式中,所述目标多肽是光遗传学驱动剂。当在本文中使用时,术语“光遗传学驱动剂”是指使用维生素a或其同工型作为发色团的光化学反应性多肽。光遗传学驱动剂是吸收光并被光激活的光门控离子泵或通道。所述光遗传学驱动剂可以来自于原核生物或真核生物。特别地,它可以是微生物视蛋白或脊椎动物视蛋白。所述光遗传学驱动剂可以是光遗传学激活剂或光遗传学抑制剂。光遗传学激活剂导致细胞在暴露于光之后去极化。当细胞去极化时,细胞的内部负电荷短期变正。细胞内部环境从负到正的转变允许在细胞内和任选地细胞之间两者传输电脉冲。光遗传学激活剂的实例包括但不限于视紫红质,光视蛋白,黑视蛋白,松果体视蛋白,松果体旁视蛋白,va视蛋白,周视蛋白,神经视蛋白,脑视蛋白,视网膜色素,rgr视蛋白,具有红移的光谱性质的微生物视蛋白例如reachr、chrimson或chrimsonr,可以召集gi/o信号传导的脊椎动物视蛋白例如短波长脊椎动物视蛋白或长波长脊椎动物视蛋白,来自于衣藻属(chlamydomonas)微藻的通道视紫红质例如通道视紫红质-1和通道视紫红质-2(来自于莱茵衣藻(chlamydomonasreinhardtii)),及其变体。通道视紫红质的大量变体(例如密码子优化的变体、突变体、嵌合体)不断被产生,以改进这些蛋白的某些特点。这些变体的实例包括但不限于hchr2(l132c)、chr2(h134r)、cheta(e123t)、c1v1(e122t)、c1v1(e162t)、c1v1(e122/162t)、hchr2(c128a)、hchr2(c128s)、hchr2(c128t)、hchr2(c128a/h134r)、hcatch(t159s)、hchief、hchr2(c128s/d156a)、hchr2(t159c)、hchr2(e123t/t159c)、hchr2c(c128t)、chr2c(c128t)、chr2e(q117c)和switchr(综述参见prakash等,natmethods.2012dec;9(12):1171-9)。光遗传学抑制剂在暴露于光后引起细胞超极化。当细胞超极化时,细胞的内部负电荷短期变得更负。向更负的转变通过提高使膜电位移向动作电位阈值所需的刺激来抑制动作电位。在特定实施方式中,光遗传学抑制剂是光门控的离子泵,其在吸收光子后向内运输氯离子和/或向外运输阳离子。在吸收光子后向内运输氯离子或向外运输阳离子的任何适合的光门控、视网膜依赖性离子泵,都可用作光遗传学抑制剂。光遗传学抑制剂的实例包括但不限于嗜盐菌视紫红质例如嗜盐菌视紫红质(nphr)、增强的嗜盐菌视紫红质(enphr2.0和enphr3.0)和红移的嗜盐菌视紫红质halo57,古菌视紫红质-3(ar-3),古菌视紫红质(arch),细菌视紫红质例如增强的细菌视紫红质(ebr),变形菌视紫红质,黄单胞菌视紫红质,斑点小球腔菌(leptosphaeriamaculans)真菌视蛋白(mac),大白鲨交叉嗜盐菌视紫红质,及其变体。在更特别优选的实施方式中,所述光遗传学驱动剂是光遗传学激活剂,优选地选自通道视紫红质、chrimsonr及其变体,且更优选地选自hchr2(l132c)-hcatch和chrimsonr-tdtomato。在更特别优选的实施方式中,所述光遗传学驱动剂是光遗传学激活剂,优选地选自通道视紫红质及其变体,且更优选地是hchr2(l132c)-hcatch。在另一个实施方式中,所述可操作地连接到本发明的启动子的核酸编码报告蛋白。优选地,所述报告蛋白在活的rgc中是可检测的。报告蛋白在本发明的启动子控制下的表达允许特异性检测或识别rgc。所述报告蛋白可以是例如荧光蛋白(如gfp)、钙指示剂(如gcamp)、萤光素酶、碱性磷酸酶、β-半乳糖苷酶、β-内酰胺酶、辣根过氧化物酶及其变体。在特定实施方式中,所述报告蛋白选自荧光蛋白、钙指示剂、碱性磷酸酶、β-半乳糖苷酶、β-内酰胺酶、辣根过氧化物酶及其变体。在另一个实施方式中,所述可操作地连接到本发明的启动子的核酸编码目标核酸。所述目标核酸可以是需要在rgc中表达的任何核酸。特别地,所述目标核酸可以是治疗性核酸。所述核酸可以是例如sirna、shrna、rnai、mirna、反义rna、核酶或脱氧核酶。在特定实施方式中,所述核酸编码当从可操作地连接到本发明的启动子的核酸转录时,可以通过干扰与眼病相关的异常或过量蛋白的翻译或转录来治疗或预防所述疾病的rna。例如,所述目标核酸可以编码通过高度特异性消除或减少编码异常和/或过量蛋白的mrna来治疗所述疾病的rna。本发明的表达盒可以包含可操作地连接到本发明的启动子的一个或多个核酸。例如,所述启动子可以被可操作地连接到一个或多个治疗性基因和编码报告蛋白的核酸,或连接到治疗性基因和光遗传学驱动剂。在这种情况下,也考虑到了本发明的启动子的所有实施方式。在第三种情况下,本发明涉及一种载体,其包含本发明的启动子或本发明的表达盒。当在本文中使用时,术语“载体”是指用作媒介以在体外或体内转移遗传物质、特别是将核酸递送到宿主细胞内的核酸分子。载体包括但不限于质粒、噬粒(phasmid)、粘粒、可转座元件、病毒和人工染色体(例如yac)。优选地,本发明的载体是适用于基因或细胞疗法的载体,特别是适合于靶向rgc。本发明的载体优选为病毒基因组载体,其包括在宿主细胞中建立起目标多肽的表达所需的任何元件,例如启动子如本发明的启动子、itr、核糖体结合元件、终止子、增强子、选择标志物、内含子、polya信号和/或复制原点。在某些实施方式中,所述载体是病毒载体,例如源自于莫洛尼鼠白血病病毒载体(momlv)、mscv、sffv、mpsv或snv的载体、慢病毒载体(例如源自于人免疫缺陷病毒(hiv)、猴免疫缺陷病毒(siv)、猫免疫缺陷病毒(fiv)、牛免疫缺陷病毒(biv)或马传染性贫血病毒(eiav))、腺病毒(ad)载体、腺相关病毒(aav)载体、猴病毒40(sv-40)载体、牛乳头瘤病毒载体、epstein-barr病毒载体、疱疹病毒载体、痘苗病毒载体、哈维鼠肉瘤病毒载体、鼠乳腺肿瘤病毒载体、劳氏肉瘤病毒载体。在特定实施方式中,所述载体是反转录病毒载体,优选为慢病毒载体或非致病性细小病毒。正如在本领域中已知的,取决于考虑使用的具体病毒载体,应该将适合的序列引入到本发明的载体中以获得功能性病毒载体,例如用于aav载体的aavitr或用于慢病毒载体的ltr。在优选实施方式中,所述载体是aav载体。人类细小病毒腺相关病毒(aav)是一种依赖病毒,其天然地有关于复制的缺陷,能够整合到被感染的细胞的基因组中,以建立潜伏感染。最后一种性质在哺乳动物病毒中似乎是独一无二的,因为所述整合发生在人类基因组中位于19号染色体上被称为aavsl的特定位点处(19ql3.3-qter)。因此,aav作为用于人类基因疗法的潜在载体,唤起了相当大的兴趣。所述病毒的有利性质包括它与任何人类疾病缺乏关联,它感染分裂和非分裂细胞两者的能力,以及可以感染源自于不同组织的广范围的细胞系。当在本文中使用时,术语“aav载体”是指包含一个或多个异源序列(即不是aav起源的核酸序列)的多核苷酸载体,所述异源序列侧接有至少一个aav末端反向重复序列(itr),优选为两个itr。这种aav载体当存在于已用适合的辅助病毒(或表达适合的辅助病毒功能的病毒)感染且表达aavrep和cap基因产物(即aavrep和cap蛋白)的宿主细胞中时,可以被复制并包装在感染性病毒粒子中。“末端反向重复序列”或“itr”序列是本领域中公知的术语,并且是指存在于病毒基因组的末端处、方向相反的相对短的序列。“aav末端反向重复序列(itr)”序列是存在于本源单链aav基因组的两个末端处大约145个核苷酸的序列。所述itr的最外部的125个核苷酸可以以两种可选取向中的任一种存在,引起不同aav基因组之间和单个aav基因组的两个末端之间的不均一性。最外部的125个核苷酸也含有几个更短的自身互补的区域(被称为a、a'、b、b'、c、c和d区),允许在itr的这一部分内发生链内碱基配对。在本发明的载体中使用的aavitr可以具有野生型核苷酸序列,或者可以通过插入、缺失或替换被改变。aav载体的末端反向重复序列(itr)的血清型可以选自任何已知的人类或非人类aav血清型。当aav载体被并入到更大的多核苷酸中(例如染色体中或另一个载体例如用于克隆或转染的质粒中)时,所述aav载体可以被称为“前载体”,其可以在aav包装功能和适合的辅助病毒功能存在下通过复制和衣壳化来被“挽救”。本发明的aav载体可以采取多种形式中的任一种,包括但不限于质粒、线性人工染色体,与脂质复合,包封在脂质体内以及包封在病毒粒子例如aav粒子中。本发明的启动子或表达盒可以通过专业技术人员已知的任何方法引入到所述载体中。所述载体还可以包含一个或多个下述核酸序列,所述核酸序列编码可选择标志物例如营养缺陷型标志物(例如leu2、ura3、trp1或his3)、可检测标签例如荧光或发光蛋白(例如gfp、egfp、dsred、cfp)或提供对化学/有毒化合物的抗性的蛋白(例如提供对替莫唑胺的抗性的mgmt基因)。这些标志物可用于选择或检测包含所述载体的宿主细胞,并且可以由专业技术人员根据所述宿主细胞容易地选择。在这种情况下,也考虑到了本发明的启动子和表达盒的所有实施方式。可以将本发明的载体包装在病毒衣壳中以产生“病毒粒子”。因此,在另一种情况下,本发明还涉及一种包含本发明的载体的病毒粒子。在特定实施方式中,所述载体是aav载体,并被包装在aav来源的衣壳中,以产生“腺相关病毒粒子”或“aav粒子”。因此,本文中使用的术语“aav粒子”是指由至少一种aav衣壳蛋白和被衣壳化的aav载体基因组构成的病毒粒子。衣壳血清型决定所述aav粒子的嗜性范围。现在已鉴定到腺相关病毒(aav)的多种血清型,包括12种人类血清型和超过100种来自于非人类灵长动物的血清型(howarth等,2010,cellbioltoxicol26:1-10)。在这些血清型中,人类血清型2是被开发作为基因转移载体的第一种aav。其他目前使用的aav血清型包括但不限于aav1、aav3、aav4、aav5、aav6、aav7、aav8、aavrh8、aav9、aav10、aavrh10、aav11、aav12、aavrh74和aavdj等。此外,非天然的工程改造的变体和嵌合aav也可以是有用的。特别地,所述衣壳蛋白可以是包含增强转导效率的一个或多个氨基酸替换的变体。不同的aav血清型被用于优化特定靶细胞的转导或靶向特定靶组织内的特定细胞类型(例如rgc)。aav粒子可以包含同一血清型的病毒蛋白和病毒核酸或aav的任何天然或人工序列变体。例如,所述aav粒子可以包含aav2衣壳蛋白和至少一个、优选地两个aav2itr。本文中提供了用于生产aav粒子的aav血清型的任何组合,如同每种组合已在本文中明确陈述。在优选实施方式中,所述aav粒子包含选自aav2、aav-5、aav-7m8(aav2-7m8,dalkara等,scitranslmed(2013),5,189ra76)、aav9或aav8衣壳的aav来源的衣壳。aav病毒可以使用常规的分子生物学技术进行工程改造,使得可以优化这些粒子以用于核酸序列的细胞特异性递送,用于最小化免疫原性,用于调节稳定性和粒子寿命,用于高效降解,用于向细胞核的准确递送。作为使用aav天然血清型的可替选方式,在本发明的情形中可以使用人工aav血清型,包括但不限于具有非天然存在的衣壳蛋白的aav。这种人工衣壳可以通过任何适合的技术,使用所选的aav序列(例如vpl衣壳蛋白的片段)与异源序列的组合来产生,所述异源序列可以从不同的选定aav血清型、同一aav血清型的非毗连部分、非aav病毒来源或非病毒来源获得。人工aav血清型可以是但不限于嵌合的aav衣壳或突变的aav衣壳。嵌合衣壳包含源自于至少两种不同aav血清型的vp衣壳蛋白,或包含将源自于至少两种aav血清型的vp蛋白区域或结构域组合的至少一种嵌合的vp蛋白。衣壳蛋白也可以被突变,特别是用于提高转导效率。突变的aav衣壳可以从通过易错pcr和/或肽插入或通过包含一个或几个氨基酸替换而插入的衣壳修饰来获得。特别地,可以在天然或非天然衣壳蛋白(例如vp1、vp2或vp3)的任一个或多个酪氨酸残基中制造突变。优选地,突变的残基是表面暴露的酪氨酸残基。示例性突变包括但不限于酪氨酸到苯丙氨酸的替换,例如y252f、y272f、y444f、y500f、y700f、y704f、y730f、y275f、y281f、y508f、y576f、y612g、y673f和y720f。在优选实施方式中,所述aav粒子包含aav2来源的衣壳。在这个实施方式中,所述衣壳可以包含一个或多个酪氨酸到苯丙氨酸的替换,优选地包含y444f替换。此外,所述aav粒子的基因组载体(即本发明的载体)可以是单链或自身互补的双链基因组。自身互补的双链aav载体通过从aav末端重复序列之一缺失末端分离位点(trs)来产生。这些其复制基因组是野生型aav基因组长度的一半的修饰的载体,具有包装dna二聚体的倾向性。在优选实施方式中,在本发明的实践中应用的aav粒子具有单链基因组。在本领域中,已知大量用于生产病毒粒子、特别是aav粒子的方法,包括转染、稳定细胞系生产和感染性杂合病毒生产系统,包括腺病毒-aav杂合体、疱疹病毒-aav杂合体(conway,je等,(1997)virology71(11):8780-8789)和杆状病毒-aav杂合体。用于生产aav病毒粒子的aav生产培养物都需要:1)适合的宿主细胞,包括例如人类来源的细胞系例如hela、a549或293细胞,或在杆状病毒生产系统的情况下昆虫来源的细胞系例如sf-9;2)适合的辅助病毒功能,其由野生型或突变的腺病毒(例如温度敏感型腺病毒)、疱疹病毒、杆状病毒或提供辅助病毒功能的质粒构建物提供;3)aavrep和cap基因和基因产物;4)侧接有至少一个aavitr序列的目标核酸,例如本发明的载体;以及5)本领域中公知的支持aav生产的适合的培养基和培养基组分。在实践本发明中,用于生产aav粒子的宿主细胞包括哺乳动物细胞、昆虫细胞、植物细胞、微生物和酵母。宿主细胞可以是其中aavrep和cap基因被稳定地维持在所述宿主细胞中的包装细胞或aav载体基因组被稳定地维持在其中的生产细胞。示例性的包装和生产细胞源自于293、a549或hela细胞。然后使用本领域中已知的标准技术纯化并配制aav粒子。在这种情况下,也考虑到了本发明的启动子、表达盒和载体的所有实施方式。在另一种情况下,本发明还涉及一种用本发明的表达盒、载体或病毒粒子转化或转染的分离的宿主细胞。所述宿主细胞可以是任何动物细胞、植物细胞、细菌细胞或酵母。优选地,所述宿主细胞是哺乳动物细胞或昆虫细胞。更优选地,所述宿主细胞是人类细胞。在优选实施方式中,所述宿主细胞是视网膜神经节细胞,特别是人类rgc。可以使用任何已知的技术将本发明的表达盒或载体转移到宿主细胞中,所述技术包括但不限于磷酸钙-dna沉淀、deae-dextran转染、电穿孔、微注射、基因枪、脂质转染或病毒感染,并且本发明的表达盒或载体可以以异位(ectopic)形式维持在所述宿主细胞中,或者可以整合到基因组中。在优选实施方式中,通过病毒感染将本发明的表达盒或载体转移到所述宿主细胞中,优选地使用本发明的病毒粒子,更优选地使用本发明的aav粒子。在这种情况下,也考虑到了本发明的启动子、表达盒、载体和病毒粒子的所有实施方式。本发明还涉及包含本发明的表达盒、载体、病毒粒子或细胞的药物组合物。这些组合物包含治疗有效量的治疗性药剂(本发明的表达盒、载体、病毒粒子或细胞)和可药用赋形剂。当在本文中使用时,术语“可药用的”意味着被监管机构或公认的药典例如《欧洲药典》批准用于动物和/或人类。术语“赋形剂”是指治疗性药剂与其一起给药的稀释剂、佐剂、载体或运载工具。正如本领域中公知的,可药用赋形剂是便于药理有效物质的给药的相对惰性的物质,并且可以被提供为液体溶液或悬液、乳液或适合于在使用之前溶解或悬浮在液体中的固体形式。例如,赋形剂可以提供外形或稠度,或充当稀释剂。适合的赋形剂包括但不限于稳定剂、润湿和乳化剂、用于改变渗透压的盐类、囊封剂、ph缓冲物质和缓冲剂。适合的赋形剂包括任何适合于直接递送到眼的药剂,其可以被给药而没有过度毒性。可药用赋形剂包括但不限于山梨糖醇、各种不同的吐温化合物中的任一者以及液体例如水、盐水、甘油和乙醇。其中可以包括可药用盐,例如无机酸盐如盐酸盐、氢溴酸盐、磷酸盐、硫酸盐等,以及有机酸的盐例如乙酸盐、丙酸盐、丙二酸盐、苯甲酸盐等。可药用赋形剂的充分讨论可以在《remington制药学》(remington'spharmaceuticalsciences)第15版中获得。优选地,所述组合物被配制成给药到眼,特别是通过眼内注射例如通过视网膜下和/或玻璃体内给药。因此,所述组合物可以合并有可药用赋形剂例如盐水、ringer's平衡盐溶液(ph7.4)等。本文中描述的药物组合物可以以单一单元剂量或多剂量形式包装。在一个实施方式中,所述药物组合物包含本发明的载体或病毒粒子,更优选为aav载体或粒子。在另一个实施方式中,所述药物组合物包含本发明的宿主细胞,优选为本发明的人类宿主细胞,即用本发明的表达盒、载体或病毒粒子、优选地用aav粒子转化或转染的宿主细胞。任选地,所述包含宿主细胞的组合物可以在适合于储存细胞的任何温度下冷冻储存。例如,所述细胞可以在约-20℃、-80℃或任何其他适合的温度下冷冻。低温冷冻的细胞可以储存在适合的容器中并制备成用于储存,以降低细胞损伤的风险并最大化细胞融化时存活的可能性。或者,所述细胞也可以维持在冷藏室温,例如约4℃下。待给药的药物组合物的量可以通过本领域普通技术人员公知的标准程序来确定。为了确定适合的剂量,必须将患者的生理学数据(例如年龄、大小和体重)和待治疗的疾病的类型和严重性考虑在内。本发明的药物组合物可以作为单剂量或在多剂量中给药。在特定实施方式中,所述组合物包含本发明的病毒粒子,并且每个单元剂量包含108至1013个病毒粒子,优选地109至1012个粒子。所述药物组合物还可以包含一种或几种其他活性化合物例如皮质甾类、抗生素、镇痛药、免疫抑制剂、营养因子或其任何组合。在这种情况下,也考虑到了本发明的启动子、表达盒、载体、病毒粒子和宿主细胞的所有实施方式。在另一种情况下,本发明还涉及:-本发明的药物组合物,其用于治疗眼病,-本发明的表达盒、载体、病毒粒子或宿主细胞,其用于治疗眼病,-本发明的表达盒、载体、病毒粒子或宿主细胞的用途,其用于制造药物以用于治疗眼病,以及-一种治疗眼病的方法,所述方法包括向需要的对象给药治疗有效量的本发明的药物组合物。在一个实施方式中,所述眼病是与视网膜神经节细胞变性相关的疾病。与视网膜神经节细胞变性相关的疾病的实例包括但不限于遗传性视神经病(利伯氏遗传性视神经病、显性视神经病)、压迫性视神经病(眶假性肿瘤、甲状腺眼病)、自体免疫性视神经病(狼疮)、糖尿病性视网膜病、青光眼性视神经病(gond)、包括青光眼、动脉缺血性视神经病(巨细胞动脉炎)、非动脉缺血性视神经病、浸润性视神经病(肉状瘤病)、传染性视神经病(梅毒、莱姆病、弓形体病、带状疱疹)、来自于脱髓鞘病的视神经炎、辐射后视神经病和肠病性肢端皮炎(acrodermatitisenteropathica)。在特定实施方式中,所述眼病是遗传性视神经病,优选地选自利伯氏遗传性视神经病(lhon;omim#535000)、视神经萎缩1(kjer型视神经萎缩;omim#165500)、视神经萎缩和白内障(视神经萎缩3;omim#165300)和伴有或不伴有听神经病的视神经萎缩7(omim#612989)。优选地,所述眼病是与视网膜神经节细胞变性相关的遗传性眼病,例如lhon或显性视神经病,并且从本发明的表达盒、载体或病毒粒子表达的目标多肽是治疗性蛋白,特别是在所述患者中校正所述遗传缺陷的治疗性蛋白。在优选实施方式中,所述眼病选自lhon和显性视神经病,优选地选自视神经萎缩1、视神经萎缩和白内障(视神经萎缩3)和伴有或不伴有听神经病的视神经萎缩7,并且所述目标多肽选自mt-nd4、mt-nd1、mt-nd6、mt-cyb、mt-co3、mt-nd5、mt-nd2、mt-coi、mt-atp6、mt-nd4l、opa1、opa3、opa7和aco2。在感光细胞由于遗传性或获得性疾病而丧失的疾病中,rgc在感光细胞变性后仍长期存留。因此,rgc构成了使用光遗传学恢复视网膜的治疗靶点。在这种情形中,rgc是独立于变性细胞的细胞靶点,其中光敏蛋白即光遗传学驱动剂以强烈且受限的方式表达对于视力恢复的成功来说是必不可少的。因此,在另一个实施方式中,所述眼病是与感光细胞变性相关的疾病。优选地,在这个实施方式中,所述目标多肽是如上所述的光遗传学驱动剂,并且所述治疗是光遗传学治疗。与感光细胞变性相关的疾病的实例包括但不限于年龄相关性黄斑变性、利伯氏遗传性视神经病、视锥细胞-视杆细胞营养不良、利伯氏先天性黑朦、斯特格氏病、糖尿病性视网膜病、视网膜脱离、贝斯特氏病、色素性视网膜炎、无脉络膜症和视网膜毯层变性。或者,所述眼病选自不必须或特异性与视网膜神经节细胞或感光细胞变性相关,但可以通过在视网膜神经节细胞中特异性表达编码目标多肽或目标核酸的核酸来治疗或预防的疾病(例如青光眼)。当在本文中使用时,术语“治疗”是指旨在改善患者的健康状况的任何行动,例如疾病的疗法、阻止、预防和迟滞。在某些实施方式中,这个术语是指疾病或与疾病相关的症状的改善或根除。在其他实施方式中,该术语是指由向患有疾病的对象给药一种或多种治疗性药剂引起的最小化所述疾病的蔓延或恶化。特别地,术语“眼病的治疗”可以是指提供改善的视力、防止疾病发展至完全失明、防止损伤蔓延到未受伤的眼细胞、在受伤的眼细胞中改善损伤、防止视网膜损伤的发生或挽救具有轻度或晚期疾病的眼的治疗。在某些实施方式中,该术语是指通过提供校正患者的遗传缺陷的治疗性蛋白以防止、减轻或停止rgc变性的治疗。在某些其他实施方式中,该术语是指使用光遗传学恢复视网膜或恢复视力的治疗。“治疗有效量”意味着本发明的药物组合物给药到对象的足以构成如上所定义的眼病的治疗的量。所述药物组合物可以作为单剂量或在多剂量中给药。在特定实施方式中,所述药物组合物包含本发明的病毒粒子,并且每个单元剂量包含108至1013个病毒粒子,优选地109至1012个粒子。在本发明的用于治疗眼病的方法中,本发明的药物组合物优选地眼内给药,更优选地通过视网膜下或玻璃体内给药。本发明的方法还可以包括向所述对象给药至少一种另外的治疗性药剂。特别地,所述治疗性药剂可以选自皮质甾类、抗生素、镇痛剂、免疫抑制剂或营养因子或其任何组合。本发明的组合物可以在所述疾病变得出现症状之前或之后,例如在部分或完全rgc或感光细胞变性之前或之后和/或在部分或完全失去视力之前或之后给药。在这种情况下,也考虑到了本发明的启动子、表达盒、载体、病毒粒子、宿主细胞和药物组合物的所有实施方式。rgc合在一起将形成图像和不形成图像的视觉信息以动作电位的形式从视网膜传输到大脑。因此,对研究rgc的功能存在极大兴趣,因为每种类型的rgc的形状、尺寸和投影是截然不同的,并且因为它们据认为在视觉功能中发挥相当不同并可能独立的作用。因此,在另一种情况下,本发明还涉及一种包含本发明的表达盒、载体、病毒粒子或宿主细胞的非人类动物模型。这种动物模型可用于rgc功能的体内研究。使用本发明的启动子、表达盒、载体或病毒粒子可以鉴定或追踪rgc或监测它们的活性,例如通过报告蛋白或电压或钙敏感性蛋白的表达。所述非人类动物模型也可用于筛选方法中,用于鉴定或选择作用于rgc的药剂。优选地,所述非人类动物模型是哺乳动物,更优选为灵长动物、啮齿动物、兔或小型猪。所述启动子、表达盒或载体可以以游离体(episomic)形式维持在这种模型的细胞中,或者可以整合在其基因组中。用于转染或转化动物细胞或用于生产在所选启动子、即本发明的启动子的控制之下表达目标核酸序列的转基因动物的方法,对专业技术人员来说是公知的,并且可以根据细胞和动物容易地调整。在这种情况下,也考虑到了本发明的启动子、表达盒、载体、病毒粒子、宿主细胞的所有实施方式。本文中提到或引用的所有专利、专利申请、临时申请和出版物,其整体、包括所有的图表,在它们不与本说明书的明确教示不一致的范围内,通过参考并入本文。提供下面的实施例是出于说明而不是限制的目的。实施例材料和方法动物所有实验按照国立卫生研究院实验动物护理和使用指南(nationalinstitutesofhealthguideforcareanduseoflaboratoryanimals)来进行。所述方案得到当地动物伦理学委员会(localanimalethicscommittees)批准,并按照欧洲议会的指令2010/63/eu进行。在本研究中使用的所有小鼠都是来自于janvierlaboratories(legenestsaintisle,france)的c3h/hen(rd1小鼠)或c57bl6j小鼠(野生型),或来自于外国来源的食蟹猴(macacafasicularis)。aav生产重组aav通过质粒共转染方法来生产(choi等,curr.protoc.hum.genet.2007;chapter12:unit12.9),并将得到的裂解液如先前所述通过碘克沙醇梯度超速离心进行纯化。简单来说,将40%碘克沙醇级分浓缩并使用amiconultra-15离心过滤装置进行缓冲液更换。然后将载体储用物相对于标准品通过实时pcr进行dna酶抗性载体基因组滴定(aurnhammerc等,humgenethermethods.2012feb;23(1):18-28)。注射将小鼠用氯胺酮(50mg/kg)和甲苯噻嗪(10mg/kg隆朋)麻醉。瞳孔扩张,并将30号超细一次性针头在赤道处并紧靠角膜缘通过巩膜进入玻璃体腔。在直接观察到所述针头在玻璃体腔中心时,进行含有107至1011个aav粒子的1μl储用物的注射。将灵长动物用10:1mg/kg氯胺酮:甲苯噻嗪麻醉。瞳孔扩张,并使用30号针头将含有1x1011或5x1011个病毒粒子的100μl病毒载体在角膜缘后约4mm处通过巩膜注射到每只眼的玻璃体中。在注射后向角膜施用眼用甾类和抗生素软膏。免疫组织化学解剖转导过的小鼠的视网膜,将其在4%聚甲醛中在室温固定30min,并用pbs清洗。然后将视网膜在含有1%tritonx-100、0.5%tween20和5%牛血清白蛋白的pbs的阻断缓冲液中,在室温(rt)处理1h。将小鼠视网膜在稀释一倍的阻断缓冲液中与针对gfp的多克隆抗体(lifetechnologies;1:2000)和抗brn3a单克隆抗体(milliporechemicon;1:100)在4℃下温浴过夜。然后将视网膜在稀释一倍的阻断缓冲液中与分别偶联有alexatm594、alexatm488和alexatm647的抗兔igg、抗小鼠igg第二抗体(molecularprobes;1:500)在rt温浴1h。将灵长动物视网膜在相似条件下用针对brn3a、gfp和通道视紫红质的抗体标记。随后通过将样本与4’,6-二脒基-2-苯基吲哚(sigma-aldrich;10μg/ml)温浴来显示细胞核。将视网膜清洗并平放固定在两个盖玻片之间的固定介质中,然后进行初始共聚焦获取。先前标记的平放固定物的组织切片,通过解除固定、低温保存并包埋在oct中,然后冷冻切片来获得(15μm),并通过共聚焦显微术来观察。共聚焦显微术共聚焦显微术在olympusfv1000激光扫描共聚焦显微镜上进行。图像被逐行顺序获取以便减少激发和发射串扰,步级大小按照nyquist-shannon采样定理确定。使用最小化最终图像中的过饱和像素的曝光设置。然后将12位图像用fiji处理,将z-剖面在z-投影功能下使用最大强度投影在单一平面上,并最终转变成8位rgb颜色模式。转导效率通过对小鼠中和灵长动物视网膜的窝区中转导有catch-gfp的brn3a(+)细胞进行计数来评估。通过rgc层的共聚焦堆叠图使用20x来获取。分离的视网膜的mea记录将小鼠麻醉并通过快速颈椎脱位处死,灵长动物接受致死剂量的戊巴比妥。取下眼球并置于室温下用95%o2和5%co2鼓泡的ames培养基(sigmaaldricha1420)中。将分离的视网膜置于纤维素膜上并轻柔压向mea(mea256100/30ir-ito,multichannelsystems,germany),使rgc面朝电极。在实验期间,将视网膜在34℃下用鼓泡的ames培养基以1-2ml/min的速率连续灌注。将代谢型谷氨酸受体激动剂l-(+)-2-氨基-4-膦酰基丁酸(lap-4,tocrisbioscience,catno.0103)和甘氨酸受体拮抗剂马钱子碱盐酸盐(sigmaaldrichs8753)分别新鲜稀释到50μm和10μm的浓度,并在记录之前10分钟通过灌注系统水浴施加。全视野光刺激使用由stg2008刺激发生器(mcs)驱动的polychromev单色仪(olympus)施加。将输出光强度校准到1.1014个光子/cm2/s至1.1017个光子/cm2/s的范围。刺激出现2秒,间隔为10秒。响应的波长灵敏度通过从400nm至650nm以10nm的步级刺激10次来确定。所试验的波长的顺序是随机的,以防止视网膜的任何适应。将原始的细胞外rgc活动放大并以20khz采样。将得到的数据储存并用200hz高通滤波器过滤,用于随后使用spike2软件v.7(cedco,uk)的离线分析。单一单元光栅图使用基于波形的主成分分析的模板匹配和群聚分组的组合来获得。在我们的群体分析中,在z-分值分析的基础上确定显著响应。我们估算了刺激之前的活动的平均值和标准偏差,并认为如果在刺激发生或抵消后2s内(对于50ms的面元大小来说)活动超过所述平均值多于4倍的标准偏差,则检测到响应。在不同实验上计算误差条。对于针对不同波长的光的响应来说,我们在刺激后1s的窗口中测量对每次闪光的响应。然后我们将每个细胞的响应针对它的最大放电率响应进行归一化。对于针对不同强度的光的响应来说,我们通过在成组的记录细胞上进行自举来估算误差条。双光子成像和膜片钳记录使用装备有25x水浸物镜(xlpln25xwmp/na1.05,olympus)和脉冲飞秒激光器(insighttmdeepseetm-newportcorporation)的定制双光子显微镜对catch-gfp阳性视网膜神经节细胞进行成像。在充氧(95%o2,5%co2)ames培养基(sigma-aldrich)中分离来自于rd1小鼠的aav处理的视网膜。对于活体双光子成像来说,使用剃须刀片组织切片机(stoelting)切出视网膜切片(300μm),将其置于显微镜的记录室中,并使用波长为930nm的激发激光获取z-堆叠图。图像使用imagej离线处理。在成像期间,将视网膜用充氧的ames培养基浇注(superfuse)。我们将axonmulticlamp700b放大器用于全细胞记录。膜片电极由硼硅酸盐玻璃(bf100-50-10,sutterinstruments)制成,并拉制到8-10mω。将移液管装填112.5mmcsmeso4,1mmmgso4,7.8×10-3mmcacl2,0.5mmbapta,10mmhepes,4mmatp-na2,0.5mmgtp-na3,5mmn-乙基利多卡因溴化物(qx314-br)(ph7.2)。将细胞在-60mv的电位下钳住以分离兴奋电流。视觉皮层中的体内记录将小鼠用低剂量的氯胺酮-甲苯噻嗪注射液(氯胺酮:100mg/kg,甲苯噻嗪:10mg/kg)镇静,然后用乌拉坦(1.0g/kg,10%w/v盐水溶液)麻醉。将动物置于立体定位架中。将温度维持在37℃,并将覆盖有维生素a(allergan)的盖玻片置于双眼上以防止角膜脱水。在被治疗眼的对侧半球中v1上方进行颅骨切开术(1mm2),其中心位于距λ点横向3mm和前方0.5mm处。移除硬脑膜,并使用3-轴显微操纵器(sutterinstruments)以与皮层表面成30°角插入电极。将它推进800μm,并将暴露出的表面用琼脂糖(1.2%,在皮层缓冲液中)覆盖。视觉刺激通过放置在距眼1cm处的470nm照准led(m470l3型,thorlabs)产生。隔离锥确保光照被限制到受刺激的眼。使用线性多位点硅微探针(间隔50μm的16个电极)进行记录。对于每次采样来说,在对200次试验进行平均后,选择显示出具有最大峰值幅度的vep的电极用于定量。所述刺激由通过digidata(axon)引发的以1hz重复200次的200ms蓝光脉冲构成。信号在matlab中使用自定义脚本进行分析。对于局部场电位来说,将信号以300hz低通滤波并对200个试验进行平均。在非人类灵长动物中的体内成像和眼科检查gfp的荧光图像(眼底自荧光模式:激发波长为488nm,阻挡滤光片为500nm)和眼底的红外图片和oct图像,在瞳孔扩张后使用spectralishra+oct系统(heidelbergengineering,heidelberg,germany)获取。在给药之前、2周时和之后每个月,对所有恒河猴进行由裂隙灯生物显微术(sl-14型便携式裂隙灯,kowa)和间接检眼镜检查(hk150-1uno型间接双筒检眼镜,heine)构成的眼科检查。对恒河猴视网膜的组织病理学研究将来自于用高剂量注射的nhp的眼在注射后3个月时剜出,插入针头并注入0.15-0.3ml固定液,直至眼球变得肿胀。将眼在固定液中浸没固定过夜并处理,以制造横跨整个结构的水平横截面。然后将呈现出所有所需眼结构的视网膜横截面在nanozoomer(hamamatsu,japan)上成像。实施例1hsncg的启动子序列sncg基因位于10号染色体(10q23.3)上(图1)。它含有5个外显子,从+1转录位点到第5个外显子的末端延伸跨越3.5kb。multimerine2基因(mmrn2)的第一个外显子位于+1sncg转录位点下游863bp。为了提取人类sncg启动子的序列,从hek293t细胞扩增-785至+163区域(在图1中用箭头指示)。扩增引物如下:正向引物:5'-cacaagccagttcctgtcc-3'(seqidno:2),和反向引物:5'-gggtgtgcagggttgtg-3'(seqidno:3)。所述启动子序列通过30个连续的循环进行扩增,所述循环由下述步骤构成:94℃下30秒的变性步骤,然后是54℃下1分钟的退火步骤,以及72℃下1分钟的延伸步骤。然后通过使用dna拓扑异构酶i的方法将pcr产物(seqidno:1)亚克隆到pentr-d/topo质粒中并测序。确认所述序列与genbank中在geneid号6623下发表的序列相一致。本发明人从这个质粒生产aav载体和源自于hiv-1的慢病毒载体,其在seqidno:1的启动子(图1)控制之下表达gfp报告基因。包含mpgk或hsncg启动子和编码gfp蛋白的核酸的aav-2/y444f载体的构建和生产构建使用gateway方法,通过同源重组将sncg启动子(seqidno:1)和pgk启动子序列引入到用于aav生产的穿梭质粒中,所述质粒从5’itr至3’itr含有:rfa插入片段(允许使用gateway系统进行同源重组),编码gfp的cdna,和牛生长激素的多腺苷化信号(bghpolya)。将该载体使用具有引起替换y444f的点突变的血清型2衣壳制成假型。从编码aav的rep和cap基因的包装质粒通过定点突变来引入所述突变。生产aav粒子通过用携带含有表达盒的重组aav2基因组的质粒、表达rep2和cap2-y444f基因的包装质粒和辅助质粒共转染(使用磷酸钙共沉淀)hek-293t细胞来生产。然后通过不连续碘克沙醇梯度超速离心从被转染细胞的细胞质提取液纯化并浓缩aav粒子。病毒滴度通过aav粒子的基因组dna的itr序列的定量pcr扩增来测量。实施例2c57bl6/j成年小鼠(6周)接受以1011vg(载体基因组)的剂量在pbs中稀释的包含seqidno:1的启动子和编码gfp蛋白的核酸(参见实施例1和图1)的aav-2/y444f载体的玻璃体内注射。在注射后1个月,眼底和视网膜具有正常外观,表明载体或手术程序没有毒性(图2a)。gfp报告基因在视网膜中的表达通过使用直接荧光对眼底进行体内成像来观察(图2a)。通过腹膜内注射氯胺酮与甲苯噻嗪的混合物将动物麻醉,并通过表面施用新辛弗林和托吡卡胺将瞳孔扩张。在瞳孔完全扩张后,通过特殊设计用于观察啮齿动物的眼底的荧光照相机(microniii,phoenixlaboratories)检查动物。使用荧光时,检测到大量表达gfp的细胞体,并且也观察到朝向乳突或视神经头会聚的神经纤维(未示出)。这些神经纤维的存在证实了gfp在rgc中表达。实施例3为了表征hsncg启动子在视网膜中的表达模式,本发明人将hsncg启动子(seqidno:1)与mpgk启动子这种已知在视网膜中提供高水平表达的遍在启动子进行比较。将两组c57bl6/j小鼠用以1011vg的剂量在pbs中稀释并在mpgk或hsncg启动子的控制之下编码gfp的aav2-y444f载体进行玻璃体内注射。在注射后1个月,如上所述对gfp表达进行体内分析。然后将动物安乐死,并通过含有4%聚甲醛的pbs溶液的心内灌注将组织固定。随后取出眼球,在相同的固定液中后固定1小时,在含有25%蔗糖的pbs溶液中冷冻保护,然后使用低温恒温器切片到16μm的厚度。然后在显微镜下通过观察直接荧光和在使用bnr3a作为神经节细胞的特异性标志物进行免疫标记后,分析gfp表达。在注射有包含遍在启动子mpgk的aav载体的小鼠中,大量转导的细胞存在于rgc层中,但是也存在于双极细胞层(inl)和感光细胞层(onl)处(图2f)。也清楚地检测到具有感光细胞或müller细胞形态的细胞。此外,转导的细胞在inl中的定位表明双极或无长突神经元也被转导。在注射有包含seqidno:1的启动子的aav载体的小鼠中,rgc被非常强地标记。在它们的细胞体和它们在内丛状层处的树突分枝中检测到gfp,揭示了这些分枝的层状组织(图2c)。除了少数水平细胞之外,gfp的表达限于神经节细胞层。实施例4我们通过与brn3a进行共标记以调查表达的定位,来评估rgc中基因表达的强度和特异性。brn3a在rgc中特异性表达,并且针对这种转录因子的抗体被当作鉴定鼠类rgc的可靠标志物(quina等,j.neurosci.2005;25(50):11595–11604)。将两组c57bl6/j小鼠用以1011vg的剂量在pbs中稀释并在cmv或hsncg启动子的控制之下编码gfp的aav2载体进行玻璃体内注射。在注射后1个月,将动物安乐死,并通过含有4%聚甲醛的pbs溶液的心内灌注将组织固定。随后取出眼球,在相同的固定液中后固定1小时,在含有25%蔗糖的pbs溶液中冷冻保护,然后使用低温恒温器切片到16μm的厚度。然后在显微镜下通过观察直接荧光和在使用bnr3a作为神经节细胞的特异性标志物进行免疫标记后,分析gfp表达。在注射有包含seqidno:1的启动子的aav2载体的小鼠中,rgc被非常强地标记。在它们的细胞体和它们在内丛状层处的树突分枝中检测到gfp,揭示了这些分枝的层状组织。来自于sncg-gfp视网膜的横截面的共聚焦显微术图像(图3b)显示出在rgc中强烈的gfp表达,并且这种表达与bnr3a标记高度共定位。实施例5将每种aav2-cmv-gfp或aav2-sncg-gfp载体的5x1011个病毒粒子在100μl体积中玻璃体内注射到正常恒河猴(食蟹猴(macacafascicularis))的眼中。我们通过眼底荧光成像评估食蟹猴视网膜中的gfp表达。gfp的荧光图像(眼底自荧光模式:激发波长为488nm,阻挡滤光片为500nm)在瞳孔扩张后使用spectralishra+oct系统(spectralishra+oct;heidelbergengineering,heidelberg,germany)获取。荧光图像显示出使用含有sncg启动子的aav-gfp载体(图4a)与使用cmv启动子(图4b)相比,在转导区域(窝周环)与背景之间的gfp表达的最大强度。这个实验证实,在非人类灵长动物中,使用sncg启动子(seqidno:1)获得更高的转入基因表达。实施例6使用seqidno:1的启动子序列时小鼠视网膜中强烈的rgc特异性表达将在实施例1中从人γ突触核蛋白(sncg)的调控区获得的启动子序列(seqidno:1)克隆到gfp上游。我们在小鼠视网膜中表征了aav介导的表达模式,并在rgc中看到高水平gfp表达。然后我们将这个序列克隆到aav骨架中人源化catch(带有l132c突变的人类密码子优化的通道视紫红质)的上游。aav2载体使用驱动与gfp融合的hcatch的表达的cmv或sncg启动子来生产。用驱动hcatch-gfp的表达的cmv或sncg注射5只rd1小鼠眼。荧光眼底图像显示,相对于用cmv注射的眼,用sncg注射的所有眼中荧光更高(图5a)。眼在注射后8周剜出,并且与cmv相比,使用sncg启动子时视网膜平放固定物证实了更高强度的荧光(图5b)。通过使用brn3a进行共标记来调查表达的定位,我们评估了rgc中基因表达的强度和效能(图5c)。brn3a特异性表达在rgc中,并且针对这种转录因子的抗体被认为是鉴定和定量鼠类rgc的可靠标志物(quina等,j.neurosci.2005;25(50):11595–11604)。来自于sncg-catch-gfp视网膜的视网膜平放固定物(图5d)和横截面(图5e)的共聚焦显微术图像显示出rgc中强烈的gfp表达,并且这种表达与bnr3a标记高度共定位。在这些图像的细胞定量中,我们显示在用sncg或cmv启动子转染的视网膜上,brn3a抗体标记等量的rgc。在sncg视网膜中,57%的这些brn3a阳性rgc也表达gfp,而在cmv视网膜中,这个比例降低到21%(图5c)。sncg与cmv视网膜之间的差异是统计学显著的。表达gfp的brn3a阳性rgc的这种更大比例证实了sncg启动子(seqidno:1)在rgc中驱动高水平基因表达的更高效能。catch在rd1视网膜的rgc中、在seqidno:1的sncg启动子之下表达后的视网膜和皮层响应为了证实hcatch-gfp的选择性rgc靶向可以在失明的rd1视网膜(年龄>12周)中恢复视觉功能,我们使用多电极阵列(mea)记录了来自于视网膜神经节细胞的动作电位活动。将小鼠在出生后4-8周用3剂在cmv或sncg(seqidno:1)启动子下编码hcatch-gfp的aav2注射,并在注射后8-12周进行mea记录(图6a-e)。光遗传学响应的光敏感度作为在1014至1017个光子/cm2/s范围内的光条件下252个电极的阵列上的读数来测量。当用2秒的全视野闪光刺激处理过的rd1视网膜时观察到光诱发的动作电位活动(图6a-e),而对照rd1视网膜没有显示出对光做出响应的动作电位活动的任何增加(数据未示出)。对光响应的细胞的百分数依赖于病毒剂量(图6a-b)。在1014个光子/cm2/s下,在用sncg启动子以最高aav剂量注射的rd1动物中,更大数量的细胞产生响应(图6a)。这种提高的灵敏度证实了sncg启动子(seqidno:1)在rgc中驱动更高水平的catch表达,因此更高百分率的细胞对相同的病毒载量变得光响应。放电率频率是强度依赖性的,对于在每只眼5x109vg的病毒剂量下在sncg启动子下表达的catch来说,在1014个光子/cm2/s下产生稳健的光响应(图6a)。归一化的放电率随着光强度升高而增加(图6c-d)。注意使用cmv启动子时只有最高的病毒剂量才在1014个光子/cm2/s下产生对光的响应(图6a)。此外,在这些条件下,非常少的细胞对光响应。即使在最高的光强度下,在中等病毒剂量(每只眼5x108vg)下响应的细胞也较少(图6b)。这个实验证实了sncg启动子(seqidno:1)在rgc中驱动功能性蛋白的表达的效能更高。为了证实这种rgc活化被传递到大脑,我们在体内在视网膜刺激后记录了皮层水平的光响应。为了进行这个实验,将另一系列rd1小鼠用aav2-sncg-hcatch-gfp注射,并且我们使用它们来记录对增加的光强度做出响应,视觉皮层中的动作电位活动和局部场电位(vep)。rgc响应在视觉皮层中转变为高度光敏感性的活动(图6f-j)。将处理过的眼(记录半球的对侧)用以1hz重复200次的200ms的蓝光脉冲(光强度高达1.71017个光子/cm2/s)进行刺激(图6f-h)。在来自于未处理rd1小鼠的记录上没有观察到vep(平坦迹线)。当与在野生型小鼠上测量的vep相比时,catch驱动的vep具有较慢的潜伏期(图6i)。由于绕过了光转导级联和随后的视网膜计算,预期潜伏期较短。图6f-h和j说明了动作电位响应的强度依赖性,其中在较高光强度下渐进性出现较短潜伏期的主峰。在catch处理的rd1小鼠中动作电位的潜伏期(10.1+/-2ms,n=3)再次短于野生型小鼠中的平均on潜伏期(52.98+/-3.83ms,n=3)。这些响应与光刺激的持续时间严格相关,并且是catch引发的rgc活化的结果。这些功能结果清楚地证实,在sncg启动子下aav驱动的catch表达可以在失明小鼠视网膜中激活rgc以恢复光敏感性,并且这些细胞将光信号传递到大脑直至视觉皮层。在nhp眼中的体内炎性响应在小鼠研究中,我们使用5x107至5x109vg/眼范围内的剂量。我们观察到,使用在人类中最小化光毒性所需的低的光强度(1014-1015个光子/cm2/s的范围),在mea上获得光响应所必需的粒子数目在5x108至5x109vg/眼的范围内。由于恒河猴玻璃体的体积比小鼠的玻璃体体积约大100倍,因此我们决定在我们的非人类灵长动物实验中使用这个剂量范围的药理学当量。基于在血清中不存在针对aav2的中和抗体滴度,选择了5只非人类灵长动物(kotterman等,genether.2015feb;22(2):116-26)。将这些成年恒河猴中的4只用在sncg启动子下编码hcatch的aav2的1x1011(n=4只眼)或5x1011个粒子(n=4只眼)进行玻璃体内注射(表1)。表1:非人类灵长动物中的注射:动物编号,aav载体和玻璃体内注射的病毒剂量由于gfp可以是免疫原性的,为了区分对gfp和hcatch的可能的炎性响应,我们使用没有荧光标签的hcatch。然而,将1只灵长动物用同样的两种剂量进行注射(一只眼用低剂量,另一只眼用高剂量),但这次编码与gfp融合的hcatch以监测体内基因表达(nhp1)。玻璃体保持足够透明,使得如玻璃体浑浊的分级方案中所定义的炎症的严重性几乎没有发展(图7下图)。在低剂量组中,在注射后1和3个月时,只在1只眼中检测到眼底可视化的轻微损伤;并且在高剂量组中,在注射后2-3个月时,在所有眼中检测到眼底可视化的轻微损伤(图7下图)。通过后葡萄膜炎分级进行的评估(图7–上图)显示,在所有研究组中,从注射后第一个月开始,在玻璃体中持久地存在细胞(图7–上图)。在注射后5-6个月时,玻璃体中的大多数细胞似乎是衰老的。对中等和高剂量组进行玻璃体中细胞的定量和分析,显示出炎性反应性的两波曲线(图7)。两个组的所有眼揭示出在注射后第一个月的时间点处第一波玻璃体的炎性响应,并且在两种病毒构造(sncg-catch和cmv-catch)的高剂量组中以及cmv-catch构建的中等剂量组中,玻璃体细胞炎性反应的水平较高。在注射后3-4个月的时间点处,在第二波玻璃体细胞炎性反应中注意到相同的情况但水平较低。使用裂隙灯和间接检眼镜进行的眼底检查揭示出视网膜、视网膜血管、视盘和脉络膜没有炎性迹象。上述的炎性迹象很好地反映出眼对基因疗法的天然免疫反应。这个充分且详细的分析的目的是为了理解对基因疗法的炎性响应的动力学。在整个5-6个月的观察期中观察到的炎性反应事件都对视觉没有显著影响。来自于高剂量组的一只眼的组织病理学检查显示出没有炎性细胞在注射后3个月时来自于高剂量组的我们所分析的唯一一只眼中,没有观察到组织学病患。将整只眼固定,切片,并使用允许切片内任何地方40x分辨率的nanozoomer技术来观察(图8)。没有注意到指示炎症的结构变化(小梁网状结构和虹膜-角膜角中淋巴细胞或浆细胞、玻璃体中炎性细胞或视网膜中血管周淋巴细胞的存在)(图8b-f)。重要的是,来自于5×1011vg剂量组的这只动物(nhp3)在注射后1-2个月时在间接检眼镜检查后表现出可变水平的玻璃体混浊和细胞(图7)。在3个月时不存在炎性细胞和视网膜损伤,表明任何先前的前房闪辉或玻璃体混浊不引起视网膜结构的永久性变化,并且总体来说眼的视网膜和前段没有任何损伤或炎症的迹象。因此,在sncg启动子(seqidno:1)控制之下的光基因表达似乎不引起炎性反应。在nhp的窝周区中表达catch的rgc的比例然后,在mea记录后,将视网膜平放固定物用针对通道视紫红质(busskamp等,science2010;3(june):413–7)、brn3a和gfp(当存在时)的抗体染色。来自于nhp1的组织被抗gfp抗体标记成绿色,并被抗brn3a抗体标记成红色(图9b)。这是我们可以在其中与指示catch的定位的抗体相结合使用rgc特异性标志物brn3a的唯一视网膜,因为brn3a和抗通道视紫红质抗体两者在同一物种中产生。在这个从窝的中心跨越~1mm2的组织中,我们在窝周围半径为600μm的半个圆中对brn3a(+)和catch-gfp(+)细胞进行计数(图9b)。在这个区域中,37%左右的brn3a(+)细胞也对gfp阳性(对于1413个brn3a阳性细胞来说个523gfp阳性细胞)。在来自于nhp2的组织中,我们在从窝中心跨越600μm的区域中,对眼的一半计数到1351个catch阳性细胞,在对侧眼中为455个(图9c)。来自于高剂量组的视网膜之一在mea记录过程后受损,并且不能用于免疫荧光标记。这些结果表明,在用5x1011vg注射后,至少四分之一的窝周rgc被catch标记。单细胞膜片钳记录揭示了在窝周围的各个rgc中catch驱动的光电流将用aav2-sncg-hcatch-gfp注射的nhp1在注射后3个月处死。将视网膜剖下,并将窝区小心地切成两半,用于mea和膜片钳记录,因为归因于gfp的绿色荧光在这个区域中最大(图9a)。这种表达模式与先前的nhp研究相一致(dalkara等,scitranslmed.2013jun12;5(189):189ra76;yin等,investophthalmolvissci.2011apr25;52(5):2775-83)。在所有我们的实验中,nhp视网膜中的内源光响应使用槽溶液中浓度为50μm的代谢型谷氨酸受体激动剂l-(+)-2-氨基-4-膦酰基丁酸(l-ap4)来阻断。我们以前确认了在小鼠(nagel等,proc.natl.acad.sci.u.s.a.2003;100(24):13940–5)和人类视网膜(tomita等,molther.2014aug;22(8):1434-40)两者中,l-ap4阻断野生型视网膜中的所有on响应。在单细胞水平上,膜片钳记录证实了在来自于aav2-sncg-hcatch和aav2-sncg-hcatch-gfp两种条件的rgc中(分别为n=2和n=3个细胞),在470nm下在1.461016个光子/cm2/s下的光响应(图10)。aav2-sncg-hcatchrgc必须在没有荧光标记物帮助的情况下夹上膜片。所有响应性细胞存在于窝中心周围的圆盘(500-600μm)中(图10a)。在某些情况下,在细胞附着构型中记录到的细胞表现出快速且稳健的动作电位模式(图10b)。我们在利多卡因存在下,在全细胞构型下,在-60mv的保持电位下,观察到典型的通道视紫红质诱发的光电流,其由快速的瞬变电流和随后的稳态电流构成(图10c)。所述光电流在450nm下刺激后出现峰值,直至500nm仍保持显著(图10d),并且它们快得足以追随22hz光脉冲(图10e)。当用双光子激光扫描时,catch-gfp神经节细胞在窝周区中显示出浓密的膜结合的gfp标记(图10f-g)。将用aav2-cmv-hcatch或aav2-sncg-hcatch以5x1011或1x1012vg/剂注射的猴在注射后6个月处死。使用单细胞记录技术(细胞附着和膜片钳记录),我们能够从所有组记录光响应(光电流和动作电位活动),如图10h上使用在低剂量下用sncg组获得的实施例所示。来自于在注射后6个月时在nhp视网膜中表达catch的rgc的单细胞记录(细胞附着和膜片钳)然后,我们根据响应性细胞的比例(图11a-c)和最大放电频率(图11d)或光电流(图11e,只使用最高剂量)随光强度的变化比较了所述4组。我们发现,对于两种病毒剂量来说,从注射有aav2-sncg-hcatch的动物记录的窝周细胞与从注射有aav2-cmv-hcatch的动物记录的细胞相比,具有高得多的是光响应性的可能性。我们的结果还表明,sncg响应性细胞组(在两种剂量下)与使用cmv启动子的组相比,具有更高光敏感性(更快的放电活动)。通过nhp视网膜的多电极阵列(mea)记录测量的来自于表达catch的rgc的功能性响应为了确定这些光电流如何在群体水平上控制rgc活动,用多电极阵列(mea)技术记录视网膜平放固定物。图12b示出了来自于nhp1左眼(高剂量)的单一单元记录的光栅图。光响应与在视网膜平放固定物上看到的窝周gfp表达模式相关(图12a-d)。从注射有低5倍的剂量的对侧眼,没有获得响应。接下来,我们处死了其他用高剂量的无gfp标签的aav2-hcatch注射的动物。来自于高剂量组的所有4个视网膜在l-ap4阻断下都显示出相似的光响应,其中多达90%的记录的rgc对光做出响应(图12a)。类似地,光响应性细胞的分布总是以窝区为中心,即使是使用aav2-sncg-hcatch载体时。这些结果表明,对于在rgc中获得功能性catch表达,并不需要gfp标签。计算放电频率的光谱调谐,并对480nm的光显示出最高频率响应,所述光对应于chr2的激发峰。响应性细胞的放电率频率是强度依赖性的,在以1017个光子/cm2/s施加的最大光强度下达到最大值(图12d)。在低剂量组中,5个记录的视网膜中只有2个显示出光遗传学光响应,并且在这些视网膜中记录的rgc的少于10%对光做出响应。其他视网膜显示出自发的rgc活动,但在l-ap4下没有光响应。这些结果表明1011个粒子处在我们可以通过catch的表达预期rgc的可靠光遗传学激活的阈值处。在注射后6个月时,rgc中catch的表达与3个月时的响应相当。在所有试验的视网膜中观察到catch介导的光响应。在1.1014至1.1017个光子.cm-2.s-1范围内的强度下,与用aav2-cmv-hcatch感染的视网膜相比,在用aav2-sncg-hcatch载体感染的组织中光响应期间的放电频率更高(图12e)。在sncg视网膜中,引发光响应的阈值更低(分别为6.1014和8.1015个光子.cm-2.s-1)。在sncg组织中,在所有强度下放电频率也与病毒粒子的剂量相关,具有较高病毒剂量的组织显示出最强的响应。这些结果合在一起表明,与cmv启动子相比,sncg启动子在恒河猴视网膜神经节细胞中在驱动catch表达上更加高效,允许在更暗淡的光水平下更强的光响应。在注射后6个月时,rgc中catch的表达与3个月时的响应相当。在所有试验的视网膜中观察到catch介导的光响应。在1.10e14至1.10e17个光子.cm-2.s-1范围内的强度下,与用aav2-cmv-hcatch感染的视网膜相比,在用aav2-sncg-hcatch载体感染的组织中光响应期间的放电频率更高。在sncg视网膜中,引发光响应的阈值更低(分别为6.10e14和8.10e15个光子.cm-2.s-1)。在sncg组织中,在所有强度下放电频率也与病毒粒子的剂量相关,具有较高病毒剂量的组织显示出最强的响应。这些结果合在一起表明,在恒河猴视网膜神经节细胞中,sncg启动子在驱动catch表达上更加高效。实施例7使用seqidno:1的启动子序列在灵长动物视网膜中的强的、rgc特异性表达这种载体由被优化用于视网膜转导的aav衣壳变体aav2-7m8构成(dalkara等,scitransmed,2013jun12;5(189):189ra76),其将在sncg启动子(seqidno:1)控制之下的chrimsonr-tdtomato的编码序列(klapoetke等,natmethods,2014mar;11(3):338-46)衣壳化。在血清中不存在针对aav2的中和抗体滴度的基础上选择4只非人类灵长动物(kotterman等,genether.2015feb;22(2):116-26)。将这些成年恒河猴中的4只用5x1011个在sncg启动子下编码chrimsonr-tdtomato的aav2-7m8粒子玻璃体内注射(表2)。表2:在非人类灵长动物中的注射:动物编号,aav载体和玻璃体内注射的病毒剂量非人类灵长动物#aav载体剂量(vg/眼)nhp1–右眼aav2-7m8-sncg-chrimsonr-tdtomato5x1011–左眼aav2-7m8-sncg-chrimsonr-tdtomato5x1011nhp2–右眼aav2-7m8-sncg-chrimsonr-tdtomato5x1011–左眼aav2-7m8-sncg-chrimsonr-tdtomato5x1011nhp3–右眼aav2-7m8-cag-chrimsonr-tdtomato5x1011–左眼aav2-7m8-cag-chrimsonr-tdtomato5x1011nhp4–右眼aav2-7m8-cag-chrimsonr-tdtomato5x1011–左眼aav2-7m8-cag-chrimsonr-tdtomato5x1011使用眼底荧光对nhp跟踪2个月。荧光眼底图像显示,相对于用cag启动子注射的眼来说,在所有用sncg启动子注射的眼中荧光更高(图13和14)。在nhp2的右眼以及其他眼中,可以清楚地看到chrimsonr-tdtomato表达远远扩展到外周中。通过nhp视网膜的多电极阵列(mea)测量的来自于表达chrimsonr的rgc的功能性响应为了证实在灵长动物中chrimsonr-tdtomato的选择性rgc靶向可以恢复视觉功能,我们使用多电极阵列(mea)记录了来自于视网膜神经节细胞的动作电位活动。mea记录在注射后6个月进行(图15)。颜色编码的响应图使用mcrack软件来产生,并代表了在不同记录电极处的活动。频率基于在包括10msec全视野闪光(在600+/-20nm处2x1017个光子.cm2.sec-1)的300ms时间窗中存在的动作电位的数目来计算。动作电位在进行200hz高通二阶巴特沃斯滤波后检测,并且得到的滤波信号以20μv为阈值。同样的参数用于所有不同视网膜片中的所有电极。在mea记录网格上的chrimsonr-tdtomato荧光的图像证实,与使用非特异性cag启动子相比,在sncg启动子(seqidno:1)下在更大区域中获得chrimsonr表达。此外,与cmv启动子相比,对于sncg启动子(seqidno:1)来说也在更宽的区域中记录到rgc中的动作电位活动。这个实验为与使用cag启动子相比,使用sncg启动子时更大视野的光遗传学激活,提供了证据。在单细胞电生理实验之前,对所有恒河猴视网膜进行成像。将一半的窝片置于显微镜的记录室中,使神经节细胞面朝上,在实验的持续时间内在36℃下在充氧(95%o2/5%co2)的ames培养基(sigma-aldrich)中。对于落射荧光或活体双光子成像(图16)来说,td-tomato荧光的获取分别使用td-tomato滤光片和ccd相机(hamamatsucorp.,bridgewater,nj)或使用波长为1030nm的双光子激光激发来进行。使用放大倍数为5x和40x的物镜。这些荧光观察进一步证实与在cag启动子下相比,在sncg启动子下chrimsonr-tdtomato的表达更宽,它们甚至显示,使用sncg启动子可以获得在窝周环外部的表达,正如由荧光斑点所指示的(图15b)。最后,在双光子显微术下,使用sncg启动子时chrimsonr-tdtomato的位置似乎被限制到细胞质膜(图15d-右)。序列表<110>巴黎第六大学法国国家卫生及研究医学协会法国国家科学研究中心<120>启动子及其用途<130>b2149pc<160>3<170>patentinversion3.5<210>1<211>953<212>dna<213>智人(homosapiens)<400>1cacccacaagccagttcctgtccctgaggacttggctcagggactctgggaatgtggtag60acatggggtggccccaccaaatgcatccttatgggaacctgctccctgggagccatgaaa120agagcgtggacttcgaggtggggccacaggaagtggtcaggtccatctcaggggacctgc180tgcccatccacactgctggccaggaaatggggggcaattcatgcctcctcagcaccttca240gcactgggcggctcaaagaaggcaagggactattctggggtcacacagcatgcagccaga300ggccaaggcatgaggaagtccttcatttccccacccccacccacctcagatcctccaacc360ggtttcatggcagcccagggtccagcggcatccaggatgctggtgggtagctgcacagcc420caggccgcgggaggttggctgctctcacctaacaggcctatgtggccctgacccctacct480aggaagctggggacaatggccaaggcgcctcccctctctgtgcctgtctgtccaggtgca540gcatagacacagcacccctggggccaagagcacccagccagggctgcccccatgggtggg600cagggcagtaaatgaatgagggacaggttgggaggtggccagccccctccagcccatgga660gggcacggggcaggagagctgggctgagccagcaggagcccagggagcctggtctctgcc720ttcctatcctggaggaaggtgaggctgaacctccttccctccctccctccctccccgccc780ccactgcacgcagggctggctgggctccagctggcctccgcatcaatatttcatcggcgt840caataggaggcatcggggacagccgctgcggcagcactcgagccagctcaagcccgcagc900tcgcagggagatccagctccgtcctgcctgcagcagcacaaccctgcacaccc953<210>2<211>19<212>dna<213>人工序列<220><223>用于sncg启动子扩增的正向引物<400>2cacaagccagttcctgtcc19<210>3<211>17<212>dna<213>人工序列<220><223>用于sncg启动子扩增的反向引物<400>3gggtgtgcagggttgtg17当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种基于转录组测序构建的棒状杆菌组成型表达载体启动子的制造方法与工艺
- 一种棒状杆菌组成型表达载体启动子、含有该启动子及gnd基因的表达载体的制造方法与工艺
- 一种棒状杆菌组成型表达载体启动子、含有该启动子及lrp基因的表达载体的制造方法与工艺
- 一株呕吐毒素降解菌及其应用的制造方法与工艺
- 一种具有家蚕血细胞特异性活性的启动子的鉴定方法与流程
- 一种改造的质粒复制子及其应用的制造方法与工艺
- 一种水稻种子特异性启动子Posseed及其应用的制造方法与工艺
- 一种在水稻幼穗特异表达的启动子及其应用的制造方法与工艺
- 一种表达外源基因的启动子及其应用的制造方法与工艺
- 可诱导的CRISPRon或CRISPRi小鼠胚胎干细胞及其应用的制造方法与工艺