多位点组合修饰的内吗啡肽类似物及其合成和应用的制作方法
本发明属于生物医药领域,涉及一类使用多位点组合修饰的内吗啡肽(包括内吗啡肽-1和内吗啡肽-2)类似物及其合成方法,尤其涉及一种酪氨酸或2,6-二甲基酪氨酸,n-甲基-d型丙氨酸和非天然α-烯基-β-氨基酸共同修饰的内吗啡肽类似物及其合成方法,本发明同时还涉及该内吗啡肽类似物在制备镇痛药物中的应用。
背景技术:
随着现代社会人们生活、工作压力的不断增大和老年社会的到来,疼痛遍及范围不断扩大,如何对其进行药物治疗已成为重大的公共卫生课题。阿片类药物用于疼痛的治疗已经有数千年的历史,其主要通过与大量分布于中枢神经系统的μ,δ和κ三种经典阿片受体相互结合而发挥生理作用,时至今日仍然在临床中广泛应用,但传统的阿片药物(如吗啡)在长期使用后会产生耐受、依赖、呼吸抑制以及影响胃肠运动等副作用,严重限制了其临床应用。
内吗啡肽是人体内广泛存在的一类内源性阿片类多肽物质,包括内吗啡肽-1(tyr-pro-trp-phe-nh2,em-1)和内吗啡肽-2(tyr-pro-phe-phe-nh2,em-2),其可通过与μ阿片受体结合,参与包括痛觉、呼吸、心血管、胃肠、内分泌、行为等诸多功能的调节,但其主要作用体现在镇痛方面(nature.1997,386,499),且不会诱发耐受、呼吸抑制和血压下降等常见的副作用,被认为是一种有极大应用潜力的镇痛候选药。然而,由于人体内同时存在大量的蛋白水解酶,内吗啡肽在人体内会被迅速降解,大大缩短了药物作用的半衰期。鉴于此,大量化学修饰的方法被应用于阿片肽的改造优化中,以期能提高它们的生物利用度,从而发挥更好的镇痛作用。另外,非天然氨基酸砌块在研究多肽药物构效关系方面有非常重要的作用,通过引入非天然氨基酸代替原有的天然结构,修饰关键酶切位点,能够有助于延长药物作用时间,提高生物利用度。近年来大量研究显示,多肽药物通过多位点修饰后能够对其结构和生理活性产生显著影响(expertopin.ther.patents2012,22,1;medicinalresearchreviews,2012,32,536)。因此,通过化学组合修饰内吗啡肽提高其作用效果和作用时间,以获得一系列神经肽受体的高效配体成为近年来镇痛药物研究的方向。
申请号为201210426909.4的中国发明专利公开了一种多位点修饰的内吗啡肽-1类似物,其是将内吗啡肽-1的第1位氨基酸由酪氨酸或2,6-二甲基酪氨酸替代,第2位氨基酸由脯氨酸或(s/r)β-脯氨酸替代,第4位氨基酸分别由苯基或2-呋喃基取代的α-烯基-β-氨基酸替代得到。但内吗啡肽第2位的脯氨酸是主要的酶切位点,该内吗啡肽-1类似物制备成镇痛药物依然存在作用时间短的问题,且从工业生产角度而言,(s/r)β-脯氨酸价格昂贵,生产成本较高。基于此,申请号为20111089179.9的中国发明专利“内吗啡肽-1类似物及其合成和在制备镇痛药物中的应用”提供了一种内吗啡肽-1第2位氨基酸由d-型丙氨酸替代的内吗啡肽-1类似物,可显著延长药物作用时间,但其μ阿片受体的亲和力较弱,镇痛作用不够显著。
技术实现要素:
本发明的目的是提供一类多位点组合修饰的内吗啡肽(em-1和em-2)类似物。
本发明的另一目的是提供一种多位点组合修饰内吗啡肽类似物的合成方法。
本发明还有一个目的,就是提供一种上述多位点组合修饰的内吗啡肽类似物在制备镇痛药物中的应用。
本发明的目的是通过以下技术方案实现的:
一、多位点组合修饰的内吗啡肽类似物
1、多位点修饰内吗啡肽类似物的结构
本发明多位点组合修饰的内吗啡肽类似物,是针对内吗啡肽的第1、2、4位氨基酸进行的组合改造,即内吗啡肽的第1位氨基酸由酪氨酸或2,6-二甲基酪氨酸替代,第2位氨基酸由n-甲基-d型丙氨酸替代,第4位氨基酸分别由苯基或2-呋喃基取代的α-烯基-β-氨基酸替代。
其结构通式为下列之一:
其中,r1为h或甲基;r2为苯基或2-呋喃基,标记为mel-n16系列,包括以下8中化合物:
第1位氨基酸为酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为色氨酸,第4位r为苯基的化合物,标记为mel-n1601;
第1位氨基酸为酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为色氨酸,第4位r为2-呋喃基的化合物,标记为mel-n1602;
第1位氨基酸为酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为苯丙氨酸,第4位r为苯基的化合物,标记为mel-n1603;
第1位氨基酸为酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为苯丙氨酸,第4位r为2-呋喃基的化合物,标记为mel-n1604;
第1位氨基酸为2,6-二甲基酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为色氨酸,第4位r为苯基的化合物,标记为mel-n1605;
第1位氨基酸为2,6-二甲基酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为色氨酸,第4位r为2-呋喃基的化合物,标记为mel-n1606;
第1位氨基酸为2,6-二甲基酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为苯丙氨酸,第4位r为苯基的化合物,标记为mel-n1607;
第1位氨基酸为2,6-二甲基酪氨酸,第2位为n-甲基-d型丙氨酸,第3位为苯丙氨酸,第4位r为2-呋喃基的化合物,标记为mel-n1608。
2、多位点组合修饰的内吗啡肽类似物mel-n16系列的合成
本发明多位点修饰的内吗啡肽类似物mel-n16系列的合成方法,包括以下步骤:
(1)n-叔丁氧羰基-α-烯基-β-氨基酸酰胺的合成
将n-叔丁氧羰基-α-烯基-β-氨基酸溶于无水处理的二氯甲烷,于0-5℃下依次加入n-叔丁氧羰基-α-烯基-β-氨基酸摩尔量4.5-5倍量的n,n-二异丙基乙基胺,1.6-1.8倍量的1-羟基苯并三唑,1.6-1.8倍量的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌使其充分溶解后加入n-叔丁氧羰基-α-烯基-β-氨基酸摩尔量1.6-1.8倍的氨水,室温反应16-18h后洗涤,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-α-烯基-β-氨基酸酰胺;
(2)α-烯基-β-氨基酸酰胺三氟乙酸盐的合成
将化合物n-叔丁氧羰基-α-烯基-β-氨基酸酰胺溶于三氟乙酸和二氯甲烷的混合溶液中,室温反应2.5-3h后,减压蒸馏,得到白色固体产物α-烯基-β-氨基酸酰胺三氟乙酸盐;
(3)n-叔丁氧羰基-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺的合成
将n-叔丁氧羰基-色氨酸/苯丙氨酸溶于无水处理的二氯甲烷,于0-5℃下依次加入n-叔丁氧羰基-色氨酸/苯丙氨酸摩尔量4.5-5倍量的n,n-二异丙基乙基胺,1.6-1.8倍量的1-羟基苯并三唑,1.6-1.8倍量的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌使其充分溶解后加入α-烯基-β-氨基酸酰胺三氟乙酸盐的二氯甲烷溶液,室温反应16-18h后洗涤,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺;所述α-烯基-β-氨基酸酰胺的摩尔量为n-叔丁氧羰基-色氨酸/苯丙氨酸的1.6-1.8倍;
(4)n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸的合成
将n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸溶于无水二氯甲烷,0-5℃搅拌下依次加入n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸摩尔量4.5-5倍量的n,n-二异丙基乙基胺,1.6-1.8倍量的1-羟基苯并三唑,1.6-1.8倍量的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16-18h后洗涤,无水硫酸钠干燥,减压蒸馏,得到油状液体产物n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸;所述n甲基d型丙氨酸的摩尔量为n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸的1.6-1.8倍;
(5)色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺三氟乙酸盐的合成
将n-叔丁氧羰基-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺溶于三氟乙酸和二氯甲烷的混合溶液中,室温反应2.5-3h后,减压蒸馏,得到白色固体产物色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺三氟乙酸盐;
(6)n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺的合成
将n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0-5℃下依次加入n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸摩尔量4.5-5倍量的n,n-二异丙基乙基胺,1.6-1.8倍量的1-羟基苯并三唑,1.6-1.8倍量的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺三氟乙酸盐的二氯甲烷溶液,室温反应18-20h后洗涤,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺;所述色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺三氟乙酸盐的摩尔量为n-叔丁氧羰基-酪氨酸或2,6-二甲基酪氨酸-n甲基d型丙氨酸的1.6-1.8倍;
(7)酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺的合成
将n-叔丁氧羰基-酪氨酸/2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺溶于乙酸乙酯和盐酸的混合溶液中,室温反应4-5h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得到白色固体产物酪氨酸或2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸/苯丙氨酸-α-烯基-β-氨基酸酰胺。
其中,上述步骤(2)和步骤(5)中三氟乙酸和二氯甲烷的混合体积比为1-1.2:1,以达到产率高,副产物少的目的。
步骤(7)中乙酸乙酯和盐酸的混合体积比为4-4.5:1,反应产率高,产物容易浓缩、方便后续处理。
α-烯基-β-氨基酸为3-氨基-2-甲烯基-3苯基丙酸或3-氨基-2-甲烯基-3-(2-呋喃)丙酸,引入该氨基酸有助于提高内吗啡肽类似物mel-n16系列的血脑屏障通透性,间接延长药物作用时间,提高其生物利用度。
本发明多位点组合修饰的内吗啡肽类似物mel-n16系列的esi-ms测试(图3-图10)结果表明,上述方法成功合成了8种内吗啡肽类似物。em1和em2及其类似物的理化特征见表1。
表1.em1和em2及其类似物的理化特征
二、多位点组合修饰的内吗啡肽类似物mel-n16系列的药理活性实验
内吗啡肽在体内容易被多种多肽酶降解,其中第2位的脯氨酸是主要的酶切位点,因此要延长药物的作用时间主要针对该酶切位点进行修饰。本发明第2位氨基酸由结构与脯氨酸近似的非环状氨基酸n-甲基-d-丙氨酸替代,可以显著延长药物作用时间,相比与单纯的d-丙氨酸替代可进一步提升阿片受体亲和力,结合第1位和第2位氨基酸分别由酪氨酸或2,6-二甲基酪氨酸和α-烯基-β-氨基酸的组合修饰,产生了更好的镇痛作用。
本发明合成的多位点组合修饰的内吗啡肽类似物mel-n16系列,具备良好的药理学活性和潜在的药用价值。现通过通过放射配体受体结合实验,离体器官生物检定,离体酶解稳定性和温浴甩尾镇痛实验对其药理学活性进行鉴定。
1放射配体受体结合实验
1.1稳定表达细胞株的筛选和培养
本实验细胞采用hek293(人胚胎肾细胞),用含有10%胎牛血清的dmem培养液培养,并放于co2培养箱中促进其生长;设计引物pcdna3.1(+)-flag-mor和pcdna3.1(+)-ha-dor构建含有目的基因的真核表达质粒,然后将该真核表达质粒用转染试剂转入hek293细胞中,48h后将细胞无限稀释并用抗生素g418进行筛选,3周后对存活细胞进行基因组、rna、蛋白、功能方面的一系列鉴定,筛选出稳定表达μ/δ阿片受体的细胞株。筛选出的稳定细胞株加入800ug/ml的g418隔天培养后,将细胞用pbs缓冲液吹下,离心后用适量亲和缓冲液(25mmhepes,5mmmgcl2,1mmcacl2,2.5mmedta,0.4%bsa,盐酸调ph=7.4)重悬备用。
1.2受体结合实验
实验分为总结合管、竞争结合管和非特异性结合管,每个反应管中依次加入放射配体,纳洛酮(naloxone,nx)/非放射性药物,tris-hcl(ph=7.4)和细胞悬液(200μl)。其中,在总结合管中只加入[3h]damgo(0.5nm)和细胞悬液(200μl),在非特异性结合管和竞争结合管中分别另加入10μmnx/不同浓度的类似物和细胞悬液,最后补充tris-hcl缓冲液(ph=7.4)至总体积0.4ml。振荡混匀反应液,37℃摇床反应1h后经zt-ii型细胞收集器收集,gf/c型玻璃纤维素膜过滤。80℃油浴下烘烤玻璃纤维素膜30min后取出滤膜,放入24孔板中,每孔加入0.7ml闪烁液,封盖膜封盖。隔夜用β液体闪烁计数仪记录放射性强度(cpm)。计算类似物对特异性结合的抑制率,以浓度的负对数为横坐标,抑制率为纵坐标,线性回归求得ic50值,根据公式ki=ic50/(1+[l]/kd)计算ki值。每个实验数据分别未3组平行实验的平均值。
1.3实验结果
实验结果见表2。表2中实验数据显示,内吗啡肽类似物mel-n16系列中,第1位氨基酸为酪氨酸的mel-n1601至mel-n1604,其μ阿片受体的亲和力高于母体约5-10倍,δ阿片受体的亲和力略高于母体,而第1位氨基酸为酪氨酸2,6-二甲基酪氨酸的mel-n1605至mel-n1608,其μ阿片受体和δ阿片受体的亲和力均明显高于母体。
表2.内吗啡肽及其类似物的μ/δ阿片受体亲和能力
2.离体生物活性功能检定
2.1豚鼠离体回肠纵行肌实验(gpi实验)
体重250-300g豚鼠,雌雄不限,实验前禁食12h,饮水不限。棒击枕部处死,剖腹取出近盲肠端的回肠6厘米两段,浸入持续通入95%o2和5%co2混合气的kreb’s液(g/l:氯化钠6.9,cac120.28,kcl0.35,kh2po40.16,mgso4·7h2o0.30,碳酸氢钠2.1,葡萄糖1.98,苯海拉明50×10-6,氯化胆碱2.8×10-3)中,湿润后套在一根玻璃棒上,沿回肠壁的一根纵形血管将纵行肌与环形肌分离,然后用零号丝线将纵行肌的一端缚在玻璃电极的小钩上,另一端缚在jz-1型肌肉张力传感器上,制备好后立即放入恒温37±0.5℃玻璃浴管中盛有的持续通入气体(95%o2和5%co2)的kreb’s液,预负荷500mg。前30min每5min换一次营养液,以后每10min换液一次,平衡2h后开始实验。给予电刺激,刺激参数:波宽0.3-0.1ms的单方波,频率6次/min,负载电压80v。记录基础收缩强度,再给予适量内吗啡肽-1鉴定其活性,然后分别给予不同剂量的待试药物,记录收缩强度,计算抑制百分率。每次药物作用后,用营养液冲洗3次,平衡15min。根据公式:抑制百分率=(反应前收缩高度-反应后收缩高度)/反应前收缩高度×100%,用剂量-效应半对数作图法,以抑制百分率为纵坐标,以待测药物浓度的对数为横坐标作图,求得抑制50%收缩高度的药物浓度(ic50)。
2.2小鼠输精管实验(mvd实验)
体重30-35g雄性昆明系小白鼠,颈椎脱臼处死,剖腹取出两侧输精管,浸入持续通入95%o2和5%co2混合气的kreb’s液(g/l:氯化钠6.9,cac120.28,kcl0.35,kh2po40.16,mgso4·7h2o0.30,碳酸氢钠2.1,葡萄糖1.98),剥离附着于其上的脂肪及血管。剪去输精管的一端,用小棉花球轻轻从末端向开口端压出管内精液,然后用零号丝线将其一端缚在玻璃电极的小钩上,另一端缚在jz-1型肌肉张力传感器上,制备好后立即放入恒温37±0.5℃玻璃浴管中盛有的持续通入气体(95%o2和5%co2)的kreb’s液,预负荷l00mg。前30min每5min换一次营养液,以后每10min换液一次,平衡2h后开始实验。给予电刺激,刺激参数:波宽2ms,频率6次/min,负载电压80v。记录基础收缩强度,再给予适量内吗啡肽-1鉴定其活性,然后分别给予不同剂量的待试药物,记录收缩强度。每次药物作用后,用营养液冲洗5次,平衡15min。ic50测定方法同gpi实验。
2.3实验结果
上述实验结果见表3。表3中实验数据显示,gpi和mvd的实验结果与放射配体结合实验结果的趋势一致。内吗啡肽类似物mel-n16系列中,第1位氨基酸为酪氨酸的mel-n1601至mel-n1604,其生物活性为母体的1-3倍,而第1位氨基酸为2,6-二甲基酪氨酸的mel-n1605至mel-n1608,其生物活性均明显高于母体,gpi与mvd的ic50最小值分别为母体的1/37和1/16;使用δ阿片受体特异性拮抗剂naltrindole部分(39%-66%)拮抗这些类似物的mvd激动效应,提示这些多肽的高dor激动效应可能部分由共存于mvd上的mor介导。实验结果表明这些类似物在离体生物标本中对μ/δ阿片受体有强的激动活性,生物活性高。
表3.内吗啡肽及其类似物的离体生物活性
3.离体酶解稳定性实验
3.115%小鼠脑质膜标本制备
体重30-35g成年雄性小鼠,颈椎脱臼处死,取大脑(去除小脑及脑桥)用滤纸吸干后称重。用温度为4摄氏度的1mm的tris-hcl缓冲液(ph=7.4)冲洗除去溢血后,再加入50倍体积(v/w)的上述tris-hcl缓冲液,0℃下用匀浆器使之成胞浆匀浆后置于冰浴中放置30min促进细胞溶解。然后按每1ml匀浆液补加0.5ml50mm温度为4摄氏度的tris-hcl,再次匀浆,吹打悬浮。49,000g离心45min,弃上清,将沉淀重悬于50倍体积(v/w)的冰冷50mm的tris-hcl中,吹打悬浮。49,000g再次离心45min,弃上清,沉淀悬浮于50mmtris-hcl中,使脑膜蛋白浓度约为2.3mg/ml。振荡器震荡涡旋混匀,分装,-80℃冻存。
3.2脑质膜孵育试验
取10μl多肽母液(10-2m),加入到190μl脑质膜中,立即振荡混匀,然后迅速取出20μl混合液,加入离心管中并计时为0min,余者于37℃下继续孵育,并分别在5、10、15、30、60、120、240和480min取出20μl。取出的样品中加入90μl乙腈振荡混匀,置于冰上放置5min,再用90μl0.5%的温度为4摄氏度乙酸稀释以确保酶解过程停止。然后于4℃下13,000g离心15min,收集上清,-80℃冻存,直至rp-hplc分析。
3.3反相-高效液相色谱分析
运用rp-hplc分析各个时间点样品的离体稳定性。rp-hplc系统使用watersdelta600控制器、紫外监测器和watersdeltapakc18柱(3.9mm×150mm);检测波长280nm,流动相=乙腈含0.05%tfa(a)+水含0.05%tfa(b),流速0.8ml/min;采用梯度洗脱,a:b=10:90-90:10,洗脱时间30min。分别测定每个时间点样品的浓度,并根据药物代谢公式以每个时间点的药物浓度为纵坐标,时间为横坐标绘制药物浓度变化曲线,计算求得药物的半衰期。每个实验数据为3组平行实验的平均值。
3.4实验结果
实验结果见表4。表4中实验数据显示,所有化合物的小鼠脑质膜半衰期均明显长于母体,其中通过2,6-二甲基酪氨酸修饰的mel-n1605至mel-n1608,其酶解稳定性更加显著。实验结果表明这些化合物在离体生物组织中具有好的酶解稳定性,因此可以延长其对痛觉的调节作用。
表4.内吗啡肽及其类似物的离体大脑半衰期
4镇痛实验
4.1实验方法
采用小鼠温浴甩尾法。体重18-20g昆明系雄性小鼠,环境温度20℃,水浴温度50±0.5℃。给药前先测定小鼠的基础痛阈(controllatency,cl),将小鼠鼠尾的1/3-1/2浸入水浴,记录鼠尾从刚浸入水浴至发生收缩的时间。过于敏感(<2.5s)或迟钝的(>5s)小鼠弃去不用,浸入截止时间为10s以防小鼠烫伤。药物注射剂量:a.侧脑室注射(i.c.v.)4ul/只;b.尾静脉注射(i.v.)100ul/只。每只小鼠分别注射8种mel-n16系列化合物,检测给药后60min内的甩尾潜伏期(testlatency,tl),前30min每5min测一次,后30min每10min测一次,实验过程以0.9%生理盐水作为空白对照。结果以最大可能效应百分比(maximumpossibleeffect,mpe%)表示:mpe%=100×(tl-cl)/(10-cl)。
4.2实验结果
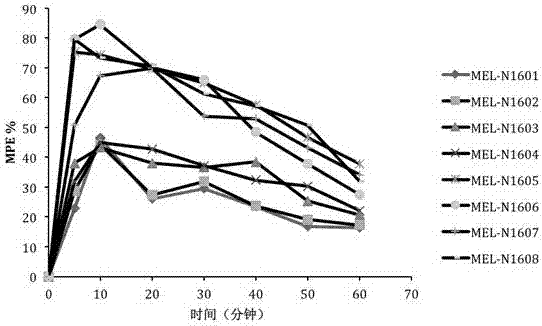
实验结果见图1和图2。图1为侧脑室注射20nmol/kg的mel-n16系列产生的镇痛时效曲线,结果显示,8种mel-n16系列化合物均产生强效的镇痛作用,镇痛效力和镇痛持续时间都明显增加,其最高镇痛能力达到68-95%,且第1位氨基酸为2,6-二甲基酪氨酸的mel-n1605至mel-n1608,其镇痛能力明显高于第1位氨基酸为酪氨酸的mel-n1601至mel-n1604;图2为尾静脉注射3mg/kg的mel-n16系列产生的镇痛时效曲线,8种mel-n16系列化合物均产生强效的镇痛作用,镇痛效力和镇痛持续时间都明显增加,其最高镇痛能力可达43-84%,且第1位氨基酸为2,6-二甲基酪氨酸的mel-n1605至mel-n1608,其镇痛能力同样明显高于第1位氨基酸为酪氨酸的mel-n1601至mel-n1604。实验结果表明本发明内啡肽类似物在体内能够发挥有效的镇痛作用。
综上,本发明多位点组合修饰的内吗啡肽类似物mel-n16系列较内吗啡肽母体具有更高的亲和力、高酶解稳定性和高镇痛活性,在制备镇痛药物方面具有很好的临床应用价值。
本发明相对现有技术具有以下有益效果:
1、本发明通过对两种内吗啡肽母体进行1、2、4位氨基酸的多位点以及非天然氨基酸2,6-二甲基酪氨酸、n甲基d型丙氨酸、α-烯基-β-氨基酸的组合修饰,合成出了具有更好μ阿片受体亲和力及酶解稳定性的内吗啡肽类似物mel-n16系列,该内吗啡肽类似物mel-n16系列体内镇痛效果好,且长期使用不会诱发耐受、呼吸抑制和血压下降等常见的副作用,可广泛用于镇痛药物的制备方面。
2、本发明内吗啡肽类似物mel-n16系列的合成采用hobt/edc活化酯法接肽,n端二肽和c端二肽可以同时合成,然后将两个合成好的片段对接,该方法大大简化了合成线路,减少了工作时间,产率≥93%、成本低廉,产物不易消旋、易纯化。
附图说明
图1为侧脑室注射内吗啡肽类似物mel-n16系列镇痛效应-时间曲线。
图2为尾静脉注射内吗啡肽类似物mel-n16系列镇痛效应-时间曲线。
图3为内吗啡肽类似物mel-n1601的esi-ms谱图。
图4为内吗啡肽类似物mel-n1602的esi-ms谱图。
图5为内吗啡肽类似物mel-n1603的esi-ms谱图
图6为内吗啡肽类似物mel-n1604的esi-ms谱图。
图7为内吗啡肽类似物mel-n1605的esi-ms谱图。
图8为内吗啡肽类似物mel-n1606的esi-ms谱图。
图9为内吗啡肽类似物mel-n1607的esi-ms谱图。
图10为内吗啡肽类似物mel-n1608的esi-ms谱图。
具体实施方式
下面通过附图和具体实施例对本发明多位点组合修饰的内吗啡肽类似物mel-n16系列的结构、合成及其理化特征作进一步详细说明。
实施例1mel-n1601的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.5mol的n,n-二异丙基乙基胺,1.6mol的1-羟基苯并三唑和1.6mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.6mol的氨水,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为为91%;
(2)3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-色氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.5mol的n,n-二异丙基乙基胺,1.6mol的1-羟基苯并三唑和1.6mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.6mol的3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为88%;
(4)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸的合成:将1moln-叔丁氧羰基-酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.5mol的n,n-二异丙基乙基胺,1.6mol的1-羟基苯并三唑和1.6mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.6mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸,产率为90%;
(5)色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.5mol的n,n-二异丙基乙基胺,1.6mol的1-羟基苯并三唑和1.6mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.6mol色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为80%;
(7)酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应4h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得到白色固体酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,标记为mel-n1601,其产率为97%。
mel-n1601的结构式为:
其理化特征见表1,esi-ms谱图见图3。
实施例2mel-n1602的制备
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.65mol的氨水,室温反应16h加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为89%;
(2)3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-色氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.65mol的3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为88%;
(4)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.65mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应12h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸,产率为90%;
(5)色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.65mol色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为82%;
(7)酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应2.5h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得白色固体产物酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,标记为mel-n1602,产率为95%。
mel-n1602的结构式为:
其理化特征见表1,esi-ms谱图见图4。
实施例3mel-n1603的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.65mol的氨水,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为91%;
(2)3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-苯丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.65mol的3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为82%;
(4)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.65mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸,产率为90%;
(5)苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.6mol的n,n-二异丙基乙基胺,1.65mol的1-羟基苯并三唑和1.65mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.65mol苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为77%;
(7)酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应4h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得到白色固体产物酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,标记为mel-n1603,其产率为96%。
mel-n1603的结构式为:
其理化特征见表1,esi-ms谱图见图5。
实施例4mel-n1604的制备
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.7mol的氨水,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为89%;
(2)3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-苯丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应16h,后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为87%;
(4)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸,产率为90%;
(5)苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.05l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应2.5h后,减压蒸馏,得到白色固体苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.7mol苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应18h,后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为81%;
(7)酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成
:将1mol的n-叔丁氧羰基-酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应4h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得到白色固体产物酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,标记为mel-n1604,其产率为96%。
mel-n1604的结构式为:
其理化特征见表1,esi-ms谱图见图6。
实施例5mel-n1605的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.7mol的氨水,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺;产率为91%;
(2)3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-色氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为88%;
(4)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16h,反应结束后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n-甲基-d型丙氨酸,产率为88%;
(5)色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得到白色固体产物色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.7mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.7mol色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应18h,反应结束后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得到白色固体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n-甲基-d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为81%;
(7)2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应3h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得白色固体2,6-二甲基酪氨酸-n-甲基-d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,标记为mel-n1605,其产率为96%。
mel-n1605的结构式为:
其理化特征见表1,esi-ms谱图见图7。
实施例6mel-n1606的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.8mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.7mol的氨水,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为92%;
(2)3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得到白色固体产物3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%。
(3)n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-色氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.8mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为86%;
(4)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.8mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.7mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸,产率为87%;
(5)色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应4h后,减压蒸馏,得白色固体产物色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.8mol的n,n-二异丙基乙基胺,1.7mol的1-羟基苯并三唑和1.7mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.7mol色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤2次,无水硫酸钠干燥,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为80%;
(7)2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于2l乙酸乙酯和0.4l盐酸的混合溶液中,室温反应4h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得白色固体产物2,6-二甲基酪氨酸-n甲基d型丙氨酸-色氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,标记为mel-n1606,其产率为95%。
mel-n1606的结构式为:
其理化特征见表1,esi-ms谱图见图8。
实施例7mel-n1607的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.9mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.8mol的氨水,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺;产率为91%;
(2)3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将0.8mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得白色固体3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-苯丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.9mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.8mol的3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为88%;
(4)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.9mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.8mol的n-甲基-d型丙氨酸的饱和碳酸氢钠溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n-甲基-d型丙氨酸,产率为88%;
(5)苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得白色固体产物苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入4.9mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.8mol苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的二氯甲烷溶液,室温反应20h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,产率为81%;
(7)2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺溶于2.75l乙酸乙酯和0.5l盐酸的混合溶液中,室温反应5h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得白色固体产物2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3苯基丙酸酰胺,标记为mel-n1607,其产率为93%。
mel-n1607的结构式为:
其理化特征见表1,esi-ms谱图见图9。
实施例8mel-n1608的合成
(1)n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入5mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后加入1.8mol的氨水,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为92%;
(2)3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷混合溶液中,室温反应3h后,减压蒸馏,得白色固体3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(3)n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-苯丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入5mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.8mol的3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和碳酸氢钠洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为88%;
(4)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入5mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑,1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌充分溶解后,加入1.8mol的n甲基d型丙氨酸的饱和碳酸氢钠溶液,室温反应18h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得油状液体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸,产率为87%;
(5)苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐的合成:将1mol的n-叔丁氧羰基苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于0.06l三氟乙酸和0.05l二氯甲烷的混合溶液中,室温反应3h后,减压蒸馏,得白色固体产物苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺三氟乙酸盐,产率为99%;
(6)n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸溶于无水二氯甲烷,于0℃在搅拌状态下依次加入5mol的n,n-二异丙基乙基胺,1.8mol的1-羟基苯并三唑和1.8mol的1-乙基-3-(3-二甲胺丙基)碳二亚胺,搅拌下充分溶解后加入1.8mol苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的二氯甲烷溶液,室温反应16h后加入二氯甲烷稀释,5%柠檬酸溶液洗涤2次,饱和氯化钠洗涤1次,无水硫酸钠干燥,减压蒸馏,得白色固体产物n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,产率为80%;
(7)2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺的合成:将1mol的n-叔丁氧羰基-2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺溶于2.75l乙酸乙酯和0.5l盐酸的混合溶液中,室温反应5h后,调节ph=9-10,二氯甲烷萃取,无水硫酸钠干燥,减压蒸馏,得白色固体产物2,6-二甲基酪氨酸-n甲基d型丙氨酸-苯丙氨酸-3-氨基-2-甲烯基-3(2-呋喃)丙酸酰胺,标记为mel-n1608,其产率为95%。
mel-n1608的结构式为:
其理化特征见表1,esi-ms谱图见图10。
- 还没有人留言评论。精彩留言会获得点赞!