一种化合物的新晶型及其制备方法与应用与流程
本发明属于药物化学,特别是涉及一种化合物的新晶型及其制备方法与应用。
背景技术:
目前没有针对HIV病毒感染的治愈方法。20世纪90年代中期,高效抗反转录病毒疗法(highly active antiretroviral therapy,HAART)的出现被认为是艾滋病治疗史上里程碑性的事件。HAART联合使用数种能够阻断或抑制HIV病毒入胞、复制、转录、翻译、装配等过程的抗逆转录病毒药物,从而充分抑制病毒的增殖,将感染者体内的病毒载量降低到实验室检测水平以下(≤50拷贝/ml),使之免疫系统功能得到一定程度的恢复,最终显著延缓疾病的进展,大大降低AIDS的发病率和病死率,同时减少了HIV的传播。近几年来,HIV逆转录酶抑制剂已经成为重要的一类控制和治疗HIV感染的药物。迄今为止,美国FDA批准的抗HIV药物共有20多种,主要分为六大类:核苷(酸)类逆转录酶抑制剂(nucleoside/nucleotide reverse transcriptase inhibitors,N(t)RTI)、非核苷类逆转录酶抑制剂(non-nucleoside reverse transcriptase inhibitors,NNRTI)、蛋白酶抑制剂(PI)、融合抑制剂、整合酶链转移抑制剂(INSTI)和辅助受体抑制剂。初治AIDS患者的优选抗病毒治疗方案目前由2种N(t)RTI再联合1种NNRTI或PI、或INSTI组成,DHHS发布的指南自2009年开始列出了4种此类治疗方案:①替诺福韦+恩曲他滨+依非韦伦;②替诺福韦+恩曲他滨+达茹那韦/利托那韦;③替诺福韦+恩曲他滨+阿扎那韦/利托那韦;④替诺福韦+恩曲他滨+雷特格韦。
3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈,是一种新型非核苷类逆转录酶抑制剂,可用于HIV病毒感染预防和治疗,其英文名为3-[[3-ethyl-1,2,3,6-tetrahydro-5-(1-methylethyl)-2,6-dioxo-4-pyrimidinyl]carbonyl]-5-methyl benzonitrile,其化学结构式如下式:
分子式:C18H19N3O3 分子量:325.14
该化合物的CAS号为1097628-00-6,曾用代号包括:GS9441(吉利德科学公司)、KM023(Kaino Medicine)以及ACC007(江苏艾迪药业有限公司)。
美国专利US2009/0163712 A1报道了该化合物的合成工艺方法,部分反应操作再经优化,可用于工业化生产,生产成本较低,可满足我国对抗HIV药物的迫切需求。但是用于制备医药组合物的活性物质结晶,应该具有高纯度和高稳定性,即使在较苛刻的储存条件下,也应该保持稳定,还需确保该结晶形态在随后的制剂制备和储存中不会改变。至今为止,未见其相关晶型的研究结果报道。
技术实现要素:
本发明的目的在于提供一种具有高纯度和高稳定性的3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈I晶型。
本发明的目的还在于提供上述3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈I晶型的制备方法与应用。
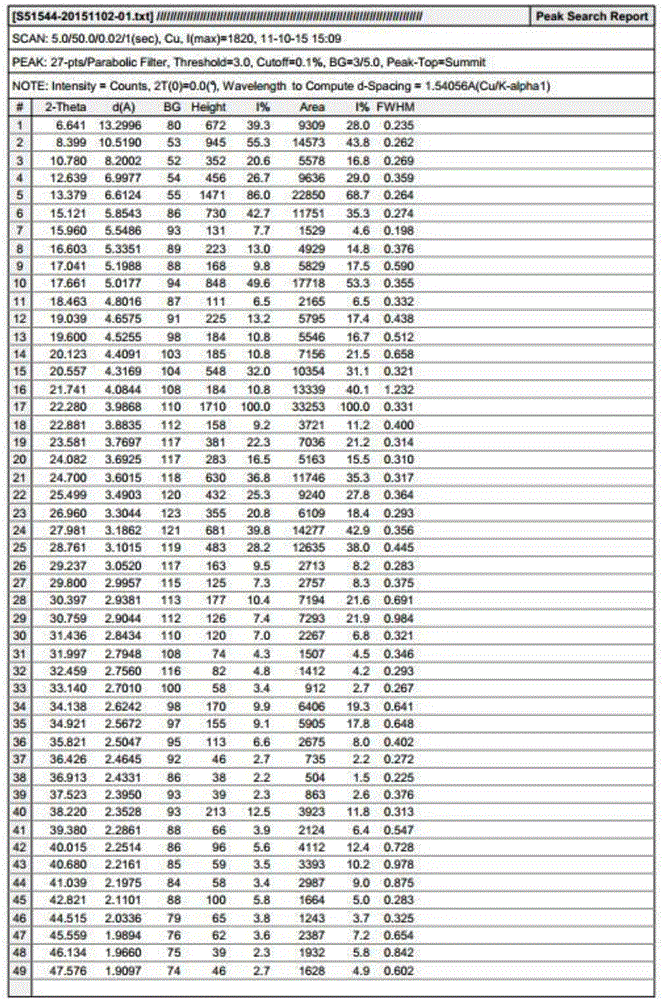
本发明所述的一种3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈I晶型,该晶型以2θ角度表示的X-射线粉末衍射图谱如附图1所示,在以下位置具有特征峰:6.6±0.1°,8.3±0.1°,10.7±0.1°,12.6±0.1°,13.3±0.1°,15.1±0.1°,16.6±0.1°,17.6±0.1°,19.0±0.1°,19.6±0.1°,20.1±0.1°,20.5±0.1°,21.7±0.1°,22.2±0.1°,23.5±0.1°,24.0±0.1°,24.7±0.1°,25.4±0.1°,26.9±0.1°,27.9±0.1°,28.7±0.1°,30.3±0.1°,38.2±0.1°。
如附图2该晶型的X射线粉末衍射数据可见,本发明的3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈I晶型X-射线粉末衍射光谱,还显示了多个特征吸收峰。
所述化合物I晶型的DSC图谱如图3所示,在227±1.5℃处有吸热峰。
所述化合物I晶型的熔程为223~231℃。
上述化合物I晶型的制备方法,包括以下步骤:取3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品,加入有机溶剂,加热至溶剂回流,并搅拌一定时间;降温至0℃~35℃并保持温度,搅拌养晶至析晶完全;然后分离并收集晶体,干燥即得I晶型。
所述溶解加热温度为溶剂回流温度;搅拌时间为0.5~10h,优先为1~2h。
所述有机溶剂选自异丙醇、乙醇、乙腈和乙酸乙酯中的一种或者多种。
优选的,所述有机溶剂为乙醇或异丙醇。最优选为乙醇。
所述3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品和有机溶剂的质量体积比为1:3~1:10。
优选的,所述的3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品和有机溶剂的质量体积比为1:5~1:7。
上述质量体积比的单位是指,当质量单位为g,体积单位为mL,当质量单位为kg,体积单位为L。
溶解后降温采用自然冷却或通冷凝水冷却,冷凝水温度为-10℃~25℃。
养晶温度为0~35℃,优选为20~25℃;养晶时间为0.5~5h,优选为1~2h。
养晶至析晶完全后采用真空抽滤或离心分离。
所述干燥采用鼓风或真空干燥,干燥温度为40℃~80℃,优选为60~65℃;干燥时间为30~60h,优选为40~50h。
本发明所述的3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I,以及含有该结晶的药物组合物,可用于各种HIV感染者的预防和治疗。
有益效果:本发明提供了一种抗HIV新药分子(3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈)的I晶型,所述晶型具有优良的稳定性、利于后处理及存储;并且制备方法简单,可用于制备抗HIV的药物,对后续相关药物的优化和开发具有重要的价值。
附图说明
图1是3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的X射线粉末衍射代表性谱图;
图2是3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的X射线粉末衍射代表性谱图数据;
图3是3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的DSC代表性谱图。
具体实施方式
下面结合具体实施例对本发明作出详细说明。
试剂来源:
3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品购自桑迪亚医药技术(上海)有限责任公司,粗品采用HPLC面积归一化法检测,纯度不低于98%。
实施例1:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的制备
取3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品20g于反应瓶中,加入60mL异丙醇,加热至回流,保温搅拌10h;边搅拌,边通冷凝水降温至0℃,继续保温搅拌0.5h,真空抽滤,滤饼于80℃真空干燥60h,得19g类白色固体,纯度99.3%,收率95%。
对制备所得3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I进行了粉末X射线衍射分析,其X射线粉末衍射谱图与代表性谱图一致,如图1所示;X射线粉末衍射数据与代表性谱图数据一致,如图2所示;DSC图谱与代表性谱图一致,如图3所示。
实施例2:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的制备
取3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品200g于反应瓶中,加入1200ml乙醇,加热至回流,保温搅拌4~5h;边搅拌,边通冷凝水降温至25℃,继续保温搅拌1.5h,真空抽滤,滤饼于60~65℃真空干燥48h,得144g类白色固体,纯度99.57%,收率72%。
对制备所得3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I进行了粉末X射线衍射分析,其X射线粉末衍射谱图与代表性谱图一致,如图1所示;X射线粉末衍射数据与代表性谱图数据一致,如图2所示;DSC图谱与代表性谱图一致,如图3所示。
实施例3:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的制备
取3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品200g于反应瓶中,加入2000ml乙腈,加热至回流,搅拌至溶清;边搅拌,边自然降温至35℃,继续保温搅拌5h,离心分离,滤饼于40℃鼓风干燥30h,得128g类白色固体,纯度99.30%,收率64%。
对制备所得3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I进行了粉末X射线衍射分析,其X射线粉末衍射谱图与代表性谱图一致,如图1所示;X射线粉末衍射数据与代表性谱图数据一致,如图2所示;DSC图谱与代表性谱图一致,如图3所示。
实施例4:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的制备
取3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈粗品200g于反应瓶中,加入1000mL乙醇中,加热至回流,搅拌1.5h;边搅拌,边自然降温至25℃,继续保温搅拌1.5h,离心分离,滤饼于60~65℃下,真空干燥60h,得156g类白色固体,纯度99.56%,收率78%。
对制备所得3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I进行了粉末X射线衍射分析,其X射线粉末衍射谱图与代表性谱图一致,如图1所示;X射线粉末衍射数据与代表性谱图数据一致,如图2所示;DSC图谱与代表性谱图一致,如图3所示。
实施例5:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的热稳定性测定
取实施例1-3制备所得3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I,在50~60℃,70~80℃,90~100℃下,烘干48h,并对烘干后样品纯度进行检验,实验结果如表1所示。
表1 3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈的热稳定性
结果表明,在50~100℃的烘干温度下,本品的含量没有显著变化,质量稳定。
实施例6:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I在加速条件的稳定性测定
对实施例1、2、3制备所得的晶型I进行了加速条件下的储存,对0天样品熔程及熔点进行了毛细管法及DSC法检测,加速6个月后的熔程进行了毛细管法检测,如表2所示。
表2 3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I加速条件的稳定性
结果表明,三批样品在加速条件下放置6个月后,熔点和熔程没有发生显著变化,证明本品在此条件下,具有很好的稳定性。
实施例7:3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的抗病毒活性测定
通过5天多循环试验法检测了实施例4所得的3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I在MT-2、MT-4细胞系中的抗病毒活性,如表3所示。
表3 3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的抗病毒活性
SD=standard deviation(标准差);EC50=half-maximal effective concentration(半数有效浓度);CC50=half-maximal cytotoxic concentration(半数细胞毒浓度)
a N(number of independent experiments)(独立试验数)≥10.
b N≥4.
c N≥3.
根据检测结果可见,其抗病毒效力,在MT-2细胞中测定的EC50值为6.8nM,在MT-4细胞中,EC50值为7.6nM,在同等试验条件下,3-{[3-乙基-2,6-二氧-5-(丙基-2-基)-1,2,3,6-四氢嘧啶-4-基]羰基}-5-甲基苯腈晶型I的抗病毒活性略低于依非韦伦(Efavirenz),但其细胞毒性较依非韦伦低。因此,本品具有优良的抗病毒活性,且具有很好的安全性。
- 还没有人留言评论。精彩留言会获得点赞!