一种检测铜离子和锌离子的探针及制备方法与应用与流程
【技术领域】
本发明属于金属离子检测的分子探针领域,特别是一种用于选择性检测铜离子和锌离子的分子探针及其制备方法与应用。
背景技术:
离子探针能够将离子存在信息转换成易被检测的光信号,进而获得特定离子的识别功能。在体系中与特定离子的相互作用会发生特定的物理化学变化,从而导致相应的光信号发生改变。离子探针具有高灵敏度,简单易行等诸多优点。
铜离子是常见的有毒重金属之一,对动植物及环境有严重危害。同时,铜离子还是人体必需的微量元素,与细胞繁殖、内分泌以及造血功能相关,但如果体内过量铜离子无法降解,会对人体产生危害。迄今为止的铜离子检测方法存在局限性,多依赖昂贵的检测仪器,成本较高。因此发展快速、简便、灵敏的铜离子检测方法具有十分重要的意义。
锌离子是人体必需的微量元素,在体内的含量仅次于铁离子。锌离子参与生物体内的诸多生理活动,比如脑功能、基因转染、免疫功能以及中枢神经信号传导等。由于锌离子的3d104s0的电子结构,自身无可测定的光谱以及核磁信号,因此常用的检测手段如紫外光谱、核磁共振、电子顺磁共振等都难以应用于锌离子的检测。现有的锌离子检测手段大多基于荧光探针方法,但是检测过程中易受到镉离子的干扰。
技术实现要素:
本发明的目的是针对上述技术分析和存在问题,提供了一系列基于[5]螺烯母体的亚胺化合物及其制备方法,及其在铜离子和锌离子检测中的应用。
本发明的技术方案:
该化合物是在[5]螺烯羟基的邻位引入亚胺结构,研究发现亚胺的n和螺烯的o能够与金属离子配位,能够利用紫外吸收光谱以及荧光光谱分别选择性检测铜离子和锌离子。
本发明用于检测铜离子和锌离子的荧光分子探针试剂dc,为螺烯的亚胺衍生物,符合通式结构:
其中,r选自碳原子数为1-10的直链或支链烷基、碳原子数为2-10的直链或支链烯基、具有3-8个环碳原子的环烷基、6-20个碳原子的单环或多环芳族基、5-20个碳原子的单环或是多环杂芳族基。
一种所述用于铜离子和锌离子检测的分子探针试剂的制备方法,步骤如下:
(1)冰浴条件下,dmf中加入氢化钠,慢慢加入螺烯(化合物a),搅拌反应0.5小时后,滴加氯甲基甲醚,滴加完成后室温搅拌2小时,抽滤,得到化合物b。
(2)氩气保护下,化合物b加入异丙醚中,冰浴下加入四甲基乙二胺0.5小时后,滴加正丁基锂,滴加完毕后,冰浴搅拌2小时,室温搅拌2小时,冰浴下加入dmf,继续冰浴搅拌2小时,加饱和氯化铵溶液淬灭反应,用乙酸乙酯萃取,用饱和氯化钠洗涤。有机层旋干,柱层析方法提纯得到化合物c。
(3)冰浴条件下,浓盐酸滴加化合物c的异丙醚溶液中,滴完后继续冰浴搅拌1小时,继续升至室温搅拌4小时。饱和碳酸氢钠溶液调ph至中性,抽滤得到化合物d。
(4)化合物d与r-nh2溶于乙醇中,加热回流1小时。过滤得到通式dc的化合物。r的选择如前面所述。
其中步骤(1)中所述化合物a、氢化钠与氯甲基甲醚的摩尔比为1mol:5-10mol:2-10mol,具体可为1mol:6-8mol:3-5mol
步骤(2)中所述反应需在氩气保护下进行;
所述化合物b、1.6m正丁基锂及dmf的用量比为1mol:2-3l:0.6-1l,具体可为1mol:2.8l:0.7l
步骤(3)中所述化合物c、异丙醚与浓盐酸的用量比为1mol:5-15l:2-10l,具体可为1mol:10l:3.7l
步骤(4)中所述化合物d、r-nh2的摩尔比为1mol:2-5mol,具体可为1mol:2-3mol
本发明的优点是:本发明制备的螺烯衍生物dc,合成简单方便,产率高,易于制备,适于放大合成及实际生产应用。能够利用紫外可见吸收光谱检测二价铜离子,并能够利用荧光方法检测二价锌离子,其作为新型探针可以应用于离子检测领域。探针分子选择性好且灵敏度高,具有响应快、现象明显的优势,有着广阔的应用前景。
【附图说明】
图1为dc-1加入10当量不同金属离子后的吸收光谱。
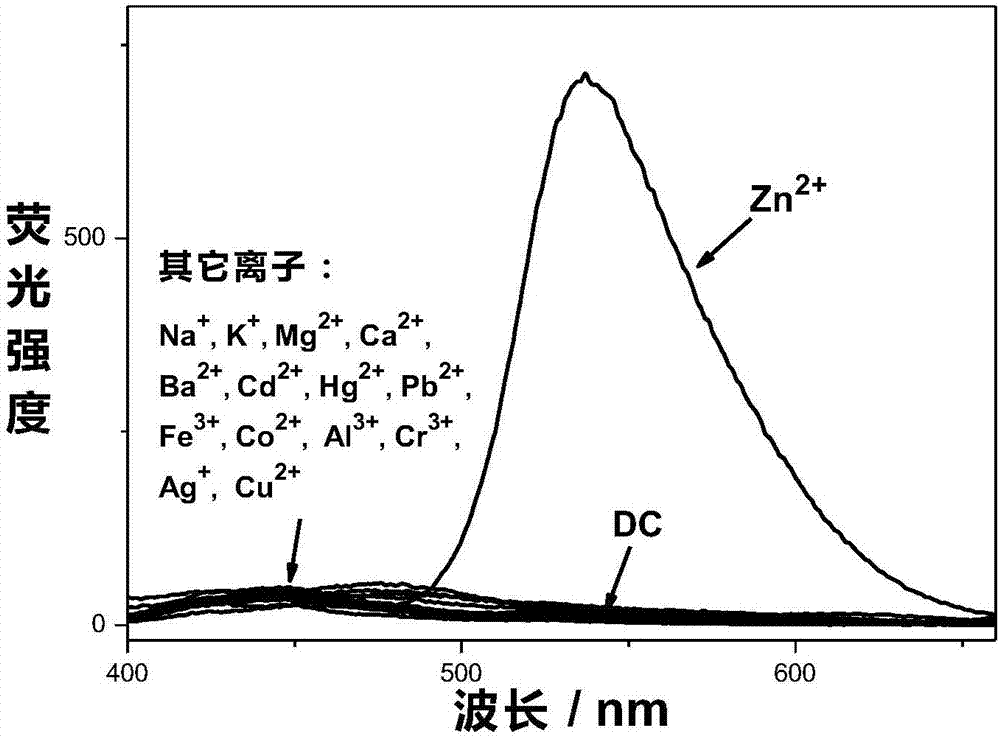
图2为dc-1加入10当量不同金属离子后的荧光光谱。
图3为dc-1加入0-7当量铜离子的吸收光谱。
图4为dc-1加入0-7当量锌离子的荧光光谱。
【具体实施方式】
为了进一步说明本发明,给出以下系列具体实施例,但本发明并不受这些具体实施例的限制,了解该领域的技术人员对本发明的些许改动将可以达到类似的结果,这些改动也包含在本发明中。
实施例1:
制备r=正丁基的化合物dc-1
(1)在100ml单口瓶内,加入氢化钠0.46g(19.2mmol),后加入50ml的dmf作为溶剂,冰浴下加入1g(2.77mmol)化合物a,搅拌0.5h后滴加氯甲基甲醚0.9ml(11.85mmol),滴加完成后室温搅拌2小时,抽滤,得到化合物b,产率为95%。
(2)在50ml双口瓶内加入0.5g(1.11mmol)化合物b后,加入异丙醚25ml作为溶剂,冰浴下搅拌通氩气5分钟。氩气保护下加入四甲基乙二胺0.84ml(5.47mmol),后滴加1.6m的正丁基锂3.12ml(5.0mmol),冰浴搅拌2小时,室温搅拌2小时,后冰浴下加入0.77ml(9.99mmol)的dmf,继续冰浴搅拌2小时,加饱和氯化铵7ml淬灭反应,用乙酸乙酯萃取分出有机层,。有机层旋干,经过柱层析分离,得到化合物c,产率为44.7%。
(3)在50ml单口瓶内,加入0.1g(0.2mmol)化合物c,加入15ml异丙醚作为溶剂,后在冰浴搅拌下滴加0.74ml浓盐酸,滴完后继续冰浴搅拌1小时,继续升至室温搅拌4小时。饱和碳酸氢钠溶液调ph至中性,抽滤得到化合物d,产率为95%。
(4)化合物d(416mg,1mmol)溶于5ml乙醇中,缓慢加入正丁胺(2mmol),滴加完毕,回流1小时,有沉淀析出,冷却,过滤固体,并用冰乙醇洗涤,固体真空干燥得到化合物dc-1,产率90%。
检测结果:1hnmr(500mhz,cdcl3)δ12.98(s,2h),8.70-8.62(m,2h),8.53(s,2h),8.48(d,j=8.8hz,2h),7.97(d,j=8.7hz,2h),7.87(s,2h),7.69(dd,j=5.9,2.9hz,2h),7.60(s,2h),3.64(t,j=6.7hz,4h),1.76-1.64(m,4h),1.50-1.36(m,4h),0.96(t,j=7.3hz,6h).
13cnmr(126mhz,cdcl3)δ164.01,156.74,133.44,131.82,130.61,130.44,127.82,127.38,125.99,124.87,123.59,120.59,117.89,114.30,59.73,32.82,13.73.
实施例2:
制备r=环己基的化合物dc-2
(1)化合物d的制备按照实施例1中的制备方法制备。
(2)化合物d(416mg,1mmol)溶于5ml乙醇中,缓慢加入环己胺(2mmol),滴加完毕,回流2小时,有沉淀析出,冷却,过滤固体,并用冰乙醇洗涤,固体真空干燥得到化合物dc-2,产率92%。
检测结果:1hnmr(500mhz,cdcl3)δ13.08(s,2h),8.66(dd,j=5.7,3.2hz,2h),8.55(s,2h),8.47(d,j=8.8hz,2h),7.95(d,j=8.8hz,2h),7.85(s,2h),7.68(dd,j=5.9,2.9hz,2h),7.59(s,2h),3.29(s,2h),1.95–1.74(m,8h),1.57(m,6h),1.33(m,6h).
本发明的具体应用及效果如下:
用紫外可见分光光度计以及荧光分光光度计分别对其识别cu2+和zn2+的性能进行了研究。所有测试均在乙腈溶液中进行。dc浓度为2×10-5m以及1×10-6m,分别用于紫外以及荧光测试。测试用的盐溶液为对应的高氯酸盐的乙腈溶液。
图1为dc-1化合物对于金属阳离子的选择性吸收图。2×10-5m的dc-1的乙腈溶液中,分别加入10当量不同的金属离子(na+,k+,mg2+,ca2+,ba2+,cd2+,hg2+,pb2+,fe3+,co2+,al3+,cr3+,ag+,cu2+,zn2+),发现只有加入铜离子会在可见光区400-600nm出现吸收峰,对应溶液的颜色由无色变为红色。
图2为dc-1化合物对于金属阳离子的选择性荧光图。1×10-6m的dc-1的乙腈溶液中,分别加入10当量不同的金属离子(na+,k+,mg2+,ca2+,ba2+,cd2+,hg2+,pb2+,fe3+,co2+,al3+,cr3+,ag+,cu2+,zn2+),发现只有加入锌离子会在480nm处出现荧光发射峰,其它离子不会导致探针的荧光变化。
图3是dc-1在加入0-7当量的铜离子的吸收光谱变化图。不加铜离子时,dc-1在可见光区400-600nm处没有吸收。随着铜离子的量的逐步增加,400-600nm处的吸收峰逐渐变强。
图4是dc-1在加入0-7当量的锌离子的发射光谱变化图。不加锌离子时,dc-1几乎没有荧光发射峰。随着锌离子的量的逐步增加,480nm处的荧光强度逐渐变强。
结果表明,合成的基于螺烯骨架的亚胺衍生物dc对于铜离子和锌离子都有很好的响应,可以作为比色探针检测铜离子也可以作为荧光探针检测锌离子,本类化合物在铜离子和锌离子检测中有广泛的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!