一种合成新型的氮氧杂桥联唑啉化合物的方法与流程
本发明涉及三唑啉衍生物的合成技术领域,尤其涉及新型的氮氧杂桥联唑啉化合物,以及合成新型的氮氧杂桥联唑啉化合物的方法。
背景技术:
唑啉及其衍生物是重要的含氮杂环化合物之一,许多具有生物活性物质的结构中都含有唑啉骨架单元。因此,唑啉及其衍生物广泛应用于生物、农业和医药等领域中。四氢化萘砌块存在于许多生物活性化合物中,也是最常见的骨架之一。含有四氢化萘砌块的化合物包括抗生素、去氧鬼臼素葡萄糖酯苷、异紫杉脂素(存在于中国紫杉醇中)以及肾上腺激素等。这些化合物具备的生理活性包括抗菌、抗癌、抗帕金森、止痛、抗抑郁等。近年来,化学家们发展了一些有效的方法来构建这类具有生物活性的有机骨架。而环加成修饰对氧杂苯并降冰片烯及氮杂苯并降冰片烯的官能化,具有非常实用的科学意义和应用价值。
三唑啉类化合物和具有四氢化萘结构单元的化合物由于其稳定的代谢,高选择性和较少的不良反应,在化学、生物学和医学上的研究受到越来越多的关注。它们被用作抗真菌剂、抗惊厥剂等,并且在设计抗癌药剂中得到了广泛应用。三唑啉类抗惊厥药物(如add17014)与常规抗惊厥药物不同,三唑啉类抗惊厥药大多数具有酰脲或二甲酰亚胺基团,如乙内酰脲、巴比妥类、恶唑烷二酮和琥珀酰亚胺等。这些基团具有的镇静和催眠作用可减轻潜在的三唑啉抗惊厥药中的毒副作用。在小鼠的抗惊厥活性测定实验中,在30mg/kg或100mg/kg的剂量的情况下,实验结果显示抗惊厥活性的化合物对小鼠没有产生损害神经功能的情况。研究发现,三唑啉类药物的抗惊厥效能和极小的神经毒性,与临床使用的四种传统的抗癫痫药物(苯妥英、乙酰亚胺、丙戊酸和苯巴比妥)的作用相当。它们不仅能增加癫痫病发作的阈值,还可以预防癫痫发作,今后有望发展为优良的抗癫痫药物。
因此,研究由含杂原子苯并降并片烯或其衍生物的环加成反应合成三唑啉衍生物的反应,以期可在环境友好及更温和的反应条件下实现高产率和高反应速率,对于开发新型药物及工业生产具有重要的意义。
技术实现要素:
本发明针对三唑啉衍生物有待进一步开发,以及由苯并降并片烯及其衍生物通过多组分一步成环反应合成三唑啉衍生物,需对反应条件进行优化,使产率和反应速率进一步提高。因此,本发明提供一种新型的氮氧杂桥联唑啉化合物的合成方法。
为实现上述目的,本发明采用以下技术方案。
一种新型的氮氧杂桥联唑啉化合物,所述化合物的结构如下:
其中,r1为h或ome,r2为h或ome或f或br,x为o或n-ts或n-fs或n-bs,alkyl为ch2ch2cl或ch2ch3或ch2ch2ch2ch3或ch2ch2ch2ch2cl。
一种合成新型的氮氧杂桥联唑啉化合物的方法,包括以下步骤:
s1、将苯并降冰片烯或其衍生物、叠氮化钠和溶剂混合在一起,得混合体系;然后向混合物体系中加入添加剂,得反应体系;接着将反应体系加热至60-70℃。
所述叠氮化钠的物质的量大于或等于苯并降冰片烯或其衍生物的物质的量。优选的,苯并降冰片烯或其衍生物与叠氮化钠的物质的量之比为1:2。
所述苯并降冰片烯或其衍生物与添加剂的物质的量之比为100:2-10。
s2、反应体系在60-70℃下反应10-24h。
优选的,反应体系在65℃下进行反应12h或24h。
s3、用有机溶剂萃取反应体系,收集有机层;然后真空浓缩有机层,接着通过柱层析色谱法纯化,收集氮氧杂桥联唑啉化合物。
所述苯并降冰片烯的衍生物为:
所述溶剂为水与卤代烷烃的混合物,所述水与卤代烷烃的体积比为1-3:1。优选的,所述水与卤代烷烃的体积比为1:1。
所述卤代烷烃为clch2ch2cl或clch2ch3或clch2ch2ch2ch3或clch2ch2ch2ch2cl。
所述添加剂为bu4nbr或bu4nbf4或bu4noac。优选的,所述苯并降冰片烯或其衍生物与添加剂的物质的量之比为100:5。
与现有技术相比,本发明的有益效果是:本发明首次利用苯并降冰片烯或其衍生物、叠氮化钠和卤代烷烃这三种组分构建三唑啉衍生物,通过添加适量的bu4noac添加剂,使反应可在水相体系中顺利进行,且原子利用率高、反应速率快、产率高,反应12h产率即可高达99%。本发明的合成方法可在环境友好及温和的反应条件下实现高产率和高反应速率,对开发新型药物及工业生产具有重要的意义。
附图说明
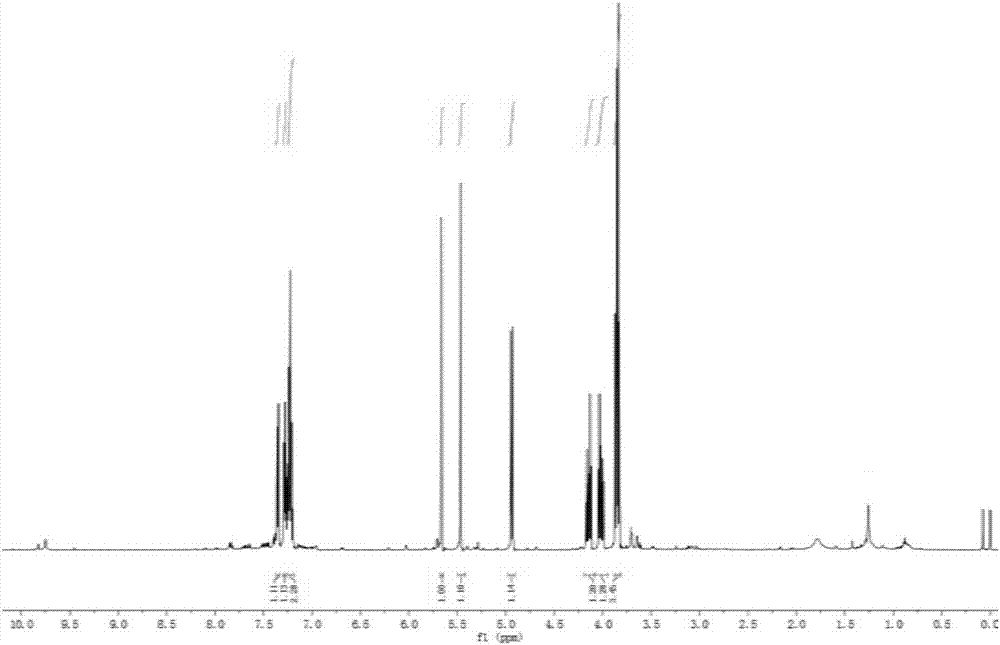
图1为化合物3aa的核磁共振氢谱;
图2为化合物3aa的核磁共振碳谱;
图3为化合物3ha的核磁共振氢谱;
图4为化合物3ha的核磁共振碳谱。
具体实施方式
为了更充分的理解本发明的技术内容,下面结合具体实施例对本发明的技术方案作进一步介绍和说明。
实施例1-37
实施例1-37提供的合成新型的氮氧杂桥联唑啉化合物的方法,具体步骤如下:
(1)将苯并降冰片烯或其衍生物、叠氮化钠和溶剂混合在一起,得混合体系;然后向混合物体系中加入添加剂,得反应体系;接着将反应体系加热至60-70℃。
(2)反应体系在60-70℃下反应10-24h。
(3)用乙酸乙酯萃取反应体系,分离水层,收集有机层。
(3)真空浓缩有机层,再通过硅胶柱层析色谱法纯化(洗脱液为乙酸乙酯/石油醚=1:5,v/v),收集氮氧杂桥联唑啉化合物。
实施例1-37的反应条件及产率如下表1所示。
表1实施例1-37的反应条件及产率
表1中反应物1指苯并降冰片烯或苯并降冰片烯的衍生物,反应物1所包含的具体化合物的结构式如下表2所示;表1中实施例合成的新型的氮氧杂桥联唑啉化合物的结构式如下表3所示。
表2反应物1所包含的具体化合物的结构式
表3实施例5-7、9-37合成的新型的氮氧杂桥联唑啉化合物的结构式
由上述实施例合成的化合物3aa和3ha的核磁共振氢谱和核磁共振碳谱如图1-4所示。
由实施例5-7、9-37合成的上述化合物的性状、核磁共振氢谱、核磁共振碳谱和质谱数据分别如下所示。
化合物3aa:
1-(2-chloroethyl)-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(500mhz,cdcl3)δ7.38(d,j=6.5hz,1h),7.33–7.29(m,1h),7.28–7.23(m,2h),5.69(s,1h),5.50(d,j=10.1hz,1h),4.97(t,j=9.4hz,1h),4.23–4.12(m,1h),4.09–4.00(m,1h),3.87(dd,j=13.8,7.7hz,3h).13cnmr(125mhz,cdcl3)δ143.4,143.0,128.0,127.7,120.5,120.4,87.6,83.3,82.7,63.8,49.9,42.8.hrmsm/z(ei)(m+)calcdforc12h12cln3o:249.0669,found:249.0668.
化合物3ba:
1-(2-chloroethyl)-5,8-dimethoxy-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.116.5-117.0℃.1hnmr(500mhz,cdcl3)δ5.74(s,1h),5.51(s,1h),4.89(d,j=8.7hz,1h),4.06(dt,j=14.0,6.2hz,1h),3.99–3.86(m,1h),3.77(dd,j=10.3,5.9hz,3h),3.74(s,3h),3.72(s,3h).13cnmr(125mhz,cdcl3)δ146.3,146.3,131.2,130.8,111.3,110.8,86.1,80.4,79.6,62.1,55.1,54.9,48.7,41.4.hrmsm/z(ei)(m+)calcdforc14h16cln3o3:309.0880,found:309.0887.
化合物3ca:
1-(2-chloroethyl)-6,7-dimethoxy-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(600mhz,cdcl3)δ6.95(s,1h),6.88(s,1h),5.61(s,1h),5.43(s,1h),4.90(d,j=8.7hz,1h),4.16–4.09(m,1h),4.04–3.97(m,2h),3.89(s,3h),3.88(s,3h),3.84(dd,j=12.3,6.6hz,3h).13cnmr(150mhz,cdcl3)δ149.0,148.7,135.4,135.1,104.9,104.8,87.9,83.5,82.9,64.0,56.3,49.9,42.8.hrmsm/z(ei)(m+)calcdforc14h16cln3o3:309.0880,found:309.0877.
化合物3da:
6,7-dibromo-1-(2-chloroethyl)-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.114.5-115.0℃.1hnmr(500mhz,cdcl3)δ7.66(d,j=19.5hz,1h),7.57(dd,j=21.0,17.1hz,1h),5.66(dd,j=11.6,7.8hz,1h),5.52–5.42(m,1h),4.98(dd,j=19.3,8.5hz,1h),4.21–4.12(m,1h),4.04(ddd,j=28.5,14.1,8.2hz,1h),3.96–3.80(m,3h).13cnmr(125mhz,cdcl3)δ144.3,144.0,125.9,125.8,124.1,123.9,87.2,82.7,82.3,63.6,50.0,43.0.hrmsm/z(ei)(m+)calcdforc12h10br2cln3o:404.8879,found:404.8874.
化合物3ea:
1-(2-chloroethyl)-10-tosyl-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.102.5-103.0℃.1hnmr(500mhz,cdcl3)δ7.42(d,j=8.2hz,2h),7.10(t,j=6.4hz,1h),7.06–6.98(m,5h),5.38(s,1h),5.23(s,1h),4.86(d,j=8.9hz,1h),4.23–4.12(m,1h),3.96(dt,j=14.7,6.5hz,1h),3.88–3.77(m,3h),2.30(s,3h).13cnmr(125mhz,cdcl3)δ143.5,141.5,141.3,135.2,129.2,127.9,127.8,127.6,121.5,121.5,87.8,67.6,66.6,63.8,49.4,42.8,21.4.hrmsm/z(ei)(m+)calcdforc19h19cln4o2s:402.0917,found:402.0916.
化合物3fa:
1-(2-chloroethyl)-6,7-dimethoxy-10-tosyl-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.134.5-135.0℃.1hnmr(500mhz,cdcl3)δ7.36(dd,j=8.2,6.6hz,2h),6.98(d,j=8.0hz,2h),6.61(s,1h),6.55(d,j=7.6hz,1h),5.27–5.19(m,1h),5.08(d,j=10.5hz,1h),4.76(t,j=9.2hz,1h),4.06(tt,j=8.1,4.1hz,1h),3.88–3.84(m,1h),3.75(ddd,j=7.9,7.0,4.0hz,3h),3.72(d,j=3.0hz,3h),3.71(s,3h),2.24(s,3h).13cnmr(125mhz,cdcl3)δ147.9,147.6,142.5,134.6,133.0,132.7,128.1,127.0,105.0,104.8,87.1,66.9,65.9,63.0,55.2,48.4,41.8,20.4.hrmsm/z(ei)(m+)calcdforc21h23cln4o4s:462.1129,found:462.1143.
化合物3ga:
1-(2-chloroethyl)-10-((4-fluorophenyl)sulfonyl)-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.122.0-122.5℃.1hnmr(500mhz,cdcl3)δ7.45(dd,j=8.6,5.1hz,2h),7.02(d,j=6.1hz,1h),6.99–6.90(m,3h),6.79(t,j=8.5hz,2h),5.31(s,1h),5.15(s,1h),4.79(d,j=8.9hz,1h),4.16–4.06(m,1h),3.94–3.86(m,1h),3.84–3.70(m,3h).13cnmr(125mhz,cdcl3)δ166.0,163.9,141.3,141.1,134.2,130.6,130.5,128.2,127.9,121.6,121.5,115.9,115.7,87.8,67.7,66.8,63.9,49.6,42.9.hrmsm/z(ei)(m+)calcdforc18h16clfn4o2s:406.0667,found:406.0654.
化合物3ha:
10-((4-bromophenyl)sulfonyl)-1-(2-chloroethyl)-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.126.5-127.0℃.1hnmr(500mhz,cdcl3)δ7.30–7.22(m,4h),7.03–6.92(m,4h),5.31(s,1h),5.15(s,1h),4.80(d,j=9.0hz,1h),4.10(ddd,j=17.1,11.4,5.7hz,1h),3.90(dt,j=14.8,6.3hz,1h),3.81–3.74(m,3h).13cnmr(125mhz,cdcl3)δ140.3,140.0,136.1,130.8,128.2,127.1,126.8,126.8,120.6,120.6,86.7,66.7,65.9,62.9,48.5,41.8.hrmsm/z(ei)(m+)calcdforc18h16brcln4o2s:465.9866,found:465.9879.
化合物3ia:
10-((4-bromophenyl)sulfonyl)-1-(2-chloroethyl)-6,7-difluoro-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.132.6-133.0℃.1hnmr(600mhz,cdcl3)δ7.53–7.50(m,2h),7.50–7.46(m,2h),7.06(dd,j=8.4,6.8hz,1h),6.99(dd,j=8.4,6.8hz,1h),5.38(s,1h),5.24(s,1h),4.89(d,j=8.9hz,1h),4.18–4.09(m,1h),3.97(ddd,j=14.9,6.7,5.6hz,1h),3.89–3.78(m,3h).13cnmr(150mhz,cdcl3)δ138.0,137.9,137.6,137.6,137.2,132.1,129.3,128.4,111.9,111.9,111.8,111.7,87.6,67.2,66.6,63.9,49.8,43.0.hrmsm/z(ei)(m+)calcdforc18h14brclf2n4o2s:501.9677,found:501.9669.
化合物3ab:
1-ethyl-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(600mhz,cdcl3)δ7.27(d,j=7.0hz,1h),7.20(d,j=7.1hz,1h),7.15(dt,j=14.8,7.4hz,2h),5.58(s,1h),5.33(s,1h),4.79(d,j=8.8hz,1h),3.87–3.73(m,1h),3.67(d,j=8.7hz,1h),3.65–3.60(m,1h),1.31(t,j=7.3hz,3h).13cnmr(150mhz,cdcl3)δ143.6,143.2,127.9,127.6,120.4,120.4,86.5,83.5,82.6,63.1,43.0,14.0.hrmsm/z(ei)(m+)calcdforc12h13n3o:215.1059,found:215.1050.
化合物3ac:
1-butyl-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(500mhz,cdcl3)δ7.37(d,j=6.7hz,1h),7.30(d,j=7.1hz,1h),7.28–7.22(m,2h),5.67(s,1h),5.43(s,1h),4.90(d,j=8.8hz,1h),3.86(dt,j=13.7,8.0hz,1h),3.80–3.69(m,2h),3.63(dd,j=12.3,6.6hz,2h),2.01–1.88(m,5h).13cnmr(125mhz,cdcl3)δ143.5,143.1,128.0,127.6,120.4,86.7,83.5,82.4,63.3,47.4,44.6,29.6,25.8.hrmsm/z(ei)(m+)calcdforc14h17n3o:243.1372,found:243.1354.
化合物3ae:
1-(4-chlorobutyl)-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(600mhz,cdcl3)δ7.35(t,j=8.8hz,1h),7.29–7.26(m,1h),7.24–7.19(m,2h),5.65(s,1h),5.39(s,1h),4.86(d,j=8.9hz,1h),3.86–3.77(m,1h),3.72(d,j=8.9hz,1h),3.65(ddd,j=13.9,7.9,6.1hz,1h),1.73(dt,j=13.9,7.1hz,2h),1.43(dt,j=12.5,6.2hz,2h),0.97(d,j=7.4hz,2h).13cnmr(150mhz,cdcl3)δ143.6,143.2,127.9,127.6,120.4,120.4,86.4,83.5,82.5,63.3,47.9,30.6,20.0,13.7.hrmsm/z(ei)(m+)calcdforc14h16cln3o:277.0982,found:277.0962.
化合物3fe:
1-(4-chlorobutyl)-10-tosyl-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.;1hnmr(500mhz,cdcl3)δ7.39(t,j=11.7hz,2h),7.07(t,j=6.6hz,1h),7.04–6.96(m,5h),5.35(s,1h),5.14(s,1h),4.79(d,j=9.0hz,1h),3.78(dt,j=13.4,6.6hz,1h),3.71–3.59(m,4h),2.28(s,3h),1.96–1.87(m,4h);13cnmr(125mhz,cdcl3)δ142.4,140.7,140.4,134.2,128.1,126.9,126.8,126.5,120.4,86.0,66.7,65.6,62.6,46.1,43.7,28.5,24.7,20.4.hrmsm/z(ei)(m+)calcdforc21h23cln4o2s:430.1230,found:430.1221.
化合物3ge:
10-((4-fluorophenyl)sulfonyl)-1-(4-chlorobutyl)-3a,4,9,9a-tetrahydro-1h-4,9-epiminonaphtho[2,3-d][1,2,3]triazole.白色固体.m.p.105.5-106.0℃.1hnmr(600mhz,cdcl3)δ7.56–7.46(m,2h),7.08(d,j=6.5hz,1h),7.03–6.99(m,2h),6.86(dd,j=12.3,4.6hz,2h),5.37(s,1h),5.16(s,1h),4.81(d,j=9.0hz,1h),3.85–3.77(m,1h),3.71(dd,j=13.7,7.0hz,1h),3.68(d,j=8.9hz,1h),3.64(t,j=5.5hz,2h),1.92(ddd,j=14.9,8.4,3.9hz,4h).13cnmr(150mhz,cdcl3)δ165.8,164.1,141.4,141.1,134.2,130.6,130.5,128.2,127.8,121.5,115.8,115.7,87.0,67.8,66.8,63.7,47.2,44.7,29.5,25.8.hrmsm/z(ei)(m+)calcdforc20h20clfn4o2s:434.0980,found:434.0969.
化合物3bc:
5,8-dimethoxy-1-propyl-3a,4,9,9a-tetrahydro-1h-4,9-epoxynaphtho[2,3-d][1,2,3]triazole.黄色油状.1hnmr(500mhz,cdcl3)δ6.61(d,j=4.4hz,2h),5.74(s,1h),5.47(s,1h),4.82(d,j=8.8hz,1h),3.76(t,j=2.6hz,1h),3.75(s,3h),3.73(s,3h),3.72–3.68(m,2h),1.72–1.62(m,2h),1.38(dt,j=15.0,7.5hz,2h),0.94–0.89(m,3h).13cnmr(125mhz,cdcl3)δ146.3,146.3,131.5,131.2,111.2,110.6,85.0,80.6,79.4,61.9,55.1,54.9,46.8,29.6,19.0,12.7.hrmsm/z(ei)(m+)calcdforc16h21n3o3:303.1583,found:303.1569.
以上所述仅以实施例来进一步说明本发明的技术内容,以便于读者更容易理解,但不代表本发明的实施方式仅限于此,任何依本发明所做的技术延伸或再创造,均受本发明的保护。
- 还没有人留言评论。精彩留言会获得点赞!