一种胃癌分子标志物hsa_circ_0000705及其应用的制作方法
本发明属于肿瘤标志物领域,特别涉及一种胃癌分子标志物hsa_circ_0000705及其应用。
背景技术:
随着高通量全基因组测序技术的普遍应用,人们惊奇地发现哺乳动物细胞中约98%的转录物为非编码rna分子(noncodingrna,ncrna)。在这些非编码rna分子中有包括目前人们所熟知的“看家(housekeeping)”非编码rna(如transferrnas和ribosomalrnas等)、小非编码rna(如micrornas和pirnas等)、长链非编码rna(longnoncodingrna,lncrna),而更多的则是尚待深入研究的环状rna(circularrna,circrna)分子。
circrna是指一类由前体rna经可变剪接产生、并以5'末端和3'末端反向共价键结合的内源性环状rna分子。国内外初步研究结果显示circrna是一类具有重要生物学功能的新型rna分子,它可通过与rna或蛋白质相互作用,在转录、转录后多个水平参与基因表达调控。同时由于circrna序列高度保守,性质稳定,不易被核酸外切酶降解,并且具有组织、时序和疾病相对特异性,所以circrna具备成为临床疾病精准诊断分子标志物的潜质。
胃癌是世界最常见的消化道恶性肿瘤之一,其发病率在所有恶性肿瘤中居第4位,死亡率排第2位。在我国,每年新发胃癌患者高达40万,居世界首位;死亡人数30万,占全球因胃癌死亡人数一半。胃癌的早期诊断是全球性的研究热点,也是研究的难点。长期临床实践证明胃癌筛查是早期发现并诊断胃癌的有效办法。然而遗憾的是,即使是目前临床最先进的物理检测手段(如:ct、核磁共振等)发现肿瘤的极限直径仅为1cm,而常用肿瘤标志物的灵敏度和特异度亦不够理想,如癌胚抗原(carcinoembryonicantigen,cea)筛查胃癌的灵敏度和特异性分别仅为36.0%和86.2%。因此,结合临床成本效益原则,开发新型肿瘤标志物尤其是针对早期胃癌精准诊断分子标志物对于提高胃癌诊断率具有重要意义。
技术实现要素:
本发明所要解决的技术问题是提供一种胃癌分子标志物hsa_circ_0000705及其应用,该分子标志物具有极好的胃癌组织特异性和胃癌相关性,并且可通过rt-pcr方法实现定量检测,为早期胃癌的发现和检测提供了新的分子标志物,对进一步提高当前胃癌诊治水平,具有一定的意义。
本发明提供了一种胃癌分子标志物hsa_circ_0000705,其核苷酸序列如seqidno.1所示。
所述hsa_circ_0000705定位于人16号染色体58593707~58594266区域,由cnot1基因转录后经剪切形成。hsa_circ_0000705本质上是一种环状rna分子。本发明利用消化内科放大胃镜、细胞显微切割、circrna芯片技术检测并比较了3对胃癌组织与癌旁组织circrna表达谱的差异,其中环状rnahsa_circ_0000705在胃癌组织中显著低表达。
用于所述hsa_circ_0000705检测的特异性pcr反向引物为:
上游序列为5’-taactggggctcttcagctc-3’;
下游序列为5’-tggtggttgtctggccttat-3’。通过对该引物的pcr产物测序,验证了引物扩增的特异性。
所述hsa_circ_0000705在胃癌前病变组织及胃癌组织中低表达。
本发明还提供了一种胃癌分子标志物hsa_circ_0000705的应用,应用于研究胃癌组织的表达情况。
本发明借助样本rna提取、rna质量鉴定与目标的定量rt-pcr检测方法,大样本验证hsa_circ_0000705在胃癌组织表达情况,hsa_circ_0000705在79.2%胃癌患者癌组织中显著低表达。进一步大样本检测并横向比较hsa_circ_0000705分子在健康人胃组织、良性胃病变(胃溃疡、胃炎)组织、胃癌前病变(异型增生)组织及各期胃癌组织中的水平及其变化规律,最终鉴定出hsa_circ_0000705只在胃癌前病变(异型增生)组织及胃癌组织中低表达,具有极好的胃癌组织特异性。
本发明通过构建受试者工作特征(roc)曲线证明胃癌组织hsa_circ_0000705具有良好的敏感性与特异性。hsa_circ_0000705的roc曲线下面积为0.719(95%ci,0.648-0.791)。当其截断值为9.125,敏感性和特异性分别为64.58%和69.79%(均超过现有胃癌标志物cea、ca19-9水平)。结合肿瘤临床病理因素,本发明证明胃癌组织中hsa_circ_0000705的表达水平与肿瘤阶段、borrmann分型、病理类型和组织ca19-9表达密切相关。本发明通过上述研究证明hsa_circ_0000705具有极好的胃癌相关性。
有益效果
本发明应用circrna芯片、定量pcr检测等技术,确认hsa_circ_0000705只在胃癌前病变(异型增生)组织及胃癌组织中低表达,具有极好的胃癌组织特异性和胃癌相关性,并且可通过rt-pcr方法实现定量检测,为早期胃癌的发现和检测提供了新的分子标志物,对进一步提高当前胃癌诊治水平具有一定的意义。
附图说明
图1为hsa_circ_0000705的pcr产物测序图;
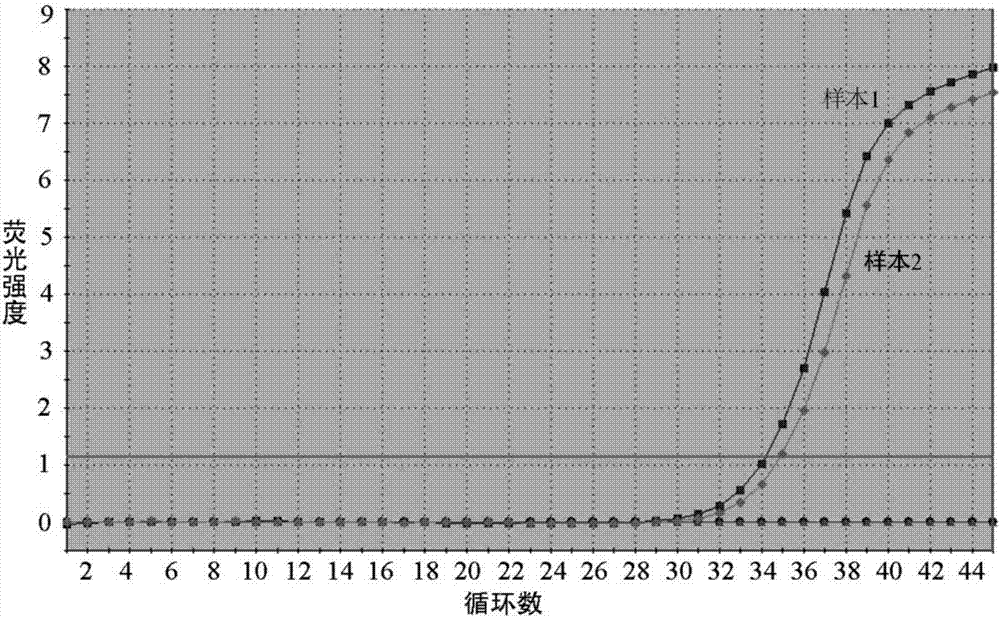
图2为两个组织标本中hsa_circ_0000705的扩增曲线图;
图3为两个组织标本中hsa_circ_0000705的解链曲线图;
图4为两个组织标本中gapdh的扩增曲线图;
图5为两个组织标本中gapdh的解链曲线图;
图6为hsa_circ_0000705在胃癌组织及其配对癌旁组织中表达情况;
图7为胃黏膜异型增生组织及其配对正常组织中hsa_circ_0000705的表达水平;
图8为hsa_circ_0000705在健康人胃组织、良性胃病变(胃溃疡、胃炎)组织、胃癌前病变(异型增生)组织及各期胃癌组织中的表达水平及其变化规律;
图9为hsa_circ_0000705的roc曲线。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1
(一)样本的采集与处理
对胃癌患者进行外科手术治疗,切除病变组织。在胃癌病灶和远离病灶部位3cm外分别切取黄豆样大小组织一块,用手术刀切成厚度不超过0.5cm的组织小块,浸泡入1mlrnafixer非液氮型样品rna保存液(北京百泰克)中,放入-80℃超低温冰箱中备用。
(二)特异性pcr反向引物设计与合成
借助于primerpremier引物设计软件,自主设计了用于hsa_circ_0000705检测的特异性pcr反向引物(divergentprimer),并委托上海生工生物工程股份有限公司合成。该引物上游引物序列为5’-taactggggctcttcagctc-3’,下游引物序列为5’-tggtggttgtctggccttat-3’。通过对该引物pcr产物测序,验证了引物扩增的特异性(图1)。
(三)总rna提取与hsa_circ_0000705的rcr检测
1.将组织标本从-80℃超低温冰箱中取出,室温解冻。
2.从rnafixer非液氮型样品rna保存液取出组织块,用滤纸吸干后,多位点剪取50mg~100mg组织,置于2ml无rnase离心管中,加入trizol试剂(美国invitrogen)1ml,用手持式匀浆器充分匀浆至无可见固体后,室温静置10min。
3.三氯甲烷提取:加入0.2ml三氯甲烷,漩涡振荡10秒,室温下静置5分钟后,4℃下,12000rpm离心15分钟,吸取上层水相(宁少勿滥原则,一般可取到400μl)移入一新无rnase离心管中。
4.异丙醇沉淀:在上一步无rnase离心管中加入与所述上层水相等体积的异丙醇,混匀,4℃条件下静置20分钟后,4℃下12000rpm离心10分钟,弃上清得沉淀。
5.75%乙醇洗涤:在上述沉淀中加入质量分数为75%的乙醇1ml(-20度预冷),颠倒数次,4℃下12000rpm离心5分钟,弃上清,再用75%乙醇重复洗涤一次,4℃下12000rpm离心5分钟,弃上清。
6.干燥rna:上一步弃上清后,再次4℃下12000rpm离心1分钟,可见管壁残余液体汇集于管底,用100μl移液器缓慢吸除残余液体后,见一针尖大小半透明白色rna沉淀,室温条件下干燥1分钟,加10μl无rnase水溶解,反复吹打,得到rna提取液,-80℃保存备用。
7.rna逆转录:用goscript逆转录(reversetranscription,rt)试剂盒(购于美国promega公司)对上一步的rna提取液进行逆转录反应,得到cdna溶液,置-20℃保存备用,具体操作依该试剂盒说明书进行:在0.5ml离心管中加入9.5μlrna提取液、1μlrandomprimers、1μlpcrnucleotidemix、2μlmgcl2、1μlreversetranscriptase、4μlreactionbuffer和0.5μlribonucleaseinhibitor;然后在25℃保温5分钟,42℃1小时,再在70℃保温15分钟,加入80μl无rnase水,就得到cdna溶液。
8.pcr检测:用
(四)hsa_circ_0000705表达水平的计算
与hsa_circ_0000705检测方法基本相同,所不同的只是将扩增的上下游引物由gapdh特异性扩增上下游引物代替hsa_circ_0000705,检测得到样本中gapdh表达水平的扩增曲线(图4)和解链曲线(图5),从扩增曲线可以得到所检测的二个标本的ct值分别为29.87和26.25;从解链曲线中可以了解到该曲线为较窄的单一峰,可以看出每个标本的gapdh均被特异性扩增,没有引物二聚体和杂带的干扰。本实施例样本cdna的ctgapdh值≤30,rna(即cdna)质量合格。所用的gapdh特异性扩增上下游引物序列为:上游序列为5’-acccactcctccacctttgac-3’;下游序列为5’-tgttgctgtagccaaattcgtt-3’。
利用同一标本中hsa_circ_0000705和gapdh的ct值,就可根据公式δct=ctcircrna-ctgapdh计算出该hsa_circ_0000705的δct值,根据δct值的大小就可判断该hsa_circ_0000705的相对表达水平;δct值小者,其对应circrna的表达水平高;而δct值大者,其对应circrna的表达水平低。
(五)胃癌组织hsa_circ_0000705表达情况验证分析
借助上述qrt-pcr技术,大样本验证hsa_circ_0000705在胃癌组织及其配对癌旁组织中表达情况,结果表明hsa_circ_0000705在79.2%胃癌患者癌组织中显著低表达(图6)。胃黏膜异型增生(gastricdysplasia,gd)是目前公认的胃癌前病变,具有明显的恶变倾向。为了揭示组织hsa_circ_0000705是否与胃癌前病变相关,通过qrt-pcr检测并比较了胃黏膜异型增生组织及其配对正常组织中hsa_circ_0000705的表达水平。结果显示,hsa_circ_0000705表达水平除了在胃癌组织明显减少外,在胃癌前病变阶段其表达就有了显著降低(图7)。结合临床病理资料,进一步分析了胃癌组织hsa_circ_0000705表达水平与胃癌临床病理因素的潜在关系。如表1显示,胃癌组织的hsa_circ_0000705表达水平与肿瘤阶段(p=0.024)、borrmann分型(p=0.005)、病理类型(p=0.045)和组织ca19-9表达(p=0.010)等密切相关。
表1胃癌组织hsa_circ_0000705表达水平(δct)与患者临床病理因素相关性分析
(六)不同组别患者hsa_circ_0000705表达情况分析
胃癌的发生是一个多阶段、多步骤并逐级演进的过程。为了揭示hsa_circ_0000705是否参与了胃癌的逐级演进过程,使用qrt-pcr技术检测并比较hsa_circ_0000705分子在健康人胃组织、良性胃病变(胃溃疡、胃炎)组织、胃癌前病变(异型增生)组织及各期胃癌组织中的水平及其变化规律(图8)。结果显示,hsa_circ_0000705表达水平除了在胃癌组织和癌前病变组织(异性增生组织)中有显著降低外,在胃良性病变(胃溃疡和胃炎)组织中并没有明显改变(图8),提示hsa_circ_0000705作为胃癌筛查标志物可能具有良好的特异性。通过构建受试者工作特征(roc)曲线进一步证明胃癌组织hsa_circ_0000705具有良好的敏感性与特异性(图9)。hsa_circ_0000705的roc曲线下面积为0.719(95%ci,0.648-0.791)(图9)。当其截断值为9.125,敏感性和特异性分别为64.58%和69.79%(均超过现有胃癌标志物cea、ca19-9水平)。
本实施例通过上述研究证明hsa_circ_0000705只在胃癌前病变(异型增生)组织及胃癌组织中低表达,具有极好的胃癌组织特异性和胃癌相关性,并且可通过qrt-pcr方法实现定量检测。
sequencelisting
<110>宁波大学医学院附属医院
<120>一种胃癌分子标志物hsa_circ_0000705及其应用
<130>1
<160>5
<170>patentinversion3.3
<210>1
<211>559
<212>dna
<213>人工序列
<400>1
gagtgtttctcaggagctatcagaaactatcctcaccatggtagccaattgcagtaatgt60
tatgaataaggccagacaaccaccacctggagttatgccaaaaggacgtcctcctagtgc120
tagcagcttagatgccatttctcctgttcaggtaaatgagtgctacatttgatacatctt180
catttgccatagatttggaatagaataagctcctatgtcattaataaattgtctgaattt240
attacattttagataactgcatgtctagcatccacttattttaaaggagatatgtaaata300
ggcattgtagttaacaatagattttatcatcaaatagaacgtgactctaagaggaaatat360
acagacaatttatttaggtaaatgaagagggtttctttttaaaatatgaattacgtagac420
tcttgagacataagcactgcctttgaacctgatgtgtcttgtttgtagcttcacgggcca480
agcaacagtgctagagcataacgacttgttataactggggctcttcagctctcaactgaa540
ctgctcttttaaaaacaag559
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
taactggggctcttcagctc20
<210>3
<211>20
<212>dna
<213>人工序列
<400>3
tggtggttgtctggccttat20
<210>4
<211>21
<212>dna
<213>人工序列
<400>4
acccactcctccacctttgac21
<210>5
<211>22
<212>dna
<213>人工序列
<400>5
tgttgctgtagccaaattcgtt22
- 还没有人留言评论。精彩留言会获得点赞!