利用1‑氰基环己基乙酸直接合成加巴喷丁的方法与流程
(一)技术领域
本发明涉及一种加巴喷丁的合成工艺,即1-(氨甲基)环己基乙酸的合成工艺,特别涉及一种用1-氰基环己基乙酸直接合成加巴喷丁的方法,属于药物合成的技术领域。
(二)
背景技术:
加巴喷丁(gabapentin),商品名为neurontin,化学名为1-(氨甲基)环己基乙酸,结构与γ-氨基丁酸(gaba)类似,最早由美国的warner-lambert公司研制开发,并于1993年首次在英国上市。加巴喷丁是新一代的抗癫痫药物,同时也适用于各种类型的神经痛,具有不良反应轻微且持续时间短,不经肝代谢等特点。自其上市以来,销售额连续上升,在抗癫痫药市场中占有较大份额。
由于加巴喷丁含有一个环己烷基的结构,因此,在现有的报道中加巴喷丁的合成多以环己烷化合物为起始原料,其他的还有苯甲腈等。然而目前,这些途径多为化学合成途径,均存在一定的缺陷。
在us20030009055中以环己酮为原料,在氢氧化钾,乙腈中55℃加热回流7h,加水溶解,分层干燥后得到环己基乙腈。环己基乙腈在含有dmso,碳酸钾和硝基甲烷的环境中加热,获得1-硝甲基环己基乙腈,溶于乙醇,通过pd/c催化加氢,得到3-氨基-2-氮杂螺[4.5]癸烷-2-醇。之后在氢氧化钠溶液中加热回流,加入盐酸调节ph,低温析出2-羟基-2-氮杂螺[4.5]癸烷-3-酮,后溶于甲醇,通过雷尼镍催化加氢,干燥后,在盐酸中加热回流,冷却后用二氯甲烷萃取干燥。经离子交换获得加巴喷丁。该方法需要使用具有一定毒性和爆炸性的硝基甲烷,而且需要经过两次催化加氢对设备要求较高。
在us68469508中,利用1,1-环己基-二乙酸为原料,在乙酸酐和乙酸铵的混合液中,高温反应,调节不同的ph值,在利用叔丁醇萃取,之后与氢氧化钠/次氯酸钠反应,盐酸水解,再经过二环乙胺碱化,甲醇、异丙醇重结晶得到加巴喷丁精品。其中二环乙胺处理后可用氢氧化钠吸附氯离子回收二环乙胺循环利用。该法采用乙酸酐和乙酸铵的混合物,一步得到内酰胺,而且对二环乙胺进行了回收再利用,但整体收率较低,其中的一些步骤对设备的要求高,工艺仍较为繁琐。
在ep0414262和us5132451中1-氰基环己基乙腈在乙醇,甲苯,氯化氢的环境下反应,通过移除多余气体,调节ph,水洗,再以甲苯作为相转移试剂,后与甲醇,氢氧化钠溶液反应,调节ph,低温结晶得到1-氰基环己基乙酸。1-氰基环己基乙酸在碱性条件下,通过雷尼镍催化加氢,加入冰乙酸调节ph至中性,以四氢呋喃结晶得到加巴喷丁粗品,再以甲醇、水和异丙醇重结晶得到加巴喷丁精品。该方法的原料使用量大,废物排量大,收率较低。
在上述路径中由于其环境友好性差(消耗大量的hcl气体,甲醇,甲苯,氢氧化钠,水等试剂),收率低(收率最高达61.62%),经济性较低,因而限制了其工业化应用。因此,在此路线上我们对其进行了改进。由于生物催化则具有反应条件温和,具有良好的选择性,催化效率高等优点。因此需要筛选出能够特异选择性催化1-氰基环己基乙腈且高酶活的腈水解酶。
此前在本实验室发表的一篇论文中报道(processbiochemistry49(2014),2141-2148)利用纯酶催化1-氰基环己基乙腈生产1-氰基环己基乙酸。然而纯酶催化存在明显的弊端:稳定性差、需要繁琐复杂的纯化过程、酶催化剂不易回收等等。因此,为了适用于工业化生产,我们决定利用含腈水解酶的静息细胞催化1-氰基环己基乙腈生产1-氰基环己基乙酸,这在我们实验室发表的另外的一项专利(cn104212850a)和论文(catalysiscommunications66(2015),121-125)均有详细的报道。
在利用含腈水解酶的静息细胞催化1-氰基环己基乙腈生成1-氰基环己基乙酸的过程中,由于静息细胞的破碎,导致大量的蛋白质及有机大分子释放到胞外,这对于下一步的催化加氢反应是不利的,这是由于蛋白质等大分子物质会使得加氢催化剂中毒。此外利用静息细胞作为催化剂催化1-氰基环己基乙腈时,在经过一批反应后,酶活力迅速衰减,无法重复使用。因此经过后续改进,采用固定化技术对细胞进行固定化,这在本实验室发表的另外一项专利(cn10491225a)中有详细的报道。采用固定化技术可以极大的增强酶的稳定性,增强机械强度,保证细胞的完整性,重复利用等。
在xue等人发表的论文和专利cn10491225a中均有报道利用由静息细胞或者固定化细胞催化1-氰基环己基乙腈合成关键中间体1-氰基环己基乙酸,通过雷尼镍催化加氢合成加巴喷丁内酰胺。加巴喷丁内酰胺在盐酸的作用下水解,碳酸钠溶液调节ph,中和过多的氯离子,经异丙醇重结晶后得到加巴喷丁精品。该方法以酶法催化和化学催化相结合,反应条件温和,特异选择性高,环境友好,整体收率较高,步骤简短。
目前,多数学者采用化学法合成加巴喷丁,需要使用大量的试剂,条件步骤冗长、繁琐;而之前xue等人采用化学-酶法合成加巴喷丁需要通过酶法催化,直接加氢和化学水解三个主要步骤,步骤仍较为繁琐。
因此通过对比研究发现,前人对于直接一步加氢催化合成加巴喷丁并未有大量研究,而且之前采用的工艺是将1-氰基环己基乙酸直接加氢合成环化物,再水解得到加巴喷丁。因此研究开发一种只经过一步加氢技能合成加巴喷丁的技术具有极大的意义。此外,需要设计产品的提纯工艺和中间产物的循环利用工艺,从而实现完全转化。本发明正是对于一步加氢催化合成加巴喷丁以及加巴喷丁的提纯和1-氰基环己基乙酸的循环利用这一思路展开了研究。
(三)
技术实现要素:
本发明目的是提供一种通过1-氰基环己基乙酸的直接催化加氢生成加巴喷丁的制备方法,即通过对含有1-氰基环己基乙酸的酶催化转化液进行直接加氢生产加巴喷丁,以及通过离子交换分离加氢转化液中的加巴喷丁和1-氰基环己基乙酸,并对分离出来的1-氰基环己基乙酸进行循环利用的方法。
本发明采用的技术方案是:
本发明提供一种利用1-氰基环己基乙酸直接合成加巴喷丁的方法(工艺流程如图1),所述方法为:(1)转化液:将腈水解酶基因工程菌固定化细胞分散于去离子水中,加入1-氰基环己基乙腈,在20-50℃、10-350rpm条件下搅拌反应完全后(优选35℃,200rpm下搅拌反应8h),抽滤,获得滤饼a和含1-氰基环己基乙酸的滤液a;滤饼a为回收固定化细胞;所述腈水解酶基因工程菌固定化细胞是将seqidno.1所示腈水解酶基因构建的工程菌以硅藻土为载体制备获得的(具体制备方法参照专利申请cn104911225a实施例1,腈水解酶基因同cn104911225a中seqidno.1所示);所述1-氰基环己基乙腈与固定化细胞质量比为1:1.0-1.1,所述去离子水的体积用量以1-氰基环己基乙腈质量计为6.5-7.0ml/g;(2)加巴喷丁的合成:取步骤(1)滤液a至加氢反应釜中,加入催化剂和助剂,通入氢气,于20-150℃、300-1100rpm条件下反应(优选以10℃幅度逐步升温模式进行反应,每次升温后通入氢气反应12h,再排除氢气,优选反应温度为30-80℃),反应完全后将反应液冷却至30-80℃(优选60℃),排空氢气,过滤,获得滤液b和滤饼b,滤饼b为回收催化剂;所述催化剂为雷尼镍、铑碳(铑质量负载量5%)或钯炭(钯质量负载量10%)(优选雷尼镍),所述助剂有机酸、无机酸、无机碱或有机碱,更优选为甲酸、乙酸、甲酸铵或三乙胺中的一种或多种;所述催化剂与滤液a中1-氰基环己基乙酸质量比为0.1-1:1,所述助剂用量以滤液a体积计为0.5-2.5%(优选1-2%);(3)分离纯化:将步骤(2)获得的滤液b冷却后调节ph值至4.0-5.0,上样过阳离子交换树脂,首先以蒸馏水洗涤,收集ph为3.0-6.0范围内的流出液a为含有1-氰基环己基乙酸的洗出液;再以体积浓度15%的氨水溶液为洗脱液,收集ph为7.5-13.0范围内的流出液b;流出液b减压浓缩至原体积的1/10,获得浓缩液a,浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至原体积的1/6-1/5,获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,收集晶体干燥,得到加巴喷丁;流出液a回收循环利用。
进一步,步骤(2)所述助剂为甲酸和三乙胺以体积比0.1-3.6:1的混合或者2m乙酸水溶液与三乙胺以体积比0.1-3.6:1的混合。
进一步,步骤(3)所述阳离子交换树脂为001×7型强酸性阳离子交换树脂,购买自宁波争光树脂厂,其他型号的阳离子交换树脂也在本发明的保护范围内。
进一步,步骤(2)所述反应以升温幅度10℃的梯度逐步升温至80℃,每次升温后通入氢气反应12h,然后排出气体,通入氢气量为0-2mpa(优选0.5-1.0mpa)。
进一步,步骤(2)所述反应在40℃,500rpm下反应12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气,升温至60℃通入氢气反应12h,排除氢气后,将反应液过滤,获得滤液b和滤饼b。
进一步,步骤(3)所述流出液b在50℃下浓缩至原来体积的1/10,获得的浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至原体积的1/6-1/5,获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁。
本发明所述催化剂铑碳的铑质量负载量为5%;钯炭中钯质量负载量为10%。所述雷尼镍购买自大连通用化工有限公司,其他型号的雷尼镍也在本发明的保护范围内;钯炭(钯负载量为10%)购买自上海麦克林生化科技有限公司,其他型号的钯炭也在本发明的保护范围内。
本发明步骤(3)中流出液a(即含1-氰基环己基乙酸的溶液)的循环利用可采用直接加氢反应,也可采用与步骤(1)的滤液a(即固定化细胞催化后的1-氰基环己基乙酸转化液)混合后再进行直接加氢反应,更优选采用与固定化细胞催化的1-氰基环己基乙酸转化液混合后再加氢。
本发明所述滤液a和滤液b,滤饼a和滤饼b均为不同步骤过滤所得滤液和滤饼,所述流出液a和流出液b为不同洗脱液获得的流出液,浓缩液a和浓缩液b均指浓缩液,字母本身没有含义。
与现有技术相比,本发明有益效果主要体现在:
原子经济性好,采用生物催化与化学催化相结合生产加巴喷丁,其中在催化加氢步骤中能够将固定化细胞催化后的反应液直接用于加氢反应生成产物加巴喷丁,因此避免提纯1-氰基环己基乙酸,且利用水作为介质,利于回收循环利用,减少污染。而且通过助剂的添加和升温策略的改变,可直接催化1-氰基环己基乙酸一步合成加巴喷丁,在最优条件下,反应一个批次加巴喷丁收率达53.3%;利用离子交换法对加巴喷丁与1-氰基环己基乙酸进行分离,可将未反应完的1-氰基环己基乙酸回收循环利用于二次加氢反应,实现中间产物的完全转化,通过过对1-氰基环己基乙酸的回收并进行加氢反应,经过5次循环后,使得加巴喷丁收率达到80%以上,比已报道的化学工艺提高了近20%(ep0414262)。
(四)附图说明
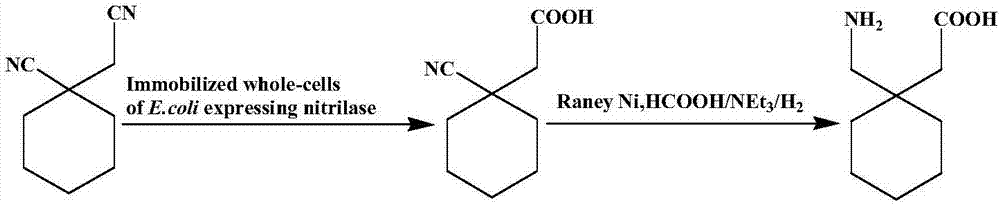
图1从1-氰基环己基乙腈选择性水解、直接加氢一步合成加巴喷丁的路径图。
图2为化学-酶法合成加巴喷丁的工艺流程图。
图3为不同的升温策略对于1-氰基环己基乙酸在该体系中直接加氢生成加巴喷丁的反应曲线图,a:实施例2梯度升温;b:实施例8恒温60℃。
图4为1-氰基环己基乙酸经过回收循环利用后多批次反应柱状图。
(五)具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
lb液体培养基:酵母粉5g/l,蛋白胨10g/l,nacl10g/l,溶剂为去离子水,ph值自然。
发酵培养基:蛋白胨15g/l,酵母粉12g/l,nacl10g/l,甘油12g/l,(nh4)2so45g/l,kh2po41.36g/l,k2hpo4·3h2o2.28g/l,mgso4·7h2o0.375g/l,溶剂为去离子水,ph值自然。
加巴喷丁与1-氰基环己基乙酸的hplc检测条件:色谱柱welchromc18柱(5μm×250mm×4.6mm);流动相:缓冲液(5mmnh4h2po4/13mmnaclo4·h2o,高氯酸调节ph至1.8):乙腈=76:24,v/v;柱温:40℃;波长:215nm;流速1ml/min。
实施例1:一种化学-酶法合成加巴喷丁的方法,步骤如下:
(1)种子液的制备:将实验室之前已构建好的含腈水解酶基因(seqidno.1)的工程菌e.colibl21(de3)/pet28b(+)-f168v(同专利申请cn104911225a实施例1)接种于含有终浓度5g/l卡那霉素的lb平板培养基,于37℃条件下过夜培养,挑取单菌落接种于100ml含有终浓度5g/l卡那霉素的lb液体培养基中,与37℃,150rpm下过夜培养,获得种子液。
(2)发酵培养:接种种子液于含有终浓度5g/l卡那霉素的3l发酵培养基的5l发酵罐中,接种量为3%(v/v),调节通气比为1.3vvm,在37℃,500rpm条件下进行发酵培养,发酵过程流加体积浓度8%的氨水和体积浓度10%的磷酸水溶液以维持发酵液ph在6.5左右,培养4h后,降温至28℃,加入乳糖诱导,乳糖终浓度为12.5g/l(m/v),培养10h,停止发酵,放罐获得发酵液。于8000rpm离心10min,弃上清,收集获得湿菌体。
(3)固定化细胞的制备:取20g湿菌体完全悬浮于200ml蒸馏水中,添加1.2g硅藻土在磁力搅拌器搅拌1h,后加入6ml的体积浓度5%的聚乙烯亚胺水溶液搅拌1h,添加2ml的体积浓度25%戊二醛水溶液搅拌30min后抽滤,蒸馏水洗2-3次,滤饼即为固定化细胞,称重得31.44g。
(4)中间产物1-氰基环己基乙酸的合成:取15.72g固定化细胞于100ml去离子水中,搅拌使其分散均匀后加入14.8g1-氰基环己基乙腈,在35℃,200rpm下搅拌反应8h后,抽滤,获得滤液a和滤饼a。滤液a(hplc检测1-氰基环己基乙酸浓度为1mm)用于下一步的催化加氢,滤饼a为固定化细胞,用于下一个批次的酶催化反应。
(5)加巴喷丁的合成:取用蒸馏水稀释4倍后的步骤(4)滤液a(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0graneyni(购自大连通用化工有限公司),加入1ml(98%)三乙胺和0.5ml(98%)甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h。排除反应釜内的气体后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。
(6)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b200ml在50℃下浓缩至20ml,获得浓缩液a,再加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至10ml,获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到50%。流出液a(即未吸附在阳离子交换树脂上的物质)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
剩余1-氰基环己基乙酸的循环利用:经过hplc检测,流出液a中1-氰基环己基乙酸未发生较大改变以及未引入其他杂质。并与上述固定化细胞催化转化液(即步骤(4)滤液a)混合后浓度为215.6mm,按照上述加巴喷丁合成体系进行二次加氢。在对1-氰基环己基乙酸进行5次循环利用之后,加巴喷丁收率达到80%以上(1-氰基环己基乙酸的回收利用如图4)。
实验例2:含1-氰基环己基乙酸的固定化细胞催化的转化液直接加氢生产加巴喷丁
(1)加巴喷丁的合成:取实施例1中步骤(4)的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0graneyni,加入1ml98%三乙胺和0.5ml98%甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于30℃,500rpm下保留12h后排除氢气,升温至40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h,通入氢气于70℃,500rpm下保留12h后排除氢气,升温至80℃后再通入氢气,保留12h后排除氢气后,反应液降温至60℃后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。反应进程见图3中a所示。
(2)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b200ml在50℃下浓缩至20ml,获得的浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至10ml,获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到48%。流出液a(即未吸附在阳离子交换树脂上的物质)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
实验例3:含1-氰基环己基乙酸的固定化细胞催化的转化液直接加氢生产加巴喷丁
(1)加巴喷丁的合成:取实施例1步骤(4)中的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0gpd/c(pd质量负载量10%),1ml98%三乙胺和0.5ml98%甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h。排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。
(2)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b300ml在50℃下浓缩至30ml,获得浓缩液a,取浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至15ml,将获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到84%,但同时约有10%加巴喷丁内酰胺。流出液a(即未吸附在阳离子交换树脂上的溶液)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
结果表明,pd/c具有更佳的催化活力,但同时催化选择性略低于raneyni。
实验例4:含1-氰基环己基乙酸的固定化细胞催化的转化液直接加氢生产加巴喷丁。
(1)加巴喷丁的合成:取实施例1步骤(4)中的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0graneyni,加入1.07ml98%三乙胺和0.43ml98%甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h,排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。
(2)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b200ml在50℃下浓缩至20ml,获得浓缩液a,将浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至10ml,将获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到60%。流出液a(即未吸附在阳离子交换树脂上的溶液)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
结果表明,助剂中酸和碱的比例影响1-氰基环己基乙酸在该体系中加巴喷丁的合成,最合适体积比例为1:2。
实施例5:含1-氰基环己基乙酸的固定化细胞催化的转化液直接加氢生产加巴喷丁。
(1)加巴喷丁的合成:取实施例1中步骤(4)的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0gpd/c(pd质量负载量10%),加入1ml98%三乙胺和0.5ml甲酸。通入氮气置换空气,置换3次,不通入氢气,直接在40℃,500rpm下保留12h,升温至50℃保留12h,后再升温至60℃保留12h,排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。
(2)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b200ml在50℃下浓缩至20ml,获得浓缩液a,再加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至10ml,获得的浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到37.2%。流出液a(即未吸附在阳离子交换树脂上的物质)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
结果表明,在该体系中,即使没有氢气作为氢供体,pd/c依然能够催化部分1-氰基环己基乙酸加氢合成加巴喷丁,这是由于甲酸可以作为氢供体。
实施例6:含1-氰基环己基乙酸的固定化细胞催化转化液直接加氢合成加巴喷丁
(1)加巴喷丁的合成:取实施例1中步骤(4)的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0graneyni,加入0.715ml98%三乙胺和0.285ml甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h,排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。
(2)加巴喷丁的提纯:取上述滤液b加入提前配制好的2mol/l甲酸水溶液调节ph至5.0左右;通过001×7型强酸性阳离子交换树脂(购买自宁波争光树脂厂)吸附,完全吸附之后首先用蒸馏水洗涤,收集ph值在3.0-6.0范围内的流出液a,再用体积浓度为15%的氨水洗脱,收集ph值在7.5-13.0范围内的流出液b(即获得含有加巴喷丁的洗脱液)。流出液b200ml在50℃下浓缩至20ml,获得的浓缩液a加入2倍体积的异丙醇静置1h后再次在50℃下浓缩至10ml,获得浓缩液b加入2-5倍体积的异丙醇冰浴搅拌后在0-4℃下冷却静置,有白色晶体析出,抽滤后滤饼烘干即为加巴喷丁,质量收率达到50.6%。流出液a(即未吸附在阳离子交换树脂上的物质)为含有1-氰基环己基乙酸的转化液,回收用于二次加氢使用。
结果表明,减少甲酸和三乙胺的加入量,对于加巴喷丁的积累具有一定的抑制。
实施例7:含1-氰基环己基乙酸的固定化细胞催化转化液直接加氢生成加巴喷丁
加巴喷丁的合成:取实施例1中步骤(4)的含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜中,加入约1.0graneyni,加入1.0ml98%三乙胺和3.5ml2m的乙酸水溶液;通入氮气置换空气,置换3次后,通入1mpa氢气于40℃,500rpm下保留12h后排除氢气,升温至50℃后再通入氢气,保留12h后排除氢气后,升温至60℃通入氢气后,保留12h,排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。对滤液b进行hplc检测,加巴喷丁收率达到81.6%。
实施例8:含1-氰基环己基乙酸的固定化细胞催化转化液直接加氢生成加巴喷丁
(1)加巴喷丁合成:取实施例1中步骤(4)含1-氰基环己基乙酸的固定化细胞催化的滤液a用蒸馏水稀释4倍后(1-氰基环己基乙酸浓度为250mm)100ml至加氢反应釜,加入约1.0graneyni,加入0.715ml98%三乙胺和0.285ml甲酸;通入氮气置换空气,置换3次后,通入1mpa氢气于60℃,500rpm下反应24h,排除氢气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b冷却至室温。利用hplc检测滤液b,结果显示反应液中只有少量的加巴喷丁生成,大部分产物为加巴喷丁内酰胺,底物转化率只有61.5%。反应进程见图3中b所示。
结果表明,在某一温度下进行恒温催化不利于加巴喷丁在该加氢体系中积累。
实施例9:含1-氰基环己基乙酸晶体直接加氢生成加巴喷丁
(1)1-氰基环己基乙酸晶体的提纯:取实施例1中步骤(4)含1-氰基环己基乙酸的固定化细胞催化的滤液100ml(1-氰基环己基乙酸浓度为250mm)与0.6g活性炭混合后在60℃条件下搅拌1h,待混合液降温至室温后,抽滤,滤液用2mhcl溶液调节ph至2.0,此时有大量晶体析出,抽滤即可获得1-氰基环己基乙酸晶体,在50℃过夜烘干,即可获得干燥的1-氰基环己基乙酸晶体。
(2)加巴喷丁合成:取14.5g1-氰基环己基乙酸晶体溶于70ml甲醇,之后加入1grh/c(rh质量负载量为5%);通入氮气置换空气,置换3次后,通入0.5mpa氢气于室温下,反应2h,排气后,将反应液过滤,获得滤液b和滤饼b,滤饼b为回收催化剂,滤液b即为加氢反应液,经hplc检测,发现只有少量的加巴喷丁生成,转化率极低。
结果表明,rh/c在催化溶于甲醇的1-氰基环己基乙酸生成加巴喷丁时,催化活性低,无法达到工业化生产的要求。
- 还没有人留言评论。精彩留言会获得点赞!