AntiMUC1CAR‑T细胞及其制备方法和应用与流程
本发明涉及一种antimuc1car-t细胞及其制备方法和应用,属于基因修饰细胞及肿瘤治疗技术领域。
背景技术:
在肿瘤免疫治疗方法中,淋巴细胞免疫技术包括细胞因子诱导杀伤细胞、细胞毒性t淋巴细胞和浸润性t淋巴细胞等在国内外已经用于临床治疗恶性肿瘤,并取得一些临床疗效,但其为非特异性免疫作用,由于肿瘤细胞本身免疫逃逸和抗原隐蔽性,其对体内肿瘤细胞清除还非常有限。嵌合抗原受体基因修饰淋巴细胞技术的出现为临床治疗癌症提供了新的方向。嵌合抗原受体t细胞(chimericantigenreceptortcell,简称:car-tcell)疗法是通过提取患者体内t淋巴细胞,经过体外10至14天的培养改造,通过载体整合进入到正常t细胞基因序列,形成嵌合抗原受体t细胞(car-t)。被重新编码的t细胞就能获得特异性识别和攻击杀伤肿瘤细胞的能力,能精确杀伤肿瘤细胞,但又不会伤及正常细胞。由于是诱导、激活自体细胞,因此该疗法没有通常放、化疗的毒副反应,也没有传统治疗中出现的耐药性。
嵌合抗原受体(chimericantigenreceptor,简称:car)主要由两部分构成,一端位于细胞外,能够特异性识别癌细胞表面的某一抗原;另一端位于细胞内,含有信号激活元件(如t细胞受体的zeta链),起传递信号激活t细胞的作用。这样表达car的t淋巴细胞(car-t细胞)就能避免t细胞受体识别靶细胞的限制,从而起到靶向癌细胞的的杀伤作用。目前,car-t治疗的临床试验正在迅速增长,其中大部分是对b细胞恶性肿瘤治疗的评估。不同的临床试验所采用的cd19car-t细胞都报道了显著的效果,复发性或难治性淋巴细胞白血病的治疗能达到60-90%的反应率,一部分患者达到持续的缓解,最长的达到2年,这种免疫治疗已经给一些患者带来了前所未有的效果。除了血液系统肿瘤外,研究者们一直在努力将car-t治疗扩展到实体瘤,但是,car-t治疗实体瘤还处于早期阶段,还有许多问题需要解决。
mucin1是膜结合型粘蛋白家族成员,简称muc1。在正常情况下,muc1呈低水平表达在乳腺,胰腺,胃肠道,呼吸道及泌尿生殖道的上皮细胞的近管腔面,不能被机体免疫系统识别,其表达特点为极性表达,顶端分布,糖基化丰富。在大多数腺癌、血液系恶性肿瘤中muc1呈异常过表达,可通过调控多个信号通路调节细胞恶性转化,是促进肿瘤发生与发展的重要癌基因。由于muc1在肿瘤细胞中的表达糖基化不全,并失去极性,遍布于整个细胞表面,容易被抗体识别,因此,muc1蛋白可作为car-t细胞抗肿瘤治疗的一个理想靶点。
技术实现要素:
本发明提供一种antimuc1car-t细胞及其制备方法和应用,该细胞经过t细胞修饰和改造得到,并且能够特异性识别和杀伤腺癌、血液系恶性肿瘤,适用于相应肿瘤疾病的预防和治疗。
本发明提供一种antimuc1car-t细胞,所述antimuc1car-t细胞在t细胞内表达scfv–igd–cd28–ox40–cd3ζ融合蛋白;所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述scfv用于结合所述muc1蛋白,并且所述scfv的氨基酸序列为第一序列,所述第一序列为:
evqlqqsggglvqpggsmklscvaskftfsnywmnwvrqspekglewvaeirlksnnyathyaesvkgrftisrddskssvylqmnnlraedtgiyyctfgnsfaywgqgttvtvssggggsggggsggggsdivvtqesalttspgetvtltcrsstgavttsnysnwvqekpdhlftgliggtnnrapgvparfsgskigdkaaltitgaqtedeaiyfcalwesnhwvfgggtkltvlgse
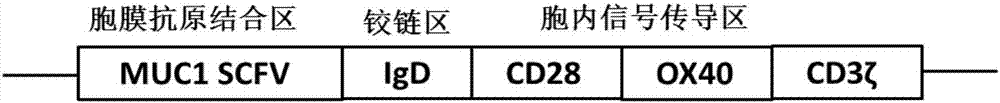
该antimuc1car-t细胞以muc1为靶点,具体地,所述antimuc1car-t细胞的嵌合抗原受体car包括胞膜外抗原结合区、铰链区和胞内信号传导区,所述胞膜外抗原结合区为scfv,所述铰链区为igd,所述胞内信号传导区为cd28–ox40–cd3ζ。图1为本发明的antimuc1car的设计示意图,请参考图1。
进一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述igd的氨基酸序列为第二序列。
具体地,第二序列为:
tftcfvvgsdlkdahltwevagkvptggveegllerhsngsqsqhsrltlprslwnagtsvtctlahpslppqrlmalrepaaqapvklstnllassdppeaa
进一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述cd28的氨基酸序列为第三序列。
具体地,第三序列为:
fwvlvvvggvlacysllvtvafiifwvrskrsallhsdymnmtprrpgptrkhyqpyapprdfaayrs
进一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,所述ox40的氨基酸序列为第四序列,所述cd3ζ的氨基酸序列为第五序列。
具体地,第四序列为:
rrdqrlppdshkppgggsfrtpiqeeqadahstlaki
具体地,第五序列为:
rvkfsrsaeppayqqgqnqlynelnlgrseeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
进一步地,所述scfv–igd–cd28–ox40–cd3ζ融合蛋白中,
所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的氨基酸序列为第六序列。
具体地,第六序列为:
evqlvqsgaevkkpgesltisckasgysfpnywitwvrqmsggglewmgridpgdsyttynpsfqghvtisidkstntaylhwnslkasdtamyycaryyvslvdiwgqgtlvtvssggggsggggsggggsqsvltqpasvsgspgqsitisctgtsskvggynyvswyqqhpgkapklmiydvnnrpsevsnrfsgsksgntasltisglqaedeadyykssyttgsravfgggtkltvlgtftcfvvgsdlkdahltwevagkvptggveegllerhsngsqsqhsrltlpralwnagtsvtctlnhpslppqrlmalrepaaqapvklslnllassdppeaafwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrrdqrlppdahkppgggsfrtpiqeeqadahstlakirvkfsrsaeppakqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
进一步地,所述antimuc1car-t细胞通过慢病毒感染t淋巴细胞获得,所述慢病毒通过携带有所述scfv–igd–cd28–ox40–cd3ζ融合蛋白的慢病毒表达载体感染293t细胞得到。
本发明还提供一种上述任一所述的antimuc1car-t细胞的制备方法,包括如下步骤:
1)构建慢病毒表达载体,所述慢病毒表达载体具有所述scfv–igd–cd28–ox40–cd3ζ融合蛋白;
2)利用慢病毒包装质粒和所述慢病毒表达载体感染293t细胞,获得慢病毒,所述慢病毒被所述scfv–igd–cd28–ox40–cd3ζ融合蛋白包装;
3)分离t淋巴细胞,并用所述慢病毒感染所述t淋巴细胞,获得所述antimuc1car-t细胞,所述antimuc1car-t细胞的t细胞内表达所述scfv–igd–cd28–ox40–cd3ζ融合蛋白。
在步骤1)中,通过基因工程手段,将scfv–igd–cd28–ox40–cd3ζ融合蛋白基因克隆到慢病毒表达载体上,从而完成对慢病毒表达载体的构建。在步骤2)中,利用步骤1)所得的慢病毒表达载体对293t细胞感染,获得被scfv–igd–cd28–ox40–cd3ζ融合蛋白包装的慢病毒。在步骤3)中,将步骤2)中的慢病毒表达于人外周血中分离收集的t淋巴细胞以获得car-t细胞。
进一步地,在所述步骤1)之前,还包括合成和扩增所述scfv–igd–cd28–ox40–cd3ζ融合蛋白基因。具体合成和扩增方法可按照本领域常规技术手段获得。
进一步地,还包括对所述慢病毒进行纯化,并用所述纯化后的慢病毒感染所述t淋巴细胞。一般的,该纯化手段可以使用本领域常规手段进行,例如过滤、超滤等。
本发明还提供了上述任一所述的antimuc1car-t细胞在制备治疗腺癌药物中的应用,尤其能够用于muc1分子高表达的肿瘤的治疗。
本发明方案具有以下优点:
1、本发明的antimuc1car-t细胞将muc1抗体用于car-t细胞的构建,能够对muc1蛋白进行有效结合。
2、本发明提供的antimuc1car-t细胞制备方法能简单、有效的制备具有特异性识别和杀伤肿瘤的antimuc1car-t细胞。
3、本发明的antimuc1car-t细胞具有高效的肿瘤杀伤活性,能够用于制备治疗肿瘤药物中,尤其能够以muc1分子为靶抗原,用于muc1分子高表达肿瘤的治疗。
附图说明
图1为本发明的antimuc1car的设计示意图;
图2为本发明实施例的antimuc1car-t细胞以及未感染的t细胞对靶细胞mcf-7(乳腺癌)的杀伤效果示意图;
图3为本发明实施例的antimuc1car-t细胞以及未感染的t细胞对靶细胞bxpc-3(胰腺癌)的杀伤效果示意图;
图4为本发明实施例的antimuc1car-t细胞、对照例以及空白例对治疗乳腺癌(mcf-7)移植瘤模型小鼠后的小鼠生存期示意图。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明的实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
本发明antimuc1car-t细胞的制备
1、构建慢病毒表达载体
通过常规的基因工程手段,合成scfv–igd–cd28–ox40–cd3ζ融合蛋白基因序列,将scfv–igd–cd28–ox40–cd3ζ融合蛋白基因序列克隆到慢病毒表达载体上,获得scfv–igd–cd28–ox40–cd3ζ慢病毒表达载体pgreenpuro-car。其中,scfv–igd–cd28–ox40–cd3ζ融合蛋白的各序列如前所述。
2、慢病毒包装
1)用质量分数为10wt%胎牛血清(fetalbovineserum,简称:fbs)的1640培养基培养293t细胞;
2)将293t细胞以3x105/cm2的密度传至直径15cm的培养皿中培养20h,保证转染时细胞汇合度为80-90%;
用不含血清的1640培养基换液,备用;
3)取两个ep管,分别在两个ep管中加入1ml1640,将慢病毒载体pgreenpuro-car与pmdlgprre、prsv-rev和pmd2.g质粒按照摩尔比1:1:1:1于其中一个ep管中混匀;在另一个ep管中加入150ullipo2000,混匀放置5min;将混有lipo2000的1640加入含有质粒的ep管中,混匀得混合液,室温放置20min,然后将混合液逐滴加入上述2)中制备的细胞培养皿中,继续培养4h后,用含10%fbs的1640培养基更换培养液,继续培养48h后收集细胞上清液,获得被scfv–igd–cd28–ox40–cd3ζ融合蛋白包装的慢病毒。
3、慢病毒纯化
将2中获得的被包装的慢病毒用0.22μm过滤膜过滤,滤液收集在50ml超滤管中,以3000g/min的速度离心45min;将剩余的上层病毒浓缩液转移至ep管,放-80℃保存备用。
4、cd8+t细胞的分离
1)全血倒入50ml离心管,室温离心20分钟,控制离心力ref为700g(普通离心);
2)取上述离心下部细胞成分,加杜氏磷酸盐缓冲液dpbs至50ml;
3)分别取25ml上述液体加到20ml人淋巴细胞分离液,将离心管室温离心15分钟,控制离心力ref为800g;
5)取白膜层细胞,加入dpbs,补足至50ml;
6)离心10分钟,控制离心力ref为600g,弃上清液,得外周血单个细胞(peripheralbloodmononuclearcell,简称:pbmc);
7)采用cd8+t细胞磁珠分选试剂盒分选cd8+t细胞。
5、慢病毒载体感染t淋巴细胞
用质量分数为10wt%fbs的rpmi1640完全培养基培养cd8+t细胞,第一天加入抗cd3单克隆抗体活化;第三天加入150moi的3中纯化后的慢病毒(antimuc1car),16h后将培养基更换为含有50iu/ml重组人il-2的rpmi1640完全培养基,继续培养10-20天,得到antimuc1car-t细胞。
实施例2
对实施例1制备的antimuc1car-t细胞体外抗肿瘤效果进行评价,包括以下步骤:
以稳定表达muc1的乳腺癌细胞系mcf-7和胰腺癌细胞系bxpc-3作为靶细胞,分别用慢病毒载体pgreenpuro-car感染的t细胞(即,实施例1制得antimuc1car-t细胞)和未感染的t细胞制得效应细胞,将靶细胞按照密度1x105个/ml接种96孔板,每孔100μl,按照5:1,10:1,20:1效靶比将效应细胞加入靶细胞,置于5%co2,37℃培养箱培养4h,采用wst-1检测细胞活力,计算杀伤效率。
图2为本发明实施例的antimuc1car-t细胞以及未感染的t细胞对靶细胞mcf-7(乳腺癌)的杀伤效果示意图;图3为本发明实施例的antimuc1car-t细胞以及未感染的t细胞对靶细胞bxpc-3(胰腺癌)的杀伤效果示意图。
图2和图3结果表明,表达muc1car的t淋巴细胞对muc1阳性肿瘤细胞具有很强的杀伤作用。
实施例3
对实施例1制备的antimuc1car-t细胞体内抗肿瘤效果进行评价,包括以下步骤:
取6周龄雌裸鼠15只,右腋下皮下注射5x106mcf-7(乳腺癌)细胞,待肿瘤长到60mm3大小,肿瘤模型随机分成3组:对照组、antimuc1car-t细胞组、t细胞组;对照组尾静脉注射生理盐水200ul/次,每周2次;antimuc1car-t细胞组尾静脉注射antimuc1car-t细胞1×107个/次,每周2次;t细胞组尾静脉注射t细胞1×107个/次,每周2次;统计100天内小鼠生存状态,做生存率曲线。图4为本发明实施例的antimuc1car-t细胞、对照例以及空白例对治疗乳腺癌(mcf-7)移植瘤模型小鼠后的小鼠生存期示意图。
图4结果表明,antimuc1car-t细胞相对于未感染的t细胞以及空白例可延迟muc1高表达的乳腺癌移植瘤小鼠模型的生存期。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
- 还没有人留言评论。精彩留言会获得点赞!