一种具有抗炎效果的牛樟芝寡糖及其制备方法和用途与流程
本发明属于多糖的制备及其应用领域,具体涉及一种具有抗炎效果的牛樟芝寡糖及其制备方法和用途。
背景技术:
急性炎症反应,是机体应对病原相关化合物或自身局部组织损伤所调动的一系列免疫杀伤作用。当身体的某个部位受到有害刺激时,血液循环使白细胞向该受伤组织富集,产生炎症初级反应,然后血液系统、免疫系统和受伤组织内的各种细胞等一系列的生化作用使得炎症反应蔓延扩大。正常的炎症反应能有效地激活免疫系统,并且在消灭病原后快速消退。然而,剧烈的急性炎症若持续不断,严重时可危机生命。特殊器官或部位的急性炎症产生巨大影响,如脑或脑的炎症可压迫生命中枢,声带炎症阻塞喉部导致窒息,严重的心肌炎可以影响心脏功能,此时,抗炎症药物成为抑制炎症反应的重要途径。经典的合成类药物的消炎药(主要为抗生素)均不同程度地存在一定毒副作用,易造成肝肾损伤,产生明显耐药性。因此,开发出具有较少毒副作用或无毒副作用的具有抗炎作用的药物制剂或保健食品尤为重要。
牛樟芝,又名樟芝,属于担子门、担子菌类纲、非褶菌目、多孔菌科、薄孔菌属,拉丁名为antrodiacamphorata。在自然条件下,牛樟芝仅生长于中国台湾山区海拔450-2000米的树心腐朽或枯死倒伏的牛樟树潮湿表面,属于中国台湾特有稀少野生真菌。因樟芝具有解毒保肝、抗癌、强化免疫、抗过敏、降血脂等独特功效,在中国台湾民间素有“药芝之王”、“森林红宝石”的美誉。虽然牛樟芝广泛应用于中国台湾民间,具有许多疗效作用,但直至1995年才被中国台湾研究者们公开报道。牛樟芝具有许多的生理活性成分,包括多糖、三萜类化合物、脂肪酸类化合物等等。而其中牛樟芝多糖具有抗氧化、抗肿瘤、抗炎、调节免疫等多种活性,且本身具有毒副作用小的特点,在调节炎症反应方面具有重要的开发潜力。由于寡糖溶解度相对较高,吸收性能更好,粘度小等独特优势,理论上牛樟芝寡糖更具重要的开发价值。但是,目前并没有专门针对牛樟芝寡糖进行专门研究以拓展其应用。
技术实现要素:
本发明的一个目的在于提供一种具有抗炎作用的牛樟芝寡糖,本发明的另一个目的在于提供所述牛樟芝寡糖及其应用方法。
本发明首先提供了一种牛樟芝寡糖,所述牛樟芝寡糖的分子量范围为200da-5000da,所述牛樟芝寡糖的单糖组成包括:0.1%-2.0%阿拉伯糖,2%-6%葡萄糖,0.1%-2.0%岩藻糖,20%-30%半乳糖,60%-80%甘露糖。
作为上述牛樟芝寡糖一种更好的选择,依据毛细管电泳进行分析时,所述牛樟芝寡糖的分子量范围为400da-2000da,单糖组成为:0.5%阿拉伯糖,4%葡萄糖,0.5%岩藻糖,24%半乳糖,70%甘露糖。
所述单糖的组成分布为依据毛细管电泳获得。
作为上述牛樟芝寡糖一种更好的选择,制备所述牛樟芝寡糖的原料为牛樟芝。其可以选用在中国台湾自然条件下生长的牛樟芝子实体粉末,通过人工培养的于其他领域种植的牛樟芝也可以用于本发明的寡糖的制备。
所述牛樟芝寡糖可以以牛樟芝为原料制备,在以相当于其组成的各种单糖组成的混合物,经实验证实,其也可以起到类似的效果。
本发明还提供了制备所述牛樟芝寡糖的方法,包括:
提供牛樟芝粉末和水的混合液,并在高温下溶解抽提,所得的抽提液过滤得到滤液;从浓缩后的滤液中提取第一中间体,第一中间体经水解后得到牛樟芝寡糖。
作为上述方法一种更好的选择,所述抽提的温度为25-100摄氏度,抽提时间为1-12h。更优选的抽提温度为70-90摄氏度,更优选90摄氏度。
作为上述方法一种更好的选择,所述提取第一中间体的步骤为向滤液内加入单糖的不良溶剂至第一中间体析出,析出的第一中间体复溶后经萃取得到用于水解的第一中间体。
作为上述方法一种更好的选择,所述第一中间体经三氟乙酸水解,三氟乙酸浓度为0.5-3mol/l,可优选为1.25mol/l,其他可以用于降解的试剂还可以为盐酸、硫酸或者其他可以降解相应的糖但是不足以氧化多糖为其他成分的可以被人体接受的酸类。
作为上述方法一种更好的选择,水解后的第一中间体使用氨水中和,其他可中和的碱还包括氢氧化钠或氢氧化钾等,之后并经冷冻干燥得到产物。
在选择较强的碱或者较强的酸时,或者选择浓度较大的酸或者碱时,应当缓慢或者小心的加入,以避免其他副反应的发生。
在本发明中,所述的牛樟芝寡糖可按照如下方法制备:
(1)取一定质量牛樟芝子实体粉末,加入5-100倍重量的水混匀,在25-100℃条件下溶解抽提1-12h,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成6-10倍浓度的浓缩液;
(3)步骤(2)所述浓缩液加入2-4倍体积的95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入1-3倍氯仿和正丁醇混合液(2-4:1)进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉。
优选的,所述的牛樟芝寡糖可按照如下方法制备:
(1)取一定质量牛樟芝子实体粉末,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
(3)步骤(2)所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉;
本发明还提供了上述牛樟芝寡糖用于制备抗菌药物或保健食品的用途。
本发明还提供了所述牛樟芝寡糖按照常规工艺制备而成的临床可接受的药物制剂或保健食品。
制备临床可接受的药物制剂或保健食品包括如下步骤:
(1)取一定质量牛樟芝子实体粉末,加入水混匀,高温条件下溶解抽提,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成浓缩液;
(3)步骤(2)所述浓缩液加入95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入氯仿和正丁醇混合液进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉;
(6)向步骤(5)所述牛樟芝寡糖干粉添加常规辅料,可按照常规工艺制成临床上可接受的药物制剂或保健食品。
更优选的,制备临床可接受的药物制剂或保健食品包括如下步骤:
(1)取一定质量牛樟芝子实体粉末,加入5-100倍重量的水混匀,在25-100℃条件下溶解抽提1-12h,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成6-10倍浓度的浓缩液;
(3)步骤(2)所述浓缩液加入2-4倍体积的95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入1-3倍氯仿和正丁醇混合液(2-4:1)进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉。
(6)步骤(5)所述牛樟芝寡糖干粉添加常规辅料,可按照常规工艺制成临床上可接受的药物制剂或保健食品。
作为上述方法一种更好的选择,制备临床可接受的药物制剂或保健食品包括如下步骤:
(1)取一定质量牛樟芝子实体粉末,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
(3)步骤(2)所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉。
(6)步骤(5)所述牛樟芝寡糖干粉添加常规辅料,可按照常规工艺制成临床上可接受的药物制剂或保健食品。
本发明所述牛樟芝寡糖是通过降解牛樟芝子实体中的多糖成分得到的,并且经实验证明其类似物和其均具有明显的抗炎效果。动物实验证明,在脂多糖诱导的急性炎症的小鼠模型中,提前两周通过饮水给小鼠喂食一定剂量的牛樟芝寡糖,小鼠在应对急性炎症时反应并不剧烈,相应的促炎因子的转录水平明显下调,显示出牛樟芝寡糖具有明显的急性炎症的预保护作用。实验结果提示,所述牛樟芝寡糖对急性炎症有较好的缓解作用,可进一步用于药物制剂或保健食品的开发和应用。
附图说明
图1.高效液相色谱—质谱分析牛樟芝寡糖所具有的主要分子量分布;
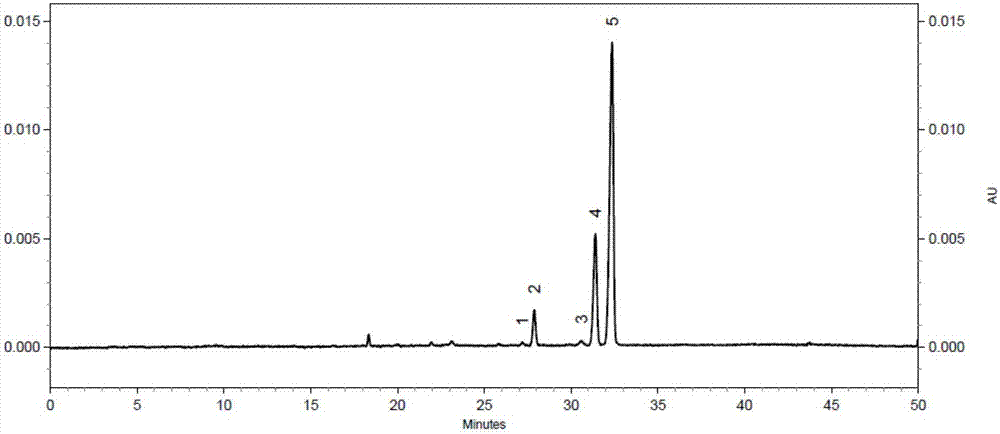
图2.毛细管电泳分析牛樟芝寡糖的单糖组成;其中峰1-5分别对应了阿拉伯糖、葡萄糖、岩藻糖、半乳糖和甘露糖。
具体实施方式
如下为本发明的实施例,其仅用做对本发明的解释而并非限制。
实施例1牛樟芝寡糖抗炎作用
(1)在本实施例中,为评价牛樟芝多糖对急性炎症小鼠的抗炎作用,将24只四周龄的c57bl/6小鼠随机分成4组,每组6只,分别对应正常处理组、脂多糖刺激组、牛樟芝寡糖处理组、牛樟芝寡糖和脂多糖刺激联合组等。小鼠在温度、湿度恒定的环境中饲养,经过1周的适应期。对应脂多糖刺激组按2mg每公斤小鼠体重(2mg/kg)的剂量给小鼠腹腔注射脂多糖一次,24小时后,开始解剖获取组织样本。
(2)脂多糖注射的小鼠在24h之内,由于小鼠对细菌表面脂多糖的先天性免疫识别,短时间内激活大量的炎症反应,肺部促炎因子如肿瘤坏死因子α(tnfα),趋化因子(mcp-1),白介素8(il-8)的转录水平明显升高,而经过牛樟芝寡糖预处理的小鼠,其促炎因子的转录水平均明显下调。
表1.动物实验后各组促炎因子转录变化(*p<0.05,**p<0.01vs正常组,#p<0.05,##p<0.01,vs模型组)
本实施例中寡糖可以按照下述的方法进行制备:
(1)取一定质量牛樟芝子实体粉末,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
(2)将步骤(1)所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
(3)步骤(2)所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
(4)步骤(3)所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
(5)向步骤(4)所述上层清液中加入适量1m的三氟乙酸或者缓慢的加入盐酸或硫酸进行水解,然后使用氨水或缓慢的加入氢氧化钾或者氢氧化钠中和其水解产物,减压浓缩后,冻干成牛樟芝寡糖干粉。
实施例2牛樟芝寡糖的应用方法
(1)胶囊剂
a.取一定质量牛樟芝子实体粉末4kg,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
b.将步骤a所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
c.步骤b所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
d.步骤c所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
e.向步骤d所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,-80℃冻成牛樟芝寡糖干粉;
f.步骤e所述牛樟芝寡糖干粉,加入适量常规辅料混合均匀,冷冻干燥,粉碎,填充胶囊,分装,即得。
(2)颗粒剂
a.取一定质量牛樟芝子实体粉末2kg,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
b.将步骤a所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
c.步骤b所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
d.步骤c所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
e.向步骤d所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,-80℃冻成牛樟芝寡糖干粉;
f.步骤e所述牛樟芝寡糖干粉,加入适量常规辅料混合均匀,过20目筛挤压制粒,60度沸腾干燥,分装即得。
(3)口服液
a.取一定质量牛樟芝子实体粉末3kg,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
b.将步骤a所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
c.步骤b所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
d.步骤c所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
e.向步骤d所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压浓缩后,-80℃冻成牛樟芝寡糖干粉;
f.步骤e所述牛樟芝寡糖干粉加水和适量矫味剂、防腐剂混合均匀,配制成溶液,灌装,灭菌,即得。
(4)固体饮料
a.取一定质量牛樟芝子实体粉末3kg,加入40倍重量的水混匀,在90℃条件下溶解抽提4h,得到抽提液;
b.将步骤a所述抽提液过滤,截留沉淀后获得滤出液,减压蒸馏成8倍浓度的浓缩液;
c.步骤b所述浓缩液加入3倍体积的95%乙醇,静置过夜获得沉淀物;
d.步骤c所述沉淀物加水复溶,加入2倍氯仿和正丁醇混合液(3:1)进行震荡萃取,获取上层清液;
e.向步骤d所述上层清液中加入适量三氟乙酸进行水解,然后使用氨水中和其水解产物,减压成浓缩液;
f.步骤e所述浓缩液中加入适量常规辅料混合均匀,喷雾干燥,将所得喷雾干粉分装,即得。
上述实施例仅为清楚说明举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其他不同形式的变化或变动。这里无需也无法对所有的实施方式给予穷举。而由此所引申出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!