一种利用生物样本直接构建靶向文库的方法与流程
本发明属于生物
技术领域:
,具体涉及一种利用生物样本直接构建靶向文库的方法。
背景技术:
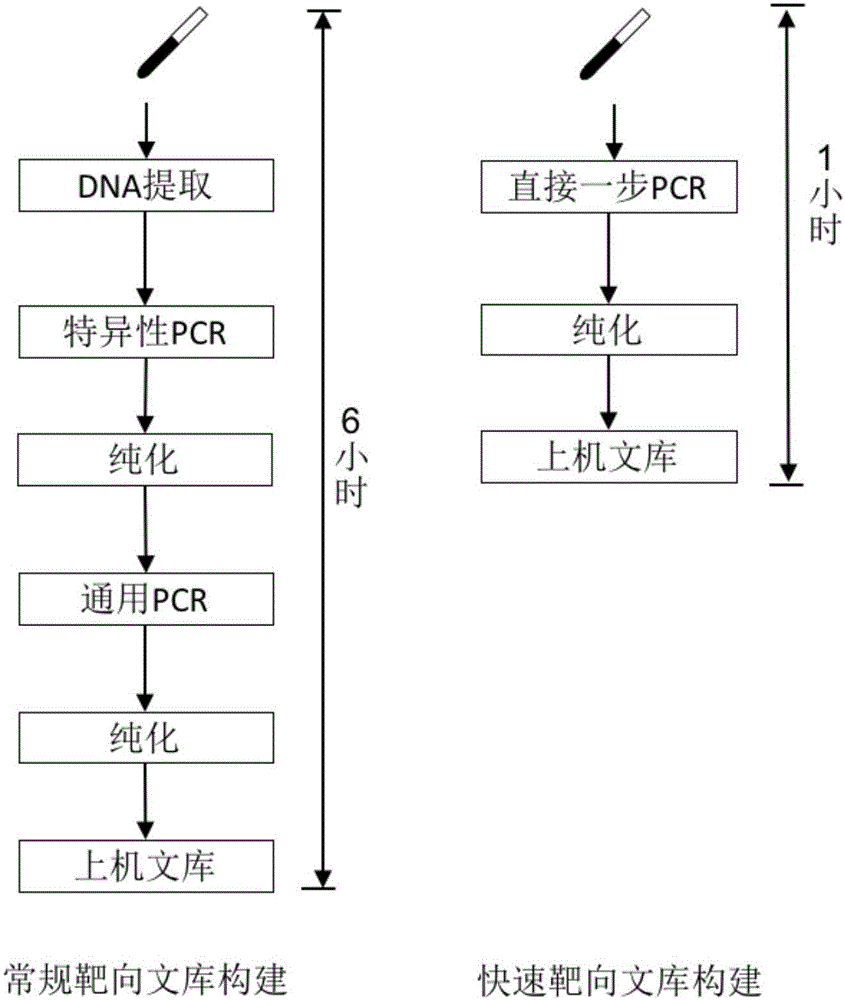
:测序技术的发展为现代基因组学的研究打开了新的局面,然而全基因组测序的成本和分析的复杂程度还是让科研人员倍感困难。尽管新一代测序(ngs)的通量越来越高,而费用越来越低,但它仍不是大多数遗传实验室的可行选择。对于复杂疾病的研究更是如此,这类研究至少需要数百个样本,以实现足够的统计能力。然而,如此多样本的全基因组测序,无论从成本考虑,还是从数据分析考虑,都是相对困难的。目标区域靶向富集测序技术(targetregionsequencing)是对目标基因进行富集并结合二代测序技术进行测序的技术。采用该技术可得到目标区域的碱基信息,从而达到检测疾病的目的,相对于全基因组测序,该技术可以降低测序成本,简化信息分析流程,提高目标区域测序深度,提高检测的灵敏性和准确性,目标区域测序在基因分型、罕见病诊断、肿瘤检测等领域具有独特的优势。常规靶向文库的构建过程见图1。常规靶向文库的构建,整个实验流程长,需要分别进行两步pcr扩增,且标准化程度低,实验稳定性差,尤其对于大型的snp分型研究或动辄上万份的样本检测,生物样本dna的抽提和两步pcr扩增带来的操作也十分繁重,而且样本量大的时候,抽提过程容易造成样本之间的污染。技术实现要素:本发明的目的是提供一种构建靶向文库的方法。本发明提供的构建靶向文库的方法,可包括如下步骤:(1)以生物样本为模板,采用若干个特异引物对和至少一个通用引物对进行pcr扩增,得到pcr扩增产物;(2)取步骤(1)得到pcr扩增产物,纯化,得到的纯化产物即为靶向文库;每个特异引物对可包括两条引物;一条引物从5’末端到3’末端依次可包括通用接头序列甲和区段a,另一条引物从5’末端到3’末端依次可包括通用接头序列乙和区段b;区段a和区段b均根据靶基因的核苷酸序列设计;各个特异引物对中区段a和区段b的核苷酸序列不同,可结合至靶基因的不同位置;每个通用引物对可包括两条引物;一条引物从5’末端到3’末端依次可包括测序接头序列甲和通用接头序列甲,另一条引物从5’末端到3’末端依次可包括测序接头序列乙和通用接头序列乙。上述构建靶向文库的方法中,所有特异引物对的靶序列拼接后可覆盖靶基因全长。上述构建靶向文库的方法中,所述测序接头序列甲和所述测序接头序列乙的核苷酸序列可以相同,也可以不同。所述通用接头序列甲和所述通用接头序列乙的核苷酸序列可以相同,也可以不同。通用引物对的引物中添加测序接头序列甲和测序接头序列乙的目的是为了便于进行测序,根据测序平台的不同,也可以替换成由其它核苷酸序列组成的测序接头序列。在本发明的实施例中,采用bgiseq-500测序平台进行测序。相应的,通用接头序列甲的核苷酸序列为5’-cttggcctccgactt-3’,通用接头序列乙的核苷酸序列为5’-ggctacgatccgactt-3’,测序接头序列甲的核苷酸序列为5’-tgtgagccaaggagttgctgcgtacatttgtcttcctaagaccg-3’,测序接头序列乙的核苷酸序列为5’-phos/gaacgacat-3’(phos/表示5’末端磷酸化)。上述构建靶向文库的方法中,每个特异引物对具体可由两条引物组成。一条引物从5’末端到3’末端依次可由通用接头序列甲和区段a组成,另一条引物从5’末端到3’末端依次可由通用接头序列乙和区段b组成。上述构建靶向文库的方法中,每个通用引物对由两条引物组成。一条引物从5’末端到3’末端依次可由测序接头序列甲和通用接头序列甲组成。另一条引物从5’末端到3’末端依次可由测序接头序列乙和通用接头序列乙组成。上述构建靶向文库的方法中,所述区段a和所述区段b的退火温度为60-65℃。所述通用接头序列甲和所述通用接头序列乙的退火温度为50-55℃。上述构建靶向文库的方法中,所述进行pcr扩增的酶为dna聚合酶。所述dna聚合酶可具有如下特点:对生物样本中存在的pcr抑制剂具有很高的耐受性且对含40-99%(v/v)全血的生物样本具有dna聚合酶活性(在优化条件下)。所述dna聚合酶具体可为phusionhotstartii高保真dna聚合酶(经修饰的)。上述构建靶向文库的方法中,所述进行pcr扩增的反应程序可为:92-98℃3-7min;92-98℃5-15s,60-65℃1-3min,72℃xs,10-25个循环;92-98℃5-15s,50-55℃1-2min,72℃ys,10-20个循环;72℃3-10min;x和y均为自然数,x和y的具体值根据dna聚合酶的特点和pcr扩增产物的长度确定。本发明还保护上述任一所述构建靶向文库的方法的应用,可为(z1)或(z2)或(z3)或(z4)或(z5):(z1)从生物样本中捕获靶序列;(z2)从生物样本中分离靶序列;(z3)从生物样本中富集靶序列;(z4)测序;(z5)检测突变。上述任一所述构建靶向文库的方法构建的靶向文库也属于本发明的保护范围。本发明还保护采用上述任一所述构建靶向文库的方法构建的靶向文库的应用,可为(z1)或(z2)或(z3)或(z4)或(z5):(z1)从生物样本中捕获靶序列;(z2)从生物样本中分离靶序列;(z3)从生物样本中富集靶序列;(z4)测序;(z5)检测突变。上述任一所述构建靶向文库的方法或上述任一所述的应用中,所述生物样本可为(a1)或(a2)或(a3)或(a4)或(a5)或(a6):(a1)血液;(a2)尿液;(a3)唾液;(a4)血液的基因组dna;(a5)尿液的基因组dna;(a6)唾液的基因组dna。实验证明,采用本发明提供的方法构建的快速靶向文库不仅准确率高、耗时短、操作简便,而且不容易造成样本之间的污染,具有重大的应用价值。附图说明图1为常规靶向文库和快速靶向文库的构建过程。图2为实施例1构建的快速靶向文库中每个特异引物对富集目标区域的深度的统计结果。图3为快速靶向文库稳定性的检测结果。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的实验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量实验,均设置三次重复实验,结果取平均值。agencourtampurexp磁珠为美国贝克曼库尔特有限公司的产品。phusionblooddirectpcrmastermix(2×)为thermofisher公司的产品,货号为f175s。下述实施例中的全血样本为全血样本1、全血样本2或全血样本3。每个全血样本在肝豆状核变性基因的突变位点信息详见表1。表1样本名称在肝豆状核变性基因的突变位点信息全血样本12621c>t全血样本22975c>t全血样本32975c>t,2621c>t实施例1、快速靶向文库的构建和分析快速靶向文库的构建过程见图1。一、引物的设计和合成根据肝豆状核变性基因容易发生突变的位点,设计并合成17个特异引物对和1个通用引物对。每个引物对均由两条引物组成。每个特异引物对的一条引物(由5’到3’)由通用接头序列甲和区段a组成,另一条引物(由5’到3’)由通用接头序列乙和区段b组成。区段a和区段b均可结合肝豆状核变性基因。由于区段a和区段b的核苷酸序列不同,各个特异引物对可以结合肝豆状核变性基因的不同位置。通用引物对由通用引物1和通用引物2组成;通用引物2(由5’到3’)由测序接头序列甲和通用接头序列甲组成,通用引物1(由5’到3’)由测序接头序列乙和通用接头序列乙组成。添加测序接头序列甲和测序接头序列乙的目的是为了便于进行测序,根据测序平台的不同,当然也可以替换成由其它核苷酸序列组成的测序接头序列。通用引物2的通用接头序列甲和特异引物对中的通用接头序列甲完全相同(即重叠),通用引物1的通用接头序列乙和特异引物对中的通用接头序列乙完全相同(即重叠)。由于特异引物对和通用引物对均在一个反应体系,为减少非特异性扩增,必须保证两次pcr扩增的退火温度不同,具体为:特异引物对的退火温度为60-65℃,通用引物对的退火温度为50-55℃。每个特异引物对的上下游引物的核苷酸序列(名称中含“f”的为上游引物,名称中含“r”的为下游引物)和用于扩增肝豆状核变性基因发生突变的位点的名称见表2。通用引物对的上下游引物的核苷酸序列见表3。表2注:单下划线标注的为通用接头序列甲,方框标注的为区段a,双下划线标注的为通用接头序列乙,波浪线标注的为区段b。表3注:双下划线标注的为通用接头序列乙,斜体为测序接头序列乙,单下划线标注的为通用接头序列甲,虚线为测序接头序列甲。二、pcr扩增1、配置反应体系。反应体系为50μl,由25μlphusionblooddirectpcrmastermix(2×)、5μl全血样本、1μl正向引物池(由表2中名称含“f”的引物组成且各个引物的浓度均为10μm)、1μl反向引物池(由表2中名称含“r”的引物组成且各个引物的浓度均为10μm)、1.5μl通用引物1(浓度为10μm)、1.5μl通用引物2(浓度为10μm)和15μl蒸馏水组成。2、取所述反应体系,进行pcr扩增,得到pcr扩增产物。反应程序:98℃5min;98℃10s,65℃2min,72℃30s,20个循环;98℃10s,55℃30s,72℃30s,8个循环;72℃5min。三、快速靶向文库的获得取步骤二得到的pcr扩增产物,加入50μlagencourtampurexp磁珠,然后按照agencourtampurexp磁珠的说明书步骤进行纯化,最后用20μl蒸馏水溶解,得到快速靶向文库。四、快速靶向文库的质检取步骤三构建的快速靶向文库,采用安捷伦2100进行质检。质检结果表明,步骤三构建的快速靶向文库的目标主带在220bp左右且浓度大于10ng/μl。由此可见,步骤三构建的快速靶向文库质检合格。五、测序及结果分析1、取步骤三构建的快速靶向文库,采用bgiseq-500测序平台进行双端50bp测序,得到下机数据。2、取步骤1得到的下机数据,先进行质量过滤(目的为去掉测序质量低的reads),然后去接头,得到双端测序结果。3、将步骤2得到的双端测序结果和人参考基因组进行比对,统计基本参数(如比对率、捕获率(即目标区域比例))。统计结果见表4。表44、根据步骤2得到的双端测序结果,统计每个特异引物对富集目标区域的深度,获得每个特异引物对扩增效率的信息。实验结果见图2(横坐标为特异引物对富集的目标区域,1-17依次为特异引物对gsp01-特异引物对gsp17富集的目标区域)。5、根据步骤2得到的双端测序结果,统计肝豆状核变性基因发生突变的位点的深度及四碱基比例,得到突变位点的突变信息。突变位点的突变信息见表5。结果表明,每个全血样本的检测结果和已知突变信息完全一致。表5六、稳定性按照上述步骤一至五的方法,检测全血样本。每个全血样本检测两次。将测序后得到的每个区域的深度的比例进行对比。实验结果见图3(横纵坐标表示每个特异引物对富集目标区域得到测序reads数量占总数的百分比)。结果表明,采用上述方法构建的快速靶向文库稳定性较高。上述结果表明,采用上述方法可以构建快速靶向文库,且该快速靶向文库可以用于检测突变。实施例2、常规靶向文库的构建和分析常规靶向文库的构建过程见图1。一、引物的设计和合成根据肝豆状核变性基因容易发生突变的位点,设计并合成17个特异引物对和1个通用引物对。每个引物对均由两条引物组成。每个特异引物对的上下游引物的核苷酸序列(名称中含“f”的为上游引物,名称中含“r”的为下游引物)和用于扩增肝豆状核变性基因发生突变的位点的名称见表2。通用引物对的上下游引物的核苷酸序列见表3。二、基因组dna的提取提取全血样本的基因组dna。三、特异性pcr扩增1、配置反应体系。反应体系为50μl,由25μlkapa2gmultiplexmastermix(罗氏公司的产品)、5μl全血样本的基因组dna(含10-20ng全血样本的基因组dna)、1μl正向引物池(由表2中名称含“f”的引物组成且各个引物的浓度均为10μm)、1μl反向引物池(由表2中名称含“r”的引物组成且各个引物的浓度均为10μm)和18μl蒸馏水组成。2、取所述反应体系,进行pcr扩增,得到pcr扩增产物。反应程序:98℃5min;98℃10s,65℃2min,72℃30s,20个循环;72℃5min。四、纯化取步骤三得到的pcr扩增产物,加入50μlagencourtampurexp磁珠,然后按照agencourtampurexp磁珠的说明书步骤进行纯化,最后用22μl蒸馏水溶解,得到纯化产物。五、通用pcr扩增1、配置反应体系。反应体系为50μl,由25μlkapa2gmultiplexmastermix(罗氏公司的产品)、20μl步骤四得到的纯化产物(含1ng纯化产物)、1μl通用引物1(浓度为10μm)、1μl通用引物2(浓度为10μm)和3μl蒸馏水组成。2、取所述反应体系,进行pcr扩增,得到pcr扩增产物。反应程序:98℃5min;98℃10s,55℃30s,72℃30s,8个循环;72℃5min。六、常规靶向文库的获得取步骤五得到的pcr扩增产物,加入50μlagencourtampurexp磁珠,然后按照agencourtampurexp磁珠的说明书步骤进行纯化,最后用20μl蒸馏水溶解,得到常规靶向文库。七、常规靶向文库的质检取步骤六构建的常规靶向文库,采用安捷伦2100进行质检。质检结果表明,步骤六构建的常规靶向文库的目标主带在220bp左右且浓度大于10ng/μl。由此可见,步骤六构建的常规靶向文库质检合格。八、测序及结果分析1、取步骤六构建的常规靶向文库,采用bgiseq-500测序平台进行双端50bp测序,得到下机数据。2、取步骤1得到的下机数据,先进行质量过滤(目的为去掉测序质量低的reads),然后去接头,得到双端测序结果。3、将步骤2得到的双端测序结果和人参考基因组进行比对,统计基本参数(如比对率、捕获率(即目标区域比例))。统计结果见表4。4、根据步骤2得到的双端测序结果,统计肝豆状核变性基因发生突变的位点的深度及四碱基比例,得到突变位点的突变信息。突变位点的突变信息见表5。结果表明,每个全血样本的检测结果和已知突变信息完全一致。上述结果表明,快速靶向文库和常规靶向文库的检测结果基本一致。由此可见,本发明提供的方法构建的快速靶向文库不仅准确率高、耗时短、操作简便,而且不容易造成样本之间的污染,具有重大的应用价值。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1