一种氘代甲基对硫磷的制备方法与流程
本发明涉及化学分析技术领域。具体地说是一种氘代甲基对硫磷的制备方法。
背景技术
甲基对硫磷俗称甲基1605(式化合物va),学名o,o-二甲基-o-(4-硝基苯基)硫代磷酸酯,一种有机磷杀虫剂,属高毒级农药。我国是农业大国,农药使用量大,有机磷杀虫剂,其使用范围广,毒性高。近年来,因该类药物引发的投毒、自杀、误服等刑事案件时有发生。这就要求公安司法鉴定部门对涉及该类药物的检材样本进行检测。而为了确保检测方法准备、可靠的手段是在检测时添加内标物,而对应的氘代物则是最佳的内标物,由于其用途为非民用,带有特殊性,为此我国对于此类商品的研究与生产相对较少,而这类标准品在分析检测中又是必需而不可或缺的。氘代内标物稳定性差,我国尚未突破这一制约我国氘代物生产的技术瓶颈,尚无生产涉案毒物的氘代物的厂家,该产品的使用仅能依赖进口。长期以来,我国所用氘代内标物均是依赖进口,而且国外进口均为溶液,而不是固体粉末,加上其价格昂贵,严重限制了该类标准品的在国内的广泛使用。
关于氘代甲基对硫磷(式化合物v)的合成,目前尚无完整详细的文献报道。因此,急需开发一种具有自知识产权的新工艺合成氘代甲基对硫磷。
技术实现要素:
为此,本发明所要解决的技术问题在于一种氘代甲基对硫磷的制备方法。
为解决上述技术问题,本发明提供如下技术方案:
一种氘代甲基对硫磷的制备方法,包括如下步骤:
(1)三氯硫磷与氘代甲醇单酯化,得到反应产物ⅱ;
(2)反应产物ⅱ与对硝基苯酚进行酯化,得到反应产物ⅳ;
(3)反应产物ⅳ与氘代甲醇进行酯化,得到反应产物ⅴ,反应产物ⅴ即为氘代甲基对硫磷。
上述氘代甲基对硫磷的制备方法,包括如下步骤:
(1)三氯硫磷与氘代甲醇在-10到-5℃进行单酯化反应,得到反应产物ⅱ,如下式所示,所述反应产物ⅱ为o-(甲基-d3)-硫代磷酰二氯;
(2)将相等物质的量的反应产物ⅱ和对硝基苯酚溶于有机溶剂中,加入无机碱,在室温下反应产物ⅱ与对硝基苯酚进行酯化,得到反应产物ⅳ,如下式所示,所述反应产物ⅳ为o-(甲基-d3)-o-(4-硝基苯基)-硫代磷酰胺;
(3)反应产物ⅳ在-5℃下,滴加naoh的氘代甲醇溶液,进行酯化,得到反应产物ⅴ,如下式所示,反应产物ⅴ即为氘代甲基对硫磷;
上述氘代甲基对硫磷的制备方法,在步骤(1)中,氘代甲醇与三氯硫磷的物质的量之比为3:1。
上述氘代甲基对硫磷的制备方法,在步骤(2)中,所述无机碱为k2co3和na2co3中的一种或多种。
上述氘代甲基对硫磷的制备方法,在步骤(2)中,反应产物ⅱ与无机碱的物质的量之比为1:1。
上述氘代甲基对硫磷的制备方法,在步骤(2)中,所述有机溶剂为四氢呋喃、乙醚和1,4-二氧六环中的一种或多种。
上述氘代甲基对硫磷的制备方法,在步骤(3)中,naoh与反应产物ⅳ的物质的量之比为5:1。
上述氘代甲基对硫磷的制备方法,在步骤(3)中,氘代甲醇与反应产物ⅳ的质量比4:1。
上述氘代甲基对硫磷的制备方法,包括如下步骤:
(1)取122.4mmol三氯硫磷置于100ml圆底烧瓶中,冰盐浴降温至-10到-5℃,随后滴加367.2mmol的氘代甲醇,在15-20min滴加完毕,升温至-5℃继续搅拌反应1h,向反应体系中加入50ml冰水,搅拌5min后,分液,保留分液后的有机相,分液后的水相用二氯甲烷萃取两次,每次用二氯甲烷20ml萃取,然后合并分液后的有机相和萃取得到的有机相,用25g无水硫酸镁干燥,过滤后,减压浓缩,得到反应产物ⅱ;
(2)取115.5mmol反应产物ⅱ置于100ml圆底烧瓶中,加入30ml有机溶剂搅拌至溶解,随后加入116.45mmol的对硝基苯酚,搅拌下分3批次加入115.5mmol的无机碱,每次间隔时间为0.5h,室温下搅拌反应1h,随后向反应体系中加入60ml水,然后用二氯甲烷萃取3次,每次用50ml二氯甲烷萃取,合并萃取后的有机相,用30g无水硫酸镁干燥,过滤并降压浓缩,柱层析纯化,淋洗剂为石油醚和乙酸乙酯的混合物,石油醚和乙酸乙酯的体积比为15:1,得到反应产物ⅳ;
(3)取7.3mmol的反应产物ⅳ置于10ml圆底烧瓶中,冰盐浴降温至-5℃,滴加氘代甲醇和naoh的混合溶液,氘代甲醇和naoh的混合溶液为37mmol的naoh溶于8.0g氘代甲醇,15min滴加完毕;保持反应温度在-5℃下,继续搅拌反应2h,薄层色谱tlc监控反应至反应产物ⅳ消失,回收氘代甲醇,并向反应体系中加入20ml水,然后用乙酸乙酯萃取3次,每次用20ml乙酸乙酯萃取,合并萃取后的有机相,用体积分数为1%的稀盐酸洗涤有机相,然后用20g无水硫酸镁干燥有机相,过滤并减压浓缩,柱层析纯化,淋洗剂为石油醚和乙酸乙酯的混合物,石油醚和乙酸乙酯的体积比为15:1,得到反应产物ⅴ。
上述氘代甲基对硫磷的制备方法,所述无极碱为na2co3或k2co3,所述有机溶剂为四氢呋喃或1,4-二氧六环。
本发明的技术方案取得了如下有益的技术效果:
本发明氘代甲基对硫磷制备方法具有反应条件温和、操作简单,所得氘代甲基对硫磷产品质量好,稳定性好等优点。
附图说明
图1本发明氘代甲基对硫磷的制备方法的合成路线图;
图2本发明氘代甲基对硫磷的制备方法的氘代甲基对硫磷的核磁共振氢谱图;
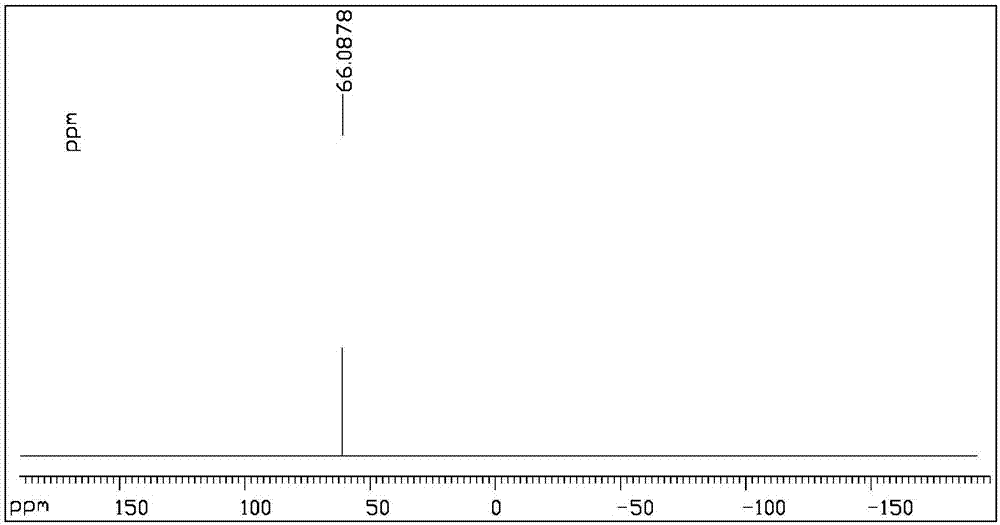
图3本发明氘代甲基对硫磷的制备方法的氘代甲基对硫磷的核磁共振磷谱图;
图4本发明氘代甲基对硫磷的制备方法的氘代甲基对硫磷的质谱图;
图5本发明氘代甲基对硫磷的制备方法的氘代甲基对硫磷的高效液相色谱图。
图中附图标记表示为:ⅰ-三氯硫磷;ⅱ-o-(甲基-d3)-硫代磷酰二氯;ⅲ-对硝基苯酚;ⅳ-o-(甲基-d3)-o-(4-硝基苯基)-硫代磷酰胺;ⅴ-氘代甲基对硫磷。
具体实施方式
氘代甲基对硫磷,如下式所示;cas号:96740-32-8。
实施例1
(1)三氯硫磷与氘代甲醇单酯化,得到反应产物ⅱ(分子量169.979)
称取三氯硫磷20.8g(化合物i,122.4mmol)置于100ml圆底烧瓶中,冰盐浴降温至-10℃,随后滴加13.3g的氘代甲醇(367.2mmol),在15-20min滴加完毕,升温至-5℃继续搅拌反应1h,向反应体系加入50ml冰水(0℃的水),搅拌5min后,分液,保留分液后的有机相,分液后的水相用二氯甲烷萃取两次,每次用20ml二氯甲烷萃取。合并分液后的有机相和萃取得到的有机相,用25g无水硫酸镁干燥,过滤后减压浓缩,可得反应物ⅱ,即为o-(甲基-d3)-硫代磷酰二氯。
(2)反应产物ⅱ与对硝基苯酚进行酯化,得到反应产物ⅳ
取19.4g反应产物ⅱ(115.5mmol)置于100ml圆底烧瓶中,加入30ml四氢呋喃搅拌至溶解,随后加入16.2g的对硝基苯酚(分子量139.11,式ⅲ,116.45mmol),搅拌下分3批次加入的无机碱碳酸钾15.9g(115.5mmol),每次间隔时间为0.5h,室温下搅拌反应1h,随后向反应体系中加入60ml自来水,然后用二氯甲烷萃取3次,每次用50ml二氯甲烷萃取,合并萃取后的有机相,用30g无水硫酸镁干燥,过滤并降压浓缩,柱层析纯化(pe:ea=15:1,pe为石油醚,ea为乙酸乙酯,pe与pa的体积比为15:1),得到28g反应产物ⅳ,反应产物ⅳ为o-(甲基-d3)-o-(4-硝基苯基)-硫代磷酰胺。
(3)反应产物ⅳ与氘代甲醇进行酯化,得到反应产物ⅴ,反应产物ⅴ
即为氘代甲基对硫磷。
取2.0g反应产物ⅳ(7.3mmol,分子量272.639)置于10ml圆底烧瓶中,冰盐浴降温至-5℃,滴加naoh的氘代甲醇溶液,naoh的氘代甲醇溶液为37mmol的naoh(1.48g)溶于8.0g氘代甲醇中制成,15min滴加完毕;保持反应温度在-5℃,继续搅拌反应2h,薄层色谱tlc监控反应至反应产物ⅳ消失,回收氘代甲醇,并向反应体系中加入20ml水,然后用乙酸乙酯萃取3次,每次用20ml乙酸乙酯萃取,合并萃取后的有机相,用质量分数为1%的稀盐酸洗涤有机相,然后用20g无水硫酸镁干燥有机相,过滤并减压浓缩,柱层析纯化(pe:ea=15:1,pe为石油醚,ea为乙酸乙酯,pe与ea的体积比为15:1),得到反应产物ⅴ,反应产物ⅴ的质量为1.7g,收率为85%。
实施例2
(1)三氯硫磷与氘代甲醇单酯化,得到反应产物ⅱ
称取三氯硫磷20.8g(化合物i,122.4mmol)置于100ml圆底烧瓶中,冰盐浴降温至-10℃,随后滴加13.3g的氘代甲醇(367.2mmol),在15-20min滴加完毕,升温至-5℃继续搅拌反应1h,向反应体系加入50ml冰水(0℃的水),搅拌5min后,分液,保留分液后的有机相,分液后的水相用二氯甲烷萃取两次,每次用二氯甲烷20ml萃取。合并分液后的有机相和萃取得到的有机相,用25g无水硫酸镁干燥,过滤后减压浓缩,可得反应物ⅱ,即为o-(甲基-d3)-硫代磷酰二氯。
(2)反应产物ⅱ与对硝基苯酚进行酯化,得到反应产物ⅳ
取19.4g反应产物ⅱ(115.5mmol)置于100ml圆底烧瓶中,加入30ml的有机溶剂1,4-二氧六环搅拌至溶解,随后加入16.2g的对硝基苯酚(化合式ⅲ,116.45mmol),搅拌下分3批次加入的碳酸钠12.2g(115.1mmol,分子量105.99),每次间隔时间为0.5h,室温下搅拌反应1h,随后向反应体系中加入60ml自来水,然后用二氯甲烷萃取3次,每次用50ml二氯甲烷萃取,合并萃取后的有机相,用30g无水硫酸镁干燥,过滤并降压浓缩,柱层析纯化(pe:ea=15:1,pe为石油醚,ea为乙酸乙酯,pe与pa的体积比为15:1),得到27g反应产物ⅳ,反应产物ⅳ为o-(甲基-d3)-o-(4-硝基苯基)-硫代磷酰胺。
(3)反应产物ⅳ与氘代甲醇进行酯化,得到反应产物ⅴ,反应产物ⅴ即为氘代甲基对硫磷。
取2.0g反应产物ⅳ(7.3mmol,分子量272.639)置于10ml圆底烧瓶中,冰盐浴降温至-5℃,滴加naoh的氘代甲醇溶液,naoh的氘代甲醇溶液为37mmol的naoh(1.48g)溶于8.0g氘代甲醇中制成,15min滴加完毕;保持反应温度在-5℃,继续搅拌反应2h,薄层色谱tlc监控反应至反应产物ⅳ消失,回收氘代甲醇,并向反应体系中加入20ml自来水,然后用乙酸乙酯萃取3次,每次用20ml乙酸乙酯萃取,合并萃取后的有机相,用质量分数为1%的稀盐酸洗涤有机相,然后用20g无水硫酸镁干燥有机相,过滤并减压浓缩,柱层析纯化(pe:ea=15:1,pe为石油醚,pa为乙酸乙酯,pe与ea的体积比为15:1),得到反应产物ⅴ,反应产物ⅴ的质量为1.7g,收率为85%。
对所制备的氘代甲基对硫磷,分别采用核磁共振氢谱、核磁共振磷谱、质谱和高效液相色谱对其进行表征。具体如下:
如图2所示,核磁共振氢谱:1hnmr(300mhz,chloroform-d)δ7.28-7.34(m,2h),8.21-8.25(m,2h);表明合成的化合物中只含有苯环上的4个h,甲基上的h,已经完全被氘代。
如图3所示,核磁共振磷谱:1pnmr(121mhz,cdcl3)δ66.1;表明合成的化合物中含有p。
如图4所示,质谱:hrms(esi)calcd.forc8h5d6no5ps[m+h]+270.0467,found:270.0471。
如图5所示,在5.129s时,出现氘代甲基对硫磷的保留峰。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本专利申请权利要求的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!