一种棕榈果序原花青素的制备方法及用途与流程
本发明涉及天然产物提取纯化技术领域,具体是一种棕榈果序原花青素的制备方法及用途。
背景技术:
棕榈(trachycarpusfortunei),为棕榈科(palmae)棕榈属(trachycarpus)植物,是我国最普遍、分布范围最广、资源蕴藏量最大的棕榈科植物之一,也是能够广泛地生长在亚热带和温带最耐寒的棕榈科植物。棕榈是我国重要的经济作物,棕榈的每一部分都能利用,新鲜花可以吃,种子用作饲料,树干能建房。
棕榈果序,为棕榈的果序轴及未成熟果实,其味涩性平,具有收敛、止血、涩肠、固精之功效,用于肠风、吐血、衄血、崩漏、痔血、带下、泻下、遗精等。已有研究报道指出棕榈未成熟果实中含有一定量的黄酮,棕榈果实黄酮具有较强的清除dpph值·自由基及抑制脂质过氧化活性作用,但其化学成分尚不清楚。
原花青素,又名原花色素,是由单体黄烷-3-醇以不同聚合度连接而成的聚多酚类化合物的混合物,具有广泛的生化和药理活性,在医药、化妆品及保健食品等领域具有广泛的用途,每年的需求量逐年增加。
我们的研究发现,棕榈果序中含有大量的原花青素类成分,其含量最高可达干重的8%左右。由此可见,棕榈果序是非常值得开发利用的原花青素植物资源,但现有技术中,未见到有关从棕榈果序中制备原花青素的报道。
为综合利用棕榈植物资源,以棕榈果序为原料开发高附加值原花青素产品,本申请提出一种棕榈果序原花青素的制备方法及用途。
技术实现要素:
本发明所要解决的技术问题是,针对现有技术的不足,提供一种棕榈果序原花青素的制备方法及用途,本发明对棕榈资源进行深度利用,创造出高附加值的棕榈产品,具有原料易得、工艺简单、成本低廉、操作便利、可大规模生产、易于产业化等特点,实现了以棕榈果序为原料制备出高纯度原花青素的技术效果,填补了从棕榈果序中提取制备原花青素的技术空白。
本发明解决上述技术问题所采用的技术方案为:一种棕榈果序原花青素的制备方法,包括以下步骤:
步骤一:取新鲜的棕榈果序,洗净、晾干、切碎并制成匀浆样品;向匀浆样品中分别加入柠檬酸盐缓冲液及抗坏血酸,混匀,得到混匀后的样品;
步骤二:将混匀后的样品置于超声波发生器中进行超声预处理;再向超声预处理后的样品中加入生物酶,混匀,进行生物酶处理,得到生物酶处理后的样品;
步骤三:向生物酶处理后的样品中加入提取溶剂,混匀;再将混匀后的样品置于超声波发生器中进行超声处理;最后将超声处理后的样品进行固液分离,得到的液体为棕榈果序原花青素粗提取物;
步骤四:取大孔树脂,将大孔树脂装填入层析柱中后,以体积分数为70~100%的乙醇浸泡6~24h,之后换用去离子水洗脱至流出液澄清及无乙醇味为止;然后换用20~50g/l的hcl溶液浸泡6~24h,用去离子水洗脱至流出液为中性;再以20~50g/l的naoh溶液浸泡6~24h,以去离子水洗脱至流出液为中性,得到前处理后的大孔树脂;
步骤五:将前处理后的大孔树脂装填至层析柱中,用水以0.5~5bv/h的流速在温度5~40℃下平衡0.5~24h,得到平衡后的大孔树脂柱;再将步骤三得到的棕榈果序原花青素粗提取物上样吸附,上样完成后关闭层析柱活塞并静置1~24h;再用1~10bv的水以0.5~4bv/h的流速,在温度5~40℃下洗脱未被大孔树脂吸附的原花青素及杂质;
步骤六:将吸附在大孔树脂上的原花青素用洗脱溶剂洗脱,得到棕榈果序原花青素纯化物;对棕榈果序原花青素纯化物进行干燥,得到棕榈果序原花青素成品。
作为优选,步骤一中,所述的柠檬酸盐缓冲液的浓度为0.02~0.2mol/l,温度为5~40℃,ph值为2~7,每kg棕榈果序对应加入0.25~20kg的所述的柠檬酸盐缓冲液;每kg棕榈果序对应加入0.05~20g的所述的抗坏血酸。
作为优选,步骤二中,所述的超声预处理的参数为:超声波频率20~40khz,功率50~5000w,温度5~60℃,时间1~15min。
作为优选,步骤二中,所述的生物酶为纤维素酶和果胶酶,每kg棕榈果序对应的纤维素酶和果胶酶的用量分别为1000~2500000单位和1000~5000000单位;所述的生物酶处理的过程为:在10~65℃温度,2~7的ph值下处理10~600min。
作为优选,步骤三中,所述的超声处理的参数为:超声波频率20~40khz,功率50~5000w,温度5~60℃,时间5~120min,次数1~4次。
作为优选,步骤三中,所述的提取溶剂为体积分数为5~90%的甲醇、体积分数为5~95%的乙醇和体积分数为10~90%的丙酮中的任一种或以上三者任意比例的混合物,每kg棕榈果序对应加入提取溶剂0.25~100l。
作为优选,步骤四中,所述的大孔树脂的类型为ab-8、x-5、d101、hpd-100、hpd-300、hpd-400、hpd-500、hpd-600、hpd-750、nka-ii、nka-9、sp850和hp20中的任意一种或几种的混合物。
作为优选,步骤五中,所述的上样的参数为:上样浓度0.5~20mg/ml,ph值1~7,温度5~40℃,流速0.5~10bv/h,上样量1~20bv。
作为优选,步骤六中,所述的洗脱溶剂为体积分数为5~100%的乙醇,所述的洗脱的参数为:ph值2~7,温度5~40℃,流速0.5~5bv/h,洗脱溶剂用量1~5bv。
上述棕榈果序原花青素在制备涂膜保鲜剂中的用途。涂膜保鲜利用成膜剂在被保鲜物品表面形成一层半透膜,该半透膜能够有效阻止病菌的入侵以及抑制呼吸。这种膜对o2、co2、ch4等有一定的选择渗透作用,能够限制被保鲜物品与外界进行气体交换,使被保鲜物品内部形成一个低o2和高co2的微环境,从而抑制呼吸作用、乙烯产生及膜脂过氧化等需氧生理生化过程,在一定程度上能够延缓组织衰老,减少腐烂发生,保持新鲜品质,延长被保鲜物品贮藏寿命。涂膜保鲜技术简单、操作便利、成本低廉,可用于各种鲜花、果蔬、肉类、水产等鲜活物品的保鲜。含有本发明制备的棕榈果序原花青素的涂膜保鲜剂可有效延长被保鲜物的贮藏寿命。棕榈果序原花青素具有非常强的抗氧化能力,在低浓度下能够有效地清除各种自由基,是现有技术中活性最强的天然抗氧化剂之一,同时,大量的研究表明,棕榈果序原花青素具有优异的抗微生物活性,在较低浓度下可抑制多种病原微生物的生长和繁殖。花青素来源于植物,大量的研究表明,它是一种生物安全性非常好的天然产品,无抗原性、无毒、不致癌、不致畸,可直接食用,将棕榈果序原花青素作为添加剂制备得到含有棕榈果序原花青素的涂膜保鲜剂,无论从理论上,技术上都是切实可行的。
与现有技术相比,本发明具有如下优点:
1、本发明提供了一种棕榈果序原花青素的制备方法,以棕榈科(palmae)棕榈属(trachycarpus)植物棕榈(trachycarpusfortunei)的新鲜果序轴及未成熟果实作为有效部位,经过提取、纯化得到棕榈果序原花青素,主要制备过程包括:棕榈果序预处理、超声预处理及生物酶处理、超声处理提取得到棕榈果序原花青素粗提取物、大孔树脂前处理、粗提取物上样及杂质洗脱、原花青素洗脱及干燥,最终得到高纯度的棕榈果序原花青素成品。本发明对棕榈资源进行深度利用,创造出高附加值的棕榈产品,具有原料易得、工艺简单、成本低廉、操作便利、可大规模生产、易于产业化等特点,实现了以棕榈果序为原料制备出高纯度原花青素的技术效果,填补了从棕榈果序中提取制备原花青素的技术空白。
2、本发明创造性地将生物酶辅助提取和超声波提取及大孔树脂纯化等技术有机结合,实现了对棕榈果序原花青素的高效制备,拓展了棕榈资源的高附加值利用途径。
3、本发明在对棕榈果序预处理过程中,加入柠檬酸盐缓冲液及还原剂抗坏血酸,且整个制备流程在较低温度下进行,在不显著增加提取成本的前提下有效地避免了原花青素在提取过程中因外界因素而氧化,保证了原花青素的提取效率以及原花青素成品的品质。
4、本发明在超声波提取步骤之前,引入生物酶处理步骤,与现有技术中单纯地使用生物酶辅助提取或者超声波提取相比,可在不显著增加提取成本的前提下,有效提高提取效率,降低有机溶剂使用量,节约提取成本。
5、本发明选用大孔树脂进行纯化,并结合特定的技术参数,有利于快速、简便、高效地制备出高纯度的原花青素成品。
6、本发明制备的棕榈果序原花青素可用于制备涂膜保鲜剂。制备的涂膜保鲜剂可用于禽蛋类等物品的保鲜剂。例如,用于鸡蛋的保鲜,一方面利用原花青素优异的抗病原微生物活性,能够有效地抑制病原微生物的生长繁殖;另一方面利用原花青素优异的的抗氧化能力,能够有效地清除自由基,抗氧化,降低鸡蛋呼吸强度,达到延长鸡蛋的保存期的目的。
附图说明
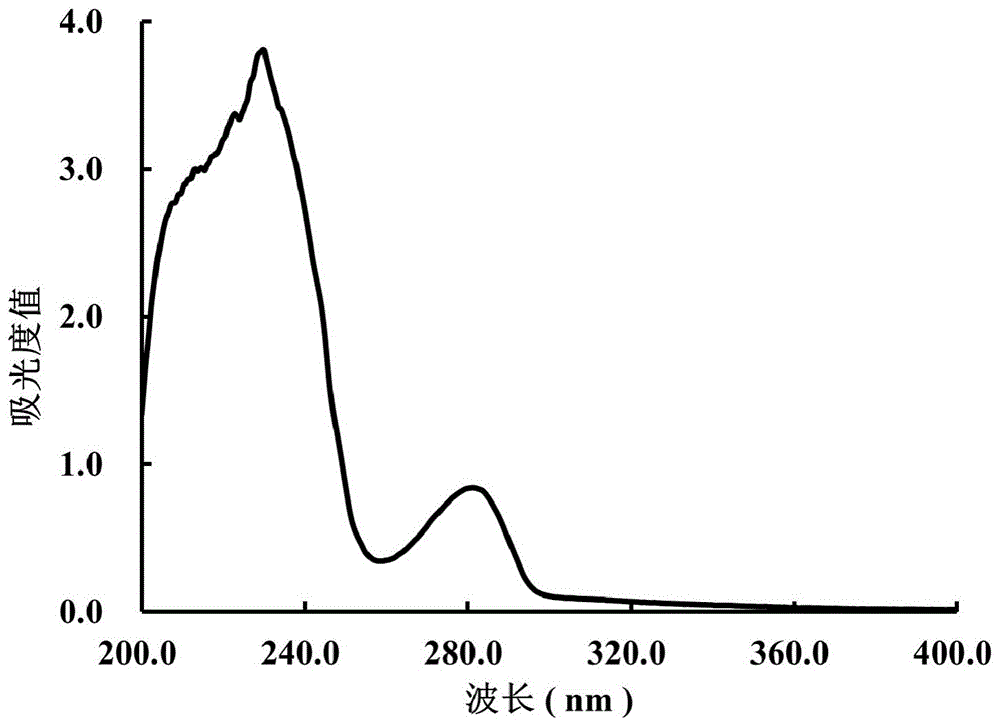
图1为实施例1中制备的棕榈果序原花青素的甲醇溶液在0.05mg/ml浓度下200~400nm间的紫外吸收光谱图;
图2为葡萄籽原花青素分析标准品(粗线)和实施例1中制备的棕榈果序原花青素(细线)的甲醇溶液在0.05mg/ml浓度下230~350nm间的紫外吸收光谱对比;
图3为葡萄籽原花青素分析标准品和实施例1中制备的棕榈果序原花青素在280nm处的相对吸收强度对比;
图4为不同浓度下葡萄籽原花青素分析标准品和实施例1中制备的棕榈果序原花青素经nano2-alcl3-naoh显色后在在506nm处的吸光度值对比;
图5为相同浓度下葡萄籽原花青素分析标准品(粗线)和实施例1中制备的棕榈果序原花青素(细线)经nano2-alcl3-naoh显色后在400~600nm间的吸收光谱图对比;
图6为葡萄籽原花青素分析标准品和实施例1中制备的棕榈果序原花青素黄酮当量值对比;
图7为葡萄籽原花青素分析标准品和实施例1中制备的棕榈果序原花青素多酚当量值对比。
具体实施方式
以下结合附图实施例对本发明作进一步详细描述。
实施例1的棕榈果序原花青素的制备方法,包括以下步骤:
步骤一:取新鲜的采集自陕西咸阳的棕榈果序0.5kg,洗净、晾干、切碎,投入组织捣碎匀浆机中制成匀浆样品;向匀浆样品中依次加入1.2l浓度为0.1mol/l、ph值为4的柠檬酸盐缓冲液及抗坏血酸5g,混匀,得到混匀后的样品;
步骤二:将混匀后的样品置于超声波发生器中进行超声预处理,设定超声波频率40khz,功率350w,在50℃下处理5min,待处理完成后向样品中依次加入纤维素酶20000单位及果胶酶25000单位,混匀,调整溶液ph值为4,在50℃下处理150min,得到生物酶处理后的样品;
步骤三:向生物酶处理后的样品中加入1.5l体积分数为60%的乙醇作为提取溶剂,混匀;再将混匀后的样品置于超声波发生器中进行超声处理,设定超声波频率40khz,功率500w,在50℃下处理30min,处理完成后过滤,滤渣加入1.2l体积分数为60%的乙醇,在超声波频率40khz,功率500w,以及50℃下处理25min,处理完成后过滤,滤渣,再按照前述条件加入体积分数为60%的乙醇适量处理1次并过滤,合并3次滤液,滤液在40℃减压浓缩回收溶剂,得到的液体为棕榈果序原花青素粗提取物;
步骤四:取x-5大孔树脂,将大孔树脂装填入层析柱中后,以体积分数为90%的乙醇浸泡12h,之后换用去离子水洗脱至流出液澄清及无乙醇味为止;然后换用40g/l的hcl溶液浸泡12h,用去离子水洗脱至流出液为中性;再以30g/l的naoh溶液浸泡12h,以去离子水洗脱至流出液为中性,得到前处理后的大孔树脂;
步骤五:将前处理后的大孔树脂装填至层析柱中,用水以2bv/h的流速在温度25℃下平衡6h,得到平衡后的大孔树脂柱;将棕榈果序原花青素粗提取物配制成浓度为8mg/ml的溶液,调整ph值为6,在25℃下以1.0bv/h的流速上样,共上样16bv,待上样完成后关闭层析柱活塞,静置3h;静置后用水以2bv/h的流速,在25℃下洗脱未被大孔树脂吸附的原花青素及杂质,直至流出液澄清透明为止,总共用水10bv;
步骤六:配制体积分数为70%的乙醇,调整ph值至6,在25℃下,以1.0bv/h的流速,对吸附在大孔树脂上的棕榈果序原花青素进行洗脱,总共消耗体积分数为70%的乙醇4bv,收集洗脱液,将洗脱液在40℃减压浓缩回收溶剂,45℃下烘干,得到实施例1的棕榈果序原花青素成品。
分别取实施例1的棕榈果序原花青素样品及葡萄籽原花青素分析标准品,以分析纯甲醇溶解,稀释成浓度为0.01mg/ml、0.02mg/ml、0.03mg/ml、0.04mg/ml、0.05mg/ml以及0.06mg/ml的待测溶液;分别取待测液溶液,置于10mm石英比色皿中,以甲醇调零,记录200~400nm处的吸收曲线,找出最大吸收峰,并记录最大吸收峰处的吸光度值。
实施例1中所制备的棕榈果序原花青素的uv光谱如图1及图2所示,其甲醇溶液在280nm附近有一个对称的吸收峰,在255~260nm附近有一个吸收谷,在230nm附近有一个吸收峰,在300~400nm范围内无吸收峰、吸收谷;在浓度为50μg/ml时,使用10mm光程石英比色皿,以甲醇为空白,测得280nm处的吸光度值为0.841±0.004。
对实施例1中所制备的棕榈果序原花青素,使用280nm直接比色法测定并以市售葡萄籽原花青素分析标准品(uv纯度≥95%)作为分析对照品(图3),每g样品相对于葡萄籽原花青素分析标准品的当量值为876±12mg。
分析实施例1中所制备的棕榈果序原花青素中的黄酮含量。通过测定总黄酮含量对原花青素进行分析的方法属于分析原花青素的非特异性方法,当使用nano2-alcl3-naoh比色法分析时,阳性反应是样品中存在原花青素的必要不充分条件。黄酮含量使用亚硝酸钠-三氯化铝-氢氧化钠(nano2-alcl3-naoh)比色法测定并以而儿茶素分析标准品作为分析对照品,其结果如图4~6所示,每g样品相对于儿茶素分析标准品的当量值为641±11mg。
分析实施例1中所制备的棕榈果序原花青素中的总酚含量。总酚含量以folin-ciocalteu比色法测定并以没食子酸分析标准品作为分析对照品,其结果如图7所示,每g样品相对于没食子酸分析标准品的当量值为613±15mg。
实施例2的棕榈果序原花青素的制备方法,包括以下步骤:
步骤一:取新鲜的采集自陕西咸阳的棕榈果序1.0kg,洗净、晾干、切碎,投入组织捣碎匀浆机中制成匀浆样品;向匀浆样品中依次加入2l浓度为0.05mol/l、ph值为4.5的柠檬酸盐缓冲液及抗坏血酸5g,混匀,得到混匀后的样品;
步骤二:将混匀后的样品置于超声波发生器中进行超声预处理,设定超声波频率40khz,功率600w,在45℃下处理10min,待处理完成后向样品中依次加入纤维素酶60000单位及果胶酶100000单位,混匀,调整溶液ph值为4,在45℃下处理120min,得到生物酶处理后的样品;
步骤三:向生物酶处理后的样品中加入4.0l体积分数为70%的丙酮作为提取溶剂,混匀;再将混匀后的样品置于超声波发生器中进行超声处理,设定超声波频率28khz,功率1200w,在40℃下处理40min,处理完成后过滤,滤渣加入2.0l体积分数为50%的丙酮,在超声波频率28khz,功率1200w,以及40℃下处理25min,处理完成后过滤,滤渣,再按照前述条件加入体积分数为50%的丙酮适量处理2次并过滤,合并4次滤液,滤液在38℃减压浓缩回收溶剂,得到的液体为棕榈果序原花青素粗提取物;
步骤四:取hpd-100大孔树脂,将大孔树脂装填入层析柱中后,以体积分数为95%的乙醇浸泡24h,之后换用去离子水洗脱至流出液澄清及无乙醇味为止;然后换用20g/l的hcl溶液浸泡24h,用去离子水洗脱至流出液为中性;再以20g/l的naoh溶液浸泡24h,以去离子水洗脱至流出液为中性,得到前处理后的大孔树脂;
步骤五:将前处理后的大孔树脂装填至层析柱中,用水以2bv/h的流速在温度30℃下平衡5h,得到平衡后的大孔树脂柱;将棕榈果序原花青素粗提取物配制成浓度为14mg/ml的溶液,调整ph值为5.5,在30℃下以1.5bv/h的流速上样,共上样8bv,待上样完成后关闭层析柱活塞,静置4h;静置后用水以2bv/h的流速,在30℃下洗脱未被大孔树脂吸附的原花青素及杂质,直至流出液澄清透明为止,总共用水8bv;
步骤六:配制体积分数为80%的乙醇,调整ph值至6,在30℃下,以0.75bv/h的流速,对吸附在大孔树脂上的棕榈果序原花青素进行洗脱,总共消耗体积分数为80%的乙醇2.5bv,收集洗脱液,将洗脱液在45℃减压浓缩回收溶剂,45℃下烘干,得到实施例2的棕榈果序原花青素成品。
实施例2中,紫外光谱图与实施例1中所制备的棕榈果序原花青素一致,在浓度为50μg/ml时,使用10mm光程石英比色皿,以甲醇为空白,测得280nm处的吸光度值为0.825±0.008。
对实施例2中所制备的棕榈果序原花青素,使用280nm直接比色法测定并以市售葡萄籽原花青素分析标准品(uv纯度≥95%)作为分析对照品,每g样品相对于葡萄籽原花青素分析标准品的当量值为855±7mg。
分析实施例2中所制备的棕榈果序原花青素中的黄酮含量。黄酮含量使用亚硝酸钠-三氯化铝-氢氧化钠(nano2-alcl3-naoh)比色法测定并以而儿茶素分析标准品作为分析对照品,每g样品相对于儿茶素分析标准品的当量值为620±11mg。
分析实施例2中所制备的棕榈果序原花青素中的总酚含量。总酚含量以folin-ciocalteu比色法测定并以没食子酸分析标准品作为分析对照品,每g样品相对于没食子酸分析标准品的当量值为607±8mg。
实施例3的棕榈果序原花青素的制备方法,包括以下步骤:
步骤一:取新鲜的采集自陕西咸阳的棕榈果序0.3kg,洗净、晾干、切碎,投入组织捣碎匀浆机中制成匀浆样品;向匀浆样品中依次加入1.5l浓度为0.1mol/l、ph值为4.5的柠檬酸盐缓冲液及抗坏血酸1.2g,混匀,得到混匀后的样品;
步骤二:将混匀后的样品置于超声波发生器中进行超声预处理,设定超声波频率40khz,功率300w,在45℃下处理10min,待处理完成后向样品中依次加入纤维素酶12000单位及果胶酶30000单位,混匀,调整溶液ph值为4.5,在50℃下处理150min,得到生物酶处理后的样品;
步骤三:向生物酶处理后的样品中加入1.4l体积分数为80%的甲醇作为提取溶剂,混匀;再将混匀后的样品置于超声波发生器中进行超声处理,设定超声波频率40khz,功率500w,在40℃下处理30min,处理完成后过滤,滤渣加入1.5l体积分数为60%的甲醇,在超声波频率40khz,功率500w,以及40℃下处理20min,处理完成后过滤,滤渣,再按照前述条件加入体积分数为60%的甲醇适量处理1次并过滤,合并3次滤液,滤液在45℃减压浓缩回收溶剂,得到的液体为棕榈果序原花青素粗提取物;
步骤四:取ab-8大孔树脂,将大孔树脂装填入层析柱中后,以体积分数为80%的乙醇浸泡12h,之后换用去离子水洗脱至流出液澄清及无乙醇味为止;然后换用40g/l的hcl溶液浸泡24h,用去离子水洗脱至流出液为中性;再以30g/l的naoh溶液浸泡12h,以去离子水洗脱至流出液为中性,得到前处理后的大孔树脂;
步骤五:将前处理后的大孔树脂装填至层析柱中,用水以2bv/h的流速在温度20℃下平衡4h,得到平衡后的大孔树脂柱;将棕榈果序原花青素粗提取物配制成浓度为16mg/ml的溶液,调整ph值为5,在20℃下以1bv/h的流速上样,共上样12bv,待上样完成后关闭层析柱活塞,静置4h;静置后用水以2bv/h的流速,在20℃下洗脱未被大孔树脂吸附的原花青素及杂质,直至流出液澄清透明为止,总共用水10bv;
步骤六:配制体积分数为60%的乙醇,调整ph值至6,在20℃下,以0.5bv/h的流速,对吸附在大孔树脂上的棕榈果序原花青素进行洗脱,总共消耗体积分数为60%的乙醇2bv,收集洗脱液,将洗脱液在45℃减压浓缩回收溶剂,45℃下烘干,得到实施例3的棕榈果序原花青素成品。
实施例3中,紫外光谱图与实施例1中所制备的棕榈果序原花青素一致,在浓度为50μg/ml时,使用10mm光程石英比色皿,以甲醇为空白,测得280nm处的吸光度值为0.819±0.012。
对实施例3中所制备的棕榈果序原花青素,使用280nm直接比色法测定并以市售葡萄籽原花青素分析标准品(uv纯度≥95%)作为分析对照品,每g样品相对于葡萄籽原花青素分析标准品的当量值为844±23mg。
分析实施例3中所制备的棕榈果序原花青素中的黄酮含量。黄酮含量使用亚硝酸钠-三氯化铝-氢氧化钠(nano2-alcl3-naoh)比色法测定并以而儿茶素分析标准品作为分析对照品,每g样品相对于儿茶素分析标准品的当量值为623±15mg。
分析实施例3中所制备的棕榈果序原花青素中的总酚含量。总酚含量以folin-ciocalteu比色法测定并以没食子酸分析标准品作为分析对照品,每g样品相对于没食子酸分析标准品的当量值为590±17mg。
实施例4,以实施例3制备的棕榈果序原花青素为原料,制备涂膜保鲜剂,该涂膜保鲜剂由如下重量百分比的物质组成:食用果胶2~10%;食用醋酸0.1~2%;食用甘油0.5~5%;棕榈果序原花青素0.1~5%;余量为水。以实施例4为实验组,作为对比,制备了对照组的保鲜剂,以同等质量水替换棕榈果序原花青素,其余的物质组成与实验组相同。分别取鲜鸡蛋,浸入实验组和对照组的溶液中,浸泡5min后取出,沥干水分,置于阴凉处晾干,装箱保存。
实验结果表明,与对照组相比,添加了棕榈果序原花青素的实验组在相同的保存条件下,可将鲜鸡蛋的保存时间延长25~30%。因此添加棕榈果序原花青素可有效延长鸡蛋的保存期,表明棕榈果序原花青素可以显著提高涂膜保鲜技术在鸡蛋保鲜中的保鲜效果。
- 还没有人留言评论。精彩留言会获得点赞!