用于检测肝脏疾病的方法
联邦赞助的研究或开发
本发明是在由美国国立卫生研究院(nationalinstitutesofhealth)授予的批准号dk007191、eb012493、ca172738和dk078772下的政府资助下完成的。政府拥有本发明的某些权利。
本发明涉及通过分离和分析循环上皮细胞(cec)来检测和表征受试者的肝脏疾病的方法。
背景技术:
液体活检是指对源自实体器官并且进入血流的细胞物质进行采样。在局部癌症(stottsl等人,scitranslmed2010;2:25ra23;luccia等人,lancetoncol2012;13:688-95)和甚至胰腺癌前病变(rhimad等人,gastroenterology2014;146:647-51;fransesjw等人,oncologist2017)的情况下,可以通过液体活检检测到循环上皮细胞(cec),表明循环上皮细胞的存在并非癌变所独有。
由于cec在血流中的稀有性和用于细胞捕获的抗原的可变表达,因此分离cec是一项技术挑战。例如,在两项独立研究中,epcam依赖性veridex平台得出肝细胞癌(hcc)cec检出率仅为35%和41%(kelleyrk等人,bmccancer2015;15:206;sunyf等人,hepatology2013;57:1458-68)。为了克服该限制,已经开发了一种称为ichip的抗原不确定(antigen-agnostic)细胞分选装置,该装置分离cec,同时保持细胞活力和高质量的rna含量。此前,已将ichip装置与基于已确立的肝特异性标志物的rna标记(rnasignature)组合,以创建用于hcc中cec的富集和检测的分析方法(kalinichm等人,procnatlacadsciusa2017;114:1123-1128)。
用于hcc的非侵入性诊断的其它方法尚未成功实现高检出率。例如,最近的研究显示,通过结合无细胞dna和基于蛋白质血液的生物标志物来检测hcc对于预测hcc产生仅44%的准确度,这很可能是由于缺乏常见的频发突变(recurrentmutation)和hcc固有的特异性蛋白标志物(参见cohenjd等人,science2018)。
通过使用非侵入性方法来诊断某些肝脏疾病的另一个挑战是cec可能存在于两种不同的疾病中,使得cec的定量分析可能无法提供区分这两种疾病的必要信息。
迄今为止,还没有非侵入性的基于血液的方法可用于准确检测例如hcc等肝脏疾病、或者在患有慢性肝脏疾病(cld)的受试者中区分不同的肝脏疾病或肝脏疾病的不同分期。
因此,需要用于以高准确度来检测例如hcc等肝脏疾病的存在并且确定cld患者中肝脏疾病的分期的非侵入性方法。
技术实现要素:
本发明至少部分地基于以下发现:肝cec(hcec)并非癌变所独有,而且还可以存在于患有非癌症疾病或病况例如慢性肝脏疾病(cld)的受试者中。此外,本发明至少部分地基于以下发现:可以定量地或定性地分析患有cld的受试者中的hcec,以准确地检测例如肝细胞癌(hcc)等癌症的存在,和/或准确地表征例如肝纤维化等肝脏疾病或病况的不同分期(例如早期或晚期)。
一方面,本发明涉及测量受试者的循环上皮细胞(cec)中肝细胞癌(hcc)分类器基因(classifiergenes)的表达水平的方法,其中hcc分类器基因包括tesc、osbp2、slc6a8、sept5、f2rl3、e2f1、ezh2、cdc20、ccna2、ccnb1、plxnb3、cdc6、mybl2、apobec3b、spp1、akr1b10、top2a、aspm、slc6a9、recql4、nusap1、plvap、fmo1、pdzk1ip1、和fbxo32中的一种或多种。
在一些实施方案中,hcc分类器基因由tesc、osbp2、slc6a8、sept5、f2rl3、e2f1、ezh2、cdc20、ccna2、ccnb1、plxnb3、cdc6、mybl2、apobec3b、spp1、akr1b10、top2a、aspm、slc6a9、recql4、nusap1、plvap、fmo1、pdzk1ip1、和fbxo32中的一种或多种组成。
在一些实施方案中,hcc分类器基因由tesc、osbp2、slc6a8、sept5、f2rl3、e2f1、ezh2、cdc20、ccna2、ccnb1、plxnb3、cdc6、mybl2、apobec3b、spp1、akr1b10、top2a、aspm、slc6a9、recql4、nusap1、plvap、fmo1、pdzk1ip1、和fbxo32组成。
在一些实施方案中,hcc分类器基因还包括选自由以下组成的组中的一种、两种、三种或更多种另外的基因:actg2、adm2、afp、agr2、aldh3a1、alpk3、amigo3、ankrd65、anln、ap1m2、arhgap11a、arhgef39、asf1b、asphd1、aurka、axin2、baiap2l2、bex2、c15orf48、c1orf106、c1qtnf3、c6orf223、ca12、ca9、camk2n2、cap2、cbx2、ccdc170、ccdc28b、ccdc64、ccne2、ccnf、cd109、cd34、cdc25a、cdc7、cdca5、cdca8、cdh13、cdk1、cdkn2a、cdkn2c、cdt1、celf6、cenpf、cenph、cenpl、cenpu、cenpw、ckb、cnnm1、col15a1、col4a5、col7a1、col9a2、crip3、cspg4、ctnnd2、cxorf36、cyp17a1、dlk1、dmkn、dscc1、dtl、duox2、ect2、eef1a2、efna3、ephb2、eppk1、etv4、fabp4、fam111b、fam3b、fam83d、fancd2、fanci、fbxl18、fermt1、fgf19、flnc、flvcr1、foxd2-as1、foxm1、fxyd2、gabre、gal3st1、gcnt3、gins1、gjc1、gmnn、gnaz、golga2p7、gpc3、gpr64、gpsm1、hrct1、igf2bp2、igsf1、igsf3、iqgap3、itga2、itpka、kiaa0101、kif11、kifc1、kifc2、kntc1、krt23、lama3、lef1、lgr5、linc00152、lingo1、lpl、lrrc1、lypd1、mad2l1、maged4、maged4b、mapk12、mapk8ip2、mapt、mcm2、mdga1、mdk、mfap2、misp、mki67、mmp11、mns1、mpz、msc、msh5、mtmr11、muc13、muc5b、myh4、naaladl1、nav3、ncapg、ndufa4l2、neb、nkd1、nmb、notch3、notum、npm2、nqo1、nrcam、nt5dc2、nts、obscn、olfml2a、olfml2b、paqr4、peg10、pi3、plce1、plch2、plk1、plxdc1、podxl2、pole2、ppap2c、prc1、ptges、ptgfr、pthlh、ptk7、ptp4a3、pttg1、pycr1、racgap1、rbm24、rhbg、rnf157、robo1、rp4-800g7.2、rps6kl1、rrm2、s100a1、scgn、5-sep、serpina12、sez6l2、sfn、sgol2、slc22a11、slc51b、slc6a2、sncg、soat2、sp5、sparcl1、spink1、stil、stk39、sult1c2、tcf19、tdgf1、thy1、tk1、tmc5、tmem132a、tmem150b、tnfrsf19、tnfrsf25、tonsl、tpx2、trim16、trim16l、trim31、trim45、ttc39a、ubd、ube2c、ube2t、ugt2b11、ush1c、vsig10l、wdr62、wdr76、和zwint。
一方面,本发明涉及用于在患有慢性肝脏疾病(cld)的受试者中检测hcc的存在的方法,该方法包括:(a)测量受试者的cec中的本文所述的hcc分类器基因的表达水平;(b)将受试者的cec中的hcc分类器基因的表达水平与hcc分类器基因的参比表达水平进行比较,从而确定hcc的存在。
在一些实施方案中,hcc分类器基因的表达水平用于计算hcc得分,并且将计算出的hcc得分与参比得分进行比较,基于高于参比得分的hcc得分的存在来确定hcc的存在。
在一些实施方案中,使用随机森林分析来计算hcc得分。
在一些实施方案中,使用多元逻辑回归建模方法将hcc分类器基因的表达水平与hcc分类器基因的参比表达水平进行比较。
在一些实施方案中,通过以下步骤测量循环上皮细胞(cec)中的hcc分类器基因的表达水平:(a)从受试者获得包括血液的样品;(b)通过基于尺寸的排除从样品中除去红细胞、血小板和血浆;(c)通过磁泳法从样品中除去白细胞(wbc);和(d)使用rna测序、qrt-pct、rna原位杂交、蛋白质微阵列、或质谱法和蛋白质谱来测量cec中一组基因的表达。
在一些实施方案中,检测到的hcc是早期hcc或晚期hcc。
在一些实施方案中,用于在患有cld的受试者中检测hcc的存在的方法还包括:(a)通过超声成像、动态ct、mri成像、穿刺活检和/或活检确认或已经确认患者中hcc的存在;和(b)如果确认患者中hcc的存在,则通过hcc组织的手术切除、hcc组织的射频消融、hcc组织的栓塞、hcc组织的栓塞、化疗和/或冷冻疗法来对受试者治疗hcc或使受试者治疗hcc。
一方面,本发明涉及监测患有cld的受试者的hcc的发展的方法,该方法包括:(a)在初始时间点检测如本文所述的患有cld的受试者中hcc的存在,并且如果hcc得分低于参比得分,则(b)在一个或多个后续时间点进行检测步骤。在一些实施方案中,在一个或多个后续时间点进行检测步骤,直到确定hcc的存在。在一些实施方案中,初始时间点和每个后续时间点相隔约三个月、六个月或一年。
一方面,本发明涉及在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法,该方法包括:(a)检测受试者的血液样品中的cec的浓度;(b)将受试者的血液样品中的cec的浓度与参比值进行比较;(c)将那些血液样品中的cec浓度低于参比值的受试者诊断为患有早期纤维化;和(d)将那些血液样品中的cec浓度高于参比值的受试者诊断为患有晚期纤维化(latestagefibrosis)。
在一些实施方案中,受试者患有乙型肝炎。在一些实施方案中,通过免疫荧光来测量cec的浓度。在一些实施方案中,通过检测磷脂酰肌醇蛋白聚糖-3(gpc3)和/或细胞角蛋白(ck)来测量cec的浓度。
一方面,本发明涉及监测患有cld的受试者的进展期纤维化(advancedfibrosis)的发展的方法,该方法包括:(a)在本文所述的患有cld的受试者中进行区分早期肝纤维化和晚期肝纤维化的存在的方法;并且如果受试者的血液样品中的cec的浓度低于参比值,则(b)在一个或多个后续时间点进行在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法。
在一些实施方案中,在一个或多个后续时间点进行在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法,直到该受试者被诊断为患有晚期纤维化。在一些实施方案中,初始时间点和每个后续时间点相隔约三个月、六个月或一年。
一方面,本发明涉及监测正在治疗以预防纤维化或hcc的进展的患有cld的受试者的方法,该方法包括:(a)进行本文所述的在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法;并且如果受试者的血液样品中的cec的浓度低于参比值,则在一个或多个后续时间点进行在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法;和(b)进行本文所述的在患有cld的受试者中检测hcc的存在的方法,并且如果表达水平的hcc得分低于参比得分,则在一个或多个后续时间点进行该检测方法。
在一些实施方案中,在一个或多个后续时间点进行在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法,直到该受试者被诊断为患有晚期纤维化,和/或在一个或多个后续时间点进行在患有cld的受试者中检测hcc的存在的方法,直到确定hcc的存在。在一些实施方案中,用于进行在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法或在患有cld的受试者中检测hcc的存在的方法的第一初始时间点和每个后续时间点相隔约三个月、六个月或一年,并且第二初始时间点和每个后续时间点相隔约三个月、六个月或一年。
在一些实施方案中,使用微流控装置来纯化或富集受试者血液中的cec。在一些实施方案中,微流控装置为ichip装置。
除非另有定义,否则本文中使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常所理解的相同含义。本文描述了用于本发明的方法和材料;另外,也可以使用本领域已知的合适方法和材料。材料、方法和实例仅是说明性的,并且不旨在于限制。本文提及的所有出版物、专利申请、专利、序列、数据库条目和其它参考文献通过引用以其整体并入本文。另外,美国专利申请us2016/0312298a1特别地通过引用以其整体并入本文,并且在一些实施方案中,本文描述的方法可以与该申请中描述的方法结合使用。在有冲突的情况下,以包括定义的本说明书为准。
根据以下详细描述和附图以及权利要求,本发明的其它特征和优点将变得显而易见。
附图说明
该专利或申请文件包含至少一幅彩色附图。专利局将在要求和支付必要费用时提供带有彩色附图的本专利或专利申请公开的副本。
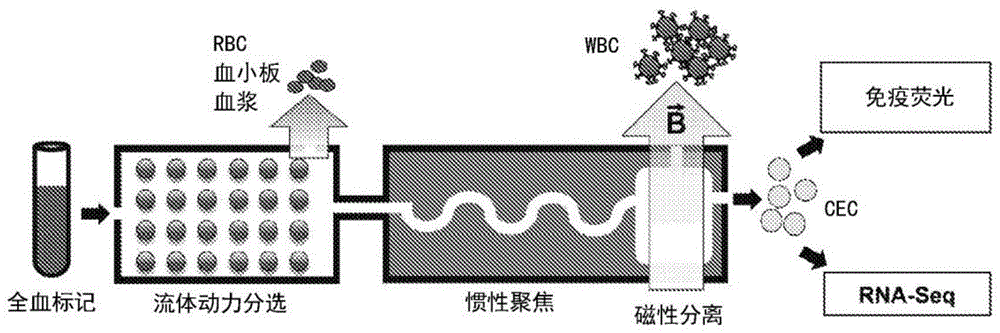
图1是用于耗竭造血细胞的ichip抗原不确定细胞分选装置(ichip装置)的示意图。使用ichip装置处理样品以富集样品的cec,其可以通过免疫荧光或rna测序来分析。
图2a示出来自患有cld的受试者的外周血的免疫荧光标记的hcec的荧光显微图像。使用ichip装置处理来自患有hcc或cld的患者的血液样品以分离cec,并且对dapi、cd45、磷脂酰肌醇蛋白聚糖-3(gpc3)和广谱细胞角蛋白(ck-ws)进行染色。显示白细胞(wbc)以用于比较。
图2b是示出来自健康供体(hd)、患有cld的患者、患有hcc的患者、或接受过hcc治疗且无恶性疾病迹象的患者(hccned)的经ichip装置处理的血液样品中免疫荧光标记的hcec的检测的图。通过mann-whitney检验计算p值。
图2c是示出患有早期肝纤维化的cld患者和患有进展期纤维化的患者中hcec的检测的图。通过mann-whitney检验计算p值。
图3a是从对照血液、加入有1-50个hepg2细胞的对照血液中的hcec的rna-seq和hepg2单细胞rna-seq获得的hepg2基因表达标记的热图(heatmap)。
图3b是从来自cld患者、hcc患者的hcec的rna-seq和从流式分选的wbc获得的肝特异性基因标记的热图(b,b细胞;c,细胞毒性t细胞;h,辅助t细胞;m,单核细胞;n,nk细胞;g,粒细胞)。热图单位表示为log2(每百万的读数+1)。
图3c是本文所述的随机森林算法的示意图。
图3d是示出cld、早期hcc和晚期hcc中的hcc得分(来自随机森林分类器的投票分数(votefraction))的图。通过mann-whitney检验计算p值。
图4a是示出来自健康供体(hd)或者患有cld的患者(cld)、患有hcc的患者、或之前患有hcc但在接受hcc治疗后不显示恶性疾病迹象的患者(hccned)的经ichip装置处理的血液样品中磷脂酰肌醇蛋白聚糖-3(gpc3)阳性cec的检测的图。通过mann-whitney检验计算p值。
图4b是示出来自健康供体(hd)或者患有cld的患者(cld)、患有hcc的患者(hcc)、或之前患有hcc但在接受hcc治疗后不显示恶性疾病迹象的患者(hccned)的经ichip装置处理的血液样品中表达广谱细胞角蛋白的cec(ck+细胞)的检测的图。通过mann-whitney检验计算p值。
图4c是示出通过纤维化阶段(将早期定义为f1或f2,并且将进展期纤维化定义为f3或f4)分层的hbvcld患者(无hcc)中hcec(细胞为ck+或gpc3+)的检测的图。通过mann-whitney检验计算p值。
图4d是示出通过肝脏疾病的病因分层的cld患者中的cec浓度的图:非酒精性脂肪性肝炎(nash);乙型肝炎病毒(hbv);丙型肝炎病毒(hcv);自身免疫性肝炎(aih);原发性硬化性胆管炎(psc)。通过mann-whitney检验计算p值。
图5a是示出cld患者、接受治疗但在抽血时仍患有活动性疾病的hcc患者(hccontx)、和未接受过治疗的患有活动性hcc的患者(hccnotx)中cec的hcc得分(来自随机森林分类器的投票分数)的图。所示的p值通过mann-whitney检验来计算。
图5b是示出通过多元逻辑回归建模创建的hcc分类器的受试者操作特征(receiveroperatingcharacteristic,roc)曲线的图。
图5c是示出hcc随机森林分类器的roc曲线的图。
具体实施方式
本发明至少部分地基于以下发现:hcec并非癌变所独有,而且还可以存在于患有非癌症疾病或病况例如慢性肝脏疾病(cld)的受试者中。此外,本发明至少部分地基于以下发现:可以定量地或定性地分析患有cld的受试者中的hcec,以准确地检测例如肝细胞癌(hcc)等癌症的存在,和/或准确地表征例如肝纤维化等肝脏疾病或肝脏病况的分期(例如早期或晚期)。
如本文所证明的,定量地(例如,通过免疫荧光)和定性地(例如,hcc分类器基因的基因表达谱或表达水平)检测在血流中循环的来自患病肝脏的细胞(即,hcec)用于hcc和cld的诊断。该液体活检的重要应用包括例如hcc等肝脏疾病或病况的检测或诊断、cld病因确定、肝纤维化分期、和hcc监控或监测。本发明可以应用于患有例如cld等肝脏病况的患者的诊断和监测二者。
如本文所使用的,针对疾病或病况的短语“准确地诊断”和“准确地检测”是指以高度的灵敏度(即,当存在疾病或病况时检测出疾病或病况的真阳性率)或高度的特异性(即,当不存在疾病或病况时不检测出疾病或病况的真阴性率)预测疾病或病况的存在。在一些实施方案中,短语“准确地诊断”和“准确地检测”也可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阳性率检测到疾病或病况的存在。在一些实施方案中,短语“准确地诊断”和“准确地检测”可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阴性率检测到疾病或病况的存在。
如本文所使用的,针对两种疾病或病况的短语“准确地区分”可以指以高度的灵敏度(即,当存在第一疾病或病况时检测出第一疾病或病况,即真阳性率)或高度的特异性(即,当不存在第一疾病或病况时不检测出第一疾病或病况,即真阴性率)检测第一疾病或第一病况的存在,而无论是否还存在或不存在第二疾病或病况。在一些实施方案中,短语“准确地区分”可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阳性率检测出疾病或病况的存在。在一些实施方案中,短语“准确地区分”可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阴性率检测出疾病或病况的存在。
如本文中所使用的,针对疾病或病况的不同分期的短语“准确地区分”可以指以高度的灵敏度(即,当疾病或病况处于某分期时,检测出疾病或病况的该分期,即真阳性率)或高度的特异性(即,当疾病或病况不处于某分期时,不会检测出疾病或病况的该分期,即真阴性率)检测疾病的特定分期(例如,肝脏中的进展期纤维化)的存在,使得可以预测病况或疾病的特定分期。在一些实施方案中,短语“准确地区分”可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阳性率检测出疾病或病况的分期的存在。在一些实施方案中,短语“准确地诊断”可以意指能够以至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%、至少约99%、和至少约99.9%的真阴性率检测出疾病或病况的存在。
如本文所使用的,术语“循环上皮细胞(cec)”可以指从组织(例如,患病的组织、肿瘤组织或非肿瘤组织)脱落并且存在于血液中(即循环中)的上皮起源的细胞。在下文中描述了可用于从血液的其它组分中鉴定和/或分离cec的细胞标志物(例如标志物基因)。在一些实施方案中,来自患有肝脏疾病(例如,hcc和/或cld)的受试者的cec主要是肝cec(hcec),例如,如通过具有在肝细胞中表达的基因(例如,gpc3和ck)的cec的免疫荧光染色所确定的。
如本文所使用的,术语“慢性肝脏疾病(cld)”是指涉及肝实质的进行性破坏和再生的肝脏的疾病过程。在一些实施方案中,cld可导致纤维化肝硬化。在一些其它实施方案中,cld可导致并发症,例如门静脉高压症(例如腹水、脾功能亢进、以及下段食管静脉曲张和直肠静脉曲张),肝肺综合征,肝肾综合征,脑病或hcc。cld也可以指持续六个月、一年、两年、三年、四年、五年或超过五年时间的肝脏疾病。cld可以由乙型肝炎病毒,丙型肝炎病毒,巨细胞病毒,爱泼斯坦-巴尔病毒(epsteinbarvirus),黄热病病毒,酒精性肝病,和/或由甲氨蝶呤、胺碘酮、呋喃妥因或对乙酰氨基酚引起的药物诱发的肝脏疾病引起。在其它实施方案中,cld可以由非酒精性脂肪肝疾病、血色素沉着症、威尔逊氏病、或者自身免疫反应例如原发性胆汁性胆管炎或原发性硬化性胆管炎引起。
如本文所使用的,术语“监测”或“监控”是指周期性地评估受试者或患者(例如,有发生病况的风险的受试者)的疾病或病况的存在。在一些实施方案中,周期性的评估可以发生在约每天、约每隔一天、约每周一次、约每隔一周一次、约每个月、约每2个月、约每3个月、约每4个月、约每5个月、约每6个月、约每7个月、约每8个月、约每9个月、约每年、约每18个月、约每2年、约每3年、约每4年、约每5年、约每6年、约每7年、约每8年、约每9年或约每10年。对受试者或患者是否存在疾病或病况的这种反复评估可以持续直到(1)在受试者或患者中检测到该疾病或病况;(2)患者不再有发生该疾病或病况的风险;(3)由接受监测的受试者或实施监测的人酌情决定;或(4)由于其它原因导致有必要中止反复评估。可以在监测的过程期间调整评估受试者是否存在疾病或病况的间隔。
如本文所使用的,术语“集成学习方法(ensemblelearningmethod)”是指可以被训练然后用于做出预测的例如随机森林等监督学习算法(supervisedlearningalgorithm)。
如本文所使用的,术语“肝细胞癌(hcc)”是指在患有cld的受试者中普遍存在的一种原发性肝癌。hcc可以在患有各种病因的潜在肝硬化性肝病的患者中发生,所述患者包括具有hbv感染的阴性标志物并且具有整合在肝细胞基因组中的hbvdna的患者。在ghouriya等人,jcarcinog2017;16:1(通过引用并入本文)中描述了hcc的流行病学、病因学和癌变。
如本文所使用的,短语“早期hcc”可以指在米兰标准(milancriteria)内的hcc。如本文中所使用的,短语“晚期hcc”可以指在米兰标准外的hcc。米兰标准要求患有hcc的受试者满足以下标准:hcc为小于5cm的一处病变,或者至多3处病变,每处小于3cm;无肝外表现;并且没有明显的血管浸润迹象。换言之,“早期hcc”符合所有米兰标准,并且“晚期hcc”不符合所有米兰标准。
如本文所使用的,术语“早期肝纤维化”和“晚期肝纤维化”分别指如由metavir分类所定义的f1或f2期、以及f3或f4期。
本文所述的方法通过使用例如随机森林分类器等基于集成学习方法的分类器来检测和分析患者的cec中的一组基因的表达,可用于在患有例如cld等非癌性疾病状况的患者中准确地诊断或预测例如hcc等癌症的存在。
在一些实施方案中,可以分析(例如,定性地)来自患有cld的受试者(例如,患有乙型肝炎的受试者或感染有乙型肝炎病毒的受试者)的hcec,以准确地区分患有和不患有hcc的受试者。在其它实施方案中,可以定量地测量来自患有cld的受试者的hcec,以准确地区分患有早期肝纤维化的受试者和患有晚期肝纤维化的受试者。
如本文所证明的,例如hcc等癌症的存在和例如cld等非癌症疾病或病况的存在与增加的cec的存在有关。增加的cec的存在也与先前的经治疗导致没有疾病的临床迹象(例如,在经历根治性治疗(curativetreatment)且没有疾病的临床迹象的hcc患者中)的癌症(例如hcc)的存在有关。
因此,该方法可以包括使用各种统计和计算预测方法(例如,例如随机森林分类器等集成学习方法或例如多元逻辑回归等统计方法)来检测和分析一组基因(例如,hcc分类器基因),从而检测例如hcc等癌症的存在。
在一些实施方案中,该方法可以在早期检测到癌症的存在,这是使用例如超声成像、动态ct、mri成像、穿刺活检或活检等目前已知的方法难以检测的。
在一些实施方案中,微流控(例如,“芯片实验室(lab-on-a-chip)”或ichip装置)在本方法中可用于分离、纯化、富集或制备cec。此类装置已成功用于微流控流式细胞术、连续的基于尺寸的分离、色谱分离或磁泳分离。例如,在美国专利申请us2016/0312298a1(其通过引用并入本文)中描述了ichip装置和此类装置的各种其它实施方案,其可以用于从细胞的混合物中分离hcec,或者制备hcec的富集群体。特别地,此类装置可用于从例如全血等复杂混合物中分离hcec。
在一些实施方案中,与初始样品混合物相比,该装置保留至少75%,例如80%、90%、95%、98%或99%的期望细胞,同时以相对于一种或多种不期望的细胞类型至少100倍,例如1000、10,000、100,000或甚至1,000,000倍富集期望细胞的群体。在一个实例中,检测模块可以与分离或富集装置流体连通。检测模块可以使用本文公开的任何检测方法或本领域已知的其它方法来操作。例如,检测模块包括显微镜、细胞计数器、磁体、生物腔激光器(biocavitylaser)(参见例如gourley等人,j.phys.d:appl.phys.,36:r228-r239(2003))、质谱仪、pcr装置、rt-pcr装置、微阵列、用于进行rna原位杂交的装置、或高光谱成像系统(参见例如vo-dinh等人,ieeeeng.med.biol.mag.,23:40-49(2004))。在一些实施方案中,计算机终端可以连接至检测模块。例如,检测模块可以检测与目标细胞、蛋白质或核酸(例如hcc分类器基因的转录物或编码的蛋白质)选择性结合的标记。
在一些实施方案中,微流控系统包括(i)用于分离或富集cec(例如hcec)的装置;(ii)用于裂解富集的cec的装置;和(iii)用于检测基因转录物(例如,hcc分类器基因的转录物)或编码的蛋白质的装置。
在一些实施方案中,使用如本文所述的微流控装置制备的cec群体用于使用已知的分子生物学技术来分析基因转录物的表达或蛋白质,所述分子生物学技术例如如上文所述以及sambrook,molecularcloning:alaboratorymanual,第三版(coldspringharborlaboratorypress;第3版(jan.15,2001));和shortprotocolsinmolecularbiology,ausubel等人,eds.(currentprotocols;第52版(nov.5,2002))中所述。
通常,本文描述了用于检测和/或定量富集的cec群(例如,ctc)中的可用于癌症诊断的分类器基因的表达或编码的蛋白质的装置,并且该装置可以用于例如上皮起源的肿瘤等癌症的早期检测,例如肝癌、胰腺癌、肺癌、乳腺癌、前列腺癌、肾癌、卵巢癌或结肠癌的早期检测。
如本文所述,短语“差异表达分析”可以指对样品(例如,细胞,例如,cec,例如,hcec)中的单个基因(例如,单个hcc分类器基因)的表达水平和/或多个基因(例如,多个hcc分类器基因)的表达模式进行计算或统计分析。术语“差异表达”可以意指过表达(以高于参比值的水平表达基因)或低表达(以低于参比值的水平表达基因)。在一些实施方案中,差异表达分析可以将样品中的表达水平或模式与参比值(例如,来自未患病的对应细胞或组织的样品中的一个或多个基因的表达水平或模式)进行比较。在其它实施方案中,可以将表达水平或模式相对于一个或多个对照基因的表达水平进行标准化,或者可以以非相对方式(例如,每体积的转录物拷贝或绝对拷贝数)进行定量。可以通过任意已知方法,例如rna测序、qrt-pct、rna原位杂交、蛋白质微阵列、和/或质谱法和蛋白质谱来测量基因表达水平。可以使用其它已知的生物化学技术或分子生物学技术来检测基因的表达。在一些实施方案中,rna测序和qrt-pct是用于测量基因表达水平的优选方法。
可以通过任意一种已知的统计或计算方法,例如,例如随机森林分类器等集成学习方法或者例如多元逻辑回归等统计方法来进行差异表达分析。
一方面,本发明提供包括测量受试者的循环上皮细胞(cec)中的肝细胞癌(hcc)分类器基因的表达水平的方法。将受试者的cec的hcc分类器基因的过表达确定为高度预测受试者中hcc的存在(参见例如,实施例1-4)。在一些实施方案中,hcc分类器基因包括tesc、osbp2、slc6a8、sept5、f2rl3、e2f1、ezh2、cdc20、ccna2、ccnb1、plxnb3、cdc6、mybl2、apobec3b、spp1、akr1b10、top2a、aspm、slc6a9、recql4、nusap1、plvap、fmo1、pdzk1ip1、和fbxo32中的一种、两种、三种或更多种(例如,全部)。在一些实施方案中,hcc分类器基因可以包括tesc、osbp2、slc6a8、sept5、f2rl3、e2f1、ezh2、cdc20、ccna2、ccnb1、plxnb3、cdc6、mybl2、apobec3b、spp1、akr1b10、top2a、aspm、slc6a9、recql4、nusap1、plvap、fmo1、pdzk1ip1的全部。在其它实施方案中,hcc分类器基因还可以包括在hcc中过表达的一种或多种其它基因,例如以下基因中的一种或多种:actg2、adm2、afp、agr2、aldh3a1、alpk3、amigo3、ankrd65、anln、ap1m2、arhgap11a、arhgef39、asf1b、asphd1、aurka、axin2、baiap2l2、bex2、c15orf48、c1orf106、c1qtnf3、c6orf223、ca12、ca9、camk2n2、cap2、cbx2、ccdc170、ccdc28b、ccdc64、ccne2、ccnf、cd109、cd34、cdc25a、cdc7、cdca5、cdca8、cdh13、cdk1、cdkn2a、cdkn2c、cdt1、celf6、cenpf、cenph、cenpl、cenpu、cenpw、ckb、cnnm1、col15a1、col4a5、col7a1、col9a2、crip3、cspg4、ctnnd2、cxorf36、cyp17a1、dlk1、dmkn、dscc1、dtl、duox2、ect2、eef1a2、efna3、ephb2、eppk1、etv4、fabp4、fam111b、fam3b、fam83d、fancd2、fanci、fbxl18、fermt1、fgf19、flnc、flvcr1、foxd2-as1、foxm1、fxyd2、gabre、gal3st1、gcnt3、gins1、gjc1、gmnn、gnaz、golga2p7、gpc3、gpr64、gpsm1、hrct1、igf2bp2、igsf1、igsf3、iqgap3、itga2、itpka、kiaa0101、kif11、kifc1、kifc2、kntc1、krt23、lama3、lef1、lgr5、linc00152、lingo1、lpl、lrrc1、lypd1、mad2l1、maged4、maged4b、mapk12、mapk8ip2、mapt、mcm2、mdga1、mdk、mfap2、misp、mki67、mmp11、mns1、mpz、msc、msh5、mtmr11、muc13、muc5b、myh4、naaladl1、nav3、ncapg、ndufa4l2、neb、nkd1、nmb、notch3、notum、npm2、nqo1、nrcam、nt5dc2、nts、obscn、olfml2a、olfml2b、paqr4、peg10、pi3、plce1、plch2、plk1、plxdc1、podxl2、pole2、ppap2c、prc1、ptges、ptgfr、pthlh、ptk7、ptp4a3、pttg1、pycr1、racgap1、rbm24、rhbg、rnf157、robo1、rp4-800g7.2、rps6kl1、rrm2、s100a1、scgn、5-sep、serpina12、sez6l2、sfn、sgol2、slc22a11、slc51b、slc6a2、sncg、soat2、sp5、sparcl1、spink1、stil、stk39、sult1c2、tcf19、tdgf1、thy1、tk1、tmc5、tmem132a、tmem150b、tnfrsf19、tnfrsf25、tonsl、tpx2、trim16、trim16l、trim31、trim45、ttc39a、ubd、ube2c、ube2t、ugt2b11、ush1c、vsig10l、wdr62、wdr76、和zwint。
另一方面,本发明提供用于在患有慢性肝脏疾病(cld)的受试者中检测hcc的存在的方法。该方法可以包括:(a)测量受试者的cec中的hcc分类器基因的表达水平;(b)将受试者的cec中的hcc分类器基因的表达水平与hcc分类器基因的参比表达水平进行比较,从而确定hcc的存在。
另一方面,本发明提供监测患有cld的受试者的hcc的发展的方法。该方法可以包括:(a)在初始时间点测量受试者的cec中的hcc分类器基因的表达水平,并且将受试者的cec中的hcc分类器基因的表达水平与hcc分类器基因的参比表达水平进行比较;并且如果hcc分类器基因的表达水平低于参比水平,则(b)在后续时间点并且任选地在另外的时间点再次进行该步骤,例如,直到hcc分类器基因的表达水平高于参比水平。可以通过首先计算hcc得分(例如,来自rf分类器的投票分数)或者表示受试者的cec中hcc分类器基因的差异表达程度的其它量度(metric),与参比得分或其它参比量度值进行比较,从而形成该评估。
另一方面,本发明提供在患有cld的受试者中区分早期肝纤维化和晚期肝纤维化的存在的方法。该方法可以包括:(a)检测受试者的血液样品中的cec的浓度;(b)将受试者的血液样品中的cec的浓度与参比值进行比较;(c)如果受试者的cec的血液浓度低于参比值,则诊断该受试者患有早期纤维化;和(d)如果受试者的cec的血液浓度高于参比值,则诊断该受试者患有晚期纤维化。
另一方面,本发明提供监测患有cld的受试者的进展期纤维化的发展的方法。该方法可以包括:(a)检测受试者的血液样品中的cec的浓度,并且将血液cec浓度与参比值进行比较;并且如果受试者的血液样品中的cec的浓度低于参比值,则(b)在一个或多个后续时间点进行相同的检测和比较步骤,例如,直到受试者的血液样品中的cec的浓度高于参比值。
在一些实施方案中,使用hcc分类器基因的表达水平来计算hcc得分,优选使用随机森林分析,并且该方法包括将hcc得分与参比得分进行比较,其中基于高于参比得分的hcc得分的存在来确定hcc的存在。
在一些实施方案中,使用多元逻辑回归建模方法将hcc分类器基因的表达水平与hcc分类器基因的参比表达水平进行比较。
在一些实施方案中,通过以下步骤测量循环上皮细胞(cec)中的hcc分类器基因的表达水平:(a)从受试者获得包括血液的样品;(b)通过基于尺寸的排除从样品中除去红细胞、血小板和血浆;(c)通过磁泳法从样品中除去白细胞(wbc);和(d)使用rna测序、qrt-pct、rna原位杂交、蛋白质微阵列、或质谱法和蛋白质谱来测量cec中一组基因的表达。
在一些实施方案中,检测到的hcc是早期hcc或晚期hcc。
在一些实施方案中,该方法还包括:(a)通过超声成像、动态ct、mri成像、穿刺活检和/或活检确认或已经确认患者中hcc的存在;和(b)如果确认患者中hcc的存在,则通过hcc组织的手术切除、hcc组织的射频消融、hcc组织的栓塞、hcc组织的栓塞、化疗和/或冷冻疗法来对受试者治疗hcc或使受试者治疗hcc。
在一些实施方案中,用于测量和比较血液cec浓度或者用于测量和比较hcc分类器基因的初始时间点和每个后续时间点相隔约三个月、六个月或一年。在一些实施方案中,受试者患有乙型肝炎或不患有乙型肝炎。在一些实施方案中,通过免疫荧光来测量cec的浓度。在一些实施方案中,通过检测磷脂酰肌醇蛋白聚糖-3(gpc3)和/或细胞角蛋白(ck)来测量cec的浓度。
肝脏疾病的诊断和治疗
一旦在受试者中检测到例如cld或hcc等肝脏疾病,就可以使用其它方法来确认例如cld或hcc等疾病的存在。
hcc的诊断或检测
可以通过使用传统方法分析血液样品来进一步确认或诊断hcc,所述传统方法包括全血细胞计数(cbc)、电解质、肝功能测试(lft)、凝血研究(例如国际标准化比率(internationalnormalizedratio,inr)和部分凝血活酶时间(partialthromboplastintime,ptt))、以及甲胎蛋白(afp)测定。
可以使用各种成像技术来诊断hcc。例如,超声检查法提供了相对廉价的筛查方法,而无需磁共振成像(mri)的花费、或者对计算机断层扫描(ct)所需的放射和潜在肾毒性造影剂的暴露。据报道,超声检查法作为一种筛查方法在肝硬化人群中具有60%的灵敏度和97%的特异性,并且已被证明具有成本效益。由于这种低灵敏度,应当使用进一步的成像研究和可能的活检来确认超声检查的结果。
可以使用ct成像来检测hcc,优选在动脉相具有早期增强并且在三相造影扫描(three-phasecontrastscan)的门静脉相快速清除造影剂。还可以使用mri检测hcc。
可以通过活检来检测hcc,尤其是对于患有大于2cm的hcc且具有低水平的甲胎蛋白、或者禁忌消融治疗或移植的受试者。
在具有升高的afp和一致的成像特征的患者中,无需活检就可以假定患者接受hcc治疗。优选地,患者还可以用横断层面成像进行肝外疾病(主要是肺转移)的评估;这将排除根治性局部治疗。
hcc的治疗
可以使用本领域已知的许多方法,包括通过肝移植来治疗hcc,然而供体器官的有限供给限制了移植作为许多受试者的选择的可用性。也可以使用切除、射频消融(rfa)来治疗hcc。使用索拉非尼(或者如果索拉非尼失败,则使用瑞戈非尼、纳武单抗或乐伐替尼)的全身治疗可用于桥接患者至移植或延迟hcc的复发。在切除或移植后经历复发的患者中,积极的手术治疗似乎与可能的最佳结果有关。
可以通过经导管的动脉化疗栓塞来治疗hcc,所述经导管的动脉化疗栓塞选择性地将供血动脉插管至肿瘤,并且递送高局部剂量的化疗,包括阿霉素、顺铂或丝裂霉素c。为了防止全身毒性,用明胶海绵或线圈堵塞供血动脉以阻止血流。
可以通过化疗来治疗hcc,然而,hcc对全身化疗的反应最小。例如,似乎具有最大功效的基于阿霉素的方案具有20-30%的应答率和对存活的最小影响。
对于患有childc级肝硬化和有移植禁忌症的患者,可以通过关注疼痛控制、腹水、水肿和门体脑病管理来管理hcc。
可以通过手术来治疗hcc。目前,鉴于没有有效的化疗以及hcc对放疗的不敏感性,彻底肿瘤切除是长期治愈的唯一选择。由于潜在肝硬化的程度,导致在有限数量的患者(通常<15-30%)中可以通过部分肝切除术完成肿瘤的切除。
肝硬化的诊断和治疗
慢性肝脏疾病可以包括肝硬化,其特征在于纤维化和正常肝结构向结构异常的结节的转化。肝损伤向肝硬化的进展可能经数周至数年发生。除纤维化以外,肝硬化的并发症包括但不限于,门静脉高压症、腹水、肝肾综合征和肝性脑病。
在丙型肝炎、酒精性肝病、nash和乙型肝炎中可能发生肝硬化。肝纤维化可能由于肝脏中细胞外基质产生和降解的正常平衡过程中的改变而发生。在肝硬化中,星状细胞可以通过多种旁分泌因子活化成胶原形成细胞。在肝损伤后,此类因子可以由肝细胞、库普弗细胞(kupffercells)和窦内皮(sinusoidalendothelium)释放。例如,在患有慢性丙型肝炎的患者中和患有肝硬化的患者中观察到细胞因子转化生长因子β1(tgf-β1)的水平升高。tgf-β1转而刺激活化的星状细胞以产生i型胶原。
肝硬化的诊断
通常使用child-turcotte-pugh(ctp)系统来评估肝硬化的严重程度,该系统是通过考虑临床变量脑病、腹水的存在和/或严重程度、血液中胆红素的水平和白蛋白水平、以及凝血酶原时间来评估肝硬化的严重程度的评分系统。
还可以通过考虑需要的透析次数、血液中肌酐水平、胆红素水平、钠和凝血酶原时间的临床变量,使用终末期肝病模型(modelforend-stageliverdisease(meld))评分系统来评估肝硬化的严重程度。
肝硬化的治疗
患有严重的cld(例如失代偿性肝硬化)的受试者可以使用肝移植来进行治疗。肝移植具有85-90%的1年存活率和超过70%的5年存活率。在大多数情况下,肝移植后的生活质量良好或优异。然而,供体器官的有限供给限制了移植作为许多受试者的选择的可用性。
许多疗法可用于预防或延迟患有cld的受试者中肝硬化的发展:用于治疗自身免疫性肝炎的泼尼松和硫唑嘌呤,用于治疗乙型肝炎和丙型肝炎的干扰素和其它抗病毒药剂,用于血色素沉着症的静脉切开术,用于原发性胆汁性肝硬化的熊去氧胆酸,以及用于威尔逊氏病的曲恩汀和锌。nash是非酒精性脂肪肝疾病(nafld)的进展期形式,对于使用以下药物的治疗正在进行评价:变构乙酰辅酶a羧化酶(acc)抑制剂(例如ndi-010976/gs-0976),奥贝胆酸,噻唑烷二酮类(例如,吡格列酮、罗格列酮、洛贝格列酮、环格列酮(ciglitazone)、达格列酮(darglitazone)、恩格列酮(englitazone)、萘格列酮(netoglitazone)、利格列酮(rivoglitazone)、曲格列酮、巴格列酮(balaglitazone)),elafibranor(gft505),奥贝胆酸(oca),凋亡信号调节激酶1(ask1)抑制剂(selonsertib),双重ccr2/ccr5抑制剂cenicriviroc(cvc,也为tbr-652或tak-652),和维生素e。
如果慢性肝脏疾病发展为肝硬化,则这些疗法的效果较差。一旦肝硬化发展,治疗的目标是管理由肝硬化引起的并发症。例如,可以每天两次口服220mg硫酸锌来治疗与肝硬化相关的锌缺乏症,以改善味觉障碍并且刺激食欲。此外,锌在治疗肌肉痉挛方面是有效的,并且是用于肝性脑病的辅助疗法。可以用消胆胺,抗组胺药(例如苯海拉明、羟嗪)和12%乳酸铵护肤乳(lac-hydrin),包括熊去氧胆酸、多塞平和利福平来治疗患有cld(例如胆汁淤积性肝病或丙型肝炎)的受试者的瘙痒症。纳曲酮可能有效,但通常耐受性差。加巴喷丁是不可靠的疗法。患有严重瘙痒症的患者可能需要紫外线疗法的建立或血浆置换。患有cld的男性受试者的性腺功能减退可以用局部睾酮制剂来治疗。患有cld(尤其是慢性胆汁淤积或原发性胆汁性肝硬化)的受试者的骨质疏松症可以用钙和维生素d补充剂来治疗。此外,患有cld的患者可以接种甲型肝炎疫苗。
实施例
在以下实施例中进一步描述本发明,这些实施例不限制权利要求中描述的本发明的范围。
方法
在以下阐述的实施例中使用以下材料和方法。
临床方案
在患者许可的情况下,从患者的电子病历中收集患者医疗数据,并且在两个10-mledta管中以任意给定的抽血量从患者获得最多20ml血液,并且每位患者处理约8-15ml的血液。
使用ichip装置从全血中微流控纯化cec
将针对抗人cd45抗体(clone2d1,r&dsystems,bam1430)和抗人cd66b抗体(abdserotec,80h3)的生物素化一抗分别以100fg/wbc和37.5fg/wbc加入至全血(总体积为5-10ml)中,并且在室温下摇动温育20min。然后添加dynabeadsmyonestrepavidint1(lifetechnologies,65602)磁珠,并且在室温下摇动温育另外的20min。然后,如先前所述,在ichip装置上运行总血液体积(5-10ml)8。
cec的免疫荧光染色
将经ichip装置处理的血液样品的等分试样中的细胞用2%多聚甲醛固定10分钟,然后使用shandonezmegafunnel(thermofishera78710001)经由细胞离心涂片机(cytospin)在2000rpm下施涂至载玻片5min。用pbs洗涤玻片,并且在室温(rt)下用在pbs中的5%驴血清+0.3%triton-x封闭1小时。然后添加针对广谱细胞角蛋白(wsck,abcamab9377)、磷脂酰肌醇蛋白聚糖-3(abcamab81263)和cd45(bectondickenson555480)的一抗(分别在pbs、0.1%bsa、0.3%triton-x中以1:50稀释),并且在室温下温育1小时。然后将针对每种一抗的二抗(分别在pbs、0.1%bsa、0.3%triton-x中以1:200稀释)用于荧光标记,避光在室温下温育1小时:分别为1)细胞角蛋白-驴抗兔alexa-647(jacksonimmunoresearch711-605-152);2)磷脂酰肌醇蛋白聚糖-3-驴抗绵羊cy3(jacksonimmunoresearch713-165-003);3)cd45-驴抗小鼠alexa-488(jacksonimmunoresearch715-545-150)。细胞核用dapi(在pbs中5μg/ml,lifetechnologies)来复染。使用prolonggoldantifadereagent(lifetechnologies)固定玻片。使用用于图像采集的适当的滤光立方体(filtercube)和用于自动化图像分析的bioview平台,通过荧光显微法(tie或eclipse90i,nikon)使染色的细胞成像。对所有检测到的候选cec进行检查并且基于完整的形态、带有dapi核复染的cec标志物(wsckalexa-647和/或gpc3cy3)的定位、以及白细胞标志物(cd45alexa-488)的缺失来评分。
hepg2细胞加入
按照美国典型培养物保藏中心(americantypeculturecollection)建议的培养条件培养hepg2细胞。在通过ichip装置处理之前,使用eppendorftransfermannk2显微操纵器对单个细胞进行微量移液,并且引入至来自健康供体的4ml血液中。
cec的rna测序
将经ichip装置处理的血液样品等分试样沉淀,并且在-80摄氏度下在rnalater(thermo-fisherscientific)中快速冷冻。提取rna(rneasymicro,qiagen)并且如下处理以进行rna-seq。根据制造商的方案,使用用于测序的smarterultralowinputrna试剂盒(v3或v4)(clontechlaboratories)从来自各样品的rna产生扩增的cdna。简而言之,将1μl的1:50,000稀释的erccrnaspike-inmix(lifetechnologies)添加至各样品中。使用基于聚dt的3’-smartcds引物iia进行rna分子的第一链合成,然后是延伸和借助逆转录酶的模板转换。第二链合成和扩增pcr运行18个循环,并且用1×agencourtampurexp珠清除法(beadcleanup)(beckmancoulter)纯化扩增的cdna。根据制造商的方案将
白细胞的流式分选
对于hcc患者的一个子集,将经ichip装置处理的血液样品分为两份等同的等分试样:将一份等分试样沉淀并且如上所述快速冷冻;将第二份等分试样进行流式分选以分离污染白细胞的子类型(单核细胞、粒细胞、nk细胞、细胞毒性t细胞、辅助t细胞、和b细胞)。细胞用cytofix(bdbiosciences554655)来固定。使用以下抗体:cd45(beckmancoulterim0782u)、cd56(beckmancoulterim2073u)、cd16(biolegend360712)、cd14(biolegend301808)、cd3(biolegend317330)、cd19(biolegend302216)、cd4(biolegend300556)、cd8(biolegend301016)、cd66b(biolegend305112)。如上所述,将流式分选的细胞沉淀,在rnalater中快速冷冻,并且进行rna-seq。
实施例1:使用随机森林分类器对cld患者进行分类的概述
rna-seq原始数据由64个cld样品和52个hcc样品的59,074个转录物的读段数(readcounts)构成。其中,仅保留总读段超过250k的样品,留下44个cld样品和39个hcc样品。为了将我们数据集中的特征列表缩小到与预测hcc状态具有更高的相关可能性的那些特征,从包含正常肝脏和hcc组织二者的表达计数的cancergenomeatlas(tcga)肝癌计划(lihc)获得rna-seq表达数据。使用在r中用于多重假设检验的具有benjamini-hochberg校正的deseq2包(版本1.16.1),对该数据集进行差异表达分析,以鉴定hcc与正常肝组织中过表达的转录物。将该分析与经由流式分选获得的大量白细胞(wbc)亚群的rna-seq数据结合使用,构建了其中在总wbc亚群中经调整的p值<0.05、log2差异倍数>2、wbc<50rpm并且在健康肝组织中的平均表达>0.5rpm的转录物的列表。该列表用于将原始数据集中的59,074个特征缩小至更可能预测hcc的一组248个转录物。该组的248个转录物为:actg2、adm2、afp、agr2、akr1b10、aldh3a1、alpk3、amigo3、ankrd65、anln、ap1m2、apobec3b、arhgap11a、arhgef39、asf1b、asphd1、aspm、aurka、axin2、baiap2l2、bex2、c15orf48、c1orf106、c1qtnf3、c6orf223、ca12、ca9、camk2n2、cap2、cbx2、ccdc170、ccdc28b、ccdc64、ccna2、ccnb1、ccne2、ccnf、cd109、cd34、cdc20、cdc25a、cdc6、cdc7、cdca5、cdca8、cdh13、cdk1、cdkn2a、cdkn2c、cdt1、celf6、cenpf、cenph、cenpl、cenpu、cenpw、ckb、cnnm1、col15a1、col4a5、col7a1、col9a2、crip3、cspg4、ctnnd2、cxorf36、cyp17a1、dlk1、dmkn、dscc1、dtl、duox2、e2f1、ect2、eef1a2、efna3、ephb2、eppk1、etv4、ezh2、f2rl3、fabp4、fam111b、fam3b、fam83d、fancd2、fanci、fbxl18、fbxo32、fermt1、fgf19、flnc、flvcr1、fmo1、foxd2-as1、foxm1、fxyd2、gabre、gal3st1、gcnt3、gins1、gjc1、gmnn、gnaz、golga2p7、gpc3、gpr64、gpsm1、hrct1、igf2bp2、igsf1、igsf3、iqgap3、itga2、itpka、kiaa0101、kif11、kifc1、kifc2、kntc1、krt23、lama3、lef1、lgr5、linc00152、lingo1、lpl、lrrc1、lypd1、mad2l1、maged4、maged4b、mapk12、mapk8ip2、mapt、mcm2、mdga1、mdk、mfap2、misp、mki67、mmp11、mns1、mpz、msc、msh5、mtmr11、muc13、muc5b、mybl2、myh4、naaladl1、nav3、ncapg、ndufa4l2、neb、nkd1、nmb、notch3、notum、npm2、nqo1、nrcam、nt5dc2、nts、nusap1、obscn、olfml2a、olfml2b、osbp2、paqr4、pdzk1ip1、peg10、pi3、plce1、plch2、plk1、plvap、plxdc1、plxnb3、podxl2、pole2、ppap2c、prc1、ptges、ptgfr、pthlh、ptk7、ptp4a3、pttg1、pycr1、racgap1、rbm24、recql4、rhbg、rnf157、robo1、rp4-800g7.2、rps6kl1、rrm2、s100a1、scgn、5-sep、serpina12、sez6l2、sfn、sgol2、slc22a11、slc51b、slc6a2、slc6a8、slc6a9、sncg、soat2、sp5、sparcl1、spink1、spp1、stil、stk39、sult1c2、tcf19、tdgf1、tesc、thy1、tk1、tmc5、tmem132a、tmem150b、tnfrsf19、tnfrsf25、tonsl、top2a、tpx2、trim16、trim16l、trim31、trim45、ttc39a、ubd、ube2c、ube2t、ugt2b11、ush1c、vsig10l、wdr62、wdr76、zwint。
所有分析中使用的最终数据集由如上所述鉴定的248个转录物和83个样品的log2(1+rpm)构成。为了评价分类算法的性能,实施了10倍交叉验证的十次迭代,下面对其进行逐步描述:
1.特征选择。使用rstats包(版本3.4.2)对针对由tcga差异表达分析鉴定的248个转录物中的每一个的训练集进行具有备择假设ha:μcld<μhcc的单侧t检验。仅保留p值小于0.05的那些。
2.随机森林分类器。将从特征选择步骤保留的所有转录物用于训练随机森林,所述随机森林使用r中的randomforest包(版本4.6-12)来构建。参数mtry保留在其默认值sqrt(p),其中p为数据集中的特征数,并且构建了ntree=500棵树。根据疾病状况分层抽样。作为比较器分类器(comparatorclassifier),使用来自特征选择步骤的10个p值最显著的基因来创建多元逻辑回归模型。
3.预测。从随机森林输出获得对测试集(testset)中的各样品进行癌症分类投票的随机森林中树木的比例,并且用于使用proc包(版本1.10.0)来构建roc曲线。
实施例2:通过免疫荧光检测cec
首先通过免疫荧光(if)检测cec。从10名健康血液供体、39名经历例行临床监控但无hcc迹象的cld患者、54名患有hcc的患者、和10名经历根治性治疗且无疾病的临床迹象(ned)的hcc患者获得血液样品(参见表1-4)。ichip装置进行了红细胞、血小板和血浆的基于尺寸的排除,然后进行经标记的白细胞(wbc)的磁泳(如在ozkumure等人,scitranslmed2013;5:179ra47中所述)(参见图1)。然后通过对磷脂酰肌醇蛋白聚糖-3(在hcc中表达而且也在cld肝组织中表达的癌胚蛋白)(如在wanghl等人,archpathollabmed2008;132:1723-8中所述)或者细胞角蛋白(上皮标志物)进行if染色来对cec进行计数(参见图2a)。使用每10ml全血5个细胞的阈值,以cld患者(79%)、hcc患者(81%)和ned患者(90%)的相似的比例鉴定出cec,但是仅在20%的健康供体中鉴定出cec(参见图2b和图4a-b;p<0.01,各组对健康供体)。使用ichip装置的纯化与免疫荧光定量相结合,证明在hcc和cld患者中在相似的浓度下cec检测的高灵敏度。在cld患者中,患有进展期纤维化(metavirf3或f4)的患者与未患有进展期纤维化的患者(0.7个细胞/ml,p<0.01,参见图2c)相比,具有更高的cec浓度(中值为5.1个细胞/ml)。因为cld研究人群仅包括具有足够高的hcc风险而经历监控的患者,因此未患有进展期纤维化的亚组中的各患者的cld病因为乙型肝炎感染。与纤维化分期有关的cec浓度的差异似乎不是由于cld病因引起的,这是因为当将该分析限于仅患有乙型肝炎诱导的cld的患者时,这种趋势仍然存在(患有进展期纤维化,中值为5.0个细胞/ml,未患有进展期纤维化,0.7个细胞/ml,p=0.06,参见图4c)。另外,cld病因不会导致cec浓度的差异(参见图4d)。
实施例3:通过rna测序检测cec
进行rna测序(rna-seq)以检测cec。为了确定该方法的灵敏度,将0、1、3、5、10或50个hepg2hcc细胞加入4ml的健康供体血液中,并且通过ichip装置处理以用于rna-seq。在全血中可检测到来自单个细胞的hepg2特异性基因表达(参见图3a)。在来自64名cld患者和52名hcc患者的临床血液样品中鉴定出cec。首先,基于genotypetissueexpression(gtex)表达数据创建了17种肝特异性基因标记。在来自两个患者组的样品中均鉴定出肝特异性基因,但是在从经ichip装置处理的血液流式分选的wbc亚群中不存在肝特异性基因(参见图3b)。因此,肝特异性标记在污染的wbc中鉴定出稀少的cec,而不是这些基因的异常表达。
实施例4:用于检测hcc的分类器的生成
为了显示cec可能取决于潜在的疾病状态而在表型上不同,在cld对hcc的情况下,进行基因表达谱分析以鉴定cec之间的定性差异而不是定量差异(参见图3c)。使用cancergenomeatlas(tcga)数据库,鉴定出248个与肝组织相比在hcc中过表达的基因,并且排除了在wbc中表达的基因。使用随机森林(rf)机器学习方法来产生基于这些基因的分类器,以区分cldcec和hcccec。更具体地,随机森林中的每个决策树都进行了“投票”,将样品分类为cld或hcc。最终的分类器使用在表5中列出的25个基因。显而易见的是,分类器中三个信息最丰富的基因(tesc,slc6a8,spp1)与癌症转移有关,并且另一个(e2f1)是已确定的细胞增殖标志物(参见kangj等人,tumourbiol2016;37:13843-13853;loojm等人,cell2015;160:393-406;和sangalettis等人,cancerres2014;74:4706-19)。
交叉验证的分类器提供了cld和hcc样品之间的优异分离,在95%的特异性(即真阴性率)下具有85%的灵敏度(即真阳性率),并且鉴定出早期hcc和晚期hcc两者(按照米兰标准)(参见图3d和图5a-c)。与最近的一项将无细胞dna与基于蛋白质血液的生物标志物相结合的研究(cohenjd等人,science2018)(达到仅44%的预测hcc的准确度)(可能是由于缺乏常见的频发突变和hcc固有的特异性蛋白标志物)相比,在该实施例中达到的准确度(灵敏度和特异性)的水平更高。
表1:经历hcc监控的cld患者的人口统计学和结果。借助免疫荧光,将cec定义为表达ck或gpc3的细胞。hcc得分为来自rf分类器的投票分数。hbv,乙型肝炎病毒;hcv,丙型肝炎病毒;psc,原发性硬化性胆管炎;nash,非酒精性脂肪性肝炎;aih(自身免疫性肝炎)。
表2:患有活动性疾病(抽血前接受或未接受治疗)的hcc患者的人口统计学和结果。借助免疫荧光,将cec定义为表达ck或gpc3的细胞。hcc得分为来自rf分类器的投票分数。nash,非酒精性脂肪性肝炎;psc,原发性硬化性胆管炎;hbv,乙型肝炎病毒;hcv,丙型肝炎病毒;a1atα-1-抗胰蛋白酶缺乏症;rt,放疗(外部);tace,经动脉化疗栓塞;sirt,选择性内部放射疗法。
表3:治疗后无疾病迹象的hcc患者的人口统计学和结果。借助免疫荧光,将cec定义为表达ck或gpc3的细胞。nash,非酒精性脂肪性肝炎;hbv,乙型肝炎病毒;hcv,丙型肝炎病毒。
表4:健康血液供体人口统计学。
表5:用于诊断hcc的基于血液的生物标志物的基因标记。基因权重(geneweight)是基尼(gini)的平均下降,所述基尼是基因对分类器的贡献的量度。
其它实施方案
应当理解,尽管已经结合本发明的详细描述描述了本发明,但是前述描述旨在说明而不是限制本发明的范围,本发明的范围由所附权利要求的范围限定。其它方面、优点和修改在所附权利要求的范围内。
- 还没有人留言评论。精彩留言会获得点赞!