用于无标签编码化学文库筛选的微珠的制作方法
本发明涉及微珠和包含微珠的微区室(例如微滴),以及根据其编码的化学文库。本发明还涉及用于筛选编码文库的方法。
背景技术:
药物发现通常包括:大型化合物文库的汇编,然后进行测试或筛选,其中将化合物各自添加到包含目标物的微孔中以鉴定“命中物(hits)”,该“命中物”在目标物上显示所需活性(例如酶活性或标签位移)。此过程被称为高通量筛选(hts)。尽管可以通过使用机器人设备使该过程自动化以测试数百万种化学物质,但它既费力又昂贵。
因此,存在根本性问题,其源于增加的文库规模增加了筛选负担的事实:由于筛选测试具有离散性,筛选时间和成本规模与文库大小近似呈线性关系。这对可使用这种方法筛选的化学文库大小施加了严重的实际限制:hts通常应用于包含103-106个成员的文库。
基于选择的筛选技术(例如,淘选(panning)技术)的发展已经解决了这个问题。在此技术中,文库中的所有化合物同时进行测试,以一锅(one-pot)式的方式测试它们与感兴趣的目标物进行相互作用的能力。在这类测试中,筛选步骤的时间和成本与文库大小无关,因此该方法可应用于相对较大的文库。含多达1012个成员的文库已经采用这类方法进行筛选。
基于微滴的文库的开发也已经解决了这个问题,其可以通过微流体技术进行处理,将通量提高几个数量级(参见,例如,clausell-tormos等人,(2008)chemistry&biology15:427-437)。
但是,基于选择的试验和基于微滴的筛选都需要能够容易地鉴定出所选择的化合物(即“命中物(hits)”):可筛选的但不可解码的文库是无用的。
在1992年,brenner和lerner(brennerandlerner(1992)proc.natl.acad.sci.usa89:5381-5383)首次提出解决这个问题的方案,该方案基于dna编码化合物文库(decl)的生成。在decl中,每个化合物与对应于其结构或反应历史的dna序列连接(标记),由此作为该特定化合物的唯一标识符(即dna标签“编码”该化合物,由此用作分子的“条形码”)。
化合物可以采用多种不同的方式加标签(tagged),并且还可能的是,使用dna标签不仅可以编码特定的化合物结构(“dna记录”),还可以作为指导其合成的模板(“dna模板”)。近年来,对这类技术有如下综述:mannocci等,(2011)chem.commun.,47:12747-12753;kleiner等,(2011)chemsocrev.40(12):5707-5717;mullard(2016)nature530:367-369对。
decl技术现在在制药行业已经很成熟:在2007年,gsk(葛兰素史克)以5500万美元收购了decl的先驱之一praecis制药(praecispharmaceuticals),而其他排名前十的制药公司也开始了他们自己内部的dna编码文库项目。包括x-chem、vipergen、ensembletherapeutics和philochem在内的其他生物技术公司也在积极开发和利用decl技术。
但是目前,当前decl的应用受到与标签存在及命中评估性质相关问题的限制,这仅通过结合活性来完成。例如,编码标签可能会:(a)在化学上或空间上干扰被标记化合物接近感兴趣的目标物上的分子结合位点,从而限制回收的命中物的数量和/或类型;(b)限制细胞渗透性和/或扩散性,有效地防止细胞吸收,并排除基于细胞表型的筛选的使用,该使用依赖于进入细胞质;(c)限制标记后化合物可以进行化学修饰的程度(某些反应在化学上与标签不相容);以及(d)限制结构-活性分析的有用性,因为这种分析会被标签本身对活性的潜在影响所混淆,并且只检测到与靶结合的活性,而不是功能(例如酶)的活性。
因此,需要新的hts技术,其允许筛选可解码的化学文库并解决前述问题。
技术实现要素:
根据本发明的第一方面,提供了一种经编码的化学文库的微珠,该微珠上或微珠内已固定有:(i)编码标签;和(ii)靶测试系统报告部分(targetassaysystemreportermoiety),其中所述报告部分(reportermoiety)在不存在针对所述靶的活性的情况下以第一状态存在,并且在所述活性存在的情况下以第二状态存在,并且其中所述微珠进一步包含一个或多个化学结构的克隆群(clonalpopulation),所述化学结构可释放地连接到所述标签并由所述标签编码。
根据本发明的第二方面,提供了一种化学文库微区室,其包含水性溶剂和本发明的微珠。
根据本发明的第三方面,提供了包括多个本发明的微区室的编码化学文库(ecl),其中每个微区室包含不同的化学结构。
根据本发明的第四方面,提供了一种用于筛选本发明的ecl中对靶具有活性的化学结构的方法,该方法包括以下步骤:
(a)提供所述ecl;
(b)从微珠中释放出所述化学结构,以产生多个游离的、无标签的化学结构(tcs),这些化学结构溶解在溶剂中并与释放它们的微珠一起包含在微区室内,从而维持每个tcs和其编码标签之间的空间关联;
(c)通过在以下条件下孵育步骤(b)的ecl微区室来测定tcs:通过对靶的活性水平来确定报告部分的状态,其中该报告部分被固定在微区室中的微珠上或微珠内;
(d)通过打开微区室释放微珠;
(e)通过确定所述报告部分的状态来筛选释放的微珠,从而可以通过对处于第二状态的具有报告部分的微珠的标签进行解码来鉴定对靶具有活性的化学结构。
在下面列出的编号段落中定义和描述了本发明的其他方面、优选特征和优选可操作的组合。
1.编码化学文库微珠,该微珠上和/或微珠内已经固定有:(i)编码标签;和(ii)靶测试系统报告部分,其中,所述报告部分在不存在针对靶的活性的情况下以第一状态存在,并且在所述活性存在的情况下以第二状态存在,并且其中所述微珠进一步包含一个或多个化学结构的克隆群,所述化学结构可释放地连接到所述标签并由所述标签编码。
2.根据段落1所述的微珠,其中,所述编码标签还编码靶测试系统报告部分。
3.根据段落1或段落2所述的微珠,其中,所述编码标签还编码所述靶。
4.根据前述段落中任一项所述的微珠,其中,所述化学结构以每微珠1至1013个分子的负载存在。
5.根据前述段落中任一项所述的微珠,其中,所述微珠包含多个化学结构的克隆群,任选地,其中所述编码标签还编码所述化学结构的负载。
6.根据前述段落中任一项所述的微珠,其中,所述微珠上或微珠内已固定有多个靶测试系统报告部分,任选地,其中所述编码标签还编码报告部分的负载。
7.根据段落6所述的微珠,其中,第一状态与第二状态的报告部分的比例与针对所述靶的活性水平相关。
8.根据前述段落中任一项所述的微珠,其中,所述微珠基本上为球形。
9.根据段落8所述的微珠,其中,所述微珠的直径最高达400μm。
10.根据段落8所述的微珠,其中,所述微珠的直径为1-100μm。
11.根据段落8所述的微珠,其中,所述微珠的直径<50μm。
12.根据前述段落中任一项所述的微珠,其中,所述微珠由水凝胶或聚合物形成。
13.根据段落12所述的微珠,其中,所述微珠由固体例如硅酮、聚合物例如聚苯乙烯、聚丙烯和二乙烯基苯或水凝胶形成,所述水凝胶例如选自琼脂糖、海藻酸盐、聚丙烯酰胺和聚乳酸。
14.根据前述段落中任一项所述的微珠,其中,所述编码标签包含核酸。
15.根据段落14所述的微珠,其中,所述核酸是dna。
16.根据段落1-14中任一项所述的微珠,其中,所述微珠包含非dna标签、非rna标签、经修饰的核酸标签、肽标签、基于光的条形码(例如,量子点)、rfid标签、通过点击化学连接的报告化学物质和质谱-可解码标签。
17.根据前述段落中任一项所述的微珠,其中,所述化学结构是小分子。
18.根据前述段落中任一项所述的微珠,其中,所述化学结构通过可裂解的连接子(linker)可释放地连接至所述微珠。
19.根据段落18所述的微珠,其中,所述连接子是无疤痕型的,使得化学结构可以以其完全或基本上不含连接子残基的形式从所述微珠上裂解。
20.根据段落18或19所述的微珠,其中,所述可裂解的连接子包含选自以下的连接子:酶可裂解连接子;化学可裂解连接子;光可裂解连接子以及前述两种或两种以上的组合。
21.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子选自:亲核试剂/碱敏感连接子;还原敏感连接子;紫外线敏感连接子;亲电试剂/酸敏感连接子;金属辅助型裂解敏感连接子;氧化敏感连接子;以及前述两种或两种以上的组合。
22.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子是酶可裂解连接子,例如可被选自以下的酶裂解:蛋白酶(包括肠激酶)、核酸酶、硝基还原酶、磷酸酶、β-葡萄糖醛酸酶、溶酶体酶、tev、胰蛋白酶、凝血酶、组织蛋白酶b、b和k、胱天蛋白酶、基质金属蛋白酶、磷酸二酯酶、磷脂酶、酯酶、还原酶和β-半乳糖苷酶的酶。
23.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子包含rna,并且其中所述化学结构可通过与核糖核酸酶接触而被释放。
24.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子包含肽,并且其中所述化学结构可通过与肽酶接触而被释放。
25.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子包含dna,并且其中所述化学结构可通过与位点特异性核酸内切酶接触而被释放。
26.根据段落18-20中任一项所述的微珠,其中,所述可裂解的连接子是包含裂解部分和自脱落部分(sim)的自脱落连接子,任选地,其中所述裂解部分是肽或非肽可酶裂解部分,例如val-cit-pab。
27.根据前述段落中任一项所述的微珠,其中,所述化学结构间接地或直接地连接至所述微珠。
28.根据段落27所述的微珠,其中,所述化学结构经由所述编码标签间接地连接至所述微珠。
29.根据段落28所述的微珠,其中,所述化学结构通过核酸杂交连接至所述编码标签。
30.根据前述段落中任一项所述的微珠,其中,所述靶是酶,任选地是哺乳动物(例如人)、细菌酶或病毒酶,例如选自以下的酶:蛋白酶;激酶;脱氢酶和磷酸酶。
31.根据段落30所述的微珠,其中,所述靶测试系统报告部分是:(a)酶的底物、抑制剂、活化剂或分子伴侣;或(b)酶或其片段。
32.根据段落31所述的微珠,其中,所述靶测试系统报告部分包含:(a)酶的催化位点;和/或(b)酶的变构位点。
33.根据段落1-29中任一项所述的微珠,其中,所述靶是蛋白质,例如哺乳动物(例如人)、细菌或病毒蛋白。
34.根据段落33所述的微珠,其中,所述靶测试系统报告部分是:(a)所述蛋白质的结合伴侣;或(b)蛋白质或其片段。
35.根据段落1-29中任一项所述的微珠,其中,所述靶是受体,例如哺乳动物(例如人)、细菌或病毒蛋白。
36.根据段落35所述的微珠,其中,所述靶测试系统报告部分是:(a)所述受体的配体;或(b)受体或其片段。
37.根据段落1-29中任一项所述的微珠,其中,所述靶是受体配体。
38.根据段落37所述的微珠,其中,所述靶测试系统报告部分是:(a)所述受体配体或其片段;或(b)受体或其片段。
39.根据段落1-29中任一项所述的微珠,其中,所述靶是酶底物。
40.根据段落39所述的微珠,其中,所述靶测试系统报告部分是:(a)酶底物;或(b)酶或其片段。
41.根据段落1-29中任一项所述的微珠,其中,所述靶是分子伴侣。
42.根据段落41所述的微珠,其中,所述靶测试系统报告部分是:(a)所述分子伴侣或其片段;或(b)伴侣分子,例如分子伴侣结合肽。
43.根据段落1-29中任一项所述的微珠,其中,所述靶是毒素。
44.根据段落43所述的微珠,其中,所述靶测试系统报告部分是:(a)毒素或其片段;或(b)毒素的结合伴侣。
45.根据段落1-29中任一项所述的微珠,其中,所述靶是药物。
46.根据段落45所述的微珠,其中,所述靶测试系统报告部分是:(a)药物或其片段;或(b)药物的结合伴侣。
47.根据段落1-29中任一项所述的微珠,其中,所述靶测试系统报告部分被翻转,并且具有催化活性的化学结构可以通过解码具有处于翻转状态的报告部分的微珠的标签来鉴定。
48.根据段落1-29中任一项所述的微珠,其中,所述靶测试系统报告部分是荧光的,并且具有猝灭活性的化学结构可以通过解码具有处于猝灭状态的报告部分的微珠的标签来鉴定。
49.根据段落1-29中任一项所述的微珠,其中,所述靶测试系统报告部分是非荧光底物,并且可以通过解码具有荧光报告部分的微珠的标签来鉴定发挥荧光团涂层作用的化学结构。
50.根据段落1-29中任一项所述的微珠,其中,所述靶测试系统报告部分是底物,并且可以通过解码具有彩色报告部分的微珠的标签来鉴定发挥生色团涂层作用的化学结构。
51.根据段落1-29中任一项所述的微珠,其中,所述靶测试系统报告部分是底物,并且可以通过解码具有涂层的报告部分的微珠的标签来鉴定发挥底物涂层作用的化学结构。
52.根据前述段落中任一项所述的微珠,其中,所述靶测试系统报告部分的第一状态和第二状态通过以下进行区分:(a)荧光,例如猝灭或未猝灭的荧光;和/或(b)裂解或未裂解的构象;和/或(c)磷酸化或非磷酸化状态;(d)不同的糖基化类型、模式或程度;和/或(e)不同的抗原决定簇;和/或(f)与配体结合或未结合;和/或(g)与一种或多种其他测试系统组分复合或不复合。
53.化学文库微区室,其包含前述段落中任一项所定义的微珠和溶剂,例如水性溶剂。
54.根据段落53所述的微区室,其还包含用于将化学结构从所述微珠释放到溶液中的裂解剂,任选地,其中所述裂解剂是酶,所述酶例如选自蛋白酶(包括肠激酶)、核酸酶、硝基还原酶、磷酸酶、β-葡萄糖醛酸酶、溶酶体酶、tev、胰蛋白酶、凝血酶、组织蛋白酶b、b和k、胱天蛋白酶、基质金属蛋白酶、磷酸二酯酶、磷脂酶、酯酶和β-半乳糖苷酶。
55.根据段落53-54中任一项所述的微区室,其为微滴、微粒或微泡的形式,任选地是具有表面活性剂稳定的界面的油包水乳液的微滴。
56.根据段落53-55中任一项所述的微区室,其中,所述化学结构以至少以下浓度存在:0.1nm、0.5nm、1.0nm、5.0nm、10.0nm、15.0nm、20.0nm、30.0nm、50.0nm、75.0nm、0.1μm、0.5μm、1.0μm、5.0μm、10.0μm、15.0μm、20.0μm、30.0μm、50.0μm、75.0μm、100.0μm、200.0μm、300.0μm、500.0μm、1mm、2mm、5mm或10mm。
57.根据段落53-56中任一项所述的微区室,其中,所述微区室基本上为球形。
58.根据段落57所述的微区室,其中,所述微区室的直径为1至500μm,可选地小于<100μm。
59.根据段落53-58中任一项所述的微区室,其中,所述化学结构已经从所述微珠中释放出来以产生溶解在溶剂中并与编码标签在空间上相关的游离的、无标签的化学结构(tcs)。
60.根据段落53-59中任一项所述的微区室,其还包含所述靶测试系统的一种或多种附加组分。
61.根据段落60所述的微区室,其中,所述附加组分包含抗体。
62.根据段落61所述的微区室,其中,所述抗体特异性结合第一状态或第二状态的报告部分。
63.根据段落61或62所述的微区室,其中,所述抗体附着于磁珠或可检测标签,任选地荧光标签。
64.根据段落60-63中任一项所述的微区室,其中,所述附加组分包含靶,所述靶选自段落30、34、37、40、43、46和49中任一项中定义的靶,任选地为标记形式。
65.根据段落64所述的微区室,其中:
(a)附加组分包含的靶选自段落30、34、37、40、43、46和49中任一项定义的靶,任选地为标记形式;
(b)所述靶测试系统报告部分选自以下段落任一项定义的那些:31-33;35-36;38-49;41-42;44-45;47-48和50-51。
66.根据段落53-65中任一项所述的微区室,其还包含附加部分,所述附加部分溶解在溶剂中并由固定在所述微珠中或微珠上的第二标签编码。
67.根据段落66所述的微区室,其可通过以下方式可得到或获得:将段落1-52中任一项所定义的微珠与所述附加部分和第二编码标签共封装,然后将所述第二标签固定在所述微珠上或微珠内。
68.根据段落67所述的微区室,其中,所述编码标签是dna标签,并且所述第二编码标签在共包封之后与编码所述化学结构的标签连接。
69.编码的化学文库(ecl),其包含根据段落53-68中任一项所定义的多个微区室,其中,每个微区室包含不同的化学结构。
70.根据段落69所述的ecl,其包含化学结构的n个不同克隆群,每个克隆群被限制在n个离散的文库微区室中。
71.根据段落70所述的ecl,其中:(a)n>103;或(b)n>104;或(c)n>105;或(d)n>106;或(e)n>107;或(f)n>108;或(g)n>109;或(h)n>1010;或(i)n>1011;(j)n>1012;(k)n>1013;(i)n>1014;或(m)n>1015。
72.根据段落71所述的ecl,其中n=106至109。
73.一种用于筛选根据段落69-72中任一项所定义的化学结构的ecl的方法,所述化学结构具有针对靶的活性,所述方法包括以下步骤:
(a)提供所述ecl;
(b)从微珠中释放出所述化学结构,以产生多个游离的、无标签的化学结构(tcs),这些化学结构溶解在溶剂中并与释放他们的微珠一起包含在微区室内,从而维持每个tcs和其编码标签之间的空间关联;
(c)通过在以下条件下孵育步骤(b)的ecl微区室来测定tcs:通过针对靶的活性水平来确定微区室内所包含的微珠上或微珠内固定的报告部分的状态;
(d)通过打开微区室释放被测试的微珠;以及
(e)通过确定所述报告部分的状态来筛选释放的和测试的微珠,从而可以通过对处于第二状态的具有报告部分的微珠的标签进行解码来鉴定对靶具有活性的化学结构。
74.根据段落73所述的方法,其中,步骤(a)包括以下步骤:化学结构的核酸记录(例如dna记录)的合成。
75.根据段落73所述的方法,其中,步骤(a)包括以下步骤:化学结构的分开与合并(split-and-pool)核酸记录的合成。
76.根据段落73-75中任一项所述的方法,其中,步骤(c)包括在均相水相测试系统中孵育。
77.根据段落73-76中任一项所述的方法,其中,步骤(d)还包括例如通过热变性、冷冻、添加抑制剂或破坏所述微区室来停止孵育。
78.根据段落77所述的方法,其中,通过离心、超声处理和/或过滤或通过添加溶剂和/或表面活性剂来破坏所述微区室。
79.根据段落73-78中任一项所述的方法,还包括以下步骤:在筛选步骤(e)期间或之前分离在步骤(d)中释放的微珠。
80.根据段落73-79中任一项所述的方法,其中,所述筛选步骤包括对所述释放的和测试的微珠的分级和/或选择。
81.根据段落80所述的方法,其中,所述筛选步骤包括fret、facs、免疫沉淀、免疫沉降、免疫过滤、亲和柱色谱和/或磁性微珠亲和力选择高通量筛选。
82.根据段落73-81中任一项所述的方法,其中,所述筛选步骤(e)包括通过测量报告部分在第一状态与第二状态下的比率来确定针对靶的活性水平。
83.根据段落73-82中任一项所述的方法,其中,所述微珠包括多个化学结构的克隆群,并且所述编码标签还编码化学结构的负载,并且其中,所述筛选步骤(e)包括通过使化学结构的负载与报告部分在第一状态与第二状态下的比率相关联来确定针对靶的活性水平。
发明详述
出于所有目的,本文提及的所有出版物、专利、专利申请和其它参考文献都通过整体引用的方式合并至本申请中,正如每个单独的出版物、专利或专利申请以其全部的内容被明确地和单独地注明通过引用合并至本申请中。
定义和一般性优选
除非明确地特别指出,以下术语除了具有本领域中可能具有的任何更宽(或更窄)的含义以外,本文所用的以下术语还旨在具有以下含义:
除非上下文另有要求,本文使用的单数将被理解为包括复数,反之亦然。术语“一(a)”或“一(an)”涉及的实体将被理解为指代一个或多个所述实体。因此,术语“一(a)”(或“一(an)”)、“一个或多个”和“至少一个”在本文中可互换使用。
如本文所使用的,术语“包括(comprise)”或其变体例如“包含(comprises)”或“含有(comprising)”将理解为表明包含任何所列举的整体(integer)(例如,特征、元素、特性、性质、方法/工艺步骤或限制)或整体组(例如,特征、元素、特性、性质、方法/工艺步骤或限制),但不排除包含其它任何整体或整体组。因此,如本文使用的术语“包括(comprising)”是包括性的或开放式的,并且不排除额外的、未列举的整体或方法/工艺步骤。
如本文所使用的,术语“基本上由...组成(consistessentiallyof)”在本文中用于定义指定的整体、特征或步骤以及那些实质上不影响所定义的整体、特征或步骤的特征或功能(但排除实质上影响所定义的整体、特征或步骤的其它整体、特征或步骤)。如本文所使用的,术语“由...组成(consisting)”用于表明所列举的整体、特征或步骤(例如,特征、元素、特性、性质、方法/工艺步骤或限制)或整体组(例如,特征、元素、特性、性质、方法/工艺步骤或限制)单独存在,并排除其它整体、特征或步骤。
如本文所使用的,术语“测试系统(assaysystem)”限定用于检测针对靶的活性的手段。靶通常是药物靶点,因此可以是与疾病有关的分子(例如蛋白质)。当测试系统的一种或多种组分与存在于文库中且具有所需活性的化学结构接触或反应时,该测试系统直接或间接地产生可检测的和/或可测量的信号。根据本发明,可以使用任何测试系统,只要其包括固定的靶测试系统报告部分,其中,当不存在针对靶的活性时,该报告部分以第一状态存在,当存在针对靶的所述活性时,以第二状态存在。在一些情况下,该测试系统可以由或基本上由固定的靶测试系统报告部分(即该测试系统不包括固定的报告部分以外的组分)组成,例如在一些实施方案中,游离化学结构与报告部分(例如通过选择性地与其结合)直接相互作用,或报告部分自身单独发出与游离化学结构相互作用的信号(例如通过在游离化学结构存在下进行自磷酸化,转换构象,发荧光或猝灭荧光)。
所需活性可以是靶蛋白结合、药理活性、细胞受体结合、抗生素、抗癌、抗病毒、抗真菌、抗寄生虫、农药、药理学、免疫学活性、产生任何所需的化合物、提高化合物产量、特定产品分解。所需活性可以是针对药理学靶细胞、细胞蛋白或代谢途径的活性。所需活性也可以是调节基因表达的能力,例如,通过降低或增强一个或多个基因的表达和/或它们的时间或空间(例如组织特异性)表达模式。所需活性可以是结合活性,例如作为靶蛋白的配体。所需活性也可以是在各种工业过程有用的性质,包括生物修复、微生物强化油采收、污水处理、食品生产、生物燃料生产、能量产生、生物生产、生物消化/降解、疫苗生产和益生菌生产。它也可以是化学试剂,如荧光团或颜料,特定的化学反应或可以与颜色、基质结构或折射率变化相关的任何化学反应。
所述测试系统可以包括化学指示剂,该化学指示剂包括报告分子和可检测标签(如本文所限定的)。例如,它可以是比色的(即,导致在可见光范围内吸收光的有色反应产物)、荧光的(例如,基于酶将底物转化成反应产物,当由特定波长的光激发时,该反应产物发出荧光)和/或发光的(例如,基于生物发光、化学发光和/或光致发光)。
所述测试系统可以包括细胞,例如,如本文所述的靶细胞。所述分析系统还可以包括蛋白质,例如,如本文所述的靶蛋白。可替代地,或另外地,所述测试系统可以包括细胞碎片(cellfractions)、细胞组分、组织、组织提取物、多蛋白复合物、膜结合蛋白膜碎片和/或类器官。
如文本所使用的术语“配体”定义为用于在体内结合生物靶分子的结合伴侣(例如,酶或受体)。因此,这样的配体包括那些与体内的靶标结合(或直接物理相互作用)的结构,而不考虑该结合的生理后果。因此,本发明的配体可以结合作为细胞信号级联的一部分的靶标,其中所述靶标形成其一部分。或者,在细胞生理学一些其他方面的情况下,它们可结合靶标。在后一种情况下,配体可以例如在细胞表面结合靶标而不触发信号级联,在这种情况下,结合可能影响细胞功能的其它方面。因此,本发明的配体可以结合细胞表面和/或细胞内的靶标。
如本文所使用的,术语“小分子”是指分子量为1500da或更小的任何分子,优选1000da或更小,例如小于900da、小于800da、小于600da或小于500da。优选地,本发明的文库中存在的化学结构可以是本文所限定的小分子,尤其是分子量小于600da的小分子。
如本文所使用的,术语“大分子”是指分子量大于1500da的任何分子。这样的分子可以包括,例如,大环和肽(其分子量通常在kda范围内)以及抗体和蛋白质(其分子量可以在100kda范围内)。
如本文所使用的,术语“抗体”限定为所有抗体(包括多克隆抗体和单克隆抗体(mabs))。该术语此处也用于指抗体片段,包括f(ab)、f(ab')、f(ab')2、fv、fc3和单链抗体(及它们的组合),这些抗体片段可以通过重组dna技术或通过酶解或化学裂解完整抗体生成。术语“抗体”此处也用于涵盖双特异性或双功能抗体,它们是合成的具有两个不同的重/轻链对和两个不同结合位点的杂合抗体。双特异性抗体可以通过多种方法产生,包括杂交瘤融合或fab'片段连接。术语“抗体”还包括嵌合抗体(具有人类恒定抗体免疫球蛋白域,该域被连接到一个或多个非人类的可变抗体免疫球蛋白域,或其片段)。因此,这种嵌合抗体包括“人源化”抗体。术语“抗体”还涵盖微型抗体(参见wo94/09817)、单链fv-fc融合体和转基因动物产生的人抗体。术语“抗体”还包括多聚体抗体(multimericantibodies)和高阶蛋白质复合物(例如,异二聚体抗体)。
如本文所使用的,术语肽、多肽和蛋白质可以互换使用,以限定包括通过肽键共价结合的两个或更多个氨基酸的有机化合物。相应的形容词“肽的”相应地解释。肽可以相对于组成氨基酸的数量而提及,即,二肽含有两个氨基酸残基,三肽含有三个氨基酸残基等等。含有十个或更少的氨基酸的肽可以称之为寡肽,而含有多于十个氨基酸残基的肽称之为多肽。这些肽也可以包括任何修饰的和附加的氨基和羧基。
如本文所使用的,术语“点击化学(clickchemistry)”是sharpless在2001年提出的术语,用于描述高产率的、宽范围的反应,所述反应生成的副产物不需要采用色谱就能去除,所述反应具有立体特异性,易于进行,并能够在容易去除的溶剂或良性溶剂中进行。它已经以许多不同的形式被实施,在化学和生物学上应用广泛。点击反应的一个亚类涉及到对周围生物环境呈惰性的反应物。这种点击反应被称为生物正交反应。适用于生物正交点击化学的生物正交反应物对是具有以下性质的分子群:(1)它们相互反应,但不与细胞内环境中的细胞生物化学系统发生显著的交叉反应或相互作用;(2)在生理环境中它们和它们的产物和副产物是稳定的和无毒的;(3)它们的反应是高度特异性和快速的。反应部分(或点击反应物)可以参照所使用的具体点击化学来选择,因此,根据本发明,本领域技术人员已知的范围广泛的任何生物正交反应物的相容对都可以使用,包括反电子需求diels-alder环化加成反应(inverseelectrondemanddiels-aldercycloadditionreaction,iedda)、力引发叠氮炔环加成(strain-promotedalkyneazidecycloaddition,spaac)和施陶丁格连接(staudingerligation)。
术语“分离的”(及相关术语)在此用于指任何物质(例如,化合物、测试试剂、微珠、靶蛋白或靶细胞),以表明该物质存在的物理环境与其天然存在的环境不同(或与分离之前的存在不同)。例如,对从微区室释放的微珠的分离可包括简单地将微珠从已打开(例如破损)的微区室的一个或多个物理化学组分中分离,例如通过从以下的一个或多个中分离:(a)游离的、无标记的化学结构;和/或(b)溶剂;和/或(c)裂解剂;和/或(d)靶测试系统的另外组分。例如,分离的细胞可以指,相对于它们天然存在的复合组织环境,基本上被分离的(例如纯化的)分离的细胞。分离的细胞可以是,例如,纯化或分开的。在这种情况下,分离的细胞可以占存在的总的细胞类型的至少60%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或100%。分离的细胞可以通过本领域技术人员已知的常规技术获得,包括facs、密度梯度离心、富集培养、选择性培养、细胞分选和使用抗表面蛋白的固定化抗体的淘筛技术。
当分离的材料被纯化时,绝对纯度水平不是关键的,本领域技术人员可以根据材料的用途很容易地确定适当的纯度水平。然而,优选纯度水平为至少60%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或者100%w/w。在某些情况下,分离的材料形成组合物(例如,含有许多其他细胞组分的或多或少的粗细胞提取物)或缓冲系统的一部分,这可能包含其他组分。
本文使用的术语“接触”及相关术语是用于指允许至少两个不同的部分(moiety)或系统(例如化学结构和测试系统的组分,例如报告部分)变得足够近,足以发生反应、相互作用或物理接触或结合的过程。
术语“可检测的标签”在本文中用于定义通过光谱、荧光、光化学、生物化学、免疫化学、化学、电化学、射频或通过任何其它物理手段可检测的部分。合适的标签包括荧光蛋白、荧光染料、电子致密试剂、酶(例如,在elisa中常用的)、生物素、地高辛或半抗原和蛋白质或其他可检测的实体,例如通过将放射性或荧光标签结合到肽或抗体(与靶肽特异性反应)来检测。
如本文所使用的,术语“微珠(microbead)”用于定义最长尺寸最大为400μm,优选为1-100μm,更优选小于50μm的固体(例如,聚合物、聚苯乙烯)或水凝胶(例如,海藻酸盐)颗粒。优选的是直径最大为400μm,优选1-100μm,更优选小于50μm的基本上球形的颗粒。优选的微珠由凝胶(包括诸如琼脂糖之类的水凝胶)形成,例如通过使胶凝的本体组合物破碎或从预胶凝状态模制而形成。
如本文所使用的,应用于本发明的化学文库的术语“微区室(microcompartment)”定义了任何可以包含或包封本发明的微珠并在游离化学结构和从其释放的微珠之间维持空间关联的结构。因此,本发明的微区室用作包含溶剂的封闭反应室,其中游离的、无标签的化学结构在空间上与其同源的编码标签,以及靶测试系统报告部分、靶测试系统的任何其他组分和/或裂解剂相关联。适用于本发明的微区室可通过微区室化方便地实现,这是物理上限制微珠的过程。如下所述,可以通过使用各种微区室(包括微滴、微粒和微泡)来实现物理限制。
如本文所使用的,术语“微滴(microdroplet)”限定小的、离散体积的流体、液体或胶体,其直径为0.1μm至1000μm和/或体积在5×10-7pl至500nl之间。典型地,微滴的直径小于1000μm,例如小于500μm、小于500μm、小于400μm、小于300μm、小于200μm、小于100μm、小于50μm、小于40μm、小于30μm、小于20μm、小于10μm、小于5μm或小于1μm。因此,微滴可以基本为球形,该球形直径为:(a)小于1μm;(b)小于10μm;(c)0.1-10μm;(d)10μm至500μm;(b)10μm至200μm;(c)10μm至150μm;(d)10μm至100μm;(e)10μm至50μm;或(f)大约100μm。
本发明的微滴典型地包含第一流体、液体或胶体的分离部分,该第一流体、液体或胶体的分离部分完全被第二流体、液体或胶体(例如,不混溶的液体或气体)包围。在一些情况下,所述滴可以是球形或基本上为球形。然而,在一些情况下,微滴可以是非球形的,并且具有不规则的形状(例如,由于外部环境施加的力,或在本文所描述的测试和筛选过程的物理操作过程中施加的力)。因此,微滴可以是基本上圆柱形的、塞状的或椭圆形的(例如,在它们符合周围微通道的几何形状的情况下)。
如本文所使用的,术语“微粒”定义为颗粒直径小于1000μm(例如小于500μm)、小于500μm、小于400μm、小于300μm、小于200μm、小于100μm、小于50μm、小于40μm、小于30μm、小于20μm、小于10μm、小于5μm或小于1μm。优选地,所述微粒是非平面的,并且具有的最大尺寸为(或者当基本上为球形时其直径为):(a)10μm至500μm;(b)10μm至200μm;(c)10μm至150μm;(d)10μm至100μm;(e)10μm至50μm;或(f)大约100μm。如本文所定义的,微粒可因此被封装在微滴内。微粒可以由刚性固体、柔性凝胶、多孔固体、多孔凝胶或网状物,或刚性或半刚性原纤维或小管基质形成。
术语“微泡”在本文中用于定义中空微粒,所述中空微粒包括封闭内部体积的外壁或膜,如脂质体。
本发明的微滴、微粒和微泡可以是单分散的。应用于根据本发明使用的微滴和微粒的术语“单分散”限定具有液滴/粒径分散系数ε的微滴/微粒群,ε不大于1.0、不大于0.5,优选地,不大于0.3。所述分散系数ε通过下述公式计算:
ε=(90dp-10dp)/50dp(1)
其中,10dp、50dp和90dp是用乳液的相对积累粒度分布曲线估计累积频率分别为10%、50%和90%的颗粒尺寸。ε=0表示一种理想状态,在该状态下乳液颗粒根本没有显示粒径分散。
如本文所使用的,术语“编码标签”与化学结构相关,用于限定包含唯一地鉴定化学结构或它的反应历史的信息的部分或试剂,从而用作那个特定的化学结构的唯一的标识符(即,所述标签“编码”那个结构并用作分子“条形码”)。所述信息可以以任何形式被编码,但是在优选的实施例中,所述标签是核酸标签(例如,dna),其中所述信息被编码在核酸序列中。但是,也可以使用其它标签,包括非dna标签、非rna标签、经修饰的核酸标签、肽标签、基于光的条形码(例如,量子点)和rfid标签。
如本文所使用的,与化学结构群相关的术语“克隆”定义了一个或多个化学结构的群,其中每一个化学结构由共同的标签编码。克隆的化学结构在化学性质上相同,或仅在可裂解连接子的性质和/或位置上不同,该可裂解连接子将化学结构可逆地连接到微珠上(或在这种连接子裂解后残留下的疤痕上有差异)。
如本文所使用的,应用于化学结构的术语“游离的”用于定义未结合至固相的或处于溶液中的化学结构。在一些实施方案中,该术语定义了未与固相共价结合的化学结构。游离的化学结构可以因此进入液相或胶体相和/或溶液,并且在一些实施方案中与靶测试系统的一个或多个组分相互作用(例如,本发明的微珠的固定化靶测试系统报告部分)。
如本文所使用的,术语“自脱落连接子(self-immolativelinker)”定义为包括自脱落化学基团(在本文中可以称为自分解部分或“sim”)的连接子,该连接子能够直接或间接地(例如,通过肽部分)共价连接所述化学结构和其编码标签以形成稳定的加标签的化学结构,并且其通过涉及所述化学结构的自发释放的机制能够从所述化学结构上释放所述编码标签(例如,通过由酶裂解触发的电子级联反应,导致离去基团的排除和游离化学结构的释放)。
微珠
本发明的微珠可以有任何几何形状,可以是球状、球形、长方体、锥体、长方形、圆柱形或环形。它们可以由固体或凝胶形成。
合适的凝胶包括聚合物凝胶,例如多糖或多肽凝胶,其可以例如通过加热、冷却或ph调节从液体固化成凝胶。其他合适的凝胶包括水凝胶,包括海藻酸盐、明胶、琼脂糖和自组装肽凝胶。
其他合适的材料包括脂类、多肽、塑料(例如聚苯乙烯、聚氯乙烯、环烯烃共聚物、聚丙烯酰胺、聚乳酸、聚丙烯酸酯、聚乙烯、聚丙烯、聚(4-甲基丁烯)、聚甲基丙烯酸酯、聚(对苯二甲酸乙二醇酯)、聚四氟乙烯(ptfe)、尼龙和聚乙烯基丁醛。
因此,微珠可以由聚合物或聚合物的组合形成。在这些实施方案中,所述微珠可包括聚酯,例如聚酯偶联亲水性聚合物。此处,聚酯可包括聚(乳酸)、聚(乙醇酸)、聚(乳酸-共聚乙醇酸)或聚己内酯和/或亲水性聚合物可包括聚醚(例如,包括聚乙二醇)。
合适的微粒材料也包括无机材料,如硅、玻璃、金属和陶瓷。
所述微珠可以用反应性基团或部分(例如链霉亲和素、胺、溴化氰或羧酸)来官能化。或者,根据本发明使用的微珠可以是固体支持物,例如由硅、聚苯乙烯(ps)、交联的聚(苯乙烯/二乙烯基苯)(p[s/dvb])以及聚(甲基丙烯酸甲酯)(pmma)制成。
编码标签
根据本发明,可以使用任何编码标签,只要它包含唯一地鉴定其同源(cognate)化学结构(或其反应历史)的信息(例如,以化学和/或光学性质/特性的形式),从而作为该特定化学结构的唯一标识符。因此,该标签“编码”特定化学结构并作为分子“条形码”。
在优选的实施方案中,所述标签是核酸(例如,dna)标签,其中所述信息被编码在核酸序列中。但是,也可以使用其它标签,其包括非dna标签、非rna标签、经修饰的核酸标签、肽标签、基于光的条形码(例如,量子点)和rfid标签。
正如上文所解释的,化学结构可以采用各种不同的方式加标签,并且还可能不仅使用dna标签来编码特定的化学结构(“dna记录”),而且还作为指导其合成的模板(“dna模板”—参见下文)。近年来对该技术有如下综述:mannocci等(2011)chem.commun.,47:12747-12753;kleiner等(2011)chemsocrev.40(12):5707-5717;以及mullard(2016)nature530:367-369。
编码标签还可以编码其他有用的信息。例如,标签还可以包括指定以下信息:(a)化合物在微珠上的负载;和/或(b)报告部分的性质和/或负载;和/或(c)靶的性质和/或负载。在此类实施方案中,编码标签可以作为单独的标签固定在微珠上,或者作为统一的级联标签的一部分存在。在此类实施方案中,可以用多个不同的交联基团对编码标签进行官能化,从而可以在微珠上的多个不同的交联位点处进行标记。
这种标签的使用允许筛选多个靶并允许建立剂量效应。
标签还可以包括指定与微珠一起微区室化的附加部分的性质和/或负载的信息。在此类实施方案中,可以在封装期间合并大量附加因素,并作为文库筛选的一部分对其进行快速筛选。这可能是多种靶、附加因素、化合物或蛋白质。这可以通过利用本领域技术人员众所周知的不同的流体通道、微注射(pico-injection)或液滴融合(dropletmerging)技术来完成。
标签测序
任何合适的测序技术都可以使用,包括sanger测序,但优选的是称为下一代测序(ngs)(也称为高通量测序)的测序方法和平台。存在许多商业上可获得的ngs测序平台适用于本发明的方法。基于边合成边测序(sbs)的测序平台尤其适用。特别优选的是illuminatm系统(其产生数百万个相对短的序列解读(54、75、100或300bp))。在该方法中,dna分子首先被附着在载玻片上的引物上并且扩增,从而形成局部克隆集落(桥式扩增)。加入四种类型的ddntp,并且洗去未掺入的核苷酸。与焦磷酸测序不同,dna一次只能延伸一个核苷酸。相机拍摄荧光标记的核苷酸图像,然后染料连同末端3'阻断剂被从dna中化学地去除,允许下一个循环。
其他能够读取短序列的系统包括solidtm和iontorrent技术(均由thermofisherscientificcorporation出售)。solidtm技术通过连接法测序。该技术中,所有可能的固定长度的寡核苷酸的库都根据测序位置进行标记。对寡核苷酸进行退火和连接;dna连接酶对匹配序列优先连接,产生该位置处核苷酸的信号信息。测序前,用乳液pcr法扩增dna。将获得的珠粒沉积在载玻片上,每个珠粒仅包含相同dna分子的拷贝。结果是相媲美于illumina测序的数量和长度的序列。
iontorrentsystems公司已经开发了基于使用标准测序化学的系统,但具有新颖的基于半导体的检测系统。此测序方法是基于检测在dna聚合过程中释放的氢离子,而不是其他测序系统中使用的光学方法。含有将被测序的模板dna链的微孔被单一类型的核苷酸浸没。如果引入的核苷酸与先导(leading)模板核苷酸互补,则其被合并到正在生长的互补链中。这导致氢离子的释放,从而触发超灵敏的离子传感器,这表明反应已经发生。如果模板序列中存在均聚物重复序列,则多个核苷酸将在单独的循环中合并。这将导致相应数量的氢被释放,并成比例地产生更高的电子信号。
例如或类似于oxfordnanoporetechnologies(牛津纳米孔技术)所使用的方法,其中核酸或其它大分子通过纳米尺度的孔,并且使用特定的离子电流变化或产生的电信号来鉴定它。例如,寡核苷酸的单个碱基可以在连续碱基通过离子孔时被鉴定为寡核苷酸的一部分,或者在连续的裂解步骤后被鉴定为单个核苷酸。
靶测试系统报告部分
本发明的微珠包含固定的靶测试系统报告部分。报告部分发挥作用的方式为:在包含微珠和水性溶剂的化学文库微区室中,其中已释放出化学结构以产生溶解在溶剂中的游离的、无标签的化学结构(tcs)。在这种情况下,tcs是游离的以接触靶测试系统报告部分和/或靶测试系统的一个或多个附加组分,并且微珠可以在本发明的筛选方法中测定。
可以使用任何合适的报告部分,只要该部分至少以第一状态(在不存在针对靶的活性的情况下采用)和第二状态(在所述活性存在的情况下采用)存在。因此,确定报告部分从第一状态到第二状态的变化可作为针对靶标的活性信号,该信号是在微珠微区室化并将化学结构释放到溶液中后获得的(产生用于筛选针对靶的活性的tcs)。
将理解的是,这样的信号可以是正信号(例如荧光的捕获或构象移位)或空信号(例如荧光的丢失或不存在构象移位)。
因此,在最简单的情况下,报告部分是靶标本身(或其片段),而测试系统用于靶标结合活性。在此类实施方案中,第一状态是未结合的靶标,第二状态是靶标-化合物配合物。在这种情况下,测试系统由报告部分组成(或基本上由报告部分组成),因为在第一状态到第二状态的变化驱动中不涉及其他测试系统组分。在这种情况下,微区室无需包含其它靶测试系统组分:通过物理技术或通过使用合适的检测探针和/或直接应用于所筛选的微珠的试剂筛选从打开的微区室中释放的微珠,通过分析该微珠来检测报告部分的状态变化。
在另一个简单的情况下,报告部分是酶靶的底物,并且该测试是针对酶靶的抑制活性。在此类实施方案中,第一状态是酶修饰的底物,第二状态是非酶修饰的底物。在这种情况下,测试系统需要靶酶作为附加组分,并且该酶包含在测定微珠的微区室中。报告部分状态的变化可以通过任何方便的检测系统进行检测,包括抗体探针或伴随酶修饰、标记标记物的酶促掺入的荧光的增加(或丢失)。因此,通过物理技术或通过使用合适的检测探针和/或直接应用于所筛选的微珠的试剂筛选从打开的微区室中释放的微珠,通过分析该微珠再次检测报告部分的状态变化。
在又一个简单的情况下,报告部分是受体靶的结合伴侣(例如配体),并且该分析是针对受体阻断活性的。在此类实施方案中,第一状态是与受体复合的报告部分,而第二状态是未复合的报告部分。在这种情况下,测试系统需要靶受体作为附加成分,并且这包括在其中测定微珠的微区室中。报告部分的状态变化可以通过任何方便的检测系统进行检测,包括抗体探针或配体-受体结合所伴随的荧光的增加(或丢失)(例如,通过受体上的猝灭基团猝灭报告部分上的荧光标记)。因此,通过物理技术或通过使用合适的检测探针和/或直接应用于所筛选的微珠的试剂筛选从打开的微区室中释放的微珠,通过分析该微珠再次检测报告部分的状态变化。
因此,本领域技术人员将理解,可以根据靶的性质和要筛选的活性来选择系统报告部分,并且可以基于在状态变化期间发生的任何修饰来区分靶测试的第一状态和第二状态。
这可以通过测量以下各项来检测:(a)荧光,例如淬灭或未淬灭的荧光;和/或(b)裂解或未裂解的构象;和/或(c)磷酸化或非磷酸化状态;(d)不同的糖基化类型、模式或程度;和/或(e)不同的抗原决定簇;和/或(f)与配体结合或未结合;和/或(g)与一种或多种其他测试系统组分络合或不络合。
这意味着本发明的微珠可以编码的信息不仅可以是化学结构的性质,而且当测试针对溶液中的靶进行测试且无任何空间抑制的情况下,可以编码的信息还可以是这些化学结构的活性。
这极大地促进了反应后的筛选,因为在报告部分的状态固定后(并由此产生信号),微珠不需要维持在微区室中,因为一旦信号被获取,就不再需要与tcs和/或测试系统的其它组分的空间关联。
因此,可以从微区室除去、分离和/或隔离微珠,其中进行释放的tcs的分析,然后进行多种物理化学操作,包括选择和分级分离技术,这些操作会物理上破坏相对较大和脆弱的微区室。这提供了极大的灵活性,可以用来极大地提高hts的通量以及命中反褶积(deconvolution)和特性。
此类测试后反应的物理化学操作包括hts方案,包括使用fret、facs、免疫沉淀、免疫沉降、免疫过滤、离心分离、梯度离心、差异浮力分离、过滤、亲和柱色谱和/或磁性微珠亲和力选择高通量筛选。因此,本发明的筛选方法可以包括fads和/或facs。筛选步骤还可包括荧光分析,包括但不限于fret、flim、荧光团标记的抗体、荧光团标记的dna序列或荧光染料。
化学结构
所述化学结构可以是小分子(如本文所限定)。在一些实施方案中,所述结构由许多相连接的结构组成。在优选的实施方案中,所述化学结构是通过分开与合并(split-and-pool)方法论来阐述的(如下所述)。
在其他实施例中,化学结构可以是大分子(如此处所定义)。
分开与合并(split-and-pool)产生化学结构
在优选的实施方案中,使用了分开与合并(split-and-pool)化学结构/标记技术(参见mannocci等(2011)chem.commun.,47:12747-12753,特别是其图3,该文件在此通过引用并入本文)。
在这种方法中,首先将一个核或一系列核固定在微珠表面上。通过在此阶段改变核的负载,可以控制最终会在珠粒上产生的化合物的数量,从而可以确定剂量效应(可以很方便地通过将指定负载的信息合并到标签中进行)。在许多实施方案中,选择化学结构的负载,使得微区室化(例如,微滴内的包封)后的浓度在pmolar到molar浓度范围内。因此,在此阶段添加相同序列的多个dna片段以编码该核结构以及微珠上该核的负载。因此,编码标签可以以多个拷贝存在,并且在一些实施方案中,将标签的几百万个拷贝固定在单个微珠上。
由于核的表面上有多个载体(vector),因此可以通过不同的化学反应对其进行化学修饰,以允许使用分开与合并方法。在这种方法论中,通过将大量不同的化学单体添加到特定载体中来修饰核,唯一的限制是每个载体必须通过兼容的化学方法进行修饰。这可能涉及1到100,000个单体。单体添加的性质是通过将一条新的dna片段连接到已经附着在珠子上的dna片段上来编码。然后,将含有单体的珠粒再次合并到一个单库(singlepool)中,然后分开成新的群,并添加第二组单体,然后通过dna连接对其进行编码。可以对任意数量的单体添加重复进行此操作。但是,在优选的方法论中,每个核使用2或3个载体。
现有的化学文库的克隆标签
可以通过任何合适的手段来提供加标签的化学结构。例如,根据本发明供使用的微珠可以包含化学结构的克隆群,编码标签或标签可释放地连接到所述微珠。在此类实施方案中,化学结构的克隆群可以是商售化学文库的一部分(element)。
合适的基于核酸的标签是可商购的(例如来自twistbiosciencecorporation),但是可以如wo2015/021080中所描述的,合成这些标签(该内容在此通过引用并入本文)。
化学结构的模板化合成
在某些实施方案中,编码的核酸标签用作化学结构的模板。在此类实施方案中,以核酸为模板(例如,以dna为模板)合成所述化学结构,然后与微粒进行可释放的连接,以提供加标签的化学结构的文库。可以使用任何合适的模板化技术,例如以下文献中描述了合适的技术:mannocci等(2011)chem.commun.,47:12747-12753;kleiner等(2011)chemsocrev.40(12):5707-5717;和mullard(2016)nature530:367-369。同样适用的是pehrharbury教授和他的同事们(斯坦福大学,usa)开发的dna路由方法(dna-routingapproach)。dna模板可以以任何方式绘制或构造:例如,yocto反应系统(yoctoreactorsystem)采用三链的dna发夹环连接体(three-waydna-hairpin-loopedjunction),通过将合适的供体化学部分(moiety)转移到核受体位点来辅助文库合成(参见wo2006/048025,在此通过引用方式合并其公开内容)。
也可以使用可替代的结构几何图形,例如,lundberg等(2008)nucleicacidssymposium(52):683-684中描述的四链dna霍利迪连结体(hollidayjunctions)和六边形结构,以及由rothemund(2006)nature440:297-302综述的“dna支架折纸术(scaffoldeddnaorigami)”技术创建的复杂形状和图形。
可裂解的连接子
所述化学结构通过可裂解的连接子可释放地连接到所述微珠上。
任何可裂解的连接子均可以用于将化学结构的克隆群可裂解地连接到所述微珠上(因此间接地连接到其编码标签上)。在优选的实施方案中,所述可裂解的连接子为“无疤痕的(scarless)”。在此类实施方案中,经编码的化学结构以完全或基本上不含连接子残基的形式被释放,使其活性在筛选中不受连接子裂解后残留的“疤痕(scars)”的影响。应当理解,一些连接子“疤痕”可被容忍,如-oh和/或-sh和/或-nh基团。裂解的方法/裂解剂优选与测试系统兼容。
范围宽阔的合适的可裂解连接子是本领域技术人员所熟知的,并且leriche等人(2012)bioorganic&medicinalchemistry20(2):571-582中描述了合适的实施例。因此合适的连接子可以包括以下连接子:酶可裂解连接子;亲核试剂/碱敏感连接子;还原敏感的连接子;光可裂解连接子;亲电试剂/酸敏感连接子;金属辅助型裂敏感连接子;氧化敏感连接子;以及前述两种或两种以上的组合。
例如,以下文件中描述了酶可裂解连接子:wo2017/089894;wo2016/146638;us2010273843;wo2005/112919;wo2017/089894;degroot等人(1999)j.med.chem.42:5277;degroot等(2000)jorg.chem.43:3093(2000);degroot等人,(2001)jmed.chem.66:8815;wo02/083180;carl等(1981)jmed.chem.lett.24:479;studer等人(1992)bioconjugatechem3(5):424-429;carl等人(1981)j.med.chem.24(5):479-480和dubowchik等人(1998)bioorg&med.chem.lett.8:3347。它们包括酶的可裂解的连接子,选自以下:蛋白酶(包括肠激酶)、核酸酶、硝基还原酶、磷酸酶、β-葡萄糖醛酸酶、溶酶体酶、tev、胰蛋白酶、凝血酶、组织蛋白酶b、b和k、胱天蛋白酶、基质金属蛋白酶、磷酸二酯酶、磷脂酶、酯酶和β-半乳糖苷酶的酶。亲核试剂/碱可裂解连接子包括:二烷基二烷氧基硅烷、氰乙基、砜、乙二醇二琥珀酸盐、2-n-丙烯基硝基苯磺酰胺、α-噻吩酯(α-thiophenylester)、不饱和乙烯基硫化物、磺胺、丙二醛吲哚衍生物、乙酰丙酸酯(levulinoylester)、肼、酰基腙、烷基硫酯。还原可裂解连接子包括二硫桥和偶氮化合物。辐射可裂解连接子包括:2-硝基苄基衍生物、苯酰基酯、8-喹啉基苯磺酸盐、香豆素、磷酸三酯、双芳酰腙、双胺双硫代丙酸(bimanebi-thiopropionicacid)衍生物。亲电试剂/酸敏感连接子包括:对甲氧苄基衍生物、叔丁基氨基甲酸酯类似物、二烷基或二芳基二烷氧基硅烷、原酸酯、缩醛、乌头酰基(aconityl)、肼、β-硫代丙酸盐、磷酸亚胺(phosphoramadite)、亚胺基、三苯甲基、乙烯基醚、聚酮基、烷基2-(二苯基膦基)苯甲酸酯衍生物。有机金属/金属催化可裂解连接子包括:烯丙基酯、8-羟基喹啉酯和吡啶甲酸酯。氧化可裂解连接子包括:邻二醇和硒化合物。
在某些实施方案中,可裂解的连接子包含共价和非共价键(例如,从核酸杂交产生的氢键)的组合。因此,可以通过核酸杂交将所述化学结构(直接地或间接地)可释放地连接到所述微粒。在此类实施方案中,所述可裂解的连接子可以包括rna,并且,在此类实施方案中,裂解剂可以包括核糖核酸酶(rnase)。在其他实施方案中,所述可裂解的连接子可以包括dna,并且,在此类实施方案中,裂解剂可以包括位点特异性核酸内切酶。当可裂解的连接子来自于核酸杂交,则所述裂解剂可以包括使核酸去杂交化,例如,融解(melting),所述核酸与所述化学结构偶联并与偶联到所述微粒的核酸杂交。
在其它实施方案中,可裂解连接体可包括肽,在此类实施方案中,裂解剂可包括肽酶。可裂解的(例如酶可裂解的)肽连接子可以包含由单个氨基酸组成的肽部分,或氨基酸的二肽或三肽序列。所述氨基酸可以选自天然氨基酸和非天然的氨基酸,并且在每种情况下,侧链碳原子可以是d或l(r或s)构型。示例性氨基酸包括:丙氨酸、2-氨基-2-环己基乙酸、2-氨基-2-苯乙酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酰胺、谷氨酸、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、蛋氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、色氨酸、酪氨酸、缬氨酸、γ-氨基丁酸、β,β-二甲基γ-氨基丁酸、α,α-二甲基γ-氨基丁酸、鸟氨酸和瓜氨酸(cit)。合适的氨基酸还包括上述氨基酸的保护形式,其中侧链的反应性功能受到保护。这种被保护的氨基酸包括由乙酰基、甲酰基、三苯基甲基(三苯甲基)和单甲氧基三苯甲基(mmt)保护的赖氨酸。其它受保护的氨基酸单元包括甲苯磺酰基或硝基保护的精氨酸以及乙酰基或甲酰基基团保护的鸟氨酸。
自脱落连接子
特别适合作为可裂解连接子用于本发明的是自脱落连接子,其包括:(a)裂解部分;和(b)自脱落部分(“sim”)。
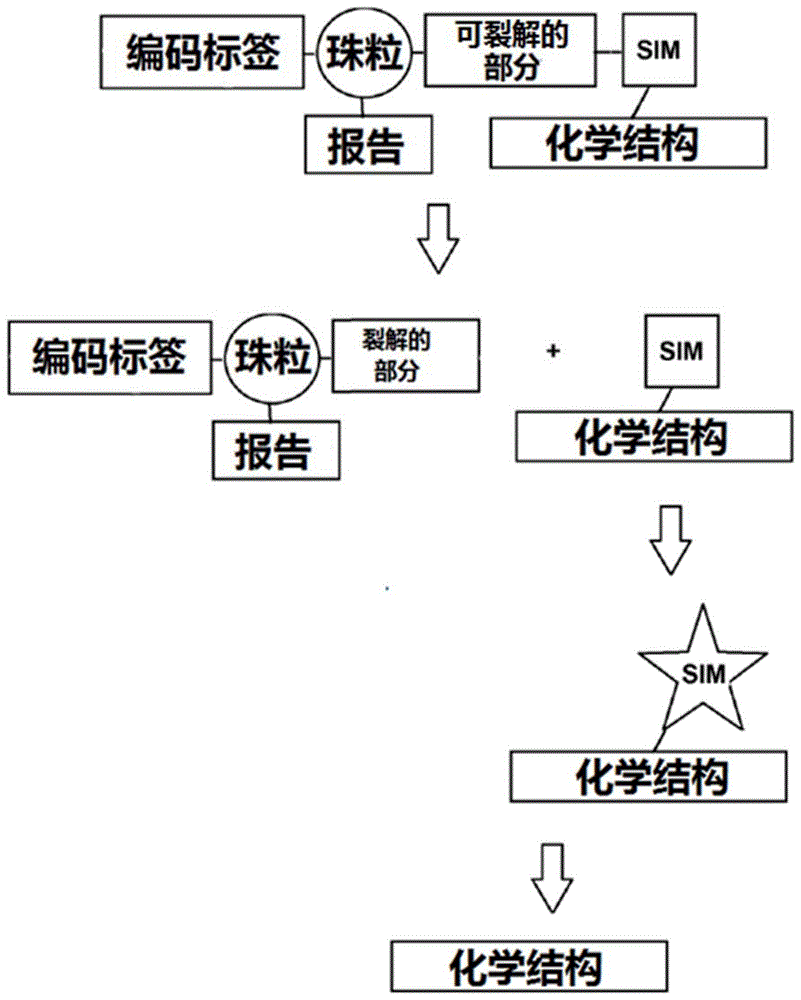
这样的连接子可以如图1所示使用,其表明sim在裂解后会自发消失,从而释放出游离的化学结构。
特别适合的自脱落连接子包含:(a)酶可裂解部分;(b)sim。在此类实施方案中,酶可裂解部分可以是肽序列(用蛋白酶裂解)或非肽酶可裂解基团,例如,包含β-葡萄糖醛酸酶可裂解的亲水性糖基的葡糖苷酸部分(如在mccombsandowen(2015)antibodydrugconjugates:designandselectionoflinker,payloadandconjugationchemistrytheaapsjournal17(2):339-351所解释),其显示以下:
在wo2007/011968、us20170189542和wo2017/089894(它们的内容在此通过引用并入)中描述了合适的基于β-葡糖苷酸的连接子。因此这样的连接子可以具有下式:
其中,r3是氢或羧基保护基团,以及每个r4独立地是氢或羟基保护基。
对于本发明中使用的自脱落连接子的sim可以选自:取代的烷基、未取代的烷基、取代杂烷基、未取代的杂烷基、未取代的杂环烷基、取代的杂环烷基、取代和未取代的芳基,或取代和未取代的杂芳基。合适的sim因此包括对氨基苄醇(pab)单元和在电子方面与pab基团相似的芳香化合物(例如,hay等人(1999)bioorg.med.chem.lett.9:2237中描述的2-氨基咪唑-5-甲醇衍生物)以及邻位或对位氨基苄基乙缩醛(ortho-orpara-aminobenzylacetals)。
其它合适的sim是在酰胺键水解后发生环化的那些,例如,rodrigues等在(1995)chemistrybiology2:223中描述的取代的和未取代的4-氨基丁酸酰胺。进一步的合适的sim包括适当被取代的双环[2.2.1]和双环[2.2.2]环系统,如storm等人(1972)jamer.chemsoc.94:5815中描述的,以及各种2-氨基苯丙酸酰胺(参见,例如,amsberry等人(1990)j.orgchem.55:5867)。
特别合适的是包含肽作为裂解部分的自脱落肽连接子。图2和图3显示了使用这种连接子构建和使用编码化学文库。在此,可裂解肽为二肽缬氨酸-瓜氨酸,sim为对氨基苄醇(pab)。在此类实施方案中,酰胺连接的pab的酶裂解触发1,6-去除二氧化碳以及伴随释放游离化学结构。如图2也显示,编码标签和化学结构可以通过珠粒连接,并且单个珠粒可以装载有多个(其中,n>1)化学结构,例如,使编码标签与连接的化学结构的比率为1:10至1:1000。在此类实施方案中,肽连接子相对较小的尺寸使扩散速率提高和珠粒负载更高,而化学结构只需要单一胺用于官能化。
根据本发明用作自脱落连接子的合适的裂解部分和sim的非限制性实例,例如,在wo2017/089894;wo2016/146638;us2010273843;wo2005/112919;wo2017/089894;degroot等人(1999)j.med.chem.42:5277;degroot等人(2000)jorg.chem.43:3093(2000);degroot等人,(2001)jmed.chem.66:8815;wo02/083180;carl等人(1981)jmed.chem.lett.24:479;studer等人(1992)bioconjugatechem.3(5):424-429;carl等人(1981)j.med.chem.24(5):479-480和dubowchik等人(1998)bioorg&med.chem.lett.8:3347(在此通过引用合并其公开内容)中描述。
靶
靶蛋白
本发明的测试系统的靶可以包括靶蛋白。它可以包括分离的靶蛋白或分离的靶蛋白复合物。例如,所述靶蛋白/蛋白复合物可以是胞内靶蛋白/蛋白复合物。所述靶蛋白/蛋白复合物可以在溶液中,或者可以由膜蛋白/蛋白复合物或跨膜蛋白/蛋白复合物组成。在此类实施方案中,可以筛选化学结构配体,所述配体结合到靶蛋白/蛋白复合物。所述配体可以是所述靶蛋白/蛋白复合物的抑制剂。
可以使用任何合适的靶蛋白,包括上面部分中讨论的任何靶细胞的蛋白。因此,适用于根据本发明测试系统的靶蛋白可以选自真核蛋白、原核蛋白、真菌蛋白和病毒蛋白。
因此合适的靶蛋白包括但不限于:癌蛋白、运输(核、载体、离子、通道、电子、蛋白质)、行为、受体、细胞死亡、细胞分化、细胞表面、结构蛋白、细胞粘附、细胞通讯、细胞运动、酶、细胞功能(解旋酶、生物合成、马达、抗氧化、催化、代谢、蛋白水解)、膜融合、发育、调节生物过程的蛋白质、具有信号转导活性的蛋白质、受体活性、异构酶活性、酶调节活性、伴侣调节、结合活性、转录调节活性、翻译调节活性、结构分子活性、连接酶活性、细胞外组织活性、激酶活性、生物发生活性、连接酶活性和核酸结合活性。
靶蛋白可以选自并且因此不限于:dna甲基转移酶、akt途径蛋白、mapk/erk途径蛋白、酪氨酸激酶、上皮生长因子受体(egfr)、成纤维细胞生长因子受体(fgfr)、血管内皮生长因子受体(vegfr)、产生红细胞生成素的人肝细胞受体(eph)、原肌球蛋白受体激酶、肿瘤坏死因子、细胞凋亡调节bcl-2家族蛋白、极光激酶、染色质、g蛋白偶联受体(gpcr)、nf-κβ通路、hcv蛋白、hiv蛋白、天冬氨酰蛋白酶、组蛋白脱乙酰酶(hdac)、糖苷酶、脂肪酶、组蛋白乙酰转移酶(hat)、细胞因子和激素。
特定的靶蛋白质可选自:erk1/2、erk5、a-raf、b-raf、c-raf、c-mos、tpl2/cot、mek、mkk1、mkk2、mkk3、mkk4、mkk5、mkk6、mkk7、tyk2、jnk1、jnk2、jnk3、mekk1、mekk2、mekk3、mekk4、ask1、ask2、mlk1、mlk2、mlk3、p38α、p38β、p38γ、p38δ、brd2、brd3、brd4、磷脂酰肌醇-3激酶(pi3k)、akt、蛋白激酶a(pka)、蛋白激酶b(pkb)、蛋白激酶c(pkc)、pgc1α、sirt1、pd-l1、mtor、pdk-1、p70s6激酶、叉头易位因子、melk、elf4e、hsp90、hsp70、hsp60、i型拓扑异构酶、ii型拓扑异构酶、dnmt1、dnmt3a、dnmt3b、cdk11、cdk2、cdk3、cdk4、cdk5、cdk6、cdk7、α-微管蛋白、(β-微管蛋白、γ-微管蛋白、δ-微管蛋白、ε-微管蛋白、janus激酶(jak1、jak2、jak3)、abl1、abl2、egfr、epha1、epha2、epha3、epha4、epha5、epha6、epha7、epha8、epha10、ephb1、ephb2、ephb3、ephb4、ephb6、her2/neu、her3、her4、alk、fgfr1、fgfr2、fgfr3、fgfr4、igf1r、insr、insrr、vegfr-1、vegfr-2、vegfr-3、flt-3、flt4、pdgfra、pdgfrb、csf1r、axl、irak4、scfr、fyn、musk、btk、csk、plk4、fes、mer、c-met、lmtk2、frk、ilk、lck、tie1、fak、ptk6、tnni3、roscck4、zap-70、c-src、tec、lyn、trka、trkb、trkc、ret、ror1、ror2、ack1、syk、mdm2、hras、kras、nras、rock、pi3k、bace1、bace2、ctsd、ctse、napsa、pgc、肾素、mmset、极光激酶a、极光激酶b、极光激酶c、法尼基转移酶、端粒酶、腺苷酸环化酶、camp磷酸二酯酶、parp1、parp2、parp4、parp-5a、parp-5b、pkm2、keapl、nrf2、tnf、trail、ox40l淋巴毒素-α、ifnar1、ifnar2、ifn-α、ifn-β、ifn-γ、ifnlr1、ccl3、ccl4、ccl5、il1α、il1β、il-2、il-2、il-4、il-5、il-6、il-7、il-9、il-9、il-10、il-11、il-12、il-13、il-15、il-17、bcl-2、bcl-xl、bax、hcv解旋酶、e1、e2、p7、ns2、ns3、ns4a、ns4b、ns5a、ns5b、nf-kb1、nf-kb2、rela、relb、c-rel、rip1、ace、hiv蛋白酶、hiv整合酶、gag、pol、gp160、tat、rev、nef、vpr、vif、vpu、rna聚合酶、gaba转氨酶、逆转录酶、dna聚合酶、催乳素、acth、anp、胰岛素、pde、ampk、inos、hdac1、hdac2、hdac3、hdac4、hdac5、hdac6、hdac7、hdac8、hdac9、hdac10、hdac11、乳糖酶、淀粉酶溶菌酶、神经氨酸酶、转化酶(invertase)、几丁质酶、透明质酸酶、麦芽糖酶、蔗糖酶、磷酸酶、磷酸化酶、p、组氨酸脱羧酶、pten、组蛋白赖氨酸脱甲基酶(kdm)、gcn5、pcaf、hat1、atf-2、tip60、moz、morf、hbo1、p300、cbp、src-1、src-3、actr、tif-2、taf1、tfiiic、蛋白o甘露糖基转移酶1(pomt1)、淀粉样蛋白β和tau。
靶细胞
由于可以将活细胞或死细胞与本发明的微珠一起进行微区室化,因此本发明发现了在基于细胞、表型的分析法中的特定应用。在此类实施方案中,靶测试系统报告部分响应于靶细胞的变化而改变状态,其中靶细胞的变化由对该靶细胞具有特定所需活性的化学结构诱导。这些变化包括细胞因子、代谢产物、毒素、抗体、激素、信号分子或酶的释放。在一些实施方案中,测试系统可以是均相水相测试系统,并且可以包括表型筛选。在此类实施方案中,测试系统可以包含活靶细胞。
如下所述,可以采用任何合适的靶细胞。
靶细胞可以是古细菌,例如选自以下门类中的古细菌:(a)泉古菌(crenarchaeota)、(b)广古菌(euryarchaeota)、(c)初古菌(korarchaeota)、(d)纳古菌(nanoarchaeota)和(e)奇古菌(thaumarchaeota),例如沃氏富盐菌(haloferaxvolcanii)或硫化叶菌(sulfolobusspp.)。
根据本发明,适于用作靶细胞的原核细胞包括细菌细胞。在此类实施方案中,靶细胞可以是致病菌。其它细菌靶细胞包括选自革兰氏阳性细菌的细胞(例如,选自粪肠球菌(enterococcusfaecalis)、屎肠球菌(enterococcusfaecium)和金黄色葡萄球菌(staphylococcusaureus));革兰氏阴性细菌(例如,选自肺炎克雷伯氏菌(klebsiellapneumoniae)、鲍氏不动杆菌(acinetobacterbaumanii)、大肠埃希氏菌(escherichiacoli)、大肠杆菌st131菌株、铜绿假单胞菌(pseudomonasaeruginosa)、阴沟肠杆菌(enterobactercloacae)、产气肠杆菌(enterobacteraerogenes)和淋病奈瑟氏菌(neisseriagonorrhoeae))和表现出不确定的革兰氏反应的细菌。
根据本发明,适于用作靶细胞的真核细胞包括:(a)真菌细胞、(b)哺乳动物细胞、(c)高等植物细胞、(d)原生动物、(e)寄生虫(helminth)细胞;(f)藻类细胞;(g)来自临床组织样品的细胞(例如人类患者的样品)和(h)无脊椎动物细胞。
合适的哺乳动物细胞包括癌细胞,例如人癌细胞、肌肉细胞、人类神经元细胞和来自活人患者的显示疾病相关表型的其它细胞。
在所述细胞为真核细胞的情况下(例如人类细胞),所述细胞可以选自:全能细胞、多能细胞、诱导多能细胞、专能细胞、寡能细胞、干细胞、胚胎干细胞(es)、体细胞、生殖系细胞、最终分化的细胞、不分裂的(有丝分裂后)细胞、有丝分裂细胞、原代细胞、细胞系来源的细胞和肿瘤细胞。
所述细胞优选地是分离的(即,不存在于它天然的细胞/组织环境中)和/或有代谢活性(例如,与维持细胞活力和/或活性和/或支持细胞生长或增殖的培养物或转运介质一起存在于测试系统中)。
合适的真核细胞可以从生物体分离,例如选自以下生物体:后生动物、真菌(如酵母)、哺乳动物、非哺乳动物、植物、原生动物、寄生虫、藻类、昆虫(如苍蝇)、鱼类(如斑马鱼)、两栖类(如青蛙)、鸟类、无脊椎动物及脊椎动物。
合适的真核细胞也可从下列非人类动物中分离:哺乳动物、啮齿动物、兔、猪、绵羊、山羊、牛、大鼠、小鼠、非人灵长类动物和仓鼠。在其它实施方案中,所述细胞可以从表达异源基因的非人类疾病模型或转基因非人类动物中分离,所述异源基因例如编码治疗产品的异源基因。
细菌作为靶细胞
本发明使用的靶细胞可以是细菌细胞。在这些实施方案中,细菌可以选自:(a)革兰氏阳性、革兰氏阴性和/或革兰氏染色不定(gran-variable)细菌;(b)孢子形成细菌;(c)非孢子形成细菌;(d)丝状细菌;(e)细胞内细菌;(f)专性需氧菌;(g)专性厌氧菌;(h)兼性厌氧菌;(i)微需氧细菌和/或(f)条件性细菌病原体。
在某些实施方案中,根据本发明使用的靶细胞可以选自以下属的细菌:不动杆菌(acinetobacter)(例如鲍氏不动杆菌(a.baumannii));气单孢菌(aeromonas)(例如嗜水气单胞菌(a.hydrophila));芽孢杆菌(bacillus)(例如炭疽杆菌(b.anthracis));拟杆菌(bacteroides)(例如脆弱拟杆菌(b.fragilis));博德特氏菌(bordetella)(例如百日咳杆菌(b.pertussis));疏螺旋体(borrelia)(例如伯氏疏螺旋体(b.burgdorferi));布鲁氏菌(brucella)(例如流产布鲁氏菌(b.abortus)、犬种布鲁氏菌(b.canis)、羊种布鲁氏菌(b.melitensis)和猪布鲁氏菌(b.suis));伯克氏菌(burkholderia)(例如洋葱伯克氏菌群(b.cepaciacomplex));弯曲杆菌(campylobacter)(例如空肠弯曲杆菌(c.jejuni));衣原体(chlamydia)(例如沙眼衣原体(c.trachomatis)、猪衣原体(c.suis)和鼠衣原体(c.muridarum));嗜性衣原体(chlamydophila)(例如(例如肺炎嗜性衣原体(c.pneumoniae)、反刍动物嗜性衣原体(c.pecorum)、鹦鹉热嗜性衣原体(c.psittaci)、流产嗜性衣原体(c.abortus)、猫嗜性衣原体(c.felis)和豚鼠嗜性衣原体(c.caviae));柠檬酸杆菌(citrobacter)(例如弗氏柠檬酸杆菌(c.freundii));梭菌(clostridium)(例如肉毒梭菌(c.botulinum)、艰难梭菌(c.difficile)、产气荚膜梭菌(c.perfringens)和破伤风梭菌(c.tetani));棒状杆菌(corynebacterium)(例如白喉棒状杆菌(c.diphteriae)和谷氨酸棒状杆菌(c.glutamicum));肠杆菌(enterobacter)(例如阴沟肠杆菌(e.cloacae)和产气肠杆菌(e.aerogenes));肠球菌(enterococcus)(例如粪肠球菌(e.faecalis)和屎肠球菌(e.faecium));埃希氏菌(escherichia)(例如大肠埃希氏杆菌(e.coli));黄杆菌(flavobacterium);弗朗西斯菌(francisella)(例如土拉热弗朗西丝菌(f.tularensis));梭杆菌(fusobacterium)(例如坏死梭杆菌(f.necrophorum));嗜血杆菌(haemophilus)(例如睡眠嗜血杆菌(h.somnus)、流感嗜血杆菌(h.influenzae)和副流感嗜血杆菌(h.parainfiuenzae));螺杆菌(helicobacter)(例如幽门螺杆菌(h.pylon));克雷伯氏菌(klebsiella)(例如产酸克雷伯氏菌(k.oxytoca)和肺炎克雷伯氏菌(k.pneumoniae));军团菌(legionella)(例如嗜肺军团菌(l.pneumophila));钩端螺旋体(leptospira)(例如问号钩端螺旋体(l.interrogans));李斯特菌(listeria)(例如单核细胞增生李斯特菌(l.monocytogenes));莫拉氏菌(moraxella)(例如卡他莫拉菌(m.catarrhalis));摩根氏菌(morganella)(例如摩氏摩根氏菌(m.morganii));分枝杆菌(mycobacterium)(例如麻风分枝杆菌(m.leprae)和结核分枝杆菌(m.tuberculosis));支原体(mycoplasma)(例如肺炎支原体(m.pneumoniae));奈瑟氏菌(neisseria)(例如淋病奈瑟氏菌(n.gonorrhoeae)和脑膜炎奈瑟球菌(n.meningitidis));巴氏杆菌(pasteurelia)(例如多杀性巴氏杆菌(p.multocida));消化链球菌(peptostreptococcus);普雷沃菌(prevotella);变形杆菌(proteus)(例如奇异变形杆菌(p.mirabilis)和普通变形杆菌(p.vulgaris));假单胞菌(pseudomonas)(例如铜绿假单胞菌(p.aeruginosa));立克次氏体(rickettsia)(例如立克次氏立克次氏体(r.rickettsii));沙门氏菌(salmonella)(例如伤寒(typhi)和鼠伤寒(typhimurium)血清型);沙雷氏菌(serratia)(例如粘质沙雷氏菌(s.marcesens));志贺氏菌(shigella)(例如福氏志贺氏菌(s.flexnaria)、痢疾志贺氏菌(sdysenteriae)和宋内氏志贺氏菌(s.sonnei));葡萄球菌(staphylococcus)(例如金黄色葡萄球菌(s.aureus)、溶血性葡萄球菌(shaemolyticus)、中间葡萄球菌(s.intermedius)、表皮葡萄球菌(s.epidermidis)和腐生葡萄球菌(s.saprophyticus);寡养单胞菌(stenotrophomonas)(例如嗜麦芽寡养单胞菌(s.maltophila));链球菌(streptococcus)(例如无乳链球菌(s.agalactiae)、变形链球菌(s.mutans)、肺炎链球菌(s.pneumoniae)和酿脓链球菌(s.pyogenes));密螺旋体(treponema)(例如苍白密螺旋体(t.pallidum));弧菌(vibrio)(例如霍乱弧菌(v.cholerae))和耶尔森氏菌(yersinia)(例如鼠疫耶尔森氏菌(y.pestis))。
根据本发明使用的靶细胞可选自高g+c革兰氏阳性细菌和低g+c革兰氏阳性细菌。
致病菌作为靶细胞
人类或动物细菌性病原体包括细菌例如:军团菌(legionellaspp.)、李斯特菌(listeriaspp.)、假单胞菌(pseudomonasspp.)、沙门氏菌(salmonellaspp.)、克雷伯氏菌(klebsiellaspp.)、哈夫尼菌(hafniaspp.)、嗜血杆菌(haemophilusspp.)、变形杆菌(proteusspp.)、沙雷氏菌(serratiaspp.)、志贺氏菌(shigellaspp.)、弧菌(vibriospp.)、芽孢杆菌(bacillusspp.)、弯曲杆菌(campylobacterspp.)、耶尔森氏菌(yersiniaspp.)、梭菌(clostridiumspp.)、肠球菌(enterococcusspp.)、奈瑟氏菌(neisseriaspp.)、链球菌(streptococcusspp.)、葡萄球菌(staphylococcusspp.)、分枝杆菌(mycobacteriumspp.)、肠杆菌(enterobacterspp.)。
真菌作为靶细胞
本发明使用的靶细胞可以是真菌细胞。它们包括酵母,例如念珠菌属,包括白色念珠菌(c.albicans)、克鲁斯念珠菌(ckrusei)和热带念珠菌(ctropicalis);以及丝状真菌,例如曲霉(aspergillusspp.)和青霉(penicilliumspp.),以及皮肤真菌,例如毛癣菌(trichophytonspp.)。
植物病原体作为靶细胞
根据本发明使用的靶细胞可以是植物病原体,例如假单胞菌(pseudomonasspp.)、木杆菌(xylellaspp.)、青枯菌(ralstoniaspp.)、黄单胞菌(xanthomonasspp.)、欧文氏菌(erwiniaspp.)、镰刀菌(fusariumspp.)、疫霉菌(phytophthoraspp.)、葡萄孢菌(botrytisspp.)、小球腔菌(leptosphaeriaspp.)、白粉菌(powderymildews)(子囊菌(ascomycota))和锈菌(rusts)(担子菌(basidiomycota))。
癌细胞作为靶标
癌细胞可以用作靶细胞。此类细胞可以源自细胞系或源自原发性肿瘤。癌细胞可以是哺乳动物细胞,且优选是人的癌细胞。在某些实施方案中,所述癌细胞选自黑色素瘤、肺、肾、结肠、前列腺、卵巢、乳腺、中枢神经系统和白血病细胞系。
合适的癌细胞系包括但不限于:卵巢癌细胞系(例如,caov-3、ovcar-3、es-2、sk-ov-3、sw626、tov-21g、tov-112d、ov-90、mda-h2774和pa-i);乳腺癌细胞系(例如,mcf7、mda-mb-231、mda-mb-468、mda-mb-361、mda-md-453、bt-474、hs578t、hcc1008、hcc1954、hcc38、hcci143、hcci187、hcc1395、hcc1599、hcc1937、hcc2218、hs574.t、hs742.t、hs605.t和hs606);肺癌细胞系(例如,nci-h2126、nci-h1395、nci-h1437、nci-h2009、nci-h1672、nci-h2171、nci-h2195、nci-hi184、nci-h209、nci-h2107和nci-h128);皮肤癌细胞系(例如colo829、te354.t、hs925.t、wm-115和hs688(a).t);骨癌细胞系(例如,hs919.t、hs821.t、hs820.t、hs704.t、hs707(a).t、hs735.t、hs860.t、hs888.t、hs889.t、hs890.t和hs709.t);结肠癌细胞系(例如,caco-2、dld-i、hct-116、ht-29和sw480);以及胃癌细胞系(例如,rf-i)。在本发明方法中有用的癌细胞系可以从任何方便的来源获得,包括美国典型培养物保藏中心(americantypeculturecollection,atcc)和国家癌症研究所(nationalcancerinstitute)。
其它癌症细胞系包括来自肿瘤细胞/受试者患有癌变的细胞系,包括增生性疾病、良性、癌前和恶性肿瘤、增生、化生和异型增生。增生性疾病包括但不限于癌症、癌症转移、平滑肌细胞增殖、系统性硬化、肝硬化、成人呼吸窘迫综合征、特发性心肌病、红斑狼疮、视网膜病变(例如糖尿病视网膜病变)、心脏增生、良性前列腺增生、卵巢囊肿、肺纤维化、子宫内膜异位症、纤维瘤病、错构瘤(harmatomas)、淋巴管瘤、结节病和硬纤维瘤。涉及平滑肌细胞增殖的肿瘤包括血管系统中细胞的过度增殖(例如,内膜平滑肌细胞增生、再狭窄和血管闭塞,特别是包括生物或机械介导的血管损伤后的狭窄,如血管成形术)。此外,内膜平滑肌细胞增生可以包括血管系统以外的平滑肌增生(例如,胆管、支气管气道阻塞和肾间质纤维化患者的肾脏阻塞)。非癌性增生性疾病还包括皮肤细胞的过度增殖,例如,银屑病及其各种临床表现形式,瑞特氏综合征(reiter'ssyndrome)、毛发红糠疹(pityriasisrubrapilaris)和角化病的过度增生性变异(包括光化性角化病、老年性角化病和硬皮病)。
细胞系作为靶标
从细胞系获得的其他细胞可以用作靶细胞。这些细胞包括患有罕见疾病患者的具有可检测的细胞表型的细胞,优选人类或哺乳动物细胞。所述细胞可以是任何类型的,包括但不限于血细胞、免疫细胞、骨髓细胞、皮肤细胞、神经组织和肌肉细胞。
在本发明方法中有用的细胞系可以从任何方便的来源获得,包括美国典型培养物保藏中心(americantypeculturecollection,atcc)和国家癌症研究所(nationalcancerinstitute)。
例如,所述细胞/细胞系可能来源于患有溶酶体贮积病、肌营养不良、囊性纤维化、马凡氏综合征、镰状细胞贫血、侏儒症、苯丙酮尿症、神经纤维瘤病、亨廷顿病、成骨不全症、地中海贫血和血色素沉着症的受试者。
例如,所述细胞/细胞系可以来源于患有其他疾病的受试者,包括:血液、凝血、细胞增殖和失调、肿瘤(包括癌症)、炎症过程、免疫系统(包括自身免疫性疾病)、代谢、肝、肾、肌肉骨骼、神经、神经元和眼部组织的疾病和紊乱。示例性的血液和凝血疾病和紊乱包括:贫血,裸淋巴细胞综合征,出血障碍,因子h、因子h样1、因子v、因子viii、因子vii、因子x、因子xi、因子xii、因子xiiia、因子xiiib缺陷,凡科尼贫血,噬血细胞性淋巴组织细胞增多症,血友病a,血友病b,出血性疾病,白细胞缺乏症,镰状细胞贫血和地中海贫血。
免疫相关疾病和紊乱的实例包括:aids;自身免疫性淋巴增生综合征;联合免疫缺陷;hiv-1;hiv易感性或感染;免疫缺陷和严重联合免疫缺陷(scid)。本发明可治疗的自身免疫性疾病包括格雷夫氏病、类风湿关节炎、桥本甲状腺炎、白癜风、i型(早发)糖尿病、恶性贫血、多发性硬化、肾小球肾炎、系统性红斑狼疮e(sle,狼疮)和干燥综合征。其他自身免疫性疾病包括硬皮病、银屑病、强直性脊柱炎、重症肌无力、天疱疮、多肌炎、皮肌炎、葡萄膜炎、格林-巴利综合征、克罗恩病和溃疡性结肠炎(通常统称炎症性肠病(ibd))。
其他典型疾病包括:淀粉样神经病变;淀粉样变性病;囊性纤维化;溶酶体贮积疾病;肝腺瘤;肝衰竭;神经系统疾病;肝脂酶缺乏症;肝母细胞瘤、癌症或癌;髓样囊性肾病;苯丙酮酸尿;多囊肾;或肝脏疾病。
典型的肌肉骨骼疾病和紊乱包括:肌营养不良(如duchenne和becker肌营养不良)、骨质疏松症和肌萎缩。
典型的神经和神经元疾病和紊乱包括:als,阿尔茨海默病;自闭症;脆性x综合征、亨廷顿病、帕金森病、精神分裂症、分泌酶相关疾病、三核苷酸重复疾病、肯尼迪病、弗里德里希共济失调、马沙多-约瑟夫病、脊髓小脑共济失调、强直性肌营养不良、齿状核红核苍白球路易体萎缩症(drpla)。
典型眼病包括:年龄相关性黄斑变性、角膜混浊和营养不良、先天性扁平角膜、青光眼、利伯尔先天性黑内障和黄斑营养不良。
所述细胞/细胞系可以,例如,来自患有至少部分由蛋白质稳态缺陷介导的疾病的受试者,包括聚集性和错误折叠性蛋白稳态(proteostatic)疾病,特别是包括神经退行性疾病(例如,帕金森氏症、阿尔茨海默病和亨廷顿氏病)、溶酶体贮积疾病、糖尿病、气肿、癌症和囊性纤维化。
古细菌作为靶细胞
靶细胞可以是古细菌,例如选自以下门类中的古细菌:(a)泉古菌(crenarchaeota)、(b)广古菌(euryarchaeota)、(c)初古菌(korarchaeota)、(d)纳古菌(nanoarchaeota)和(e)奇古菌(thaumarchaeota),例如沃氏富盐菌(haloferaxvolcanii)和硫化叶菌(sulfolobusspp.)。
示例性的古细菌属包括喜酸菌属(acidianus)、酸叶菌属(acidilobus)、嗜酸球菌属(acidococcus)、aciduliprofundum、气火菌属(aeropyrum)、古丸菌属(archaeoglobus)、bacilloviridae、caldisphaera、暖枝菌属(caldivirga)、caldococus、餐古菌属(cenarchaeum)、除硫球菌属(desulfurococcus)、铁丸菌属(ferroglobus)、铁原体属(ferroplasma)、地球菌属(geogemma)、地丸菌属(geoglobus)、haladaptaus、盐碱球菌属(halalkalicoccus)、haloalcalophilium、盐盒菌属(haloarcula)、盐杆菌属(halobacterium)、盐棒菌属(halobaculum)、盐二型菌属(halobiforma)、盐球菌属(halococcus)、富盐菌属(haloferax)、盐几何菌属(halogeometricum)、盐微菌属(halomicrobium)、盐惰菌属(halopiger)、盐盘菌属(haloplanus)、盐方菌属(haloquadratum)、盐棍菌属(halorhabdus)、盐红菌属(halorubrum)、halosarcina、盐简菌属(halosimplex)、盐池栖菌属(halostagnicola)、盐陆生菌属(haloterrigena)、盐长命菌属(halovivax)、超热菌属(hyperthermus)、燃球菌属(ignicoccus)、燃球形菌属(ignisphaera)、生金球形菌属(metallosphaera)、甲烷微球菌属(methanimicrococcus)、甲烷杆菌属(methanobacterium)、甲烷短杆菌属(methanobrevibacter)、甲烷砾菌属(methanocalculus)、methantxaldococcus、甲烷胞菌属(methanocella)、甲烷类球菌属(methanococcoides)、甲烷球菌属(methanococcus)、甲烷粒菌属(methanocorpusculum)、甲烷囊菌属(methanoculleus)、甲烷泡菌属(methanofollis)、产甲烷菌属(methanogenium)、甲烷盐菌属(methanohalobium)、甲烷嗜盐菌属(methanohalophilus)、甲烷裂叶菌属(methanolacinia)、甲烷叶菌属(methanolobus)、甲烷食甲基菌属(methanomethylovorans)、甲烷微菌属(methanomicrobium)、甲烷盘菌属(methanoplanus)、甲烷火菌属(methanopyrus)、甲烷规则菌属(methanoregula)、甲烷鬃菌属(methanosaeta)、甲烷咸菌属(methanosalsum)、甲烷八叠球菌属(methanosarcina)、甲烷球形菌属(methanosphaera)、甲烷螺旋菌属(melthanospirillum)、甲烷热杆菌属(methanothermobacter)、甲烷热球菌属(methanothermococcus)、甲烷热菌属(methanothermus)、甲烷发菌属(methanothrix)、甲烷炎菌属(methanotorris)、纳古菌属(nanoarchaeum)、钠白菌属(natrialba)、钠线菌属(natrinema)、盐碱杆菌属(natronobacterium)、盐碱球菌属(natronococcus)、盐碱湖菌属(natronolimnobius)、盐碱单胞菌属(natronomonas)、盐碱红菌属(natronorubrum)、短小亚硝酸菌属(nitracopumilus)、古老球菌属(palaeococcus)、嗜苦菌属(picrophilus)、火棒菌属(pyrobaculum)、火球菌属(pyrococcus)、热网菌属(pyrodictium)、火叶菌属(pyrolobus)、葡萄热菌属(staphylothermus)、施铁特菌属(stetteria)、憎叶菌属(stygiolobus)、硫化叶菌属(sulfolobus)、厌硫球菌属(sulfophobococcus)、硫磺球形菌属(sulfurisphaera)、热分支菌属(thermocladium)、热球菌属(thermococcus)、热盘菌属(thermodiscus)、热丝菌属(thermofilum)、热原体属(thermoplasma)、热变形菌属(thermoproteus)、热球形菌属(thermosphaera)和火山鬃菌属(vulcanisaeta)。
示例性古细菌种类包括:敏捷气热菌(aeropyrumpernix)、闪烁古生球菌(archaeglobusfulgidus)、闪烁古生球菌(archaeoglobusfulgidus)、desulforcoccusspeciestok、嗜热自养甲烷杆菌(methanobacteriumthermoantorophicum)、詹氏甲烷球菌(methanococcusjannaschii)、需氧热棒菌(pyrobaculumaerophilum)、pyrobaculumcalidifontis、冰岛火棒菌(pyrobaculumislandicum)、深海热球菌(pyrococcusabyssi)、火球菌gb-d(pyrococcusgb-d)、pyrococcusglycovorans、掘越氏火球菌(pyrococcushorikoshii)、火球菌ge23(pyrococcusspp.ge23)、火球菌st700(pyrococcusspp.st700)、沃氏热球菌(pyrococcuswoesii)、隐蔽热网菌(pyrodictiumoccultum)、嗜酸热硫化叶菌(sulfolobusacidocaldarium)、sulfolobussolataricus、东工大硫化叶菌(sulfolobustokodalii)、thermococcusaggregans、thermococcusbarossii、速生热球菌(thermococcusceler)、thermococcusfumicolans、蛇发女怪热球菌(thermococcusgorgonarius)、热水高温球菌(thermococcushydrothermalis)、thermococcusonnurineusna1、太平洋热球菌(thermococcuspacificus)、thermococcusprofundus、thermococcussiculi、热球菌ge8(thermococcussppge8)、热球菌jdf-3(thermococcussppjdf-3)、热球菌ty(thermococcussppty)、thermococcusthioreducens、thermococcuszilligti、嗜酸热原体菌(thermoplasmaacidophilum)、火山嗜热支原体(thermoplasmavolcanium)、好客嗜酸两面菌(acidianushospitalis)、acidilobussacharovorans、aciduliprofundumboonei、敏捷气热菌(aeropyrumpernix)、闪烁古生球菌(archaeoglobusfulgidus)、archaeoglobusprofundus、嗜热硫酸盐还原菌(archaeoglobusveneficus)、caldivirgamaquilingensis、candidatuskorarchaeumcryptofilum、candidatusmethanoregulaboonei、candidatusnitrosoarchaeumlimnia、cenarchaeumsymbiosum、desulfurococcuskamchatkensis、ferroglobusplacidus、ferroplasmaacidarmanus、halalkalicoccusjeotgali、西班牙盐盒菌(haloarculahispanica)、holaoarculamarismortui、halobacteriumsalinarum、盐杆菌(halobacteriumspecies)、halobiformalucisalsi、沃氏嗜盐富饶菌(haloferaxvolvanii)、波多黎各盐几何形菌(halogeometricumborinquense)、向烟氏盐微菌(halomicrobiummukohataei)、halophilicarchaceonsp.dl31、halopigerxanaduensis、haloquadratumwalsbyi、halorhabdustiamatea、halorhabdusutahensis、湖渊盐红菌(halorubrumlacusprofundi)、haloterrigenaturkmenica、丁酸栖高温菌(hyperthermusbutylicus)、igniococcushospitalis、ignisphaeraaggregans、metallosphaeracuprina、勤奋生金球菌(metallosphaerasedula)、甲烷杆菌al-21(methanobacteriumsp.al-21)、甲烷杆菌swan-1(methanobacteriumsp.swan-1)、嗜热自养甲烷杆菌(methanobacteriumthermoautrophicum)、瘤胃甲烷短杆菌(methanobrevibacterruminantium)、史密斯甲烷杆菌(methanobrevibactersmithii)、methanocaldococcusfervens、methanocaldococcusinfernus、詹氏甲烷球菌(methanocaldococcusjannaschii)、甲烷暖球菌fs406-22(methanocaldococcussp.fs406-22)、methanocaldococcusvulcanius、methanocellaconradii、methanocellapaludicola、产甲烷胞菌水稻簇i(methanocellasp.riceclusteri(rc-i))、布氏拟甲烷球菌(methanococcoidesburtonii)、methanococcusaeolicus、海沼甲烷球菌(methanococcusmaripaludis)、万氏甲烷球菌(methanococcusvannielii)、沃氏甲烷球菌(methanococcusvoltae)、methanocorpusculumlabreantum、黑海甲烷袋状菌(methanoculleusmarisnigri)、methanohalobiumevestigatum、马氏甲烷嗜盐菌(methanohalophilusmahii)、methanoplanuspetrolearius、坎氏甲烷嗜高热菌(methanopyruskandleri)、联合甲烷鬃毛菌(methanosaetaconcilii)、竹节状甲烷鬃菌(methanosaetaharundinacea)、methanosaetathermophila、织里甲烷咸菌(methanosalsumzhilinae)、乙酸甲烷八叠球菌(methanosarcinaacetivorans)、巴氏甲烷八叠球菌(methanosarcinabarkeri)、马氏甲烷八叠球菌(methanosarcinamazei)、methanosphaerastadtmanae、methanosphaerulapalustris、亨氏甲烷螺菌(methanospiriullumhungatei)、mathanothermobactermarburgensis、冲绳甲烷球菌(methanothermococcusokinawensis)、炽热甲烷嗜热菌(methanothermusfervidus)、methanotorrisigneus、骑行纳古菌(nanoarchaeumequitans)、中亚无色需碱菌(natrialbaasiatica)、加蒂湖无色嗜盐菌(natrialbamagadii)、法老嗜盐碱单胞菌(natronomonaspharaonis)、海洋氨氧化古菌(nitrosopumilusmaritimus)、picrophilustorridus、需氧热棒菌(pyrobaculumaerophilum)、pyrobaculumarsenaticum、pyrobaculumcalidifontis、冰岛火棒菌(pyrobaculumislandicum)、热棒菌1860(pyrobaculumsp.1860)、深海热球菌(pyrococcusabyssi)、强烈炽热球菌(pyrococcusfuriosus)、pyrococcushorikoshii、火球菌na42(pyrococcussp.na42)、pyrococcusyayanosii、烟孔火叶菌(pyrolobusfumarii)、staphylothermushellenicus、staphylothermusmarinus、sulfolobusacidocaldirius、冰岛硫化叶菌(sulfolobusislandicus)、硫磺矿硫化叶菌(sulfolobussolfataricus)、sulfolobustokodaii、thermococcusbarophilus、thermococcusgammatolerans、thermococcuskodakaraensis、thermococcuslitoralis、thermococcusonnurineus、thermococcussibiricus、热球菌4557(thermococcussp.4557)、热球菌am4(thermococcussp.am4)、thermofilumpendens、嗜酸热原体菌(thermoplasmaacidophilum)、火山嗜热支原体(thermoplasmavolcanium)、thermoproteusneutrophilus、顽固热变形菌(thermoproteustenax)、thermoproteusuzoniensis、thermosphaeraaggregans、vulcanisaetadistributa和vulcanisaetamoutnovskia。
根据本发明,用作生产细胞的古细菌细胞的具体实例包括沃氏富盐菌(haloferaxvolcanii)和硫化叶菌(sulfolobusspp.)。
文库微区室(librarymicrocompartment)
当微区室化时,本发明的微珠可用于hts中。文库微区室可以采取任何形式,只要维持从微珠释放的tcs的空间关联,即必须实现微区室化,以使tcs及其从中释放的同源微珠被限制在空间距离内(spatialproximity)。
化学结构可以以足够高的浓度存在于文库微区室中,以允许进行基于细胞或表型的筛选,特别是基于均质细胞表型的分析。在某些实施方案中,加标签的化学结构可以以至少以下浓度存在于文库微区室中:0.1nm、0.5nm、1.0nm、5.0nm、10.0nm、15.0nm、20.0nm、30.0nm、50.0nm、75.0nm、0.1μm、0.5μm、1.0μm、5.0μm、10.0μm、15.0μm、20.0μm、30.0μm、50.0μm、75.0μm、100.0μm、200.0μm、300.0μm、500.0μm、1mm、2mm、5mm或者10mm。
在其他实施方案中,化学结构可以以至少以下浓度存在于文库微区室中:0.1pm、0.5pm、1.0pm、5.0pm、10.0pm、15.0pm、20.0pm、30.0pm、50.0pm、75.0pm、0.1nm、0.5nm、1.0nm、5.0nm、10.0nm、15.0nm、20.0nm、30.0nm、50.0nm、75.0nm、0.1μm、0.5μm、1.0μm、5.0μm、10.0μm、15.0μm、20.0μm、30.0μm、50.0μm、75.0μm、100.0μm、200.0μm、300.0μm、500.0μm、1mm、2mm、5mm或者10mm。
在其它实施方案中,化学结构可以以下浓度存在于文库微区室中:少于1μm;1-100μm;大于100μm;5-50μm或者10-20μm。
文库微区室包含本发明的微珠和水性溶剂。微区室还可包含其它组分,例如用于将化学结构从微珠释放到溶液中的裂解剂和/或所述靶测试系统的一个或多个其它组分。在靶是细胞的实施方案中,文库微区室还可包含一个或多个靶细胞。
本发明的方法涉及从其微珠释放每个化学结构的步骤,以产生多个游离的、无标签的化学结构(tcs)。所述tcs可以通过扩散便利地释放到文库微区室内,例如通过在溶剂化后扩散。
物理限制能够通过采用各种微区室获得,包括微滴、微粒和微泡。优选的是微滴,如下节段更详细地描述。
微滴
对于本领域技术人员来说,合适的材料以及根据本发明适于在微区室化中使用的制备和处理微滴的方法是公知常识的一部分,例如,在wo2010/009365、wo2006/040551、wo2006/040554、wo2004/002627、wo2004/091763、wo2005/021151、wo2006/096571、wo2007/089541、wo2007/081385和wo2008/063227中所描述的(在此通过引用合并其整体内容)。
微滴的大小将通过参照化学结构的性质和将被封装的测试系统进行选择。微滴可以基本上为球形,其直径为:(a)小于1μm;(b)小于10μm;(c)0.1-10μm;(d)10μm至500μm;(b)10μm至200μm;(c)10μm至150μm;(d)10μm至100μm;(e)10μm至50μm;或(f)约100μm。
优选地,微滴是大小均匀的,由此相对于同一个文库中其他液滴的直径,所述文库内任何液滴的直径变化小于5%、4%、3%、2%、1%或0.5%。在一些实施方案中,微滴是单分散的。然而,根据本发明也可以使用多分散微滴。
在单一w/o型乳液中,载液可以是任何与水不混溶的液体,例如油,任选地选自:(a)烃油;(b)氟碳油;(c)酯油;(d)硅油;(e)对水相生物组分溶解度低的油;(f)抑制微滴之间分子扩散的油;(g)疏水性和疏脂的油;(h)对于气体有良好溶解性的油;和/或(i)任何两种或更多种前述物质的组合。
因此,微滴可被包含在w/o乳液中,其中所述微滴构成水性分散相,以及载液构成连续的油相。
在其它实施方案中,微滴被包含在w/o/w双乳液中,并且载液可以是水性液体。在此类实施方案中,所述水性液体可以是磷酸盐缓冲液(pbs)。
微滴因此可以被包含在w/o/w双乳液中,其中所述微滴包括:(a)含水生长培养基(growthmedia)的内核,其被包封在作为分散相的外油壳中,以及(b)载液,所述载液作为连续水相。当然应该理解的是,o/w/o液滴对于筛选非生物实体特别有用。
微滴中使用的表面活性剂
在微滴被包含在乳液中的实施方案中,载液可以构成连续相,微滴构成分散相,并且在这种实施例中,乳液可进一步包含表面活性剂和任选的助表面活性剂。
表面活性剂和/或助表面活性剂可以位于分散相和连续相的界面处,并且当微滴被包括在w/o/w双乳液中时,表面活性剂和/或助表面活性剂可以位于水性核和油壳的界面处及油壳和外连续相的界面处。
范围广泛的合适的表面活性剂是可用的,并且本领域技术人员根据所选择的筛选参数能够选择合适的表面活性剂(和助表面活性剂,如果需要的话)。例如,以下文件中描述了合适的表面活性剂:bernath等(2004)analyticalbiochemistry325:151-157;holtze和weitz(2008)labchip8(10):1632-1639;和holtze等(2008)labchip8(10):1632-1639。在wo2010/009365和wo2008/021123(在此通过引用并入它们的内容)中描述了其它合适的表面活性剂,尤其包括含氟表面活性剂。
优选地,表面活性剂和/或助表面活性剂并入到w/o的界面中,因此,在采用单一w/o型乳液的实施方案中,表面活性剂和或助表面活性剂可以存在于水性生长培养基微滴和连续(例如,油)相的界面处。类似地,根据本发明双w/o/w型乳液用于共封装时,表面活性剂和或助表面活性剂可以存在于水性芯和不混溶的(例如油)壳的界面处以及油壳和连续水相之间的界面处这两种情况中的任一或两种界面处。
表面活性剂优选生物相容性的。例如,表面活性剂可以选择对筛选中使用的任何细胞都是无毒的。所选择的表面活性剂也可以对气体有良好的溶解性,这对任何被封装的细胞的生长和/或活力可能是必要的。
生物相容性可以通过任何合适的测试法测定,包括采用对照敏感性生化测试(例如,体外翻译)测试相容性的试验,该对照敏感性生化测试用作细胞水平生物相容性的替代。例如,使用荧光底物进行的编码酶β-半乳糖苷酶的质粒dna的体外翻译(ivt)(荧光素-二-β-d-吡喃半乳糖苷(fdg))可以作为生物相容性的指示剂,因为当被封装的dna、参与转录和翻译的分子和翻译的蛋白质没有吸附到液滴界面,并且蛋白质的高级结构保持完整时,形成荧光产物。
生物相容性的测定还可以通过:在存在表面活性剂的情况下,培养将用于测试的细胞,然后,用抗体或活细胞染料使细胞染色,以及相对于不存在表面活性剂的对照,测定细胞群的整体活力。
表面活性剂也可以防止生物分子吸附在微滴界面处。表面活性剂也可以起到分离单个微滴(和相应的微培养物)的作用。表面活性剂优选能稳定(即,防止合并)微滴。稳定性能可以通过例如相差显微术、光散射、聚焦光束反射测量、离心和/或流变学监控。
表面活性剂也可以形成测试系统的功能部分,并且可以例如用作区分或隔离测试法中存在的反应物和/或分析物和/或其它部分(例如,释放的标签)。例如,功能性表面活性剂亲水头部基团中的镍络合物能够将组氨酸标记的蛋白质集中在表面(参见,例如kreutz等人(2009)jamchemsoc.131(17):6042-6043)。这种官能化的表面活性剂也可以作为催化剂用于小分子合成(参见,例如theberge等人(2009)chem.commun.:6225-6227)。它们也可用于使细胞溶解(参见,例如clausell-tormos等人(2008)chembiol.15(5):427-37)。因此,本发明涵盖了使用这类官能化表面活性剂。
用于乳液共封装的油
应当理解的是,与不连续相不混溶的任何液体都可以用于形成据本发明使用的微滴乳液,所述不混溶的流体典型地是油。
优选地,选择对水相生物组分溶解度低的油。其它优选的功能性质包括:对于气体的可调节(例如,高或低)溶解度、抑制微滴之间的分子扩散的能力,和/或组合的疏水性和疏油性。油可以是烃油,例如轻质矿物油、氟碳油、硅油或酯油。两种或更多种上述油的混合物也是优选的。
在wo2010/009365、wo2006/040551、wo2006/040554、wo2004/002627、wo2004/091763、wo2005/021151、wo2006/096571、wo2007/089541、wo2007/081385和wo2008/063227中已描述了合适的油的实例(在此通过引用并入其内容)。
微滴乳化过程
范围广泛的不同的乳化方法是本领域技术人员所熟知的,其中的任何一个方法都可以用来产生本发明的微滴。
很多乳化技术包括大批量地混合两种液体,通常使用湍流以增强水滴破碎。这样的方法包括涡旋、超声处理、均质化或它们的组合。
在这些“自顶向下(top-down)”乳化的方法中,对单个液滴的形成几乎无法控制,并通常产生分布宽的微滴尺寸。可替代的“自底向上(bottomup)”的方法在单个微滴水平下操作,并且可能涉及使用微流体设备。例如,在微流体装置中,可以通过在t形连接处使油流和水流碰撞来形成乳液:产生的微滴大小取决于每个液流的流速而不同。
制备根据本发明使用的微滴的优选方法包括流动聚焦(如在例如anna等人(2003)appl.phys.lett.82(3):364-366中所描述的)。在此,连续相流体(聚焦或鞘流体)在分散相旁边或围绕分散相(被聚焦或核心流体),在两个流体都被挤出的孔附近产生液滴破裂。流动聚焦装置由使用连续聚焦液体供给进行加压的压力室组成。在内部,一个或多个聚焦流体通过毛细管进料管注入,其末端在连接压力室和外部环境的小孔前面打开。聚焦流体流将流体弯月面模压成尖头,通过孔产生流出腔室的稳定的微米或纳米射流;射流尺寸远小于出口孔。毛细不稳定性将稳定的射流打破为均匀的液滴或气泡。
进料管可以由两个或更多个同心针和注入的不同的导致复合液滴的不混溶液体或气体组成。流动聚焦确保了在射流破裂时极快地且可控地每秒产生数百万液滴。
其他微流体加工技术包括微注射(pico-injection),这是一种使用电场将试剂注入水滴中的技术(参见,例如eastburn等人(2013)picoinjectionenablesdigitaldetectionofrnawithdropletrt-pcr.plosone8(4):e62961.doi:10.1371/journal.pone.0062961)。微滴能够被融合以使两种试剂在一起,例如,主动地通过电熔(参见,例如tan和takeuchi(2006)labchip.6(6):757-63)或被动地(如由simon和lee(2012)“microdroplettechnology”,integratedanalyticalsystemspp23-50,10.1007/978-1-4614-3265-4_2所综述的)。
在所有的情况下,所选择的微滴形成过程的性能可以通过相差显微术、光散射、聚焦光束反射测量、离心和/或流变学监控。
荧光激活微滴分选
如本文所解释的,本发明的方法适合于高通量筛选,因为本发明的方法涉及微区室化微小体积溶剂中的离散的微滴的形式的微珠。这使得每个微滴都可以作为一个单独的培养容器来处理,允许使用已建立的微流体和/或细胞分选方法快速筛选大量单独的液体共培养物。
通过调整成熟的荧光激活细胞分选(facs)设备和方案,可以对微滴进行分选。这种技术已被称为荧光激活液滴分选(fads),并且,例如,在baret等人(2009)lapchip9:1850-1858中描述。可以通过使用荧光部分检测的任何变化都能够进行筛选。
如以上所解释的,固定在包含在微滴内的微珠上的报告部分的状态变化可能是荧光信号。这允许应用fads。多种荧光蛋白能够用作这个目的的标签,包括,例如,水晶果冻水母(aequoreavictoria)野生型绿色荧光蛋白(gfp)(chalfie等人1994,science263:802-805),以及修饰的gfp(heim等人1995,nature373:663-4;pct公布wo96/23810)。或者,dna2.0's
这种类型的报告基因的转录和翻译导致细胞中荧光蛋白的积累,因此使它们适合于fads。
可替代地,范围非常广泛的染料是可用的,所述染料在细胞内特定水平和条件下发出荧光。实例包括购自molecularprobes公司(thermoscientific)的那些。可替代地,可以用抗体检测细胞组分,这些组分可以用市售试剂盒用任意数量的荧光团染色。类似地,dna序列可以用荧光团标记引入细胞内,并通过在细胞内与互补的dna和rna序列杂交而附着,从而可以在称为荧光原位杂交(fish)的过程中直接检测基因表达。
任何可以应用于当前高通量筛选的标记过程都可以应用于fads,并检测为荧光信号相对于对照的变化。
编码化学文库(encodedchemicallibrary,ecl)
本发明的筛选方法应用于包含本发明的多个微区室的编码化学文库(ecl),其中每个微区室包含不同的化学结构。
优选地,ecl包含化学结构的n个克隆群,每个克隆群被限制在n个离散(discrete)的文库微区室。在此类实施方案中:(a)n>103;或者(b)n>104;或者(c)n>105;或者(d)n>106;或者(e)n>107;或者(f)n>108;或者(g)n>109;或者(h)n>1010;或者(i)n>1011;(j)n>1012;(k)n>1013;(i)n>1014;或者(m)n>1015。特别优选的是其中n=106至109的ecl。
基于序列的结构-活性分析
本发明的筛选方法包括通过确定报告部分的状态来筛选释放的微珠的步骤,由此可以在第一状态下通过对具有报告部分的微珠的标签进行解码来鉴定对靶具有活性的化学结构。
在所述标签包括核酸序列的情况下,所述解码步骤可以包括对核酸测序。在此类实施方案中,所述方法可以进一步包括比对多个不同的筛选的tcs的序列。这样的步骤之后,可以是对筛选出的tcs进行序列活性关系分析的步骤,其能够使被筛选出的文库成员分类成不同的化学类型。
范例
本发明现将参照具体实例加以说明。这些仅仅是范例,并且仅仅供说明:它们并非以任何方式限制所要求的独占范围或所本发明描述的范围。
附图说明
图1:使用自脱落连接子释放游离的化学结构的示意图。
图2:使用自脱落二肽连接子的分开与合并(split-and-pool)decl的示意图。
图3:使用val-cit-pab自脱落肽连接子释放游离的化学结构的示意图。
图4:显示底物a的减少以及产物b的增加的自脱落过程。
图5:珠粒上按比例的化合物负载,显示每个负载样品的明显不同种群。
图6:使用荧光报告部分在微滴中测量酶活性的示意图。
图7:使用荧光报告部分的微滴中fitc信号的相对强度。
实施例1:从珠-连接-兼容的连接子“无疤痕”释放小分子化合物
在40mmmops,ph7.5、150mmnacl中的10mg/mldmso和10mg/ml(11.9mm)nadph(sigmaaldrich)中配制测试底物a的原液。
将20μl底物a溶液与480μl40mmmopsph7.5150mmnacl缓冲液和500μlnadph溶液合并。加入3μl(29.6mg/ml)硝基还原酶(prozomix)引发反应,并在室温下孵育20分钟。将50μl反应溶液与200μl3:1acn:h2o+0.1%甲酸在lcms(agilenttechnologies,infinity1290)混合。
可以观察到底物a的明显减少和产物b的增加(参见图4),证明了自脱落过程,其中所需的“药物分子”在3分钟时释放出来。该结果表明有用的特异性连接子的可控酶裂解作用,导致小分子“无疤痕”释放。因此,该连接子可用于将小分子可释放地附着到珠粒上,以用于活性分析。
实施例2:在珠粒上准确按比例添加化合物
制备
使用1.99mgamf.hcl于50ml100mmmops、150mmnacl溶液,用4-(氨基甲基)荧光素盐酸盐(amf.hcl)溶液制成50ml的100μm原液。根据需要,使用100mmmopsph7.5、150mmnacl将溶液稀释至10μm和3μm。
将以下溶液放入5×50mlfalcon管中(每个1ml)进行负载测试。
在所有情况下,dmtmm(4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物,sigmaaldrich))用作偶联剂(假设珠粒上所有酸的10%)=4.77×10-7mol-每个falcon管中添加的4.8mm的原液100μl的体积:
falcon1-0.11%负载-所需amf5.247×10-9mol–所用的100μm(amf.hcl)(fisher)原液的体积=52.5μl;
falcon2-0.033%负载-所需amf1.574×10-9mol–所用的100μmamf.hcl原液的体积=15.7μl;
falcon3-0.011%负载-所需amf5.247×10-10mol-所用的10μmamf.hcl原液的体积=52.5μl;
falcon4-0.0033%负载-所需amf1.574×10-10mol–所用的3μmamf.hcl原液的体积=15.7μl;
falcon5-0.0011%负载-所需amf5.247×10-11mol–所用的10μmamf.hcl原液的体积=5.25μl.
过程
将3.9ml100mmmopsph7.5、150mmnacl加入到5×50mlfalcon管中。加入100μl新制的4.8mmdmtmm原液并充分混合。将1ml50μm的珠粒悬浮液(35珠粒/μl)添加到每个falcon管中,并混合60分钟。如上所示,在五个单独的falcon中分别添加50mlamf.hci。
将珠粒与dmtmm反应60分钟,然后倒入相应的amf50mlfalcon中,并在室温下反应过夜。
将珠粒以1000g制粒10分钟,并除去尽可能多的溶剂。加入15ml新制缓冲液,混合,并将洗涤步骤再重复2次。使用facs(mofloxdp,beckmanncoulter)对珠粒样品进行分析,使用488nm激光在exciteafm上对exciteafm进行激发,并使用540nm+/-20nm滤光片测量发射。分别对样品进行测量,并以对数标度进行合并(pool)。
如图5所示,对于每个相对负载样品,可以看到清晰的不同种群,显示出与相对amf.hci珠粒负载量cv’s<6.5%成正比的荧光增加。这意味着可以将不同量的化合物准确地加载到珠粒上,从而可以在活性测试中进行定量的剂量效应。
实施例3:微滴中的酶活性测量
将500μl的-cooh磁珠(bangbeadsinc)用10mmmopsph5.5、150mmnacl洗涤5×1ml,然后最终重悬浮于500μl的相同缓冲液中。
将寡核苷酸1和2各自重悬浮于无核酸酶的水中至100mm的浓度。
寡核苷酸1-/5ammc6/atgc/iflurot/acgtgcatccaagca/3iabkfq/(seqidno.1)
寡核苷酸2-tgcttggatgcacgtagcat(seqidno.2)
5amc6=c6胺连接子,iflurot是fitc融合的dt,3iabkdq是3'端的黑洞淬灭剂。下划线是bstci限制酶位点。
首先通过将相等比例的每种寡核苷酸在100μl的总体积中混合来对寡核苷酸1和2(用于珠粒连接)进行退火,该总体积由每个寡核苷酸40μl、10μl的10×t4dna连接酶缓冲液(50mmtris-hcl,10mmmgcl2和10mm二硫苏糖醇,1mmatp,ph7.5)和10μl无核酸酶的水组成。将混合物在热块中加热至95℃,持续10分钟,然后通过关闭该块将其缓慢冷却至室温(25℃),但将样品留在铝块中。
为了将双链寡核苷酸偶联至珠粒:将30mgedc溶解在400μl的10mmmesph5.5、150mmnacl中。用磁铁将珠粒拉下,然后重悬在含edc的缓冲液中。一旦重新悬浮,就加入寡核苷酸混合物,并在37℃下以颠倒混合的方式进行温育2小时。
将珠粒用1ml的10mmtris1mmedtaph7.5缓冲液洗涤5次,然后用1ml水洗涤2次。
建立具有抑制剂和不具有抑制剂的消化样品:每个反应分别在25μl,2.5μl的cutsmart缓冲液3.1(newenglandbiolabs,uk),17.5μl的珠粒的水溶液中进行,然后用抑制剂将其补足至25μl和/或依次添加水,最后在每个实例中添加酶。
样品1+5μl无核酸酶的水无酶
样品2+4μl无核酸酶的水和1μl的bstci
样品3+3.5μl无核酸酶的水,0.5μl0.5medta(抑制剂1)和1μlbstci
样品4+3.5μl无核酸酶的水,50mm亚精胺(抑制剂2,sigmaaldrich)和1μlbstci
立即将样品乳化;使用200μl矿物油(73%tegosoftdec,evonik,7%abilem90,evonik和10%轻质矿物油,sigmaaldrich)的涡流体进行乳化。该步骤也可以使用微滴产生装置进行。
将含有反应/含珠粒的微滴的乳化混合物在37℃下混合孵育30分钟,然后使乳液破碎。加入500μl100%的乙醇,然后将样品以14000g离心1分钟,使珠粒成丸。然后将它们用1ml的10mmtris、1mmedtaph7.5缓冲液洗涤3次,并重悬浮于500μl的相同缓冲液中。
然后通过在缓冲液中稀释20倍将珠粒稀释至大约100万/ml,并在cytoflex流式细胞仪(beckmancoulter)上运行。校准机器以检测小颗粒(即细菌)。激发波长为488nm,检测波长为525nm+/-40nm;检测到10,000个事件,并绘制平均荧光图。
结果如图7所示。样品2具有活性,显示出控制信号的3倍,表明保留在珠粒和微滴中的寡核苷酸裂解,而具有抑制剂和阴性对照(无酶)的样品相似,表明对裂解珠粒的酶的抑制作用可以使用微滴培养系统进行目标底物的检测并清楚地检测出目标底物。
应当理解,荧光/非荧光珠粒可以很容易地用facs分离。因此,初始负载的带有化合物的珠粒将允许编码鉴定特异性抑制剂化合物及其各自的微珠负载。
等同
上文的描述给出了本发明优选的实施方案的细节。可以预期的是,本领域技术人员在考虑这些描述时可以进行许多修改和变化。那些修改和变化应理解为包括在本文所附的权利要求中。
sequencelisting
<110>南纳治疗有限公司
<120>用于无标签编码化学文库筛选的微珠
<130>p40642wo
<150>gb1817321.1
<151>2018-10-24
<160>2
<170>patentinversion3.5
<210>1
<211>20
<212>dna
<213>artificialsequence
<220>
<223>testoligonucleotideforenzymeactivitymeasurementin
micro-droplets
<220>
<221>misc_feature
<222>(1)..(1)
<223>c6aminelinker,specifically5amc6
<220>
<221>misc_feature
<222>(5)..(5)
<223>dtfusedtofitc,specifically"ifluort"
<220>
<221>misc_feature
<222>(9)..(15)
<223>bstcirestrictionenzymesite
<220>
<221>misc_feature
<222>(20)..(20)
<223>blackholequencheronthe3'endoftheoligo,specifically
3iabkfq
<400>1
atgctacgtgcatccaagca20
<210>2
<211>20
<212>dna
<213>artificialsequence
<220>
<223>testoligonucleotideforenzymeactivitymeasurementin
micro-droplets
<400>2
tgcttggatgcacgtagcat20
- 还没有人留言评论。精彩留言会获得点赞!