基于三蝶烯衍生物单分子树脂的合成、正性光刻胶及其在光刻中的应用
本发明属于材料技术领域,具体涉及一类基于三蝶烯衍生物单分子树脂的合成、正性光刻胶及其在光刻中的应用。
背景技术:
光刻胶又称为光致抗蚀剂,是一类通过紫外光、准分子激光、电子束、离子束或x射线等光源的照射或辐射后,其溶解度发生变化的耐蚀刻薄膜材料,被广泛应用于集成电路和半导体分立器件的微细加工。光刻胶作为刻蚀阻挡层,可将所需的微细图形从掩膜版转移至待加工的基片上,实现图形的转移。为实现更高精度的图形转移,光刻胶的曝光波长由宽谱紫外向g线(436nm)→i线(365nm)→krf(248nm)→arf(193nm)→euv(13.5nm)的方向移动。目前的研究热点是极紫外光刻技术,它使用的曝光波长是13.5nm,可达到10nm以下的高分辨率光刻,而与之相对应的光刻胶也有更苛刻的要求。传统的光刻胶主体材料通常采用分子量5000~15000道尔顿的聚合物树脂,这类聚合物材料由于分子尺寸大,分子量分布较广以及分子链的缠绕等对曝光图案的边缘粗糙度或线宽粗糙度有很大影响,无法满足更为精细光刻的要求。
单分子树脂是一类相对分子质量较低的小分子化合物,呈现稳定的非结晶形态,具有玻璃化转变温度。相比于传统的聚合物光刻胶,这类分子具有单分散性和小的回旋半径,同时又具有聚合物的热稳定性和成膜性,是一类新的光刻胶主体材料。以三蝶烯为核心设计的单分子树脂可充分利用其结构上的优点,如高的玻璃化转变温度、好的热稳定性等。同时其刚性结构的空间立体几何骨架能有效抑制化合物分子的结晶性,更好的成膜。将该单分子树脂作为正性光刻胶的主体材料,可应用于光刻,尤其适用于高分辨率的极紫外和电子束光刻。
技术实现要素:
为改善上述问题,本发明提供一种如式(a)所示的三蝶烯衍生物:
其中,r1、r2、r3、r4、r5、r6相同或不同,彼此独立的选自氢或被1-5个ra取代的芳基、杂芳基;r1和r2组、r3和r4组、r5和r6组三组取代基中,每组至少有一个取代基为被1-5个ra取代的芳基、杂芳基;每一个ra相同或不同,彼此独立的选自氢、或-orb,所述rb为酸敏感基团,所述式(a)分子中的ra至少有一个为-orb。
所述酸敏感基团是指可在酸性条件下发生反应,从而从主体上脱去的基团。
在本发明的一个实施方案中,所述酸敏感基团rb为-cr1-o-r1、-co-o-r1、-ch2-co-o-r1、
其中r1相同或不同,彼此独立地选自未取代,或任选被一个、两个或更多个rs2取代的如下基团:c1-15烷基,c3-20环烷基;
m为1至4的任一整数,
rs2相同或不同,彼此独立地选自如下基团:no2、卤素、c1-15烷基、c1-15烷氧基、c3-20环烷基。
在一个实施方案中,所述r1为被c1-6烷基取代或未取代的如下基团:c1-6烷基,c3-8单环环烷基、c7-12桥环环烷基。
根据本发明的实施方案,r1、r2、r3、r4、r5、r6相同或不同,彼此独立的选自氢或被1个、2个、或3个ra取代的c6-10芳基、杂芳基;r1和r2组、r3和r4组、r5和r6组三组取代基中,每组至少有一个取代基为被1个、2个、或3个ra取代的c6-10芳基、杂芳基;每一个ra相同或不同,彼此独立的选自氢、或-orb,每个式(a)分子中的ra至少有一个为-orb;
根据本发明的实施方案,r1、r2、r3、r4、r5、r6相同或不同,彼此独立的选自氢或被1个、2个或3个ra取代的苯基;r1和r2组、r3和r4组、r5和r6组三组取代基中,每组至少有一个取代基为被1个、2个或3个ra取代的苯基;每一个ra相同或不同,彼此独立的选自氢或-orb,每个式(a)分子中的ra至少有一个为-orb;
根据本发明的实施方案,r1、r2、r3、r4、r5、r6相同或不同,彼此独立的选自氢或
优选地,所述基团rb选自如下基团:
其中,
优选地,本发明还提供如式(i)、式(ii)和式(iii)所示的化合物:
其中:ra1、ra2、ra3与上述ra定义相同;
根据本发明的实施方案,所述三蝶烯衍生物选自以下结构:
其中,boc表示
本发明还提供给式(a)所示三蝶烯衍生物的制备方法,包括以下步骤:
1)将化合物a与化合物b发生suzuki偶联反应得到化合物c,所述化合物b选自被1-5个ra'取代的芳基硼酸、芳基硼酸酯、杂芳基硼酸或杂芳基硼酸酯,如:3,4-二甲氧基苯硼酸、4-甲氧基苯硼酸、3,5-二甲氧基苯硼酸;ra'选自c1-12烷氧基或芳基c1-6烷氧基,如甲氧基、乙氧基、苄氧基;
其中,r1'、r2'、r3'、r4'、r5'、r6'相同或不同,彼此独立的选自氢、氟、氯、溴或碘,且不同时为氢;
r1”、r2”、r3”、r4”、r5”、r6”相同或不同,彼此独立的选自氢或被1-5个ra'取代的芳基或杂芳基,且不同时为氢;ra'选自c1-12烷氧基或芳基c1-6烷氧基,如甲氧基、乙氧基、苄氧基;
2).将化合物c与还原剂反应得到化合物d;
其中,r1”'、r2”'、r3”'、r4”'、r5”'、r6”'相同或不同,彼此独立的选自氢或被1个、2个或3个oh取代的芳基或杂芳基,且不同时为氢;
3).将化合物d与化合物rb-l反应,得到式(a)所示三蝶烯衍生物,其中l为离去基团或者l与rb构成含rb的酸酐,rb如上所述,
其中,r1、r2、r3、r4、r5、r6如上所定义。
根据本发明,所述化合物rb-l例如为二碳酸二叔丁酯、α-氯代醋酸金刚烷酯、氯乙酸降冰片酯。
所述还原剂例如选自三溴化硼或三氯化硼。
本发明还提供上述化合物(a)的用途,其用于光刻胶的主体材料。
本发明还提供了一种正性光刻胶组合物,包括如式(a)所示三蝶烯衍生物,光酸产生剂和光刻胶溶剂;
本发明中,式(a)所示三蝶烯衍生物的质量为所述正性光刻胶组合物总质量的1~10wt%,所述光酸产生剂的质量为0.01~1wt%,其余为光刻胶溶剂。
本发明中,所述光酸产生剂选自离子型或非离子型光酸产生剂,包括三氟甲磺酸三苯基硫鎓盐、全氟丁基磺酸三苯基硫鎓盐、对甲苯磺酸二(4-叔丁基苯基)碘鎓盐或n-羟基萘酰亚胺三氟甲磺酸盐中的一种或几种。
本发明中,所述光刻胶溶剂选自丙二醇单甲醚醋酸酯、乳酸乙酯、乙二醇单甲醚或环己酮中的一种或多种。
本发明还提供了一种正性光刻胶薄膜,包括本发明式(a)所示化合物。
本发明还提供了一种正性光刻胶薄膜的制备方法,包括将上述正性光刻胶组合物施加在基底上成膜得到。所述施加方式为旋涂法。
在一个实施方式中,所述基底可以为硅片。
本发明还提供如上所述正性光刻胶组合物、正性光刻胶薄膜在光刻中的应用。
根据本发明,所述光刻为248nm光刻、193nm光刻、极紫外光刻(euv)、纳米压印光刻或电子束光刻,特别的,所述正性光刻胶组合物、正性光刻胶涂层用于电子束光刻和极紫外光刻。
有益效果
本发明提供了一系列式(a)所示的基于三蝶烯衍生物的新型单分子树脂。其具有玻璃化温度高(大于100℃),热稳定性好的特点。所述单分子树脂本身具有确定的分子结构,分子尺寸小且单一,很好地满足光刻的要求。
本发明充分利用三蝶烯具有空间立体几何骨架的特点,能有效地抑制分子的结晶,因此,以该单分子树脂为主体材料的光刻胶易于成膜。
本发明所述单分子树脂合成过程简单,反应中间体和终产物通过重结晶或沉淀即可实现产物与体系的分离,适用于工业化生产。
术语定义与说明
除非另有定义,否则本文所有科技术语具有的含义与权利要求主题所属领域技术人员通常理解的含义相同。
术语“烷基”应理解为表示具有1~12个碳原子的直链或支链饱和一价烃基。例如,“c1-6烷基”表示具有1、2、3、4、5、或6个碳原子的直链和支链烷基。所述烷基是例如甲基、乙基、丙基、丁基、戊基、己基、异丙基、异丁基、仲丁基、叔丁基、异戊基、2-甲基丁基、1-甲基丁基、1-乙基丙基、1,2-二甲基丙基、新戊基、1,1-二甲基丙基、4-甲基戊基、3-甲基戊基、2-甲基戊基、1-甲基戊基、2-乙基丁基、1-乙基丁基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、2,3-二甲基丁基、1,3-二甲基丁基或1,2-二甲基丁基等或它们的异构体。
术语“烷氧基”应理解为-o-c1-12烷基,其中c1-12烷基具有上述定义。
术语“环烷基”应理解为表示饱和的一价单环、双环烃环或多环烃环(也称稠环烃环),其具有3-20个,优选3-10个碳原子。双环或多环环烷基包括并环环烷基、桥环烷基、螺环烷基;所述的并环是指由两个或两个以上环状结构彼此共用两个相邻的环原子(即共用一个键)所形成的稠环结构。所述的桥环是指有两个或两个以上环状结构彼此共用两个非相邻的环原子所形成的稠环结构。所述的螺环是指由两个或两个以上环状结构彼此共用一个环原子所形成的稠环结构。例如所述环烷基可以是c3-8单环环烷基,如环丙基、环丁基、环戊基、环己基、环庚基、环辛基,或者是c7-12并环环烷基,如十氢化萘环;也可以是c7-12桥环环烷基,如降冰片烷、金刚烷、二环[2,2,2]辛烷。
术语“芳基”应理解为具有6-20个碳原子,优选6~10个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环,优选“c6-8芳基”。术语“c6-8芳基”应理解为优选表示具有6、7或8个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“c6-14芳基”),特别是具有6个碳原子的环(“c6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“c9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“c10芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“c13芳基”),例如芴基,或者是具有14个碳原子的环(“c14芳基”),例如蒽基。当所述c6-10芳基被取代时,其可以为单取代或者多取代。并且,对其取代位点没有限制,例如可以为邻位、对位或间位取代。
术语“杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具有5~20个环原子且包含1-5个独立选自n、o和s的杂原子,例如“5-14元杂芳基”。术语“5-14元杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具有5、6、7、8、9、10、11、12、13或14个环原子,特别是5或6或9或10个碳原子,且其包含1-5个,优选1-3个独立选自n、o和s的杂原子,并且,另外在每一种情况下可为苯并稠合的。特别地,杂芳基选自噻吩基、呋喃基、吡咯基、噁唑基、噻唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、噁二唑基、三唑基、噻二唑基等以及它们的苯并衍生物,例如苯并呋喃基、苯并噻吩基、苯并噁唑基、苯并异噁唑基、苯并咪唑基、苯并三唑基、吲唑基、吲哚基、异吲哚基等;或吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基等,以及它们的苯并衍生物,例如喹啉基、喹唑啉基、异喹啉基等;或吖辛因基、吲嗪基、嘌呤基等以及它们的苯并衍生物;或噌啉基、酞嗪基、喹唑啉基、喹喔啉基、萘啶基、蝶啶基、咔唑基、吖啶基、吩嗪基、吩噻嗪基、吩噁嗪基等。
附图说明
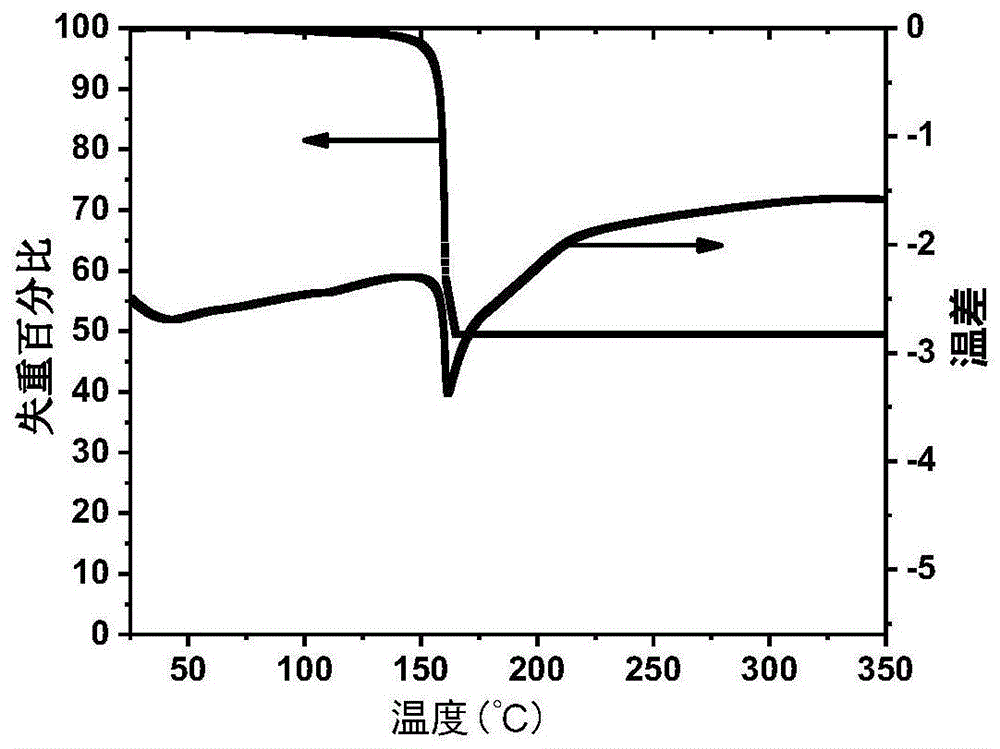
图1为本发明实施例3(2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯)的差示扫描量热曲线图和热失重曲线图。
图2为本发明实施例4(2,3,6,7,14,15-六-(4-醋酸金刚烷酯基苯基)三蝶烯)的差示扫描量热曲线图和热失重曲线图。
图3为本发明实施例3(2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯)主体材料正胶成膜euv光刻条纹的扫描电子显微镜(sem)图。
图4为本发明实施例4(2,3,6,7,14,15-六-(4-醋酸金刚烷酯基苯基)三蝶烯)主体材料正胶成膜电子束光刻条纹的扫描电子显微镜(sem)图。
具体实施方式
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
本发明中所述2,3,6,7,14,15-六溴三蝶烯、2,7,14-三溴三蝶烯和2,6,14-三溴三蝶烯可参考现有文献naturechemistry.2014,6,774-778和j.org.chem.2006,71,6626-6629制得。(这类溴代化合物商业可得,以下也提供它们的一些制备方法)
实施例1
2,3,6,7,14,15-六溴三蝶烯的制备
具体步骤:在500ml的反应瓶中加入三蝶烯(3.0g,11.80mmol),铁粉(0.085g,1.52mmol)和200ml三氯甲烷,反应体系在室温下搅拌均匀。再向反应体系中加入溴素(3.8ml,11.80g,73.84mmol),剧烈搅拌并回流。反应4h后,结束反应,将反应液冷却至室温,再经饱和亚硫酸钠溶液和水洗,有机层旋干得到黄色固体。黄色固体经丙酮重结晶可得到纯的无色晶体5g,产率60%。1hnmr(400mhz,cdcl3):δ(ppm)7.62(s,6h),5.23(s,2h)。
实施例2
2,6,14-三溴三蝶烯和2,7,14-三溴三蝶烯的制备(包含三蝶烯的硝化、还原及溴代)
1)三蝶烯的硝化
具体步骤:在250ml的反应瓶中加入三蝶烯(2.5g,10mmol)和100ml浓硝酸,反应体系升温至75℃,搅拌24h。反应结束时,待反应液冷却至室温,将反应液滴入1000ml水,收集沉淀。沉淀经柱层析分离可得到白色固体2,6,14-三硝基三蝶烯(2.5g,65%)和2,7,14-三硝基三蝶烯(0.82g,21%)。
2,6,14-三硝基三蝶烯1hnmr(300mhz,cdcl3):δ5.82(s,1h),5.84(s,1h),7.62-7.67(m,3h),8.03-8.07(m,3h),8.32-8.34(m,3h);
2,7,14-三硝基三蝶烯1hnmr(300mhz,cdcl3):δ5.80(s,1h),5.84(s,1h),7.62(d,j=8.2hz,3h),8.05(dd,j=8.2,2.2hz,3h),8.34(d,j=2.2hz,3h)。
2)2,6,14-三硝基三蝶烯的还原
具体步骤:在100ml的反应瓶中加入2,6,14-三硝基三蝶烯(1.0g,2.6mmol),1.5ml水合肼,raneyni(1.0g)和20ml四氢呋喃,反应体系升温至60℃,搅拌3h。反应结束时,待反应液冷却至室温,过滤,减压蒸馏除去溶剂,得到白色固体(760mg,99%)。1hnmr(300mhz,cdcl3):δ3.47(s,6h),5.01(s,1h),5.04(s,1h),6.21-6.26(m,3h),6.69-6.73(m,3h),7.04-7.07(m,3h)。
2,7,14-三硝基三蝶烯的还原同上,产率99%,1hnmr(300mhz,cdcl3):δ3.40(s,6h),4.97(s,1h),5.05(s,1h),6.23(dd,j=7.7,2.1hz,3h),6.70(d,j=7.7hz,3h),7.03(d,j=2.1hz,3h)。
3)2,6,14-三氨基三蝶烯的溴代
具体步骤:在100ml的反应瓶中加入2,6,14-三氨基三蝶烯(1.0g,3.6mmol),3ml浓溴酸和10ml水,反应体系置于冰水浴中,逐滴加入亚硝酸钠(0.8g,12.6mmol)的水溶液。反应体系搅拌20min后,缓缓将反应混合物加入至溴化亚铜(2.2g,15.0mmol)和氢溴酸(5ml)的回流溶液中。反应体系搅拌回流2h,冷却后用二氯甲烷萃取,水洗,无水硫酸钠干燥。减压蒸馏除去溶剂,粗品经乙醇重结晶得白色固体1.1g,产率67%。1hnmr(300mhz,cdcl3):δ5.26(s,1h),5.29(s,1h),7.12(dd,j=7.8,1.8hz,3h),7.20(d,j=7.8hz,3h),7.49(d,j=1.8hz,3h)。
2,7,14-三氨基三蝶烯的溴代同上,产率63%,1hnmr(300mhz,cdcl3):δ5.25(s,1h),5.31(s,1h),7.13(dd,j)7.8,1.8hz,3h),7.21(d,j=7.8hz,3h),7.49(d,j=1.8hz,3h)。
实施例3
2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯的制备方法,该方法包括以下步骤:
1)2,7,14-三-(3,4-二甲氧基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在高纯氮气保护下,向100mlschlenk反应瓶中加入2,7,14-三溴三蝶烯(975.6mg,2mmol,1.0eq),四三苯基膦钯(230mg,0.2mmol,0.1eq),3,4-二甲氧基苯硼酸(1.64g,9mmol,4.5eq)和重蒸的甲苯30ml,搅拌溶解后向反应瓶中加入乙醇溶液6ml和2mna2co3水溶液3ml,反应液升温至60~100℃,回流12h,冷却至室温,用二氯甲烷/水萃取,合并有机层,有机层经饱和食盐水洗涤一次,再用无水硫酸钠进行干燥。抽滤,将滤液减压蒸馏,得到灰色固体。用5ml二氯甲烷将固体溶解,在100ml乙醇中沉淀,过滤,真空烘箱干燥,得到白色固体1.2g,产率91%。1hnmr(400mhz,cdcl3):δ(ppm)6.97-6.99(d,3h,benzene),6.80-6.82(d,3h,benzene),7.08(s,3h,benzene),7.32-7.36(d,3h,benzene),7.41-7.45(d,3h,benzene),7.50(s,3h,benzene),5.82(s,2h,-ch),3.93-3.94(d,18h,-och3)。ms(maldi-tof):m/z=662.3,计算值(c44h38o6)m/z=662.4(m+)。
2)2,7,14-三-(3,4-二羟基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在100ml的反应瓶中加入2,7,14-三-(3,4-二甲氧基苯基)三蝶烯(662mg,1mmol,1.0eq)和二氯甲烷30ml,氮气氛围下溶解,在低温-78℃下,用注射器向反应液中滴加三溴化硼的二氯甲烷溶液(1.0ml,10.0mmol,10.0eq),反应体系置于-78℃下反应1h后逐渐升至室温,继续反应12h,向反应体系中缓慢加入10ml冰水淬灭反应。反应液经水洗至中性,再用饱和食盐水洗涤一次,无水硫酸钠干燥。抽滤,将滤液减压蒸馏,得到白色固体540mg,产率93%。1hnmr(400mhz,cdcl3):δ(ppm)6.95-6.99(d,3h,benzene),6.83-6.87(d,3h,benzene),7.21(s,3h,benzene),7.32-7.36(d,3h,benzene),7.41-7.45(d,3h,benzene),7.50(s,3h,benzene),5.86(s,2h,-ch),5.42(s,6h,-oh)。ms(maldi-tof):m/z=578.1,计算值(c38h26o6)m/z=578.0(m+)。
3)2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯(化合物(1))的制备,合成路线式如下:
反应式中,boc表示
具体步骤:在100ml的反应瓶中加入2,7,14-三-(3,4-二羟基苯基)三蝶烯(578.1mg,1mmol,1.0eq),boc酸酐(二碳酸二叔丁酯)(2.0g,9mmol,9.0eq)和干燥四氢呋喃20ml,氮气氛围下搅拌溶解完,向溶液中加入催化量dmap(12.2mg,0.1mmol,0.1eq)引发反应,室温下搅拌24h。反应液用二氯甲烷/水萃取,有机相先用水洗涤两次,再用饱和食盐水洗涤一次,无水硫酸钠干燥,减压除去溶剂,得到半固体状物。将半固体状物溶于4ml的四氢呋喃中,滴加至100ml乙醇中沉淀,得到白色固体0.95g,产率80%。1hnmr(400mhz,cdcl3):δ(ppm)6.97-6.99(d,3h,benzene),6.80-6.82(d,3h,benzene),7.08(s,3h,benzene),7.32-7.36(d,3h,benzene),7.41-7.45(d,3h,benzene),7.50(s,3h,benzene),5.82(s,2h,-ch),1.55(d,54h,-o(ch3)3)。ms(maldi-tof):m/z=1179.3,计算值(c68h74o18)m/z=1179.2(m+)。
实施例4
化合物(2)的制备
所述制备方法包括以下步骤:
1)2,3,6,7,14,15-六-(4-甲氧基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在高纯氮气保护下,向100mlschlenk反应瓶中加入2,3,6,7,14,15-六溴三蝶烯(728mg,1mmol,1.0eq),四三苯基膦钯(115mg,0.1mmol,0.1eq),4-甲氧基苯硼酸(1.4g,9mmol,9.0eq)和重蒸的甲苯20ml,搅拌溶解后向反应瓶中加入乙醇溶液5ml和2mna2co3水溶液2ml,反应液升温至60~100℃,回流12h,冷却至室温,用二氯甲烷/水萃取,合并有机层,有机层经饱和食盐水洗涤一次,再用无水硫酸钠进行干燥。抽滤,将滤液减压蒸馏,得到灰色固体。用4ml二氯甲烷将固体溶解,在100ml乙醇中沉淀,过滤,真空烘箱干燥,得到白色固体803mg,产率90%。1hnmr(400mhz,cdcl3):δ(ppm)7.48(s,6h,benzene),7.01-7.03(d,12h,benzene),6.74-6.76(d,12h,benzene),5.59(s,2h,-ch),3.77(s,18h,-och3)。ms(maldi-tof):m/z=891.1,计算值(c62h50o6)m/z=891.2(m+)。
2)2,3,6,7,14,15-六-(4-羟基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在100ml的反应瓶中加入2,3,6,7,14,15-六-(4-甲氧基苯基)三蝶烯(890mg,1mmol,1.0eq)和二氯甲烷40ml,氮气氛围下溶解,在低温-78℃下,用注射器向反应液中滴加三溴化硼的二氯甲烷溶液(2.0ml,10.0mmol,10.0eq),反应体系置于-78℃下反应1h后逐渐升至室温,继续反应12h,向反应体系中缓慢加入15ml冰水淬灭反应,有白色固体析出。过滤得白色固体,溶于乙酸乙酯,水洗至中性,再用饱和食盐水洗涤一次,无水硫酸钠干燥。抽滤,将滤液减压蒸馏,得到白色固体750mg,产率93%。1hnmr(400mhz,cdcl3):δ(ppm)7.49(s,6h,benzene),7.05-7.08(d,12h,benzene),6.79-6.78(d,12h,benzene),5.61(s,2h,-ch),5.46(s,6h,-oh)。ms(maldi-tof):m/z=806.3,计算值(c56h38o6)m/z=806.5(m+)。
3)2,3,6,7,14,15-六-(4-醋酸金刚烷酯基苯基)三蝶烯的制备,合成路线式如下:
反应式中,ad表示
具体步骤:在100ml的反应瓶中加入2,3,6,7,14,15-六-(4-羟基苯基)三蝶烯(806mg,1mmol,1.0eq),四丁基溴化铵(800mg,2.4mmol,2.4eq),碳酸钾(5.6g,40mmol)和n-甲基吡咯烷酮(nmp,50ml),常温下搅拌2h,向反应液中慢慢滴加α-氯代醋酸金刚烷酯(2.9g,12mmol,12eq)的nmp(20ml)溶液,升温至60℃反应48h。反应完全后,冷却至室温,反应液用乙酸乙酯/水萃取,有机相分别用3wt%的草酸溶液和水洗涤一次,合并有机层,无水硫酸钠干燥,减压除去溶剂,用乙酸乙酯/正己烷混合溶剂重结晶,得到白色固体1.6g,产率78%。1hnmr(400mhz,cdcl3):δ(ppm)7.48(s,6h,benzene),7.01-7.03(d,12h,benzene),6.74-6.76(d,12h,benzene),5.59(s,2h,-ch),1.67-1.70(m,114h)。ms(maldi-tof):m/z=2044.1,计算值(c134h146o18)m/z=2044.3(m+)。
实施例5
化合物(3)的制备
所述制备方法包括以下步骤:
1)2,6,14-三-(3,5-二甲氧基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在高纯氮气保护下,向100mlschlenk反应瓶中加入2,6,14-三溴三蝶烯(975.6mg,2mmol,1.0eq),四三苯基膦钯(230mg,0.2mmol,0.1eq),3,5-二甲氧基苯硼酸(1.64g,9mmol,4.5eq)和重蒸的甲苯30ml,搅拌溶解后向反应瓶中加入乙醇溶液6ml和2mna2co3水溶液3ml,反应液升温至60~100℃,回流12h,冷却至室温,用二氯甲烷/水萃取,合并有机层,有机层经饱和食盐水洗涤一次,再用无水硫酸钠进行干燥。抽滤,将滤液减压蒸馏,得到灰色固体。用4ml二氯甲烷将固体溶解,在100ml乙醇中沉淀,过滤,真空烘箱干燥,得到白色固体1.3g,产率98%。1hnmr(400mhz,cdcl3):δ(ppm)6.96(s,3h,benzene),7.14(s,6h,benzene),7.20(s,3h,benzene),7.32-7.36(d,3h,benzene),7.45(d,3h,benzene),5.82(s,2h,-ch),3.93-3.94(s,18h,-och3)。ms(maldi-tof):m/z=662.3,计算值(c44h38o6)m/z=662.4(m+)。
2)2,6,14-三-(3,5-二羟基苯基)三蝶烯的制备,合成路线式如下:
具体步骤:在100ml的反应瓶中加入2,6,14-三-(3,5-二甲氧基苯基)三蝶烯(662mg,1mmol,1.0eq)和二氯甲烷30ml,氮气氛围下溶解,在低温-78℃下,用注射器向反应液中滴加三溴化硼的二氯甲烷溶液(1.0ml,10.0mmol,10.0eq),反应体系置于-78℃下反应1h后逐渐升至室温,继续反应12h,向反应体系中缓慢加入10ml冰水淬灭反应。反应液经水洗至中性,再用饱和食盐水洗涤一次,无水硫酸钠干燥。抽滤,将滤液减压蒸馏,得到白色固体540mg,产率93%。1hnmr(400mhz,cdcl3):δ(ppm)6.97(s,3h,benzene),7.16(s,6h,benzene),7.22(s,3h,benzene),7.34-7.35(d,3h,benzene),7.45(d,3h,benzene),5.85(s,2h,-ch),3.93-3.94(s,6h,-oh)。ms(maldi-tof):m/z=578.1,计算值(c38h26o6)m/z=578.0(m+)。
3)2,6,14-三-(3,5-二醋酸降冰片酯基苯基)三蝶烯的制备,合成路线式如下:
反应式中,bh表示
具体步骤:在100ml的反应瓶中加入2,6,14-三-(3,5-二羟基苯基)三蝶烯(578.1mg,1mmol,1.0eq),四丁基溴化铵(800mg,2.4mmol,2.4eq),碳酸钾(5.6g,40mmol)和n-甲基吡咯烷酮(nmp,50ml),常温下搅拌2h,向反应液中慢慢滴加氯乙酸降冰片酯(2.9g,12mmol,12eq)的nmp(20ml)溶液,升温至60℃反应48h。反应完全后,冷却至室温,反应液用乙酸乙酯/水萃取,有机相分别用3wt%的草酸溶液和水洗涤一次,合并有机层,无水硫酸钠干燥,减压除去溶剂,用乙酸乙酯/正己烷混合溶剂重结晶,得到白色固体1.1g,产率70%。1hnmr(400mhz,cdcl3):δ(ppm)6.95(s,3h,benzene),7.12(s,6h,benzene),7.21(s,3h,benzene),7.32-7.36(d,3h,benzene),7.45(d,3h,benzene),5.83(s,2h,-ch),1.63-1.70(m,90h,-och3)。ms(maldi-tof):m/z=1576.2,计算值(c98h110o18)m/z=1576.4(m+)。
实施例6
实施例3制备得到的2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯(化合物(1))的热性质,通过差式扫描量热曲线和热重分析见图1,结果显示其玻璃化温度达到了150℃以上,具有很好的热稳定性。
实施例7
一种正性光刻胶组合物,包括实施例3制备的2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯、丙二醇单甲醚醋酸酯(pgmea)和三氟甲磺酸三苯基硫鎓盐。具体方法如下:将实施例3制备的2,7,14-三-(3,4-二叔丁基碳酸酯基苯基)三蝶烯溶于丙二醇单甲醚醋酸酯(pgmea)中,制得质量浓度5%的溶液,并加入0.1wt%的三氟甲磺酸三苯基硫鎓盐为光酸产生剂,用孔径0.22μm的微孔过滤器过滤,得到旋涂液,在经过酸碱处理的硅基底上进行旋涂制膜,在100℃下烘烤3分钟,将制备得到的薄膜在上海光源干涉光刻线站(bl08u1b)上进行极紫外曝光实验,曝光周期为140nm,得到非常均匀的光刻条纹,如图2所示,光刻条纹的分辨率为44.1nm。
实施例8
一种正性光刻胶组合物,包括实施例4制备的化合物(2)、环己酮和全氟丁基磺酸三苯基硫鎓盐。具体方法如下:将实施例4制备的化合物(2)溶于环己酮中,制得质量浓度10%的溶液,并加入0.1wt%的全氟丁基磺酸三苯基硫鎓盐为光酸产生剂,用孔径0.22μm的微孔过滤器过滤,得到旋涂液,在经过酸碱处理的硅基底上进行旋涂制膜,在100℃下烘烤3分钟,将制备得到的薄膜进行电子束曝光实验,曝光周期为150nm,得到非常均匀的光刻条纹,如图4所示,光刻条纹的分辨率为59.5nm。
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!