用于检测piRNA与mRNA结合的可视化方法及其应用与流程
本发明涉及分子生物学技术领域,尤其是涉及一种用于检测pirna与mrna结合的可视化方法及其应用。
背景技术:
pirna(piwi-interactingrna)是从哺乳动物生殖细胞中分离得到的一类长度约为27-32nt的小rna,并且这种小rna与piwi蛋白家族成员相结合才能发挥它的调控作用。目前,越来越多的文献表明pirna在细胞的生长发育中可以调控mrna的稳定性、蛋白质的合成、染色质组织和基因组的结构。研究表明,pirna主要存在于哺乳动物的生殖细胞和干细胞中,通过与piwi亚家族蛋白结合形成pirna沉默复合物(pirna-inducedsilencingcomplex,pirisc)来调控基因沉默途径。近几年来,pirna在体细胞中的功能也逐渐有文献报道。pirna的发现为pirna的研究开辟了一个新领域,被science评为2006年十大科技进展之一。因此,pirna的研究不仅可以丰富小分子rna的研究内容,同时,也有利于进一步了解生物配子发生的分子调控及其机理,具有十分重要的理论价值和应用前景。
目前研究pirna调控基因沉默的功能主要使用的是双荧光素酶报告基因实验,其方法是通过构建pirna调控mrna结合区域的双荧光素酶报告基因载体,与pirna模拟物共转染进入细胞,36-72小时后,裂解细胞取细胞上清液检测荧光素酶的表达情况来判断pirna与mrna的结合。荧光素酶报告基因实验操作繁琐,耗时长,所需试剂种类多成本高。因此,改进检测pirna与mrna是否能够结合的方法是必要的。
有鉴于此,特提出本发明。
技术实现要素:
本发明的目的在于提供一种用于检测pirna与mrna结合的可视化方法,该方法具有操作简便、时间短、灵敏度高和可视化等优点。
为解决上述技术问题,本发明特采用如下技术方案:
根据本发明的一个方面,本发明提供了一种用于检测pirna与mrna结合的可视化方法,包括:
(a)提供探针,所述探针为单链rna,所述探针包括pirna探针和mrna探针;
所述pirna探针的核苷酸序列为待检测的pirna的核苷酸序列;
所述mrna探针的核苷酸序列为所述待检测的pirna和mrna的预测的结合区域的核苷酸序列;
(b)配置反应体系,所述反应体系包括第一反应体系、第二反应体系和第三反应体系;
所述第一反应体系中探针为标记的所述pirna探针;
所述第二反应体系中探针为标记的所述mrna探针;
所述第三反应体系中探针为标记的所述pirna探针和标记的所述mrna探针;
(c)各反应体系进行结合反应,反应后各体系的反应产物经电泳后观察条带,若第三反应体系出现相比于第一反应体系和第二反应体系滞后的条带,则所述待检测的pirna与mrna结合。
优选地,所述探针还包括阴性对照探针,所述阴性对照探针与所述pirna探针和所述mrna探针均不结合;所述反应体系还包括第四反应体系;
所述第四反应体系中探针为标记的所述pirna探针、标记的所述mrna探针和未标记的阴性对照探针;未标记的阴性对照探针的摩尔浓度为标记的所述mrna探针的20~100倍;
若第四反应体系出现和第三反应体系相同的滞后的条带,则所述待检测的pirna与mrna结合;
优选地,未标记的阴性对照探针的摩尔浓度为标记的所述mrna探针的40~60倍,优选为50倍。
优选地,所述反应体系还包括第五反应体系,所述第五反应体系中探针为标记的所述pirna探针、标记的所述mrna探针和未标记的所述pirna探针,未标记的所述pirna探针的摩尔浓度为标记的所述mrna探针的20~100倍;
若第五反应体系无游离的标记的所述mrna探针条带,则所述待检测的pirna与mrna结合;
优选地,未标记的所述pirna探针的摩尔浓度为标记的所述mrna探针的40~60倍,优选为50倍。
优选地,所述检测pirna与mrna结合包括检测has-pir-016659与hnf1a结合;和/或,检测has-pir-020391与znf10结合。
优选地,当所述反应体系中同时含有标记的所述pirna探针和标记的所述mrna探针时,标记的所述pirna探针和标记的所述mrna探针的摩尔比为(0.8~1.2):(0.8~1.2),优选为1:1。
优选地,所述标记包括荧光染料标记;
优选地,荧光染料的发射波长为650~850nm;
优选地,用于标记所述pirna探针的荧光染料和用于标记所述mrna探针的荧光染料发射波长不相同;
优选地,发射波长为650~850nm荧光染料包括irdye800、cy5、cy5.5、thiadicarbocyanine、irdye680lt、alexa
优选地,标记pirna探针的荧光染料包括irdye荧光染料,优选包括irdye800荧光染料;
优选地,标记mrna探针的荧光染料包括cy荧光染料,优选包括cy5.5荧光染料;
优选地,所述荧光染料标记于探针的5’端或3’端。
优选地,所述反应体系包括depc-h2o、bindingbuffer和探针;
优选地,反应体系中带有标记的探针浓度为30~50nm,优选为40nm;
优选地,所述bindingbuffer包含如下组分:ph为7.2-7.4的hepesbuffer、甘油、kcl和mgcl2;
优选地,所述bindingbuffer中各组分在反应体系中的终浓度为:ph为7.2-7.4的hepesbuffer8~12mm、甘油4~6%(w/w)、kcl0.15~0.25m和mgcl20.5~0.15m;
优选地,所述bindingbuffer中各组分在反应体系中的终浓度为:ph为7.2-7.4的hepesbuffer10mm、甘油5%(w/w)、kcl0.2m和mgcl20.1m。
优选地,先将探针使用depc-h2o稀释,再添加至反应体系中;
优选地,将探针使用depc-h2o稀释后,于94-96℃加热1.5-2.5min,随后放冰上冷却1.8-2.5min后添加于反应体系中;
优选地,所述结合反应的反应条件为24-26℃保温18-22min。
优选地,所述电泳包括非变性聚丙烯酰胺凝胶电泳。
根据本发明的另一个方面,本发明还提供了所述用于检测pirna与mrna结合的可视化方法在研究pirna对基因调控作用中的应用。
与现有技术相比,本发明具有如下有益效果:
目前检测pirna与mrna结合的方法主要有双荧光素酶报告基因的方法,但是该技术操作比较繁琐,所需试剂种类多,耗时长,本发明通过标记物标记pirna探针和mrna探针,混合反应后电泳,然后观察电泳迁移率是否发生改变,若形成较pirna探针或者mrna探针游离带滞后的迁移带,则说明有结合作用。本发明提供的方法拓展了传统的凝胶迁移电泳法的应用范围,用于体外检测rna与rna相互作用,而且操作过程简单,时间短,信号不容易损失,可快速获得测试结果,还具有灵敏度高和可视化等优点。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为本发明实施例1中has-pir-016659与hnf1a结合的结果图;
图2为本发明实施例2中has-pir-020391与znf10结合的结果图。
具体实施方式
下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
根据本发明的一个方面,本发明提供了一种用于检测pirna与mrna结合的可视化方法,包括:
(a)提供探针,所述探针为单链rna,所述探针包括pirna探针和mrna探针;所述pirna探针的核苷酸序列为待检测的pirna的核苷酸序列,用来模拟pirna;所述mrna探针的核苷酸序列为预测的所述待检测的pirna和mrna的结合区域的核苷酸序列,用来模拟真实的mrna,以检测预测的mrna的结合区域是否能够和pirna发生结合,以进一步判断实际的mrna能否和pirna结合。预测pirna和mrna的结合区域可采用本领域可接受的方法和软件预测,本发明对此不作限制。
(b)配置反应体系,所述反应体系包括第一反应体系、第二反应体系和第三反应体系;所述第一反应体系中探针为标记的所述pirna探针;所述第二反应体系中探针为标记的所述mrna探针;所述第三反应体系中探针为标记的所述pirna探针和标记的所述mrna探针。第一反应体系和第二反应体系用于在电泳时作为未结合单链rna的游离探针的参照条带,第三反应体系用于检测pirna探针和mrna探针是否发生结合。其中“标记”指的是在电泳后使条带可以被观察到的标记,本领域中具有该作用的标记均可用于标记本发明中的探针,例如以荧光染料作为标记物标记探针,电泳后可以通过荧光染料特定的发射波长来观察条带的位置,从而实现实验结果的可视化。pirna探针和mrna探针可以采用相同的标记物标记,也可以采用不同的标记物标记,优选采用不同的标记物标记,以便观察和区分凝胶中各游离的探针条带和杂交后的条带。
(c)将各反应体系进行结合反应,反应后各体系的反应产物经电泳后观察条带。如果反应体系中的探针有结合,在电泳时相比于未发生结合的游离的探针电泳迁移率降低。换言之,就是会相比第一反应体系中游离的pirna探针或者第二反应体系中游离的mrna探针的泳动速率慢,第三反应体系会形成一条滞后的荧光迁移带,即更接近于样品电泳初始位置的条带。因此当第三反应体系中出现相比于第一反应体系和第二反应体系滞后的条带,则说明所述待检测的pirna能够与预测的mrna结合区域结合。本发明所述的“结合反应”为反应体系经过结合反应的过程,但并不代表着反应体系中一定会发生探针之间的结合。可以理解的是,第一反应体系和第二反应体系因为只含有一种探针,理论上不发生探针之间的结合反应,但是为了使只含有一种探针的反应体系和含有多种探针的反应体系经过相同的反应过程,以保证实验过程中各反应体系的处理条件相同,因此只含有一种探针的反应体系,例如第一反应体系和第二反应体系,也经过所述结合反应。
本发明所述的观察条带,可以采用肉眼观察或者采用本领域常规的用于检测电泳后条带的装置观察。例如当探针上的标记物可直接被肉眼观察,则电泳后肉眼观察即可。或者例如当探针上的标记物需要检测设备才能观察,比如标记物为荧光染料,则采用能够接受荧光染料相应波长的仪器进行成像和观测。
本发明提供的通过标记物标记pirna探针和mrna探针,混合反应后经电泳,观察电泳迁移率是否发生改变,若形成较pirna探针或者mrna探针游离带滞后的迁移带,则说明有结合作用。本发明提供的方法具有操作简便、时间短、灵敏度高和可视化等优点,可快速获得测试结果。
在一些优选的实施方式中,为了说明第三反应体系中pirna探针和mrna探针的结合是具有特异性的,排除由于其他原因导致的两种探针的结合,还设置第四反应体系。第四反应体系中除去含有标记的pirna探针和标记的mrna探针,还含有未标记的阴性对照探针。阴性对照探针是与pirna探针和mrna探针均不发生结合的探针,且第四反应体系中未标记的阴性对照探针的摩尔浓度为标记的mrna探针的20~100倍。例如可以为但不限于为20、30、40、50、60、70、80、90或100倍,优选为40~60倍,更优选为50倍。当加入大量阴性对照探针后,第四反应体系中的条带和第三反应体系中的条带位置相同,则说明滞后的条带是由于两个探针的特异性的结合造成的,而非由于其他原因导致的rna的结合。
在一些优选的实施方式中,反应体系还设置第五反应体系,第五反应体系相比于第三反应体系还加入了未标记的pirna探针,且未标记的pirna探针的摩尔浓度为标记的mrna探针的20~100倍,例如可以为但不限于为20、30、40、50、60、70、80、90或100倍,优选为40~60倍,更优选为50倍。其作用是用于竞争结合mrna探针,当pirna探针和mrna探针之间发生特异性结合,则高浓度的pirna探针能够与体系中的mrna探针充分结合,电泳后第五反应体系不会出现游离的标记的mrna探针条带。
需要说明的是,本发明第一反应体系~第五反应体系中的“第一”“第二”“第三”“第四”和“第五”只是对各反应体系的区分,不应理解为对先后顺序或重要程度的排序。
在一些优选的实施方式中,当上述反应体系中同时含有标记的pirna探针和标记的mrna探针时,标记的pirna探针和标记的mrna探针的摩尔比为(0.8~1.2):(0.8~1.2),例如可以为但不限于为0.8:1.2、0.8:1、1:1、1:0.8、1.2:0.8、1:1.2或1.2:1等,优选为1:1。
在一些优选的实施方式中,标记探针的标记物优选荧光染料标记,荧光染料标记可有效的防止信号的损失。荧光染料优选包括发射波长在650-850nm之间的荧光染料。换言之,发射波长在650-850nm之间的荧光染料均可以用于标记pirna探针和mrna探针。其中,发射波长在650-850nm之间的荧光染料包括但不限于irdye800、cy5、cy5.5、thiadicarbocyanine、irdye680lt、alexa
在一些可选的实施例中,标记pirna探针的荧光染料包括irdye荧光染料,例如标记irdye800;标记mrna探针的荧光染料包括cy荧光染料,例如可以为但不限于为cy5或cy5.5等,例如标记cy5.5。换言之,标记pirna探针均采用irdye800荧光染料,标记mrna探针均采用cy5.5荧光染料。其中,cy5.5荧光染料的发射波长在700nm附近,irdye800荧光染料的发射波长在800nm附近,因此可以分别在700nm和800nm波长下检测并获得各探针的迁移情况。
在一些可选的实施例中,探针上的标记物可以标记于5’端,也可以标记于3’端,在一些具体的实施例中,荧光染料标记于pirna探针5’端以及mrna探针的5’端。
在一些优选的实施方式中,反应体系包括depc-h2o、bindingbuffer和探针。depc-h2o的引入能够有效防止单链rna的降解,避免由于rna降解影响后续步骤中条带的观察。
在一些优选的实施方式中,反应体系中带有标记的探针浓度为30~50nm,例如可以为但不限于为30nm、35nm、40nm、45nm或50nm。具体的,在第一反应体系中,标记的pirna探针的浓度为30~50nm;在第二反应体系中,标记的mrna探针的浓度为30~50nm;在第三反应体系、第四反应体系和第五反应体系中,标记的pirna探针的浓度和标记的mrna探针的浓度分别独立的为30~50nm。
bindingbuffer可选择本领域可接受的用于寡聚核苷酸之间结合反应的buffer,本发明对此不作限制。在一些优选的实施方式中,使用包括如下组分的bindingbuffer:ph为7.2-7.4的hepesbuffer、甘油、kcl和mgcl2。bindingbuffer中各组分在反应体系中的终浓度优选如下:ph为7.2-7.4的hepesbuffer8~12mm,优选为10mm;甘油4~6%(w/w),优选为5%(w/w)、kcl0.15~0.25m,优选为0.2m;mgcl20.5~0.15m,优选为0.1m。
在一些优选的具体实施例中,按照如下方式配置bindingbuffer和各反应体系:
bindingbuffer:100mm的ph7.2-7.4的hepesbuffer、50%的甘油、2m的kcl和1m的mgcl2等体积混合所得。以20μl反应体系为例,bindingbuffer由100mmhepesbuffer(ph7.3,),50%甘油(2μl),2mkcl(2μl)和1mmgcl2(2μl)混合所得。
探针:将各探针粉末分别用depc-h2o稀释后,于94-96℃加热1.5-2.5min,随后放冰上冷却1.8-2.5min后添加于含有bingdingbuffer的反应体系中孵育。通过先使用depc-h2o稀释,溶解探针,可有效抑制单链rna探针的降解,保证pirna探针和mrna探针结合的稳定性。
第一反应体系包括:体积比依次为8:2:10的bindingbuffer、400nm标记的pirna探针以及depc-h2o。
第二反应体系包括:体积比依次为8:2:10的bindingbuffer、400nm标记的mrna探针以及depc-h2o。
第三反应体系包括:体积比依次为8:2:2:8的bindingbuffer、400nm标记的pirna探针、400nm标记的mrna探针以及depc-h2o。
第四反应体系包括:体积比依次为8:2:2:2:6的bindingbuffer、400nm标记的pirna探针、400nm标记的mrna探针、20μm的未标记的阴性对照探针以及depc-h2o。
第五反应体系包括:体积比依次为8:2:2:2:6的bindingbuffer、400nm标记的pirna探针、400nm标记的mrna探针、20μm的未标记的pirna探针以及depc-h2o。
在一些优选的实施方式中,结合反应的反应条件为24-26℃保温18-22min。例如可以为但不限于为孵育在24℃、24.5℃、25℃、25.5℃或26℃中的任一点或任意两点之间的范围值内保温18-22min,保温时间例如可以为但不限于为18min、19min、20min、21min或22min中的任一点或任意两点之间的范围值,使pirna探针和mrna探针充分结合。
在一些优选的实施方式中,采用非变性聚丙烯酰胺凝胶电泳分离结合反应后反应体系中的片段。非变性聚丙烯酰胺凝胶的配置方法以及电泳条件可参考本领域常规方法,本发明对此不作限制。下面给出一些优选的非变性聚丙烯酰胺凝胶的配置方法以及电泳条件作为参考。
电泳采用浓度为12%的非变性聚丙烯酰胺凝胶,非变性聚丙烯酰胺凝胶配置:由体积比依次为7.5:4.5:1.5:1.5:0.105:0.075的水、40%acrylamide/bis溶液、5×tbe缓冲液、甘油、过硫酸铵和temed混合所得。例如以15ml反应体系为例,非变性聚丙烯酰胺凝胶由水(7.5ml),40%acrylamide/bis溶液(4.5ml),5×tbe缓冲液(1.5ml),甘油(1.5ml),10%过硫酸铵(0.105ml)和temed(0.075ml)混合所得。
在一些优选的实施方式中,电泳的上样缓冲液为包含有15%聚蔗糖和0.4%橙黄g的水溶液。电泳条件优选为:聚丙烯酰氨凝胶电泳的缓冲液为0.5×tbe缓冲液,电泳在4℃且恒压为100v的条件下进行2-3小时。电泳后成像方式例如可以采用成像仪,具体例如:odsseyclx红外成像系统,在该成像系统中,直接观察700nm和800nm双荧光通道下的荧光条带。需要说明的是,成像系统的检测波长与具体的荧光染料相关,可参考相关技术,在此不做赘述。
根据本发明的另一个方面,本发明还提供了上述用于检测pirna与mrna结合的可视化方法在研究pirna对基因调控作用中的应用。将上述方法应用于研究pirna对基因调控作用中,能够缩短判断pirna是否能与mrna结合的时间,并且操作简便,避免构建荧光素酶报告基因载体的工作,能够显著提高实验效率,降低实验成本。
下面结合优选实施例进一步说明本发明的技术方案和有益效果。
实施例1
本具体实施例对has-pir-016659与hnf1a结合进行检测,实验过程中使用的试剂材料如下:
荧光标记pirna探针:5’端标记irdye800的has-pir-016659寡核苷酸序列,序列为:ccccccacugcuaaauuugacugguu(seqidno.1)。
荧光标记mrna探针:5’端标记cy5.5的hnf1a寡核苷酸序列,序列为:cggccggcaggcaaacgcaacccacgcgguggggga(seqidno.2)。
未标记的pirna探针:无任何标记的has-pir-016659寡核苷酸序列,序列为:ccccccacugcuaaauuugacugguu(seqidno.1)。
阴性对照探针:无任何标记的阴性对照寡核苷酸序列,序列为:ucacaaccuccuagaaauaauaga(seqidno.3)。
仪器:高速离心机,普通pcr仪,odsseyclx红外成像系统,用于聚丙烯酰胺凝胶的垂直电泳装置,包括垫片、玻璃板、梳子和凝胶浇注架。
溶液配制:
非变性聚丙烯酰氨凝胶组成成分包括(以15ml溶液体积为例):水(7.5ml),40%acrylamide/bis溶液(4.5ml),5×tbe缓冲液(1.5ml),甘油(1.5ml),10%过硫酸铵(0.105ml),temed(0.075ml)。
6×上样缓冲液:包含15%聚蔗糖和0.4%橙黄g的水溶液。
电泳缓冲液:0.5×tbe缓冲液。
具体按照以下步骤进行:
1.短暂高速离心合成好的各探针粉末,然后向合成好的荧光标记的以及未标记的寡核苷酸探针粉末中加入(10×nmol数)μl的depc-h2o,溶解成为100μm的储液。随后95℃加热2分钟,冰上冷却2分钟。有荧光标记的探针储液用depc-h2o稀释250倍成为400nm溶液待用,无荧光标记的探针储液用depc-h2o稀释5倍成为20μm溶液待用。
bindingbuffer:100mm的ph7.2-7.4的hepesbuffer、50%的甘油、2m的kcl和1m的mgcl2等体积混合所得。以20μl反应体系为例,bindingbuffer由100mmhepesbuffer(ph7.3,),50%甘油(2μl),2mkcl(2μl)和1mmgcl2(2μl)混合所得。
第一反应体系包括:体积比依次为8:2:10的bindingbuffer、400nm的pirna探针以及depc-h2o。
第二反应体系包括:体积比依次为8:2:10的bindingbuffer、400nm的mrna探针、以及depc-h2o。
第三反应体系包括:体积比依次为8:2:2:8的bindingbuffer、400nm的pirna探针、400nm的mrna探针以及depc-h2o。
第四反应体系包括:体积比依次为8:2:2:2:6的bindingbuffer、400nm的pirna探针、400nm的mrna探针、20μm的未标记的阴性对照探针以及depc-h2o。
第五反应体系包括:体积比依次为8:2:2:2:6的bindingbuffer、400nm的pirna探针、400nm的mrna探针、20μm的未标记的pirna探针以及depc-h2o。
2.配制非变性聚丙烯酰氨凝胶:将水(7.5ml),40%acrylamide/bis溶液(4.5ml),5×tbe缓冲液(1.5ml),甘油(1.5ml),10%过硫酸铵(0.105ml)和temed(0.075ml)至于50ml离心管混合均匀,随后用移液枪轻轻的加入7.25cm×10cm×1.5mm的制胶盒并插入10齿梳子。室温静置30-60分钟至胶完全凝固。
3.将配置好的非变性聚丙烯酰氨凝胶胶板装入垂直电泳系统,加入ll的0.5×tbe缓冲液,4℃恒压80v预电泳30分钟。
4.按照如下表1中的反应体系组成进行pirna探针和mrna探针的结合反应,每一个反应体系总体积均为20μl,结合反应的反应条件为25℃孵育25分钟。
表1结合反应试剂组成
5.在上样前,用1ml注射器轻轻冲洗胶孔中残余的甘油。然后向20μl结合反应体系中加入4μl预先配置好的6×上样缓冲液,上样。
6.4℃恒压100v电泳2-3小时。
7.电泳结束后,取下胶板,用水轻轻冲洗,纸擦干后,短板朝下,直接置于odsseyclx红外成像系统上,进行扫描,观测700nm和800nm下的荧光强度。
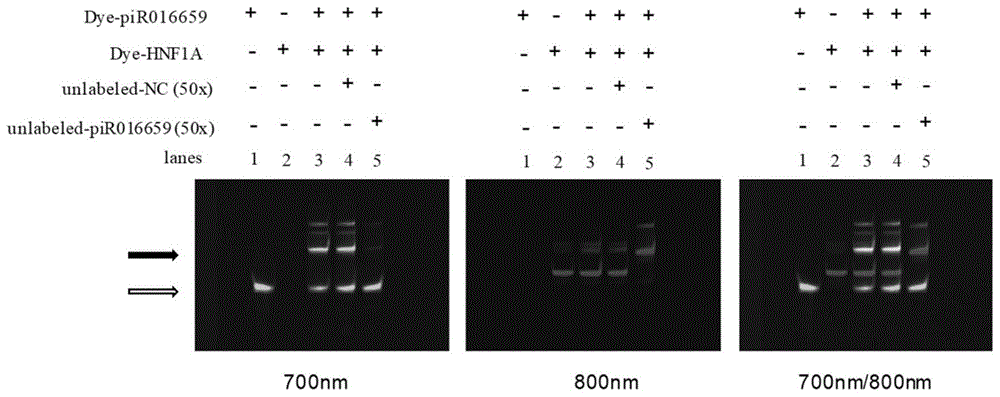
结果如图1,图中第1泳道是irdye800标记的pirna探针(has-pir-016659),第2泳道是cy5.5标记的mrna探针(hnf1a),第3泳道是irdye800标记的pirna探针(has-pir-016659)和cy5.5标记的mrna探针(hnf1a)及其结合复合物,第4泳道irdye800标记的pirna探针(has-pir-016659)和cy5.5标记的mrna探针(hnf1a)及其结合复合物,以及未标记的阴性对照探针,第5泳道是irdye800标记的pirna探针(has-pir-016659)和cy5.5标记的mrna探针(hnf1a)及其结合复合物,以及未标记的pirna探针(has-pir-016659)。其中,黑色实体箭头指示的是pirna探针(has-pir-016659)与mrna探针(hnf1a)的结合复合物,空心箭头指示的是游离的pirna探针(has-pir-016659)和mrna探针(hnf1a)单体。“+”表示添加,“-”表示未添加。
根据图1,第3泳道中,与第1和第2泳道相比,出现了pirna探针与mrna探针结合后的滞后迁移带,第4泳道中,加入未标记的阴性对照探针时,不影响pirna探针与mrna探针的结合,第5泳道中,加入50倍浓度的未标记的pirna探针时,可以竞争性的与mrna探针结合。从图1可以看出pirna探针与mrna探针结合,则说明has-pir-016659能够与hnf1a预测的区域发生结合。
实施例2
本具体实施例对has-pir-020391与znf10结合进行检测,实验过程中使用的试剂材料如下:
荧光标记pirna探针:5’端标记irdye800的has-pir-020391寡核苷酸序列,序列为:ggcucuguugcgcaauggauagcgcau(seqidno.4)。
荧光标记mrna探针:5’端标记cy5.5的znf10寡核苷酸序列,序列为:agcaaguguccucaugugauaaacagagca(seqidno.5)。
未标记的pirna探针:无任何标记的has-pir-020391寡核苷酸序列,序列为:ggcucuguugcgcaauggauagcgcau(seqidno.4)。
阴性对照探针:无任何标记的阴性对照寡核苷酸序列,序列为:ucacaaccuccuagaaagaguaga(seqidno.6)。
具体的溶液配制及实验步骤同具体实施实例1,结果如图2所示。
图2中第1泳道是irdye800标记的pirna探针(has-pir-020391),第2泳道是cy5.5标记的mrna探针(znf10),第3泳道是irdye800标记的pirna探针(has-pir-020391)和cy5.5标记的mrna探针(znf10)及其结合复合物,第4泳道irdye800标记的pirna探针(has-pir-020391)和cy5.5标记的mrna探针(znf10)及其结合复合物,以及未标记的阴性对照探针,第5泳道是irdye800标记的pirna探针(has-pir-020391)和cy5.5标记的mrna探针(znf10)及其结合复合物,以及未标记的pirna探针(has-pir-020391)。其中,黑色实体箭头指示的是pirna探针(has-pir-020391)与mrna探针(znf10)的结合复合物,空心箭头指示的是游离的pirna探针(has-pir-020391)和mrna探针(znf10)单体。“+”表示添加,“-”表示未添加。
根据图2,第3泳道中,与第1和第2泳道相比,出现了pirna探针与mrna探针结合后的滞后迁移带,第4泳道中,加入未标记的阴性对照探针时,不影响pirna探针与mrna探针的结合,第5泳道中,加入50倍浓度的未标记的pirna探针时,可以竞争性的与mrna探针结合,使结合复合物位置的红色荧光加强。从图2可以看出pirna探针与mrna探针结合,则说明has-pir-020391能够与znf10预测的区域发生结合。
综上,本发明提供的一种用于检测pirna与mrna结合的方法,其基于用标记物分别标记pirna探针和mrna探针,以达到可视化检测pirna与mrna结合,实现了操作简单、反应灵敏、快速高效且可视化的技术效果。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
sequencelisting
<110>青岛大学
<120>用于检测pirna与mrna结合的可视化方法及其应用
<160>6
<170>patentinversion3.5
<210>1
<211>26
<212>rna
<213>人工序列
<400>1
ccccccacugcuaaauuugacugguu26
<210>2
<211>36
<212>rna
<213>人工序列
<400>2
cggccggcaggcaaacgcaacccacgcgguggggga36
<210>3
<211>24
<212>rna
<213>人工序列
<400>3
ucacaaccuccuagaaauaauaga24
<210>4
<211>27
<212>rna
<213>人工序列
<400>4
ggcucuguugcgcaauggauagcgcau27
<210>5
<211>30
<212>rna
<213>人工序列
<400>5
agcaaguguccucaugugauaaacagagca30
<210>6
<211>24
<212>rna
<213>人工序列
<400>6
ucacaaccuccuagaaagaguaga24
- 还没有人留言评论。精彩留言会获得点赞!