用于新型冠状病毒核酸检测的数字PCR试剂盒的制作方法
用于新型冠状病毒核酸检测的数字pcr试剂盒
技术领域
1.本实用新型属于病毒检测技术领域,具体涉及一种用于新型冠状病毒核酸检测的数字pcr试剂盒。
背景技术:
2.2019年12月以来新型冠状病毒肆虐,新型冠状病毒(covid
‑
19)传播速度快,传播能力极强,针对病毒核酸的检测成为临床确诊的重要手段。荧光定量pcr(qpcr)的保有量高、操作简便,是本次新型冠状病毒的主要检测平台。但在临床实践中,一些有接触史、早期弱症状、病毒载量低的初诊患者样本、标本中抑制物高的患者样本、有效治疗后待复核治愈患者样本、荧光pcr检测cq值超过35的可疑样本等等会造成假阴性结果,导致此类样本的漏诊,造成了极大的传染隐患、安全风险以及医疗资源的消耗。故目前亟需更高灵敏度、高精准度、高耐抑制物能力的检测方案(包含仪器和试剂),降低假阴性,以便更准确地监控病毒。目前各大临床一线单位(疾控中心、医院)都表达了对高灵敏检测方案(包含仪器和试剂)的迫切需求,并且疫情防控常态化也将使得新冠肺炎的检测工作呈现出一个长期供需关系的状态。继荧光定量pcr之后,数字pcr是生命科学领域最令人振奋的创新之一。数字pcr可以直接数出dna分子的个数,是对起始样品的绝对定量。特别适用于拷贝数变异、突变检测、基因相对表达研究、二代测序结果验证、mirna表达分析、单细胞基因表达分析等研究领域。和传统荧光定量pcr相比,具有更高的灵敏度和准确性,并且被行业认为是支持极微量核酸检测的最有潜力的技术之一。虽然已有的数字pcr商品化早期产品为越来越多的科研机构所应用,但普遍存在操作繁杂,数据质量不可控以及产品使用时会造成实验室污染等明显缺陷。
技术实现要素:
3.针对现有新型冠状病毒核酸检测试剂盒的不足,本实用新型提供了用于新型冠状病毒核酸检测的数字pcr试剂盒,能够简单快速高灵敏度检测新型冠状病毒。
4.为了实现上述目的,本实用新型所采用的技术解决方案:
5.一种用于新型冠状病毒核酸检测的数字pcr试剂盒,其特征在于,所述试剂盒由1个装有数字pcr反应酶预混液的1.5ml离心管(1)、1个装有荧光素钠盐溶液的1.5ml离心管(2)、1个装有新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)、1个装有阳性质控品的1.5ml离心管(4)、1个装有阴性质控品的1.5ml离心管(5)组成;所述的1个装有数字pcr反应酶预混液的1.5ml离心管(1)中装有400μl数字pcr反应酶预混液;所述的1个装有荧光素钠盐溶液的1.5ml离心管(2)中装有100μl的荧光素钠盐溶液;所述的1个装有新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)中装有30μl的新型冠状病毒检测引物及探针混合物;所述的1个装有阳性质控品的1.5ml离心管(4)中装有50μl的阳性质控品;所述的1个装有阴性质控品的1.5ml离心管(5)中装有80μl的阴性质控品。
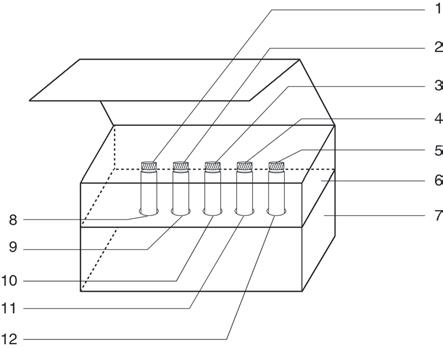
6.其中,所述试剂盒的盒体为具有盒盖结构的盒体(6),1个固定海绵衬底(7)置于盒
体底部,海绵衬底上具有5个打好的1.5ml离心管管孔(8)至(12),1个装有400μl数字pcr反应酶预混液的1.5ml离心管(1)、1个装有100μl荧光素钠盐溶液的1.5ml离心管(2)、1个装有30μl新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)、1个装有50μl阳性质控品的1.5ml离心管(4)、1个装有80μl阴性质控品的1.5ml离心管(5)分别置于固定海绵衬底(7)上打好的1.5ml离心管管孔(8)至(12)中。
7.本实用新型的有益效果在于,在三色荧光通道数字pcr技术的基础上,对新型冠状病毒的核酸检测位点进行反复设计与优化反应体系,实现了一孔内三个靶点并行检测,1个靶点是通过优化及筛选新型冠状病毒的核壳蛋白(nucleoprotein,n)区域片段保守序列并采用fam荧光(蓝色)标记探针检测;第2个靶点是新型冠状病毒的核酸的开放读码框1ab(open reading frame,orf1ab)片段序列并采用vic荧光(绿色)标记探针检测,尽可能降低病毒变异的影响;第3个检测的目的基因是人内源性管家基因(rpp30)片段序列并采用cy5荧光(红色)标记探针作为内标进行监控。利用三色荧光通道的优势,实现单孔三基因的检测,使得检测结果更加准确。
附图说明
8.图1是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒的总体结构示意图。
9.图2是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒的俯视图。
10.图中附图标记表示为:1、装有400μl数字pcr反应酶预混液的1.5ml离心管;2、装有100μl荧光素钠盐溶液的1.5ml离心管;3、装有30μl新型冠状病毒检测引物及探针混合物的1.5ml离心管;4、装有50μl阳性质控品的1.5ml离心管;5、装有80μl阴性质控品的1.5ml离心管;6、盒体;7、固定海绵衬底;8
‑
12、1.5ml离心管管孔。
11.图3是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒对于阳性质控品的fam荧光通道(蓝色荧光标记covid
‑
19
‑
n端)和vic荧光通道(绿色荧光标记covid
‑
19
‑
orf1ab)的检测2d图。
12.图4是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒对于阳性质控品的fam荧光通道(蓝色荧光标记covid
‑
19
‑
n端)和cy5荧光通道(红色荧光标记内参rpp30)的检测2d图。
13.图5是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒对于阴性质控品的fam荧光通道(蓝色荧光标记covid
‑
19
‑
n端)和vic荧光通道(绿色荧光标记covid
‑
19
‑
orf1ab)的检测2d图。
14.图6是本实用新型用于新型冠状病毒核酸检测的数字pcr试剂盒对于阴性质控品的fam荧光通道(蓝色荧光标记covid
‑
19
‑
n端)和cy5荧光通道(红色荧光标记内参rpp30)的检测2d图。
具体实施方式
15.下面结合附图和实施例对本实用新型进一步说明。
16.实施例1用于新型冠状病毒核酸检测的数字pcr试剂盒组成
17.如图1和图2所示,用于新型冠状病毒核酸检测的数字pcr试剂盒结构组成为:1个
盒体(6)、1个固定海绵衬底(7)、1个装有400μl数字pcr反应酶预混液的1.5ml离心管(1)、1个装有100μl荧光素钠盐溶液的1.5ml离心管(2)、1个装有30μl新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)、1个装有50μl阳性质控品的1.5ml离心管(4)、1个装有80μl阴性质控品的1.5ml离心管(5)组成。
18.其中,所述的1个固定海绵衬底(7)上有5个1.5ml离心管孔(8)至(12)。
19.所述的1个固定海绵衬底(7)上的离心管孔(8)内分别放置1个装有400μl数字pcr反应酶预混液的1.5ml离心管(1)、1个装有100μl荧光素钠盐溶液的1.5ml离心管(2)、1个装有30μl新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)、1个装有50μl阳性质控品的1.5ml离心管(4)、1个装有80μl阴性质控品的1.5ml离心管(5)。
20.其中,所述的1个装有400μl数字pcr反应酶预混液的1.5ml离心管(1)、1个装有100μl荧光素钠盐溶液的1.5ml离心管(2)、1个装有30μl新型冠状病毒检测引物及探针混合物的1.5ml离心管(3)、1个装有50μl阳性质控品的1.5ml离心管(4)、1个装有80μl阴性质控品的1.5ml离心管(5),优选地,分别选择不同种类及颜色的离心管,例如1个带有无色管盖的装有400μl数字pcr反应酶预混液的1.5ml透明可立离心管(1)、1个带有棕色管盖的装有100μl荧光素钠盐溶液的1.5ml棕色可立离心管(2)、1个带有浅棕色管盖的装有30μl新型冠状病毒检测引物及探针混合物的0.5ml浅棕色可立离心管(3)、1个带有红色管盖的装有50μl阳性质控品的1.5ml离心管(4)、1个带有绿色管盖的装有80μl阴性质控品的1.5ml离心管(5)。
21.实施例2用于新型冠状病毒核酸检测的数字pcr试剂盒的使用方法
22.1、打开本实用新型所述试剂盒的盒体(6),从固定海绵衬底(7)上的5个1.5ml离心管孔(8)至(12)取出实施例1中所述的五种组分(1)、(2)、(3)、(4)、(5)试剂,并于室温下平衡直至各组分试剂充分溶解,并混匀,1000rpm快速离心20秒,放置于冰上备用;
23.2、按照表1配制成一个反应为25μl的数字pcr反应工作液,一批次的样本检测需加入1个阳性质控品和1个阴性质控品进行平行检测;
24.表1、用于新型冠状病毒核酸检测的数字pcr试剂盒的反应工作液配制表
25.组分体积体积体积数字pcr反应酶预混液(1)12.5μl12.5μl12.5μl荧光素钠盐溶液(2)2.5μl2.5μl2.5μl新型冠状病毒检测引物及探针混合物(3)1μl1μl1μl待测样本9μl//阳性质控品(4)/9μl/阴性质控品(5)//9μl
26.3、配制完成后将pcr反应管涡旋混匀15秒后,快速离心15秒;
27.4、取出芯片,切勿震动,轻轻旋转白盖1/4圈,丢弃白盖,移取25μl数字pcr反应工作液加入到sapphire chip的孔井中,静置2~3分钟盖上白色长盖;
28.5、打开naica geode微滴生成扩增系统和气压泵开关,确认气压泵输出压力和微滴生成扩增系统输入(input)压力稳定在1150+/
‑
50mbar;
29.6、按照表2设置数字pcr反应程序;
30.表2、数字pcr反应程序
[0031][0032]
7、轻轻地将sapphire chip置于加热模块上,盖上naica geode机器盖,确认程序无误后,开始运行已设置好的程序,开始生成微滴和pcr反应程序;
[0033]
8、数字pcr过程结束后,取出芯片,放置于微滴阅读分析系统上进行扩增后微滴状态的扫描并采集荧光信号数据;
[0034]
9、数据采集完成后,在软件界面的每个样品孔上会显示荧光信号数据的质量状态(绿色、绿色/黄色、以及黄色图标,分别代表高质量、中质量以及低质量):
[0035]
9.1若为绿色图标,或绿色/黄色图标且微滴总数大于20000,则直接进入结果分析;
[0036]
9.2若为绿色/黄色或黄色图标,且微滴总数少于20000,需要检查曝光时间设置和qc质控,重新设置时间采集或者重新进行检测;
[0037]
10、调整荧光信号的阈值线,获得各个反应的拷贝数浓度,并进行结果分析及判读。
[0038]
10.1、试剂盒有效性判定:
[0039]
10.1.1阳性质控品:fam通道阳性微滴数10~100;vic通道阳性微滴数10~100;cy5通道阳性微滴数300~600。如图2中所示,第ⅱ象限的绿色荧光通道(vic)的荧光信号代表含有新型冠状病毒核酸片段orf1ab扩增结果的微滴(简写为covid
‑
19
‑
orf1ab)、第ⅲ象限代表无任何荧光信号的无扩增结果的微滴、第ⅳ象限代表含有新型冠状病毒核酸n端片段扩增结果的微滴(简写为covid
‑
19
‑
n端)。如图3中所示,第ⅱ象限的红色荧光通道(cy5)的荧光信号代表含有内参基因rpp30扩增结果的微滴、第ⅲ象限代表无任何荧光信号的无扩增结果的微滴、第ⅳ象限代表含有新型冠状病毒核酸n端片段扩增结果的微滴(简写为covid
‑
19
‑
n端)。
[0040]
10.1.2阴性质控品:fam或/和vic通道无阳性信号微滴或阳性微滴数<3,本次试验结果有效,可继续分析;若fam或/和vic通道阳性信号微滴数≥3个,则视为体系污染,此次检测结果无效。如图4和图5所示,阴性质控品的检测结果为无任何荧光信号的无扩增结果的微滴,即第ⅱ象限和第ⅳ象限没有带有荧光信号的微滴。
[0041]
10.2、样本有效性判定:
[0042]
10.2.1每个反应孔的质控有效微滴数均大于20000,若有效微滴数不足20000,且大约15000,实验结果仅做参考;若有效微滴数小于15000,则此次实验结果无效,建议重新检测。
[0043]
10.2.2若cy5通道阳性微滴数≥300,样本基因组rna加入量适中;当质控cy5通道阳性微滴数<300,样本rna加入量过低,只有新型冠状病毒含量较高的样本才能被检出。
[0044]
10.3、检测结果的判定:
[0045]
根据上述步骤10.1、10.2确定检测的有效性后,参照表3对样本检测结果进行判定。
[0046]
表3、用于新型冠状病毒核酸检测的数字pcr试剂盒检测结果的判定
[0047][0048]
实施例4用于新型冠状病毒核酸检测的数字pcr试剂盒灵敏度的检测
[0049]
1、将阳性质控品进行梯度稀释,稀释梯度为10倍、100倍、1000倍、10000倍,稀释后分别使用荧光定量pcr方法和数字pcr方法进行试剂盒灵敏度的检测,操作方法以及判定方法按照实施例2进行,检测结果如表4所示。
[0050]
表4、用于新型冠状病毒核酸检测的数字pcr试剂盒灵敏度的检测结果
[0051][0052]
以上表4中是20次重复检测结果的平均值,使用目前荧光定量pcr的方法进行新型冠状病毒核酸检测判定为疑似样本的标准为37≤ct值<40,阴性的判定标准是无ct值或ct=40。从表4中可以看出,稀释10倍的阳性质控品使用荧光定量pcr方法检测出的ct值均在疑似样本的范围内,按照要求需要再次进行核酸检测,而使用本实用新型数字pcr试剂盒的检测结果微滴数均≥3,均可判定为阳性。
[0053]
以上对本实用新型的实施例进行了详细说明及解释,但所述内容仅为本实用新型的最佳实施例,不能被认定用于限定本实用新型的实施范围。凡依据本实用新型申请范围所作的均等变化与改进等,均应归属于本实用新型的专利涵盖范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1