具有AIE性质和靶向活细胞线粒体功能的Mn(II)配合物及其制备方法和用途
技术领域:
本发明涉及多光子吸收材料技术领域,具体涉及一种具有aie性质和靶向活细胞线粒体功能的mn(ii)配合物及其制备方法和用途。
背景技术:
:
多光子吸收是一种非线性光学效应。在高强度激光束的照射下,物质有可能同时吸收几个、甚至几十个光子,此过程称为多光子吸收。相对于传统的单光子吸收,多光子吸收在三维可控、光解药物释放、生物荧光标记、多光子荧光显微成像(mpfm)等领域有着明显的优势,因而吸引了研究人员的极大兴趣。
但是由于现有的大多数有机材料的多光子吸收截面较小,吸收波长短,应用前景受到限制,寻找大的吸收截面和长波长的多光子吸收材料成为非线性光学领域的热点,因此结构多样、性质独特和合成简单的多光子配合物引起了研究人员的广泛关注。
过渡金属配合物具有良好的光物理性质,如量子产率高、斯托克位移大、发射峰窄、发光寿命长等(angew.chem.int.ed.,2020,59,15987-15991),其较长的荧光寿命可有效消除生物体内自发荧光的干扰。通过改变配体的结构引起配合物光物理和其它性质的变化,实现多光子光学活性配合物材料简单有效的设计合成。
基于以上考虑,本发明用具有强螯合能力的三联吡啶配体与mn(ii)形成配合物,三联吡啶配体上引入的苯胺基及丁基具有丰富的电子,引入卤素作为辅助配位原子,形成d-a结构,有利于提高推拉电子能力,增强配合物的多光子吸收性质。
技术实现要素:
:
本发明所要解决的技术问题在于提供一种具有aie性质和靶向活细胞线粒体功能的mn(ii)配合物及其制备方法和用途,通过分子设计得到具有多光子吸收性质的三吡啶mn(ii)配合物,使其具有三光子aie性质,并实现双光子细胞显影。
本发明所要解决的技术问题采用以下的技术方案来实现:
具有aie性质和靶向活细胞线粒体功能的mn(ii)配合物,简称fd-mncl2,结构式为:
上述具有aie性质和靶向活细胞线粒体功能的mn(ii)配合物的制备方法,以n,n-二丁基苯胺作为起始原料,先由n,n-二丁基苯胺与pocl3反应制得化合物o,再由化合物o与2-乙酰基吡啶反应制得化合物fd,最后由化合物fd与mncl2反应制得配合物fd-mncl2。
合成路线如下:
所述n,n-二丁基苯胺与dmf和pocl3的摩尔比为1:3:5。
所述化合物o与2-乙酰基吡啶的摩尔比为1:2-5。
所述化合物fd与mncl2的摩尔比为1:1-3。
上述具有aie性质和靶向活细胞线粒体功能的mn(ii)配合物作为多光子吸收材料的用途。
本发明中2,2:6',2”-三吡啶是含多吡啶杂环的化合物,对过渡金属离子mn(ii)有较强的配位能力,n,n-二丁基基团具有强给电子能力,有利于分子内电荷转移,调节配合物发光。卤素原子作为辅助配位原子,可以提高配合物推拉电子能力,增强非线性光学性质(dyesandpigments.,2015,117,7-15)。而且,本发明中设计的配合物具有多光子聚集诱导发射(aie)性质,克服了大多数配合物在高浓度下由于自聚集而引起的荧光猝灭(acq)。不仅如此,该配合物在800nm激发波长下,在较短时间内能进入细胞,穿透细胞膜,在线粒体内显示双光子荧光,可以用来定性追踪肝癌细胞,这一研究结果对生命科学研究具有重大的意义。
本发明的有益效果是:
1、本发明合成的新型三联吡啶mn(ii)配合物是一类具有细胞显影功能的多光子吸收材料。苯胺基及丁基有丰富的电子,有利于分子内电荷转移,调节配合物发光。引入卤素原子,提高推拉电子能力,增强非线性光学性质。该配合物与其它材料相比,具有较大的三光子吸收截面,激发能量低、波长长,穿透性强、光损伤小等特点,该配合物材料可用于多光子生物成像,具有明显的应用价值。
2、使用开孔z-扫描方法和荧光对比法研究配合物fd-mncl2的多光子吸收性质。使用开孔z-扫描方法,在800nm激发波长下,fd-mncl2的最大双光子吸收截面达到1970.63gm;在1450nm激发波长下,fd-mncl2的最大三光子吸收截面达到2.09×10-75cm6s2photon-2;使用荧光对比法,在700nm激发波长时,fd-mncl2的最大双光子吸收截面达到121.63gm,在1450nm激发波长时,fd-mncl2的最大三光子吸收截面达到2.07×10-81cm6s2photon-2。
3、本发明的mn(ii)配合物fd-mncl2具有多光子aie性能,聚集时的三光子荧光明显增强。随着水含量从0%增加到70%,荧光强度不变,发射位置在525nm处。溶质分子保持单分子状态,没有形成聚合,但随着含水量不断增加,荧光强度增强幅度明显,当h2o达到80%时,在1450nm激发波长下,fd-mncl2的三光子吸收截面为9.68×10-80cm6s2photon-2,是初始吸收截面的46倍。产生这种现象的原因是由于fd-mncl2在水中形成纳米聚合物时导致溶解度降低,激活了分子内旋转(rir)受限过程。
4、利用激光共聚焦显微镜对配合物fd-mncl2进行细胞成像研究。以800nm为激发波长时,在较短时间内fd-mncl2进入hepg2细胞(肝癌细胞)并有双光子荧光信号,说明配合物fd-mncl2具有较强的细胞渗透性。为了确认配合物fd-mncl2靶向细胞的部位,利用商业染料mitotrackerredtm进行共定位显影,结果显示fd-mncl2和mitotrackerredtm的着色部位和现象一致,fd-mncl2可以靶向活细胞的线粒体。这一研究结果表明了该配合物在双光子生物成像应用上的潜力。
5、本发明中三联吡啶锰配合物的原料易得、价格低廉、合成路线简短,合成条件温和。
附图说明:
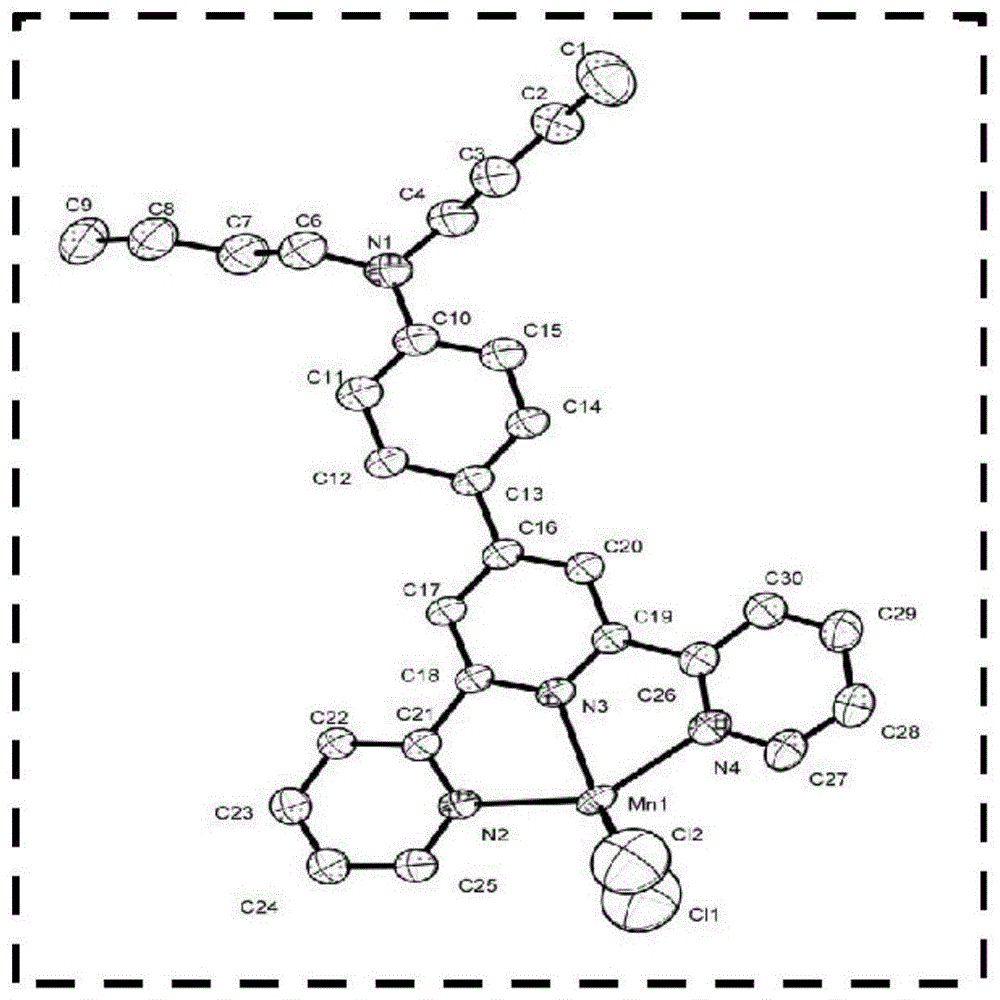
图1中为配合物fd-mncl2晶体结构图。
图2中(a-f)为开孔z-扫描方法和荧光对比法研究配合物fd-mncl2在dmso溶剂中的双/三光子吸收光谱(c=10-3mol/l)。a图使用开孔z-扫描方法,在800nm激发波长下时,fd-mncl2的最大双光子吸收截面图;b图使用开孔z-扫描方法,在1450nm激发波长下时,fd-mncl2最大三光子吸收截面图;c图使用荧光对比法,以680-860nm为激发波长时,fd-mncl2的双光子荧光光谱;d图使用荧光对比法,以680-860nm为激发波长时,fd-mncl2的双光子吸收截面图;e图使用荧光对比法,在1150-1550nm作为激发波长时,fd-mncl2的三光子荧光光谱;f图使用荧光对比法,以1150-1550nm为激发波长时,fd-mncl2三光子吸收截面图。
图3中(a-b)配合物fd-mncl2在不同比例(0%-90%,98%)ch3oh/h2o混合溶剂中的单光子荧光光谱(c=10-5mol/l);(c)800nm激发波长下,配合物fd-mncl2在0%-90%,98%ch3oh/h2o中的双光子荧光光谱(c=10-3mol/l)。(d)800nm激发波长下,配合物fd-mncl2在0%-90%,98%ch3oh/h2o的混合溶剂中的双光子吸收截面图;(e)1450nm激发波长下,fd-mncl2在0%-90%,98%ch3oh/h2o中的三光子荧光光谱(c=10-3mol/l);(f)1450nm激发波长下,配合物fd-mncl2在0%-90%,98%ch3oh/h2o的混合溶剂中的三光子吸收截面图。
图4为配合物fd-mncl2的双光子荧光显影图,激发波长=800nm,标尺=20μm;其中a是在使用800nm作为激发波长,450-490nm作为发射波长时的双光子显影图;b是在使用405nm作为激发波长,560-600nm作为发射波长时mitotrackerredtm的单光子显影图;c是单双光子叠加图;d是明场细胞显影;所有图均运用imagej软件获得。
具体实施方式:
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例和图示,进一步阐述本发明。
1、化合物o的制备
冰盐浴条件下,称取精制的dmf(4.38g,0.06mol)于500ml圆底烧瓶中,用恒压滴液漏斗向其中滴加pocl3(15.30g,0.1mol),待冻盐形成后,称取n,n-二丁基苯胺(4.10g,0.02mol),用50ml氯仿溶解后倒入冻盐中,待冻盐融化后,65℃下回流6h。待反应完全后,将反应物倒入大量冰水中,用naoh水溶液调节ph至中性后,二氯甲烷萃取,常压蒸馏出溶剂,得油状液体。将粗产物过硅胶剂柱层析,用石油醚做展开剂淋洗,第一组分即为所需产物,将展开剂蒸出即得到浅黄色油状液体3.0g,产率64%。
2、化合物fd的制备
称取2-乙酰基吡啶(3.03g,0.025mol)于500ml圆底烧瓶中,用适量的乙醇溶解,称取氢氧化钾(1.6g,0.04mol),用少量的水溶解后加入上述体系中,称取化合物o(1.17g,0.005mol)用适量的乙醇溶解后加入体系中,常温搅拌1h后用恒压滴液漏斗滴加70ml氨水,80℃回流6h后停止加热(中间补加一次氨水),旋去部分溶剂,并用乙醇重结晶得亮黄色固体3.00g,产率68%。1hnmr(400mhz,d6-acetone,ppm)δ8.76(dd,j=62.4,45.6hz,4h),8.08–7.90(m,2h),7.44(t,j=25.5hz,4h),7.27(t,j=16.5hz,1h),7.17–6.94(m,1h),6.69(t,j=19.6hz,2h),3.47–3.23(m,4h),1.58(t,j=18.5hz,4h),1.38(dt,j=27.3,13.6hz,4h),1.13–0.80(m,6h).13cnmr(100mhz,d6-acetone,ppm)δ154.19,151.80,148.26,139.25,128.79,124.05,119.73,111.53,53.49,30.07,21.77,13.79.ms(esi-ms):calc:436.60,found:437.27([m]+h+)
3、配合物fd-mncl2的制备
称量氯化锰(0.16g,1.0mmol)加入到100ml圆底烧瓶中,再加入适量的无水乙腈使其完全溶解,在常温条件下逐滴滴加配体fd(0.44g,1.0mmol)的乙腈(10ml)溶液,搅拌2h后停止反应后,过滤,得橙黄色固体0.38g产率:76%。1hnmr(400mhz,d6-dmso)δ8.75–8.53(m,6h),7.98(d,j=2.4hz,2h),7.49(s,2h),6.79(s,2h),5.63–5.05(m,3h),1.83–1.46(m,5h),1.35–1.19(m,6h),0.91(t,j=7.4hz,6h).13cnmr(100mhz,d6-dmso)δ(ppm):161.14,152.17,151.35,149.58,138.96,138.24,135.23,129.40,128.74,122.89,118.57,117.71,53.72,31.34,21.26,14.26.ft-ir(kbr,cm-1):3908(m),3844(s),3768(m),3558(m),3431(s),2962(m),2886(m),2364(m),1583(s),1532(s),1469(s),1418(s),1360(s),1202(s),1017(s),795(s).
附图分析:
图1为配合物fd-mncl2晶体结构图,证明了分子的确切结构。为了清晰的显示晶体结构,删除了氢原子及溶剂分子。配合物fd-mncl2的单晶是通过溶剂挥发法获得的,将适量的fd-mncl2溶于10ml二氯甲烷中,过滤至25ml的锥形瓶中,上面覆盖5ml的乙醇,放置于无震动的暗环境中,两周后获得橙黄色棱形晶体,单晶的尺寸大小为0.30×0.20×0.20mm。在配合物fd-mncl2的晶体数据中,该配合物属于pī空间群、三斜晶系。n,n-丁基三联吡啶作为主配体与中心mn配位,两个cl离子作为配位原子与中心mn配位。配位后的配体与金属离子处于同一平面即n^n^n-mn部分位于同一平面。
图2中a图使用开孔z-扫描方法,在800nm激发波长下时,fd-mncl2的最大双光子吸收截面达到1970.63gm;b图使用开孔z-扫描方法,在1450nm激发波长下时,fd-mncl2最大三光子吸收截面达到2.09×10-75cm6s2photon-2;c图使用荧光对比法,以680-860nm为激发波长时,fd-mncl2的双光子荧光光谱,在使用800nm作为激发波长时,其双光子荧光强度最强;d图使用荧光对比法,以680-860nm为激发波长时,fd-mncl2的最大双光子吸收截面达到121.63gm;e图使用荧光对比法,在1150-1550nm作为激发波长时,fd-mncl2的三光子荧光光谱,在使用1450nm作为激发波长时,其三光子荧光强度最强;f图使用荧光对比法,以1500nm为激发波长时,fd-mncl2最大三光子吸收截面达到2.55×10-81cm6s2photon-2。
4、aie性质测试:配置不同比例ch3oh/h2o的混合溶剂(含水量从0%-90%,98%)。测量配合物fd-mncl2在不同比例ch3oh/h2o的混合溶剂中的单/多光子荧光光谱。
图3为配合物fd-mncl2在不同比例ch3oh/h2o的混合溶剂中的单/多光子荧光光谱,探究其多光子aie性质。由a-b图可知,随着h2o含量从0%增加到50%,在525nm处荧光强度不变,当含水量大于50%,荧光增强,70%水含量时,配合物fd-mncl2的荧光强度最大;c图为在800nm激发波长下,配合物fd-mncl2在不同比例ch3oh/h2o的混合溶剂中的双光子荧光光谱,当h2o含量达到70%时,其双光子荧光强度最大;d图说明使用荧光对比法计算,在800nm激发波长下,当水组分达到70%时,最大双光子吸收截面达到67.77gm;e图为在1450nm激发波长下,配合物fd-mncl2在不同比例ch3oh/h2o的混合溶剂中的三光子荧光光谱,当h2o含量达到80%时,其三光子荧光强度最大;f图说明使用荧光对比法计算,在1450nm激发波长下,当水组分达到80%时,最大三光子吸收截面达到9.68×10-80cm6s2photon-2cm6s2photon-2,是初始吸收截面的46倍。
5、细胞培养及染色:采用hepg2细胞、dmem培养基培养24h。染色前用pbs洗涤三次以除去培养基。在培养小皿中加入200μlpbs后加入20μlfd-mncl2无水dmso溶液(1×10-3mol/l)。避光孵育15min后,用移液枪吸出溶液,pbs溶液洗涤三次后进行双光子荧光显微与成像。
从图4中可以看出,fd-mncl2作为双光子荧光探针,在800nm作为激发波长时,可以穿透细胞膜,靶向hepg2细胞线粒体,其共定位系数达0.85。
以上显示和描述了本发明的基本原理和主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!