一种合成利司那肽的方法与流程
本发明属于多肽合成领域,特别是涉及一种合成利司那肽的方法。
背景技术:
国际糖尿病联合会(idf)最新发布的第9版糖尿病地图报告指出,“糖尿病是21世纪全球进展最快的紧急情况之一”,正在影响所有年龄段、各个地区的人群。2019年,全球20-79岁人群中约4.63亿人患有糖尿病,绝大多数为2型糖尿病,相当于每11个成人中就有1名患者。
利司那肽(lixisenatide),又译为利西拉来,2016年7月27日美国fda批准赛诺菲生产的lixisenatide(商品名为adlyxin)上市,用于成人2型糖尿病的治疗。利司那肽一天仅需一次注射,原因在于利司那肽与glp-1受体亲和度高,另外,可显著抑制胃排空,因此于餐时作用显著,降低三餐ppg,可作为餐时胰岛素的替代,具有广阔的使用前景。
glp-1的受体广泛分布于胰腺、脑、心脏、肾、胃肠道等,glp-1受体激动剂与glp-1受体结合后通过camp/pka信号通路作用于胰岛细胞,葡萄糖依赖性刺激胰岛素分泌,抑制胰高血糖素分泌;同时可作用于胃肠道延缓胃排空,延缓小肠对葡萄糖的吸收,有利于餐后血糖控制;另外还可抑制中枢神经系统的摄食中枢,有利于控制体重。利司那肽在exendin-4的基础上去掉第38位的脯氨酸,并在39位的丝氨酸连接6个赖氨酸,修饰后的结构提高了药物对抗dpp-4降解的能力,半衰期可延长至3~4h。其氨基酸序列为:h-1his-gly-glu-gly-5thr–phe-thr-ser-asp-10leu-ser-lys-gln-met-15glu-glu-glu-ala-val-20arg-leu-phe-ile-glu-25trp-leu-lys-28asn-gly-30gly–pro-ser–ser-gly-35ala–pro-pro-ser-lys-40lys-lys-lys-lys–lys-nh2
利司那肽的合成,国内多采用固相fmoc化学法合成,cn102558338b和cn102875663b公开了采用常规的逐步固相合成和纯化利司那肽的方法,由于利司那肽结构中含有44个氨基酸残基,导致采用逐步固相合成的利司那肽的粗肽纯度较低,纯化难度大,总收率低。cn103709243b通过将片段1-2与片段3-44肽树脂,或者将片段1-4与片段5-44肽树脂进行固相缩合;cn103819553a利用固相化学分别合成1-17,18-29和30-44三个肽中间体片段,然后利用液相化学缩合得到利西拉来。cn106928340a采用特定的保护的丝氨酸二肽作为原料偶联到肽序中,由于形成了类似脯氨酸的环状结构,能有效的防止肽键旋转,抑制肽链卷曲剂收缩,使活性官能团(伯胺)充分暴露,从而有利于氨基酸的偶联,减少缺损等副反应的发生;cn104844706b分别合成利西拉来1-2位氨基酸片段、3-4位氨基酸片段、29-30位氨基酸片段、32-33位氨基酸片段、34-35位氨基酸片段,而后采用片段和逐一合成两种方式来制备利司那肽;cn105713082b采用片段20-44肽树脂与片段15-19进行固相缩合,然后逐步偶联剩余氨基酸至固相合成结束;cn104211801a通过液相合成片段fmoc-ser(tbu)-ser(tbu)-gly-ala-oh参与固相合成利司那肽,此工艺既能有效控制杂质di-ser33-利西拉来和di-ala35-利西拉来的含量又不影响利西拉来的收率;以上采用的片段偶联法,与常规的逐步偶联相比,提高了粗肽纯度和纯化收率;但是仍存在,制备工艺较复杂,规模化放大受限等难题。
技术实现要素:
本发明的目的在于提供一种合成利司那肽的方法,主要解决现有合成方法存在的合成周期长,生产成本高,产品收率低,不利于后期工业化放大的技术问题。
为实现以上目的,本发明提供以下技术方案:一种合成利司那肽的方法,包括如下步骤:
(a)采用siberamideresins为固相载体,用fmoc-lys(boc)-lys(boc)-oh与之偶联反应制备fmoc-lys(boc)-lys(boc)-siberamideresins,再按序列依次偶联保护氨基酸,得到h-gly-gly-pro-ser(tbu)-ser(tbu)-gly-ala–pro-pro-ser(tbu)-lys(boc)-lys(boc)-lys(boc)-lys(boc)-lys(boc)–lys(boc)-siberamideresins,经裂解得到全保护片段肽29-44:h-gly-30gly-pro-ser(tbu)–ser(tbu)-gly-35ala–pro-pro-ser(tbu)-lys(boc)-40lys(boc)-lys(boc)-lys(boc)-lys(boc)–lys(boc)-nh2;
(b)采用氨基树脂为固相载体,用fmoc-asp-all与之偶联反应制备fmoc-asp(氨基树脂)-oall,再按序列依次偶联保护氨基酸,得到片段肽1-28肽树脂boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-oall;
(c)用脱all试剂处理片段肽1-28肽树脂,得到boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-oh,然后在偶联剂存在下与全保护片段肽29-44反应,得到利司那肽肽树脂:
boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe-thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-gly-30gly-pro-ser(tbu)–ser(tbu)-gly-35ala–pro-pro-ser(tbu)-lys(boc)-40lys(boc)-lys(boc)-lys(boc)-lys(boc)–lys(boc)-nh2;
(b)利司那肽肽树脂经裂解、纯化、冻干得利司那肽精肽:h-1his-gly-glu-gly-5thr-phe-thr-ser-asp-10leu-ser-lys(boc)-gln-met-15glu-glu-glu-ala-val-20arg-leu-phe-ile-glu-25trp(boc)-leu-lys-28asn-gly-30gly–pro-ser–ser-gly-35ala–pro-pro-ser-lys-40lys-lys-lys-lys–lys-nh2。
优选的,步骤(a)中所述固相载体siberamideresins的替代度为0.2-1.0mmol/g。裂解用的试剂为三氟乙醇、三氟异丙醇与dcm的混合溶剂,体积比优选为1/4。
优选的,步骤(a)中fmoc-lys(boc)-lys(boc)-oh合成的具体操作步骤为:取碱a溶解在溶剂b中,配成碱性溶液;在低温浴下将h-lys(boc)-oh溶解于配置好的碱性溶液中,且溶解后溶液仍显碱性;低温下向反应液中加入fmoc-lys(boc)-osu/溶剂c溶液,滴加完毕后,升温继续搅拌反应,经浓缩、调酸、析晶、重结晶,得到单体fmoc-lys(boc)-lys(boc)-oh。
进一步的,所述的碱a溶解在溶剂b中配成的碱性溶液可以是氨水、氢氧化钠、氢氧化钾、碳酸钠、碳酸氢钠、碳酸氢钾、碳酸钾等水溶液或与水互溶的有机溶剂的混合溶液;同时也可以是三乙胺、二乙胺、n,n-二异丙基乙胺等有机碱的有机溶液;所述的溶剂c可以是四氢呋喃、二氧六环、n,n-二甲基甲酰胺、丙酮中的一种或一种以上的混合液。
优选的,步骤(a)中29位和30位gly采用二肽单体fmoc-gly-gly-oh作为原料引入,34位gly和35位ala采用二肽单体fmoc-gly-ala-oh作为原料引入,39位和40位lys以及41位和42位lys均采用fmoc-lys(boc)-lys(boc)-oh作为原料引入。
优选的,步骤(b)中1位his和2位gly采用二肽单体boc-his(trt)-gly-oh作为原料引入,3位glu和4位gly采用二肽单体fmoc-glu(otbu)-gly-oh作为原料引入。
优选的,步骤(b)所述的氨基树脂是替代度为0.1-0.8mmol/g的rinkamideresins、rinkamideam-resins和rinkamide-mbharesins中的一种;优选的,偶联反应中所用的缩合剂为以下组合dic/hobt、dic/hoat、tbtu/hobt/dipea、hbtu/hobt/dipea、hatu/hoat/dipea的一种。
优选的,步骤(c)中脱all试剂为pd(pph3)4/chcl3-acoh-n-甲基吗啉(37:2:1)。
优选的,所述步骤(d)中,裂解试剂为加入体积比1-5%清除剂的tfa溶液,所述清除剂为苯甲醚、苯甲硫醚、乙二硫醇、巯基乙醇、苯酚、水和tis中的一种或几种。
相对于现有技术,本发明的有益效果是:
本发明首次采用fmoc-asp-oall的侧链羧基与氨基树脂偶联反应,制备得到片段肽1-28肽树脂,脱掉28位asp的α羧基保护基all,与全保护片段肽29-44偶联,得到利司那肽;与现有技术中的合成方法相比,本发明能够有效的提高粗肽的纯度,降低纯化的难度,提高终产品的收率,有利于合成规模的放大,降低生产成本。
附图说明
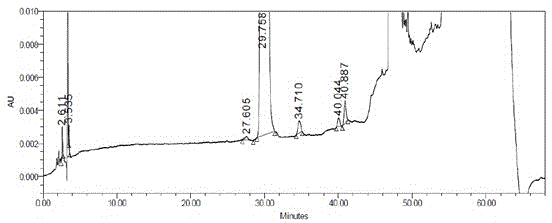
图1是利司那肽峰谱图。
图2是利司那肽峰面积结果图。
具体实施方式
下面用具体实施例对本发明进行详细说明,但不限定本专利;根据本发明改变原料的投料比、或是反应溶剂或及缩合剂等,均在本发明的保护范围内。
说明书和权利要求书中所使用的缩写含义如下:
fmoc:9-芴甲氧羰基;
tbu:叔丁基;
pbf:2,2,4,6,7-五甲基苯并呋喃-5-磺酰基;
trt:三苯甲基;
dcm:二氯甲烷;
dmf:n,n-二甲基甲酰胺;
dipea:n,n-二异丙基乙胺;
dic:n,n-二异丙基碳二亚胺;
hbtu:苯并三氮唑-n,n,n',n'-四甲基脲六氟磷酸盐;
hatu:2-(7-偶氮苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸酯;
tbtu:o-苯并三氮唑-n,n,n',n'-四甲基脲四氟硼酸;
hobt:1-羟基苯并三唑;
hoat:1-羟基-7-偶氮苯并三氮唑;
tfa:三氟乙酸;
tis:三异丙基硅烷;
boc:叔丁氧羰基;
su:琥珀酰亚胺基;
dtt:二硫苏糖醇;
all:烯丙基。
实施例1:fmoc-lys(boc)-lys(boc)-oh的合成
准确称取h-lys(boc)-oh5.92kg(1.0mol)于100l反应釜中,加入10%碳酸钠水溶液24l,搅拌下溶解;待溶清后,低温下滴加入fmoc-lys(boc)-osu11.30kg(2mol)/24l四氢呋喃溶液,搅拌反应,tlc监测终点;经减压浓缩、调酸、乙酸乙酯萃取、干燥、析晶,得纯度99.0%的二肽单体fmoc-lys(boc)-lys(boc)-oh11.16kg,收率80.1%。
实施例2:全保护片段肽29-44的制备
准确称取替代度为0.62mmol/g的siberamideresins484g(合成规模300mmol)置于10l合成釜中,加入5000mldcm溶胀30min;抽滤掉dcm后,5000mldmf洗涤2次,加入20%哌啶/dmf溶液5000ml脱保护2次,分别反应10min和10min;然后用5000mldmf、dcm、dmf分别洗涤2次;依次和fmoc-lys(boc)-lys(boc)-oh、fmoc-lys(boc)-lys(boc)-oh、fmoc-lys(boc)-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-gly-ala-oh、fmoc-ser(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-gly-gly-oh偶联,得到肽树脂h-gly-gly-pro-ser(tbu)-ser(tbu)-gly-ala–pro-pro-ser(tbu)–lys(boc)-lys(boc)-lys(boc)-lys(boc)-lys(boc)–lys(boc)-siberamideresins;然后用7000ml20%三氟乙醇/dcm(体积比)处理肽树脂60min,再分别用1000ml20%三氟乙醇/dcm(体积比)溶液洗涤两次,合并裂解液和洗涤液,旋蒸掉dcm,加入甲基叔丁基醚20l,析晶,沉降、过滤、洗涤,真空干燥得到672.6g全保护片段肽29-44:h-gly-30gly-pro-ser(tbu)–ser(tbu)-gly-35ala–pro-pro-ser(tbu)-lys(boc)-40lys(boc)-lys(boc)-lys(boc)-lys(boc)–lys(boc)-nh2,收率99.52%,纯度95.62%。
实施例3:利司那肽肽树脂的制备
准确称取替代度为0.32mmol/g的rinkamideam-resins62.5g(合成规模20mmol)置于2l合成柱中,加入600mldcm溶胀30min;抽滤掉dcm后,600mldmf洗涤2次,加入20%哌啶/dmf溶液600ml脱保护2次,分别反应10min和10min;然后用600mldmf、dcm、dmf分别洗涤2次;依次和fmoc-asp-oall、fmoc-lys(boc)–oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)–oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-glu(otbu)-gly-oh、boc–1his(trt)-gly-oh偶联,得到片段肽1-28肽树脂boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe–thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-oall;在氩气保护下向合成柱中加入69.36g(60mmol)pd(pph3)4/700mlchcl3-acoh-n-甲基吗啉(37:2:1),反应2h后,抽滤掉反应液,然后用700mldmf、dcm、dmf分别洗涤2次;然后准确称取151.37g(60mmlo)实施例2得到全保护片段肽29-44/8.91g(66mmol)hobt/8.32g(66mmol)dic/600mldmf加入反应釜中,室温下反应4h,抽滤掉反应液(加入甲基叔丁基醚回收全保护片段肽29-44),经700mldmf、dcm、甲醇分别洗涤2次,真空干燥后得利司那肽肽树脂132.60g。
实施例4:利司那肽肽树脂的制备
准确称取替代度为0.32mmol/g的rinkamideresins62.5g(合成规模20mmol)置于2l合成柱中,加入600mldcm溶胀30min;抽滤掉dcm后,600mldmf洗涤2次,加入20%哌啶/dmf溶液600ml脱保护2次,分别反应10min和10min;然后用600mldmf、dcm、dmf分别洗涤2次;依次和fmoc-asp-oall、fmoc-lys(boc)–oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)–oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-glu(otbu)-gly-oh、boc–1his(trt)-gly-oh偶联,得到片段肽1-28肽树脂boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe–thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-oall;在氩气保护下向合成柱中加入69.36g(60mmol)pd(pph3)4/700mlchcl3-acoh-n-甲基吗啉(37:2:1),反应2h后,抽滤掉反应液,然后用700mldmf、dcm、dmf分别洗涤2次;然后准确称取151.37g(60mmlo)实施例2得到全保护片段肽29-44/8.91g(66mmol)hobt/8.32g(66mmol)dic/600mldmf加入反应釜中,室温下反应4h,抽滤掉反应液(加入甲基叔丁基醚回收全保护片段肽29-44),经700mldmf、dcm、甲醇分别洗涤2次,真空干燥后得利司那肽肽树脂131.80g。
实施例5:利司那肽肽树脂的制备
准确称取替代度为0.30mmol/g的rinkamide–mbha-resins62.7g(合成规模20mmol)置于2l合成柱中,加入600mldcm溶胀30min;抽滤掉dcm后,600mldmf洗涤2次,加入20%哌啶/dmf溶液600ml脱保护2次,分别反应10min和10min;然后用600mldmf、dcm、dmf分别洗涤2次;依次和fmoc-asp-oall、fmoc-lys(boc)–oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)–oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-glu(otbu)-gly-oh、boc–1his(trt)-gly-oh偶联,得到片段肽1-28肽树脂boc–1his(trt)-gly-glu(otbu)-gly-5thr(tbu)-phe–thr(tbu)-ser(tbu)-asp(otbu)-10leu-ser(tbu)-lys(boc)-gln(trt)-met-15glu(otbu)-glu(otbu)-glu(otbu)-ala-val-20arg(pbf)-leu-phe-ile-glu(otbu)-25trp(boc)-leu-lys(boc)-28asp(氨基树脂)-oall;在氩气保护下向合成柱中加入69.36g(60mmol)pd(pph3)4/700mlchcl3-acoh-n-甲基吗啉(37:2:1),反应2h后,抽滤掉反应液,然后用700mldmf、dcm、dmf分别洗涤2次;然后准确称取151.37g(60mmlo)实施例2得到全保护片段肽29-44/8.91g(66mmol)hobt/8.32g(66mmol)dic/600mldmf加入反应釜中,室温下反应4h,抽滤掉反应液(加入甲基叔丁基醚回收全保护片段肽29-44),经700mldmf、dcm、甲醇分别洗涤2次,真空干燥后得利司那肽肽树脂132.90g。
实施例6:利司那肽肽树脂的裂解
将实施例3得到的130g肽树脂,加入到冷冻的1300ml裂解液(体积配比为tfa/苯甲硫醚/tis/h20=90/5/2.5/2.5)中,室温下搅拌反应4h;裂解反应结束,过滤树脂,130mltfa洗涤树脂2次,合并滤液和洗液,倒入16l冷冻甲叔醚中,析出白色沉淀;静置30min后,过滤,甲叔醚洗涤6次,真空干燥得粗肽94.90g,粗肽收率99.62%,纯度72.68%。
实施例7:利司那肽肽树脂的裂解
将实施例4得到的130g肽树脂,加入到冷冻的1300ml裂解液(体积配比为tfa/苯甲硫醚/tis/h20=90/5/2.5/2.5)中,室温下搅拌反应4h;裂解反应结束,过滤树脂,130mltfa洗涤树脂2次,合并滤液和洗液,倒入16l冷冻甲叔醚中,析出白色沉淀;静置30min后,过滤,甲叔醚洗涤6次,真空干燥得粗肽94.20g,粗肽收率98.29%,纯度73.82%。
实施例8:利司那肽肽树脂的裂解
将实施例5得到的130g肽树脂,加入到冷冻的1300ml裂解液(体积配比为tfa/苯甲硫醚/tis/h20=90/5/2.5/2.5)中,室温下搅拌反应4h;裂解反应结束,过滤树脂,130mltfa洗涤树脂2次,合并滤液和洗液,倒入16l冷冻甲叔醚中,析出白色沉淀;静置30min后,过滤,甲叔醚洗涤6次,真空干燥得粗肽95.00g,粗肽收率99.95%,纯度74.60%。
实施例9:利司那肽的纯化
将实施例6所得粗肽溶液用0.45um滤膜过滤备用。
内径为150mmc18制备柱,流动相为0.1%tfa/水-0.1%tfa/乙腈体系,上样量为30g/次,流速500ml/min,梯度洗脱;峰前和峰后循环进样,得到中控分析纯度合格的精肽溶液,脱盐后冻干得精肽49.67g,收率52.14.0%,纯度99.86%,单杂均小于0.2%.
实施例10:利司那肽的纯化
将实施例7所得粗肽溶液用0.45um滤膜过滤备用。
内径为150mmc18制备柱,流动相为0.1%tfa/水-0.1%tfa/乙腈体系,上样量为30g/次,流速500ml/min,梯度洗脱;峰前和峰后循环进样,得到中控分析纯度合格的精肽溶液,脱盐后冻干得精肽48.92g,收率51.04%,纯度99.80%,单杂均小于0.2%.
实施例11:利司那肽的纯化
将实施例8所得粗肽溶液用0.45um滤膜过滤备用。
内径为150mmc18制备柱,流动相为0.1%tfa/水-0.1%tfa/乙腈体系,上样量为30g/次,流速500ml/min,梯度洗脱;峰前和峰后循环进样,得到中控分析纯度合格的精肽溶液,脱盐后冻干得精肽48.62g,收率51.15%,纯度99.74%,单杂均小于0.2%。利司那肽精肽的纯度谱图见图1和图2,图1是利司那肽峰谱图,图2是利司那肽峰面积结果图。
- 还没有人留言评论。精彩留言会获得点赞!