一种酰胺类化合物及其制备方法和用途
本发明属于化学医药领域,具体涉及一种酰胺类化合物及其制备方法和用途。
背景技术:
钩藤(uncariarhynchophylla),又被称为双钩藤,倒挂刺,鹰爪凤等,为茜草科钩藤属常绿藤本植物。钩藤又分为大叶钩藤(uncariamacrophyllawall),.毛钩藤(uncariahirsutahavil.),华钩藤(uncariasinensis(oliv.)havil)或无柄果钩藤(uncariasessilifructusroxb.)。钩藤的适宜生长环境为温暖湿润、疏松肥沃的土壤,在广东、贵州、广西、福建、江西等均有种植。钩藤的药用部位通常为其带钩的枝条,其味甘苦、微寒,归心包经,具有清热透邪的作用。目前已报道的从钩藤中分离出的化学成分有100多种,包括生物碱类、黄酮类、三萜类和苷类等,其中以生物碱的含量尤为丰富,如钩藤碱、异钩藤碱、去氢钩藤碱等。钩藤的药理作用,如消炎、止痛、降压、抗癌、抗癫痫等,与其化学成分密切相关。
中药成分快速分离纯化技术对于理解中药复杂的物质基础、控制重要质量和发现潜在的活性物质具有重要意义。高压制备液相系统在分析型高效液相色谱的基础上,在保证样品分离度的前提下,大幅度提高载样量,从而快速获得高纯度的目标化合物。高压制备液相在中药、生物药、生物制品、食品等样品的分离研究中得到广泛应用。
技术实现要素:
本发明的目的在于提供一种新的酰胺化合物。本发明的另一个目的在于提供化合物的制备方法和用途。
本发明所述的一种酰胺类化合物,其化学结构式为:
本发明所述的酰胺类化合物的制备方法,包括以下步骤:
(1)取茜草科植物钩藤的干燥茎枝粉碎,加入乙醇-水(70%-30%),冷浸后过滤,重复3-5次合并提取液,减压浓缩,干燥,得粗提物;
(2)将粗提物溶于蒸馏水得混悬液,依次用正己烷、乙酸乙酯、正丁醇萃取,保留乙酸乙酯萃取相,得乙酸乙酯萃取液,将乙酸乙酯萃取液减压浓缩,干燥,得乙酸乙酯萃取物;
(3)将乙酸乙酯萃取物过硅胶柱,梯度洗脱,共分为9个组分,分别命名为fr.1-fr.9;取fr.3过液相色谱,66%甲醇-水,得到式i化合物,即该酰胺化合物。
在上述提取方法中,其中
在步骤(1)中,所述钩藤与70%乙醇水的质量体积比为1:7-13,优选为1:10,质量体积比的单位为kg/l。例如,质量体积比为1:10,即1kg钩藤需要加入10l的70%乙醇水;所述冷浸时间为13-17天,优选15天;重复次数优选为3次。
在步骤(2)中,所述钩藤粗提物与蒸馏水的质量体积比为1:1-2;所述钩藤粗提物与正己烷、乙酸乙酯、正丁醇各自的质量体积比均为1:0.5-2,优选为1:1-1.2,质量体积比的单位为kg/l。例如,质量体积比为1:1,即1kg钩藤粗提物需要加入1l正己烷、1l乙酸乙酯、1l正丁醇。
步骤(3)中,乙酸乙酯萃取物过硅胶柱时采用二氯甲烷与甲醇的混合洗脱体系,二氯甲烷与甲醇的体积比依次为9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9;每五个柱体积更换一次洗脱体系。
步骤(3)中,液相色谱中色谱柱规格为innocalods-2,10×250mm,5μm。流速为3ml/min,柱温为25℃,检测为双波长检测,分别为254nm和280nm,保留时间为22min。
本发明还提供了一种药物组合物,包含活性成分和药学上可接受的载体;所述的活性成分包括本发明所述的酰胺类化合物或者其药学上可接受的盐或互变异构体或立体异构体或溶剂化物或前药分子或代谢物或混合物。
本发明还涉及所述的酰胺化合物或所述的药物组合物在制备抗炎药物中的应用。其中,所述酰胺化合物表现出抑制炎症细胞的能力,本发明采用lps诱导raw264.7炎症模型法对其进行用体外抗炎活性检测,结果显示炎症抑制率为90.91%。
附图说明
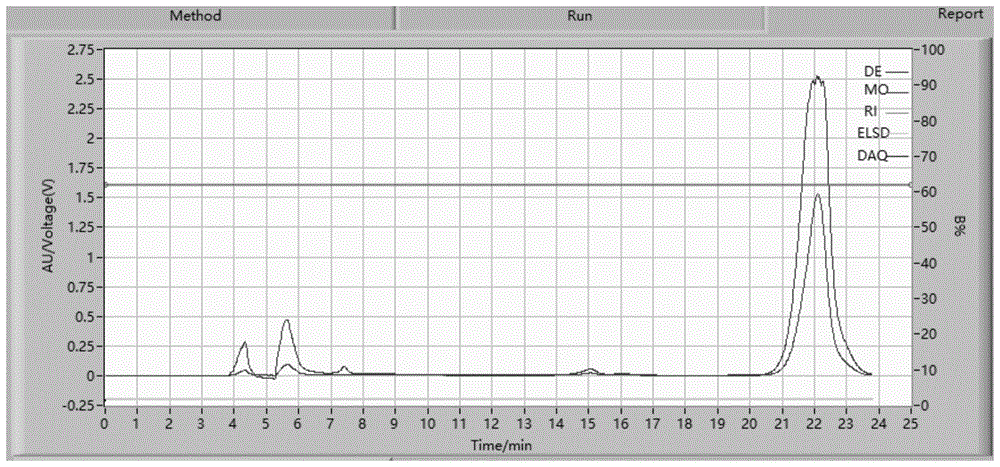
图1钩藤提取物的pre-hplc色谱图
图2式i化合物核磁共振1h谱图
图3式i化合物核磁共振13c谱图
图4式i化合物核磁共振dept135谱图
图5式i化合物核磁共振hmbc谱图
图6式i化合物核磁共振hsqc谱图
具体实施方式
下面结合实施例对本发明作进一步阐述。必须说明下述实施例是用于说明本发明而不是对本发明的限制。根据本发明的实质对本发明进行的简单改进都属于本发明要求保护的范围。
下述实施例所使用的的部分仪器和试剂为:普析tu-1950紫外分光光度计(北京普析公司);mettlerae240型电子天平(梅特勒--托利多(上海)有限公司),kq-250b超声波清洗器(昆山市超声仪器有限公司)。co2培养箱;96孔细胞培养板;am-100紫外分光光度计;deme培养基,胎牛血清(fbs,gibco公司);lps,dmso(sigma公司);cck8试剂盒;细胞计数器;其他试剂为分析纯,水为蒸馏水。其他仪器均是实验室常用仪器;其他试剂也均是常规试剂,均可以市售或者实验室获得。
实施例1式i酰胺类化合物提取
通过如下方法制备式i酰胺类化合物:
(1)称取钩藤10kg,分2批,每批5kg,每批加入50l乙醇水(70%-30%),冷浸15天,重复3次,合并提取液,减压浓缩,干燥得粗提物940.3g。
(2)将粗提物溶于1l蒸馏水,置于3l分液漏斗中,加入正己烷1l萃取,共3次,合并萃取液,减压浓缩,干燥得正己烷萃取物5.1g。对于剩余水相,采用相同方法,依次用1l乙酸乙酯、1l正丁醇萃取,分别得到乙酸乙酯萃取物9.4g和正丁醇萃取物91.9g,水层为830g。
(3)将乙酸乙酯萃取物过硅胶柱(二氯甲烷:甲醇9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9)每五个柱体积更换一次洗脱体系,梯度洗脱,共分为9个组分,分别命名为fr.1-fr.9。取fr.3过液相色谱,66%甲醇-水,得式i化合物,即酰胺化合物。液相色谱中色谱柱规格为innocalods-2,10×250mm,5μm。流速为3ml/min,柱温为25℃,检测为双波长检测,分别为254nm和280nm,保留时间为22min。如图1所示。
对得到的化合物进行结构鉴定,鉴定结果如下:
氢谱:7.00(dd,j=8.4,1.8hz,1h,h-2),6.71(d,j=8.4hz,1h,h-2),7.51(d,j=1.8hz,1h,h-6),6.66(d,j=12.6hz,1h,h-7),5.86(d,j=12.6hz,1h,h-8),7.02(dd,j=8.4,1.8hz,1h,h-2’),6.82(d,j=8.4hz,1h,h-2’),7.15(d,j=1.8hz,1h,h-6’),7.49(d,j=15.6hz,1h,h-7’),6.46(d,j=15.6hz,1h,h-8’),3.81(s,3h,5-och3),3.85(s,5’-och3)。
碳谱:128.5(c-1),125.3(c-2),115.9(c-3),148.8(c-4),148.6(c-5),114.2(c-6),139.2(c-7),120.9(c-8),173.0(c-9),128.2(c-1’),123.5(c-2’),116.6(c-3’),149.5(c-4’),150.2(c-5’),111.7(c-6’),141.7(c-7’),118.3(c-8’),171.7(c-9’),56.54(5-och3),56.46(5’-och3)。
所述化合物核磁共振1h谱图如图2所示。
所述化合物核磁共振13c谱图如图3所示。
所述化合物核磁共振dept135谱图如图4所示。
所述化合物核磁共振hmbc谱图如图5所示。
所述化合物核磁共振hsqc谱图如图6所示。
确定其结构式为:
实施例2式i化合物抗炎活性研究
供试品配制:取式i化合物,用dmso配制成50mg/ml储存液,加药时用无血清dmem培养基稀释成50μg/ml的供试品药液。另外,取姜黄素,用dmso配制成50mg/ml储存液,加药时用无血清dmem培养基稀释成50μg/ml的供试品药液。
细胞培养:raw264.7细胞用含10%fbsdmem培养,置5%co2、37℃、饱和湿度的细胞培养箱中培养。待细胞生长至对数生长期进行传代,2~3d传代1次。取至少3代后的细胞用于实验。
化合物对raw264.7细胞生长的影响:取对数生长期的raw264.7细胞0.25%胰酶-0.02%edta消化约2min后,弃胰酶,用10%fbsdmem培养基中和胰酶作用,轻轻吹打成单细胞悬液,离心弃上清,用完全培养基重悬细胞并计数后,调整细胞悬液至3×105/ml,按每孔100μl接种至96孔培养板,37℃、5%co2、饱和湿度条件下培养24h,吸尽每孔上清,每孔加入100μl无血清dmem培养基,分为对照组、阳性组(姜黄素)、式i化合物实验组;另设不含细胞的空白组(直接在孔中加入100μl无血清dmem培养基)。每组设3个复孔,加入相应药物(其中,式i化合物实验组每孔加入100μl浓度为50μg/ml的式i化合物,阳性组每孔加入100μl浓度为50μg/ml的姜黄素,对照组和空白组每孔加入100μl无血清dmem培养基)后,5%co2、37℃、饱和湿度条件下培养24h。然后,按每孔10μl加入cck-8,4h后酶标仪检测450nm处吸光度值(a450)。根据以下公式计算化合物的炎症抑制率,其中apostive为阳性组吸光度值,acontrol为对照组吸光度值,atreated为式i化合物实验组吸光度值,ablank为空白组吸光度值。
炎症抑制率=[1-(atreated-ablank)/(acontrol-ablank)]×100%
抗炎实验结果显示,apostive=0.099,atreated=0.105,acontrol=0.185,ablank=0.097。经计算,阳性组姜黄素的炎症抑制率为97.72%,式i化合物炎症抑制率为90.91%。式i化合物的抗炎效果与姜黄素相当。
- 还没有人留言评论。精彩留言会获得点赞!