一种三重态湮灭剂及其制备方法和应用与流程
本发明属于上转换材料技术领域,涉及一种三重态湮灭剂及其制备方法和应用,尤其涉及一种双发色团三重态湮灭剂及其制备方法和应用。
背景技术:
光子上转换是一种能够将低能量长波长的光转换成高能量短波长光的技术,是提高太阳能利用效率的重要方法。能够实现光子上转换的方法一般有稀土材料上转换,双光子吸收上转换,以及近年来发展起来的三重态-三重态湮灭上转换。相对于前两者来说,三重态-三重态湮灭上转换所需光照强度低,上转换效率高,而且激发发射波长灵活可调,因此三重态-三重态湮灭上转换在生物成像、光催化、光动力治疗以及太阳能电池的领域具有较大的应用价值。
在三重态-三重态湮灭上转换的体系中,敏化剂(能量给体)和能量受体是两个重要组成部分。敏化剂吸收低能量的光子,通过三重态-三重态能量转移将能量转移至受体。两个处于激发三重态的受体发生碰撞,其中一个受体回到基态,另一个受体达到能量更高的激发单重态,通过辐射跃迁实现上转换发光。基于这一特征,三重态-三重态湮灭上转换发光理论量子效率的极限为50%。为了实现高效率的上转换发光,必须开发新的能量受体。
目前为止,三重态-三重态湮灭光子上转换领域报道的最高量子效率为38%,远低于50%。因此,本发明期望开发一种能够实现接近量子效率理论极限的上转换荧光发射的三重态湮灭剂。
技术实现要素:
针对现有技术的不足,本发明的目的在于提供一种三重态湮灭剂及其制备方法和应用,尤其提供一种双发色团三重态湮灭剂及其制备方法和应用。该三重态湮灭剂具有极高的上转换发光量子效率,其量子效率饱和后最大值达到了42%,这是目前已报道的三重态-三重态湮灭上转换体系中,最高的发光量子效率。
为达到此发明目的,本发明采用以下技术方案:
第一方面,本发明提供一种三重态湮灭剂,所述三重态湮灭剂包括如式i所示结构的[2.2]对环芳烃结构化合物;
其中,r为取代的或未取代的具有联苯结构或并苯结构的基团。
所述联苯结构或并苯结构是指至少两个苯环通过共价连接或并合在一起的结构。
本发明所涉及的三重态湮灭剂由于具有[2.2]对环芳烃结构,并且在结构中含有两个联苯或并苯结构,能够保证自身具有高发光量子效率,同时能够用作三重态湮灭上转换体系的能量受体,可与敏化剂配合实现效率极高的光子上转换发射,该三重态湮灭剂材料在生物成像、光催化、光伏太阳能电池、显示、光信息的处理和存储等方面具有较大的应用价值。
优选地,所述具有联苯结构的基团包括具有三联苯结构的基团。
优选地,所述具有并苯结构的基团包括具有芘环结构的基团、具有蒽环结构的基团、具有苝环结构的基团或具有并四苯结构的基团。
优选地,所述取代的或未取代的具有联苯结构或并苯结构的基团选自如下结构中的任意一种:
其中,x独立地选自氢、烷基、烯烃基、芳基、炔烃基、卤素、羧基、酯基、磺酰基、羟基或氨基中的任意一种。
优选地,所述烷基为c1-c6(例如c1、c2、c3、c4、c5或c6)的直链烷基或支链烷基。示例性地可以为:甲基、乙基、丙基、丁基、戊基、己基、异戊基、异丙基或异丁基等。
优选地,所述烯烃基为c2-c6(例如c2、c3、c4、c5或c6)的直链烯烃基或支链烯烃基。示例性地可以为:乙烯基、丙烯基、丁烯基、戊烯基等。
优选地,所述芳基为苯基、对甲苯基、邻甲苯基、4-叔丁基苯基、2,6-二叔丁基苯基或萘基。
优选地,所述炔烃基为c2-c6(例如c2、c3、c4、c5或c6)的直链炔烃基或支链炔烃基。示例性地可以为:乙炔基、丙炔基、丁炔基、戊炔基等。
优选地,所述卤素为氟或氯。
优选地,所述酯基为甲酯、乙酯、丙酯基或丁酯基团。
优选地,所述磺酰基为甲磺酰基、乙磺酰基或丙磺酰基。
进一步优选地,所述三重态湮灭剂包括如式a-f所示结构的化合物中的任意一种或至少两种的组合:
第二方面,本发明提供一种如第一方面所述的三重态湮灭剂的制备方法,所述制备方法包括:
在保护性气体保护下,4,12-二溴[2.2]对环芳烃在溶剂中于催化剂催化下与具有取代的或未取代的联苯结构或并苯结构的硼酸或硼酸频哪醇酯反应,得到所述三重态湮灭剂。
优选地,所述保护性气体包括氮气或氩气。
优选地,所述溶剂为有机溶剂和水的混合溶剂;所述有机溶剂包括1,4-二氧六环、甲苯、邻二甲苯、间二甲苯或对二甲苯中的任意一种或至少两种的组合;所述至少两种的组合例如1,4-二氧六环和甲苯的组合、邻二甲苯和间二甲苯的组合、间二甲苯和对二甲苯的组合等,其他任意的组合方式均可选择,在此便不再一一赘述。
优选地,所述催化剂包括双(二亚芐基丙酮)钯、醋酸钯、四(三苯基膦)钯或氯化钯中的任意一种或至少两种的组合;所述至少两种的组合例如双(二亚芐基丙酮)钯和醋酸钯的组合、醋酸钯和四(三苯基膦)钯的组合、四(三苯基膦)钯和氯化钯的组合等,其他任意的组合方式均可选择,在此便不再一一赘述。
优选地,所述催化剂与4,12-二溴[2.2]对环芳烃的摩尔比为(0.01-0.2):1,例如0.01:1、0.02:1、0.05:1、0.08:1、0.1:1、0.12:1、0.15:1、0.16:1、0.18:1、0.19:1、0.2:1等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。
在本发明中,所述具有取代的或未取代的联苯结构或并苯结构的硼酸或硼酸频哪醇酯选自如下结构化合物中的任意一种或至少两种的组合:
其中x的限定范围与上述限定范围保持一致;x'为硼酸基团或硼酸频哪醇酯基团;
优选地,所述4,12-二溴[2.2]对环芳烃与所述具有取代的或未取代的联苯结构或并苯结构的硼酸或硼酸频哪醇酯的摩尔比为(0.2-1.5):1,例如0.2:1、0.4:1、0.5:1、0.8:1、1.0:1、1.2:1、1.3:1、1.4:1、1.5:1等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。
优选地,所述反应在配体和碱性物质的存在下进行。
优选地,所述配体包括三苯基膦、1,1'-双(二苯基膦)二茂铁或三环己基膦中的任意一种或至少两种的组合;所述至少两种的组合例如三苯基膦和1,1'-双(二苯基膦)二茂铁的组合、1,1'-双(二苯基膦)二茂铁和三环己基膦的组合等,其他任意的组合方式均可选择,在此便不再一一赘述。
优选地,所述配体与催化剂的摩尔比为1:(0.3-5),例如1:0.3、1:0.6、1:0.9、1:1.2、1:1.5、1:1.8、1:2、1:2.4、1:2.7、1:3、1:3.3、1:3.5、1:4或1:5等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。
优选地,所述碱性物质包括碳酸铯、碳酸钠、碳酸钾、碳酸氢钠、乙醇钠、甲醇钠或磷酸二氢钾中的任意一种或至少两种的组合;所述至少两种的组合例如碳酸铯和碳酸钠的组合、碳酸钾和碳酸氢钠的组合、乙醇钠和甲醇钠的组合等,其他任意的组合方式均可选择,在此便不再一一赘述。
优选地,所述碱性物质与4,12-二溴[2.2]对环芳烃的摩尔比为1:(0.3-5),例如1:0.3、1:0.6、1:0.9、1:1.2、1:1.5、1:1.8、1:2、1:2.4、1:2.7、1:3、1:3.3、1:3.5、1:4或1:5等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。
优选地,所述反应在回流下进行12-36h,例如12h、14h、18h、24h、26h、30h、36h等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。即使得所述反应的温度达到相应混合溶剂的沸点温度,使溶剂产生回流。
第三方面,本发明提供一种基于三重态-三重态湮灭的上转换发光材料,所述基于三重态-三重态湮灭的上转换发光材料包括敏化剂(即能量给体)和如第一方面所述的三重态湮灭剂(即能量受体)。
优选地,所述敏化剂包括如式a-e所示结构的材料中的任意一种:
其中,式c和式d中m选自钯或铂,式e中bu为叔丁基。
优选地,所述三重态湮灭剂中的联苯结构选自三联苯结构,敏化剂为式a所示结构的材料;
所述三重态湮灭剂中的并苯结构选自芘环结构,敏化剂为式b所示结构的材料;
所述三重态湮灭剂中的并苯结构选自蒽环结构,敏化剂为式c所示结构的材料;
所述三重态湮灭剂中的并苯结构选自苝环结构,敏化剂为式d所示结构的材料;
所述三重态湮灭剂中的并苯结构选自并四苯结构,敏化剂为式e所示结构的材料;
优选地,所述敏化剂与所述三重态湮灭剂的摩尔比是1:50-1:300,例如1:50、1:70、1:90、1:120、1:140、1:160、1:180、1:220、1:240、1:260、1:280、1:300等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。
第四方面,本发明提供一种如第三方面所述的基于三重态-三重态湮灭的上转换发光材料在三重态-三重态湮灭上转换中的应用。
优选地,在所述应用中,将所述上转换发光材料与有机溶剂混合配制成上转换溶液体系。所述上转换溶液体系可以在实现三重态能量转移的同时发射极高效率的上转换荧光。
优选地,所述有机溶剂包括四氢呋喃、甲基环己烷、甲苯、二甲苯、二氯甲烷、氯仿、苯腈或n,n-二甲基甲酰胺中的任意一种或至少两种的组合;所述至少两种的组合例如四氢呋喃和甲基环己烷的组合、二甲苯和二氯甲烷和氯仿的组合等,其他任意的组合方式均可选择,在此便不再一一赘述。
优选地,所述上转换溶液体系中三重态湮灭剂的浓度为0.1-10mm,例如0.1mm、0.3mm、0.8mm、1mm、2mm、3mm、4mm、5mm、6mm、7mm、8mm、9mm、10mm等,该数值范围内的其他具体点值均可选择,在此便不再一一赘述。优选0.1-5mm,进一步优选0.5-2mm。
第五方面,本发明提供一种如第一方面所述的三重态湮灭剂或如第三方面所述的基于三重态-三重态湮灭的上转换发光材料在生物成像、光催化、光伏太阳能电池、显示、光信息的处理和存储上的应用。本发明所涉及的三重态湮灭剂具有良好的光学性能以及上转换性能,在生物成像、光催化、光伏太阳能电池、显示、光信息的处理和存储等方面具有较大的应用价值。
相对于现有技术,本发明具有以下有益效果:
本发明所涉及的三重态湮灭剂由于具有[2.2]对环芳烃结构,并且在结构中含有两个联苯或并苯结构,能够保证自身具有高发光量子效率,同时能够用作三重态湮灭上转换体系的能量受体,可与敏化剂配合实现效率极高的光子上转换发射,其量子效率饱和后最大值达到了42%,这是目前已报道的三重态-三重态湮灭上转换体系中,最高的发光量子效率。该三重态湮灭剂材料在生物成像、光催化、光伏太阳能电池、显示、光信息的处理和存储等方面具有较大的应用价值。
附图说明
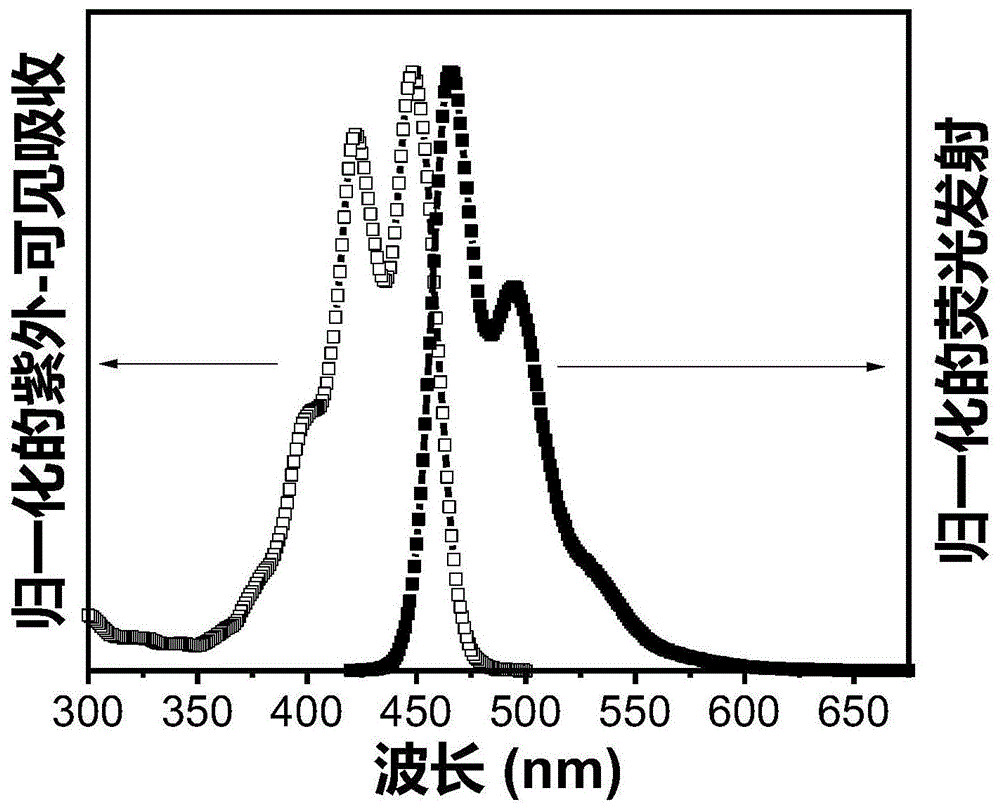
图1是化合物1的紫外-可见吸收光谱以及荧光发射光谱;
图2是化合物2的紫外-可见吸收光谱以及荧光发射光谱;
图3是化合物4的紫外-可见吸收光谱以及荧光发射光谱;
图4是化合物5的紫外-可见吸收光谱以及荧光发射光谱;
图5是化合物1与pttpbp组成的上转换体系在不同激光激发强度(47.2-6394.9mw/cm2)下的上转换发光光谱;
图6是化合物5与ptoep组成的上转换体系在不同激光激发强度(575.8-1444.6mw/cm2)下的上转换发光光谱;
图7是化合物1和pttpbp组成的上转换体系的上转换发光量子效率随激发光强的变化曲线图。
具体实施方式
下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
实施例1
本实施例提供一种三重态湮灭剂(化合物1),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、47mg四(三苯基膦)钯、以及783mg4,4,5,5-四甲基-2-(10-叔丁基苝-3-基)-1,3,2-二氧杂环戊硼烷,加入50ml的反应管当中,加入12ml甲苯,加入3ml溶解有87mg碳酸钠的超纯水,氮气保护下,加热回流,反应24小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,将反应液倒入50ml乙酸乙酯当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物1,产率88%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ8.96-8.85(m,4.07h),8.29(d,j=7.5hz,1.02h),8.21-8.19(m,4.03h),8.16-8.06(m,3.10h),7.98-7.95(m,2.05h),7.88-7.77(m,4.12h),7.69-7.67(m,2.02h),7.32(s,1.03h),7.03(s,1.1h),6.77(d,j=7.4hz,1.01h),6.59(d,j=7.5hz,1.01h),6.27(d,j=7.6,1.01h),6.19-6.15(m,1.01h),2.90-2.83(m,7.99h),1.63-1.52(m,18h).
质谱ms(maldi)计算值c64h52[m+]:821.12,测试值:820.9。
化合物1的紫外-可见吸收光谱以及荧光发射光谱(溶剂为四氢呋喃,浓度为5×10-6moll-1,荧光发射激发波长为360nm)如图1所示,由该图可以看出,化合物1的荧光发射保留了苝的特征发射,有可能作为三重态-三重态湮灭上转换当中的能量受体,实现上转换发光。
实施例2
本实施例提供一种三重态湮灭剂(化合物1),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、107mg三苯基膦、13.56mg醋酸钯以及1070mg4,4,5,5-四甲基-2-(10-叔丁基苝-3-基)-1,3,2-二氧杂环戊硼烷,加入50ml的反应管当中,加入12ml二氧六环,加入3ml溶解有130mg碳酸氢钠的超纯水,氮气保护下,加热回流,反应30小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,旋蒸除去溶剂,将混合物溶于50ml二氯甲烷当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物1,产率85%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ8.96-8.85(m,4.07h),8.29(d,j=7.5hz,1.02h),8.21-8.19(m,4.03h),8.16-8.06(m,3.10h),7.98-7.95(m,2.05h),7.88-7.77(m,4.12h),7.68-7.66(m,2.02h),7.32(s,1.03h),7.02(s,1.1h),6.77(d,j=7.4hz,1.01h),6.59(d,j=7.5hz,1.01h),6.27(d,j=7.6,1.01h),6.19-6.16(m,1.01h),2.90-2.83(m,7.99h),1.63-1.52(m,18h).
质谱ms(maldi)计算值c64h52[m+]:821.12,测试值:821.5。
实施例3
本实施例提供一种三重态湮灭剂(化合物2),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、69mg三环己基膦、9mg氯化钯以及674mg[1,1':4',1”-三联苯基]-4-基硼酸,加入50ml的反应管当中,加入12ml邻二甲苯,加入3ml溶解有316mg碳酸氢钠的超纯水,氮气保护下,加热回流,反应18小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,将混合物溶于50ml乙酸乙酯当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物2,产率91%。
核磁检测数据为:1hnmr(500mhz,chloroform-d)δ7.94–7.81(m,16.04h),7.62–7.55(m,5.88h),7.44(t,j=7.4hz,4.13h),7.37–7.26(m,4.05h),2.88(s,8h).
质谱ms(maldi)计算值c52h40[m+]:664.89,测试值:664.5。
化合物2的紫外-可见吸收光谱以及荧光发射光谱(溶剂为四氢呋喃,浓度为1×10-5moll-1,荧光测试激发波长为280nm)如图2所示,由图可知化合物2的荧光发射为四联苯的特征发射,有可能作为三重态湮灭上转换当中的能量受体,实现三重态湮灭上转换。
实施例4
本实施例提供一种三重态湮灭剂(化合物3),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、182mg1,1’-双(二苯基膦)二茂铁、95mg双(二亚苄基丙酮)钯以及807mg2-(4,4,5,5-四甲基-1,3,2-二氧环戊硼烷-2-基)芘,加入50ml的反应管当中,加入12ml甲苯,加入3ml溶解有170mg碳酸钾的超纯水,氮气保护下,加热回流,反应22小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,将混合物溶于50ml乙酸乙酯当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物3,产率87%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ9.04-9.01(m,2.02h),8.40-8.29(m,3.15h),8.24-8.16(m,6.20h),8.11-8.00(m,6.04h),7.82-7.76(m,1.88h),7.43-7.33(m,2.05h),7.22-7.11(m,2.01h),2.96-2.84(m,8h).
质谱ms(maldi)计算值c48h32[m+]:608.78,测试值:608.4。
对化合物3进行了紫外-可见吸收光谱以及荧光发射光谱的测试(溶剂为四氢呋喃,浓度为1×10-5moll-1,荧光测试激发波长为300nm),结果表明,化合物3的荧光发射相对于芘有所红移,但是由于其与芘结构具有相近的三重态能级,与芘一样有可能作为三重态湮灭上转换当中的能量受体,实现三重态湮灭上转换。
实施例5
本实施例提供一种三重态湮灭剂(化合物4),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、284mg四(三苯基膦)钯以及544mg1-芘硼酸,加入50ml的反应管当中,加入12ml1,4-二氧六环,加入3ml溶解有84mg甲醇钠的超纯水,氩气保护下,加热回流,反应36小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,旋蒸除去溶剂,将混合物溶于50ml二氯甲烷当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物4,产率95%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ8.69(d,j=7.5hz,1.02h),8.64(d,j=7.5hz,1.12h),8.60-8.53(m,2.03h),8.33-8.29(m,2.05h),8.14-7.97(m,11.08h),7.85(d,j=7.5hz,1.04h),7.83-7.76(m,1.95h),7.48-7.38(m,2.04h),7.26-7.16(m,2.11h),2.89-2.84(m,8h).
质谱ms(maldi)计算值c48h32[m+]:608.78,测试值:608.4。
化合物4的紫外-可见吸收光谱以及荧光发射光谱(溶剂为四氢呋喃,浓度为1×10-5moll-1,荧光测试激发波长为300nm)如图3所示,由图可知化合物4的荧光发射相对于芘来说有所红移,但是具有的芘环结构表明其有可能作为三重态湮灭上转换当中的能量受体,实现三重态湮灭上转换。
实施例6
本实施例提供一种三重态湮灭剂(化合物5),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、189mg四(三苯基膦)钯以及660mg(10-苯基蒽-9-基)硼酸,加入50ml的反应管当中,加入12ml间二甲苯,加入3ml溶解有56mg乙醇钠的超纯水,氩气保护下,加热回流,反应16小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,将混合物溶于50ml乙酸乙酯当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物5,产率93%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ8.63(s,10.4h),8.53(s,1.08h),8.29(s,1.07h),8.13-8.00(m,5.14h),7.88-7.79(m,2.04h),7.76-7.69(m,3.94h),7.57(d,j=1.3hz,1.04h),7.57-7.41(m,12.07h),7.39-7.29(m,4.11h),7.15(m,2h),2.91-2.84(m,8h).
质谱ms(maldi)计算值c56h40[m+]:712.94,测试值:712.6。
化合物5的紫外-可见吸收光谱以及荧光发射光谱(溶剂为甲苯,浓度为1×10-5moll-1,荧光测试激发波长为360nm)如图4所示,由图可知,化合物5的荧光发射相对于蒽来说有所红移,但是具有的蒽环结构表明其有可能作为三重态湮灭上转换当中的能量受体,实现三重态湮灭上转换。
实施例7
本实施例提供一种三重态湮灭剂(化合物6),其结构及制备流程示意图如下所示:
合成方法为:
称取300mg4,12-二溴[2.2]对环芳烃、95mg四(三苯基膦)钯以及1780mg4,4,5,5-四甲基-2-(6,11,12-三(4-叔丁基苯基)并四苯-5-基)-1,3,2-二氧杂环戊硼烷,加入50ml的反应管当中,加入12ml1,4-二氧六环,加入3ml溶解有190mg碳酸铯的超纯水,氩气保护下,加热回流,反应34小时后,通过tlc检测4,12-二溴[2.2]对环芳烃原料消失,即反应结束。降至25℃,旋蒸除去溶剂,将混合物溶于40ml二氯甲烷当中萃取,有机相使用无水硫酸钠干燥。旋蒸除去溶剂,通过硅胶柱色谱分离得到化合物6,产率83%。
核磁检测数据为:1hnmr(500mhz,氯仿-d)δ9.07-9.01(m,2.01h),8.95-8.89(m,2.06h),8.75-8.69(m,2.07h),8.21-8.10(m,4.07h),8.10-8.05(m,2.04h),7.92-7.86(m,2.07h),7.86-7.75(m,5.01h),7.74-7.63(m,4.01h),7.63-7.51(m,5.04h),7.40(s,2.04h),7.35-7.20(m,5.01h),6.90(s,1.02h),6.84(s,1.04h),6.57(s,1.04h),6.41(s,2.06h),6.25(s,1.01h),6.05(s,1.08h),2.94-2.82(m,8h),1.34-1.23(m,54.24h).
质谱ms(maldi)计算值c112h108[m+]:1454.10,测试值:1454.3。
对化合物6进行了紫外-可见吸收光谱以及荧光发射光谱的测试(溶剂为四氢呋喃,浓度为1×10-5moll-1,荧光测试激发波长为480nm),结果表明,化合物6的荧光发射相对于红荧烯有所红移,但是由于其与红荧烯结构具有相近的三重态能级,与红荧烯一样有可能作为三重态湮灭上转换当中的能量受体,实现三重态湮灭上转换。
应用例1
在本应用例中,将化合物1与pttpbp组成上转换体系,进行上转换发光测试,方法如下:
以pttpbp(四苯基四苯并卟啉铂,式d中当m=pt时)作为三重态能量给体即敏化剂,化合物1作为三重态受体材料即湮灭剂,配制得到上转换溶液体系。其中三重态敏化剂pttpbp的浓度为1×10-5mol·l-1,三重态湮灭剂化合物1的浓度为5×10-4mol·l-1,溶剂为四氢呋喃。将上述体系经过三次冻融循环除氧后,充入高纯氩气,以635nm激光激发,测试其上转换发光光谱。
图5为化合物1与pttpbp组成的上转换体系在不同激光激发强度(47.2-6394.9mw/cm2)下的上转换发光光谱,由图可知,使用635nm的红光激发上述上转换体系,荧光发射的最大波长在475nm左右,实现了由红光到青蓝光的上转换。
且由于四苯基四苯并卟啉钯(pdtpbp,式d中当m=pd时)和四苯基四苯并卟啉铂(pttpbp,式d中当m=pt时)具有相近的三重态能级,它们在三重态湮灭上转换当中起着相同的作用,即使用pdtpbp的体系也可以使用pttpbp。
应用例2
在本应用例中,将化合物5与ptoep组成上转换体系,进行上转换发光测试,方法如下:
以ptoep作为三重态能量给体即光敏剂,化合物5作为三重态受体材料即湮灭剂,配制得到上转换溶液体系。其中三重态光敏剂ptoep的浓度为1×10-5mol·l-1,三重态湮灭剂化合物5的浓度为1×10-3mol·l-1,溶剂为甲苯。将上述体系经过三次冻融循环除氧后,充入高纯氩气,以532nm激光激发,测试其上转换发光光谱。
图6为化合物5与ptoep组成的上转换体系在不同激光激发强度(575.8-1444.6mw/cm2)下的上转换发光光谱,由该图可知,使用532nm的绿光激发上述上转换体系,荧光发射的最大波长在428nm左右,实现了由绿光到蓝光的上转换。
且由于八乙基卟啉钯(pdoep,式c中当m=pd时)和八乙基卟啉铂(ptoep,式c中当m=pt时)具有相近的三重态能级,它们在三重态湮灭上转换当中起着相同的作用,即使用pdoep的体系也可以使用ptoep。
对化合物2与式a结构能量给体组成的上转换体系、化合物3和4分别与式b结构的能量给体组成的上转换体系、化合物6与式e结构的能量给体组成上转换体系也进行了相同的上转换发光测试,结果表明,化合物2与式a结构能量给体组成的上转换体系可以在445nm激光激发下在367nm处发射荧光,实现了蓝光到紫外光的上转换;化合物3和4分别与式b结构的能量给体组成的上转换体系可以在445nm激光激发下分别在390nm、391nm处发射荧光,实现了蓝光到紫外光的上转换;化合物6与式e结构的能量给体组成上转换体系可以在730nm激光激发下在580nm处发射荧光,实现了近红外光到橙黄光的上转换。
应用例3
在本应用例中,将化合物1与pttpbp组成上转换体系,进行上转换发光量子效率测试,方法如下:
以pttpbp作为三重态能量给体即光敏剂,化合物1作为三重态湮灭剂配制上转换溶液体系。其中三重态光敏剂pttpbp的浓度为1×10-5mol·l-1,三重态湮灭剂化合物1的浓度为5×10-4mol·l-1,溶剂为四氢呋喃。将上述体系经过三次冻融循环除氧后,利用参比法进行上转换发光量子效率测试。参比法所用参比染料为亚甲基蓝(荧光量子效率3%)。参比法计算上转换发光量子效率(φuc)的公式为:
其中,φ,i,a,e和η分别为量子效率、激发光强、激发波长处的吸收强度、发光强度积分和溶剂的折射指数,下标uc和std则代表上转换体系和参比体系。
图7为化合物1和pttpbp组成的上转换体系的上转换发光量子效率随激发光强的变化,由该图可知,使用635nm的红光激光激发上述上转换体系,其量子效率饱和后最大值达到了42%,这是目前已报道的三重态-三重态湮灭上转换体系中,最高的发光量子效率。
对化合物2与式a结构能量给体组成的上转换体系、化合物3和4分别与式b结构的能量给体组成的上转换体系、化合物5与ptoep组成的上转换体系、化合物6与式e结构的能量给体组成上转换体系也进行了相同的上转换发光量子效率测试,结果表明上述体系分别在445nm、445nm、445nm、532nm、730nm激光激发下,同样具有极高效率的上转换发光量子效率。
申请人声明,本发明通过上述实施例来说明本发明的一种三重态湮灭剂及其制备方法和应用,但本发明并不局限于上述实施例,即不意味着本发明必须依赖上述实施例才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
- 还没有人留言评论。精彩留言会获得点赞!